Ариламіди 1-гідроксі-3-оксо-6,7-дигідро-3н,5н-піридо[3,2,1-ij]хінолін-2-карбонової кислоти, які виявляють діуретичну активність
Номер патенту: 98869
Опубліковано: 25.06.2012
Автори: Кравченко Віра Миколаївна, Голік Микола Юрійович, Українець Ігор Васильович
Формула / Реферат
Ариламіди 1-гідроксі-3-оксо-6,7-дигідро-3H,5H-піридо[3,2,1-ij]хінолін-2-карбонової кислоти загальної формули:
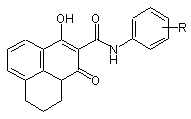 ,
,
де R=4-F або 3-ОН, або 2-ОМе, або 4-ОМе, або 2-CONH2, або 4-COOEt,
які виявляють діуретичну активність.
Текст
Реферат: Винахід належить до хіміко-фармацевтичної промисловості і стосується біологічно активних речовин, зокрема похідних хінолінкарбонової кислоти, а саме ариламідів 1-гідроксі-3-оксо-6,7дигідро-3H,5H-піридо[3,2,1-ij]хінолін-2-карбонової кислоти, які виявляють діуретичну активність. Завданням даного винаходу є синтез індивідуальних хімічних сполук з високою діуретичною дією та низькою токсичністю. Завдання винаходу вирішується шляхом одержання ариламідів 1-гідроксі-3-оксо-6,7-дигідро3H,5H-піридо[3,2,1-ij]хінолін-2-карбонової кислоти загальної формули: OH O R N H O , UA 98869 C2 (12) UA 98869 C2 де R = 4-F або 3-ОН, або 2-ОМе, або 4-ОМе, або 2-CONH2, або 4-COOEt, які виявляють діуретичну активність. OH O R N H O UA 98869 C2 5 10 15 20 25 Винахід належить до хіміко-фармацевтичної промисловості і стосується біологічно активних речовин, зокрема похідних хінолінкарбонової кислоти, а саме ариламідів 1-гідроксі-3-оксо-6,7дигідро-3Н, 5Н-піридо[3,2,1-ij]хінолін-2-карбонової кислоти, які виявляють діуретичну активність. Гіпертонічна хвороба не випадково вважається однією з основних проблем сучасної медицини. Це не просто захворювання, яке саме по собі знижує якість життя людини. На жаль, це ще й фактор, який запускає каскад багатьох патологічних змін в різних органах та тканинах, що призводять до формування цілого ряду інших хвороб та патологічних станів і тим самим сприяють розвитку ускладнень та різкому збільшенню смертності. Останнім часом провідне місце у лікуванні артеріальної гіпертензії та хронічної серцевої недостатності міцно зайняли діуретики. Не будучи безпосередньо антигіпертензивними препаратами, вони сприяють виведенню з організму великої кількості рідини, знижуючи таким чином артеріальний тиск до фізіологічної норми (Pascual J.M., Rodilla E., Costa J.A., Perez-Lahiguera F., Gonzalez С. Lurbe E., Redon J. / Body weight variation and control of cardiovascular risk factors in essential hypertension // Blood Press.-2009. -Vol. 18, No. 5. - P. 247-254). Аналогом заявлених сполук за дією є широко відомий в медицині діуретик гіпотіазид (гідрохлортіазид), який завдяки своїм вираженим сечогінним властивостям належить до особливо цінних засобів боротьби з артеріальною гіпертензією (Машковский М. Д. Лекарственные средства. - М.: РИА Новая волна: издатель Умеренков, 2009. - С. 499). Разом з певними позитивними якостями цей препарат, на жаль, виявляє ряд суттєвих побічних ефектів, які значно обмежують його практичне застосування. Основні з них - досить висока токсичність та необхідність для досягнення ефекту прийому значних доз препарату, які є причиною різноманітних негативних станів і, як наслідок, цілого ряду обмежень у застосуванні. В основу винаходу поставлено задачу одержати нові індивідуальні хімічні сполуки з більш високою діуретичною дією та низькою токсичністю. Задача винаходу вирішується шляхом одержання ариламідів 1-гідроксі-3-оксо-6,7-дигідро3H, 5H-піридо[3,2,1-ij]хінолін-2-карбонової кислоти загальної формули (1): OH O R N H O 30 35 , (1) де R=4-F (1а) або 4-Ме (1б), або 3-ОН (1в), або 2-ОМе (1г), або 4-ОМе (1д), або 2-CONH2 (1e), або 4-COOЕt (1ж), які виявляють діуретичну активність. У відповідності з винаходом заявлено 7 індивідуальних хімічних сполук, представлених у таблиці 1. Заявлені сполуки синтезують взаємодією етилового естеру 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1-ij]хінолін-2-карбонової кислоти з відповідними анілінами, які забезпечують одержання заявлених структур 1а-1ж, при температурі 140 °C в присутності невеликої кількості ДМФА або іншого висококиплячого інертного органічного розчинника з подальшим відокремленням утвореного осаду. Таблиця 1 Варіанти заявлених сполук Варіант R 1а 4-F 1б 4-Ме 1в 3-OH 1г 2-ОМе 1д 4-ОМе Заявлена сполука 4-фторанілід 1-гідроксі-3-оксо-6,7-дигідро-3H, піридо[3,2,1-ij]хінолін-2-карбонової кислоти 4-метиланілід 1-гідроксі-3-оксо-6,7-дигідро-3H, піридо[3,2,1-ij]хінолін-2-карбонової кислоти 3-гідроксіанілід 1-гідроксі-3-оксо-6,7-дигідро-3H, піридо[3,2,1-ij]хінолін-2-карбонової кислоти 2-метоксіанілід 1-гідроксі-3-оксо-6,7-дигідро-3H, піридо[3,2,1-ij]хінолін-2-карбонової кислоти 4-метоксіанілід 1-гідроксі-3-оксо-6,7-дигідро-3H, піридо[3,2,1-ij]хінолін-2-карбонової кислоти 1 5H5Н5H5Н5Н UA 98869 C2 Продовження таблиці 1 Варіант R 1е 1ж 5 10 15 20 25 30 35 40 45 50 2-CONH2 4-COOEt Заявлена сполука 2-карбамоїланілід 1-гідроксі-3-оксо-6,7-дигідро-3H, 5Нпіридо[3,2,1-ij]хінолін-2-карбонової кислоти 4-етоксікарбоніланілід 1-гідроксі-3-оксо-6,7-дигідро-3H, 5Hпіридо[3,2,1-ij]хінолін-2-карбонової кислоти Винахід ілюструються наведеними нижче прикладами. Приклад 1. Одержання 4-фтораніліду 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти (1а) Суміш 2,73 г (0,01 моль) етилового естеру 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти, 1,11 г (0,01 моль) 4-фтораніліну та 1 мл ДМФА (можна використати ксилол, бромбензол або інший висококиплячий інертний органічний розчинник) витримують на металічній бані при 140 °C протягом 5 хвилин. Охолоджують, додають 20 мл етилового спирту і ретельно перемішують. Осад аміду 1а відфільтровують, промивають холодним етиловим спиртом, сушать. Вихід 3,17 г (94 %). Кристалізують з суміші ДМФА та 1 етилового спирту. Т. пл. 193-195 °C. Спектр Н-ЯМР, , м.ч., (J, Гц): 16,37 (1Н, с, ОН); 12,65 (1H, с, NH); 7,97 (1Н, д, J=8,1, Н-10); 7,68 (2Н, дд, J=8,6 і 5,2, Н-2',6'); 7,45 (1Н, д, J=7,5, Н-8); 7,18 (1Н, т, J=7,5, Н-9); 7,06 (2Н, т, J=9,2, Н-3',5'); 4,14 (2Н, т, J=6,0, NCH2); 3,00 (2Н, т, J=6,0, 7-CH2); 2,13 (2Н, кв, J=5,8, 6-СН2). Знайдено, %: С 67,57; Н 4,56; N 8,21. C19H15FN2O3. Вирахувано, %: С 67,45; Н 4,47; N 8,28. Приклад 2. Одержання 4-метиланіліду 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти (16) Суміш 2,73 г (0,01 моль) етилового естеру 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти, 1,07 г (0,01 моль) 4-толуідину та 1 мл ДМФА витримують на металічній бані при 140 °C протягом 5 хвилин. Охолоджують, додають 20 мл етилового спирту і ретельно перемішують. Осад аміду 16 відфільтровують, промивають холодним етиловим спиртом, сушать. Вихід 3,03 г (91 %). Кристалізують з суміші ДМФА та етилового спирту. Т. пл. 1 187-189 °C. Спектр Н-ЯМР, , м.ч., (J, Гц): 16,63 (1Н, с, ОН); 12,51 (1H, с, NH); 7,98 (1Н, д, J=8,2, Н-10); 7,55 (2Н, д, J=8,4, Н-2',6'); 7,39 (1Н, д, J=7,3, Н-8); 7,15 (1Н, т, J=7,6, Н-9); 7,10 (2Н, д, J=8,4, Н-3',5'); 4,14 (2Н, т, J=6,2, NCH2); 2,99 (2Н, т, J=6,1, 7-СН2); 2,35 (3Н, с, Me); 2,13 (2Н, кв, J=5,8, 6-СН2). Знайдено, %: С 71,93; Н 5,35; N 8,46. C20Hi8N2O3. Вирахувано, %: С 71,84; Н 5,43; N 8,38. Приклад 3. Одержання 3-гідроксіаніліду 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти (1в) Суміш 2,73 г (0,01 моль) етилового естеру 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти, 1,09 г (0,01 моль) 3-амінофенолу та 1 мл ДМФА витримують на металічній бані при 140 °C протягом 5 хвилин. Охолоджують, додають 20 мл етилового спирту і ретельно перемішують. Осад аміду 1в відфільтровують, промивають холодним етиловим спиртом, сушать. Вихід 2,95 г (88 %). Кристалізують з суміші ДМФА та етилового спирту. Т. пл. 1 198-200 °C. Спектр Н-ЯМР, , м.ч., (J, Гц): 16,57 (1Н, с, ОН); 12,58 (1Н, с, NH); 9,25 (1Н, с, 3'ОН); 7,97 (1Н, д, J=8,0, Н-10); 7,50 (1Н, д, J=7,4, Н-8); 7,22 (1Н, т, J=7,5, Н-9); 7,19 (1H, с, Н-2'); 7,11 (1H, т, J=8,1, Н-5'); 6,97 (1Н, д, J=8,3, Н-4'); 6,54 (1Н, д, J=7,1, Н-6'); 4,14 (2Н, т, J=5,8, NCH2); 3,00 (2Н, т, J=6,0, 7-СН2); 2,11 (2Н, кв, J=5,8, 6-СН2). Знайдено, %: С 67,77; Н 4,89; N 8,41; C19H16N2O4. Вирахувано, %: С 67,85; Н 4,79; N 8,33. Приклад 4. Одержання 2-метоксіаніліду 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти (1г) Суміш 2,73 г (0,01 моль) етилового естеру 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти, 1,23 г (0,01 моль) 2-анізидину та 1 мл ДМФА витримують на металічній бані при 140 °C протягом 5 хвилин. Охолоджують, додають 20 мл етилового спирту і ретельно перемішують. Осад аміду 1г відфільтровують, промивають холодним етиловим спиртом, сушать. Вихід 2,94 г (84 %). Кристалізують з суміші ДМФА та етилового спирту. Т. пл. 1 220-222 °C. Спектр Н-ЯМР, , м.ч., (J, Гц): 16,67 (1Н, с, ОН); 12,70 (1Н, с, NH); 8,37 (1H, д, J=7,9, Н-3'); 7,98 (1Н, д, J=8,0, Н-10); 7,43 (1H, д, J=7,3, Н-8); 7,16 (1H, т, J=7,5, Н-9); 7,06 (1Н, т, J=7,6, Н-5'); 6,97 (1H, д, J=8,6, Н-6'); 6,91 (1Н, т, J=7,9, Н-4'); 4,17 (2Н, т, J=5,6, NCH2); 3,98 (3Н, с, ОМе); 3,01 (2Н, т, J=6,0, 7-СН2); 2,14 (2Н, кв, J=5,6, 6-СН2). Знайдено, %: С 68,67; Н 5,26; N 8,09. C20H18N2O4. Вирахувано, %: С 68,56; Н 5,18; N 8,00. 2 UA 98869 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 5. Одержання 4-метоксіаніліду 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти (1д) Суміш 2,73 г (0,01 моль) етилового естеру 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти, 1,23 г (0,01 моль) 4-анізидину та 1 мл ДМФА витримують на металічній бані при 140 °C протягом 5 хвилин. Охолоджують, додають 20 мл етилового спирту і ретельно перемішують. Осад аміду 1д відфільтровують, промивають холодним етиловим спиртом, сушать. Вихід 3,25 г (93 %). Кристалізують з суміші ДМФА та етилового спирту. Т. пл. 1 176-178 °C. Спектр Н-ЯМР, , м.ч., (J, Гц): 16,66 (1H, с, ОН); 12,47 (1Н, с, NH); 7,97 (1Н, д, J=8,1, Н-10); 7,57 (2Н, д, J=9,2, Н-3',5'); 7,43 (1Н, д, J=7,1, Н-8); 7,17 (1Н, т, J=7,7, Н-9); 6,86 (2Н, д, J=9,2, Н-2',6'); 4,14 (2Н, т, J=5,7, NCH2); 3,79 (3Н, с, ОМе); 3,00 (2Н, т, J=5,9, 7-СН2); 2.13 (2H, кв, J=5,6, 6-СН2). Знайдено, %: С 68,69; Н 5,31; N 8,11. C20H18N2O4. Вирахувано, %: С 68,56; Н 5,18; N 8,00. Приклад 6. Одержання 2-карбамоїланіліду 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти (1е) Суміш 2,73 г (0,01 моль) етилового естеру 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти, 1,36 г (0,01 моль) антраніламіду та 1 мл ДМФА витримують на металічній бані при 140 °C протягом 5 хвилин. Охолоджують, додають 20 мл етилового спирту і ретельно перемішують. Осад аміду 1е відфільтровують, промивають холодним етиловим спиртом, сушать. Вихід 2,94 г (81 %). Кристалізують з суміші ДМФА та етилового спирту. Т. пл. 1 303-305 °C. Спектр Н-ЯМР, , м.ч., (J, Гц): 16,65 (1Н, с, ОН); 12,97 (1Н, с, NH); 8,21 (1Н, д, J=8,3, Н-3'); 7,95 (1Н, д, J=8,0, Н-10); 7,80 (1Н, уш. с, CONH); 7,61 (1Н, д, J=8,2, Н-6'); 7,48 (1Н, д, J=7,5, Н-8); 7,40 (1H, т, J=8,0, Н-5'); 7,26 (1Н, уш. с, CONH); 7,18 (2Н, м, Н-9 + Н-4'); 4,13 (2Н, т, J=5,6, NCH2); 3,01 (2Н, т, J=6,0, 7-СН2); 2,11 (2Н, кв, J=5,6, 6-СН2). Знайдено, %: С 66,02; Н 4,61; N 11,63. С20Н17N3О4 Вирахувано, %: С 66,11; Н 4,72; N 11,56. Приклад 7. Одержання 4-етоксікарбоніланіліду 1-гідроксі-3-оксо-6,7-дигідро-3H, 5Hпіридо[3,2,1-ij]хінолін-2-карбонової кислоти (1ж) Суміш 2,73 г (0,01 моль) етилового естеру 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти, 1,65 г (0,01 моль) анестезину та 1 мл ДМФА витримують на металічній бані при 140 °C протягом 5 хвилин. Охолоджують, додають 20 мл етилового спирту і ретельно перемішують. Осад аміду 1ж відфільтровують, промивають холодним етиловим спиртом, сушать. Вихід 3,80 г (97 %). Кристалізують з суміші ДМФА та етилового спирту. Т. пл. 1 204-206 °C. Спектр Н-ЯМР, , м.ч., (J, Гц): 16,12 (1Н, с, ОН); 12,98 (1Н, с, NH); 7,97 (3Н, м, Н-10 1 + Н-3',5'); 7,77 (2Н, д, J=8,7, Н-2',6 ); 7,51 (1Н, д, J=7,4, Н-8); 7,23 (1Н, т, J=7,7, Н-9); 4,32 (2Н, к, J=7,2, ОСН2); 4,14 (2Н, т, J=5,7, NCH2); 3,79 (3Н, с, ОМе); 3,01 (2Н, т, J=6,0, 7-СН2); 2,12 (2H, кв, J=5,5, 6-СН2); 1,39 (3Н, т, J=7,2, ОСН2Ме). Знайдено, %: С 67,46; Н 5,22; N 7,05. C22H20N2O5. Вирахувано, %: С 67,34; Н 5,14; N 7,14. 1 Спектри Н-ЯМР заявлених сполук зареєстровані на приладі Braker WM-360 (360 МГц) в розчині ДМСО-d6, внутрішній стандарт ТМС. Приклад 8. Гостру токсичність ариламідів 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1ij]хінолін-2-карбонової кислоти 1a-ж визначали на інтактних білих мишах вагою 18-22 г по 6 тварин в серії з кожною дозою. Досліджувані речовини вводили у вигляді тонкої водної суспензії, стабілізованої твіном-80, перорально (при високих дозах за 2-3 прийоми з інтервалом 10 хвилин). Кількість тварин, що вижили, реєстрували кожні 24 години протягом 14 діб. Середньосмертельні дози (LD50) розраховували за методом Кербера (Сернов Л.Н., Гацура В.В. Элементы экспериментальной фармакологии. - М.: ППП "Типография "Наука".-2000. - С. 318). Наведені в табл. 2 дані свідчать про те, що всі заявлені речовини за класифікацією К.К. Сидорова (Сидоров К.К. О классификации токсичности ядов при парентеральных способах введения // В кн. Токсикология новых промышленных химических веществ. - М.: Медицина, 1973. - Вып. 13. - С. 50) є щонайменше малотоксичними. Гіпотіазид значно поступається їм за цим показником, оскільки за даними літератури (Kleemann A., Engel J. / Pharmaceutical substances. Synthesis, patents, applications. - Multimedia Viewer, Version 2.00. - Stuttgart: Georg Thime Verlag, 2001) його середньосмертельна доза для мишей перорально складає всього лише 1175 мг/кг. Приклад 9. Діуретична активність заявлених ариламідів 1-гідроксі-3-оксо-6,7-дигідро-3Н, 5Hпіридо[3,2,1-ij]хінолін-2-карбонової кислоти 1а-ж вивчалась на білих безпородних щурах вагою 180-200 г за стандартною методикою (Сернов Л.Н., Гацура В.В. Элементы экспериментальной фармакологии. - М.: ППП "Типография "Наука".-2000. - С. 117) паралельно та в порівнянні з гіпотіазидом. Всі піддослідні тварини отримували через шлунковий зонд водне навантаження з розрахунку 25 мл/кг. Контрольна група тварин отримувала тільки аналогічну кількість води з твіном-80. Досліджувані сполуки la-ж вводили перорально в дозі 20 мг/кг, а гіпотіазид у його 3 UA 98869 C2 ефективній дозі (40 мг/кг) у вигляді тонкої водної суспензії, стабілізованої твіном-80. Після цього піддослідних тварин поміщали в "обмінні клітки". Показником інтенсивності сечовиділення служила кількість сечі, виділена тваринами за 5 годин (Табл. 2). Таблиця 2 Токсичність та діуретична активність заявлених сполук в порівнянні з гіпотіазидом Сполука 1а 1б 1в 1г 1д 1е 1ж Гіпотіазид Контроль LD50, мг/кг >4000 >4000 >4000 >4000 >4000 >4000 >4000 1175 Діурез за 5 годин, мл 7,99±0,40 7,54±0,38 6,97±0,34 7,05±0,30 7,34±0,39 7,13±0,31 6,89±0,36 6,19±0,35 4,10±0,26 Діуретична активність, % 195 184 170 172 179 174 168 151 100 5 10 15 Дані експериментів, представлені в табл. 2, дозволяють зробити висновок, що всі заявлені сполуки за ступенем діуретичної дії помітно перевищують препарат порівняння гіпотіазид, причому в менших дозах і при значно нижчій токсичності. Таким чином, заявлено ариламіди 1-гідроксі-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1-ij]хінолін2-карбонової кислоти, які в двічі менших дозах перевищують за діуретичною активністю гіпотіазид і при цьому виявляють більше ніж в тричі нижчу токсичність. Всі сполуки синтезуються з доступних реагентів та за простими методиками, які можуть бути здійснені в умовах хімікофармацевтичних підприємств або лабораторій з використанням стандартного обладнання. Ариламіди 1-гідрокси-3-оксо-6,7-дигідро-3H, 5H-піридо[3,2,1-ij]хінолін-2-карбонової кислоти можуть бути використані як лікарські субстанції при створенні засобів діуретичної дії у різних лікарських формах. ФОРМУЛА ВИНАХОДУ 20 Ариламіди 1-гідроксі-3-оксо-6,7-дигідро-3H,5H-піридо[3,2,1-ij]хінолін-2-карбонової загальної формули: OH O R N H O , де R=4-F або 3-ОН, або 2-ОМе, або 4-ОМе, або 2-CONH2, або 4-COOEt, які виявляють діуретичну активність. 25 Комп’ютерна верстка А. Крижанівський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 4 кислоти
ДивитисяДодаткова інформація
Назва патенту англійською1-hydroxy-3-oxo-6,7-dihydro-3h,5h-pyrido[3,2,1-ij]quinoline-2-carboxylic acid arylamides exhibiting diuretic activity
Автори англійськоюUkrainets Ihor Vasyliovych, Holik Mykolai Yuriiovych, Kravchenko Vira Mykolaivna
Назва патенту російськоюАриламиды 1-гидрокси-3-оксо-6,7-дигидро-3н,5н-пиридо[3,2,1-ij]хинолин-2-карбоновой кислоты, проявляющие диуретическую активность
Автори російськоюУкраинец Игорь Васильевич, Голик Николай Юрьевич, Кравченко Вера Николаевна
МПК / Мітки
МПК: C07D 215/22, A61P 7/10, A61K 31/47
Мітки: 1-гідроксі-3-оксо-6,7-дигідро-3н,5н-піридо[3,2,1-ij]хінолін-2-карбонової, кислоти, активність, ариламіди, діуретичну, виявляють
Код посилання
<a href="https://ua.patents.su/6-98869-arilamidi-1-gidroksi-3-okso-67-digidro-3n5n-pirido321-ijkhinolin-2-karbonovo-kisloti-yaki-viyavlyayut-diuretichnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Ариламіди 1-гідроксі-3-оксо-6,7-дигідро-3н,5н-піридо[3,2,1-ij]хінолін-2-карбонової кислоти, які виявляють діуретичну активність</a>
Попередній патент: Спосіб проведення голосування коротюка-іванова
Наступний патент: Спосіб одержання похідних 2-(((5-1r-2-r-1,3-тіазол-4-іл)метил)сульфаніл)-1,3-бензтіазолу-2r
Випадковий патент: Дистиляційний пристрій