N-r-аміди 1-гідрокси-3-оксо-5,6-дигідро-3н-піроло-[3,2,1-ij]-хінолін-2-карбонової кислоти, які виявляють діуретичну активність
Номер патенту: 86286
Опубліковано: 10.04.2009
Автори: Набока Ольга Іванівна, Українець Ігор Васильович, Березнякова Наталя Леонідівна, Моспанова Олена Володимирівна
Формула / Реферат
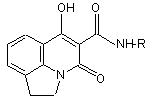
N-R-аміди 1-гідрокси-3-оксо-5,6-дигідро-3H-піроло-[3,2,1-ij]-хінолін-2-карбонової кислоти загальної формули:
 ,
,
де R = циклопентил або 4-метоксибензил, або 2-метоксифеніл, або 3-метоксифеніл, або 3-хлорфеніл, або 2-сульфамоїл, які виявляють діуретичну активність.
Текст
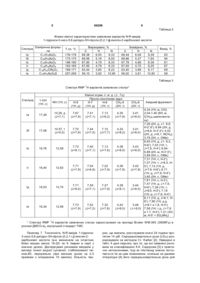
N-R-аміди 1-гідрокси-3-оксо-5,6-дигідро-3Hпіроло-[3,2,1-ij]-хінолін-2-карбонової кислоти загальної формули: Винахід відноситься до хіміко-фармацевтичної промисловості і стосується біологічно активних речовин, зокрема, похідних хінолін-карбонової кислоти, а саме N-R-амідів 1-гідрокси-3-оксо-5,6дигідро-3H-піроло-[3,2,1-ij]-хінолін-2-карбонової кислоти, які виявляють діуретичну активність. Діуретики широко використовуються в медицині для лікування патологічних станів, які супроводжуються затримкою рідини в організмі людини: при периферійних набряках, хронічній недостатності кровообігу, гіпертонії, глаукомі та інших захворюваннях. Останнім часом увагу лікарів привертає використання діуретиків в такій, поки що незвичній для них області, як лікування ниркової недостатності, отруєнь водорозчинними речовинами, нецукрового діабету, синдрому бронхіальної обструкції, муковісцидозу, онкологічних захворювань та інших хвороб. Разом з тим, не зважаючи на те, що кількість показань до застосування сечогінних препаратів в клінічній практиці неупинно зростає, на світовому ринку за останні 30 років не з'явилось жодного нового класу діуретиків і їх номенклатура залишається досить обмеженою. Аналогом заявлених сполук за дією є широко відомий в медицині діуретик гіпотіазид (гідрохлортіазид) [1]. Разом з певною терапевтичною дією цей препарат виявляє ряд характерних побічних ефектів, які суттєво обмежують його практичне застосування. Основний з них це досить висока токсичність, за рахунок якої у людей часто виникають запаморочення, слабкість, головні болі та інші негативні стани. Завданням даного винаходу є одержання N-Rамідів 1-гідрокси-3-оксо-5,6-дигідро-3H-піроло[3,2,1-ij]-хінолін-2-карбонової кислоти з високою діуретичною активністю та низькою токсичністю. Завдання винаходу вирішується шляхом одержання N-R-амідів 1-гідрокси-3-оксо-5,6-дигідро3H-піроло-[3,2,1-ij]-хінолін-2-карбонової кислоти загальної формули І: OH O NH-R N O (19) UA (11) 86286 (13) C2 , де R = циклопентил або 4-метоксибензил, або 2метоксифеніл, або 3-метоксифеніл, або 3хлорфеніл, або 2-сульфамоїл, які виявляють діуретичну активність. 3 86286 4 метоксіфеніл (Ів); 3-метоксіфеніл (Iг); 3-хлорфеніл (Ід) або 2-сульфамоїл (Іе), які виявляють діуретичну активність. У відповідності з винаходом заявлено 6 індивідуальних хімічних сполук, представлених у таблиці 1. де R=циклопентил (Іа); 4-метоксібензил (Іб); 2Таблиця 1 Варіанти заявлених сполук Варіант 1a 1б 1в 1г 1д 1e R Заявлена сполука Циклопентиламід 1-гідрокси-3-оксо-5,6-дигідро-3H-піроло-[3,2,1-ij]-хінолін-2циклопентил карбонової кислоти 4-Метоксібензиламід 1-гідрокси-3-оксо-5,6-дигідро-3H-піроло- [3,2,1-ij]-хінолін-24-метоксібензил карбонової кислоти 2-Метоксіфеніламід 1-гідрокси-3-оксо-5,6-дигідро-3H-піроло-[3,2,1-i,j]-хінолін-22-метоксіфеніл карбонової кислоти 3-Метоксіфеніламід 1-гідрокси-3-оксо-5,6-дигідро-3H-піроло-[3,2,1-i,j]-хінолін-23-метоксіфеніл карбонової кислоти 3-Хлорфеніламід 1-гідрокси-3-оксо-5,6-дигідро-3H-піроло-[3,2,1-i,j]-хінолін-23-хлорфеніл карбонової кислоти 2-Сульфамоїламід 1-гідрокси-3-оксо-5,6-дигідро-3H-піроло-[3,2,1-i,j]-хінолін-22-сульфамоїл карбонової кислоти Заявлені сполуки синтезують взаємодією етилового ефіру 1-гідрокси-3-оксо-5,6-дигідро-3Hпіроло-[3,2,1-i,j]-хінолін-2-карбонової кислоти з відповідними амінами, які забезпечують одержання заявлених структур Ia-Ie, при кип'ятінні зі зворотнім холодильником з подальшим відокремленням утвореного осаду. Фізико-хімічні та спектральні характеристики заявлених сполук наведені в таблицях 2 і 3. Винахід ілюструються наведеними нижче прикладами. Приклад 1. Одержання циклопентиламіду 1гідрокси-3-оксо-5,6-дигідро-3H-піроло-[3,2,1-і,j]хінолін-2-карбонової кислоти (Іа). До розчину 2,59г (0,01моль) етилового ефіру 1-гідрокси-3-оксо-5,6дигідро-3H-піроло-[3,2,1-i,j]-хінолін-2-карбонової кислоти в 15мл етилового спирту додають 1,1мл (0,011моль) циклопентиламіну і кип'ятять зі зворотнім холодильником протягом 4 годин. Охолоджують, розбавляють реакційну суміш водою, після чого підкислюють розведеною (1:1) HCl до рН 4,55. Осад аміду Ia відфільтровують, промивають холодною водою, сушать. Кристалізують з етилового спирту. Приклад 2. Одержання 4-метоксібензиламіду 1-гідрокси-3-оксо-5,6-дигідро-3H-піроло-[3,2,1-і,j]хінолін-2-карбонової кислоти (Іб). До розчину 2,59г (0,01моль) етилового ефіру 1-гідрокси-3-оксо-5,6дигідро-3H-піроло-[3,2,1-i,j]-хінолін-2-карбонової кислоти в 15мл етилового спирту додають 1,44мл (0,011моль) 4-метоксібензиламіну і кип'ятять зі зворотнім холодильником протягом 4 годин. Охолоджують, розбавляють реакційну суміш водою, після чого підкислюють розведеною (1:1) HCl до рН 4,5-5. Осад аміду Іб відфільтровують, промивають холодною водою, сушать. Кристалізують з етилового спирту. Приклад 3. 2-Метоксіфеніламід 1-гідрокси-3оксо-5,6-дигідро-3H-піроло-[3,2,1-i,j]-хінолін-2карбонової кислоти (Ів). Суміш 2,59г (0,01моль) етилового ефіру 1-гідрокси-3-оксо-5,6-дигідро-3Hпіроло-[3,2,1-i,j]-хінолін-2-карбонової кислоти та 1,58мл (0,014моль) орто-анізидину в 50мл бромбензолу кип'ятять зі зворотнім холодильником протягом 36 годин. Розчинник відганяють під пониженим тиском. Залишок кристалізують з ДМФА. Приклад 4. 3-Метоксіфеніламід 1-гідрокси-3оксо-5,6-дигідро-3H-піроло-[3,2,1-i,j]-хінолін-2карбонової кислоти (Iг). Суміш 2,59г (0,01моль) етилового ефіру 1-гідрокси-3-оксо-5,6-дигідро-3Hпіроло-[3,2,1-i,j]-хінолін-2-карбонової кислоти та 1,57мл (0,014моль) мета-анізидину в 50мл бромбензолу кип'ятять зі зворотнім холодильником протягом 36 годин. Розчинник відганяють під пониженим тиском. Залишок кристалізують з ДМФА. Приклад 5. З-Хлорфеніламід 1-гідрокси-3-оксо5,6-дигідро-3H-піроло-[3,2,1-і,j]-хінолін-2карбонової кислоти (Ід). Суміш 2,59г (0,01моль) етилового ефіру 1-гідрокси-3-оксо-5,6-дигідро-3Hпіроло-[3,2,1-i,j]-хінолін-2-карбонової кислоти та 1,48мл (0,014моль) мета-хлораніліну в 50мл бромбензолу кип'ятять зі зворотнім холодильником протягом 36 годин. Розчинник відганяють під пониженим тиском. Залишок кристалізують з ДМФА. Приклад 6. 2-Сульфамоїлфеніламід 1гідрокси-3-оксо-5,6-дигідро-3H-піроло-[3,2,1-i,j]хінолін-2-карбонової кислоти (Іе). Суміш 2,59г (0,01моль) етилового ефіру 1-гідрокси-3-оксо-5,6дигідро-3H-піроло-[3,2,1-i,j]-хінолін-2-карбонової кислоти та 2,41г (0,014моль) 2-сульфамоїланіліну в 50мл бромбензолу кип'ятять зі зворотнім холодильником протягом 36 годин. Розчинник відганяють під пониженим тиском. Залишок кристалізують з водного ДМФА. 5 86286 6 Таблиця 2 Фізико-хімічні характеристики заявлених варіантів N-R-амідів 1-гідрокси-3-оксо-5,6-дигідро-3Н-піроло-[3,2,1-i,j]-хінолін-2-карбонової кислоти Сполука Ia Іб IВ Iг Ід Ie Емпірична формула C17H18N2O3 C20H18N2O4 C19H16N2O4 C19H16N2O4 C18H13ClN2O3 C18H15N3O5S Т.пл, °C 176-178 173-175 188-190 163-165 169-171 257-259 Вирахувано, % C H N 68,38 6,00 9,33 68,56 5,18 8,00 67,85 4,79 8,33 67,85 4,79 8,33 63,44 3,85 8,22 56,10 3,92 10,90 C 68,44 68,66 67,78 67,93 63,40 56,02 Знайдено, % H N 6,08 9,39 5.27 7,94 4,86 8,39 4,70 8,25 3,88 8,17 3,81 10,83 Вихід, % 83 94 61 67 69 58 Таблиця 3 Спектри ЯМР 1H варіантів заявлених сполук* 1-OH (1Н, с) NH (1Н, с) Н-9 (1Н, д) Хімічні зсуви, d, м. д. (J , Гц) Піроло-хінолінове ядро H-7 H-8 СН2-5 (1Н, д) (1Н, т) (2Н, т) Ia 17,29 10,29, д (J=7,1) 7,67 (J=7,9) 7,41 (J=7,1) 7,13 (J=8,2) 4,30 (J=7,9) 3,41 (J=8,0) Іб 17,08 10.57, т (J=5,5) 7,70 (J=7,8) 7,44 (J=7,0) 7,15 (J=7,7) 4,32 (J=8,2) 3,41 (J=8,0) IВ 16,76 12,59 7,72 (J=8,1) 7,40 (J=7,1) 7,13 (J=7,6) 4,38 (J=8,0) 3,43 (J=8,0) Iг 16,44 12,63 7,71 (J=7,9) 7,54 (J=6,9) 7,22 (J=7,9) 4,36 (J=7,9) 3,42 (J=7,9) Ід 16,03 12,74 7,71 (J=8,0) 7,59 (J=7,1) 7,27 (J=7,9) 4,38 (J=8,1) 3,44 (J=8,0) Ie 16,34 12,59 7,73 (J=7,9) 7,52 (J=7,2) 7,32 (J=7,6) 4,42 (J=8,0) 3,46 (J =8,0) Сполука СН2-6 (2H, т) Амідний фрагмент 4,34 (1H, м, CH); 2,04-1,40 (8H, м, (СН2)4 циклопентану) 7,26 (2H, д, J = 8,9, Н-2',6'); 6.84 (2Н, д, J=8,9, Н-3',5'); 4,53 (2Н, д, J=6,1, NCH2); 3,78 (3Н, с, OMe) 8,40 (1H, д, J = 8,3, Н-6'); 7,03 (1Н, т, J=7,9, H-4'); 6,946,88 (2Н, м, Н-3',5'); 3,99 (3Н, с, OMe) 7,31 (1H, с, Н-2'); 7,27 (1Н, т, J=8,5, Н5'); 7,13 (1Н, д, J=7,9, Н-6'); 6,71 (1H, д, J=7,9, Н-4'); 3,80 (3Н, с, OMe) 7,81 (1Н, с, Н-2'); 7,47 (1Н, д, J =7,9, Н-6'); 7,38 (1Н, т, J=8,0, Н-5'); 7,19 (1Н, д, J =7,9, Н-4') 8,11 (1H, д, J=8,1, Н6'); 7,95 (1Н, д.д, J=8,1 и 1,8, Н-3'); 7,58 (1H, т.д, J =7,6 и 1,7, Н-4'); 7,21 (3Н, м, Н-5' + SO2NH2) * Спектри ЯМР 1 H варіантів заявлених сполук зареєстровані на приладі Bruker WM-360 (360МГц) в розчині ДМСО-d6, внутрішній стандарт TMC Приклад 7. Токсичність N-R-амідів 1-гідрокси3-оксо-5,6-дигідро-3H-піроло-[3,2,1-i,j]-хінолін-2карбонової кислоти Іа-е визначали на інтактних білих мишах вагою 18-22г по 6 тварин в серії з кожною дозою. Досліджувані речовини вводили у вигляді тонкої водної суспензії, стабілізованої твіном-80, перорально (при високих дозах за 2-3 прийоми з інтервалом 10 хвилин). Кількість тва рин, що вижили, реєстрували кожні 24 години протягом 14 діб. Середньосмертельні дози (LD50) розраховували за методом Cr. Karber [2]. Наведені в табл. 4 дані свідчать про те, що всі заявлені речовини за класифікацією К.К. Сидорова [3] є практично нетоксичними, тоді як гіпотіазид значно поступається їм за цим показником, оскільки за даними літератури [4] його середньосмертельна доза для 7 86286 8 джувані сполуки Іа-е вводили перорально в дозі мишей перорально складає всього лише 40мг/кг (ефективна доза гіпотіазиду) у вигляді тон1175мг/кг. кої водної суспензії, стабілізованої твіном-80. ПісПриклад 8. Діуретична активність заявлених ля цього піддослідні тварини поміщались в "обмінN-R-амідів 1-гідрокси-3-оксо-5,6-дигідро-3H-піролоні клітки". Показником інтенсивності сечовиділення [3,2,1-i,j]-хінолін-2-карбонової кислоти (Іа-е) вивчаслужила кількість сечі, виділена тваринами за 5 лась на білих щурах вагою 180-200г за відомою годин. Дані експерименту, представлені в таблиці методикою [2] паралельно та в порівнянні з гіпоті4, дозволяють зробити висновок, що заявлені споазидом. Всі піддослідні тварини отримували через луки за ступенем діуретичної дії суттєво перевишлунковий зонд водне навантаження з розрахунку щують препарат порівняння гіпотіазид. 50мл/кг. Контрольна група тварин отримували тільки аналогічну кількість води з твіном-80. ДосліТаблиця 4 Токсичність та діуретична активність заявлених сполук в порівнянні з гіпотіазидом Сполука Ia ІБ IВ Iг ІД Ie Гіпотіазид Контроль LD50, мг/кг 5230 5145 5280 5220 5170 5050 1175 Діурез за 5 годин, мл 6,1±0,22 6,8±0,29 6,4±0,25 6,6±0,24 6,5±0,30 6,3±0,28 5,3±0,32 3,3±0,21 Таким чином, заявлено N-R-аміди 1-гідрокси3-оксо-5,6-дигідро-3H-піроло-[3,2,1-i,j]-хінолін-2карбонової кислоти, які виявляють діуретичну активність. Всі заявлені сполуки є практично нетоксичними та суттєво перевищують за діуретичною активністю препарат порівняння гіпотіазид. Всі сполуки одержуються з доступних реагентів та за простими методиками, які можуть бути здійснені в умовах хіміко-фармацевтичних підприємств або лабораторій з використанням стандартного обладнання. Заявлені сполуки можуть бути використані як лікарські субстанції при створенні засобів діуретичної дії у різних лікарських формах. Джерела інформації Комп’ютерна верстка А. Крулевський Діуретична активність, % 184 207 194 200 197 191 161 100 1. М.Д. Машковский / Лекарственные средства. - M.: ООО Новая Волна: издатель С.Б. Дивов, 2002. - Том 1. - С.476. 2. Л.Н. Сернов, В.В. Гацура / Элементы экспериментальной фармакологии. - M.: Медицина, 2000. - С. 117. 3. К.К. Сидоров / О классификации токсичности ядов при парентеральных способах введения // Токсикология новых промышленных химическких веществ. - M.: Медицина, 1973. - Вып. 13. - С.50. 4. A. Kleemann, J. Engel / Pharmaceutical substances. Synthesis, patents, applications. Multimedia Viewer, Version 2.00, Georg Thime Verlag, Stuttgart, 2001. Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійською1-hydroxy-3-oxo-5,6-dihydro-3h-pyrrolo-[3,2,1-ij]-quinoline-2-carboxylic acid n-r-aramides that have diuretic activity
Автори англійськоюUkrainets Ihor Vasyliovych, Berezniakova Natalia Leonidivna, Mospanova Olena Volodymyrivna, Naboka Olha Ivanivna
Назва патенту російськоюN-r-амиды 1-гидрокси-3-оксо-5,6-дигидро-3н-пирроло-[3,2,1-ij]-хинолин-2-карбоновой кислоты, которые проявляют диуретическую активность
Автори російськоюУкраинец Игорь Васильевич, Березнякова Наталья Леонидовна, Моспанова Елена Владимировна, Набока Ольга Ивановна
МПК / Мітки
МПК: C07D 215/22, A61K 31/47
Мітки: виявляють, кислоти, n-r-аміди, 1-гідрокси-3-оксо-5,6-дигідро-3н-піроло-[3,2,1-ij]-хінолін-2-карбонової, активність, діуретичну
Код посилання
<a href="https://ua.patents.su/4-86286-n-r-amidi-1-gidroksi-3-okso-56-digidro-3n-pirolo-321-ij-khinolin-2-karbonovo-kisloti-yaki-viyavlyayut-diuretichnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">N-r-аміди 1-гідрокси-3-оксо-5,6-дигідро-3н-піроло-[3,2,1-ij]-хінолін-2-карбонової кислоти, які виявляють діуретичну активність</a>
Попередній патент: Лінійний приймач
Наступний патент: Пристрій маніпулювання кришками електролізера для виробництва алюмінію електролізом
Випадковий патент: Спосіб виготовлення вакцини проти пастерельозу качок емульсійної інактивованої