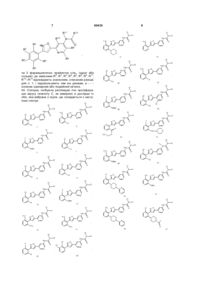
Піридилзаміщені гетероциклічні сполуки, що застосовують для лікування або запобігання інфекції вірусу гепатиту c
Номер патенту: 80435
Опубліковано: 25.09.2007
Автори: Партрідж Джон, Сінг Реджіндер, Генрі Лу, Гофф Дейн
Формула / Реферат
1. Сполука структурної формули (І) або (II):
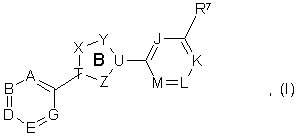
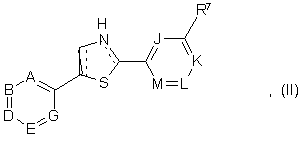
чи її фармацевтично прийнятна сіль, гідрат, сольват або N-оксид, де:
В-кільце являє собою ароматичне або неароматичне кільце, що містить від одного до чотирьох гетероатомів, у якому
X, Y, Z незалежно один від одного вибрані з С, СН, N, NR16, NR18, S або О, за умови, що Х і Y не є обидва О;
U і Т незалежно один від одного вибрані з С або СН;
А означає N або -CR2-;
В означає N або -CR3-;
D означає N або -CR4-;
Е означає N або -CR5-;
G означає N або -CR6-;
J означає N або -CR14-;
К означає N або –CR8-;
L означає N або -CR9-;
М означає N або -CR10-;
R2 і R6 незалежно один від одного вибрані з групи, що складається з водню, галогену, С1-С15алкілу, заміщеного С1-С15алкілу, С1-С15алкілтіо, заміщеного С1-С15алкілтіо, алкокси, заміщеного алкокси, алкоксикарбонілу, заміщеного алкоксикарбонілу, арил-С1-С15 алкілоксикарбонілу, заміщеного арил-С1-С15алкілоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, циклогетероалкілу, заміщеного циклогетероалкілу, карбамоїлу, заміщеного карбамоїлу, галоген-С1-С15алкілу, сульфамоїлу, заміщеного сульфамоїлу і силільного ефіру, за умови, що один із замісників R2 і R6 не є воднем;
R3 і R5 незалежно один від одного вибрані з групи, що складається з водню, галогену, С1-С15алкілу, заміщеного С1-С15алкілу, С1-С15алкілтіо, заміщеного С1-С15алкілтіо, алкокси, заміщеного алкокси, алкоксикарбонілу, заміщеного алкоксикарбонілу, арил-С1-С15алкілоксикарбонілу, заміщеного арил-С1-С15алкілоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, циклогетероалкілу, заміщеного циклогетероалкілу, карбамоїлу, заміщеного карбамоїлу, галоген-С1-С15алкілу, сульфамоїлу і заміщеного сульфамоїлу;
R4 вибраний із групи, що складається з водню, галогену, С1-С15алкілу, заміщеного С1-С15алкілу, С1-С15алкілтіо, заміщеного С1-С15алкілтіо, карбамоїлу, заміщеного карбамоїлу, алкокси, заміщеного алкокси, алкоксикарбонілу, заміщеного алкоксикарбонілу, арилС1-С15алкілоксикарбонілу, заміщеного арилС1-С15алкілоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, діС1-С15алкіламіно, заміщеного діС1-С15алкіламіно, галогенС1-С15алкілу, сульфамоїлу і заміщеного сульфамоїлу;
R7 означає-NR11C(O)R12;
R8, R9, R10 і R14 незалежно один від одного вибрані з групи, що складається з водню і галогену;
R11 являє собою водень або С1-С15алкіл; і
R12 вибраний із групи, що складається з заміщеного С1-С15алкілу, галогенС1-С15алкілу, циклогетероалкілу і заміщеного циклогетероалкілу;
R16 і R18 незалежно один від одного вибрані з групи, що складається з водню, нижчого алкілу, заміщеного нижчого алкілу, нижчого гетероалкілу, заміщеного нижчого гетероалкілу, циклоалкілу, заміщеного циклоалкілу, циклогетероалкілу, заміщеного циклогетероалкілу, нижчого галогеналкілу, нижчого алкілтіо, заміщеного нижчого алкілтіо, нижчого алкокси, заміщеного нижчого алкокси, нижчого гетероалкокси, заміщеного нижчого гетероалкокси, циклоалкокси, заміщеного циклоалкокси, циклогетероалкокси, заміщеного циклогетероалкокси, нижчого галогеналкокси, нижчого ди- або моноалкіламіно, заміщеного нижчого ди- або моноалкіламіно, арилу, заміщеного арилу, арилокси, заміщеного арилокси, арилС1-С15алкілу, заміщеного арилС1-С15алкілу, арилС1-С15алкілокси, заміщеного арилС1-С15алкілокси, гетероарилу, заміщеного гетероарилу, гетероарилокси, заміщеного гетероарилокси, гетероарилС1-С15алкілу, заміщеного гетероарилС1-С15алкілу, гетероарилС1-С15алкілокси, заміщеного гетероарилС1-С15алкілокси, карбоксилу, нижчого алкоксикарбонілу, заміщеного нижчого алкоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, арилС1-С15алкілоксикарбонілу, заміщеного арилС1-С15алкілоксикарбонілу, карбамату, заміщеного карбамату, карбамоїлу, заміщеного карбамоїлу, сульфамоїлу, заміщеного сульфамоїлу та групи формули -L-R17, де "L" є сполучною ланкою, а R17 являє собою циклоалкіл, заміщений циклоалкіл, циклогетероалкіл або заміщений циклогетероалкіл, за умови, що:
(і) щонайменше одна зі змінних А, В, D, Е, G, J, К, L або М означає N;
(іі) не більше ніж одна зі змінних А, В, D, Е або G означає N; і
(ііі) не більше ніж одна зі змінних J, К, L або М означає N.
2. Сполука за п. 1, у якій одна зі змінних А, В, D, Е або G означає N і одна зі змінних J, К, L або М означає N.
3. Сполука за п. 1, у якій одна зі змінних А, В, D, Е або G означає N і ніяка зі змінних J, К, L або М не є N.
4. Сполука за п. 1, у якій ніяка зі змінних А, В, D, Е або G не є N і одна зі змінних J, К, L або М означає N.
5. Сполука за п. 1, у якій В-кільце є оксазолом або його гідроізомером.
6. Сполука за п. 1, у якій В-кільце є тіазолом або його гідроізомером.
7. Сполука за п. 1, у якій В-кільце є імідазолом або його гідроізомером.
8. Сполука за п. 1, у якій В-кільце є триазолом або його гідроізомером.
9. Сполука за п. 1, у якій В-кільце є оксадіазолом або його гідроізомером.
10. Сполука за п. 1, у якій В-кільце є ізоксазолом або його гідроізомером.
11. Сполука за п. 1, у якій В-кільце є піразолом або його гідроізомером.
12. Сполука за п. 1, у якій В-кільце є тіадіазолом або його гідроізомером.
13. Сполука за будь-яким із пунктів 1-12, у яких R7 являє собою –NR11C(O)R12, де R11 означає водень або метил, R12 є -СНСl2.
14. Сполука за п. 13, у якій Х означає N, Y - О, a Z є -СН-.
15. Сполука за п.1, у якій А означає -CR2-, G - -CR6-, R7 є -NR11C(O)R12, де R11 являє собою водень або метил, а R12 означає –СНСl2.
16. Сполука за п. 15, у якій В являє собою -CR3-, D - N, Е - -CR5-, J - -CR14-, К - -CR8-, L - -CR9-, М - -CR10-, а кожний із замісників R3, R5, R9, R10 і R14 є воднем.
17. Сполука за п. 16, у якій R8 означає фтор.
18. Сполука за п. 15, у якій В означає -CR3-, D - -CR4-, E - -CR5-, J - -CR14-, К - -CR8-, L - -CR9-, M - N, а кожний із замісників R3, R4, R5, R8, R9 і R14 є воднем.
19. Сполука за п. 15, у якій В означає -CR3-, D - -CR4-, Е - -CR5-, J - -CR14-, К - -CR8-, L - N, М - -CR10-, а кожний із замісників R3, R4, R5, R8, R10 і R14 є воднем.
20. Сполука за будь-яким із пунктів 15-19, у якій замісники R2 і R6 незалежно один від одного вибрані з групи, що складається з хлору, фтору, метилу, трифторметилу, тіометилу, метокси, ізопропокси, N-морфоліно і N-морфоліносульфамоїлу.
21. Сполука за будь-яким із пунктів 15-19, у якій замісники R2 і R6 незалежно один від одного вибрані з групи, що складається з хлору, фтору, метилу, трифторметилу, метокси або ізопропокси.
22. Сполука за будь-яким із пунктів 15-19, у якій замісники R2 і R6 є однаковими або різними атомами галогену.
23. Сполука за будь-яким із пунктів 15-19, у якій Х являє собою N, Y - О, a Z є -СН-.
24. Сполука за п. 1, у якій А являє собою -CR2-, G - -CR6-, а R7 є -NR11C(O)R12, де R11 означає водень або метил, а R12 - -СН2І.
25. Сполука за п. 24, у якій замісники R2 і R6 незалежно один від одного вибрані з групи, що складається з хлору, фтору, метилу, трифторметилу, тіометилу, метокси, ізопропокси, N-морфоліно і N-морфоліносульфамоїлу.
26. Сполука за п. 24, у якій замісники R2 і R6 незалежно один від одного вибрані з групи, що складається з хлору, фтору, метилу, трифторметилу, метокси і ізопропокси.
27. Сполука за п. 24, у якій замісники R2 і R6 є однаковими або різними атомами галогену.
28. Сполука за п. 24, у якій Х означає N, Y - О, а Z є -СН-.
29. Сполука за п. 1, у якій А означає -CR2-, В - -CR3-, R7 - -NR11C(O)R12, де R11 є воднем або метилом, а R12 являє собою -СНСl2.
30. Сполука за п. 29, у якій D означає -CR4-, G - -CR6-, Е - -CR5-, J - -CR14-, К - -CR8-, L - -CR9-, М - N, а кожний із замісників R4, R5, R6, R8, R9 і R14 є воднем.
31. Сполука за п. 29, у якій D означає -CR4-, G - -CR6-, Е - -CR5-, J - -CR14-, К - -CR8-, L - N, М - -CR10-, а кожний із замісників R4, R5, R6, R8, R10 і R14 є воднем.
32. Сполука за кожним із пунктів 29-31, у якій R2 означає хлор, фтор, метил, трифторметил, тіометил, метокси, ізопропокси, N-морфоліно або N-морфоліносульфамоїл, а R3 є хлором, фтором, метилом, трифторметилом або метокси.
33. Сполука за будь-яким із пунктів 29-31, у якій R2 означає хлор, фтор, метил, трифторметил або метокси, а R3 є хлором, фтором або трифторметилом.
34. Сполука за будь-яким із пунктів 29-31, у якій замісники R2 і R3 є однаковими або різними атомами галогену.
35. Сполука за будь-яким із пунктів 29-31, у якій Х означає N, Y - О, a Z є -СН-.
36. Сполука за п. 1, у якій А означає -CR2-, G - -CR6-, а замісники R2 і R6 є однаковими, за умови, що R2 і R6 не означають водень.
37. Сполука за п. 1, у якій А означає –CR2-, В - -CR3-, а замісники R2 і R3 є однаковими, за умови, що R і R3 не означають водень.
38. Сполука за п. 1, у якій В означає -CR3-, Е - -CR5-, а замісники R3 і R5 є однаковими, за умови, що R і R5 не означають водень.
39. Сполука за п. 1, у якій В означає -CR3-, D - -CR4-, Е - -CR5-, J - -CR14-, К - -CR8-, а кожний із замісників R3, R4, R5, R8 і R14 означає водень.
40. Сполука за п. 1, у якій -D означає -CR4-, Е - -CR5-, G - CR6, J - -CR14-, К - -CR8-, а кожний із замісників R4, R5, R6, R8' R14 означає водень.
41. Сполука за п. 1, що має структурну формулу (Іa), (Ib), (Ic), (Id) або (Іе):
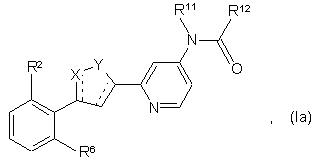
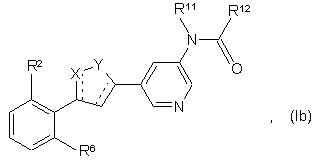
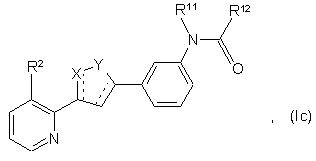
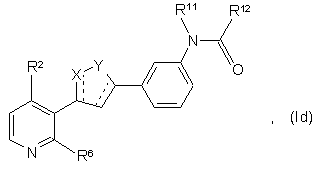
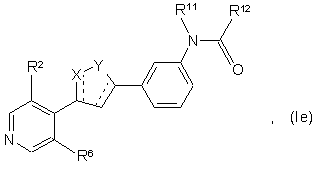
або її фармацевтично прийнятна сіль, гідрат або сольват, де X, Y, R2, R6, R11 і R12 відповідають значенням, описаним раніше для п. 1, а - - - означає одинарний або подвійний зв'язок.
42. Сполука за п. 41, у якій R11 означає водень, R1 - дихлорметил, а R2 і R незалежно один від одного вибрані з групи, що складається з фтору, хлору, трифторметилу та метокси.
43. Сполука за п. 1, що має структурну формулу (If):
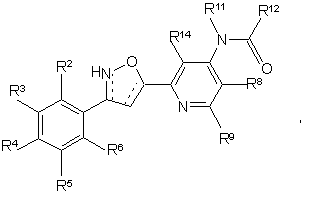
чи її фармацевтично прийнятна сіль, гідрат або сольват, де замісники R2, R3, R4, R5, R6, R8, R9, R11, R12 і R14 відповідають значенням, описаним раніше для п. 1, і задовольняють тим же умовам, а - - - означає одинарний або подвійний зв'язок.
44. Сполука, інгібуюча реплікацію і/чи проліферацію вірусу гепатиту С, як виміряно в дослідах in vitro, яка вибрана з групи, що складається з наступних сполук:
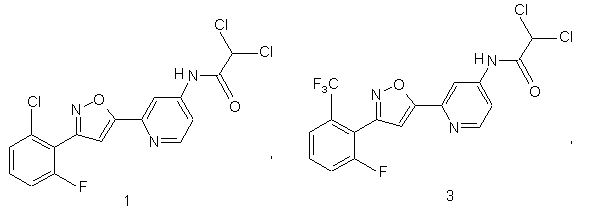
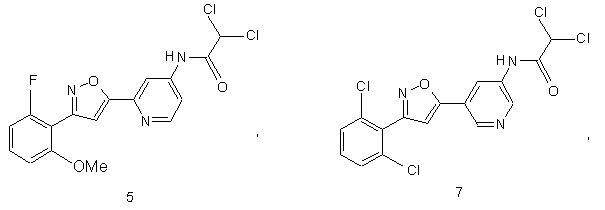
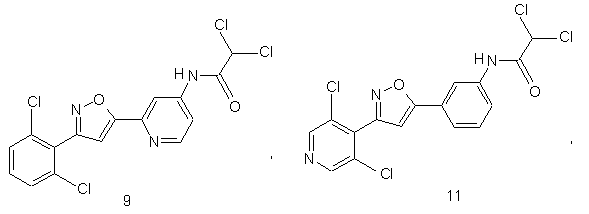

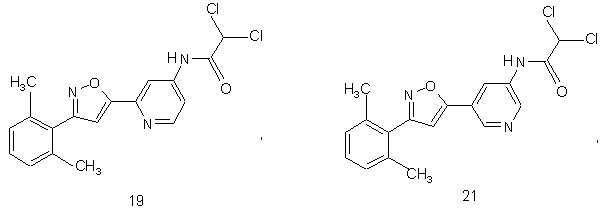
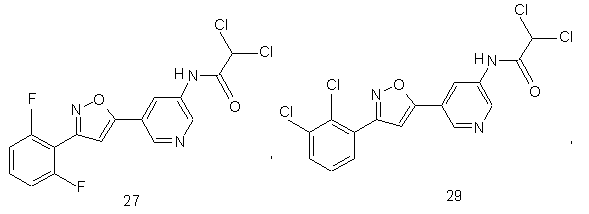
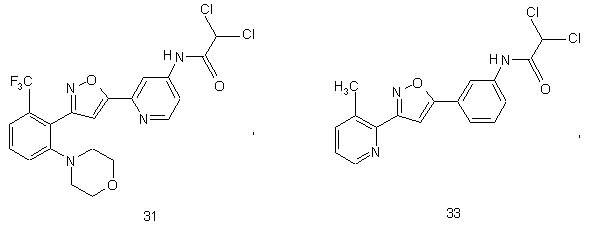
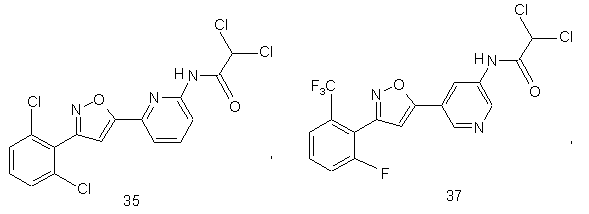
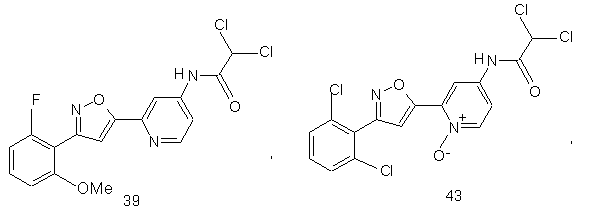
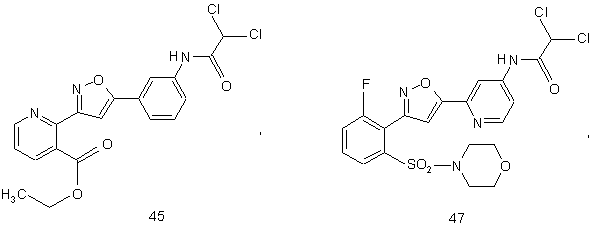
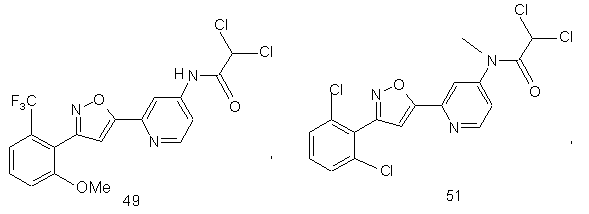

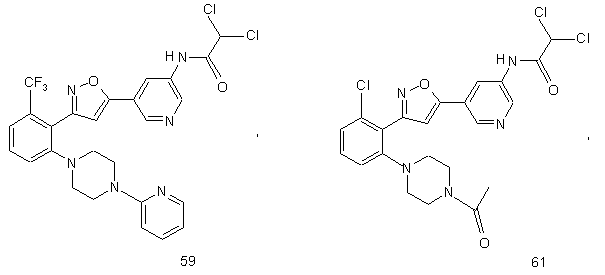
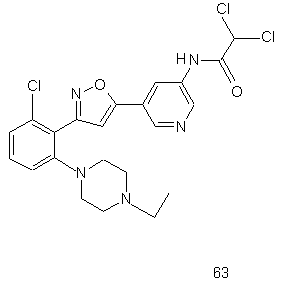 .
.
45. Композиція, що містить сполуку за будь-яким із пунктів 1-44 і фармацевтично прийнятний наповнювач.
46. Спосіб інгібування або реплікації проліферації віріону гепатиту С, при якому проводять взаємодію віріону гепатиту С з кількістю сполуки за кожним з пунктів 1-44 або композиції за п. 45, що інгібує реплікацію віріону гепатиту С.
47. Спосіб за п. 46, що здійснюють in vitro.
48. Спосіб за п. 46, що здійснюють in vivo.
49. Спосіб лікування або попередження інфекції вірусу гепатиту С, при якому вводять суб'єкту ефективну кількість сполуки за будь-яким із пунктів 1-44 або композиції за п. 45, ефективних для лікування або попередження інфекції вірусу гепатиту С.
50. Спосіб за п. 49, де суб'єктом є людина.
51. Спосіб за п. 49, де сполуку вводять у кількості від 0,1 мг/кг до 200 мг/кг.
52. Спосіб за п. 49, де сполуку вводять у кількості від 10 мг/кг до 100 мг/кг.
53. Спосіб за п. 49, де сполуку вводять перорально.
54. Спосіб за п. 49, де сполуку вводять шляхом ін'єкції.
55. Спосіб за п, 49, де вводять сполуку, яка інгібує реплікацію і/чи проліферацію вірусу гепатиту С як виміряно в дослідах in vitro та яка вибрана з групи, що складається з:

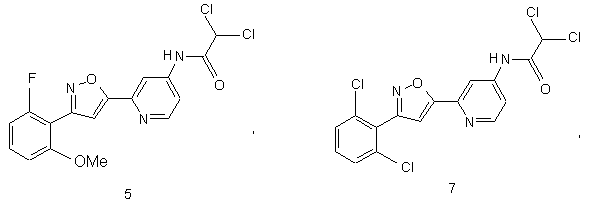


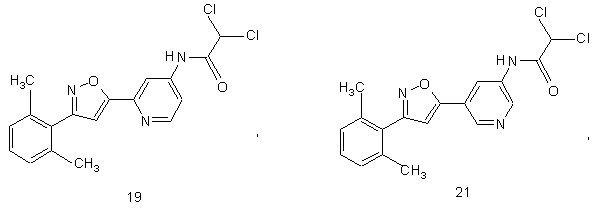



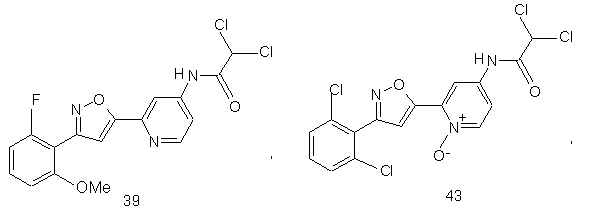
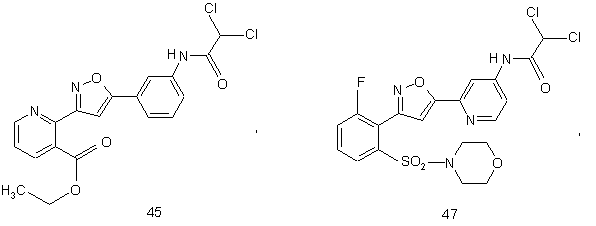
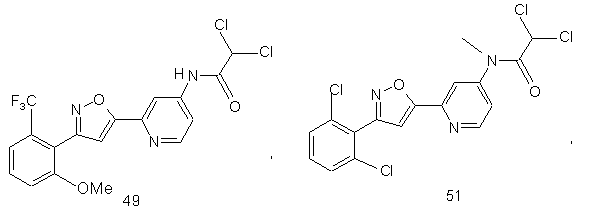

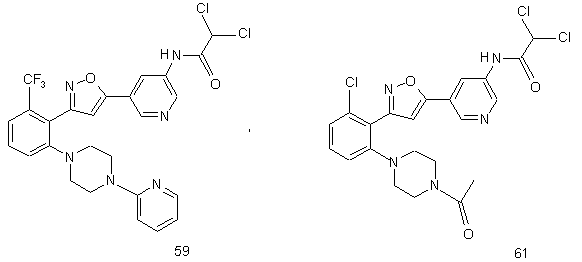 і
і
 .
.
56. Спосіб за п. 49, який застосовують терапевтично до суб'єкта, що має інфекцію вірусу гепатиту С.
57. Спосіб за п. 49, який застосовують профілактично до суб'єкта, що піддається ризику розвитку інфекції вірусу гепатиту С.
Текст
1. Сполука структурної формули (І) або (II): R7 3 за умови, що один із замісників R2 і R6 не є воднем; R3 і R5 незалежно один від одного вибрані з групи, що складається з водню, галогену, С1-С15алкілу, заміщеного С 1-С15алкілу, С1-С15алкілтіо, заміщеного С1-С15алкілтіо, алкокси, заміщеного алкокси, алкоксикарбонілу, заміщеного алкоксикарбонілу, арил-С1-С15алкілоксикарбонілу, заміщеного арилС1-С15алкілоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, циклогетероалкілу, заміщеного циклогетероалкілу, карбамоїлу, заміщеного карбамоїлу, галоген-С1-С15алкілу, сульфамоїлу і заміщеного сульфамоїлу; R4 вибраний із групи, що складається з водню, галогену, С1-С15алкілу, заміщеного С1-С15алкілу, С1-С15алкілтіо, заміщеного С1-С15алкілтіо, карбамоїлу, заміщеного карбамоїлу, алкокси, заміщеного алкокси, алкоксикарбонілу, заміщеного алкоксикарбонілу, арилС1-С15алкілоксикарбонілу, заміщеного арилС1-С15алкілоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, діС1С15алкіламіно, заміщеного діС1-С15алкіламіно, галогенС1-С15алкілу, сульфамоїлу і заміщеного сульфамоїлу; R7 означає-NR11C(O)R12; R8, R9, R10 і R14 незалежно один від одного вибрані з групи, що складається з водню і галогену; R11 являє собою водень або С1-С15алкіл; і R12 вибраний із групи, що складається з заміщеного С1-С15алкілу, галогенС1-С15алкілу, циклогетероалкілу і заміщеного циклогетероалкілу; R16 і R18 незалежно один від одного вибрані з групи, що складається з водню, нижчого алкілу, заміщеного нижчого алкілу, нижчого гетероалкілу, заміщеного нижчого гетероалкілу, циклоалкілу, заміщеного циклоалкілу, циклогетероалкілу, заміщеного циклогетероалкілу, нижчого галогеналкілу, нижчого алкілтіо, заміщеного нижчого алкілтіо, нижчого алкокси, заміщеного нижчого алкокси, нижчого гетероалкокси, заміщеного нижчого гетероалкокси, циклоалкокси, заміщеного циклоалкокси, циклогетероалкокси, заміщеного циклогетероалкокси, нижчого галогеналкокси, нижчого ди- або моноалкіламіно, заміщеного нижчого ди- або моноалкіламіно, арилу, заміщеного арилу, арилокси, заміщеного арилокси, арилС1-С15алкілу, заміщеного арилС1-С15алкілу, арилС1-С15алкілокси, заміщеного арилС1-С15алкілокси, гетероарилу, заміщеного гетероарилу, гетероарилокси, заміщеного гетероарилокси, гетероарилС1-С15алкілу, заміщеного гетероарилС1-С15алкілу, гетероарилС1С15алкілокси, заміщеного гетероарилС1С15алкілокси, карбоксилу, нижчого алкоксикарбонілу, заміщеного нижчого алкоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, арилС1-С15алкілоксикарбонілу, заміщеного арилС1-С15алкілоксикарбонілу, карбамату, заміщеного карбамату, карбамоїлу, заміщеного карбамоїлу, сульфамоїлу, заміщеного сульфамоїлу та групи формули -L-R17, де "L" є сполучною ланкою, а R17 являє собою циклоалкіл, заміщений циклоалкіл, циклогетероалкіл або заміщений циклогетероалкіл, за умови, що: (і) щонайменше одна зі змінних А, В, D, Е, G, J, К, L або М означає N; 80435 4 (іі) не більше ніж одна зі змінних А, В, D, Е або G означає N; і (ііі) не більше ніж одна зі змінних J, К, L або М означає N. 2. Сполука за п. 1, у якій одна зі змінних А, В, D, Е або G означає N і одна зі змінних J, К, L або М означає N. 3. Сполука за п. 1, у якій одна зі змінних А, В, D, Е або G означає N і ніяка зі змінних J, К, L або М не є N. 4. Сполука за п. 1, у якій ніяка зі змінних А, В, D, Е або G не є N і одна зі змінних J, К, L або М означає N. 5. Сполука за п. 1, у якій В-кільце є оксазолом або його гідроізомером. 6. Сполука за п. 1, у якій В-кільце є тіазолом або його гідроізомером. 7. Сполука за п. 1, у якій В-кільце є імідазолом або його гідроізомером. 8. Сполука за п. 1, у якій В-кільце є триазолом або його гідроізомером. 9. Сполука за п. 1, у якій В-кільце є оксадіазолом або його гідроізомером. 10. Сполука за п. 1, у якій В-кільце є ізоксазолом або його гідроізомером. 11. Сполука за п. 1, у якій В-кільце є піразолом або його гідроізомером. 12. Сполука за п. 1, у якій В-кільце є тіадіазолом або його гідроізомером. 13. Сполука за будь-яким із пунктів 1-12, у яких R7 являє собою –NR11C(O)R12, де R11 означає водень або метил, R12 є -СНСl2. 14. Сполука за п. 13, у якій Х означає N, Y - О, a Z є -СН-. 15. Сполука за п.1, у якій А означає -CR2-, G - CR6-, R7 є -NR11C(O)R12, де R11 являє собою водень або метил, а R12 означає –СНСl2. 16. Сполука за п. 15, у якій В являє собою -CR3-, D - N, Е - -CR5-, J - -CR14-, К - -CR8-, L - -CR9-, М - CR10-, а кожний із замісників R3, R5, R9, R10 і R14 є воднем. 17. Сполука за п. 16, у якій R8 означає фтор. 18. Сполука за п. 15, у якій В означає -CR3-, D - CR4-, E - -CR5-, J - -CR14-, К - -CR8-, L - -CR9-, M - N, а кожний із замісників R3, R4, R5, R8, R9 і R14 є воднем. 19. Сполука за п. 15, у якій В означає -CR3-, D - CR4-, Е - -CR5-, J - -CR14-, К - -CR8-, L - N, М - CR10-, а кожний із замісників R3, R4, R5, R8, R10 і R14 є воднем. 20. Сполука за будь-яким із пунктів 15-19, у якій замісники R2 і R6 незалежно один від одного вибрані з групи, що складається з хлору, фтору, метилу, трифторметилу, тіометилу, метокси, ізопропокси, N-морфоліно і N-морфоліносульфамоїлу. 21. Сполука за будь-яким із пунктів 15-19, у якій замісники R2 і R6 незалежно один від одного вибрані з групи, що складається з хлору, фтору, метилу, трифторметилу, метокси або ізопропокси. 22. Сполука за будь-яким із пунктів 15-19, у якій замісники R2 і R6 є однаковими або різними атомами галогену. 23. Сполука за будь-яким із пунктів 15-19, у якій Х являє собою N, Y - О, a Z є -СН-. 5 24. Сполука за п. 1, у якій А являє собою -CR2-, G -CR6-, а R7 є -NR11C(O)R12, де R11 означає водень або метил, а R12 - -СН2І. 25. Сполука за п. 24, у якій замісники R2 і R6 незалежно один від одного вибрані з групи, що складається з хлору, фтору, метилу, трифторметилу, тіометилу, метокси, ізопропокси, N-морфоліно і Nморфоліносульфамоїлу. 26. Сполука за п. 24, у якій замісники R2 і R6 незалежно один від одного вибрані з групи, що складається з хлору, фтору, метилу, трифторметилу, метокси і ізопропокси. 27. Сполука за п. 24, у якій замісники R2 і R6 є однаковими або різними атомами галогену. 28. Сполука за п. 24, у якій Х означає N, Y - О, а Z є -СН-. 29. Сполука за п. 1, у якій А означає -CR2-, В - CR3-, R7 - -NR11C(O)R12, де R11 є воднем або метилом, а R12 являє собою -СНСl2. 30. Сполука за п. 29, у якій D означає -CR4-, G - CR6-, Е - -CR5-, J - -CR14-, К - -CR8-, L - -CR9-, М - N, а кожний із замісників R4, R5, R6, R8, R9 і R14 є воднем. 31. Сполука за п. 29, у якій D означає -CR4-, G - CR6-, Е - -CR5-, J - -CR14-, К - -CR8-, L - N, М - -CR10, а кожний із замісників R4, R5, R6, R8, R10 і R14 є воднем. 32. Сполука за кожним із пунктів 29-31, у якій R2 означає хлор, фтор, метил, трифторметил, тіометил, метокси, ізопропокси, N-морфоліно або Nморфоліносульфамоїл, а R3 є хлором, фтором, метилом, трифторметилом або метокси. 33. Сполука за будь-яким із пунктів 29-31, у якій R2 означає хлор, фтор, метил, трифторметил або метокси, а R3 є хлором, фтором або трифторметилом. 34. Сполука за будь-яким із пунктів 29-31, у якій замісники R2 і R3 є однаковими або різними атомами галогену. 35. Сполука за будь-яким із пунктів 29-31, у якій Х означає N, Y - О, a Z є -СН-. 36. Сполука за п. 1, у якій А означає -CR2-, G - CR6-, а замісники R2 і R6 є однаковими, за умови, що R2 і R6 не означають водень. 37. Сполука за п. 1, у якій А означає –CR2-, В - CR3-, а замісники R2 і R3 є однаковими, за умови, що R і R3 не означають водень. 38. Сполука за п. 1, у якій В означає -CR3-, Е - CR5-, а замісники R3 і R5 є однаковими, за умови, що R і R5 не означають водень. 39. Сполука за п. 1, у якій В означає -CR3-, D - CR4-, Е - -CR5-, J - -CR14-, К - -CR8-, а кожний із замісників R3, R4, R5, R8 і R14 означає водень. 40. Сполука за п. 1, у якій -D означає -CR4-, Е - CR5-, G - CR6, J - -CR14-, К - -CR8-, а кожний із замісників R4, R5, R6, R8' R14 означає водень. 41. Сполука за п. 1, що має структурну формулу (Іa), (Ib), (Ic), (Id) або (Іе): 80435 6 R11 R12 N R2 X Y O N , (Ia) , (Ib) , (Ic) , (Id) , (Ie) R6 R11 R12 N R2 X Y O N R6 R11 R12 N R2 X Y O N R11 R12 N R2 N X Y O R6 R11 R12 N R2 N X Y O R6 або її фармацевтично прийнятна сіль, гідрат або сольват, де X, Y, R2, R6, R11 і R12 відповідають значенням, описаним раніше для п. 1, а - - - означає одинарний або подвійний зв'язок. 42. Сполука за п. 41, у якій R11 означає водень, R1 - дихлорметил, а R2 і R незалежно один від одного вибрані з групи, що складається з фтору, хлору, трифторметилу та метокси. 43. Сполука за п. 1, що має структурну формулу (If): 7 80435 R11 R14 R2 R3 Cl R12 HN O N O O H 3C N R8 N O O , , N N O , 33 31 R9 R6 Cl HN F 3C N R4 Cl Cl N O HN 8 Cl Cl Cl Cl HN R5 чи її фармацевтично прийнятна сіль, гідрат або сольват, де замісники R2, R3, R4, R5, R6, R8, R9, R11, R12 і R14 відповідають значенням, описаним раніше для п. 1, і задовольняють тим же умовам, а - - означає одинарний або подвійний зв'язок. 44. Сполука, інгібуюча реплікацію і/чи проліферацію вірусу гепатиту С, як виміряно в дослідах in vitro, яка вибрана з групи, що складається з наступних сполук: O N N O O , N N Cl H3C O O N N O Cl 51 49 Cl N O OMe 57 53 Cl Cl CF 3 N O O CH 3 , Cl Cl Cl HN N N O O N , N N N O Cl Cl Cl , 59 21 HN HN O N N CH 3 19 27 O N N , N N HN H 3C Cl HN Cl O , N , Cl O O N N 17 O O Cl 13 N N O HN F CF3 O N Cl N Cl HN , , O , , HN HN O O Cl Cl N O Cl Cl Cl F N N OMe N Cl N O N N N H 3C Cl Cl O Cl O , O Cl OMe O Cl O N 47 , Cl F O N 11 HN O O , , N Cl HN N 9 F F O Cl Cl Cl HN 45 F3C Cl N Cl HN Cl N 43 39 HN Cl Cl OMe , O Cl SO2 7 O , O Cl N N Cl HN O + N O N 5 O , O , OMe N O Cl Cl Cl Cl O Cl HN O Cl HN N Cl Cl N Cl HN N HN F N 1 Cl Cl 3 O 37 35 Cl , Cl F Cl F F , F O N N O , HN F3C O N O N Cl Cl HN F3C N O N Cl Cl Cl Cl HN O O Cl N , 29 , 61 9 80435 10 Cl Cl Cl Cl HN Cl N Cl O F O N 17 Cl Cl Cl N HN O N O H 3C N . 45. Композиція, що містить сполуку за будь-яким із пунктів 1-44 і фармацевтично прийнятний наповнювач. 46. Спосіб інгібування або реплікації проліферації віріону гепатиту С, при якому проводять взаємодію віріону гепатиту С з кількістю сполуки за кожним з пунктів 1-44 або композиції за п. 45, що інгібує реплікацію віріону гепатиту С. 47. Спосіб за п. 46, що здійснюють in vitro. 48. Спосіб за п. 46, що здійснюють in vivo. 49. Спосіб лікування або попередження інфекції вірусу гепатиту С, при якому вводять суб'єкту ефективну кількість сполуки за будь-яким із пунктів 144 або композиції за п. 45, ефективних для лікування або попередження інфекції вірусу гепатиту С. 50. Спосіб за п. 49, де суб'єктом є людина. 51. Спосіб за п. 49, де сполуку вводять у кількості від 0,1 мг/кг до 200 мг/кг. 52. Спосіб за п. 49, де сполуку вводять у кількості від 10 мг/кг до 100 мг/кг. 53. Спосіб за п. 49, де сполуку вводять перорально. 54. Спосіб за п. 49, де сполуку вводять шляхом ін'єкції. 55. Спосіб за п, 49, де вводять сполуку, яка інгібує реплікацію і/чи проліферацію вірусу гепатиту С як виміряно в дослідах in vitro та яка вибрана з групи, що складається з: O N O N N O N O N N , O 33 31 Cl Cl Cl Cl HN Cl F3C N O N HN N O O F Cl 37 35 Cl Cl Cl Cl HN F N HN Cl O N O O , Cl 43 Cl Cl Cl HN O HN F O N , O N SO2 N 45 47 Cl Cl , HN F3C N O Cl N O O N , Cl , 11 N Cl O N OMe O Cl , O O Cl N O Cl O , O 39 HN N O + N N O Cl , , H3C O Cl Cl O N , Cl O O N N 7 HN O , Cl 9 H 3C O N 5 Cl F 3C Cl HN Cl OMe N Cl HN Cl , O Cl HN Cl N 29 27 Cl N HN , , N Cl O O N Cl 3 Cl N F O N Cl N F 1 O O , , HN Cl O N O N Cl Cl OMe O Cl HN F , 21 Cl HN F3C O CH 3 19 Cl Cl HN O N CH 3 Cl Cl N , 63 Cl Cl HN H 3C N , , 13 N F O N OMe F F O N O N N HN HN O N Cl Cl Cl 49 51 , 11 80435 Cl Cl Cl Cl Cl HN Cl N O 12 Cl HN CF3 O N O HN O N , N Cl N O O , N OMe N N N N 57 53 Cl Cl Cl Cl HN CF3 N O HN Cl O N N O O N , N N N N N 63 . 56. Спосіб за п. 49, який застосовують терапевтично до суб'єкта, що має інфекцію вірусу гепатиту С. 57. Спосіб за п. 49, який застосовують профілактично до суб'єкта, що піддається ризику розвитку інфекції вірусу гепатиту С. O 59 61 і За даною заявкою заявляється пріоритет згідно [§119(е) Розділу 35 Кодексу Законів США за датою подання 23 серпня 2002 р. заявки з номером No. 60/405467, за датою подання 11 жовтня 2002 р. заявки з номером No. 60/417,837 і за датою подання 15 травня 2003 р. заявки з номером No. 60/ 471,373], зміст яких включено тут за допомогою посилань. Даний винахід відноситься до піридилзаміщених гетероциклічних сполук і композицій, що вміщають їх в собі, придатних для лікування чи попередження інфекцій вірусу гепатиту С (HCV). Зокрема, даний винахід відноситься до піридилзаміщених гетероциклічних сполук і відповідних гідроізомерів, їхніх композицій і використання таких сполук та композицій для інгібування реплікації і/чи проліферації вірусу гепатиту С як терапевтичний підхід при лікуванні і/чи запобіганні інфекцій вірусу гепатиту С у людей і тварин. Інфекція вірусу гепатиту С (HCV) є загальною проблемою здоров'я людини, тільки в Сполучених Штатах щорічно реєструється приблизно 150000 нових випадків захворювання. HCV являє собою вірус з однонитковою РНК, що є етіологічним агентом (збудником), ідентифікованим у більшості випадків посттрансфузійнного і пост/трансплантаційного гепатиту не А типу і не В типу, і є загальною причиною гострого спорадичного гепатиту [Choo et αϊ, Science 244:359, 1989; Kuo et al, Science 244:362, 1989; і Alter et al, у роботі Current Perspective in Hepatology (Сучасні перспективи гепатології), стор. 83, 1989)]. Установлено, що більше 50% пацієнтів, інфікованих HCV, стають хронічно інфікованими, і в 20% з них протягом 20 років розвивається цироз печінки [Davis et al., New Engl. J. Med. 321:1501, 1989; Alter et al, у роботі Current Perspective in Hepatolog (Сучасні перспективи гепатології), стор. 83, 1989; Alter et al., New Engl. J. Med. 327:1899, 1992; і Dienstag Gastroenterology 85:430, 1983]. Більш того, єдиною терапією, придатною для лікування HCV-інфекції, є інтерферон-α (INTRON® A, PEG-INTRON®A, Schering-Plough; ROFERON-A®, Roche]. Більшість пацієнтів, однак, є толерантними, а серед тих, хто піддається лікуванню, існує висока частота рецидивів протягом 6-12 місяців після припинення лікування [Liang et al., J. Med. Virol. 40:69, 1993]. Клінічні іспити показали, що рибавірин, аналог гуаназіну із широким спектром активності у відношенні багатьох РНК і ДНК вірусів, є ефективним проти хронічної HCV-інфекції при використанні його в комбінації з інтерфероном-α [див., наприклад, Poynard et al., Lancet 352:1426-1432, 1998; Reichard et al, Lancet 351:83-87, 1998], і така комбінована терапія була недавно апробірувана (REBETRON, Schering-Plough). Однак ступінь реакції є все-таки значно нижче 50%. Отже, існує потреба в нових сполуках для лікування і попередження HCV-інфекції. Відповідно до одного з аспектів, даний винахід представляє піридилзаміщені гетероциклічні сполуки, що є сильними інгібіторами реплікації і/чи проліферації вірусу гепатиту С («HCV»). Згідно одного зі здійснень, сполуки являють собою піридилзаміщені гетероциклічні сполуки й їхні гідроізомери по В-кільцю у відповідності зі структурною формулою (І), що має наступні «кільцеві» і числові позначення: де кільце В є ароматичним чи неароматичним кільцем, що містить від одного до чотирьох гетероатомів. Кожний із замісників Χ, Υ, Ζ, незалежно один від одного, вибрані з С, СН, N, NR16, NR18, S 13 чи О, a U і Τ незалежно один від одного вибрані з С, СН чи Ν, за умови, що X і Υ не є обоє О. Одне з кілець "А" чи "С" є піридильним кільцем, а інше фенильним чи піридильним. Якщо "А" і/чи "С" означає піридил, кільце може бути приєднане до зображеного кільця "В" за допомогою будь-якого доступного атома вуглецю. Таким чином, кільця "А" і/чи "С" можуть являти собою пірид-2-ил, пірид3-ил чи пірид-4-ил. Кільце "А" містить замісник, розташований в opwo-положенні щодо місця приєднання (2'- чи 6'положення), і може містити ще від 1 до 4 замісників. Природа замісників може бути дуже різноманітною. Типові замісні групи, що використовуються для заміщення в кільці "А", включають галоген, фтор, хлор, алкіл, алкілтіо, алкокси, алкоксикарбоніл, арилалкілоксикарбоніл, арилоксикарбоніл, циклогетероалкіл, карбамоіл, галогеналкіл, діалкіламіно- чи сульфамоільну групи, а також їхні заміщені варіанти. Відповідно до одного зі здійснень, кільце "А" є дізамісним по 2'- і 6'-положенням і не заміщено по всіх інших положеннях. Кільце "С" містить позначку-замісник (3" чи 5") формули -NRnC(O)R12, де R1 означає водень, алкіл чи метил, a R1 являє собою заміщений алкіл, галогеналкіл, дигалогенметил, дихлорметил, циклогетероалкіл чи заміщений циклогетероалкіл. Відповідно до одного зі здійснень, R12 являє собою галогеналкіл чи дихлорметильну групу. Кільце "С" також може бути заміщене по одному чи більш положеннях 2"-, 4"-, 5"- і/чи 6" однаковими чи різними атомами галогену. Фахівцям зрозуміло, що фактичний електронний розподіл чи характер подвійного зв'язку в кільці "В" буде залежати від природи замісників Χ, Υ, Ζ, Τ і/чи U. Мається на увазі, що зображена структурна формула (І), зокрема, включає, щонайменше, наступні шість структур: 80435 14 де А, В, D, Е, G, J, К, L, М, R11 і R12 визначені нижче. Мається на увазі, що зображена структурна формула (І), включає, наприклад, щонайменше, наступні гідроізомери В-кільця: 15 де А, В, D, Е, G, J, К, L, М, R11, R12, R16 і R18 визначені нижче. Відповідно до іншого аспекту, даний винахід представляє композиції, що включають сполуки винаходу. У більшості випадків композиції включають піридилзамещену гетероциклічну сполуку чи гідроізомер (як визначено в описі винаходу) винаходу чи його сіль, гідрат, сольват або N-оксид і прийнятний наповнювач, носій чи розріджувач. Композиції можуть бути виготовлені для використання у ветеринарії чи для лікування людей. Сполуки винаходу є сильними інгібіторами реплікації і/чи проліферації HCV. Таким чином, згідно ще одного аспекту, даний винахід представляє способи інгібування реплікації і/чи проліферації HCV, що включають взаємодію виріона гепатиту С з кількістю сполуки чи композиції винаходу, ефективним для інгібування реплікації і/чи проліферації HCV. Способи можуть бути здійснені in vitro чи in vivo і можуть використовуватися як терапевтичний підхід до лікування і/чи попередження інфекцій вірусу гепатиту С (HCV-інфекцій). Згідно останнього аспекту, даний винахід представляє способи лікування і/чи запобігання інфекції вірусу гепатиту С. У більшості випадків способи включають введення суб'єкту, що має HCV-інфекцію ризику чи тому, хто піддається зараженню HCV-інфекцією, кількість сполуки чи композиції винаходу, ефективної для лікування чи запобігання HCV-інфекції. Спосіб може бути використаний для лікування людей. На Фіг.1 представлені типові сполуки винаходу; і на Фіг.2-63 представлені приклади схем синтезу сполук винаходу. Докладний опис кращих здійснень винаходу Визначення У даному контексті передбачається, що наступні терміни мають наступні значення: "Алкіл," сам по собі чи як частина іншого замісника, відноситься до насичених чи ненасичених, розгалужених, нерозгалужених чи циклічних одновалентних вуглевоних радикалів, що утворені відщепленням одного атома водню від окремого атома вуглецю вихідного алкану, алкену чи алкіну. Типові алкільні групи включають, не вичерпуючись переліком, метил; етил, такі як етаніл, етеніл, етиніл; пропіли, такі як пропан-1-іл, пропан-2-іл, циклопропан-1-іл, проп-1-ен-1-іл, проп-1-ен-2-іл, проп2-ен-1-іл (аліл), циклопроп-1-ен-1-іл; циклопроп-2ен-1-іл, проп-1-ин-1-іл, проп-2-ин-1-ил і т.д.; бутили, такі як бутан-1-іл, бутан-2-іл, 2-метилпропан-1іл, 2-метилпропан-2-іл, циклобутан-1-іл, бут-1-ен 80435 16 1-іл, бут-1-ен-2-іл, 2-метилпроп-1-ен-1-іл, бут-2-ен1-іл , бут-2-ен-2-іл, буту-1,3-діен-1-іл, буту-1,3-діен2-іл, циклобут-1-ен-1-іл, циклобут-1-ен-З-іл, циклобута-1,3-діен-1-іл, бут-1-ин-1-іл, бут-1-ин-З-іл, бут3-ин-1-іл і т.д.; тощо. Зокрема, мається на увазі, що термін "алкіл" включає групи, що мають будь-який ступінь чи рівень насиченості, тобто групи, що містять тільки одинарні вуглець-вуглецеві зв'язки, групи, що містять один чи більш подвійний вуглець-вуглецевий зв'язок, групи, що містять одну чи більш потрійний вуглець-вуглецевий зв'язок, і групи, що містять суміш одинарних, подвійних і потрійних вуглецьвуглецевих зв'язків. Якщо мається на увазі конкретний рівень насиченості, то використовують вирази "алканіл," "алкеніл" і "алкиніл". Переважно, щоб алкільна група включала від 1 до 15 атомів вуглецю (C1-C15-алкил ), більш переважно - від 1 до 10 атомів вуглецю (С1-С15-алкил) і ще більш переважно - від 1 до 6 атомів вуглецю (С1-С 6-алкіл чи нижчий алкіл). "Алканіл," сам по собі чи як частина іншого замісника, відноситься до насиченого розгалуженого, нерозгалуженого чи циклічного алкільного радикала, отриманого відщепленням одного атома водню від окремого атома вуглецю вихідного алкана. Типові алканильні групи включають, не вичерпуючись переліком, метаніл; етаніл; пропаніли, такі як пропан-1-іл, пропан-2-іл (ізопропіл), циклопропан-1-іл і т.д.; бутаніли, такі як бутан-1-іл, бутан-2-іл (втор-бутил), 2-метилпропан-1-іл (ізобутил), 2-метилпропан-2-іл (трет-бутил), циклобутан1-іл і т.д.; тощо. "Алкеніл," сам по собі чи як частина іншого замісника, відноситься до ненасиченого розгалудженого, нерозгалудженого чи циклічного алкільного радикала, що містить, щонайменше, один подвійний вуглець-вуглецевий зв'язок, отриманий відщепленням одного атома водню від окремого атома вуглецю вихідного алкена. Група може знаходитися в ще- чи транс-конформації щодо подвійного зв'язку (зв'язків). Типові алкенільні групи включають, не вичерпуючись переліком, етеніл; пропеніли, такі як проп-1-ен-1-іл , проп-1-ен-2-іл, проп-2ен-1-іл (аліл), проп-2-ен-2-іл, циклопроп-1-ен-1-іл; циклопроп-2-ен-1-іл ; бутеніли, такі як бут-1-ен-1іл, бут-1-ен-2-іл, 2-метил-проп-1-ен-1-іл, бут-2-ен1-іл , бут-2-ен-1-іл, бут-2-ен-2-іл, буту-1,3-дієн-1-іл, буту-1,3-дієн-2-іл, циклобут-1-ен-1-іл, циклобут-1ен-3-іл, циклобута-1,3-дієн-1-іл і т.д.; тощо. "Алкиніл," сам по собі чи як частина іншого замісника, відноситься до ненасиченого розгалуженого, нерозгалуженого чи циклічного алкільного радикала, що містить, щонайменше, один потрійний вуглець-вуглецевий зв'язок, утворений відщепленням одного атома водню від окремого вуглецевого атома вихідного алкіна. Типові алкінільні групи включають, не вичерпуючись переліком, етиніл; пропиніли, такі як проп-1-ин-1-іл, проп-2-ин1-іл і т.д.; бутиніли, такі як бут-1-ін-1-іл, бут-1-ин-Зіл, бут-3-ин-1-іл і т.д.; тощо. "Алкокси," сам по собі чи як частина іншого замісника, відноситься до радикала формули OR30, де R30 являє собою алкільну чи циклоалкільну групу, як визначено в даному контексті. Типові 17 приклади алкоксильної групи включають, не вичерпуючись переліком, метокси, етокси, пропокси, ізопропокси, бутокси, трет-бутокси, циклопропілокси, циклопентилокси, циклогексилокси тощо. "Алкоксикарбоніл," сам по собі чи як частина іншого замісника, відноситься до радикала формули -С(О)-алкокси, де алкокси - як визначено в даному контексті. "Алкілтіо," сам по собі чи як частина іншого замісника, відноситься до радикала формули SR31, де R31 являє собою алкільну чи циклоалкільну групу як визначено в даному контексті. Типові приклади включають, не вичерпуючись переліком, метилтіо, етилтіо, пропілтіо, ізопропілтіо, бутилтіо, mpew-бутилтіо, циклопропілтіо, циклопентилтіо, циклогексилтіо тощо. "Арил," сам по собі чи як частина іншого замісника, відноситься до одновалентної ароматичоної вуглеводневої групи, утвореної відщепленням одного атома водню від окремого вуглецевого атома вихідної ароматичної циклічної системи, як визначено в даному контексті. Типові арильні групи включають, не вичерпуючись переліком, похідні ацеантрилену, аценафтілену, ацефенантрилену, антрацену, азулену, бензолу, хризену, коронену, флуорантену, флуорену, гексацену, гексафену, гексалену, as-індацену, s-індацену, індану, індену, нафталену, октацену, октафену, окталену, овалену, пента-2,4-дієну, пентацену, Пентагону, пентафену, перилену, феналену, фенантрену, піцену, плейадену, пірену, пірантрену, рубіцену, трифенілену, тринафталену тощо. Переважно, щоб арильна група містила від 6 до 20 атомів вуглецю (С6С2о-арил), більш переважно - від 6 до 15 атомів вуглецю (С6-С15-арил) і ще більш переважно - від 6 до 10 атомів вуглецю (С6-С10-арил). "Арилалкіл," сам по собі чи як частина іншого замісника, відноситься до ациклічної алкільної групи, у якій один з атомів водню, пов'язаний з атомом вуглецю, як правило, кінцевим чи знаходиться в sр3-гібридізації, заміщений арильною групою, як визначено в даному контексті. Типові арилалкільні групи включають, не вичерпуючись переліком, бензил, 2-фенілетан-1-іл, 2-фенілетен-1-іл, нафтилметил, 2-нафтилетан-1-іл, 2-нафтилетен-1-іл, нафтобензил, 2-нафтофенілетан-1-іл тощо. Якщо маються на увазі конкретні алкільні фрагменти, використовують найменування арилалканіл, арилалкеніл і/чи арилалкініл. Переважно, щоб арилалкільна група була (С6-С30) арилалкілом, наприклад, щоб алканільна, алкенільна чи алкінільна частина арилалкільної групи була (С1-С10) алкілом, а арильная складова - (С6-С2о)арилом, більш переважно, щоб арилалкільна група була (С6С20)арилалкілом, наприклад, щоб алканільна, алкенільна чи алкінільна частина арилалкільної групи була (С1-С8)алкілом, а арильна складова - (С6С12)арилом, і ще більш переважно, щоб арилалкільна група була (С1-С8)арилалкілом, наприклад, щоб алканільна, алкенільна чи алкінільна частина арилалкільної групи була (С1-С5)алкілом, а арильна - (С6-С10)арилом. "Арилокси," сам по собі чи як частина іншого замісника, відноситься до радикала формули -О 80435 18 арил, де арил являє собою як визначено в даному контексті. "Арилалкілокси, сам по собі чи як частина іншого замісника, відноситься до радикала формули -О-арилалкіл, де арилалкіл являє собою як визначено в даному контексті. "Арилоксикарбоніл," сам по собі чи як частина іншого замісника, відноситься до радикала формули -С(О)-О-арил, де арил являє собою як визначено в даному контексті. "Карбамоіл," сам по собі чи як частина іншого замісника, відноситься до радикала формули C(O)NR32R33, де R32 і R33 незалежно один від одного обрані з групи, що складається з водню, алкілу та циклоалкілу, як визначено в даному контексті, чи ж R і R разом з атомом азоту, з яким вони пов'язані, утворять циклогетероалкільне кільце, як визначено в даному контексті. "Сполуки винаходу" відноситься до сполук, охоплених різними описами і загальними формулами, розкритими в даному контексті. Сполуки винаходу можуть бути визначені за допомогою їхньої хімічної структури і/чи хімічного найменування. Якщо хімічна структура та хімічна назва не відповідають один одному, для ідентифікації сполуки визначальною буде хімічна структура. Сполуки винаходу можуть містити один чи більш хіральний центр і/чи подвійний зв'язок, і таким чином, можуть існувати у вигляді стереоізомерів, як, наприклад, ізомери по подвійному зв'язку (тобто геометричні ізомери), ротамеры, енантіомери чи діастереомери. Тому, якщо стереохімія хірального центру не визначена, хімічні структури, описані тут, охоплюють усі можливі конфігурації даних хіральних центрів, включаючи стереоізомерно чисту форму (наприклад, геометрично чисту, енантіомерно чисту чи діастереомерно чисту), а також енантіомерні та стереоізомерні суміші. Енантіомерні та стереоізомерні суміші можуть бути розділені на їх складові компоненти - енантіомери чи стереоізомери - за допомогою добре відомих методик чи поділу методик хірального синтезу. Крім того, сполуки винаходу можуть існувати в різних таутомерних формах, включаючи енольну форму, кетоформу, а також їхні суміші. Таким чином, хімічні структури, приведені тут, включають усі можливі таутомерні форми описаних сполук. Сполуки винаходу також можуть включати сполуки з ізотопними мітками, у яких один чи кілька атомів мають атомну масу, відмінну від атомної маси, що звичайно зустрічається в природі. Приклади ізотопів, що можуть бути введені в сполуки винаходу, включають, не вичерпуючись переліком, 2Н, 3Н, 13 С, 14С, 15N, 18О, 170,31Р, 32Р, 35S, 18F · 36Cl. Сполуки винаходу можуть існувати як у несольватованій формі, так і у формі сольватів, включаючи гідратні форми, і у вигляді N-оксидів. Загалом, гідратні, сольватні форми і N-оксиди включені в об'єм даного винаходу. Деякі сполуки даного винаходу можуть існувати в різних кристалічних чи аморфних формах. Взагалі кажучи, при використанні, яке припускається даним винаходом, усі фізичні форми є рівноцінними і включені до об'єму даного винаходу. 19 "Циклоалкіл," сам по собі чи як частина іншого замісника, відноситься до насиченого чи ненасиченого циклічного алкільного радикала, як визначено в даному контексті. Якщо мається на увазі конкретний ступінь насиченості, використовують терміни "циклоалканіл" чи "циклоалкеніл". Типові циклоалкільні групи включають, не вичерпуючись переліком, похідні циклопропану, циклобутану, циклопентану, циклогексану тощо. Переважно, щоб циклоалкільна група містила від 3 до 10 атомів у кільці (С3-С10-циклоалкіл), і більш переважно -від 3 до 7 кільцевих атомів (С3-С7-циклоалкіл). "Циклогетероалкіл," сам по собі чи як частина іншого замісника, відноситься до насиченого чи ненасиченого циклічного алкільного радикала, у якому один чи більше атомів вуглецю (і, можливо, будь-які суміжні атоми водню) незалежно замінені однаковими чи різними гетероатомами. Типові гетероатоми, що можуть заміщати атом (атоми) вуглецю, включають, не вичерпуючись переліком, Ν, Ρ, О, S, Si і т.д. Якщо мається на увазі конкретний ступінь насиченості, використовують терміни "циклогетероалканіл" чи "циклогетероалкеніл". Типові циклогетероалкільні групи включають, не вичерпуючись переліком, похідні епоксиду, азиріну, тиірану, імідазолідину, морфоліну, піперазину, піперидину, піразолідину, піролідону, хінуклідину тощо. Переважно, щоб циклогетероалкільна група містила від 3 до 10 кільцевих атомів (3-10-членний циклогетероалкіл) і більш переважно - від 3 до 7 кільцевих атомів (3-7-членний циклогетероалкіл). "Діалкіламіно," сам по собі чи як частина іншого замісника, відноситься до радикала формули NR R5, де R4 і R5 незалежно один від одного обрані з групи, що складається з алкілу і циклоалкілу, як визначено в даному контексті. Характерні приклади діалкіламіногрупи включають, не вичерпуючись переліком, диметиламіно-, метил етиламіно-, ди-(1-метилетил)аміно-,(циклогексил)метиламіно-, (циклогексил)етиламіно-, (циклогексил)пропіламіно-групу тощо. "Галоген" чи "гало," сам по собі чи як частина іншого замісника відноситься до радикалів - фтору, хлору, брому і/чи йоду. "Галогеналкіл," сам по собі чи як частина іншого замісника, відноситься до алкільної групи, як визначено в даному контексті, у якій один чи більше атом водню заміщений галогенною групою. Зокрема, мається на увазі, що термін "галогеналкіл" включає моногалогеналкіли, дигалогеналкіли, тригалогеналкіли і т.д. аж до пергалогеналкілів. Галогени, що входять до складу галогеналкільної групи, можуть бути однаковими чи розрізнятися. Наприклад, вираз "(С1-С2)галогеналкіл" включає 1фторметил, 1-фтор-2-хлоретил, дифторметил, трифторметил, 1-фторетил, 1,1-дифторетил, 1,2дифторетил, 1,1,1-трифторетил, перфторетил і т.д. "Гетероарил," сам по собі чи як частина іншого замісника, відноситься до одновалентного гетероароматичного радикалу, утвореного відщепленням одного атома водню від окремого атома вихідної гетероароматичної циклічної системи, як визначено в даному контексті. Типові гетероарильні групи включають, не вичерпуючись переліком, похідні 80435 20 акридину, арсиндолу, карбазолу, β-карболіну, хроману, хромену, циноліну, фурану, імідазолу, індазолу, індолу, індоліну, індолізіну, ізобензофурану, ізохромену, ізоіндолу, ізоіндоліну, ізохіноліну, ізотіазолу, ізоксазолу, нафтіридіну, оксадіазолу, оксазолу, перимідину, фенантридіну, фенантроліну, феназіну, фталазіну, птеридину, пурину, пірану, піразину, піразолу, піридазину, піридину, піримідину, піролу, піролізіну, хіназоліну, хіноліну, хінолізіну, хіноксаліну, тетразолу, тіадіазолу, тіазолу, тіофену, триазолу, ксантену тощо. Переважно, щоб гетероарильна група містила від 5 до 20 кільцевих атомів (5-20-членний гетероарил), більш переважно - від 5 до 10 кільцевих атомів (5-10-членний гетероарил). Кращими гетероарильними групами є похідні тіофену, піролу, бензотіофену, бензофурану, індолу, піридину, хіноліну, імідазолу, оксазолу і піразину. "Гетероцикл" відноситься до таких сполук, охоплених винаходом і що характеризується "Вкільцем ", що зображені нижче. Такі сполуки можуть бути ароматичними чи неароматичними (гідроізомери). В-кільце має загальну формулу: і містить від одного до чотирьох гетероатомів, де Χ, Υ, Ζ, кожен незалежно один від одного, означають С, СН, N, NR16, NR18, S чи О; a U і Т, кожен незалежно один від одного, являють собою С, СН чи N. Замісники R і R незалежно один від одного обрані з групи, що складається з водню, нижчого алкілу, заміщеного нижчого алкілу, нижчого гетероалкілу, заміщеного нижчого гетероалкілу, циклоалкілу, заміщеного циклоалкілу, циклогетероалкілу, заміщеного циклогетероалкілу, нижчого галогеналкілу, моногалогенметилу, дигалогенметилу, тригалогенметилу, трифторметилу, нижчого алкілтіо, заміщеного нижчого алкілтіо, нижчого алкокси, заміщеного нижчого алкокси, метокси, заміщеного метокси, нижчого гетероалкокси, заміщеного нижчого гетероалкокси, циклоалкокси, заміщеного циклоалкокси, циклогетероалкокси, заміщеного циклогетероалкокси, нижчого галогеналкокси, моногалогенметокси, дигалогенметокси, тригалогенметокси, трифторметокси, нижчого дічи моноалкіламіно, заміщеного нижчого ді- чи моноалкіламіно, арилу, заміщеного арилу, арилокси, заміщеного арилокси, фенокси, заміщеного фенокси, арилалкілу, заміщеного арилалкілу, арилалкілокси, заміщеного арилалкілокси, бензилу, бензилокси, гетероарилу, заміщеного гетероарилу, гетероарилокси, заміщеного гетероарилокси, гетероарилалкілу, заміщеного гетероарилалкілу, гетероарилалкілокси, заміщеного гетероарилалкілокси, карбоксилу, нижчого алкоксикарбонілу, заміщеного нижчого алкоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, арилалкілоксикарбонілу, заміщеного арилалкілоксикарбонілу, карбамату, заміщеного карбамату, карбамоілу, заміщеного карбамоілу, сульфамоілу, 21 заміщеного сульфамоілу і групи формули -L-R17, де "L" являє собою сполучна ланка, a R17 означає циклоалкіл, заміщений циклоалкіл, циклогетероалкіл чи заміщений циклогетероалкіл. Сполучною ланкою може бути будь-яка група атомів, придатна для приєднання замісника R17 до атома азоту. Прийнятні сполучні ланки включають, не вичерпуючись переліком, фрагменти, обрані з групи, що складається з -(СН2)1-6-S,-С(О)-,-SO2-,-NH-,--C(O)SO2NH-і їхніх сполук. Придатні гетероцикли включають, наприклад, ізоксазоли, піразоли, оксадіазоли, оксазоли, тіазоли, імідазоли, тріазоли, тіадіазоли та їхні гідроізомери. Відповідні гідроізомери згаданих вище гетероциклічних сполук включають, наприклад, дигідроізомери, а також тетрагідроізомери. Такі гідроізомери включають, наприклад, 2-ізоксазолін, 3-ізоксазолін, 4-ізоксазоліни, ізоксазолідини, 1,2піразоліни, 1,2-піразолідини, (3Н)-дигідро-1,2,4оксадіазоли, (5Н)-дигідро-1,2,4-оксадіазоли, оксазоліни, оксазолідини, (3Н)-дигідротіазоли, (5Н)дигідротіазоли, тіазолідини (тетрагідротіазоли), (3Н)-дигідротріазоли, (5Н)-дигідротріазоли, триазолідини (тетрагідротріазоли), дигідрооксадіазоли, тетрагідрооксадіазоли, (3Н)-дигідро-1,2,4тіадіазоли, (5Н)-дигідро-1,2,4-тіадіазоли, 1,2,4тиадіазолідини (тетрагідротіадіазоли), (3Н)дигідроімідазоли, (5Н)-дигідроімідазоли і тетрагі дроімідазо ли. "Вихідна ароматична циклічна система" відноситься до ненасиченої циклічної чи поліциклічної кільцевої системи, що містить сполучену πелектронну систему. Зокрема, до визначення "вихідна ароматична циклічна система" включені конденсовані циклічні системи, у яких одне чи більш кільце є ароматичним і одне чи більш кільце є насиченим чи ненасиченим, такі, як, наприклад, флуорен, індан, інден, фенален і т.д. Типові вихідні ароматичні циклічні системи включають, не вичерпуючись переліком, ацеантрилен, аценафтілен, ацефенантрилен, антрацен, азулен, бензол, хризен, коронен, флуорантен, флуорен, гексацен, гексафен, гексален, as-індацен, s-індацен, індан, інден, нафтален, октацен, октафен, октален, овален, пента-2,4-дієн, пентацен, пентален, пентафен, перилен, фенален, фенантрен, піцен, плейаден, пірен, пірантрен, рубіцен, трифенілен, тринафтален тощо. "Вихідна гетероароматична циклічна система" відноситься до вихідної ароматичної циклічної системи, у якій один чи більше атом вуглецю (і, можливо, будь-які пов'язані з ними атоми водню), незалежно заміщений однаковими чи різними гетероатомами. Типові гетероатоми, заміщаючі атоми вуглецю, включають, не вичерпуючись переліком, N, Р, О, S, Si і т.д. Зокрема, до визначення "вихідна гетероароматична циклічна система" включені конденсовані циклічні системи, у яких одне чи більше кільце є ароматичним і одне чи більше кільце є насиченим чи ненасиченим, такі, як, наприклад, арсиндол, бензодіоксан, бензофуран, хроман, хромен, індол, індолін, ксантен і т.д. Типові вихідні гетероароматичні циклічні системи включають, не вичерпуючись переліком, арсиндол, карбазол, β-карболін, хроман, хромен, цинолін, 80435 22 фуран, імідазол, індазол, індол, індолін, індолізін, ізобензофуран, ізохромен, ізоіндол, ізоіндолін, ізохінолін, ізотіазол, ізоксазол, нафтірідин, оксадіазол, оксазол, перімідин, фенантридін, фенантролін, феназін, фталазін, птерідин, пурин, піран, піразин, піразол, пірідазин, піридин, піримідин, пірол, піролізин, хіназолін, хінолін, хінолізин, хіноксалін, тетразол, тіадиазол, тіазол, тіофен, триазол, ксантен тощо. "Фармацевтично прийнятні солі" відноситься до солі сполуки винаходу, що утворена з протиіонами, прийнятними для фармацевтичних цілей, і має необхідну фармакологічну активність вихідної сполуки. Такі солі включають: (1) адитивні солі кислот, утворені з неорганічними кислотами, такими як соляна кислота, бромистоводнева кислота, сірчана кислота, азотна кислота, фосфорна кислота тощо; чи солі, утворені з органічними кислотами, такими як оцтова кислота, пропіонова кислота, капронова кислота, циклопентанпропіонова кислота, гліколева кислота, піровиноградна кислота,молочна кислота, малонова кислота, бурштинова кислота, яблучна кислота, малеїнова кислота, фумарова кислота, винна кислота, лимонна кислота, бензойна кислота, 3-(4гідроксибензоіл)бензойна кислота, корична кислота, мигдальна кислота, метансульфонова кислота, етансульфонова кислота, 1,2-етандисульфонова кислота, 2-гідроксиетансульфонова кислота, бензолсульфонова кислота, 4-хлорбензолсульфонова кислота, 2-нафталенсульфонова кислота, 4толуолсульфонова кислота, камфорсульфонова кислота, 4-метилбіцикло[2.2.2]-окт-2-ен-1карбонова кислота, глюкогептонова кислота, 3фенілпропіонова кислота, триметилоцтова кислота, mpem-бутилоцтова кислота, лаурилсірчана кислота, глюконова кислота, глутамінова кислота, гідроксинафтойна кислота, саліцилова кислота, стеаринова кислота, муконова кислота тощо; чи (2) солі, при утворенні яких кислий протон, що є присутнім у вихідній сполуці, заміщається іоном металу, наприклад, іоном лужного металу, іоном лужноземельного металу чи іоном алюмінію; або утворює координаційну сполуку з органічною основою, такою як етаноламін, діетаноламін, триетаноламін, N-метилглюкамін, морфолін, піперідин, диметиламін, диетиламін тощо. Включені також солі амінокислот, такі як аргінати та їм подібні, а також солі органічних кислот, таких як глюкуронова чи галактуронова кислоти тощо [див., наприклад, Berge etal, 1977, J. Pharm. Sci. 66:1-19]. "Фармацевтично прийнятний наповнювач" відноситься до розріджувача, ад'юванта, наповнювача або носія, разом з яким вводять сполуку винаходу. "Захисна група" відноситься до групи атомів, що, приєднуючись до реакційної функціональної групимолекули, маскують, знижують чи перешкоджають реакційній здатності функціональної групи. Звичайно в ході синтезу при необхідності захисна група може бути вибірково вилучена. Приклади захисних груп можна знайти в [роботі Greene і Wuts, Protective Групи in Organic Chemistry (Захисні групи в органічній хімії), 3rd Ed., 1999, John Wiley & Sons, NY і Harrison et al., Compendium of 23 Synthetic Organic Methods (Перелік органічних синтетичних методів), Vols. 1-8, 1971-1996, John Wiley & Sons, NY]. Типові захисні групи для аміногрупи включають, не вичерпуючись переліком, формил, ацетил, трифторацетил, бензил, бензилоксикарбоніл ("CBZ"), трет-бутоксикарбоніл ("Вос"), триметилсиліл ("TMS"), 2-триметилсилілетансульфоніл ("SES"), тритил і заміщені тритильні групи, алілоксикарбоніл, 9-флуоренилметилоксикарбоніл ("FMOC"), нитровератрилоксикарбоніл ("NVOC")тощо. Типові захисні групи для гідроксильної функції включають, не вичерпуючись переліком, групи, у яких гідроксил проацильований (наприклад, метилові й етилові ефіри, ацетати чи пропіонати чи гліколеві ефіри) або проалкільовані, такі як бензилові і тритилові ефіри, а також алкілові ефіри, тетрагідропіранілові ефіри, триалкілсилільні ефіри (наприклад, групи TMS чи TIPPS) і алілові ефіри. "Проліки" відноситься до похідної активної сполуки (лікарського препарату), що піддається трансформації в умовах застосування, як, наприклад, в організмі, з вивільненням активного препарату. Проліки часто, але не обов'язково, є фармакологічно неактивними до перетворення їх в активний препарат. Звичайно проліки одержують, маскуючи в препараті функціональну групу, що приблизно буде знаходитися в частині, необхідній для прояву активності, прогрупою (визначеною нижче) з утворенням профрагменту, перетерплюючого зміну, таку як розщеплення, у конкретних умовах застосування з вивільненням функціональної групи і, отже, активного препарату. Розщеплення профрагменту може відбуватися мимовільно, наприклад, у результаті реакції гідролізу, або може бути каталізовано чи індуковано іншим агентом, таким, як фермент, вплив світла, кислоти, чи шляхом зміни чи експозиції фізичних параметрів чи умов навколишнього середовища, як, наприклад, зміна температури. Агент може бути ендогенним стосовно умов застосування, таким як фермент, що є присутнім у клітинах, в які вводять проліки, чи кисле середовище шлунка, або може вводитися екзогенно. Відповідно до конкретного здійснення, термін "проліки" включає гідроізомери сполук винаходу. Такі гідроізомери, охоплені винаходом, можуть бути окислені в умовах фізіологічного середовища до відповідної ароматичної циклічної системи. Відомий цілий ряд прогруп, а також утворених в результаті профрагментів, придатних для маскування функціональної групи в активних сполуках з утворенням проліків. Наприклад, гідроксильна функція може бути захищена перетворенням у сульфонат, чи ефір карбонат, які будуть гідролізуватись in vitro з утворенням гідроксильної групи. Функціональна аміногрупа може бути перетворена в амід, імін, фосфиніл, фосфоніл, фосфорил чи сульфеніл, що можуть бути гідролізовані in vivo з вивільненням аміногрупи. Карбоксильна група може бути захищена перетворенням в ефір (включаючи силільні ефіри і тіоефіри), амід чи гідразид, які можуть гідролізуватись in vivo з утворенням карбоксильної групи. 80435 24 Інші конкретні приклади придатних прогруп і відповідних їм профрагментів будуть очевидні для фахівців у даній області. "Прогрупа" відноситься до типу захисної групи, що при використанні для маскування функціональної групи активного препарату з утворенням профрагменту, перетворює лікарський препарат у проліки. Прогрупи, як правило, приєднані до функціональної групи лікарського препарату за допомогою зв'язків, здатних розщеплюватися в конкретних умовах застосування. Таким чином, прогрупа є такою частиною профрагменту, що розщеплюється з вивільненням функціональної групи в конкретних умовах застосування. Наприклад, амідний профрагмент формули -NH-C(O)CH3 включає прогрупу -С(О)СН3. "Силільний ефір" відноситься до типу захисної групи, що при маскуванні гідроксильної функції активного лікарського препарату з утворенням профрагменту, перетворює лікарський препарат у проліки. Силільні ефіри добре відомі і належать до груп, що видаляються та запобігають участі гідроксильної функції в реакціїмолекули. Такі групи обговорюються [Т. W. Greene у главах 2 і 7 книги Protective Groups in Organic Synthesis (Захисні групи в органічному синтезі), John Wiley and Sons, New York, 1981, і J. W. Barton у главі 2 книги Protective Groups in Organic Chemistry (Захисні групи в органічній хімії), J. F. W. McOmie, ed., Plenum Press, New York, 1973], цілком приведених тут як посилальний матеріал. Силільні ефіри включають, наприклад, триметилсиліл, триетилсиліл, трет-бутилдиметилсиліл і метилдіізопропілсиліл. "Заміщений," при використанні для модифікації конкретної групи чи радикала, означає, що один чи більше атом водню конкретної групи чи радикала, кожен незалежно один від одного, замінений однаковими чи різними замісниками (замісником). Типові замісники включають, не вичерпуючись переліком, -М, -R40, -О-, =O, -OR40, -SR40, -S-, =S, NR40R41, =NR40, -CM3, -CF3, -CN, -OCN, -SCN, -NO, -N02, =N2, -N3, -S(0)2O-, -S(O)2OH, -S(O)2R40, OS(02)O-, -OS(O)2R40, -P(O)(O-)2, -P(O)(OR40)(CO, OP(O)(OR40)(OR41), -C(O)R40, -C(S)R40, -C(O)OR40, C(O)NR40R41,-C(O)O-, -C(S)OR40, 42 40 41 42 NR C(O)NR R , -NR C(S)NR40R41, NR42C(NR43)NR40R41 і -C(NR42)NR40R41, де кожна перемінна М незалежно являє собою галоген; R40, R41, R42, R43 і R44 незалежно один від одного обрані з групи, що складається з водню, алкілу, заміщеного алкілу, алкокси, заміщеного алкокси, циклоалкілу, заміщеного циклоалкілу, циклогетероалкілу, заміщеного циклогетероалкілу, -NR45R46, -C(O)R45 і -S(O)2R45, чи ж, R40 і R41 і/чи R45 і R46, разом з відповідними атомами азоту, до яких вони приєднані, утворять циклогетероалкільне чи заміщене циклогетероалкільне кільце, як визначено в даному контексті. "Сульфамоіл," сам по собі чи як частина іншого замісника, відноситься до радикала формули S(O)2NR R , де R і R , кожен незалежно один від одного, являє собою водень, алкіл чи циклоалкіл, як визначено в даному контексті, чи ж, R і R , разом з атомом азоту, до якого вони приєднані, 25 утворюють циклогетероалкільне чи заміщене циклогетероалкільне кільце, як визначено в даному контексті. Сполуки Відповідно до одного зі здійснень, сполуки винаходу являють собою піридилзаміщені гетероциклічні сполуки та гідроізомери по В-кільцю структурної формули (І): чи їх фармацевтично прийнятні солі, гідрати, сольвати чи N-оксиди, де: В-кільце являє собою ароматичне чи неароматичне кільце, що містить від одного до чотирьох гетероатомів, у якому Χ, Υ, Ζ незалежно один від одного обрані з С, СН, N, NR , NR , S чи О, за умови, що X і Υ не є обоє О; U і Τ незалежно один від одного обрані з С, СН чи Ν; Ζ означає N чи -СН-; А означає N чи -CR2-; В означає N чи -CR3-; D означає N чи -CR4-; Ε означає N чи -CR5-; G означає N чи -CR6-; J означає N чи -CR14-; К означає N чи -CR8-; L означає N чи -CR9-; Μ означає N чи -CR10-; R2 і R6 незалежно один від одного обрані з групи, що складається з водню, галогену, фтору, хлору, алкілу, метилу, заміщеного алкілу, алкілтіо, заміщеного алкілтіо, алкокси, метокси, ізопропокси, заміщеного алкокси, алкоксикарбонілу, заміщеного алкоксикарбонілу, арилалкілоксикарбонілу, заміщеного арилалкілоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, циклогетероалкілу, заміщеного циклогетероалкілу, карбамоілу, заміщеного карбамоілу, галогеналкілу, трифторметилу, сульфамоілу, заміщеного сульфамоілу і силільного ефіру, за умови, що один із замісників R і R не є воднем; R і R5 незалежно один від одного обрані з групи, що складається з водню, галогену, хлору, алкілу, заміщеного алкілу, алкілтіо, заміщеного алкілтіо, алкокси, заміщеного алкокси, алкоксикарбонілу, заміщеного алкоксикарбонілу, арилалкілоксикарбонілу, заміщеного арилалкілоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, циклогетероалкілу, заміщеного циклогетероалкілу, карбамоілу, заміщеного карбамоілу, галогеналкілу, сульфамоілу і заміщеного сульфамоілу; 80435 26 R4 обраний із групи, що складається з водню, галогену, алкілу, заміщеного алкілу, алкілтіо, заміщеного алкілтіо, карбамоілу, заміщеного карбамоілу, алкокси, заміщеного алкокси, алкоксикарбонілу, заміщеного алкоксикарбонілу, арилалкілоксикарбонілу, заміщеного арилалкілоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, діалкіламіно, заміщеного діалкіламіно, галогеналкілу, сульфамоілу і заміщеного сульфамоілу; R7 означає-NR11C(O)R12; R8, R9, R10 і R14 незалежно один від одного обрані з групи, що складається з водню, галогену та фтору; R11 являє собою водень, алкіл чи метил; і R12 означає заміщений алкіл, галогеналкіл, галогенметил, дигалогенметил, дихлорметил, циклогетероалкіл чи заміщений циклогетероалкіл; R16 і R18 незалежно один від одного обрані з групи, що складається з водню, нижчого алкілу, заміщеного нижчого алкілу, нижчого гетероалкілу, заміщеного нижчого гетероалкілу, циклоалкілу, заміщеного циклоалкілу, циклогетероалкілу, заміщеного циклогетероалкілу, нижчого галогеналкілу, моногалогенметилу, дигалогенметилу, тригалогенметилу, трифторметилу, нижчого алкілтіо, заміщеного нижчого алкілтіо, нижчого алкокси, заміщеного нижчого алкокси, метокси, заміщеного метокси, нижчого гетероалкокси, заміщеного нижчого гетероалкокси, циклоалкокси, заміщеного циклоалкокси, циклогетероалкокси, заміщеного циклогетероалкокси, нижчого галогеналкокси, моногалогенметокси, дигалогенметокси, тригалогенметокси, трифторметокси, нижчого ди- чи моноалкіламіно, заміщеного нижчого дичи моноалкіламіно, арилу, заміщеного арилу, арилокси, заміщеного арилокси, фенокси, заміщеного фенокси, арилалкілу, заміщеного арилалкілу, арилалкілокси, заміщеного арилалкілокси, бензилу, бензилокси, гетероарилу, заміщеного гетероарилу, гетероарилокси, заміщеного гетероарилокси, гетероарилалкілу, заміщеного гетероарилалкілу, гетероарилалкілокси, заміщеного гетероарилалкілокси, карбоксилу, нижчого алкоксикарбонілу, заміщеного нижчого алкоксикарбонілу, арилоксикарбонілу, заміщеного арилоксикарбонілу, арилалкілоксикарбонілу, заміщеного арилалкілоксикарбонілу, карбамату, заміщеного карбамату, карбамоілу, заміщеного карбамоілу, сульфамоілу, заміщеного сульфамоілу та групи формули -L-R17, де "L" є сполучною ланкою, a R17 являє собою циклоалкіл, заміщений циклоалкіл, циклогетероалкіл чи заміщений циклогетероалкіл, за умови, що: (і) щонайменше, одна з перемінних А, В, D, Е, G, J, К, L чи Μ означає Ν; (іі) не більше, ніж одна з перемінних А, В, D, Ε чи G означає Ν; і (ііі) не більше, ніж одна з перемінних J, К, L чи Μ означає N. Відповідно до іншого здійснення, сполуки винаходу являють собою піридилзаміщені гетероциклічні сполуки та гідроізомери по В-кільцю структурної формули (II): 27 чи їх фармацевтично прийнятні солі, гідрати, чи сольвати N-оксиди, де А, В, D, Е, G, J, К, L, Μ і R7 відповідають приведеним вище описам для структурної формули (І) і задовольняють тим же умовам, а — зображує ароматичне чи неароматичне (гідроізомер) гетероциклічне кільце. Згідно одного зі здійснень сполук структурної формули (І), Ζ означає -СН-, так що сполуки являють собою ізоксазоли чи піразоли. Відповідно до іншого здійснення сполук структурної формули (І), Ζ означає Ν, так що сполуки являють собою оксадіазоли чи азоли. Відповідно до іншого здійснення, сполуками структурної формули (І) є ізоксазоли. Згідно часткового здійснення ізоксазолів, X означає N, a Y - О. Згідно ще одного здійснення, сполуки структурної формули (І) є оксадіазолами. Згідно одного зі здійснень сполук структурної формули (І) і (II), А, В, D, Ε чи G означають N і одна з перемінних J, К, L чи Μ є N. Відповідно до іншого здійснення, одна з перемінних А, В, D, Ε чи G означає Ν, а ніодна з перемінних J, К, L чи М не є N. Згідно ще одного здійснення, ніодна з перемінних А, В, D, Ε чи G не є Ν, а одна з перемінних J, К, L чи Μ означає N. Переважно, щоб при кожному з описаних вище здійснень сполук формули (І) і/чи (II), R7 був -NRnC(O)R12, де R11 є воднем чи метилом, a R означає -СНСl2. Відповідно до іншого здійснення сполук структурної формули (І) і (II), А є –CR2 -, G - -CR6 -, a R7 являє собою -NR11C(O)R1, де R11 означає водень чи метил, а R12 є -СНСl2. Відповідно до більш конкретного здійснення, В означає -CR3-, D - N, Ε - CR5-, J - -CR14-, К - -CR8-, L - -CR9-, Μ - -CR10-, а кожний із замісників R3, R5, R9, R10 і R14 є воднем. Відповідно до іншого більш конкретного здійснення, В означає -CR3-, D - -CR4-, Ε - -CR5-, J - -CR14-, К - -CR8-, L - -CR9-, Μ - Ν , а кожний із замісників R3, R4, R5, R8, R9 і R14 є воднем. Згідно ще одного більш конкретного здійснення, В означає -CR3-, D -CR4-, Ε - -CR5-, J - -CR14-, К - -CR8-, L - Ν, Μ - CR10-, а кожний із замісників R3, R4, R5, R8, R10 і R14 є воднем. Переважно, щоб при описаному вище здійсненні замісники R і R , кожен незалежно один від одного, були обрані з групи, що складається з хлору, фтору, метилу, трифторметилу, тіометилу, метокси, ізопропокси, N-морфоліно і Nморфоліносульфамоілу. Більш переважно, щоб R2 і R6, кожен незалежно один від одного, були обрані з групи, що складається з хлору, фтору, метилу, трифторметилу, метокси та ізопропокси. Згідно іншого здійснення, кожний із замісників R2 і R являє собою однакові чи різні атоми галогену. Переважно, щоб при згаданих вище здійсненнях, X був Ν, Υ - О, a Z означав -СН-. Згідно ще одного здійснення сполук структурної формули (І) і (II), А означає -CR2-, G - -CR6- і R7 80435 28 являє собою –NR11C(O)R12, де R11 означає водень чи метил, а R1 є -СН2І. Переважно, щоб R і R , кожен незалежно один від одного, були обрані з групи, що складається з хлору, фтору, метилу, трифторметилу, тіометилу, метокси, ізопропокси, Nморфоліно і N-морфоліносульфамоілу. Більш переважно, щоб R2 і R6, кожен незалежно один від одного, були обрані з групи, що складається з хлору, фтору, метилу, трифторметилу, метокси та ізопропокси. Згідно іншого здійснення, замісники R2 і R6 є однаковими чи різними атомами галогену. Переважно, щоб при зазначених вище здійсненнях X означав Ν, Υ - О, а Ζ був -СН. Згідно ще одного здійснення сполук структурної формули (І) і (II), А є -CR2-, В - -CR3-, R7 - NRnC(O)R12, де R11 означає водень чи метил, a R12 є -СНСl2. Відповідно до більш конкретного здійснення, D являє собою -CR4- G - -CR6-, Ε - -R5-, J - CR14-, К - -CR8-, L - -CR9-, Μ - Ν, а кожний із замісників R4, R5, R6, R8, R9 і R14 є воднем. Згідно іншого більш конкретного здійснення, D означає -CR4-, G -CR6-, Ε - -CR5-, J - -CR14-, К - -CR8-, L - Ν, Μ - CR10-, а кожний із замісників R4, R5, R6, R8, R10 і R14 є воднем. Переважно, щоб R2 і R6, кожен незалежно один від одного були обрані з групи, що складається з хлору, фтору, метилу, трифторметилу, тіометилу, метокси, ізопропокси, N-морфоліно і Nморфоліносульфамоілу. Більш переважно, щоб R і R6, кожен незалежно один від одного, були обрані з групи, що складається з хлору, фтору, метилу, трифторметилу, метокси та ізопропокси. Згідно іншого здійснення, R2 і R6 є однаковими чи різними атомами галогену. Переважно, щоб при зазначених вище здійсненнях X означав Ν, Υ -О , a Z був СН-. Згідно ще одного здійснення сполук структурної формули (І) і (II), А являє собою -CR2-, G означає -CR6-, a R2 і R6 є однаковими, за умови, що вони не є воднем. Відповідно до іншого здійснення, А означає -CR -, В - -CR -, a R і R є однаковими, за умови, що вони не означають водень. Згідно ще одного здійснення, В являє собою -CR -, Ε означає -CR -, a R і R є однаковими, за умови, що вони не означають водень. Згідно ще одного здійснення, В означає -CR -, D - -CR -, Ε - -CR5-, J - CR14-, К - -CR8-, а кожний із замісників R3, R4, R5, R8' R14 є воднем. Згідно ще одного здійснення, -D означає -CR4-, Ε - -CR5-, G - CR6, J - -CR14-, К - CR8-, a кожний із замісників R4, R5, R6, R8' R14 є воднем. Згідно додаткових здійснень, сполуки структурної формули (І) та їхні гідроізомери по В-кільцю включають С-кільце, що представляє собою пірид3-іл. Згідно ще одного здійснення, сполуки структурної формули (І) та їхні гідроізомери по В-кільцю включають С-кільце, що представляє собою пірид4-іл. Згідно інших здійснень, сполуки структурної формули (І) являють собою ізоксазоли, що відповідають структурним формулам (la), (Ib), (Ic), (Id) чи (Іе): 29 80435 30 залежно один від одного, однією чи більш характерною рисою, обраною з групи, що складається з: X означає О, а Υ - Ν; XeN,aY-O; R11 означає водень; R означає дихлорметил; R2 і R6 незалежно один від одного обрані з групи, що складається з метилу, галогену, фтору, хлору, трифторметилу і метокси; і R2 і R6 незалежно один від одного обрані з групи, що складається з галогену, фтору та хлору. Відповідно до іншого аспекту винаходу, X означає Ν, Υ - О, Ζ - СН, Τ і U являють собою С (ізоксазольне кільце), А є -CR2-, G означає -CR6-. Згідно ще одного аспекта винаходу, X означає Ν, Υ - О, Ζ - СН, Τ і U являють собою С (ізоксазольне кільце), А є -CR2-, G означає -CR6-, де R6 являє собою піперазин чи заміщений піперазин. Придатний заміщений піперазин включає, наприклад, чи їх фармацевтично прийнятні солі, гідрати чи сольвати, де замісники Χ, Υ, R2, R6, R11 і R12 аналогічні описаним раніше для структурної формули (І), а — являє собою ненасичений зв'язок (ароматичний гетероцикл) чи насичений зв'язок (неароматичний гетероцикл, наприклад, гідроізомер) у кільці В. Згідно одного зі здійснень, сполуки структурних формул (la), (Ib), (Ic), (Id) і (Іе) володіють, не Згідно ще одного аспекту винаходу, Xозначає Ν, Υ - О, Ζ - СН2, Τ і U являють собою С (ізоксазольне кільце), А є -CR2-, G означає -C-O-R6-, так що R6 утворює ефір, складний ефір чи силільний ефір. Придатні групи R , що утворюють ефір, складний ефір чи силільний ефір, включають, наприклад, алкіл, метил, заміщений алкіл, алкілтіо, заміщений алкілтіо, алкокси, метокси, ізопропокси, заміщений алкокси, алкоксикарбоніл, заміщений алкоксикарбоніл, арилалкілоксикарбоніл, заміщений арилалкілоксикарбоніл, арилоксикарбоніл, заміщений арилоксикарбоніл, циклогетероалкіл, заміщений циклогетероалкіл, карбамоіл, заміщений карбамоіл, галогеналкіл, трифторметил і силільні ефіри. Приклади сполук винаходу представлені на Фіг.1 і в Таблиці 1. Фахівцю в даній області зрозуміло, що описані тут сполуки винаходу можуть містити функціональні групи, що можуть бути захищені прогрупами з утворенням проліків. Такі проліки, як правило, але не обов'язково, є фармакологічно неактивними до перетворення їх в активну лікарську форму. У проліках винаходу кожна з наявних функціональних груп може бути захищена прогрупою з утворенням проліків. Відома значна кількість прогруп, придатних для захисту таких функціональних груп з утворенням профрагментів, здатних розщеплюватися в необхідних умовах. Способи синтезу Сполуки винаходу можуть бути отримані за допомогою методів синтезу, представлених на Фіг.2-7. Варто розуміти, що значення перемінних 31 А, В, D, Е, G, J, К, L, Μ і R7 на Фіг.2-7 відповідають перемінним, описаним вище для структурної формули (І) і задовольняють тим же умовам. Вихідна сировина для одержання сполук винаходу та їхніх напівпродуктів є комерційно доступною або може бути отримана за допомогою добре відомих методів синтезу [див., наприклад, Harrison et ah, "Compendium of Synthetic Organic Methods" (Перелік органічних синтетичних методів), Vols. 1-8, John Wiley і Sons, 1971-1996; "Beilstein Handbook of Organic Chemistry," (Довідник Бейльштейна з органічної хімії) Beilstein Institute of Organic Chemistry, Frankfurt, Germany; Feiser et al., "Reagents for Organic Synthesis," (Реагенти для органічного синтезу) Volumes 1 -17, Wiley Interscience; Trost et al, "Comprehensive Organic Synthesis," (Загальний органічний синтез) Pergamon Press, 1991; "TheilheiMer's Synthetic Methods of Organic Chemistry," Volumes 1-45, Karger, 1991; March, "Advanced Organic Chemistry," (Органічна хімія) Wiley Interscience, 1991; Larock "Comprehensive Organic Transformations," (Загальні огранічні перетворення) VCH Publishers, 1989; Paquette, "Encyclopedia of Reagents for Organic Synthesis," (Енциклопедія реагентів для органічного синтезу) John Wiley & Sons, 1995]. Інші способи синтезу сполук, описаних у даному контексті, і/чи вихідної сировини описані в літературі або будуть очевидними для фахівця в даній області. Альтернативні варіанти реагентів і/чи захисних груп, приведених на Фіг.2-7, можна знайти в зазначеній вище літературі, а також в інших джерелах, добре відомих фахівцям. Посібником з вибору придатної захисної групи може служити, наприклад, [збірник Greene & Wuts, "Protective Groups in Organic Synthesis," (Захисні групи в органічному синтезі) Wiley Interscience, 1999]. Таким чином, способи синтезу і стратегія, представлені в даному контексті, є скоріше ілюстративними, ніж усеосяжними. Один зі способів синтезу заміщених ізоксазолів структурної формули (І) (де Ζ означає -СН-) представлений на Фіг.2А. Згідно Фіг.2А, альдольна конденсація метилкетону 201 з бензальдегідом 203 у лужному середовищі з наступною дегідратацією in situ приводить до αβ-ненасиченого енону 205, який може бути легко перетворений у ізоксазол 207 обробкою гідроксиламіном. Відновлення сполуки 207 приводить до аміноізоксазолу 209, що може бути перетворений різними способами, добре відомими фахівцям, у кінцевий продукт 211. Конкретний приклад синтетичного методу, зображеного на Фіг.2А, проілюстрований одержанням ізоксазолу 9 на Фіг.2В. Інший спосіб синтезу заміщеного ізоксазолу структурної формули (І) (де Ζ означає -СН-) представлений на Фіг.ЗА. Конденсація Кляйзена метилкетону 201 з ефіром 223 у лужному середовищі дає 1,3-дикетон 229, що може бути перетворений у суміш ізоксазолів 207 і 231 обробкою гідроксиламіном. Як зазначене вище, відновлення сполуки 207 приводить до аміноізоксазолу 209, що може бути перетворений у ізоксазол 211 за допомогою добре відомих способів синтезу. Слід зазначити, що ізоксазол 231 може бути перетворений у відпо 80435 32 відний регіоізомер ізоксазол 211 тим же способом синтезу. Конкретний приклад синтетичного методу, зображеного на Фіг.ЗА, проілюстрований одержанням ізоксазолу 9 на Фіг.ЗВ. Відповідно до альтернативного напрямку синтезу, зображеному на Фіг.3А, ефір 225 конденсують з метилкетоном 227 з утворенням 1,3дикетона 229, що потім бере участь в інших реакціях, як описано вище. Ще один спосіб синтезу заміщених ізоксазолів структурної формули (І) (де Ζ означає -СН-) представлений на Фіг.4А. Нуклеофільне приєднання гідроксиламіну до бензальдегіду 245 приводить до проміжного оксиму, що може бути перетворений обробкою N-хлорсукцинимідом (NCS) у ахлороксим 247. Дегідрогалогенування осхлороксима 247 дає перехідний ілід, що піддають 1,3-диполярному приєднанню з ацетиленом 249 з утворенням цільового ізоксазолу 211. Ацетилен 249 може бути легко синтезований відомими способами з комерційно доступної сировини. Як конкретний приклад способу синтезу, зображеного на Фіг.4А, на Фіг.4В представлено одержання ізоксазолу 9. Фіг.4С ілюструє одержання ацетилену 255, зображеного на Фіг.4В. Аналогічні способи можуть бути використані для синтезу інших піридил ацетиленів. Ще один спосіб синтезу заміщених ізоксазолів структурної формули (І) (де Ζ означає -СН-) представлений на Фіг.5А. Нуклеофільне приєднання гідроксиламіну до бензальдегіду 245 приводить до проміжного оксиму, що може бути відразу перетворений у сполуку 257 реакцією з NaOCl. Диполярне 1,3-циклоприєднання уліда 257 до метилкетону 259 приводить до цільового ізоксазолу 211. Метилкетон 259 може бути легко отриманий відомими способами з комерційно доступних попередників. Як конкретний приклад способу синтезу, зображеного на Фіг.5А, на Фіг.5В представлено одержання ізоксазолу 9. Способи, описані вище на Фіг.2-5, можуть бути легко адаптовані для синтезу піразолів заміною в реакційній послідовності гідроксиламіну гідразином. Крім того, фахівцям зрозуміло, що регіоізомері ізоксазолу, описаного вище на Фіг.2-5, можуть бути синтезовані при простій взаємній перестановці реакційних функціональних груп у двох різних ароматичних кільцях. Приклад такого підходу представлений на Фіг.4D для "зворотнього" ізоксазолу 262. Як можна бачити з Фіг.4D, перестановка функціональних груп хлороксиму й алкіну в двох різних ароматичних кільцях (тобто кільцях А і С) приводить до регіоізомерного ізоксазолу 262 (порівняйте 253 і 255 з 254 і 256). Крім того, деякі схеми синтезу можуть приводити відразу до обох регіоізомерів ізоксазолу (наприклад, Фіг.3А і 3В), які можна розділити з використанням стандартних методик. Один із способів синтезу заміщених оксадіазолів структурної формули (І) (де Ζ означає -Ν-) представлений на Фіг.6А. Як показано на Фіг.6А, нуклеофільне приєднання гідроксиламіну до фенілціаніду 265 приводить до а-амінооксиму 267, що може бути сконденсований з ацилхлоридом 269 з утворенням, після дегідратаційної циклізації і від 33 новлення, оксадіазолу 271. Амінооксадіазол 271 різними добре відомими способами може бути перетворений у кінцевий продукт 273. Як конкретний приклад методу синтезу, зображеного на Фіг.6А, на Фіг.6В представлене одержання оксадіазолу 283. Інший спосіб синтезу заміщених оксадіазолів структурної формули (І) (де Ζ означає -Ν-), що є регіоізомерами синтезованої вище сполуки, представлений на Фіг.7А. Як показано на Фіг.7А, аамінооксим 287 (отриманий конденсацією гідроксиламіну з фенілцианідом) може бути сконденсований з ацилхлоридом 285 з утворенням, після дегідратаційної циклізації та відновлення, оксадіазолу 289. Амінооксадіазол 289 різними відомими способами може бути перетворений у кінцевий продукт 291. Як конкретний приклад способу синтезу, зображеного на Фіг.7 А, на Фіг.7В представлене одержання оксадіазолу 301. Слід зазначити, що способи, описані вище на Фіг.6 і 7, можуть бути легко адаптовані до синтезу триазолів заміною в описаній реакційній послідовності гідроксиламіну гідразином. Тіазоли структурної формули (II) можуть бути синтезовані в результаті відповідного перетворення способів Фіг.27 або за допомогою інших широко відомих методик. Аналізи модуляції HCV Сполуки винаходу є сильними інгібіторами реплікації і/чи проліферації HCV. Активність сполук винаходу може бути підтверджена in vitro за допомогою аналізів, використовуваних для виміру інгібування вірусної чи ретровірусної реплікації чи проліферації. Такі аналізи добре відомі. Конкретний приклад аналізу реплікації, застосовуваний для підтвердження активності даних сполук, представлений у розділі «Приклади». Як альтернатива, активність сполук може бути підтверджена за допомогою вестерн-блотінгу, що використовує мічені специфічні антитіла для білків HCV. Ще один аналіз, використовуваний для підтвердження антиHCV властивостей різних сполук винаходу, описаний у [роботі Founder et al., 1998; J. Gen. Virol. 79(10):2367-2374], розкриття якої приведено як матеріал, на який можно посилатися. Відповідно до цього способу, гепатоцити можуть бути протестовані при впливі й у відсутності конкретної тестуємої сполуки, і для сполуки визначена величина ІС50· Узагалі, активними вважаються сполуки, що виявляють величину IC50 (наприклад, концентрацію сполуки, що приводить до зниження реплікації на 50% чи до зменшення кількості обмірюваного білка HCV на 50%) в окремому аналізі близько 1мМ чи нижче. Найбільш корисні в терапевтичних чи профілактичних цілях при лікуванні чи попередженні HCV-інфекцій сполуки, що показують величину ICso, наприклад, в інтервалі близько 100мКм, 10мкМ, 1мкМ, 100нМ, 10нМ, 1нМ чи навіть нижче. Або ж, активними є сполуки, що виявляють величину LD50 (тобто концентрацію сполуки, при якій гине 50% вірусу) в інтервалі близько 1мМ чи нижче. Найбільш корисні в терапевтичних чи профілактичних цілях при лікуванні чи попередженні HCVінфекцій сполуки, що показують меншу величину 80435 34 LD50, наприклад, в інтервалі близько 100мКм, 10мКм, 1мКм, 100 нМ, 10 нМ, 1 нМ чи ще нижче. Застосування і способи введення Завдяки своїй здатності інгібувати реплікацію і/чи проліферацію HCV сполуки винаходу і/чи їхні композиції можуть використовуватися в різних ситуаціях. Наприклад, сполуки винаходу можуть використовуватися в якості контрольних у дослідах in vitro для ідентифікації нових більш-менш сильних анти-HCV сполук. Чи, наприклад, сполуки винаходу і/чи їхні композиції можуть використовуватися як консерванти чи дезінфектанти в обстановці клініки для попередження інфікування медичних інструментів і приладдя вірусом HCV. При такому використанні сполуки винаходу і/чи їхньої композиції можуть застосовуватися для дезінфікування інструментів у концентрації, кратній, наприклад ЇХ, 2Х, ЗХ, 4Х, 5Х чи більше, обмірюваній величині ІС50 сполуки. Особливе застосування сполуки винаходу і/чи їхньої композиції знаходять при лікуванні і/чи попередженні HCV-інфекції у тварин і людей. При такому використанні сполуки можуть уводитися per se (самі по собі), однак, як правило, їх готують і вводять у формі фармацевтичної композиції. Точна необхідна композиція буде залежати, серед іншого, від способу введення і буде легко визначена фахівцем. Ряд прийнятних фармацевтичних композицій описаний, наприклад, у [Remington's Pharmaceutical Sciences, 17th ed., 1989]. Композиції для перорального застосування можуть складатися з (а) рідких розчинів, таких як ефективна кількість активної сполуки, суспендованного в розріджувачі, такому як вода, фізіологічний розчин чи PEG 400; (b) капсул, саше чи таблеток, кожна з яких містить задану кількість активного компоненту у вигляді рідини, порошку, чи гранул желатину; (с) суспензій у відповідній рідині; і (d) прийнятних емульсій. Таблетовані форми можуть включати один чи більше компонент із наступного переліку: лактоза, сахароза, маніт, сорбіт, фосфати кальцію, кукурудзяний крохмаль, картопляний крохмаль, мікрокристалічна целюлоза, желатин, колоїдний діоксид кремнію, тальк, стеарат магнію, стеаринова кислота та інші добавки, пігменти, наповнювачі, зв'язувальні речовини, розріджувачі, буферні агенти, зволожувачі, консерванти, ароматичні і смакові агенти, барвники, диспергуючі агенти та фармацевтично прийнятні носії. Коржі можуть включати активний інгредієнт в ароматичному чи смаковому агенті, наприклад, сахарозі, а також можуть являти собою пастилки, що містять активний інгредієнт в інертній основі, такий як желатин і гліцерин чи емульсії сахарози й аравійської камеді, гелі тощо, що включає крім активного інгредієнта відомі носії. Обрана сполука, сама по собі чи в комбінації з іншими придатними компонентами, може бути приготовлена в аерозольних упакувках (тобто вони можуть бути "розпорошеними") для введення інгаляцією. Аерозольні препарати можуть міститися в придатних стиснутих пропелентах, таких як дихлордіфторметан, пропан, азот тощо. Прийнятні рецептури для ректального застосування включають, наприклад, супозиторії, що 35 складаються з нуклеїнової кислоти, упакованої із супозиторною основою. Придатні супозиторні основи включають природні чи синтетичні тригліцериди чи парафінові вуглеводні. Крім цього можливо також використання желатинових ректальних капсул, що складаються з комбінації обраної сполуки з основою, що включає, наприклад, рідкі тригліцериди, поліетиленгліколі та парафінові вуглеводні. Рецептури, придатні для парентерального введення, такого як, наприклад, внугрішньосуглобне (в суглоб), внутрішньовенне, внутрішньомускульне, внутрішньошкірне, внутрішньочеревне і підшкірне введення, включають водяні та безводні ізотонічні стерильні розчини для ін'єкцій, що можуть містити антиоксиданти, буферні розчини, бактеріостатичні фактори та розчинені речовини, що роблять рецептури ізотонічними з кров'ю даного реципієнта, а також водяні і безводні стерильні суспензії, що можуть включати суспендуючі агенти, розчинники, загущувачі, стабілізатори і консерванти. У практиці даного винаходу композиції можуть бути введені, наприклад, внутрішньовенною інфузією, перорально, місцево, внутрішньочеревно, внутрішньоміхурно чи інтратекально. Кращими способами введення є парентеральне введення, пероральне введення і внутрішньовенне введення. Рецептури сполук можуть бути представлені в монодозних чи мультидозних запаяних ємкостях, таких як ампули і флакони. Розчини та суспензії для ін'єкції можуть бути приготовлені зі стерильних порошків, гранул і таблеток описаного вище виду. Переважно, щоб фармацевтичні препарати були у формі доз на один прийом. У такій формі препарат розділений на разові дози, що містять відповідні кількості активного компоненту. Разова лікарська форма може бути упакованим препаратом, упаковкою, що містить окремі кількості препарату, такі як упаковані таблетки, капсули і порошки у флаконах чи ампулах. Також одиниця лікарської форми сама по собі може бути капсулою, таблеткою, крохмальною капсулою чи коржем, або може являти собою відповідну кількість кожного з них в упакованій формі. При необхідності композиція також може містити інші сумісні терапевтичні агенти. У терапевтичних цілях при лікуванні HCVінфекції сполуки, використані відповідно до фармацевтичного способу винаходу, вводять пацієнтам з діагностованою HCV-інфекцією в дозах, що забезпечують терапевтичну користь. Терапевтична користь означає, що введення сполуки приводить до доброчинного впливу на пацієнта протягом часу. Наприклад, терапевтична користь досягнута, якщо титр чи вірусне навантаження HCV у пацієнта знижується або припиняє рости. Також терапевтична користь досягається, якщо введення сполуки сповільнює чи цілком зупиняє початок руйнування органу або сповільнює чи зупиняє інші негативні симптоми, що звичайно супроводжують HCV-інфекції незалежно від титру чи вірусного навантаження HCV у пацієнта. Сполуки винаходу і/чи їхні композиції також можуть вводитися профілактично пацієнтам, що піддаються ризику розвитку HCV-інфекції, чи паці 80435 36 єнтам, що піддаються впливу HCV, для запобігання розвитку HCV-інфекції. Наприклад, сполуки винаходу і/чи їхні композиції можуть вводитися лікарняним співробітникам, що випадково укололися голкою при роботі з хворими HCV, для зниження ризику чи повного запобігання розвитку HCV-інфекції. Початкові дози, що підходять для введення людині, можуть бути визначені аналітично in vitro чи на тваринних моделях. Наприклад, може бути виготовлена початкова доза, що приводить до досягнення концентрації в сироватці крові, що співвідноситься з величиною ІС50 конкретної сполуки, що вводиться, визначеної в досвіді in vitro. Або ж, початкова доза для людини може бути заснована на дозах, визначених як ефективні на тваринних моделях з HCV-інфекцією, що добре відома в даній області. Типові придатні модельні системи описані в [роботах Muchmore, 2001, Immumol. Rev. 183:86-93 і Lanford & Bigger, 2002, Virology 293(i):l-9] і посиланнях, цитованих у даному контексті, розкриття яких приведено тут як посилальний матеріал. Наприклад, початкова доза може лежати в інтервалі приблизно від 0,001мг/кг до 1000мг/кг щодня. Також може бути використана добова доза в інтервалі приблизно від 0,01мг/кг до 500мг/кг, чи приблизно від 0,1мг/кг до200мг/кг, чи приблизно від 1мг/кг до 100мг/кг, чи приблизно від 10мг/кг до 50мг/кг. Однак дози можуть варіюватися в залежності від потреб пацієнта, важкості захворювання та використованої сполуки. Крім того, розмір дози буде визначатися наявністю, природою і ступенем будь-яких несприятливих побічних ефектів, що супроводжують введення даної сполуки даному пацієнту. Визначення правильної дози в конкретній ситуації є компетенцією практикуючого лікаря. Як правило, лікування починають з невеликих доз, що менше оптимальної дози сполуки. Після цього дозу потроху підвищують до досягнення оптимального ефекту за даних умов. При необхідності для зручності загальна денна доза може бути поділена і вводитися протягом дня порціями. Комбінаційна терапія Відповідно до деяких здійснень даного винаходу, сполуки винаходу і/чи їхні композиції можуть застосовуватися в комбінаційній терапії з, щонайменше, ще одним терапевтичним агентом. Сполука винаходу і/чи його композиція і терапевтичний агент можуть діяти сукупно, що більш переважно, чи синергічно (взаємно підсилюючи дії один одного). Відповідно до кращого здійснення, сполуку винаходу і/чи його композицію вводять одночасно з введенням іншого терапевтичного агента. Відповідно до іншого здійснення, сполуку винаходу і/чи його композицію вводять перед чи слідом за введенням іншого терапевтичного агента. Згідно одного зі здійснень, сполуки винаходу і/чи їхні композиції можуть бути використані в комбінаційній терапії з іншими противірусними агентами. Згідно одного зі здійснень, сполуки винаходу і/чи їхні композиції можуть бути використані в комбінаційній терапії з інтерфероном-α. Відповідно до іншого здійснення, сполуки винаходу і/чи їхні композиції можуть бути використані в комбінаційній терапії з рибавирином. Згідно ще одного здійснен 37 ня, сполуки винаходу і/чи їхні композиції можуть бути використані в комбінаційній терапії з рибавирином й інтерфероном-α Приклади Наступний приклад приведений лише як ілюстрація, але не як обмеження. Фахівці в даній області легко визначать ряд некритичних параметрів, що можуть бути змінені чи модифіковані для одержання аналогічних, власне кажучи, результатів. Типові сполуки винаходу, інгібуючі трансляцію або реплікацію HCV Інгібуюча активність деяких типових сполук винаходу була підтверджена за допомогою аналізу реплікації HCV. Реплікон HCV може включати такі особливості як HCV IRES, HCV 3'-нетрансльовану область, окремі гени HCV, кодуючі поліпептиди HCV, селективні маркери та репортерний ген, такий як люцифераза, GFP (green fluorescent protein - «зелений білок, який світиться») і т.д. При проведенні аналізу клітин, що активно діляться і містять 5-2Luc-реплікон, сіяли зі щільністю приблизно від 5000 до 7500 клітин/лунку у 96-луночні планшети (близько 90мкл клітин у кожній лунці) та інкубували при температурі 37°С і 5% СО2 протягом 24 годин. Потім у кожну лунку додавали тестуєму сполуку (в об'ємі близько 10мкл) при різних концентраціях, після чого клітини інкубували протягом ще 24 годин перед аналізом із використанням люцифера 80435 38 зи. Клітини збирали і реєстрували реплікацію і трансляцію HCV аналізом за допомогою репортерних генів, наприклад, репортерним аналізом із використанням люциферази. З кожної клітини було аспіроване середовище й у кожну лунку додані реагенти для аналізу з використанням люциферази Bright-Glo (Pharmacia, Peapack, NJ) відповідно до інструкцій виробника. У ході цього аналізу була визначена кількість тестуємої сполуки, що приводило до зменшення емісії люциферази на 50% (IC50)· Деякі типові сполуки винаходу, крім того, були протестовані на їхню здатність інгібувати реплікацію HCV за допомогою кількісного вестернблотінгу з антитілами, специфічними для визначених білків HCV. У ході цього аналізу визначали кількість тестуємої сполуки, що приводить до 50% зменшення кількості специфічних білків HCV у порівнянні з контрольним зразком (IC50)· Результати аналізів реплікону і вестернблотінгу представлені нижче в Таблиці 1. Структури зазначених сполук зображені на Фіг.1. У Таблиці 1 знак "+" вказує на величину ICso, рівну 10мКм чи меншу в даному аналізі; а знак "-" вказує на величину ICso, більшу 10мКм у даному аналізі. Для ряду сполук при аналізі реплікона були отримані величини ICso, ню лежать у наномолярному інтервалі. 39 80435 40 41 80435 42 43 80435 44 45 Для ідентифікації неспецифічних інгібіторів репортерного гену застосовували зворотній скринінг. При зворотньому скринінгу для ідентифікації сполук, інгібуючих репортерних генів і не інгібуючих HCV, використовували лінію клітин, що несуть таку конструкцію, як CMV-керований ген люциферази. Для багатьох сполук при аналізі інгібування люциферази методом зворотнього скринінгу величини ІС50 були більше 10мКм. Цитотоксичність сполук винаходу визначали стандартним аналізом клітинної проліферації. Обмірювані величини LD50 для багатьох сполук виявилися більше 10мКм, що підтверджувало, що результати відбивали знижене продукування вірусу, а не загибель клітин. Для аналізу числа копій РНК HCV використовували аналіз TaqMan RT-PCR (Roche Molecular Systems, Pleasanton, CA), що підтвердив, що геном вірусу HCV не піддавався реплікації. Клітини 9-13 реплікону, що активно діляться, засівали зі щільністю 3 χ 104 клітин/лунку в об'ємі 1мол/лунку у 24-луночні планшети. Потім клітини інкубували при температурі 37°С і 5% СО2 протягом 24 годин. Через 24 години після висівання клітин у кожну лунку додавали різні концентрації сполук (в об'ємі 10 ул). Клітини інкубували разом зі сполуками протягом ще 24 годин, після чого середовище видаляли аспірацією і для кожної лунки готували зразки РНК. Для свіжоприготовлених зразків РНК виконували одностадійний аналіз TaqMan RT-PCR відповідно до інструкції виробника. Для визначення специфічності інгібування HCV і підтвердження того, що не відбувається реплікація вірусного геному, використовували відношення РНК HCV до клітинного GAPDH РНК. Сполуки є нетоксичними на клітинній і тваринній моделях Цитотоксичність Для сполук 1, 3, 7, 9,11,13,17,19, 21, 27, 29, 31, 33, 35, 37, 39, 47, 49, 51, 57 і 69 проводили аналіз цитотоксичності на клітинах печінки, що включають реплікон HCV (клітини 5-2 Luc, клітини 9-13 чи клітини Huh-7). У ході аналізу клітини висівали в 96-луночні планшети (приблизно 7500 клітин/лунку в об'ємі 90мкл) і вирощували протягом 24 годин при температурі 37°С. На 2 день в лунки додавали різні концентрації тестуємої сполуки (в об'ємі 10мкл), після чого клітини вирощували протягом ще 48 годин при температурі 37°С. На 4 день проводили аналіз Атф-залежної R-люциферази (Cell Titer Glo assay) для визначення кількості життєздатних клітин. За винятком сполук 13, 19 і 57 усі протестовані сполуки показали величини ICso, більші чи рівні 10мКм, що підтверджує їхню нетоксичність. Залишені сполуки за винятком 13, що показала величину іс50 ЗмКм, мали величини ІС50, більші 5мКм, що також свідчить про їхню гарну переносимість. Синтез сполук Сполуки З (R909794) і 9 (R909921) Стадія А Згідно Фіг.4С, сполуку 230 (25м, 98,1ммоль) додавали до 96% H2SO4 (50мол) при температурі 0°С, потім додавали 96% HNO3 (17,5мол) і отриману суміш нагрівали при температурі 130°С протягом 3 годин. Реакційну масу прохолоджували, 80435 46 потім виливали в лід і додавали карбонат натрію до появи осаду (р>7). Продукт відфільтровували, промивали водою, сушили й одержували сполуку 232 у вигляді кристалів жовтого кольору (17,0м, 79%). Стадія В До сполуки 232 (17м, 78ммоль) у СНСl3 (200мол) додавали РВr3 (7,4мол), і отриману суміш кип'ятили зі зворотнім холодильником протягом 1 години чи до повного завершення реакції, контролюючи методом тонкошарової хроматографії. Реакційну масу прохолоджували, при зниженому тиску видаляли основну частину розчинника, залишок виливали в лід і одержували кристалічну речовину жовтого кольору. Продукт відфільтровували й одержували сполуку 234 (14,5 м, 92%). Стадія С До суміші сполуки 234 (6м, 0,029моль), PdCl2(Ph3)2(620мг, 3мол.%), Си (338мг, 6мол.%) в атмосфері азоту додавали диізопропілетиламін (100мол). Отриману масу перемішували кілька хвилин при кімнатній температурі перед додатком ТМС-ацетилену (6,3мол, 1,5екв.). Потім вміст нагрівали при температурі 60°С протягом 24 годин. При зниженому тиску відганяли розчинник, технічний продукт фільтрували через стовпчик із силікагелем (гексан-ЕЮАс, 10:1) і одержували сполуку 236 у вигляді кристалів жовтого кольору, 4,9м (76%). Стадія D Суміш сполуки 236 (1,4г), порошку Fe (3,55м, 10екв.), концентрованої НСl (1мол) і метанолу (100мол) кип'ятили зі зворотнім холодильником протягом 3 годин. Після охолодження реакційну масу фільтрували, розчин концентрували, залишок розбавляли NaHCO3 і екстрагували ЕtOAc (кілька разів). Об'єднані ЕtOAc екстракти сушили, фільтрували, концентрували й одержували технічний продукт (1,0г) у вигляді суміші сполуки 238 і десилірованого продукту 240. Маслянисту суміш розчиняли в метанолі (100мол) і обробляли К2СО3 (приблизно 2 екв.). Після перемішування при кімнатній температурі протягом 1 години реакційну масу концентрували у вакуумі. Залишок розчиняли в ЕtOAc, промивали водою, сушили, фільтрували і концентрували у вакуумі. Продукт 240 (513мг) одержували у вигляді олії темно-пурпурового кольору. Стадія Ε Сполуку 240 (513мг) розчиняли в сухому дихлорметані (50мол) і під азотом додавали Εt3Ν (0,786мол, 1,3екв.). Суміш прохолоджували на крижаній лазні і по краплинах додавали розчин дихлорацетилхлориду (0,483мол, 1,1екв.) у сухому дихлорметані (5мол). Реакційну масу залишали нагріватися до кімнатної температури протягом 6 годин і потім розбавляли ЕЮАс, промивали насиченим розчином бікарбонату натрію, сушили, фільтрували і концентрували у вакуумі. Технічний продукт пропускали через шар силікагелю, елюіруючи сумішшю гексан- ЕtOAc, 1:1. Фракції концентрували й одержували олію пурпурного кольору, що закристалізувалася в глибокому вакуумі з утворенням сполуки 255 (658мг). 47 Стадія F Хлороксим 2-фтор-6-трифторметилбензальдегіду (645мг, 1,1екв.) і сполуку 255 (658мг) розчиняли в сухому ТГФ (30мол) і додавали Et3N (0,521мол, 1,3екв.). Реакційну масу перемішували при кімнатній температурі протягом 1 години і потім нагрівали зі зворотнім холодильником протягом 5 годин до повного завершення реакції. Розчинник відганяли у вакуумі, залишок розчиняли в ЕtOAc, промивали водою, потім насиченим розчином хлориду натрію, сушили, фільтрували і концентрували. Технічний продукт очищали хроматографією (гексан- ЕtOAc, 3:2) і одержували сполуку 3 (800мг). Сполуку 9 синтезували аналогічним чином із хлороксиму 2,6-дихлорбензальдегіду і сполуки 255. Синтез сполуки 49 (R905952) Одержання 3-(2-метокси-6-трифторметилфеніл)-5-(4-амінопіридил)ізоксазолу. До розчину К-гідрокси-(2-метокси-6трифторметилбензол)карбоксимідоілхлориду (1м, 3,94ммоль) і 4-аміно-2-етинилпіридину (310мг, 2,63ммоль) у ТГФ додавали триетиламін (550мол, 3,94ммоль). Реакційну масу перемішували при кімнатній температурі протягом 1 години і потім кип'ятили зі зворотнім холодильником протягом 3 годин. Суміш прохолоджували до кімнатної температури, додавали етилацетат і воду. Відокремлювали органічний шар, сушили його над сульфатом натрію, фільтрували і концентрували у вакуумі до одержання технічного продукту. Кінцевий продукт, 3-(2-метокси-6-трифторметилфеніл)-5-(4амінопіридил)ізоксазол (609мг), одержували очищенням за допомогою флеш-хроматографії, елюіруючи сумішшю гексан-ети л ацетат (4:1). Молекулярна маса=335,28, підтверджений ЖХ-МС, tr=8,38 хв. (Метод Y) М+=335,28 1 H ЯМР (300мгц, CDCl3): 8,24 (м., 1H), 7,48 (м., 1H), 7,4 (м., 1H), 7,26 (м., 1Н), 7,2 (м., 1Н), 7,0 (с, 1H), 6,6 (м., 1H), 4,8 (шир.с, 2Н), 3,8 (с, 3Н). Одержання 2,2-дихлор-N-[3-(2-метокси-6трифторметилфеніл)-5-ізоксазоліл]-(4-піридил) ацетаміду Суміш 3-(2-метокси-6-трифторметилфеніл)-5(4-амінопіридил)ізоксазолу (609мг, 1,82ммоль) і триетиламіну (1,8мол, 12,9ммоль) у дихлорметані прохолоджували на крижаній лазні. По краплинах додавали розчин дихлорацетилхлориду (1,3мол, 12,9ммоль) у дихлорметані. Після перемішування протягом не менше години додавали воду і етилацетат. Органічний шар відокремлювали, промивали насиченим розчином гідрокарбонату натрію, фільтрували і концентрували у вакуумі. Кінцевий продукт, 2,2-дихлор-N-[2-[3-(2-метокси-6трифторметилфеніл)-5-ізоксазоліл]-(4-піридил) ацетамід (300мг), одержували флешхроматографією, елюіруючи сумішшю гексанетилацетат (4:1). Молекулярна маса=446,21 підтверджена ЖХМС, tr=9,84 хв. (Метод Y) МН+=447.21. 1 H ЯМР (300мгц, CDCl3): 9,84 (с, 1H), 8,63 (м., 1H), 7,9 (м., 1H), 7,62 (м., 1H), 7,41 (м., 1 Η), 7,22 (м., 1H), 5,64 (с, 1Н), 3,8 (с, З3Н). (Активність реплікону ++) 80435 48 Синтез сполуки 57 (R905948) Одержання 3-(2,2-дихлорацетамідо)-5етинілпіридину Суміш 3-аміно-5-етинілпіридину (2,73м, 23,1ммоль) і триетиламіну (3,54мол, 25,42ммоль) у дихлорметані прохолоджували на крижаній лазні. По краплинах додавали розчин дихлорацетилхлориду (2,57мол, 25,42ммоль) у дихлорметані. Після перемішування протягом не менше години додавали воду і етилацетат. Органічний шар відокремлювали, промивали насиченим розчином гідрокарбонату натрію, сушили над сульфатом натрію, фільтрували, концентрували у вакуумі й одержували 3-(2,2-дихлорацетамідо)-5-етинілпіридин (3,5г). Молекулярна маса=229,31 підтверджена ЖХМС, tr=9,76 хв. (Метод Y) МН+=230,3. 1 H ЯМР (300мгц, CDCl3): 8,7 (с, 1Н), 8,52 (с, 1H), 8,2 (м., 2H), 6,08 (с, 1Н), 3,21 (с, 1Н). Одержання 2,2-дихлор-К-[3-[3-(2-метокси-6трифторметилфеніл)-5-ізоксазоліл]-(5піридил)ацетаміду До розчину К-гідрокси-(2-метокси-6трифторметилбензол)карбоксимідолілхлориду (111мг, 0,44ммоль) і 3-(2,2-дихлорацетамідо)-5етинілпіридину (100мг, 0,44ммоль) у ТГФ додавали триетиламін (0,91мол, 0,65ммоль). Реакційну масу перемішували при кімнатній температурі протягом 1 години і потім кип'ятили зі зворотнім холодильником протягом 3 годин. Суміш прохолоджували до кімнатної температури, додавали етилацетат і воду. Органічний шар відокремлювали, сушили над сульфатом натрію, фільтрували і концентрували у вакуумі до одержання технічного продукту. Кінцевий продукт, 2,2-дихлор-К-[3-[3-(2метокси-6-трифторметилфеніл)-5-ізоксазоліл]-(5піридил)ацетамід (103мг), одержували очищенням за допомогою флеш-хроматографії, елюіруючи сумішшю гексан-етилацетат (4:1). Молекулярна маса=446,31 підтверджена ЖХМС, tr= 13,45 хв. (Метод Y) N11^=447,31. 1 H ЯМР (300мгц, CDCl3): 9,4 (шир.с, 1H), 9,0 (с, 1Н), 8,9 (с, 2Н), 7,58 (м., 1Н), 7,4 (м., 1Н), 7,24 (м., 1Н), 6,8 (с, 1Н), 6,2 (а, 1H), 3,8 (с, 3Н). (Активність реплікону ++) Загальний синтез сполук винаходу Крім того, сполуки винаходу можуть бути отримані способами, зображеними на Фіг.8-63. Фахівець у даній області легко зможе синтезувати сполуки в об'ємі винаходу на підставі приведеного тут посібника, а також Фіг.1 -63, посилань, представлених на малюнках, а також маючи на увазі експериментальні методики, представлені у [Попередній Заявці US 60/467650, дата подачі 2 травня 2003р. (номер реєстру повіренного Р-71847-2], повідомлення про які проведені тут як посильний матеріал. Наприклад, для загального синтезу не утримуючий азот у "С"-кільці ізомерів див. розділи 5.3, 6.1 і наступні. Замість зображених там негетероароматичних кілець у "С"-кільці можуть бути використані пірид-2-ил, пірид-3-ил чи пірид-4-ил. Крім того, варто розуміти, що на всіх малюнках від Фіг.1 до Фіг.63 для зручності зображені "С"-циклічні позиційні ізомери. Варто розуміти, що піридильне кільце може бути пірид-2-илом, пірид-3-илом чи 49 пірид-4-илом. Крім того, слід зазначити, що в багатьох препаратах стандартне "А"-кільце являє собою 2,6-дихлорфеніл. Це лише ілюстрація і ні в якому разі не є обмеженням. Вихідна сировина для одержання сполук винаходу та їхніх напівпродуктів є комерційно доступною або може бути отримана добре відомими методами синтезу [див, наприклад, Harrison et ah, "Compendium of Synthetic Organic Methods" (Перелік органічних синтетичних методів), Vols. 1-8, John Wiley і Sons, 1971-1996; "Beilstein Handbook of Organic Chemistry," (Довідник Бейльштейна з органічної хімії) Beilstein Institute of Organic Chemistry, Frankfurt, Germany; Feiser et al, "Reagents for Organic Synthesis," (Реагенти для органічного синтезу) Volumes 1-17, Wiley Interscience; Trost et al, "Comprehensive Organic Synthesis," (Загальний органічний синтез) Pergamon Press, 1991; "TheilheiMer's Synthetic Methods of Organic Chemistry," Volumes 1-45, Karger, 1991; March, "Advanced Organic Chemistry," (Органічна хімія) Wiley Interscience, 1991; Larock "Comprehensive Organic Transformations," (Загальні огранічні перетворення) VCH Publishers, 1989; Paquette, "Encyclopedia of Reagents for Organic Synthesis," (Енциклопедія реагентів для органічного синтезу) John Wiley & Sons, 1995]. Інші способи синтезу сполук, приведених тут, і/чи вихідної сировини описані в літературі або будуть очевидні для фахівця в даній області. Альтернативу реагентам і/чи захисним групам, зображеним на Фіг.2-7, можна знайти в зазначеному вище посилальному матеріалі й інших джерелах, добре відомих фахівцям. Посібником з вибору придатної захисної групи може служити, наприклад, [збірник Greene & Wuts, "Protective Groups in Organic Synthesis," (Захисні групи в органічному синтезі) Wiley Interscience, 1999]. Таким чином, способи синтезу і стратегія, представлені в даному контексті, є скоріше ілюстративними, ніж вичерпними. Зокрема, способи синтезу заміщених дифенілізоксазолів структурної формули (І) (де Ζ означає -СН-) представлені на Фіг.2А - 7В і 12С - 12Е. Фіг.4С, 4D і Фіг. з 15 по 18, на яких описано одержання ацетиленових сполук, обговорюються в розділі «Приклади». Варто розуміти, що на Фіг.1 - 63 і на всій протяжності більшої частини опису винаходу, позначка- ізомери "С"-кільця зображені лише як приклад. Методики одержання позиційних орто-, позначкачи парів-ізомерів "С"-кільця можуть бути обрані кваліфікованим фахівцем. Тому, якщо описані позначки-ізомери "С"-кільця, аналогічна методика синтезу може бути використана для одержання орто- чи парів-ізомерів "С"-кільця. Позначка-ізомер на всіх малюнках з Фіг.1 по Фіг.63 використана для простоти і дотримання послідовності, щоб продемонструвати здатність одержувати сполуки, які зацікавили. На Фіг.1 - 63 заступники R2, R3, R4, R5, R6, R8, 9 R , R10 і R14 можуть включати реакційноздатні функціональні групи, що вимагають захисту під час синтезу. Вибір придатної захисної групи буде залежати від природи функціональної групи і використовуваного способу синтезу і буде очевидний 80435 50 для фахівця в даній області. Посібником з вибору придатної захисної групи може служити збірник Greene & Wuts, supra, а також інші приведені в даному контексті посилальні матеріали. Посібник з проведення реакцій 1,3диполярного циклоприєднання, яке також називається 1,3-диполярним приєднанням, [3+2]циклізації чи [3+2]циклоприєднання можна знайти в [роботі "Cycloaddition Reactions in Organic Synthesis" (Реакції циклоприєднання в органічному синтезі), (Kobayashi, S. and Jorgensen, Κ. Α., Editors), 2002, Wiley-VCH Publishers, pp. 1 - 332 (особливо глави б і 7 - по [3+2]циклоприєднанням і 1,3-диполярним приєднанням, стор. 211 - 248 і 249 - 300); "1,3-Dipolar Cycloaddition" (1,3-Диполярне циклоприєднання), Chemistry of Heterocyclic Compounds, Vol. 59, (Padwa, Α., Pearson, W., Editors), 2002, John Wiley, New York, pp. 1-940; "Nitrile Oxides, Nitrones, Nitronates in Organic Synthesis: Novel Strategies in Synthesis" (Оксиди нітрилів, нітрони, нітронати в органічному синтезі: нові стратегії синтезу), Torssel, К. В. G., 1988, VCH Publishers, New York, pp. 1-332; Barnes & Spriggs, 1945, J. Am. Chem Soc. 67:134; Anjaneyulu et al., 1995, Indian J. Chem., Sect. 5 34(11):933-938); і Т. L. Gilchrist, Pitman Publishing Ltd, 1985 ISBNO-27302237-7; Strategies for Organic Drug Synthesis and Design (Стратегії синтезу і створення органічних лікарських препаратів), Lednicer, D., John Wiley and Sons, 1998]. Крім того, методики синтезу ізоксазолів та їхніх гідроізомерів можна знайти в наступних роботах: [М. Sutharchanadevi, R. Murugan у Comprehensive Heterocyclic Chemistry ІЦЗагапьна гетероциклічна хімія) A.R. Katritzky, C.W. Rees, E.F.V. Scriven, Eds.; Pergamon Press, Oxford, Vol. 3, p. 221; R. Griinager, P, Vita-Finzi у Heterocyclic Compounds, (Гетероциклічні сполуки) Vol. 49, Isoxazoles, (Ізоксазоли) Part one, John Wiley і Sons, New York, 1991; К. В. G. Torssell, Nitrile Oxides, Nitrones, and Nitronates in Organic Synthesis, (Оксиди нітрилів, нітрони, нітронати в органічному синтезі) VCH Publishers, New York, 1988; Y-Y. Ku, Τ. Grieme, P. Sharma, Y.-M. Pu, P. Raje, H. Morton, S. King Organic Letters, 2001, 3, 4185; V. G. Desai, S. G. Tilve Synth. Comm., 1999, 29, 3017; X. Wei, J. Fang, Y. Hu, H. Hu Synthesis, 1992, 1205; С Kashima, N. Yoshihara, S. Shirai Heterocycles, 1981, 16,145; A.S.R. Anjaneyulu, G.S. Rani, K.G. Annapurna, U. V. Mallavadhani, Y.L.N. Murthy Indian J. Chem. Sect B, 1995, 34, 933; R.P. Barnes, A.S. Spriggs, J. Am. Chem. Soc, 1945, 67, 134; A. Alberola, L. Calvo, A.G. Ortega, M.L. Sabada, M.C. Safiudo, S.G. Granda, E.G. Rodriguez Heterocycles, 1999, 51, 2675; X. Wang, J. Tan, K. Grozinger Tetrahedron Lett. 2000, 41, 4713; A. R. Katritzky, M. Wang, S. Zhang, M.V. Voronkov J. Org. Chem., 2001, 66, 6787; J. Bohrisch, M. Patzel, С Mugge, J. Liebscher Synthesis, 1991, 1153; SHANKAR, B.B.; Yang, D.Y.; Girton, S.; Ganguly, A.K.; Tetrahedron Lett (TELEAY) 1998, 39 (17), 2447-2448. CHENG, W.C.; Wong, M.; Olmstead, M.M.; Kurth, M.J.; Org Lett (ORLEF7) 2002, 4 (5), 741-744. KHAN, M.S.Y.; Bawa, S.; Indian J. Chem, SectB: Org Chem Incl Med Chem (USBDB) 2001, 40 (12), 1207-1214. SIMONI, 51 D.; et al; J Med Chem (JMCMAR) 2001, 44 (14) 2308-2318. NUGIEL, D.A.; Tetrahedron Lett (TELEAY) 2001, 42 (21), 3545-3547. ARAI, N.; Iwakoshi, M.; Tanabe, K.; Narasaka, K.; Bull Chem Soc Jpn (BCSJA8) 1999, 72 (10), 2277-2285. SAGINOVA, L.G.; Grigorev, E.V.; Chem Heterocyd Compd (Ν Υ) (CHCCAL) 1999, 35 (2), 244-247. MURI, D.; Bode, J.W.; Carreira, E.M.; Org Lett (ORLEF7) 2000, 2 (4), 539-541. KANEMASA, S.; Matsuda, H.; Kamimura, Α.; Kakinami, Т.; Tetrahedron (TETRAB) 2000, 56 (8), 1057-1064. MOCHALOV, S.S.; Kuzmin, Y.I.; Fedotov, A.N.; Trofmova, E.V.; Gazzaeva, R.A.; Shabarov, Y.S.; Zefirov, N.S.; Zh Org Khim (ZORKAE) 1998, 34 (9), 1379-1387. DA VIES, CD.; Marsden, S.P.; Stokes, E.S.E.; Tetrahedron Lett (TELEAY) 1998, 39 (46) 8513-8516. KANEMASA, S.; Matsuda, H.; Kamimura, Α.; Kakinami, Т.; Tetrahedron (TETRAB) 2000, 56 (8), 1057-1064. WEIDNER WELLS, M.A.; Fraga Spano, S.A.; Turchi, I.J.; J Org Chem (JOCEAH) 1998, 63 (18), 6319-6328. PADMAVATHI, V.; Bhaskar Reddy, A.V.; Sumathi, R.P.; Padmaja, Α.; Bhaskar Reddy, D.; Indian J Chem, SectB: Org Chem Incl Med Chem (USBDB) 1998, 37 (12), 1286-1289. WILLIAMS, A.R.; Angel, A.J.; French, K.L.; Hurst, D.R.; Beckman, D.D.; Beam, C.F.; Synth Commun (SYNCAV) 1999, 29 (11), 1977-1988. CARAMELLA, P.; Reami, D.; Falzoni, M.; Quadrelli, P.; Tetrahedron (TETRAB) 1999, 55 (22), 7027-7044. KIDWAJ, M.; Misra, P.; Synth Commun (SYNCAV) 1999, 29 (18), 3237-3250. SYASSI, В.; El Bakkali, В.; Benabdellah, G.A.; Hassikou, Α.; Dinia, M.N.; Rivere, Μ.; Bougrin, К.; Soufiaoui, Μ.; Tetrahedron Lett (TELEAY) 1999, 40 (40), 7205-7209. SYASSI, В.; Bougrin, K.; Soufiaoui, M.; Tetrahedron Lett (TELEAY) 1997, 38 (51), 88558858. LI, P.; Gi, H.J.; Sun, L.; Zhao, K.; J Org Chem (JOCEAH) 1998, 63 (2), 366-369. BOUGRIN, K.; Lamri, M.; Soufiaoui, M.; Tetrahedron Lett (TELEAY) 1998, 39 (25), 4455-4458. SRIVASTAVA, Y.K.; Sukhwai, S.; Ashawa, Α.; Verma, B.L.; J Indian Chem Soc (JICSAH) 1997, 74 (7) 573-574. CORSARO, Α.; Buemi, G.; Chiacchio, U.; Pistara, V.; Rescifina, Α.; Heterocycles (HTCYAM) 1998, 48 (5) 905-918. CORSARO, Α.; Librando, V.; Chiacchio, U.; Pistara, V.; Rescima, Α.; Tetrahedron (TETRAB) 1998, 54 (31), 9187-9194. CORSARO, Α.; Librando, V.; Chiacchio, U.; Pistara, V.; Tetrahedron (TETRAB) 1996, 52 (40), 13027-13034. BELENKII, L.I.; Gromova, G. .; Lichitshii, B.V.; Krayushkin, M.M.; Izv Akad Nauk, Ser Khim (IASKEA) 1997, (1), 106-109. KASHIMA, C; Takahashi, K.; Fukuchi, I.; Fukusaka, K.; Heterocycles (HTCYAM) 1997, 44 (1) 289-304. BASEL, Y.; Hassner, Α.; Synthesis (SYNTBF) 1997, (3), 309-312. BANNIKOV, G.F.; Ershov, V.V.; Nikiforov, G.A.; Izv Akad Nauk, Ser Khim (IASKEA) 1996 (2), 426-429. TOKUNAGA, Y.; Ihara, M.; Fukumoto, K.; Heterocycles (HTCYAM) 1996, 43 (8), 1771-1775. AHMED, G.A.; J Indian Chem Soc (JICSAH) 1995, 72 (3) 181-183. LU, T.J.; Yang, J.F.; Sheu, L.J.; J Org Chem (JOCEAH) 1995, 60 (23) 7701-7705. EASTON, C.J.; Hughes, C.M.M.; Tiekink, E.R.T.; Savage, G.P.; Simpson, G.W.; Tetrahedron Lett (TELEAY) 1995, 36 (4) 629-632. WALLACE, R.H.; Liu, J.; Tetrahedron Lett (TELEAY) 1994, 35 (41) 7493-7496. BALDOLI, C; Gioffreda, F.; Zecchi, 80435 52 G.; J Heterocycl Chem (JHTCAD) 1994, 31 (1), 251253. WE1DNER WELLS, M.A.; Fraga, S.A.; Demers, J.P.; Tetrahedron Lett (TELEAY) 1994, 35 (35), 64736476. HANSEN, J.F.; Georgiou, P.J.; J Heterocycl Chem (JHTCAD) 1994, 31 (6), 1487-1491. ANKHIWALA, M.D.; Hathi, M.V.; J Indian Chem Soc (JICSAH) 1994 71 (9) 587-589. KAMIMURA, Α.; Hori, K.; Tetrahedron (TETRAB) 1994, 50 (27) 7969-7980. ABB AD Υ, Μ.Α.; Hebbachy, R.; Indian J Chem, Sect В (IJSBDB) 1993, 32 (11), 1119-1124. MORIYA, O.; Takenaka, H.; Iyoda, M.; Urata, Y.; Endo, Т.; J Chem Soc, Perkin Trans 1 (JCPRB4) 1994 (4), 413-417. TANAKA, S.; Kohmoto, S.; Yamamoto, M.; Yamada, K.; Nippon Kagaku Kaishi (NKAKB8) 1992 (4), 420422. NAGARAJAN, Α.; Pillay, M.K.; Indian J Chem, Sect В (IJSBDB) 1993, 32 (4), 471-474. STOYANOVICH, F.M.; Bulgakova, V.N.; Krayushkin, M.M.; Lzv Akad Nauk SSSR, Ser Khim (IASKA6) 1991 (11), 2606-2611. BALDOLI, C; Del Buttero, P.; Manorana, S.; Zecchi, G.; Moret, M.; Tetrahedron Lett (TELEAY) 1993, 34 (15), 2529-2532. MIZUNO, K.; Ichinose, N.; Tamai, Т.; Otsuji, Y.; J Org Chem (JOCEAH) 1992, 57 (17), 4669-4675. HUANG, Z.T.; Wang, MX.; Synth Commun (SYNCAV) 1991, 21, 1167-1176. MOHAMED, T.A.; Kandeel, M.M.; Awad, I.M.A.; Youssef, M.S.K.; Collect Czech Chem Commun (CCCCAK) 1991, 56 (12), 2999-3005. MORIYA, O.; Urata, Y.; Endo, Т.; J Chem Soc. Chem Commun (JCCCAT) 1991 (13), 884-885. HUANG, Z.T.; Wang, M.X.; Synth Commun (SYNCAV) 1991, 21, 1167-1176. MORIYA. O.; Takenaka, H.; Urata, Y.; Endo, Т.; J Chem Soc, Chem Commun (JCCCAT) 1991 (23), 1671-1672. SOUFIAOUI, M.; Syassi, В.; Daou, В.; Baba, N.; Tetrahedron Lett (TELEAY) 1991, 32 (30), 3699-3700. SAGINOVA, L.G.; Kukhareva, I.L.; Lebedev, A.T.; Shabarov, YU, S.; Zh Org Khim (ZORKAE) 1991, 27 (9) 1852-1860. KANEMASA, S.; Nishiuchi, M; WADA, E.; Tetrahedron Lett (TELEAY) 1992, 33 (10), 1357-1360. MAMAEVA, O.O.; Krayushkin, M.M.; Stoyanovich, F.M.; lzv Akad Nauk SSSR, Ser Khim (IASKAG) 1990 (4), 913-916. BRTOKHOVETSKII, D.B.; Belenkii, L.I.; Krayushkin, M.M.; lzv Akad Nauk SSSR, Ser Khim (IASKAG) 1990 (7), 1692-1693. ITO, S.; Sato, M.; Bull Chem Soc Jpn (BCSJA8) 1990, 63 (9), 2739-2741. MORIYA, O.; Urata, Y.; Endo, Т.; J Chem Soc, Chem Commun (JCCCAT) 1991 (1), 17-18. ALMTORP, G.T.; Bachmann, T.L.; Torssell, K.B.G.; Acta Chem Scand (ACHSE7) 1991, 45 (2), 212-215. KHAN, M.S.Y.; Khan, M.H.; Kumar, M.; Javed, K.; J Indian Chem Soc (JICSAH) 1990, 67 (8), 689-691. KHALIL, Z.H.; Yanni, A.S.; Abdel-Hafez, A.A.; Khalaf, A.A.; J Indian Chem Soc (JICSAH) 1990, 67 (10), 821-823. SHIMIZU, Т.; Hayashi, Y.; Furukawa, N.; Teramura, K.; Bull Chem Soc Jpn (BCSJA8) 1991, 64 (1), 318320. FADDA, A.A.; Indian J Chem, Sect В (IJSBDB) 1991, 30 (8), 749-753. RAMA RAO, K.; Bhanumathi, N.; Srinivasan, T.N.; Sattur, P.B.; Tetrahedron Lett (TELEAY) 1990, 31, 899. ICHINOSE, N.; Mizuno, K.; Yoshida, K.; Otsuji, Y.; Chem Lett (CMLTAG) 1988, 723. SINISTERRA, J.V.; Marinas, J.M.; Bull Soc Chim Belg (BSCBAG) 1987, 96 (4), 293. BALABAN, A.T.; Zugravescu, I.; Avramovici, S.; Silhan, W.; Monatsh Chem (MOCMB7) 1970, 101, 704. LITINAS, K.E.; Nicolaides, D.N.; Varelia, E.A.; J Heterocycl Chem 53 (JHTCAD) 1990, 27, 769. ICHINOSE, N.; Mizuno, K.; Tamai, Т.; Otsuji, Y.; Chem Lett (CMLTAG) 1988, 233. THOSEN, I.; Torsseli, K.B.G.; Acta Chem Scand, Ser В (ACBOCV) 1988, 42, 303. ROCHE; Synthesis (SYNTBF) 1984 (12), 1083. CURRAN, D.P.; J Am Chem Soc (JACSAT) 1983, 105 (18), 5826. JAGER, V.; et al.; Bull Soc Chim Belg (BSCBAG) 1983, 92, 1039. RAO, C.J.; Reddy, K.M.; Murthy, A.K.; Indian J Chem, Sect В (IJSBDB) 1981, 20, 282. EIKASABY, M.A.; Salem, M.A.I.; Indian J Chem (IJOCAP) 1950, 19, 571. CHINCHOLKAR, MM.; Jamoda, V.S.; Indian J Chem (IJOCAP) 1979, 17 610. SHABAROV, Y.S.; Saginova, L.G.; Gazzaeva, R.A.; J Org Chem USSR (Engl Transl) (JOCYA9) 1982, 18, 2319. SHIMIZU, Т.; Hayashi, Y.; Yamada, K.; Nishlo, Т.; Teramura, K.; Bull Chem Soc Jpn (BCSJA8) 1981, 54, 217. WITZCAK, Z.; Heterocycles (HTCYAM) 1980, 14, 1319. DEMINA, L.A.; et al.; Zh Org Khim (ZORKAE) 1979, 15, 735. CHEM ABSTRA (CHABA8), 91 (74512). ARCHIBALD, A.T.; Nielsen, T.G.; Tetrahedron Lett (TELEAY) 1968, 3375. KOHLER, E.P.; Barrett, G.R.; J Am Chem Soc (JACSAT) 1924, 46, 2105. DEMINA, L.A.; Khismutdinov, G.K.; Tkachev, S.V.; Fainzilberg, A.A.; J Org Chem USSR (Engl Transl) (JOCYA9) 1979, 15, 654. BAAVA, L.N.; Demina, L.A.; Trusova, T.V.; Furin, G.G.; Khisamutdinov,* G.K.; J Org Chem USSR (Engl Transl) (JOCYA9) 1979, 15, 2179. CARAMELLA, P.; Cellerino, G.; Houk, K.N.; Albini, F.M.; Santiago, C; J Org Chem (JOCEAH) 1978, 43, 3007. CARAMELLA, P.; Cellerino, G.; Houk, K.; Albini, F.M.; Santiago, C; J Org Chem (JOCEAH) 1978,43,3006. SAUTER, F.; Buyuk, G.; Monatsh Chem (MOCMB7) 1974, 105, 254. ELKASABY, M.A.; Salem, M.A.I.; Indian J Chm (IJOCAP) 1980, 19, 571. BAEVA, L.N.; Demina, L.A.; Trusova, T.V.; Furin, G.G.; Khisamutdinov, G.K.; J Org Chem USSR (Engl Transl) (JOCYA9) 1979, 15, 2179. MAKSOUD, A.A.; Hosnig, G.; Hassan, O.; Shafik, S.; Rev Roum Chim (RRCHAX) 1978, 23, 1541. FUKUNAGA, K.; Synthesis (SYNTBF) 1978, 55. FARAGHER, R; Gilchrist, T.L.; J Chem Soc, Perkin Trans 1 (JCPRB4) 1977, 1196. BIANCHI, G.; De Micheli, C; Gandolfi, R.; J Chem Soc, Perkin Trans 1 (JCPRB4) 1976, 1518. LO VECCHIO, G.; Atti Accad Peloritana Periocolanti, CI Sci Fis, Mat Nat (AAPFAO) 1972, 52, 207. JURD, L.; Chem Ind (London) (CHINAG) 1970, 2, 624. BELTRAME, P.L.; Cattania, M.G.; Redaelli, V.; Zecchi, G.; J Chem Soc, Perkin Trans 2 (JCPKBH) 1977, 706. PARK, C.A.; Beam, C.F.; Kaiser, E.M.; Hauser, C.R.; et al.; J Heterocyol Chem (JHTCAD) 1976, 13, 449. LO VECCHIO, G.; Atti Accad Peloritana Pericolanti, CI Sci Fis, Mat Nat (AAPFAO) 1972, 52, 217. BORKHADE, K.T.; Marathey, M.G.; Indian J Chem (IJOCAP) 1970, 8, 796. WAKEFIELD, B.J.; Wright, D.J.; J Chem Soc С (JSOOAX) 1970, 1165. UNTERHALT, В.; Pham Zentralhalle (PHZEBE) 1968, 107, 356. NIELSEN, A.T.; Archibald, T.G.; Tetrahedron Lett (TELEAY) 1968, 3375. KIRTZ, D.W.; Shechter, H.; J Chem Soc, Chem Commun (JCCCAT) 1965, 689. JOSHL K.C.; Jauhar, A.K.; J Indian Chem Soc (JICSAH) 1965, 42, 733. NIELSEN, A.T.; Archibald, T.G.; J Org Chem (JOCEAH) 1969, 34, 984. BATTAGLIA, Α.; Dondoni, Α.; Rio Sci (RISCAZ) 1968, 38, 201. MONIORTE, F.; Lo Vecchio, 80435 54 G.; Atti Accad Peloritana Periocolanti, Cl Sci Fis, Mat Nat (AAPFAO) 1966, 49,169. ARBASINO, M.; Finzi, P.V.; Rio Sci (RISCAZ) 1966, 36, 1339. ROTH, H.J.; Schwartz, M.; Arch Pharm Ber Dtsch Pharm Ges (APBDAJ) 1961, 294, 769. ROTH, H.J.; Schwarz, M.; Arch Pharm Ber Dtsch Pharm Ges (APBDAJ) 1961, 294, 761. GRUNANGER, P.; Gandini, C; Quilico, Α.; Rend - 1st Lomb Accad Sci Lett, A: Sci Mat, Fis, Chim Geol (RLMAAK) 1959, 93, 467. RUPE, H.; Schneider, F.; Chem Ber (CHBEAM) 1895, 28, 957. BARLUENGA, J.; Aznar, F.; Palomero, M.A.; Chem Eur J (CEUJED) 2001, 7 (24), 5318-5324. ASCHWANDEN, P.; Frantz, D.E.; Carreira, E.M.; Org Lett (ORLEF7) 2000, 2 (15), 2331-2333. BALASUNDARAM, В.; Veluchamy, T.P.; Velmurugan, D.; Perumal, P.T.; Indian J Chem, Sect В (IJSBDB) 1995, 34 (5), 367-371. CHAN, K.S.; Yeung, M.L.; Chan, W.; Wang, R.-J.; Мак, T.C.W.; J Org Chem (JOCEAH) 1995, 60 (6), 1741-1747. CHIACCHIO, U.; Casuscelli, F.; Liguori, Α.; Rescifina, Α.; Romeo, G.; Sindona, G.; Uccella, N.; Heterocycles (HTCYAM) 1993, 36 (3), 585-600. CHAN, K.S.; J Chem Soc, Perkin Trans 1 (JCPRB4) 1991 (10), 2602-2603. LIGUORI, Α.; Ottana, R; Romeo, G.; Sindona, G.; Uccelia, N.; Heterocycles (HTCYAM) 1988, 27, 1365. STAMM, H.; Staudie, H.; Arch Pharm (Weinheim, Ger) (ARPMAS) 1976, 309, 1014. TASZ, M.K.; Plenat, F.; Christau, H.-J.; Skowronski, R.; Phosphorus, Sulfur Silicon Relat Elem (PSSLEC) 1991, 57, 143-146. ALBEROIA, Α.; Gonzalez, A.M.; Laguna, M.A.; Pulido, F.J.; Synthesis (SYNTBF) 1982, 1067. JACOB K.C.; Jadhar, G.V.; Vakharia, M.N.; Pesticides (PSTDAN) 1972, 6, 94. CLERICI, F.; Gelmi, M.L.; Ріпі, Е.; Valle, M.; Tetrahedron [TETRAB] 2001, 57 (25), 5455-5459. JURD, L.; Chem Ind (London) [CHINAG] 1970, 2, 624. JURD, L.; Tetrahedron [TETRAB] 1975, 31, 2884]. Посібник із синтезу піразолів можна знайти в [J. Elguero у збірнику Comprehensive Heterocyclic Chemistry II, (Загальна гетероциклічна хімія II) A.R. Katritzky, C.W. Reees, E.F.V. Scriven., Eds.; Pergamon Press, Oxford, 1996; Vol. 3, p.l.]. Посібник із синтезу сполук, описаних на Фіг.8А і 8В, можна знайти в наступних роботах: [LHOTAK, P.; Kurfuerst, Α.; Collect Czech Chem Commun [CCCCAK] 1993, 58 (11), 2720-2728. BRAIN, СТ.; Paul, J.M.; Synlett [SYNLES] 1999, (10), 1642-1644. VARMA, R.S.; Kumar, D.; J Heterocycl Chem [JHTCAD] 1998, 35 (6), 1533-1534. FEDYUNYAEVA, I.A.; Yushko, E.G.; Bondarenko, V.E.; Khim Geterotsikl Soedin [KGSSAQ] 1996 (3), 333-337. DOROSHENKO, A.O.; Patsenker, L.D.; Baumer, V.N.; Chepeleva, L.V.; Vankevich, A.V.; Shilo, O.P.; Yarmolenko, S.N.; Shershukov, V.M.; Mitina, V.G.; Ponomarev, O.A.; Zh Obshch Khim [ZOKHA4] 1994, 64 (4), 646-652. FEDYUNYAEVA, I.A.; Shershukov, V.M.; Khim Geterotsikl Soedin [KGSSAQ] 1993 (2), 234-237. KLEIN, R.F.X.; Horak, V.; Baker, G.A.S.; Collect Czech Chem Commun [CCCCAK] 1993, 58 (7), 1631-1635. KERR, V.N.; Hayes, F.N.; Ott, D.G.; Lier, R; Hansbury, E., J Org Chem (JOCEAH] 1959, 24, 1864. NISHIO, Т.; Ori, M.; Helv Chim Acta [HCACAV] 2001, 84 (8), 2347-2354. LHOTAK, P.; Kurfuerst, Α.; Collect Czech Chem Commun [CCCCAK] 1993, 58 (11), 2720-2728. SIEGREST, 55 A.E.; Helv Chim Acta [HCACAV] 1967, 50, 906; і GABRIEL, S.; Chem Ber [CHBEAM] 1910,43,134]. Посібник із синтезу сполук, описаних на Фіг.9А і 9В можна знайти в наступних роботах [ZHANG, P.-F.; Chen, Z.-C; Synthesis (SYNTBF) 2001, (14), 2075-2077. BUTLER, R.N.; Cloonan, M.O.; McMahon, J.M.; Burke, L.A.; J Chem Soc, Perkin Trans 1 (JCPRB4) 1999, (12), 1709-1712. NAKAWISHI, S.; Otsuji, Y.; Nantaku, J.; Chem Lett (CMLTAG) 1983, 341. POCAR, D.; Stradi, R.; Tetrahedron Lett (TELEAY) 1976, 1839. POPILIN, O.N.; Tishchenko, V.G.; Khim Geterotsikl Soedin (KGSSAQ) 1972, 1264; і KUNCKELL, F.; Chem Ber (CHBEAM) 1901, 34, 637]. Посібник із синтезу сполук, описаних на Фіг.10А і 10В, можна знайти в наступних роботах: [VARLAMOV, A.V.; Turchin, K.F.; Chernyshev, A.I.; Zubkov, F.I.; Borisova, T.N.; Chem Heterocycl Compd (NY) [CHCCAL] 2000, 36 (5), 621-622. CASUSCELLI, F.; Chiacchio, U.; Rescifina, Α.; Romeo, R.; Romeo, G.; Tommasini, S.; Uccella, N.; Tetrahedron (TETRAB) 1995, 51 (10), 2979-2990. CHIACCHIO, U.; Casuscelli, F.; Corsaro, Α.; Rescifina, Α.; Romeo, G.; Uccella, N.; Tetrahedron (TETRAB) 1994, 50 (22), 6671-6680. MUKAI, C; Kim, I.J.; Cho, W.J.; Kido, M.; Hanaoka, M.; J Chem Soc, Perkin Trans 1 (JCPRB4) 1993 (20), 2495-2503. MINAMI, Т.; Isonaka, Т.; Okada, Y.; Ichikawa, J.; J Org Chem (JOCEAH) 1993, 58 (25), 7009-7015. TANAKA, К.; Mori, Τ; Mitsuhashi, К.; Bull Chem Soc Jpn (BCSJA8) 1993, 66 (1), 263-268. HUISGEN, R; et al.; Tetrahedron Lett (TELEAY) I960, 12, 5. CHEM BER (CHBEAM) 1968, 101, 2043. CHEM BER (CHBEAM) 1968, 101, 2568. CHEM BER (CHBEAM) 1969, 102, 117. SASAKI, Т.; Bull Soc Chim Fr (BSCFAS) 1968, 41, 2960; і SASAKI, Т.; Bull Chem Soc Jpn (BCSJA8) 1968,41,2964. Посібник із синтезу сполук, описаних на Фіг.ПА і 11В, можна знайти в наступних роботах: [KATRIZKY, A.R.; Qi, Μ.; Feng, D.; Zhang, G.; Griffith, M.C.; Watson, K.; Org Lett (ORLEF7) 1999, 1 (8), 1189-1191. FRANCIS, J.E.; Cash, W.D.; Barbaz, B.S.; Bernard, P.S.; Lovell, R.A.; Mazzenga, G.C.; Friedmann, R.C.; Hyun, J.L.; Braunwalder, A.F.; Loo, P.S.; Bennett, D.A.; J Med Chem (JMCMAR) 1991, 34 (1), 281-290. POTTS, K.T.; J Chem Soc (JCSOA9) 1954, 3461. EINHORN, Α.; Justus Liebigs Ann Chem (JLACBF) 1905, 343, 207. SHIBA, S.A.; El-Khamry, A.A.; Shaban, M.E.; Atia, K.S.; Pharmazie (PHARAT) 1997, 52 (3), 189-194; і MOLINA, P.; Tarranga, Α.; Espinosa, Α.; Lidon, M.J.; Synthesis (SYNTBF) 1987 (2), 128]. Посібник із синтезу сполук, описаних на Фіг.12А і 12В, можна знайти в наступних роботах: [ASCHWANDEN, P.; Frantz, D.E.; Carreira, E.M.; Org Lett (ORLEF7) 2000, 2 (15), 2331-2333. BALASUNDARAM, В.; Veluchamy, T.P.; Velmurugan, D.; Perumal, P.T.; Indian J Chem, Sect В (IJSBDB) 1995, 34 (5), 367-371. CHAN, K.S.; Yeung, M.L.; Chan, W.; Wang, R.-J.; Mak, T.C.W.; J Org Chem (JOCEAH) 1995, 60 (6), 1741-1747. ALBEROLA, Α.; Gonzalez, A.M.; Laguna, M.A.; Pulido, F.J.; Synthesis (SYNTBF) 1982, 1067; і JACOB, K.C.; Jadhar, G.V.; Vakharia, M.N.; Pesticides (PSTDAN) 1972, 6, 94]. 80435 56 Наступні сполуки є характерними прикладами винаходу. Сполуки, ідентифіковані нижче, одержували методами, приведеними в описі винаходу. Способи визначення точки плавлення Точку плавлення визначали на електротермічному цифровому приладі ІА9100 для визначення точок плавлення. Усі точки плавлення не відкореговані. Елементний аналіз Елементний аналіз виконаний аналітиками Desert Analytics, Tucson, AZ. Методи 1H ЯМР Спектри 1Н ЯМР знімали на приладі Varian Mercury system при 300мгц. Методи ЖХ-МС Загальний метод ЖХ-МС виконували на приладі Waters Micromass ZQ з іонізацією при електророзпорошенні. Частина, яка відноситься до ВЄЖХ, являла собою ділильний модуль Waters Model 2690 у поєднанні з фотодіодним детектором Waters Model 996. Метод W У даному методі використаний стовпчик зі зверненою фазою 2,1x250мм 5мКм С-18 Altima (Alltech) зі швидкістю потоку 0,25мол/хв і градієнтом 5-85% ацетонітрилу у воді, що містить 0,1% трифтороцтової кислоти, протягом 36 хв. Потім градієнт змінюється до 100% ацетонітрила протягом 0,5 хв і залишається при 100% ацетонітрилі протягом 3,5хв. Метод X У даному методі використаний стовпчик зі зверненою фазою 2,1x250мм 5мКм С-18 Altima (Alltech) зі швидкістю потоку 0,25мол/хв і градієнтом 5-85% ацетонітрила у воді, що містить 0,1% трифтороцтової кислоти, протягом 15хв. Потім градієнт змінюється до 100% ацетонітрила протягом 0,5хв і залишається при 100% ацетонітрилі протягом 25хв. Метод Υ У даному методі використаний стовпчик зі зверненою фазою 2,1x150мм Agilent Zorbax 5мКм С-18 зі швидкістю потоку 0,3мол/хв і градієнтом 10100% ацетонітрила у воді, що містить 0,1% трифтороцтової кислоти протягом 16хв., і далі підтримується протягом 2хв. 100% ацетонітрила. Метод Ζ У даному методі використаний стовпчик зі зверненою фазою 2,1x5 мм Agilent Zorbax 5мКм С18 зі швидкістю потоку 0,5мол/хв і градієнтом 5100% ацетонірила у воді, що містить 0,1% трифтороцтової кислоти, протягом 8 хв., і далі підтримуючи протягом 2хв. 100% ацетонітрила. Сполука 1. (R909850) 2,2-дихлор-N-[2-[3-(2хлор-6-фторфеніл)-5-ізоксазоліл]-(4піридил)]ацетамід Молекулярна маса=401 підтверджена ЖХ-МС, tT- 32,63 хв. (Метод W) МН+=399-403 Сполука 3. (R909794) 2,2-дихлор-N-[3-(2-фтор6-трифторметилфеніл)-5-ізоксазоліл]-(4піридил)]ацетамід Молекулярна маса=434 підтверджена ЖХ-МС, tr= 34,01 хв. (Метод W) МН+=432-436 57 Сполука 5. (R911427) 2,2-дихлор-N-[3-(2-фтор6-метоксифеніл)-5-ізоксазоліл]-(4піридил)]ацетамід Молекулярна маса=396 підтверджена ЖХ-МС, tr= 31,28 хв. (Метод W) МН+=394-398 Сполука 7. (R911418) 2,2-дихлор-N-[5-[3-(2,6дихлорфеніл)-5-ізоксазоліл]-(3-піридил)]ацетамід Молекулярна маса=417 підтверджена ЖХ-МС, tr= 33,10 хв. (Метод W) МНМ15-419 Сполука 9. (R909921) 2,2-дихлор-N-[2-[3-(2,6дихлорфеніл)-5-ізоксазоліл]-(4-піридил)]ацетамід Молекулярна маса=417 підтверджена ЖХ-МС, tr= 34,25 хв. (Метод W) МН+=415-419 т.пл. 187-188 °С Сполука 11. (R909833) 2,2-дихлор-N-[3-[3-[(2,6дихлор)-4-тридил]-5-ізоксазоліл]феніл]ацетамід Молекулярна маса=417 підтверджена ЖХ-МС, tr= 34,13 хв. (Метод W) М£Ґ=415-419 Сполука 13. (R909845) 2,2-дихлор-N-[5-[3-(2хлор-6-фторфеніл)-5-ізоксазоліл]-(3піридил)]ацетамід Молекулярна маса=401 підтверджена ЖХ-МС, tr= 32,55 хв. (Метод W) МН+=399-403 Сполука 17. (R911424) 2,2-дихлор-N-[5-[3-(2фтор-6-метоксифенш)-5-ізоксазоліл] -(3 -піридил)] ацетамід Молекулярна маса=396 підтверджена ЖХ-МС, tr= 30,47 хв. (Метод W) МН+=394-398 Сполука 19. (R909851) 2,2-дихлор-N-[2-[3-(2,6диметилфеніл)-5-ізоксазоліл]-(4-піридил)]ацетамід Молекулярна маса=376 підтверджена ЖХ-МС, tr= 34,63 хв. (Метод W) МН+=374-378 Сполука 21. (R909846) 2,2-дихлор-N-[5-[3-(2,6диметилфеніл)-5-ізоксазоліл]-(3-піридил)]ацетамід Молекулярна маса=376 підтверджена ЖХ-МС, tr= 29,69 хв. (Метод W) МН+=374-378 Сполука 27. (R911422) 2(2-дихлор-N-[5-[3-(2,6дифторфеніл)-5-ізоксазоліл]-(3-піридил)]ацетамід Молекулярна маса=384 підтверджена ЖХ-МС, tr= 31,64 хв. (Метод W) МЬҐ=382-386 Сполука 29. (R911423) 2,2-дихлор-N-[5-[3-(2,3дихлорфеніл)-5-ізоксазоліл]-(3-піридил)]ацетамід Молекулярна маса=417 підтверджена ЖХ-МС, tr= 34,99 хв. (Метод W) МН+=415-419 Сполука 31. (R909864) 2,2-дихлор-N-[3-(2морфоліно-6-трифтормети лфеніл)-5-ізоксазоліл](4-піридил)] ацетамід Молекулярна маса=501 підтверджена ЖХ-МС, tr= 6,97 хв. (Метод Z) МН+=499-503 Сполука 33. (R904855) 2,2-дихлор-N-[3-[3-(3метил-2-піридил)-5-ізоксазоліл]феніл]ацетамід Молекулярна маса=362 підтверджена ЖХ-МС, tr= 30,89 хв. (Метод W) МН+=360-364 Сполука 35. (R904800) 2,2-дихлор-N-[6-[3-(2,6дихлорфеніл)-5-ізоксазоліл]-(2-піридил)]ацетамід Молекулярна маса=417 підтверджена ЖХ-МС, tr= 20,74 хв. (Метод X) МН+=415-419 Сполука 37. (R909793) 2,2-дихлор-N-[5-[3-(2фтор-6-трифторметилфеніл)-5-ізоксазоліл]-(3піридил)]ацетамід Молекулярна маса=434 підтверджена ЖХ-МС, tr= 32,79 хв. (Метод W) МН+=432-436 Сполука 43. (R909873) 2,2-дихлор-N-[2-[3-(2,6дихлорфеніл)-5-ізоксазоліл]-[4-(1оксипіридил)]ацетамід 80435 58 Молекулярна маса=433 підтверджена ЖХ-МС, tr= 6,44 хв. (Метод Z) МН+=431-435 Сполука 45. (R909878) 2,2-дихлор-N-[3-[(3етоксикарбоніл)-2-піридил]-5ізоксазоліл]феніл]ацетамід Молекулярна маса=420 підтверджена ЖХ-МС, tr= 6,65 хв. (Метод Z) МН+=418-422 Сполука 47. (R909884) 2,2-дихлор-N-[3-(2фтор-6-морфолі носул ьфамоі л фені л)-5 ізоксазоліл]-(4-піридил)]ацетамід Молекулярна маса=515 підтверджена ЖХ-МС, tr= 6,32 хв. (Метод Z) МН+=513-517 Сполука 49. (R905952) 2,2-дихлор-N-[3-(2метокси-6-трифторметилфеніл)-5-ізоксазоліл]-(4піридил)]ацетамід Молекулярна маса=446 підтверджена ЖХ-МС, tr= 14,41 хв. (Метод Y) МН+=444-448 Сполука 51. (R909909) 2,2-дихлор-N-[2-[3-(2,6дихлорфеніл)-5-ізоксазоліл]-(4-піридил)]-Мметилацетамід Молекулярна маса=431 підтверджена ЖХ-МС, tr= 14,99 хв. (Метод Y) МН+=429-433 Сполука 53. (R905954) 2,2-дихлор-N-[2-[3-[2хлор-6-[4-(N-2-піридил)піперазино]феніл])-5ізоксазоліл]-(4-піридил)]ацетамід Молекулярна маса=544 підтверджена ЖХ-МС, tr= 11,81 хв. (Метод Y) МН+=542-546 Сполука 57. (R905948) 2,2-дихлор-N-[5-[3-(2метокси-6-трифторметилфеніл)-5-ізоксазоліл]-(3піридил)]ацетамід Молекулярна маса=446 підтверджена ЖХ-МС, tr= 13,45 хв. (Метод Y) МН+=444-448 Сполука 61. (R905961) 2,2-дихлор-N-[5-[3-[2хлор-6-[4-(N-ацетил)піперазино]феніл])-5ізоксазоліл]-(3-піридил)]ацетамід Молекулярна маса=509 підтверджена ЖХ-МС, tr= 12,11 хв. (Метод Y) МН+=507-511 Сполука 63. (R905962) 2,2-дихлор-N-[5-[3-[2хлор-6-[4-(N-етил)піперазино]феніл])-5ізоксазоліл]-(3-піридил)]ацетамід Молекулярна маса=495 підтверджена ЖХ-МС, tr= 9,48 хв. (Метод Y) МН+=493-497 Сполука 65. (R904857) 2,2-дихлор-N-[3-(2,6дихлорфеніл)-5-ізоксазоліл]-(2-піридил)]ацетамід Молекулярна маса=417 підтверджена ЖХ-МС, tr= 35,19 хв. (Метод W) МН+=415-419 Сполука 67. (R905451) 2,2-дихлор-N-[5-[3-(2трифторметилфеніл)-5-ізоксазоліл]-(3піридил)]ацетамід Молекулярна маса=416 підтверджена ЖХ-МС, tr= 13,81 хв. (Метод Y) МН+=414-418 Сполука 69. (R905949) 2,2-дихлор-N-[5-[3-[2хлор-6-[4-(N-2-піридил)піперазино]феніл])-5ізоксазоліл]-(3-піридил)]ацетамід Молекулярна маса=544 підтверджена ЖХ-МС, tr= 11,29 хв. (Метод Y) МН+=542-546 Сполука 71. (R905965) 2,2-дихлор-N-[5-[3-[2хлор-6-[4-(N-третбутоксикарбоніл)піперазино]феніл])-5-ізоксазоліл](3-піридил)]ацетамід Молекулярна маса=567 підтверджена ЖХ-МС, tr= 15,91 хв. (Метод Y) МН+=565-569 Сполука 73. (R905966) 2,2-дихлор-N-[5-[3-(2хлор-6-піперазинофеніл)-5-ізоксазоліл]-(3піридил)]ацетамід 59 Молекулярна маса=467 підтверджена ЖХ-МС, tr= 9,51 хв. (Метод Y) МН+=465-469 Сполука 75. (R905967) 2,2-дихлор-N-[5-[3-(2хлор-6-трет-бутилдиметилсилілоксифеніл)-5ізоксазоліл]-(3-піридил)]ацетамід Молекулярна маса=513 підтверджена ЖХ-МС, tr= 17,49 хв. (Метод Y) МН+=511-515 Сполука 77. (R905968) 2,2-дихлор-N-[5-[3-(2хлор-6-пдроксифешл)-5-ізоксазоліл]-(3піридил)]ацетамід Молекулярна маса=399 підтверджена ЖХ-МС, tr= 12,51 хв. (Метод Y) МН+=397-401 Сполука 79. (R905969) 2,2-дихлор-N-[5-[3-(2хлор-6-N-етилкарбамоілоксифеніл)-5-ізоксазоліл](3-піридил)]ацетамід Молекулярна маса=470 підтверджена ЖХ-МС, tr= 12,85 хв. (Метод Y) МН+=468-472 Сполука 81. (R905970) 2,2-дихлор-N-[5-[3-[2хлор-6-[4-(N-етилкарбоксамідо)піперазино]феніл])5-ізоксазоліл]-(3-піридил)]ацетамід Молекулярна маса=538 підтверджена ЖХ-МС, tr= 12,77 хв. (Метод Y) МН+=536-540 Сполука 83. (R905971) 2,2-дихлор-N-[2-[3-(2хлор-6-трет-бутилдиметилсилілоксифеніл)-5ізоксазоліл]-(4-піридил)]ацетамід Молекулярна маса=513 підтверджена ЖХ-МС, tr= 17,96 хв. (Метод Y) МН+=511-515 Сполука 85. (R905973) 2,2-дихлор-N-[2-[3-(2хлор-6-N-пропілкарбамоілоксифеніл)-5ізоксазоліл]-(4-піридил)]ацетамід Молекулярна маса=484 підтверджена ЖХ-МС, tr= 13,36 хв. (Метод Y) МН+=482-486 Сполука 87. (R905982) 2,2-дихлор-N-[2-[3-(2хлор-6-метоксиметоксифеніл)-5-ізоксазоліл]-(4піридил)]ацетамід Молекулярна маса=443 підтверджена ЖХ-МС, tr= 14,65 хв. (Метод Y) МН+=441-445 Сполука 89. (R905983) 2,2-дихлор-N-[2-[3-(2хлор-6-пдроксифеніл)-5-ізоксазоліл]-(4піридил)]ацетамід Молекулярна маса=399 підтверджена ЖХ-МС, tr= 13,53 хв. (Метод Y) МН+=397-401 Сполука 91. (R905984) 2,2-дихлор-N-[3-[3-[(4хлор-2-диметиламіно)-3-піридил]-5ізоксазоліл]феніл]ацетамід Молекулярна маса=426 підтверджена ЖХ-МС, tr= 13,33 хв. (Метод Y) МН+=424-428 Сполука 93. (R905985) 2,2-дихлор-N-[3-[3-[(2,4дихлор)-3-піридил]-5-ізоксазоліл]феніл]ацетамід Молекулярна маса=417 підтверджена ЖХ-МС, tr= 15,37 хв. (Метод Y) МН+=415-419 Сполука 95. (R905987) 2,2-дихлор-Ы-[3-[3-[(2хлор-4-морфоліно)-3-піридил]-5ізоксазоліл]феніл]ацетамід Молекулярна маса=468 підтверджена ЖХ-МС, tr= 13,73 хв. (Метод Y) МН+=466-470 Сполука 97. (R909874) 2,2-дихлор-М-[3-[3-[(6бром)-2-піридил]-5-ізоксазоліл]-(4піридил)]ацетамід Молекулярна маса=427 підтверджена ЖХ-МС, tr= 36,03 хв. (Метод W) МН+=425-429 (R904871) 2,2-дихлор-М-[2-[3-(2,6дихлорфеніл)-5-ізоксазоліл]-(4-піридил)]ацетамід Гідросhloride Salt 80435 60 Молекулярна маса=453 т.пл. 240-241°С Елементний аналіз: обчислений для C16Н10Сl5N2О2: С, 42,37; Н, 2,22; СІ, 39,09; N, 9,27; знайдено: С, 42,51; Н, 2,18; СІ, 39,06; N, 9,05 (R909919) Толуолсульфонат 2,2-дихлор-N-[2[3-(2,6-дихлорфеніл)-5-ізоксазоліл]-(4піридил)]ацетаміда Молекулярна маса=589 т.пл. 246-247°С Елементний аналіз: обчислений для C23Н17Сl4N3О5S: С, 46,88; Н, 2,91; N, 7,13; S, 5,44; знайдено: С, 47,05; Н, 3,06; N, 7,00; S, 5,30 (R909920) Етансульфонат 2,2-дихлор-N-[2-[3(2,6-дихлорфеніл)-5-ізоксазоліл]-(4піридил)]ацетаміда Молекулярна маса=527 т.пл. 210-211°С Елементний аналіз: обчислений для C18Н15Сl4N3О5S: С, 41,01; Н, 2,87; N, 7,97; S, 6,08; знайдено: С, 41,00; Н, 2,77; N, 7,72; S, 5,80 (R909923) Мононітрат 2,2-дихлор-N-[3-(2,6дихлорфеніл)-5-ізоксазоліл]-(4-піридил)]ацетаміда Молекулярна маса=480 т.пл. 175-176°С Елементний аналіз: обчислений для C16Н10Сl4N4О5: С, 40,03; Н, 2,10; N, 11,67; знайдено: С, 40,33; Н, 1,94; N, 11,25 Далі приведені додаткові експериментальні дані для синтезу деяких сполук винаходу. Спосіб F (См. Фіг.15) Стадія 1. Ацетиленові реакції перехресного сполучення Відповідним чином заміщений обромнітробензол чи заміщений о-иоднітробензол розчиняли в придатному розчиннику, такому як идіоксан чи ТГФ, і потім обробляли, щонайменше, п'ятьмамолярними еквівалентами придатного аміну, яким може бути триетиламін, диетиламін чи диізопропілентіламін. Чи ж, як розчинник використовували безпосередньо амін. Через розчин протягом декількох хвилин пропускали струм аргону, після чого додавали дихлорбіс(трифенілфосфін)палладій (II) (3-4мол.%), Сu (6-8мол.%) і, нарешті, триметилсилілацетилен (1,2-1,5молярних еквівалентів). Потім реакційну суміш нагрівали при температурі 50-80°С до завершення реакції, контролюючи методами ТСХ чи ЖХ-МС. При використанні більш реакційно здатних заміщених о-иоднітробензолів реакцію ацетиленового перехресного з'єднання можна проводити при кімнатній температурі. У випадку повільної реакції додавали додаткову кількість триметилсилілацетилену. Ця загальна методика відома в літературі як з'єднання Соногашира [К. Sonogashira et.al., TeTpahedron Lett., 1975, 4467]. Потім реакційну масу розбавляли етилацетатом, і отриманий розчин кілька разів промивали сольовим розчином. Чи ж, технічну реакційну масу фільтрували через шар целіту, розбавляли етилацетатом і промивали сольовим розчином. Отриманий у такий спосіб органічний шар сушили над сульфатом натрію, фільтрували і концентрували до повного висихання при зниженому тиску. Залишок очищали колоночною хроматографією на силіка
ДивитисяДодаткова інформація
Назва патенту англійськоюPyridyl substituted heterocycles useful for treating or preventing hcv infection.
Автори англійськоюSingh Rajinder, Goff Dane, Partridge John, Henry Lu
Назва патенту російськоюПиридилзамещенные гетероциклические соединения, которые применяют для лечения или предотвращения инфекции вируса гепатита c
Автори російськоюСинг Реджиндер, Гофф Дейн, Партридж Джон, Генри Лу
МПК / Мітки
МПК: C07D 417/14, A61P 31/12, C07D 401/14, C07D 417/04, C07D 413/04, C07D 401/04, C07D 413/14
Мітки: лікування, піридилзаміщені, гетероциклічні, запобігання, інфекції, вірусу, гепатиту, застосовують, сполуки
Код посилання
<a href="https://ua.patents.su/65-80435-piridilzamishheni-geterociklichni-spoluki-shho-zastosovuyut-dlya-likuvannya-abo-zapobigannya-infekci-virusu-gepatitu-c.html" target="_blank" rel="follow" title="База патентів України">Піридилзаміщені гетероциклічні сполуки, що застосовують для лікування або запобігання інфекції вірусу гепатиту c</a>
Попередній патент: Сівалка
Наступний патент: Спосіб експлуатації системи розподілу газу для населеного пункту
Випадковий патент: Віброекструдер для змішування і формування фібробетонних виробів круглого поперечного перерізу