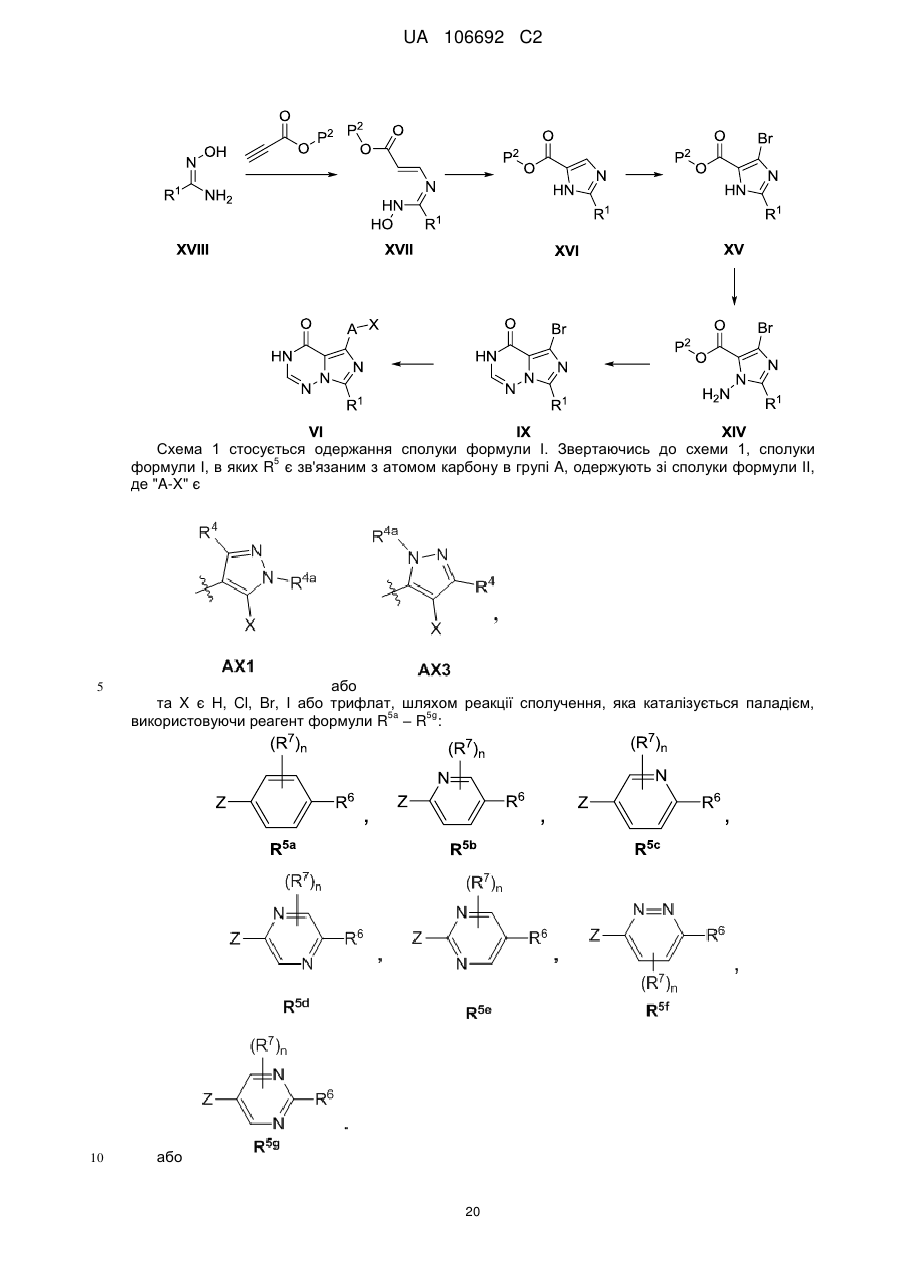
Імідазо[5,1-f][1,2,4]триазини для лікування неврологічних розладів
Номер патенту: 106692
Опубліковано: 25.09.2014
Автори: Вергоест Патрік Роберт, Янґ Едді, Чаппі Томас Аллен, Умфрей Джон Майкл, Гелал Крістофер Джон
Формула / Реферат
1. Сполука формули
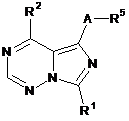 (I)
(I)
або її фармацевтично прийнятна сіль, де:
"-A-R5" є:
 ,
,
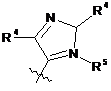 ,
,
або 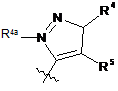 ;
;
A1R5
A2R5
A3R5
R1 є незалежно вибраним з групи, що складається з гідрогену, (С1-С6)алкілу, (С2-С6)алкенілу, (С2-С6)алкінілу, (С3-С15)циклоалкілу, -(С1-С6)алкіл-ОН, -(С1-С6)алкіл-СN, -SF5, -CF3, -CHF2 та -CH2F;
R2 є незалежно вибраним з групи, що складається з -(С1-С6)алкіл-R9, -NHR3, -N(R3)2, -O-(C1-C6)алкіл-R9, -OR8, (С3-С15)циклоалкілу, (С6-С10)арилу, 3-14-членного гетероциклілу та 5-14-членного гетероарилу; де згаданий (С3-С15)циклоалкіл та 3-14-членний гетероцикліл необов'язково може містити один подвійний або потрійний зв'язок та одну-дві оксогрупи (O=); та де згадані -(С1-С6)алкілR9, -NHR3,-N(R3)2, -O-(С1-С6)алкіл-R9, -OR8, (С3-С15)циклоалкільний, (С6-С10)арильний, 3-14-членний гетероциклічний або 5-14-членний гетероарильний фрагменти необов'язково можуть бути заміщеними одним-трьома замісниками, незалежно вибраними з групи, що складається з (С1-С6)алкілу, (С1-С6)алкокси, галогену та -CF3;
кожен R3 незалежно є вибраним з групи, що складається з -(С1-С6)алкіл-R9, -(C2-C6)алкеніл-R9, -(C2-C6)алкініл-R9 та -(С3-С15)циклоалкілR9, або, коли R2 є -N(R3)2, обидва зі згаданих R3 можуть бути взяті разом з атомом нітрогену, до якого вони приєднані, утворюючи 4-6-членне гетероциклічне кільце, яке необов'язково містить одну-дві оксогрупи (O=) та необов'язково заміщене одним-трьома замісниками, незалежно вибраними з групи, що складається з гідрогену, флуору, -CN, -CF3, -CHF2, -CH2F, -OH, -О-(С1-С6)алкілу, NH2, -NН-(С1-С6)алкілу, -N[(С1-С6)алкіл]2, (С1-С6)алкілу, (С2-С6)алкенілу, (С2-С6)алкінілу, -(C=O)-R8, -(C=O)-OR8, -(C=O)-N(R8)2, -O-(C=O)-R8, -OR8, -O-(C=O)-OR8, -SR8, -S(O)R8, -S(O)2R8, -S(O)2N(R8)2, -NH-(C=O)-R8, -NH-(C=O)-OR8, -O-(C=O)-N(R8)2, -NH-(C=O)-N(R8)2, -N[(С1-С6)алкіл](C=O)-R8, -N[(С1-С6)алкіл](C=O)-OR8, -N[(C1-C6)алкіл](C=O)-N(R8)2, (C3-С15)циклоалкілу, (С6-С10)арилу, 3-14-членного гетероциклілу та 5-14-членного гетероарилу; де згаданий (С3-С15)циклоалкіл та 3-14-членний гетероцикліл необов'язково може містити один подвійний або потрійний зв'язок та одну-дві оксогрупи (O=);
кожен R4 є незалежно вибраним з групи, що складається з гідрогену, галогену, (С1-С6)алкілу, (С2-С6)алкенілу, (С2-С6)алкінілу, -CF3, -CHF2, -CH2F та (С3-С15)циклоалкілу;
кожен R4a є незалежно вибраним з групи, що складається з гідрогену, (С1-С6)алкілу, (С3-С4)алкенілу, (С3-С4)алкінілу, -CF3, -CHF2, -CH2F та (С3-С15)циклоалкілу;
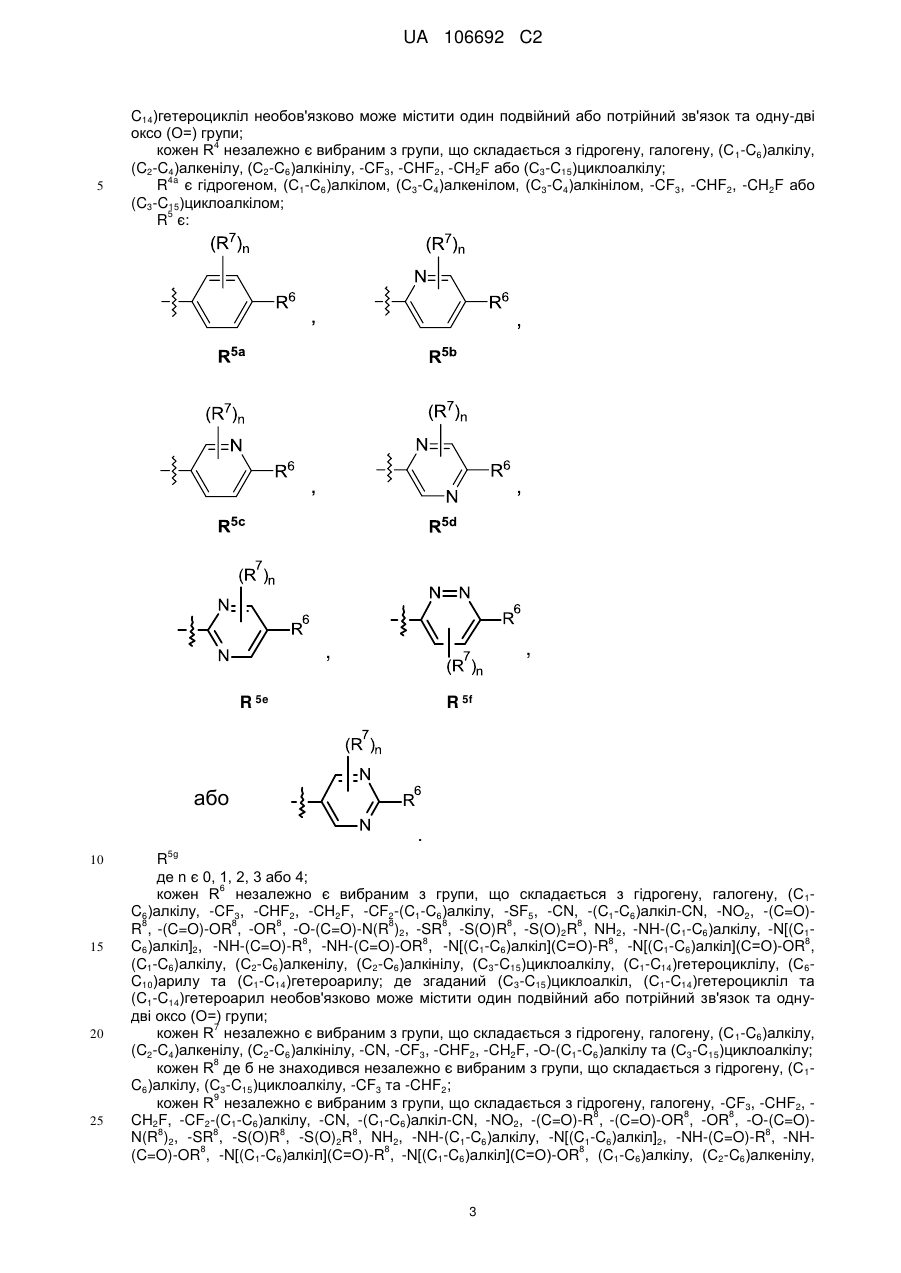
R5 є:
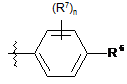 ,
,
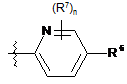 ,
,
R5a
R5b
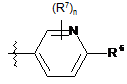 ,
,
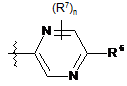 ,
,
R5c
R5d
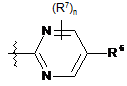 ,
,
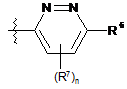
R5e
R5f
або 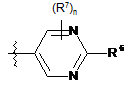 ,
,
R5g
де n є 0, 1, 2, 3 або 4;
кожен R6 є незалежно вибраним з групи, що складається з гідрогену, галогену, (С1-С6)алкілу, -CF3, -CHF2, -CH2F, -CF2-(С1-С6)алкілу, -SF5, -CN, -(С1-С6)алкіл-СN, -NO2, -(C=O)-R8, -(C=O)-OR8, -OR8, -O-(C=O)-N(R8)2, -SR8, -S(O)R8, -S(O)2R8, NH2, -NH-(С1-С6)алкілу, -N[(С1-С6)алкіл]2, -NH-(C=O)-R8, -NH-(C=O)-OR8, -N[(С1-С6)алкіл](С=О)R8, -N[(С1-С6)алкіл](C=O)-OR8, (С1-С6)алкілу, (С2-С6)алкенілу, (С2-С6)алкінілу, (С3-С15)циклоалкілу, 3-14-членного гетероциклілу, (С6-С10)арилу та 5-14-членного гетероарилу; де згаданий (С3-С15)циклоалкіл та 3-14-членний гетероцикліл необов'язково може містити один подвійний або потрійний зв'язок та одну-дві оксогрупи (O=);
кожен R7 є незалежно вибраним з групи, що складається з гідрогену, галогену, (С1-С6)алкілу, (С2-С4)алкенілу, (С2-С6)алкінілу, -CN, -CF3, -CHF2, -CH2F, -О-(С1-С6)алкілу та (С3-С15)циклоалкілу;
кожен R8 скрізь, де зустрічається, є незалежно вибраним з групи, що складається з гідрогену, (С1-С6)алкілу, (С3-С15)циклоалкілу, -CF3 та -CHF2;
кожен R9 є незалежно вибраним з групи, що складається з гідрогену, галогену, -CF3, -CHF2, -CH2F, -СF2-(С1-С6)алкілу, -CN, -(С1-С6)алкілу-СN, -NO2, -(C=O)-R8, -(C=O)-OR8, -OR8, -O-(C=O)-N(R8)2, -SR8, -S(O)R8, -S(O)2R8, NH2, -NН-(С1-С6)алкілу, -N[(С1-С6)алкіл]2, -NH-(C=O)-R8, -NH-(C=O)-OR8, -N[(С1-С6)алкіл](C=O)-R8, -N[(С1-С6)алкіл](С=О)-OR8, (С1-С6)алкілу, (С2-С6)алкенілу, (С2-С6)алкінілу, (С3-С15)циклоалкілу, 3-14-членного гетероциклілу, (С6-С10)арилу та 5-14-членного гетероарилу, де згаданий (С3-С15)циклоалкіл та 3-14-членний гетероцикліл необов'язково може містити один подвійний або потрійний зв'язок та одну-дві оксогрупи (O=); та кожен зі згаданих (С3-С15)циклоалкільного, 3-14-членного гетероциклічного, (С6-С10)арильного та 5-14-членного гетероарильного фрагментів необов'язково може бути заміщений одним-трьома замісниками, незалежно вибраними з (С1-С6)алкілу, (С1-С6)алкокси, галогену та -CF3.
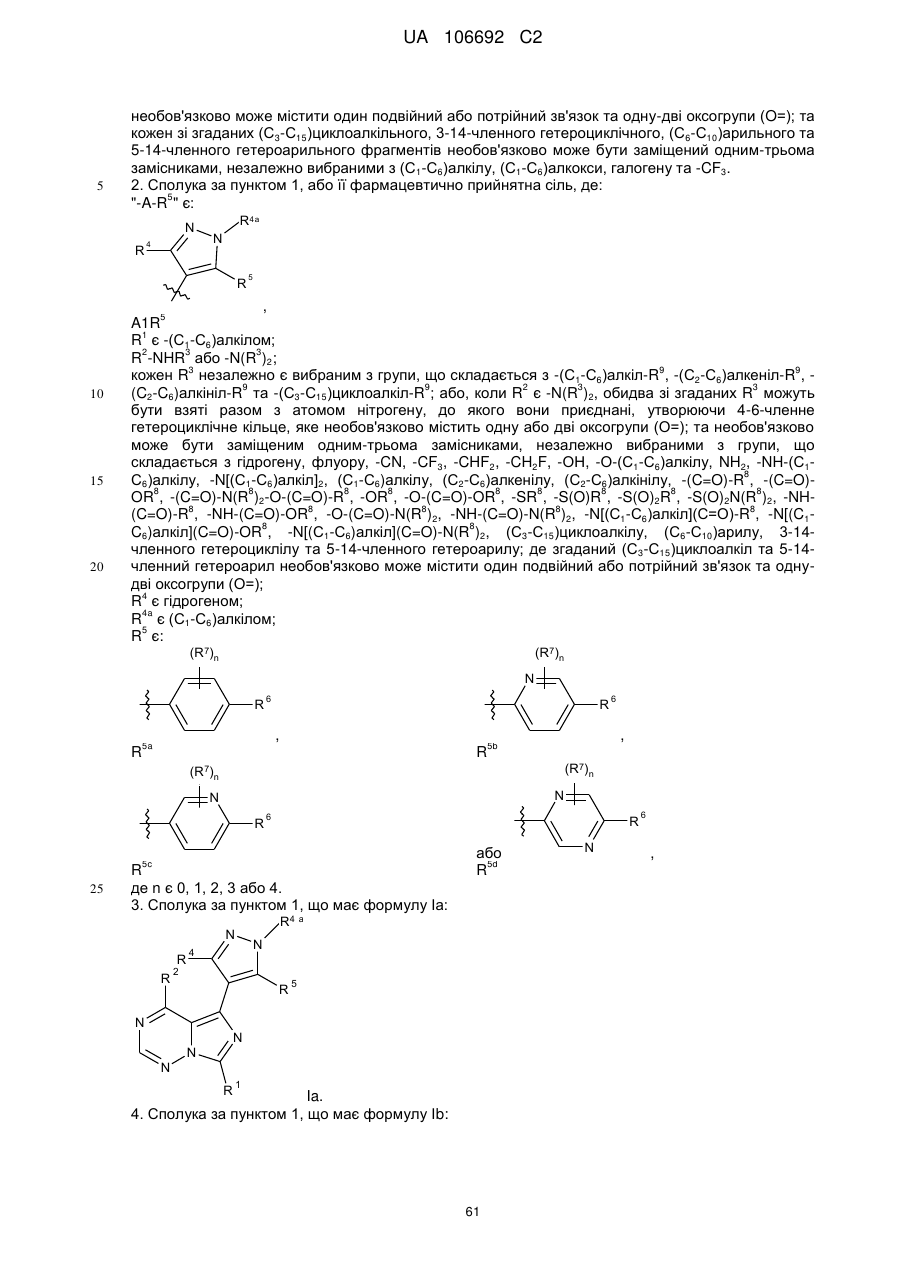
2. Сполука за пунктом 1, або її фармацевтично прийнятна сіль, де:
"-A-R5" є:
 ,
,
A1R5
R1 є -(С1-С6)алкілом;
R2-NHR3 або -N(R3)2;
кожен R3 незалежно є вибраним з групи, що складається з -(С1-С6)алкіл-R9, -(С2-С6)алкеніл-R9, -(C2-C6)алкініл-R9 та -(С3-С15)циклоалкіл-R9; або, коли R2 є -N(R3)2, обидва зі згаданих R3 можуть бути взяті разом з атомом нітрогену, до якого вони приєднані, утворюючи 4-6-членне гетероциклічне кільце, яке необов'язково містить одну або дві оксогрупи (О=); та необов'язково може бути заміщеним одним-трьома замісниками, незалежно вибраними з групи, що складається з гідрогену, флуору, -CN, -CF3, -CHF2, -CH2F, -ОН, -О-(С1-С6)алкілу, NH2, -NH-(С1-С6)алкілу, -N[(С1-С6)алкіл]2, (С1-С6)алкілу, (С2-С6)алкенілу, (С2-С6)алкінілу, -(C=O)-R8, -(C=O)-OR8, -(C=O)-N(R8)2-O-(C=O)-R8, -OR8, -O-(C=O)-OR8, -SR8, -S(O)R8, -S(O)2R8, -S(O)2N(R8)2, -NH-(C=O)-R8, -NH-(C=O)-OR8, -O-(C=O)-N(R8)2, -NH-(C=O)-N(R8)2, -N[(С1-С6)алкіл](С=О)-R8, -N[(C1-C6)алкіл](C=O)-OR8, -N[(С1-С6)алкіл](C=O)-N(R8)2, (С3-С15)циклоалкілу, (С6-С10)арилу, 3-14-членного гетероциклілу та 5-14-членного гетероарилу; де згаданий (С3-С15)циклоалкіл та 5-14-членний гетероарил необов'язково може містити один подвійний або потрійний зв'язок та одну-дві оксогрупи (O=);
R4 є гідрогеном;
R4a є (С1-С6)алкілом;
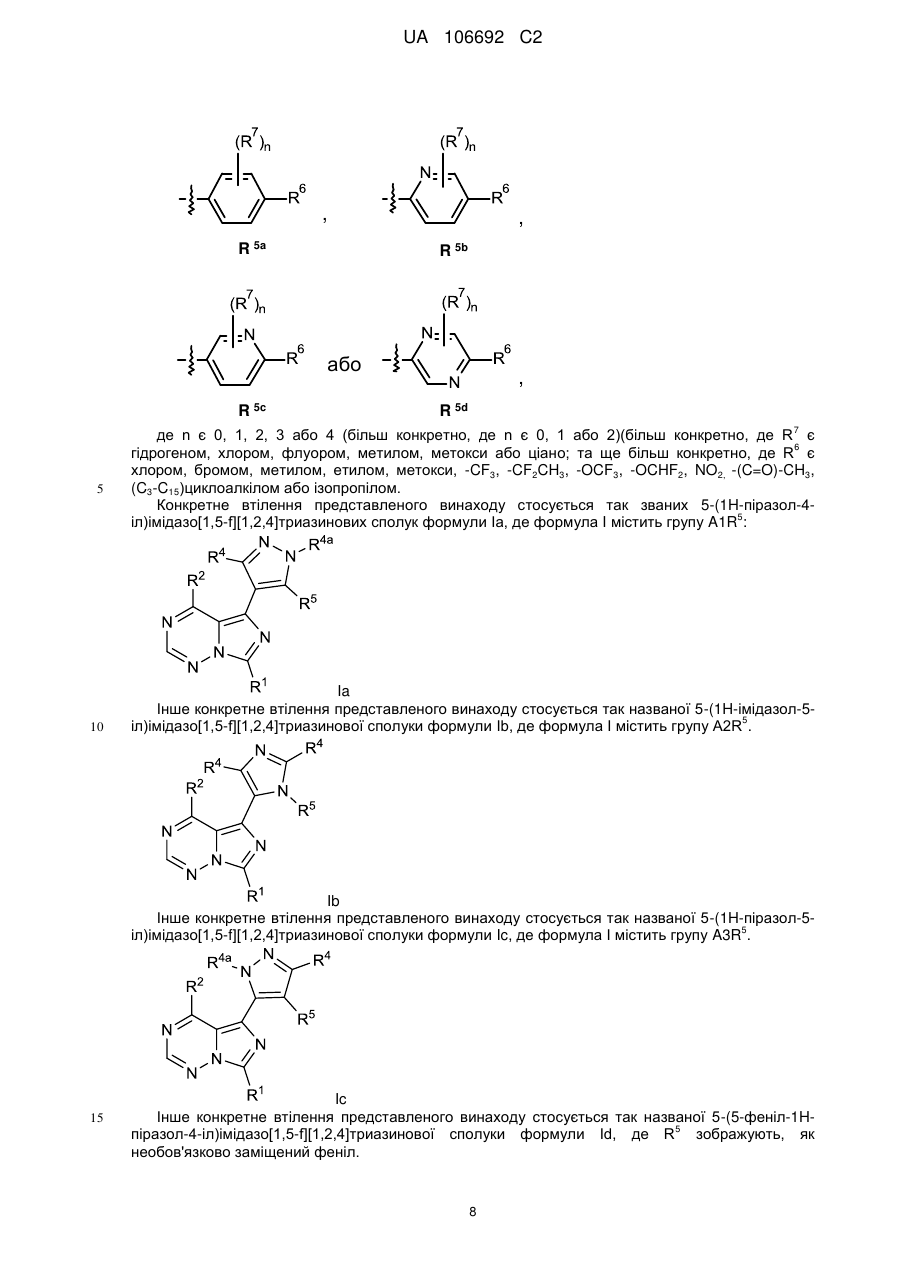
R5 є:
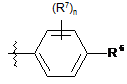 ,
,
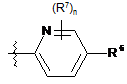 ,
,
R5a
R5b
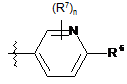
або 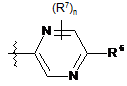 ,
,
R5c
R5d
де n є 0, 1, 2, 3 або 4.
3. Сполука за пунктом 1, що має формулу Іа:
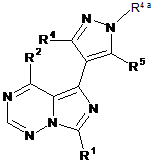 Ia.
Ia.
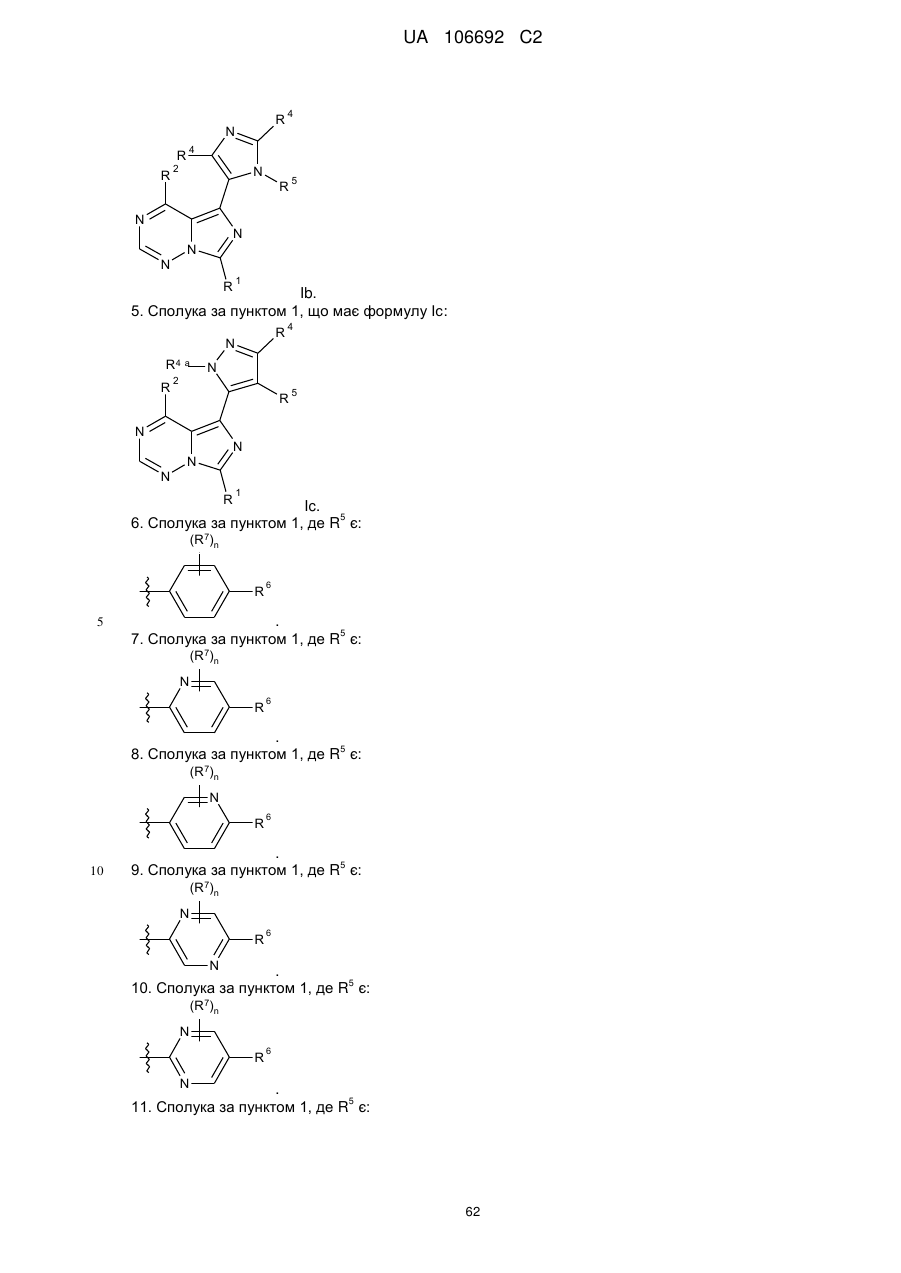
4. Сполука за пунктом 1, що має формулу Іb:
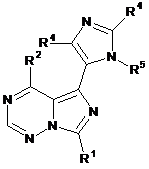 Ib.
Ib.
5. Сполука за пунктом 1, що має формулу Іс:
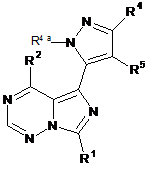 Ic.
Ic.
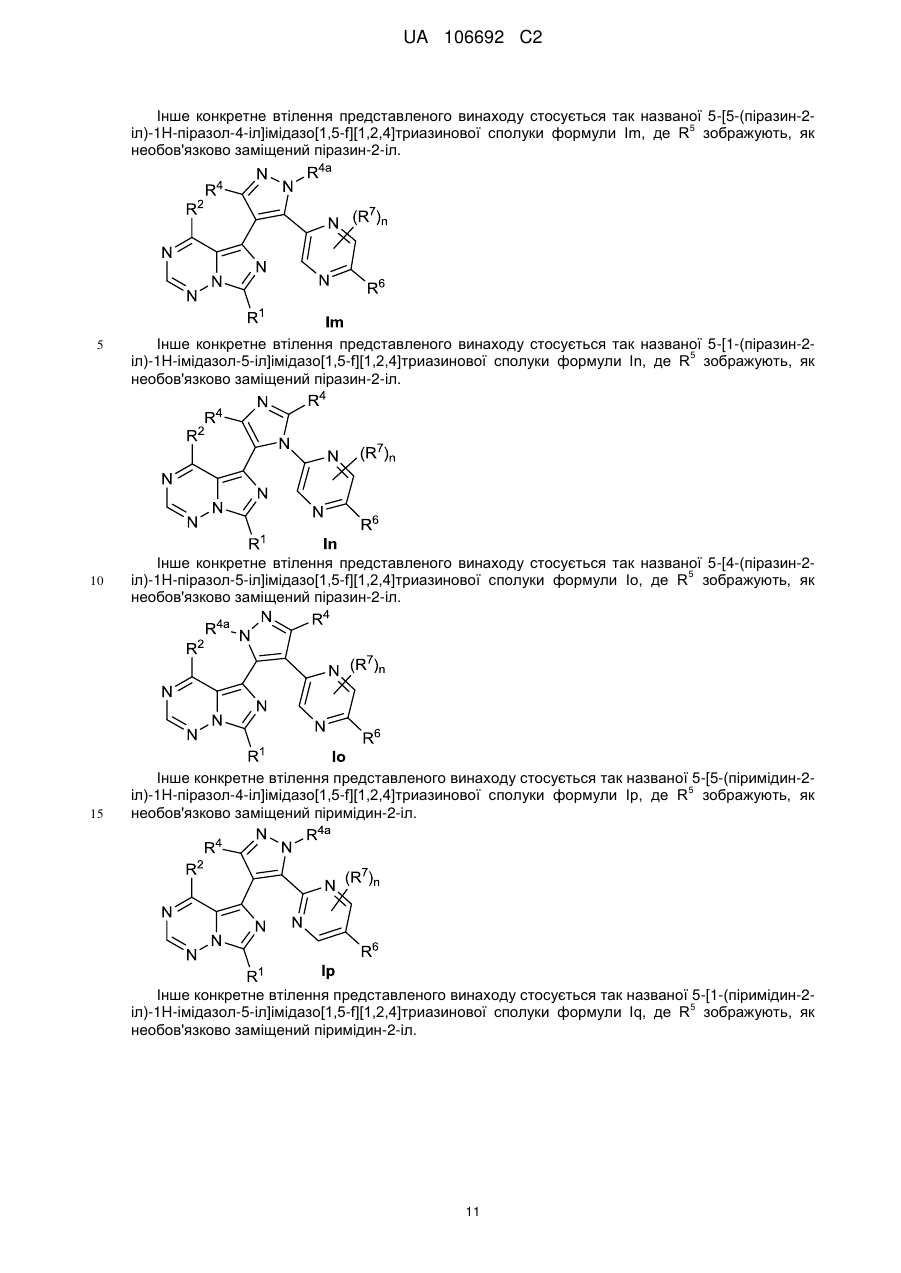
6. Сполука за пунктом 1, де R5 є:
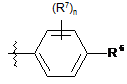 .
.
7. Сполука за пунктом 1, де R5 є:
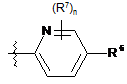 .
.
8. Сполука за пунктом 1, де R5 є:
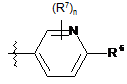 .
.
9. Сполука за пунктом 1, де R5 є:
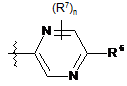 .
.
10. Сполука за пунктом 1, де R5 є:
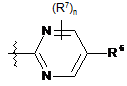 .
.
11. Сполука за пунктом 1, де R5 є:
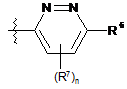 .
.
12. Сполука за пунктом 1, де R5 є:
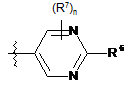 .
.
13. Сполука за пунктом 1, де R2 є вибраним з групи, що складається з -(С1-С6)алкіл-R9, -NHR3, -N(R3)2, -О-(С1-С6)алкіл-R9 та -OR8.
14. Сполука за пунктом 1, де R2 є -N(R3)2 або -NHR3.
15. Сполука за пунктом 1, де R2 є (С3-С15)циклоалкілом, (С6-С10)арилом, 3-14-членним гетероциклілом або 5-14-членним гетероарилом; де згаданий (С3-С15)циклоалкіл та 3-14-членний гетероцикліл необов'язково може містити один або два подвійних або потрійних зв'язки та одну-три оксогрупи (O=).
16. Сполука за пунктом 1, де R6 є вибраним з групи, що складається з гідрогену, галогену, -CF3, -CHF2 та -CH2F.
17. Сполука за пунктом 1, де R6 є вибраним з групи, що складається з -(C=O)-R8, -(C=O)-OR8, -OR8, -O-(C=O)-N(R8)2, -SR8, -S(O)R8, -S(O)2R8, NH2, -NН-(С1-С6)алкілу, -N[(С1-С6)алкіл]2, -NH-(C=O)-R8, -NH-(C=O)-OR8, -O-(C=O)-N(R8)2, -N((С1-С6)алкіл)-(C=O)-R8 та -N((С1-С6)алкіл)-(С=О)-ОR8.
18. Сполука за пунктом 1, де R6 є (С1-С6)алкілом або (С3-С15)циклоалкілом.
19. Сполука за пунктом 1, де R6 є вибраним з групи, що складається з (С2-С6)алкенілу, (С2-С6)алкінілу, 3-14-членного гетероциклілу, (С6-С10)арилу та 5-14-членного гетероарилу.
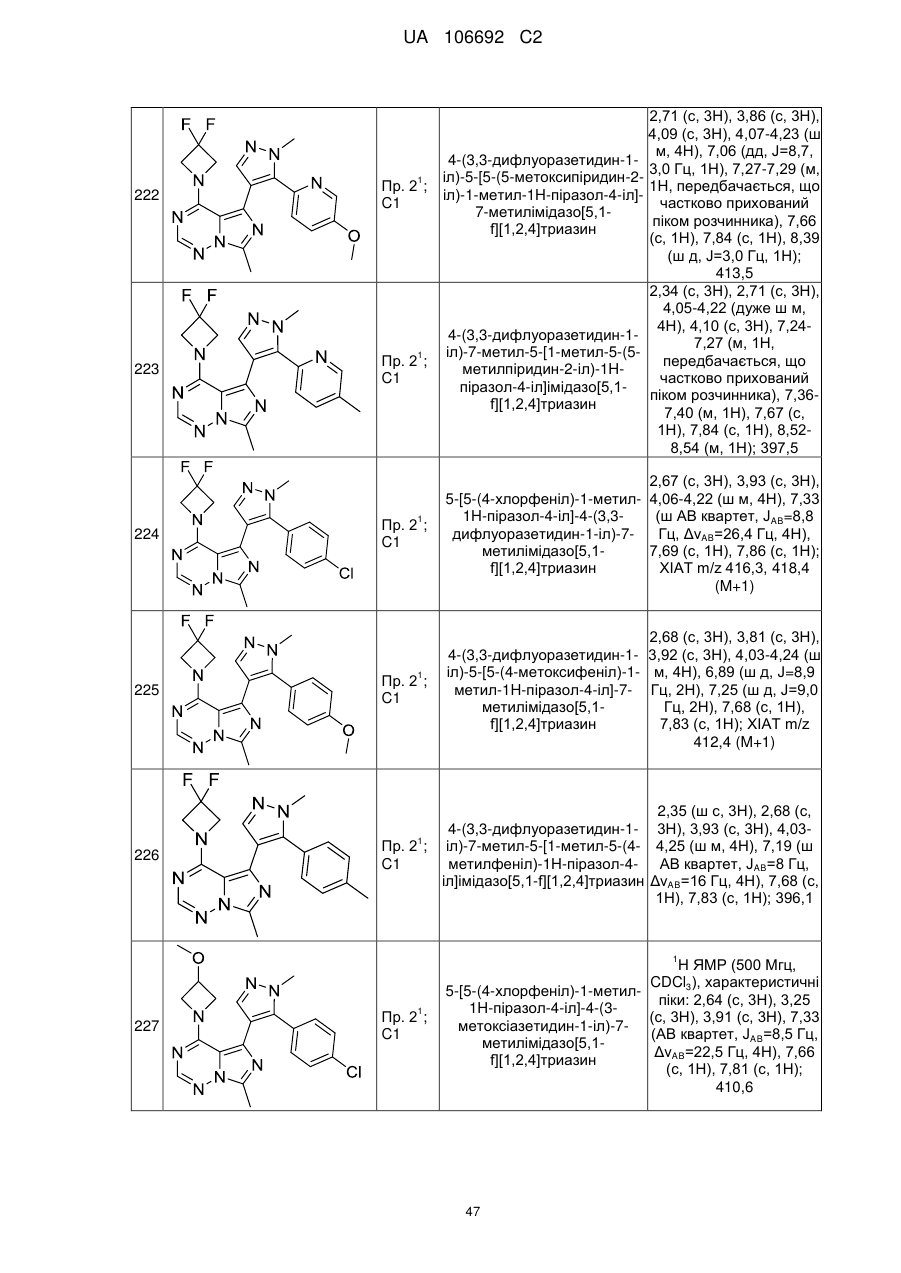
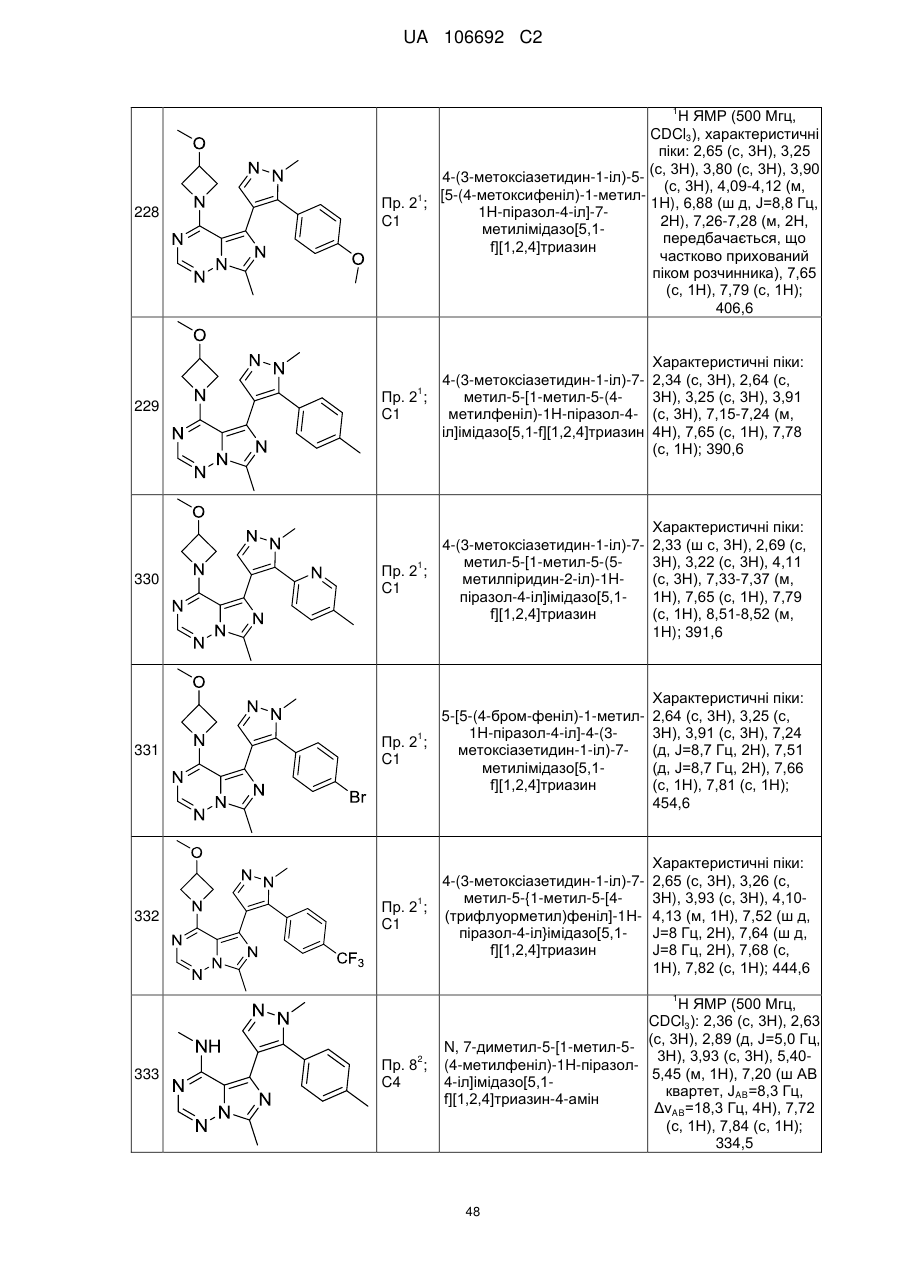
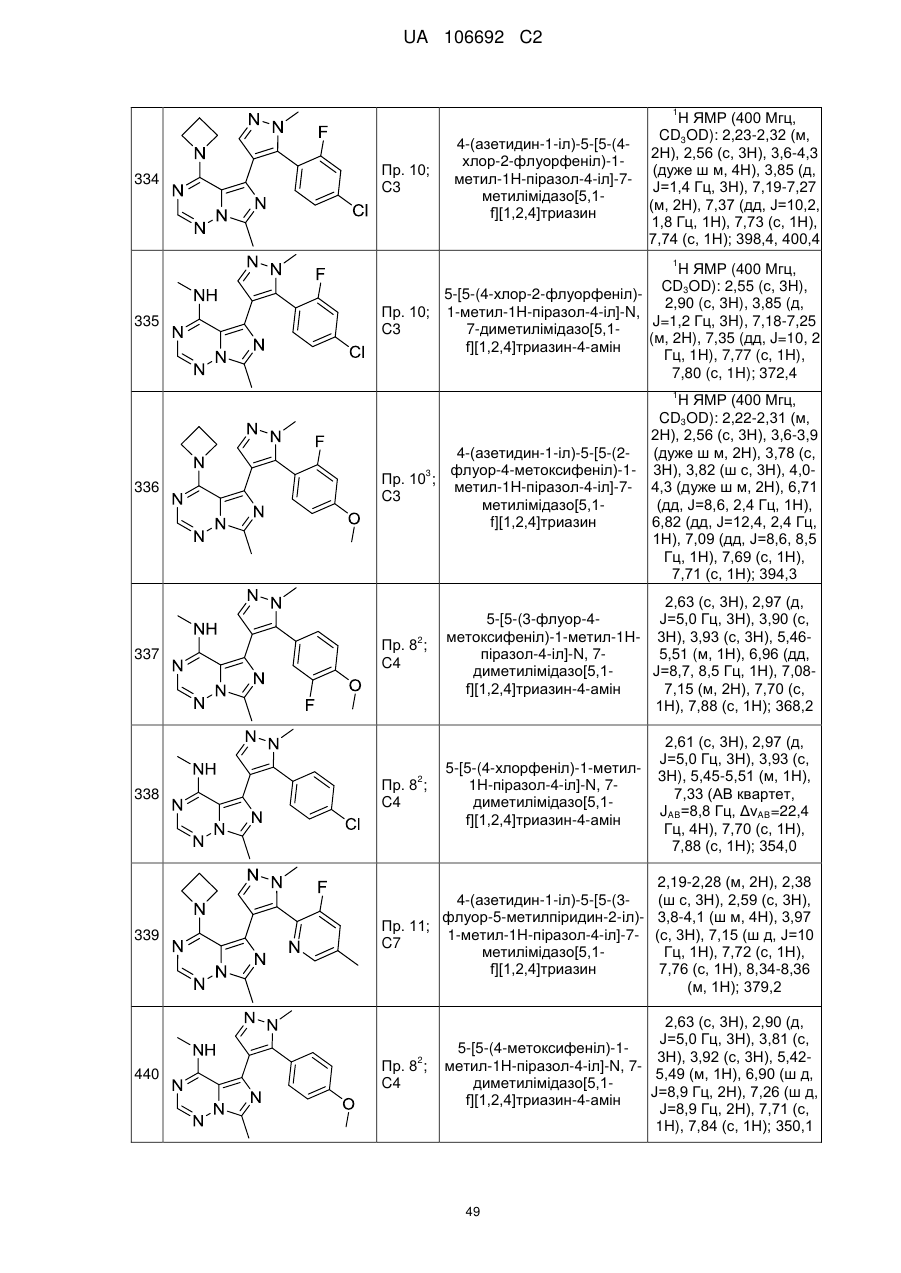
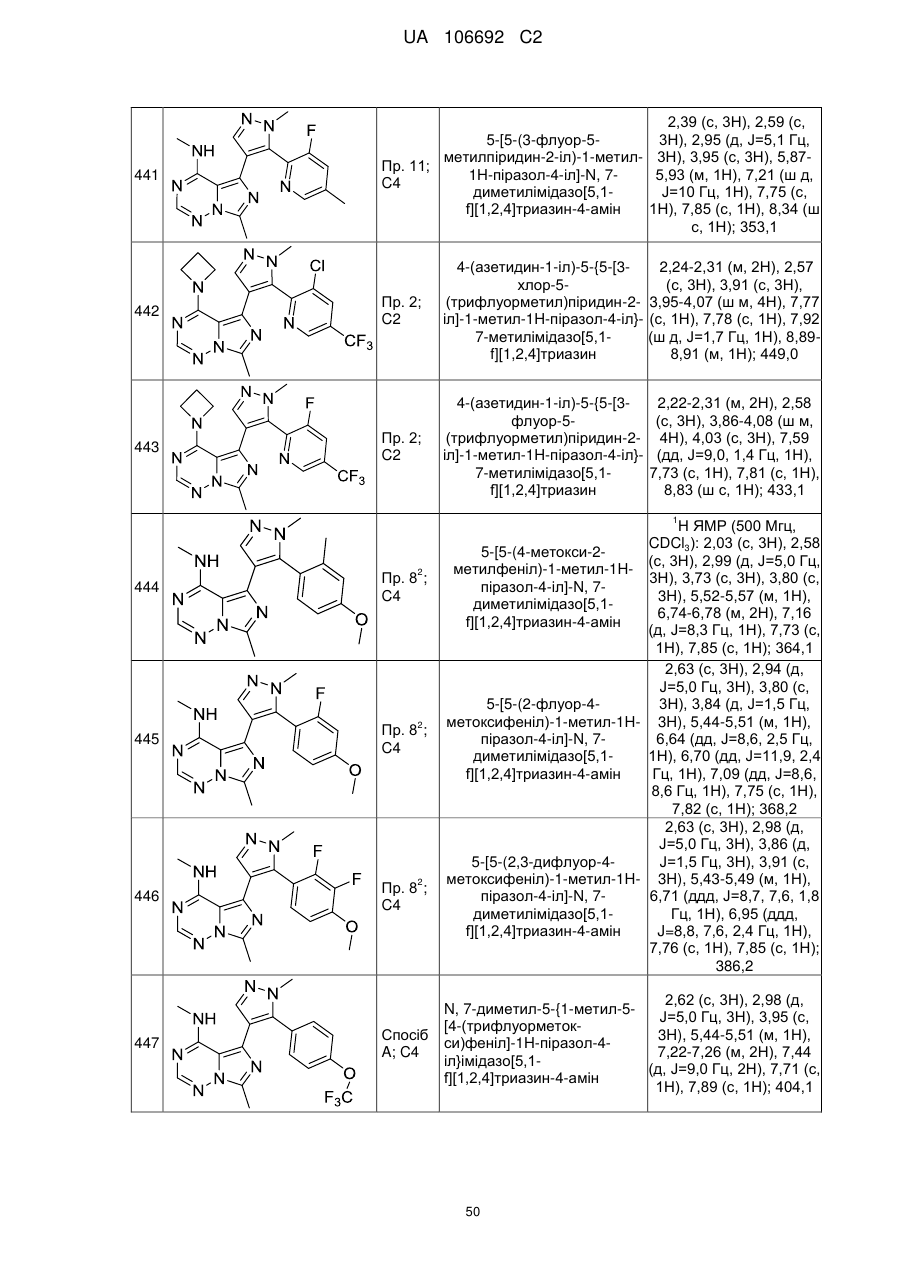
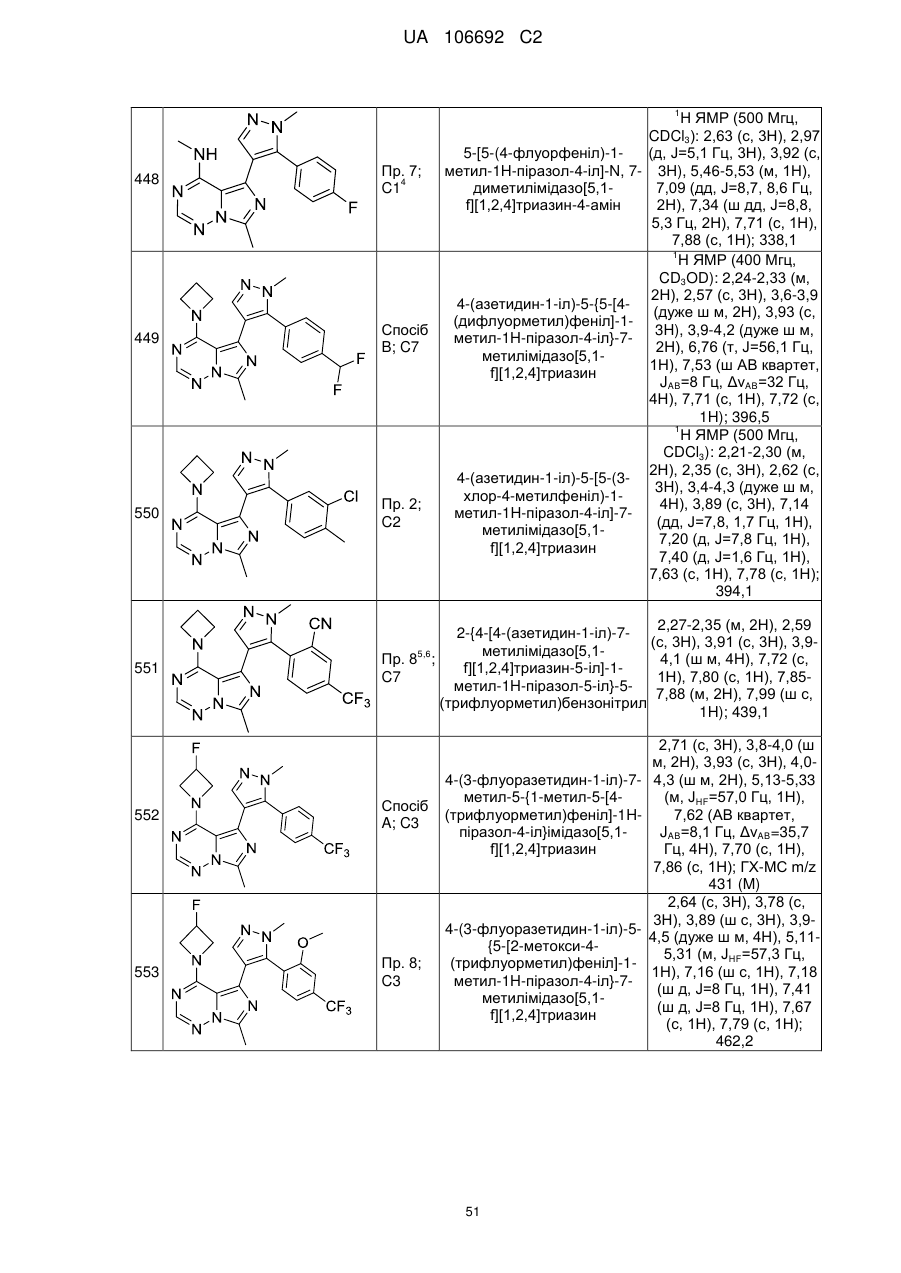
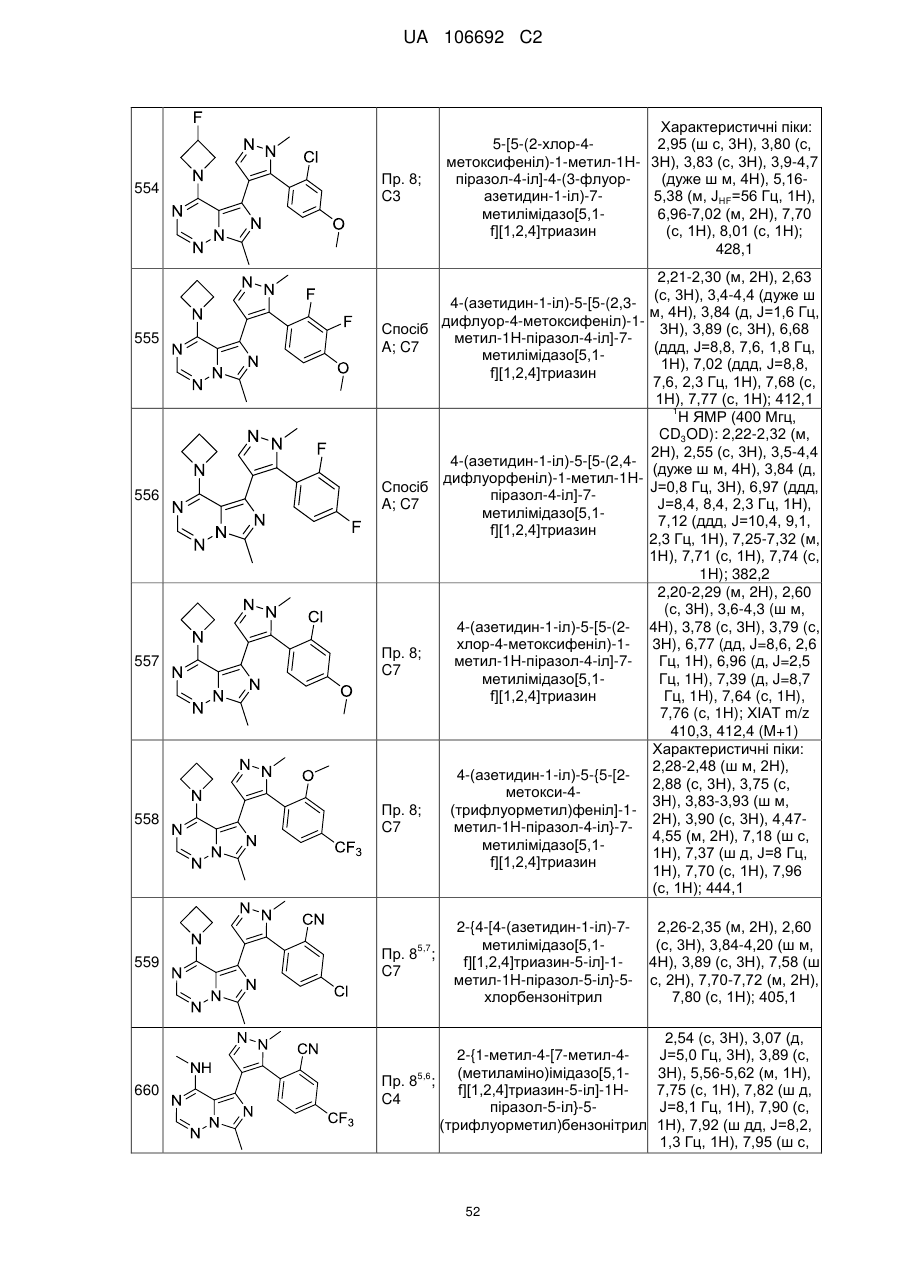
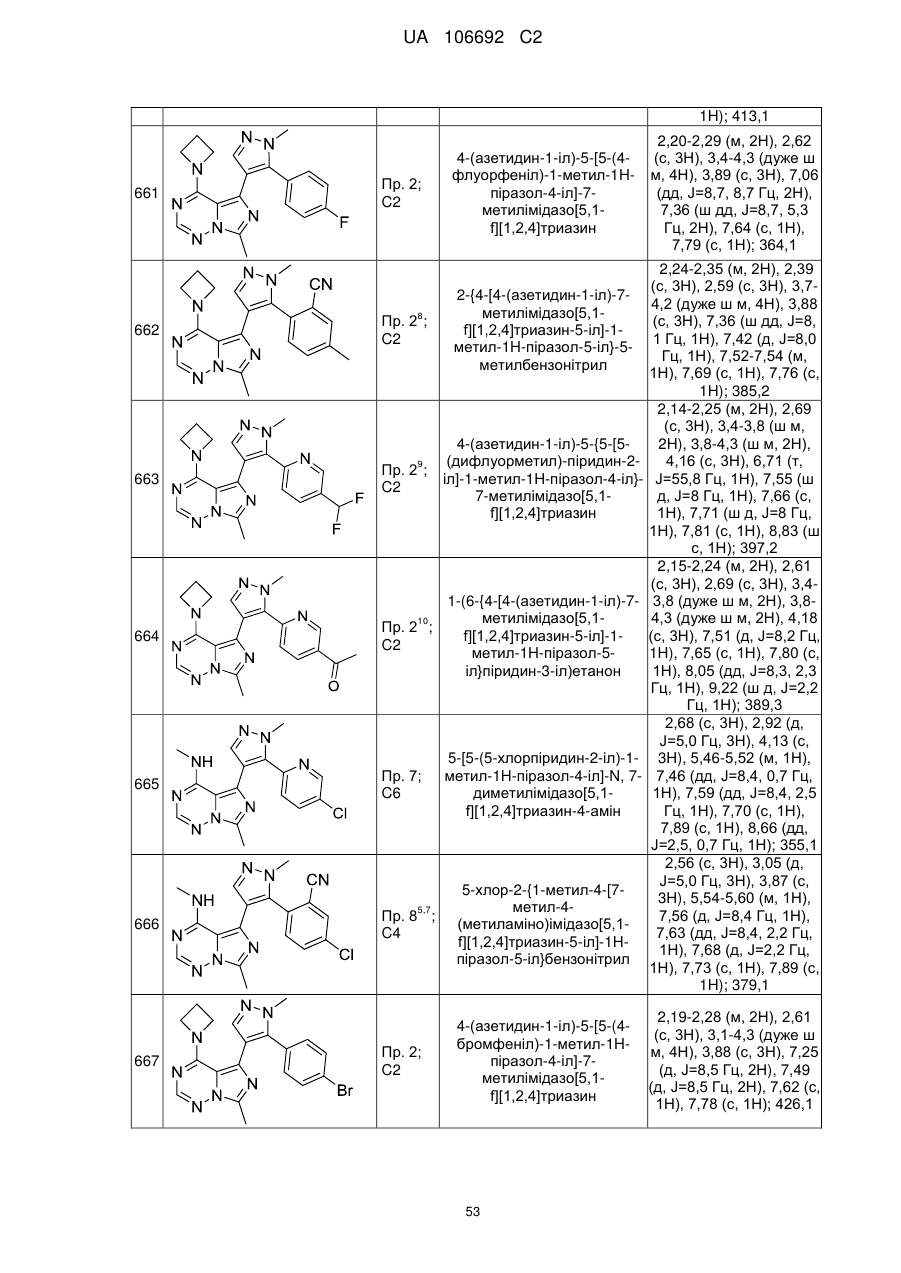
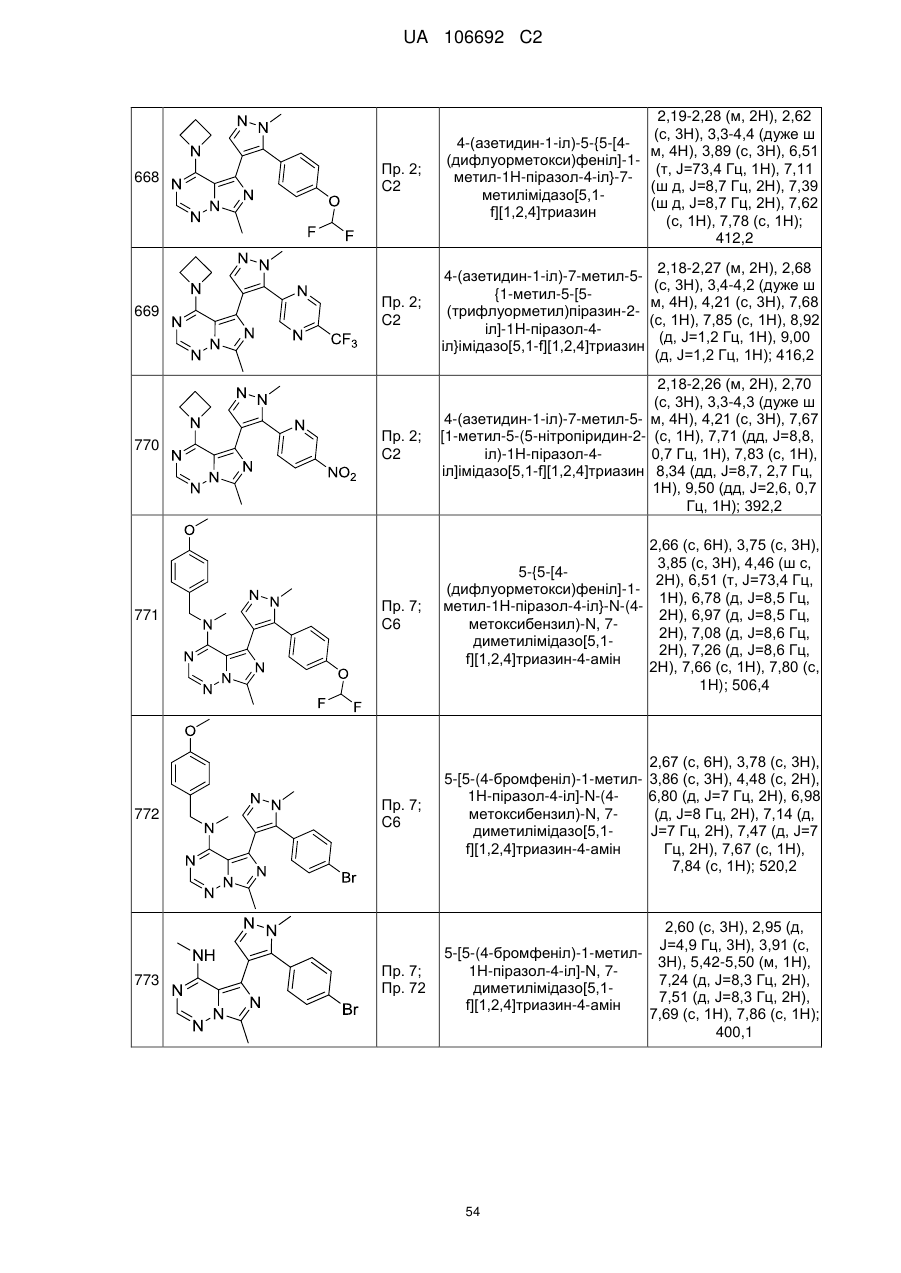
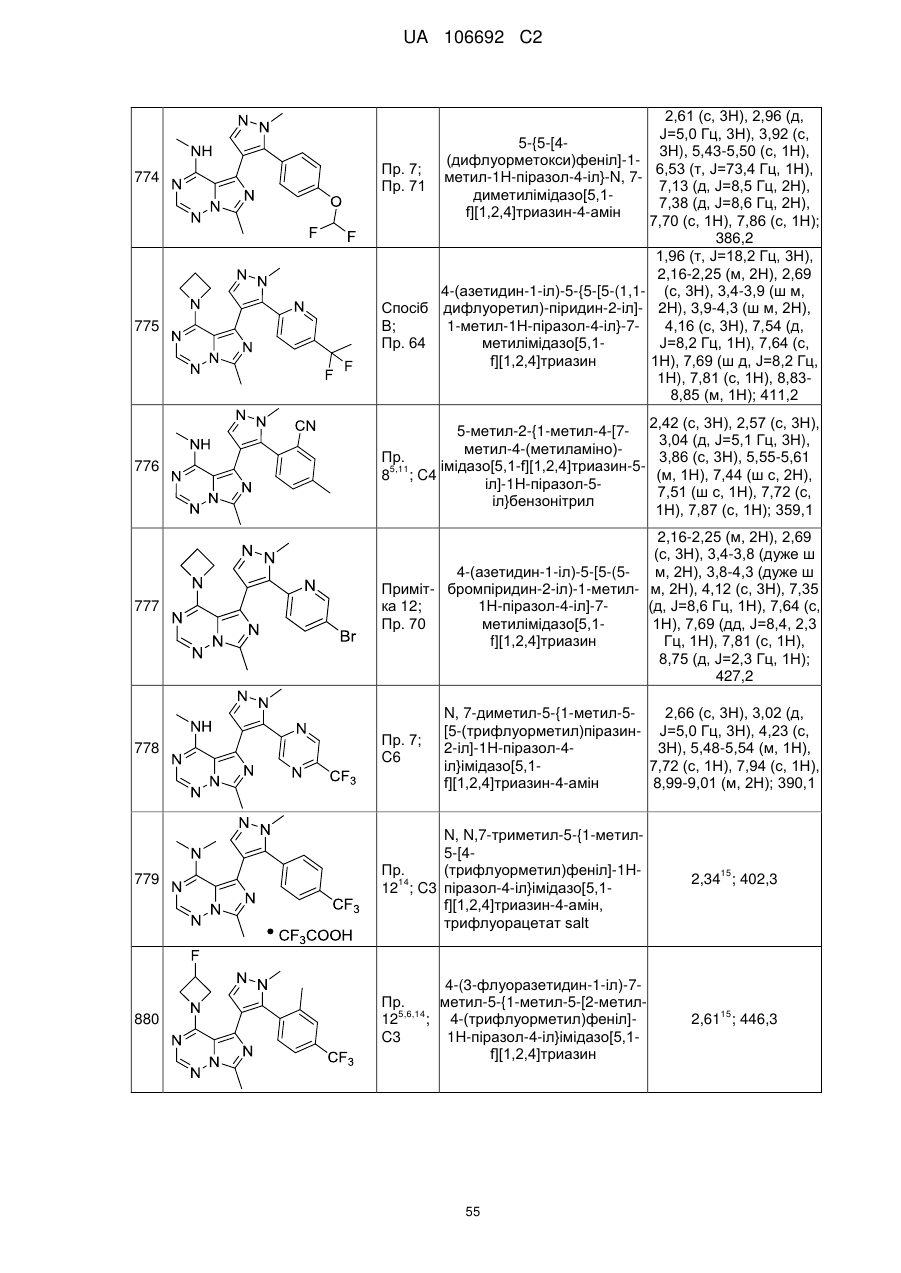
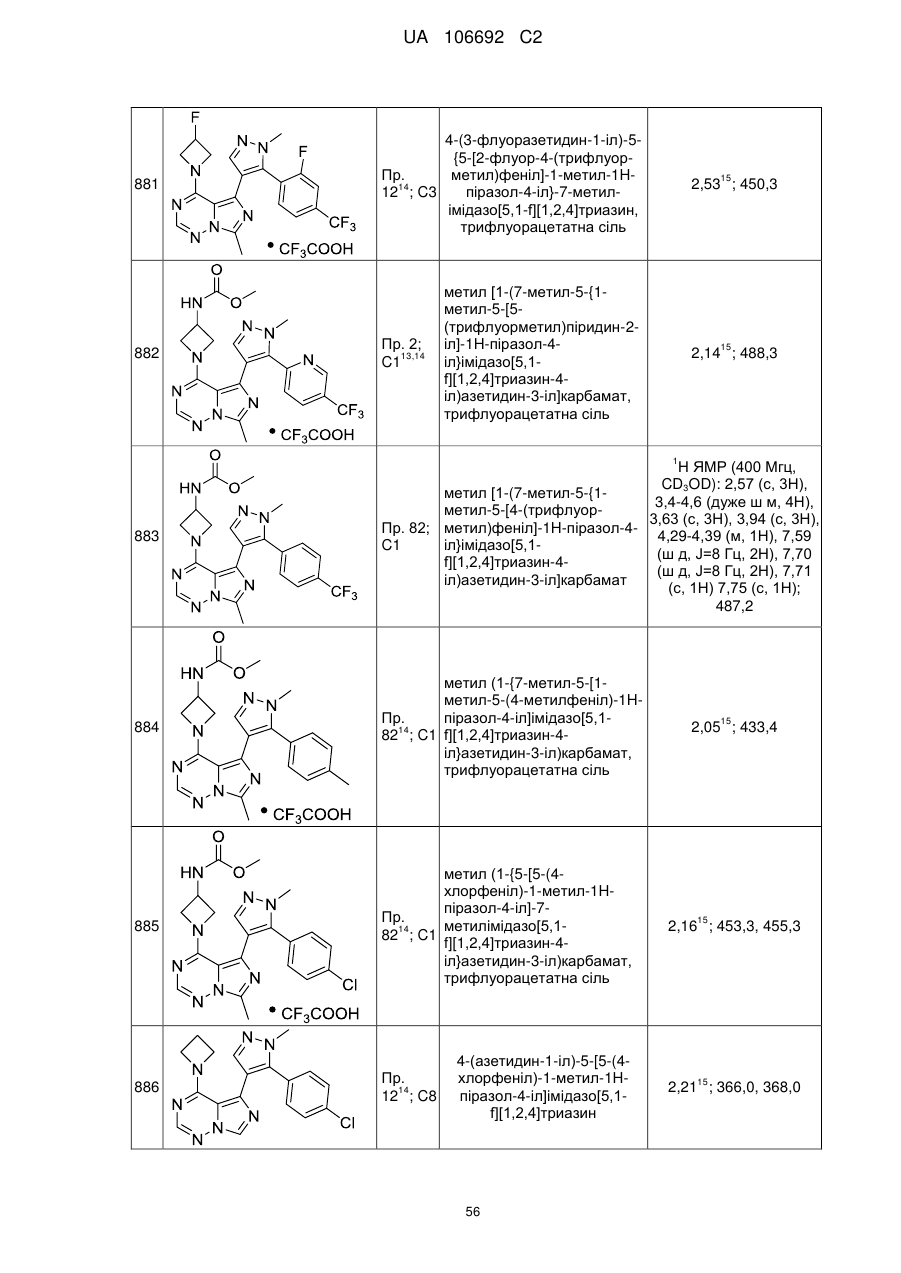
20. Сполука за пунктом 1, вибрана з групи, що включає:
4-(азетидин-1-іл)-7-метил-5-[1-метил-5-(4-метилфеніл)-1Н-піразол-4-іл]імідазо[5,1-f][1,2,4]триазин;
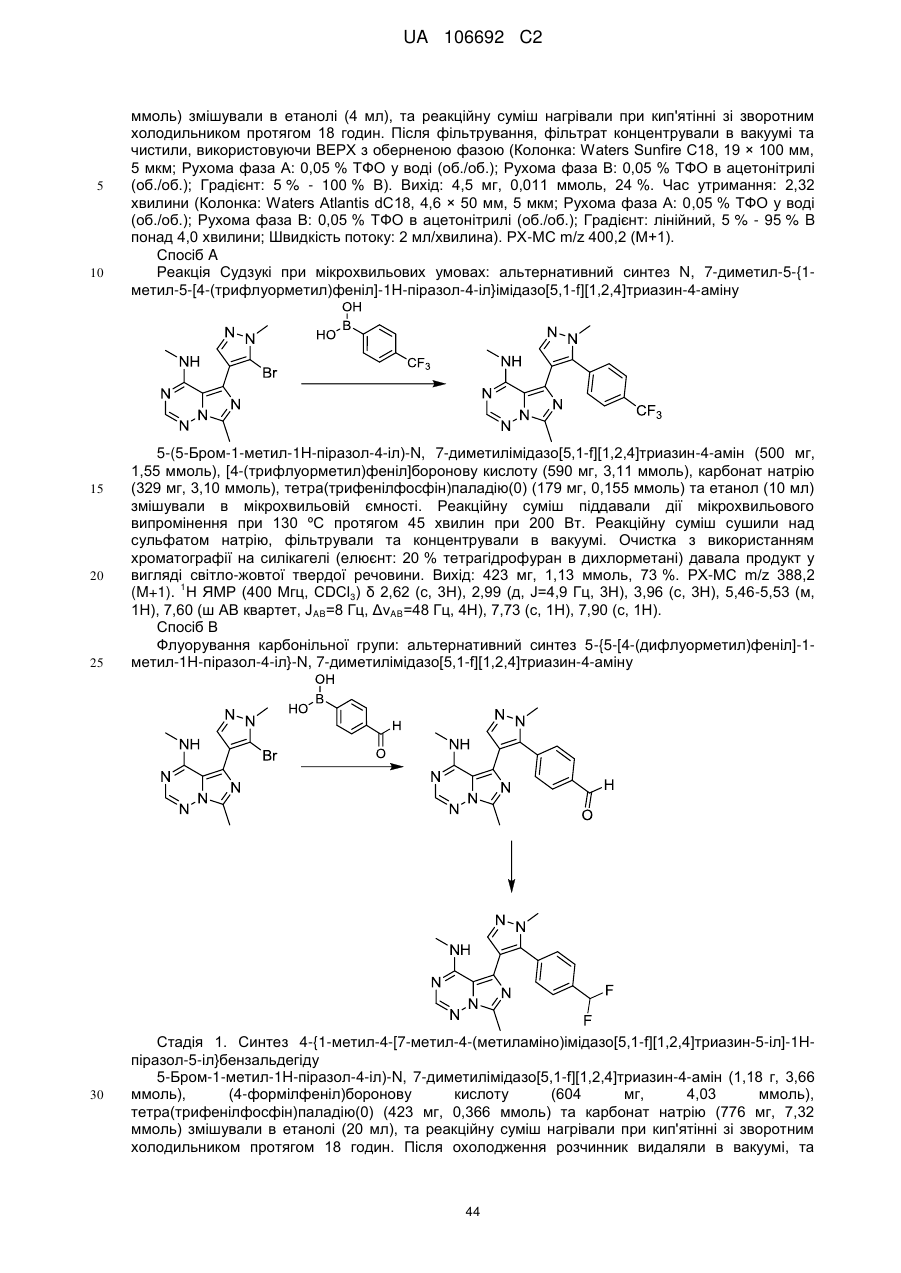
4-(азетидин-1-іл)-7-метил-5-{1-метил-5-[4-(трифлуорметил)феніл]-1Н-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин;
4-(азетидин-1-іл)-7-метил-5-{1-метил-5-[5-(трифлуорметил)піридин-2-іл]-1Н-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин;
4-(азетидин-1-іл)-5-[5-(4-хлорфеніл)-1-метил-1H-піразол-4-іл]-7-метилімідазо[5,1-f][1,2,4]триазин;
4-(азетидин-1-іл)-5-[5-(5-хлорпіридин-2-іл)-1-метил-1Н-піразол-4-іл]-7-метилімідазо[5,1-f][1,2,4]триазин;
5-{5-[4-(дифлуорметил)феніл]-1-метил-1Н-піразол-4-іл}-N,7-диметилімідазо[5,1-f][1,2,4]триазин-4-амін;
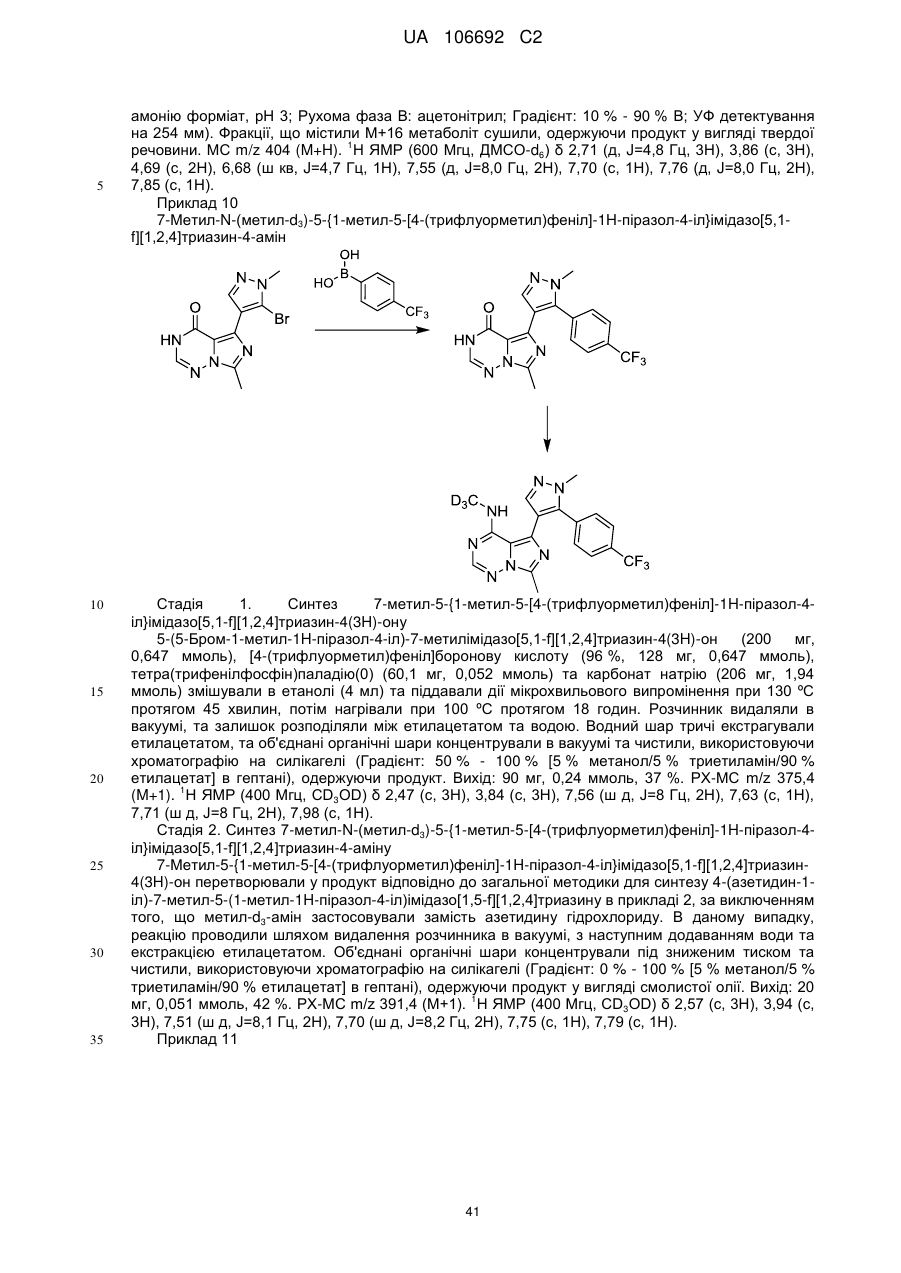
7-метил-N-(d3)метил-5-{1-метил-5-[4-(трифлуорметил)феніл]-1H-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин-4-амін;
N,7-диметил-5-{1-метил-5-[5-(трифлуорметил)піридин-2-іл]-1Н-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин-4-амін;
4-(азетидин-1-іл)-5-{5-[3-флуор-5-(трифлуорметил)піридин-2-іл]-1-метил-1Н-піразол-4-іл}-7-метилімідазо[5,1-f][1,2,4]триазин;
N,7-диметил-5-{1-метил-5-[4-(трифлуорметокси)феніл]-1Н-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин-4-амін;
4-(азетидин-1-іл)-5-{5-[4-(дифлуорметил)феніл]-1-метил-1Н-піразол-4-іл}-7-метилімідазо[5,1-f][1,2,4]триазин;
4-(3-флуоразетидин-1-іл)-7-метил-5-{1-метил-5-[4-(трифлуорметил)феніл]-1Н-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин;
4-(азетидин-1-іл)-5-[5-(4-бромфеніл)-1-метил-1Н-піразол-4-іл]-7-метилімідазо[5,1-f][1,2,4]триазин;
4-(азетидин-1-іл)-5-{5-[4-(дифлуорметокси)феніл]-1-метил-1Н-піразол-4-іл}-7-метилімідазо[5,1-f][1,2,4]триазин;
4-азетидин-1-іл-7-метил-5-{1-метил-5-[5-(трифлуорметил)піразин-2-іл]-1H-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин;
4-азетидин-1-іл-5-[5-(5-бромпіридин-2-іл)-1-метил-1Н-піразол-4-іл]-7-метилімідазо[5,1-f][1,2,4]триазин;
N,7-диметил-5-{1-метил-5-[5-(трифлуорметил)піразин-2-іл]-1Н-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин-4-амін;
або її фармацевтично прийнятна сіль.
21. Спосіб полегшення одного або більше симптомів когнітивного порушення, пов'язаного з шизофренією у людини, за яким згаданій людині вводять терапевтично ефективну кількість сполуки формули І за пунктом 1 або її фармацевтично прийнятної солі.
22. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки формули І за пунктом 1 або її фармацевтично прийнятну сіль разом з фармацевтично прийнятним носієм.
23. 4-(Азетидин-1-іл)-7-метил-5-{1-метил-5-[5-(трифлуорметил)піридин-2-іл]-1Н-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин або його фармацевтично прийнятна сіль.
24. 4-(Азетидин-1-іл)-7-метил-5-{1-метил-5-[5-(трифлуорметил)піридин-2-іл]-1Н-піразол-4-іл}імідазо[5,1-f][1,2,4]триазин.
25. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за будь-яким одним з пунктів 23 або 24 разом з фармацевтично прийнятним носієм.
26. Спосіб лікування мігрені, за яким:
пацієнту, що цього потребує, вводять терапевтично ефективну кількість сполуки формули І за пунктом 1 або її фармацевтично прийнятної солі.
Текст
Реферат: Представлений винахід стосується сполуки формули R 2 A N R 5 N N N R 1 (I) та її фармацевтично прийнятних солей, способу їх одержання, проміжних сполук, що використовують при їх одержанні, композицій, що містять такі сполуки, та застосування таких сполук в способі лікування захворювання або стану, вибраного з групи, що складається із UA 106692 C2 (12) UA 106692 C2 захворювань центральної нервової системи, когнітивних розладів, шизофренії, деменції та інших розладів у ссавців. UA 106692 C2 5 10 15 20 25 30 35 40 45 50 55 Галузь винаходу Даний винахід стосується імідозо[5,1-f][1,2,4]триазинів, які є селективними інгібіторами PDE2. Крім того, винахід стосується проміжних сполук для одержання таких сполук; фармацевтичних композицій, що містять такі сполуки; та застосування таких сполук в способах лікування певних розладів центральної нервової системи (ЦНС) або інших розладів. Крім того, винахід стосується способів лікування нейродегенеративних або психіатричних розладів, включаючи психози, порушення когнітивної діяльності, шизофренію, депресію, деменцію та інші розлади у ссавців. Передумови створення винаходу Фосфодіестерази (PDE) є класом внутрішньоклітинних ферментів, які є включеними в гідроліз нуклеотидних циклічного аденозинмонофосфату (цАМФ) та циклічного гуанозинфосфату (цГМФ) до їх відповідних нуклеотидних монофосфатів. Дані циклічні нуклеотиди слугують як вторинні месенджери в декількох клітинних шляхах, регулюючи безліч внутрішньоклітинних процесів в нейронах центральної нервової системи, включаючи активацію цАМФ- та цГМФ-залежних протеїнкіназ, яка викликає наступне фосфорилювання протеїнів, що беруть участь в регуляції синоптичної передачі, синоптичної пластичності, диференціації та виживання нейронів. На сьогоднішній ден, визначений тільки один ген для PDE2, PDE2A; однак, повідомлялось про кілька альтернативно сплайсованих ізоформ PDE2A, які включають PDE2A1, PDE2A2 та PDE2A3. PDE2A визначали як унікальну родину, що ґрунтується на первинній амінокислотній послідовності та певній ферментній активності. PDE2A3 послідовність людини була виділена в 1997 (Rosman et al., Isolation and characterization of human cDNAs encoding a cGMP-stimulated 3',5'-cyclic nucleotide phosphodiesterase, Gene, 191 (1):89-95, 1997). Інгібування PDE2A демонструє підвищену когнітивну функцію на декількох до клінічних моделях когнітивної діяльності, які відображають покращення впізнавальної пам'яті, соціальних взаємодій та короткочасної пам'яті, всі з яких є в дефіциті при шизофренії (Boess et al., Inhibition of phosphodiesterase 2 increases neuronal cGMP, synaptic plasticity and memory performance, Neuropharmacology, 47(7):1081-92, 2004). Інгібування PDE2A, крім того, покращує стан при когнітивних розладах, що розвиваються при старінні та хворобі Альцгеймера (Domek-Lopacinska and Strosznajder, The effect of selective inhibition of cyclic GMP hydrolyzing phosphodiesterases 2 and 5 on learning and memory processes and nitric oxide synthetase activity in brain during aging, Brain Research, 1216:68-77, 2008). Байєр (Bayer) опублікував біохімічний та поведінковий профіль BAY 60-7550, показуючи роль інгібування PDE2 в когнітивних розладах (Brandon et al., Potential CNS Applications for Phosphodiesterase Enzyme Inhibitors, Annual Reports in Medicinal Chemistry 42: 4-5, 2007). Однак, дана сполука показала значну ефективність щодо інших PDE ізоформ та мала високий кліренс та обмежене проникнення у мозок, що, як вважається, не призведе до одержання розвитку в клініці. Крім того, продемонстровано, що інгібітори PDE2 показали ефективність в до клінічних моделях тривожності та депресії (Masood et al., Anxiolytic effects of phosphodiesterase-2 inhibitors associated with increased cGMP signaling, JPET 331(2):690-699, 2009; Masood et al., Reversal of Oxidative Stress-Induced Anxiety by Inhibition of Phosphodiesterase-2 in Mice, JPET 326(2):369-379, 2008; Reierson et al., Repeated antidepressant therapy increases cyclic GMP signaling in rat hippocampus, Neurosci. Lett., 466(3):149-53, 2009). PDE2A протеїн, експресований в дорсальному розі спинного мозку та задньому корінчику ганглій, дозволяє PDE2A модулювати циклічні нуклеотидні рівні в цих ділянках під час процесу невропатичного та запального болю (Schmidtko et al., cGMP Produced by NO-Sensitive Guanylyl Cyclase Essentially Contributes to Inflammatory and Neuropathic Pain by Using Targets Different from cGMP-Dependent Protein Kinase I, The Journal of Neuroscience, 28(34): 8568-8576, 2008). Продемонстровано, що на периферії експресія PDE2A в ендотеліальних клітинах відіграє критичну роль в регулюванні ендотеліальної бар'єрної функції. Рівні експресії PDE2A в ендотеліальних клітинах зростають у відповідь на цитокіни запалення, такі як TNF-альфа, за умов сепсису та синдрому гострої дихальної недостатності, та сприяє порушенню ендотеліальної бар'єрної функції. Продемонстровано, що інгібування PDE2A відновлює недостатність проникності при сепсисі та підвищує показник виживання в моделі на тваринах сепсису та ендотоксикозу (Seybold et al., Tumor necrosis factor-{alpha}-dependent expression of phosphodiesterase 2: role in endothelial hyperpermeability, Blood, 105:3569-3576, 2005; Kayhan et al., The adenosinedeaminase inhibitor erythro-9-[2-hydroxyl-3-ноніл]-adenine decreases intestinal permeability and protects against experimental sepsis: a prospective, randomized laboratory investigation, Critical Care, 12(5):R125, 2008). 1 UA 106692 C2 5 10 15 20 25 Конкретні імідазотриазини опубліковані, як інгібітори кіназ, такі як: міжнародна публікація заявки на патент WO2011005909 під назвою "Process for the preparation of substituted imidazo[5,1-f][1,2,4]triazine derivatives;” публікація заявки на патент США: US20090286768 під назвою "Substituted imidazopyrazines and imidazotriazines as ACK1 inhibitors and their preparation;” міжнародна публікація заявки на патент WO200911748 під назвою "Preparation of mTOR inhibitor salt forms;” Міжнародна публікація заявки на патент: WO2009008992 під назвою "Preparation of imidazo[1,5-a]pyrazin-8-amine for use in combination therapy of cancers and cancer metastasis;” публікація заявки на патент США US20080139582 під назвою "Preparation of substituted pyrazolopyrimidinamines as inhibitors of Bruton's tyrosine kinase;” міжнародна публікація заявки на патент: WO2007106503 під назвою: "Imidazo[1,5-a]pyrazin-8-amine in combined treatment with an EGFR kinase inhibitor and an agent that sensitizes tumor cells to the effects of EGFR kinase inhibitors;” міжнародна публікація заявки на патент WO2007087395 під назвою "Preparation of ethynyl-or vinyl-imidazopyrazines and imidazotriazines as mammalian target of rapamycin (mTOR) inhibitors for the treatment of cancer and other diseases;” публікація заявки на патент США US20070112005 під назвою "Preparation of substituted imidazopyrazines and related compounds as mTOR inhibitors;” публікація заявки на патент США US20060019957 під назвою "Preparation of imidazotriazines as protein kinase inhibitors;” та міжнародна публікація заявки на патент WO2005097800 під назвою "Preparation of 6,6-bicyclic ring substituted гетероbicyclic protein kinase inhibitors” Реферат винаходу Представлений винахід стосується нових сполук формули I або їх фармацевтично прийнятних солей, де: 5" “-A-R є: , 5 30 35 40 45 5 або 5 ; A1R A2R A3R 1 R є гідрогеном, (C1-C6)алкілом, (C2-C6)алкенілом, (C2-C6)алкінілом, (C3-C15)циклоалкілом, -(C1-C6)алкіл-OH, -(C1-C6)алкіл-CN, -SF5, -CF3, -CHF2, або -CH2F; 2 9 3 3 9 8 R є -(C1-C6)алкіл-R , -NHR , -N(R )2, -O-(C1-C6)алкіл-R , -OR , (C3-C15)циклоалкілом, (C6C10)арилом, (C1-C14)гетероциклілом або (C1-C14)гетероарилом; де згаданий (C3-C15)циклоалкіл та (C1-C14)гетероцикліл необов'язково може містити один подвійний або потрійний зв'язок та 9 9 одну-дві оксо (O=) групи; та де згадані -(C1-C6)алкіл-R , -O-(C1-C6)алкіл-R , (C3-C15)циклоалкільний, (C6-C10)арильний, (C1-C14)гетероциклічний або (C1-C14)гетероарильний фрагменти можуть бути необов'язково заміщеними одним-трьома замісниками незалежно вибраними з (C1-C6)алкілу, (C1-C6)алкокси, галогену або -CF3; 3 9 кожен R незалежно є вибраним з групи, що складається з -(C1-C6)алкіл-R , -(C2-C6)алкеніл9 9 9 2 3 3 R , -(C2-C6)алкініл-R та -(C3-C15)циклоалкіл-R ; або коли R є -N(R )2 обидва зі згаданих R можуть бути взяті разом з атомом нітрогену, до якого вони приєднані, утворюючи 4-6-членне гетероциклічне кільце, яке необов'язково містить одну або дві оксо групи (O=), та необов'язково заміщене одним-трьома замісниками, незалежно вибраними з групи, що складається з гідрогену, флуору, -CN, -CF3, -CHF2, -CH2F, -OH, -O-(C1-C6)алкілу, NH2, -NH-(C1-C6)алкілу, -N[(C18 8 C6)алкіл]2, (C1-C6)алкілу, (C2-C6)алкенілу, (C2-C6)алкінілу, -(C=O)-R , -(C=O)-OR , -(C=O)8 N(R )2, -O-(C=O)8 8 8 8 8 8 8 8 R , -OR , -O-(C=O)-OR , -SR , -S(O)R , -S(O)2R , -S(O)2N(R )2, -NH-(C=O)-R , -NH-(C=O)8 8 8 OR , -O-(C=O)-N(R )2, -NH-(C=O)-N(R )2, -N[(C1-C6)алкіл](C=O)8 8 8 R , -N[(C1-C6)алкіл](C=O)-OR , -N[(C1-C6)алкіл](C=O)-N(R )2, (C3-C15)циклоалкілу, (C6-C10)арилу, (C1-C14)гетероциклілу та (C1-C14)гетероарилу; де згаданий (C3-C15)циклоалкіл та (C1 2 UA 106692 C2 5 C14)гетероцикліл необов'язково може містити один подвійний або потрійний зв'язок та одну-дві оксо (O=) групи; 4 кожен R незалежно є вибраним з групи, що складається з гідрогену, галогену, (C 1-C6)алкілу, (C2-C4)алкенілу, (C2-C6)алкінілу, -CF3, -CHF2, -CH2F або (C3-C15)циклоалкілу; 4a R є гідрогеном, (C1-C6)алкілом, (C3-C4)алкенілом, (C3-C4)алкінілом, -CF3, -CHF2, -CH2F або (C3-C15)циклоалкілом; 5 R є: , , R 5e R 5f або . 10 15 20 25 5g R де n є 0, 1, 2, 3 або 4; 6 кожен R незалежно є вибраним з групи, що складається з гідрогену, галогену, (C 1C6)алкілу, -CF3, -CHF2, -CH2F, -CF2-(C1-C6)алкілу, -SF5, -CN, -(C1-C6)алкіл-CN, -NO2, -(C=O)8 8 8 8 8 8 8 R , -(C=O)-OR , -OR , -O-(C=O)-N(R )2, -SR , -S(O)R , -S(O)2R , NH2, -NH-(C1-C6)алкілу, -N[(C18 8 8 8 C6)алкіл]2, -NH-(C=O)-R , -NH-(C=O)-OR , -N[(C1-C6)алкіл](C=O)-R , -N[(C1-C6)алкіл](C=O)-OR , (C1-C6)алкілу, (C2-C6)алкенілу, (C2-C6)алкінілу, (C3-C15)циклоалкілу, (C1-C14)гетероциклілу, (C6C10)арилу та (C1-C14)гетероарилу; де згаданий (C3-C15)циклоалкіл, (C1-C14)гетероцикліл та (C1-C14)гетероарил необов'язково може містити один подвійний або потрійний зв'язок та однудві оксо (O=) групи; 7 кожен R незалежно є вибраним з групи, що складається з гідрогену, галогену, (C 1-C6)алкілу, (C2-C4)алкенілу, (C2-C6)алкінілу, -CN, -CF3, -CHF2, -CH2F, -O-(C1-C6)алкілу та (C3-C15)циклоалкілу; 8 кожен R де б не знаходився незалежно є вибраним з групи, що складається з гідрогену, (C 1C6)алкілу, (C3-C15)циклоалкілу, -CF3 та -CHF2; 9 кожен R незалежно є вибраним з групи, що складається з гідрогену, галогену, -CF3, -CHF2, 8 8 8 CH2F, -CF2-(C1-C6)алкілу, -CN, -(C1-C6)алкіл-CN, -NO2, -(C=O)-R , -(C=O)-OR , -OR , -O-(C=O)8 8 8 8 8 N(R )2, -SR , -S(O)R , -S(O)2R , NH2, -NH-(C1-C6)алкілу, -N[(C1-C6)алкіл]2, -NH-(C=O)-R , -NH8 8 8 (C=O)-OR , -N[(C1-C6)алкіл](C=O)-R , -N[(C1-C6)алкіл](C=O)-OR , (C1-C6)алкілу, (C2-C6)алкенілу, 3 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 55 60 (C2-C6)алкінілу, (C3-C15)циклоалкілу, (C1-C14)гетероциклілу, (C6-C10)арилу та (C1-C14)гетероарилу; де згаданий (C3-C15)циклоалкіл, (C1-C14)гетероцикліл необов'язково може містити один подвійний або потрійний зв'язок та одну-дві оксо (O=) групи; та де кожен із згаданих (C 3C15)циклоалкільного, (C1-C14)гетероциклічного, (C6-C10)арильного та (C1-C14)гетероарильного фрагментів можуть бути необов'язково заміщеними одним-трьома замісниками, незалежно вибраними з (C1-C6)алкілу, (C1-C6)алкокси, галогену або -CF3. Як використано в даному документі, визначається, що термін "алкіл" включає насичений аліфатичний вуглеводень, в том числі з лінійним ланцюгом та розгалуженим ланцюгом. Переважно, алкільна група має від 1 до 6 атомів карбону. Наприклад, як використано в даному документі, термін "(C1-C6)алкіл, ” а також алкільні фрагменти інших груп, зазначених в даному документі (наприклад, (C1-C6)алкокси), стосується лінійних або розгалужених радикалів від 1 до 6 атомів карбону (наприклад, метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, втор-бутил, трет-бутил), необов'язково заміщених 1-5 прийнятними замісниками. Кожен раз, коли в даній заявці використовують числовий діапазон, наприклад, коли використовують від 1 до 6 при визначенні "алкіл", це означає, що алкільна група може містити 1 атом карбону, 2 атома карбону, 3 атома карбону, тощо, до, включаючи 6 атомів карбону. Як використано в даному документі, визначається, що термін "алкеніл" включає аліфатичні вуглеводні, що містить, щонайменше, один подвійний карбон-карбон зв'язок, включаючи лінійні ланцюги та розгалужені ланцюги, які мають, щонайменше, один подвійний карбон-карбон зв'язок. Переважно, алкенільна група має від 2 до 6 атомів карбону. Більш переважно, алкенільна група містить від 2 до 4 атомів карбону. Наприклад, як використано в даному документі, термін "(C2-C6)алкеніл" означає лінійний або розгалужений ланцюг ненасичених радикалів з від 2 до 6 атомів карбону, включаючи, але не обмежуючись цим, етеніл, 1-пропеніл, 2-пропеніл (аліл), ізопропеніл, 2-метил-1-пропеніл, 1-бутеніл, 2-бутеніл, тощо, необов'язково заміщений 1-5 прийнятними замісниками. Коли сполуки формули I містять алкенільну групу, то алкенільна група може існувати як чиста E (entgegen) форма, чиста Z (zusammen) форма, або будь-яка їх суміш. Як використано в даному документі, визначається, що термін "алкініл" включає аліфатичні вуглеводні, що містить, щонайменше, один потрійний карбон-карбон зв'язок, включаючи лінійні ланцюги та розгалужені ланцюги, які мають, щонайменше, один потрійний карбон-карбон зв'язок. Переважно, алкінільна група містить від 2 до 6 атомів карбону. Наприклад, як використано в даному документі, термін "(C2-C6)алкініл" означає лінійний або розгалужений вуглеводневий ланцюг алкінільних радикалів, як визначено вище, що містять від 2 до 6 атомів карбону та один потрійний зв'язок, необов'язково заміщений 1-5 прийнятними замісниками. Як використано в даному документі, визначається, що термін "циклоалкіл" включає насичені або ненасичені (неароматичні) моноциклічні або біциклічні вуглеводневі кільця (наприклад, моноцикли, такі як циклопропіл, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил або циклононіл, або біоцикли, включаючи місточкові або анельовані системи, такі як біцикло[2.2.1]гептаніл, біцикло[3.2.1]октаніл або біцикло[5.2.0]нонаніл, тощо), необов'язково заміщені 1-5 прийнятними замісниками. Циклоалкільна група містить від 3 до 15 атомів карбону. В одному втіленні циклоалкіл необов'язково може містити один, два або більше некумулятивних неароматичних подвійних або потрійних зв'язків та одну-три оксо групи. Переважно, біциклоалкільна група має від 6 до 15 атомів карбону. Біциклоалкіл є необов'язково заміщеним 1-5 прийнятними замісниками. В одному втіленні біциклоалкіл необов'язково може містити один, два або більше некумулятивних неароматичних подвійних або потрійних зв'язків. Як використано в даному документі, визначається, що термін "арил" включає з всіма карбонами моноциклічні або з анельованим кільцем поліциклічні групи, що мають кон'юговану пі-електронну систему. Арильна група має 6, 8 або 10 атомів карбону в кільці(ях). Більш часто, арил група має 6 або 10 атомів карбону в кільці(ях). Найбільш часто, арильна група має 6 атомів карбону в кільці. Наприклад, як використано в даному документі, термін “(C 6-C10)арил" означає ароматичні радикали, які містять від 6 до 10 атомів карбону, такі як феніл, нафтил, тетрагідронафтил, інданіл, тощо. Арильна група є необов'язково заміщеною 1-5 прийнятними замісниками. Як використано в даному документі, визначається, що термін "гетероарил" включає моноциклічні або занельованим кільцем поліциклічні ароматичні гетероциклічні групи з одним або більше гетероатомами, вибраними з O, S або N в, щонайменше, одному кільці. Гетероарильна група має від 5 до 14 атомів кільця, включаючи від 1 до 13 атомів карбону, та від 1 до 5 гетероатомів, вибраних з O, S або N. Переважно, гетероарильна група має від 5 до 10 атомів кільця, включаючи від одного до чотирьох гетероатомів. Гетероарильна група, крім того, містить, від однієї до трьох оксо груп. Більш переважно, гетероарильна група має від 5 до 8 4 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 55 60 атомів кільця, включаючи один, два або три гетероатоми. Моноциклічні гетероарили, що особливо цікавлять, включають ті, що мають 5 атомів кільця, в тому числі від одного до трьох гетероатомів, або ті, що мають 6 атомів кільця, в тому числі дин або два атоми нітрогену, як гетероатоми. Анельовані біциклічні гетероарили, що особливо цікавлять, включають два анельованих 5 та/або 6 членних моноциклічних кільця, що містять від одного до чотирьох гетероатомів. Прийнятні гетероарили включають піридил, піразиніл, піримідиніл, пірадизиніл, тієніл, фурил, імідазоліл, піроліл, оксазоліл (наприклад, 1,3-оксазоліл, 1,2-оксазоліл), тіазоліл (наприклад, 1,2-тіазоліл, 1,3-тіазоліл), піразоліл, тетразоліл, триазоліл (наприклад, 1,2,3триазоліл, 1,2,4-триазоліл), оксадіазоліл (наприклад, 1,2,3-оксадіазоліл), тіадіазоліл (наприклад, 1,3,4-тіадіазоліл), хіноліл, ізохіноліл, бензотієніл, бензофурил, індоліл, піридон, піримідон, піразинон, піримідинон, тощо. Гетероарильна група є необов'язково заміщеною 1-5 прийнятними замісниками. Як використано в даному документі, визначається, що термін "гетероцикліл" включає моноциклічну, місточкову поліциклічну або анельовану поліциклічну, насичену або ненасичену, неароматичну 3 – 14-членну кільцеву систему, 1-13 атомів карбону та, включаючи 1-5 гетероатомів, вибраних з O, S або N. Гетероциклічна група, крім того, включає одну-три оксо групи. Приклади таких гетероциклоалкільних кілець включають азетидиніл, тетрагідрофураніл, імідазолідиніл, піролідиніл, піперидиніл, піперазиніл, оксазолідиніл, тіазолідиніл, піразолідиніл, тіоморфолініл, тетрагідротіазиніл, тетрагідротіадіазиніл, морфолініл, оксетаніл, тетрагідродіазиніл, оксазиніл, оксатіазиніл, індолініл, ізоіндолініл, хінуклідиніл, хроманіл, ізохроманіл, бензоксазиніл, 2-азабіцикло[2.2.1]гептанон, 3-азабіцикло[3.1.0]гексан, 3азабіцикло[4.1.0]гептан, тощо. Наступні приклади згаданих гетероциклоалкільних кілець включають тетрагідрофуран-2-іл, тетрагідрофуран-3-іл, імідазолідин-1-іл, імідазолідин-2-іл, імідазолідин-4-іл, піролідин-1-іл, піролідин-2-іл, піролідин-3-іл, піперидин-1-іл, піперидин-2-іл, піперидин-3-іл, піперидин-4-іл, піперазин-1-іл, піперазин-2-іл, 1,3-оксазолідин-3-іл, ізотіазолідин, 1,3-тіазолідин-3-іл, 1,2-піразолідин-2-іл, 1,2-тетрагідротіазин-2-іл, 1,3-тетрагідротіазин-3-іл, 1,2тетрагідродіазин-2-іл, 1,3-тетрагідродіазин-1-іл, 1,4-оксазин-2-іл, оксазолідинон, тощо. Гетероциклоалкільне кільце є необов'язково заміщеним 1-5 прийнятними замісниками. Переважні гетероцикліли включають 5- та 6-членні моноциклічні кільця або 9- та 10- членні анельовані біциклічні кільця. Як використано в даному документі, визначається, що термін "галоген" або "атом галогену" включає флуор, хлор, бром або йод. Як зазнвчено вище, сполуки формули I можуть існувати в формі фармацевтично прийнятних солей, таких як, наприклад, кислі адитивні солі та основні адитивні солі сполуки формули I. Фраза "фармацевтично прийнятна(і) сіль(олі)”, як використано в даному документі, якщо не зазначене інше, включає кислотні адитивні або основні солі, які можуть бути присутніми в сполуках формули I. Фармацевтично прийнятна солі сполук формули (I) включають їх кислотні адитивні та основні солі. Прийнятні кислі адитивні солі утворюються з кислот, які утворюють нетоксичні солі. Приклади включають ацетатні, адипінатні, аспартатні, бензоатні, безилатні, бікарбонатні/карбонатні, бісульфатні/сульфатні, боратні, камзілатні, цитратні, цикламатні, едісілатні, езілатні, форміатні, фумаратні, глюцептатні, глюконатні, глюкуронатні, гексафлуорфосфатні, гібензатні, гідрохлоридні/хлоридні, гідробромідні/бромідні, гідройодитні/йодитні, ізетіонатні, лактатні, малатні, малеатні, малонатні, мезилатні, метилсульфатні, нафтилатні, 2-напсілатні, нікотинатні, нітратні, оротатні, оксалатні, пальмітатні, памоатні, фосфатні/гідрогенфосфатні/дигідрогенфосфатні, піроглутаматні, сахаратні, стеаратні, сукцинатні, танатні, тартратні, тозилатні, трифлуорацетатні та ксинафоатні солі. Прийнятні основні солі утворюються з основ, які утворюють нетоксичні солі. Приклади включають солі алюмінію, аргініну, бензатину, кальцію, холіну, діетиламіну, діоламіну, гліцину, лізину, магнію, меглюміну, оламіну, калію, натрію, трометаміну та цинку. Крім того, можуть утворюватися гемісолі кислот та основ, наприклад, гемісульфатні та гемі кальцієві солі. Для огляду прийнятних солей, дивись Handbook of Pharmaceutical Salts: Properties, Selection, and Use by Stahl and Wermuth (Wiley-VCH, 2002). Способи виробництва фармацевтично прийнятних солей сполук формули I є відомими кваліфікованому фахівцю в даній галузі з рівня техніки. Визначено, що, як використано в даному документі, терміни "формула I" та "формула I або її фармацевтично прийнятна сіль" включають всі форми сполуки формули I, в тому числі її 5 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 55 60 гідрати, сольвати, ізомери, кристалічні та некристалічні форми, ізоморфи, поліморфи, метаболіти та проліки. Сполуки формули I або їх фармацевтично прийнятні солі, можуть існувати в несольватованій та сольватованих формах. Коли розчинник або вода є міцно зв'язаними, комплекс буде мати стехіометрію, що добре визначається, незалежно від вологості. Коли, однак, розчинник або вода є слабо зв'язаними, як в канальних сольватах та гігроскопічних сполуках, вміст води/розчинника буде залежати від умов вологості та сухості. В таких випадках, нормою буде нестехіометрія. Сполуки формули I можуть існувати як хелати або інші комплекси. Включеними в межі винаходу є комплекси, такі як клатрати, комплекси включення лікарський засіб-господар, в яких, на відміну від згаданих вище сольватів, лікарський засіб та господар є присутніми в стехіометричних або нестехіометричних кількостях. Крім того, включеними є комплекси формули I, що містять два або більше органічних та/або неорганічних компоненти, які можуть бути в стехіометричних або нестехіометричних кількостях. Одержані в результаті комплекси можуть бути іонізованими, частково іонізованими або неіонізованими. Для огляду таких комплексів, дивись J. K. Haleblian, J. Pharm. Sci. 1975, 64, 1269-1288. Крім того, включеними в межі винаходу є метаболіти сполук формули I, що є сполуками, які утворюються in vivo при введенні лікарського засобу. Метаболіти формули I включають сполуки, 1 в яких R є гідроксіалкілом. Сполуки формули I можуть мати асиметричні атоми карбону. Зв'язки карбон-карбон сполук формули I можуть бути зображені в даному документі, використовуючи суцільну лінію ( ), суцільний клин ( ), або пунктирний клин ( ). Застосування суцільної лінії для зображення зв'язків з асиметричними атомами карбону означає, що вказуються всі можливі стереоізомери (наприклад конкретні енантіомери, рацемічні суміші, тощо) при цьому атом карбону є включеним. Застосування або суцільного, або пунктирного клина, щоб зобразити зв'язки з асиметричними атомами карбону, означає, що вказують тільки той стереоізомер, який показаний, що означає, що він є включеним. Можливо, що сполуки формули I можуть містити більше ніж один асиметричний атом карбону. В таких сполуках, застосування суцільної лінії для зображення зв'язків з асиметричними атомами карбону означає, що вказуються всі можливі стереоізомери, що означає, що вони є включеними. Наприклад, якщо не вказане інше, мається на увазі, що сполуки формули I можуть існувати як енантіомери та діастереомери або як рацемати та їх суміші. Застосування суцільної лінії для зображення зв'язків з одним або більше асиметричними атомами карбону в сполуці формули I та застосування суцільного або пунктирного клину для зображення зв'язків з іншими асиметричними атомами карбону в тій самій сполуці означає, що вказується, що суміш діастереомерів є присутньою. Стереоізомери формули I включають цис- та транс- ізомери, оптичні ізомери, такі як R та S енантіомери, діастереомери, геометричні ізомери, ротаційні ізомери, конформаційні ізомери та таутомери сполуки формули I, включаючи сполуки, що демонструють більше ніж один тип ізомерії; та їх суміші (такі як рацемати та діастереомерні пари). Крім того, включеними є кислотні адитивні або основні адитивні солі, в яких оптично активним є протиіон, наприклад, Dлактат або L-лізин, або рацемічні, наприклад, DL-тартрат або DL-аргінін. Коли будь-який рацемат кристалізується, можливими є кристали двох різних типів. Першим типом є рацемічна сполука (справжній рацемат), згадана вище, де одержують одну гомогенну форму кристалу, що містить обидва енантіомери в еквімолярних кількостях. Другим типом є рацемічна суміш або конгломерат, де одержують дві форми кристалу в еквімолярних кількостях, кожна з яких містить один енантіомер. Сполуки формули I можуть демонструвати явище таутомерії та структурної ізомерії. Наприклад, сполуки формули I можуть існувати в декількох таутомерних формах, включаючи єнольну та імінну форму, та кето й єнамінову форму, та геометричні ізомери, та їх суміші. Всі такі таутомерні форми є включеними в межі сполуки формули I. Таутомери існують як суміші таутомерного ряду в розчині. В твердій формі, як правило, переважає один таутомер. Навіть якщо один таутомер може бути описаний, представлений винахід включає всі таутомери сполуки формули I. Представлений винахід, крім того, включає ізотопно-мічені сполуки, які є ідентичними до тих, що перелічені в формулі I вище, але фактично такі, в яких один або більше атомів заміщені на атом, який має атомну масу або масове число відмінне від атомної маси або масового числа, що зазвичай зустрічається в природі. Приклади ізотопів, що можуть бути введені в сполуки формули I включають ізотопи гідрогену, карбону, нітроген, оксиген, фосфор, флуор та хлор, такі 2 3 13 14 15 17 18 32 35 18 36 як, але не обмежуючись цим, H, H, C, C, N, O, O, P, S, F та Cl. Конкретні 3 ізотопно-мічені сполуки формули I, наприклад, ті в які введені радіоактивні ізотопи, такі як H та 6 UA 106692 C2 14 5 10 C, є корисними в лікарських засобах та/або дослідженнях розподілення субстрату в тканині. 3 14 Мічений тритієм, тобто, H, та карбоном-14, тобто, C, ізотопами є особливо переважними завдяки легкості їх одержання та здатності до виявлення. До того ж, заміщення більш важкими 2 ізотопами, такими як дейтерій, тобто, H, може дати конкретні терапевтичні переваги, що в результаті призводять до більшої метаболічної стабільності, наприклад, до зростання in vivo періоду напів-виведення або зниження необхідного дозування та, тому, може бути переважним за деяких обставин. Ізотопно-мічені сполуки формули I, як правило, можуть бути одержані шляхом виконання методик, розкритих в схемах та/або в прикладах та одержаннях нижче, шляхом заміщення ізотопно-міченим реагентом неізотопно-міченого реагенту. Конкретне втілення представленого винаходу стосується сполуки формули I I або її фармацевтично прийнятної солі, де: 5" “-A-R є: 15 20 25 30 35 5 A1R 1 R є -(C1-C6)алкілом (більш конкретно метилом або етилом; ще більш конкретно метилом); 2 3 3 R є -NHR або -N(R )2; 3 9 кожен R незалежно є вибраним з групи, що складається з -(C1-C6)алкіл-R , -(C2-C6)алкеніл9 9 9 9 R , -(C2-C6)алкініл-R та -(C3-C15)циклоалкіл-R (більш конкретно -(C1-C6)алкіл-R та ще більш 2 3 3 конкретно метилом); або коли R є -N(R )2 обидва зі згаданих R можуть бути взяті разом з атомом нітрогену, до якого вони є приєднаними, утворюючи 4-6-членне гетероциклічне кільце, необов'язково заміщене одним-трьома замісниками, незалежно вибраними з групи, що складається з гідрогену, флуору, -CN, -CF3, -CHF2, -CH2F, -OH, -O-(C1-C6)алкілу, NH2, -NH-(C18 8 C6)алкілу, -N[(C1-C6)алкіл]2, (C1-C6)алкілу, (C2-C6)алкенілу, (C2-C6)алкінілу, -(C=O)-R , -(C=O)-OR , 8 8 8 8 8 8 8 8 -(C=O)-N(R )2 -O-(C=O)-R , -OR , -O-(C=O)-OR , -SR , -S(O)R , -S(O)2R , -S(O)2N(R )2, -NH-(C=O)8 8 8 8 R, -NH-(C=O)-OR , -O-(C=O)-N(R )2, -NH-(C=O)-N(R )2, -N[(C1-C6)алкіл](C=O)8 8 8 R , -N[(C1-C6)алкіл](C=O)-OR , -N[(C1-C6)алкіл](C=O)-N(R )2, (C3-C15)циклоалкілу, (C6-C10)арилу, (C1-C14)гетероциклілу та (C1-C14)гетероарилу; (більш конкретно один або два замісники, де згаданим(ими) замісником(ами) є гідроген, флуор, -CF3, -CHF2, -CH2F, -OH, -O-(C1-C6)алкіл, 8 NH2, -NH-(C1-C6)алкіл, -N[(C1-C6)алкіл]2, (C1-C6)алкіл або -NH-(C=O)-OR ; ще більш конкретно, де згаданим(ими) замісником(ами) є гідроген, флуор, метокси або метилкарбамат); 4 R є гідрогеном; 4a R є (C1-C6)алкілом (більш конкретно метилом або етилом; ще більш конкретно метилом); 5 R є: 7 UA 106692 C2 , R 5a , R 5b або R 5c , R 5d 7 5 10 де n є 0, 1, 2, 3 або 4 (більш конкретно, де n є 0, 1 або 2)(більш конкретно, де R є 6 гідрогеном, хлором, флуором, метилом, метокси або ціано; та ще більш конкретно, де R є хлором, бромом, метилом, етилом, метокси, -CF3, -CF2CH3, -OCF3, -OCHF2, NO2, -(C=O)-CH3, (C3-C15)циклоалкілом або ізопропілом. Конкретне втілення представленого винаходу стосується так званих 5-(1H-піразол-45 іл)імідазо[1,5-f][1,2,4]триазинових сполук формули Ia, де формула I містить групу A1R : Ia Інше конкретне втілення представленого винаходу стосується так названої 5-(1H-імідазол-55 іл)імідазо[1,5-f][1,2,4]триазинової сполуки формули Ib, де формула I містить групу A2R . Ib Інше конкретне втілення представленого винаходу стосується так названої 5-(1H-піразол-55 іл)імідазо[1,5-f][1,2,4]триазинової сполуки формули Ic, де формула I містить групу A3R . 15 Ic Інше конкретне втілення представленого винаходу стосується так названої 5-(5-феніл-1H5 піразол-4-іл)імідазо[1,5-f][1,2,4]триазинової сполуки формули Id, де R зображують, як необов'язково заміщений феніл. 8 UA 106692 C2 Інше конкретне втілення представленого винаходу стосується так названої 5-(1-феніл-1H5 імідазол-5-іл)імідазо[1,5-f][1,2,4]триазинової сполуки формули Ie, де R зображують, як необов'язково заміщений феніл. 5 10 15 Інше конкретне втілення представленого винаходу стосується так названої 5-(4-феніл-1H5 піразол-5-іл)імідазо[1,5-f][1,2,4]триазинової сполуки формули If, де R зображують, як необов'язково заміщений феніл. Інше конкретне втілення представленого винаходу стосується так названої 5-[5-(піридин-25 іл)-1H-піразол-4-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Ig, де R зображують, як необов'язково заміщений піридин-2-іл. Інше конкретне втілення представленого винаходу стосується так названої 5-[1-(піридин-25 іл)-1H-імідазол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Ih, де R зображують, як необов'язково заміщений піридин-2-іл. 9 UA 106692 C2 Інше конкретне втілення представленого винаходу стосується так названої 5-[4-(піридин-25 іл)-1H-піразол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Ii, відповідно, де R зображують, як необов'язково заміщений піридин-2-іл. 5 10 15 Інше конкретне втілення представленого винаходу стосується так названої 5-[5-(піридин-35 іл)-1H-піразол-4-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Ij, де R зображують, як необов'язково заміщений піридин-3-іл. Інше конкретне втілення представленого винаходу стосується так названої 5-[1-(піридин-35 іл)-1H-імідазол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Ik, де R зображують, як необов'язково заміщений піридин-3-іл. Інше конкретне втілення представленого винаходу стосується так названої 5-[4-(піридин-35 іл)-1H-піразол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Il, де R зображують, як необов'язково заміщений піридин-3-іл. 10 UA 106692 C2 Інше конкретне втілення представленого винаходу стосується так названої 5-[5-(піразин-25 іл)-1H-піразол-4-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Im, де R зображують, як необов'язково заміщений піразин-2-іл. 5 10 15 Інше конкретне втілення представленого винаходу стосується так названої 5-[1-(піразин-25 іл)-1H-імідазол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули In, де R зображують, як необов'язково заміщений піразин-2-іл. Інше конкретне втілення представленого винаходу стосується так названої 5-[4-(піразин-25 іл)-1H-піразол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Io, де R зображують, як необов'язково заміщений піразин-2-іл. Інше конкретне втілення представленого винаходу стосується так названої 5-[5-(піримідин-25 іл)-1H-піразол-4-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Ip, де R зображують, як необов'язково заміщений піримідин-2-іл. Інше конкретне втілення представленого винаходу стосується так названої 5-[1-(піримідин-25 іл)-1H-імідазол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Iq, де R зображують, як необов'язково заміщений піримідин-2-іл. 11 UA 106692 C2 Інше конкретне втілення представленого винаходу стосується так названої 5-[4-(піримідин-25 іл)-1H-піразол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Ir, де R зображують, як необов'язково заміщений піримідин-2-іл. 5 10 15 Інше конкретне втілення представленого винаходу стосується так названої 5-[5-(піридазин5 3-іл)-1H-піразол-4-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Is, де R зображують, як необов'язково заміщений піридазин-3-іл. Інше конкретне втілення представленого винаходу стосується так названої 5-[1-(піридазин5 3-іл)-1H-імідазол-5-іл]імідазо[5,1-f][1,2,4]триазинової сполуки формули It, де R зображують, як необов'язково заміщений піридазин-3-іл. Інше конкретне втілення представленого винаходу стосується так названої 5-[4-(піридазин5 3-іл)-1H-піразол-5-іл]імідазо[5,1-f][1,2,4]триазинової сполуки формули Iu, де R зображують, як необов'язково заміщений піридазин-3-іл. 12 UA 106692 C2 Інше конкретне втілення представленого винаходу стосується так названої 5-[5-(піримідин-55 іл)-1H-піразол-4-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Iv, де R зображують, як необов'язково заміщений піримідин-5-іл 5 10 15 20 25 30 Інше конкретне втілення представленого винаходу стосується так названої 5-[1-(піримідин-55 іл)-1H-імідазол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки Iw, де R зображують, як необов'язково заміщений піримідин-5-іл. Інше конкретне втілення представленого винаходу стосується так названої 5-[4-(піримідин-55 іл)-1H-піразол-5-іл]імідазо[1,5-f][1,2,4]триазинової сполуки формули Ix, де R зображують, як необов'язково заміщений піримідин-5-іл. Інше втілення, що особливо цікавить, стосується сполук формули I (та формул Ia-Ix), в яких 2 9 3 3 9 8 2 R є -(C1-C6)алкіл-R , -NHR , –N(R )2, -O-(C1-C6)алкіл-R або -OR . Конкретні R групи, що 3 3 особливо цікавлять, включають -NHR (особливо, коли R є метилом, етилом або пропілом), та 3 3 –N(R )2 (особливо, коли дві R групи взяті разом з атомом нітрогену, до якого вони приєднані, утворюючи необов'язково заміщену азетидинільну групу, зокрема, коли необов'язково заміщена 2 замісниками, які вибирають з гідрогену, флуору, дифлуору або метокси). Інші більш конкретні R 9 9 9 включають -(C1-C6)алкіл-R та -O-(C1-C6)алкіл-R , особливо коли R є гідрогеном, флуором, -CF3, -CHF2, -CH2F або -CF2-(C1-C6)алкілом, Зокрема, винахід, крім того, включає ті 2 8 8 сполуки, в яких R є -OR , особливо, коли R є гідрогеном, -CF3, -CHF2, метилом або етилом. 2 Інше втілення, що особливо цікавить, стосується сполук формули I (та формул Ia-Ix), де R є (C3-C15)циклоалкілом, (C6-C10)арилом, (C1-C14)гетероциклілом або (C1-C14)гетероарилом; де згаданий (C3-C15)циклоалкіл та (C1-C14)гетероцикліл необов'язково може містити один або два подвійних чи потрійних зв'язки та одну-три оксо (O=) групи; більш конкретно де (C 1C14)гетероцикліл або (C1-C14)гетероарил містить один-два атоми нітрогену. 6 Інше втілення, що особливо цікавить, стосується сполук формули I (та формул Ia-Ix), де R є 6 галогеном, -CF3, -CHF2 або -CH2F; більш конкретно де R є галогеном. Альтернативно, сполуки, що особливо цікавлять, включають флуорметильні замісники -CF3, -CHF2 або -CH2F. 6 Інше втілення, що особливо цікавить, стосується сполуки формули I (та формул Ia-Ix), де R 8 8 8 8 8 8 8 є -(C=O)-R , -(C=O)-OR , -OR , -O(C=O)-N(R )2, -SR , -S(O)R , -S(O)2R , NH2, -NH-(C18 8 C6)алкіл, -N[(C1-C6)алкіл]2, -NH-(C=O)-R , -NH-(C=O)-OR , -O-(C=O)8 8 8 6 N(R )2, -N((C1-C6)алкіл)-(C=O)-R або -N((C1-C6)алкіл)-(C=O)-OR ; більш конкретно, де R є 13 UA 106692 C2 8 5 10 15 20 25 30 35 40 45 50 55 60 8 8 8 (C=O)-R , -(C=O)-OR , -OR або -O(C=O)-N(R )2. Зокрема, представлений винахід передбачає 8 8 так звані аміносполуки NH2, -NH-(C1-C6)алкіл, -N[(C1-C6)алкіл]2, -NH-(C=O)-R , -NH-(C=O)-OR , 8 8 8 O-(C=O)-N(R )2, -N((C1-C6)алкіл)-(C=O)-R або -N((C1-C6)алкіл)-(C=O)-OR . Зокрема, 8 8 8 представлений винахід передбачає так звані тіосполуки -SR , -S(O)R або -S(O)2R . 6 Інше втілення, що особливо цікавить, стосується сполук формули I (та формул Ia-Ix), де R є (C1-C6)алкілом, (C2-C6)алкенілом, (C2-C6)алкінілом, (C3-C15)циклоалкілом, (C6-C10)арилом або 6 (C1-C14)гетероарилом; більш конкретно де R є (C1-C6)алкілом, (C2-C6)алкенілом або (C2-C6)алкінілом. Зокрема, представлений винахід передбачає кільцеві сполуки: (C3C15)циклоалкіл, (C1-C14)гетероцикліл, (C6-C10)арил або (C1-C14)гетероарил. Інше втілення, що цікавить, стосується сполук формули I (та формул Ia-Ix), де, щонайменше, один замісник включає SF5 фрагмент. Мається на увазі, що кожне з вищезгаданих втілень є інтерпретованим як одне самостійне втілення, а також взяте в поєднанні з кожним попереднім вищезгаданим втіленням (наприклад 6 2 кожне втілення R беруть разом з R та з формулами Ia-Ix). В іншому втіленні, винахід, крім того, стосується сполук, описаних як приклади 1-86 в розділі приклади об'єкта заявки, та їх фармацевтично прийнятних солей. В іншому втіленні, винахід стосується сполуки формули I, де згаданою сполукою є: 4-(азетидин-1-іл)-7-метил-5-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]імідазо[5,1f][1,2,4]триазин; 4-(азетидин-1-іл)-7-метил-5-{1-метил-5-[4-(трифлуорметил)феніл]-1H-піразол-4іл}імідазо[5,1-f][1,2,4]триазин; 4-(азетидин-1-іл)-7-метил-5-{1-метил-5-[6-(трифлуорметил)піридин-3-іл]-1H-піразол-4іл}імідазо[5,1-f][1,2,4]триазин; 4-(азетидин-1-іл)-5-[5-(4-хлорфеніл)-1-метил-1H-піразол-4-іл]-7-метилімідазо[5,1f][1,2,4]триазин; 4-(азетидин-1-іл)-5-[5-(5-хлорпіридин-2-іл)-1-метил-1H-піразол-4-іл]-7-метилімідазо[5,1f][1,2,4]триазин; 5-{5-[4-(дифлуорметил)феніл]-1-метил-1H-піразол-4-іл}-N, 7-диметилімідазо[5,1f][1,2,4]триазин-4-амін; 7-метил-N-(d3)метил-5-{1-метил-5-[4-(трифлуорметил)феніл]-1H-піразол-4-іл}імідазо[5,1f][1,2,4]триазин-4-амін; N, 7-диметил-5-{1-метил-5-[5-(трифлуорметил)піридин-2-іл]-1H-піразол-4-іл}імідазо[5,1f][1,2,4]триазин-4-амін; 4-(азетидин-1-іл)-5-{5-[3-флуор-5-(трифлуорметил)піридин-2-іл]-1-метил-1H-піразол-4-іл}-7метилімідазо[5,1-f][1,2,4]триазин; N, 7-диметил-5-{1-метил-5-[6-(трифлуорметил)піридин-3-іл]-1H-піразол-4-іл}імідазо[5,1f][1,2,4]триазин-4-амін; 4-(азетидин-1-іл)-5-{5-[2-флуор-6-(трифлуорметил)піридин-3-іл]-1-метил-1H-піразол-4-іл}-7метилімідазо[5,1-f][1,2,4]триазин; N, 7-диметил-5-{1-метил-5-[4-(трифлуорметокси)феніл]-1H-піразол-4-іл}імідазо[5,1f][1,2,4]триазин-4-амін; 4-(азетидин-1-іл)-5-{5-[4-(дифлуорметил)феніл]-1-метил-1H-піразол-4-іл}-7-метилімідазо[5,1f][1,2,4]триазин; 4-(3-флуоразетидин-1-іл)-7-метил-5-{1-метил-5-[4-(трифлуорметил)феніл]-1H-піразол-4іл}імідазо[5,1-f][1,2,4]триазин; 4-(азетидин-1-іл)-5-[5-(4-бромфеніл)-1-метил-1H-піразол-4-іл]-7-метилімідазо[5,1f][1,2,4]триазин; 4-(азетидин-1-іл)-5-{5-[4-(дифлуорметокси)феніл]-1-метил-1H-піразол-4-іл}-7метилімідазо[5,1-f][1,2,4]триазин; 4-азетидин-1-іл-7-метил-5-{1-метил-5-[5-(трифлуорметил)піразин-2-іл]-1H-піразол-4іл}імідазо[5,1-f][1,2,4]триазин; 4-азетидин-1-іл-5-[5-(5-бромпіридин-2-іл)-1-метил-1H-піразол-4-іл]-7-метилімідазо[5,1f][1,2,4]триазин; або N, 7-диметил-5-{1-метил-5-[5-(трифлуорметил)піразин-2-іл]-1H-піразол-4-іл}імідазо[5,1f][1,2,4]триазин-4-амін; або її фармацевтично прийнятна сіль. В іншому втіленні, винахід стосується сполуки формули I, вибраної з групи, що включає 5-(5-(3-флуор-5-(трифлуорметил)піридин-2-іл)-1-метил-1H-піразол-4-іл)-N, 7диметилімідазо[5,1-f][1,2,4]триазин-4-амін; 4-(азетидин-1-іл)-7-метил-5-(1-метил-5-(3-метил-5-(трифлуорметил)піразин-2-іл)-1H-піразол4-іл)імідазо[5,1-f][1,2,4]триазин; 14 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 55 60 4-(азетидин-1-іл)-7-метил-5-(1-метил-5-(3-метил-5-(трифлуорметил)піридин-2-іл)-1Hпіразол-4-іл)імідазо[5,1-f][1,2,4]триазин; N, 7-диметил-5-(1-метил-5-(3-метил-5-(трифлуорметил)піразин-2-іл)-1H-піразол-4іл)імідазо[5,1-f][1,2,4]триазин-4-амін; 5-(5-(3-хлор-5-(трифлуорметил)піридин-2-іл)-1-метил-1H-піразол-4-іл)-N, 7диметилімідазо[5,1-f][1,2,4]триазин-4-амін; 5-(5-(5-бром-3-флуорпіридин-2-іл)-1-метил-1H-піразол-4-іл)-N, 7-диметилімідазо[5,1f][1,2,4]триазин-4-амін; 4-(азетидин-1-іл)-5-(5-(3-хлор-5-(трифлуорметил)піридин-2-іл)-1-метил-1H-піразол-4-іл)-7метилімідазо[5,1-f][1,2,4]триазин; N, 7-диметил-5-(1-метил-5-(3-метил-5-(трифлуорметил)піридин-2-іл)-1H-піразол-4іл)імідазо[5,1-f][1,2,4]триазин-4-амін; 5-(5-(5-бром-3-хлорпіридин-2-іл)-1-метил-1H-піразол-4-іл)-N, 7-диметилімідазо[5,1f][1,2,4]триазин-4-амін; 5-(5-(5-бром-3-метилпіридин-2-іл)-1-метил-1H-піразол-4-іл)-N, 7-диметилімідазо[5,1f][1,2,4]триазин-4-амін; 5-(1,3-диметил-5-(5-(трифлуорметил)піридин-2-іл)-1H-піразол-4-іл)-N, 7-диметилімідазо[5,1f][1,2,4]триазин-4-амін; 4-(азетидин-1-іл)-5-(1,3-диметил-5-(5-(трифлуорметил)піридин-2-іл)-1H-піразол-4-іл)-7метилімідазо[1,5-f][1,2,4]триазин; 4-(азетидин-1-іл)-5-(1,3-диметил-5-(5-(трифлуорметил)піразин-2-іл)-1H-піразол-4-іл)-7метилімідазо[1,5-f][1,2,4]триазин; 3-(1-метил-4-(7-метил-4-(2,2,2-трифлуоретил)імідазо[5,1-f][1,2,4]триазин-5-іл)-1H-піразол-5іл)анілін; 5-(5-(4-хлорфеніл)-1-метил-1H-піразол-4-іл)-7-метил-4-фенілімідазо[5,1-f][1,2,4]триазин; 7-циклопропіл-5-(5-(4-метоксифеніл)-1-метил-1H-піразол-4-іл)імідазо[5,1-f][1,2,4]триазин-4-іл ацетат; 4-(4-(4-метокси-7-метилімідазо[5,1-f][1,2,4]триазин-5-іл)-1-метил-1H-піразол-5іл)бензонітрил; 7-метил-5-(1-метил-5-(4-(метилсульфоніл)феніл)-1H-піразол-4-іл)імідазо[5,1-f][1,2,4]триазин4-іл гідрогенкарбонат; метил 4-(1-метил-4-(7-метил-4-(2-метилциклопентил)імідазо[5,1-f][1,2,4]триазин-5-іл)-1Hпіразол-5-іл)бензоат; 4-(4-(4-(циклопента-1,3-дієн-1-іл)-7-метилімідазо[5,1-f][1,2,4]триазин-5-іл)-1-метил-1Hпіразол-5-іл)-N-метиланілін; 5-(5-(3-флуор-4-(трифлуорметил)феніл)-1-метил-1H-піразол-4-іл)-7-метил-4-(піролідин-3іл)імідазо[5,1-f][1,2,4]триазин; 5-(5-(4-метокси-3-метилфеніл)-1-метил-1H-піразол-4-іл)-7-метил-4-(1-метил-1H-піразол-5іл)імідазо[5,1-f][1,2,4]триазин; 2-метил-4-(2-метил-5-(4-(піролідин-1-іл)-7-(трифлуорметил)імідазо[5,1-f][1,2,4]триазин-5-іл)1H-імідазол-1-іл)феніл ацетат; 4-(5-(4-(азетидин-1-іл)-7-метилімідазо[5,1-f][1,2,4]триазин-5-іл)-3-метил-1H-піразол-4іл)бензонітрил; 4-(азетидин-1-іл)-5-(4-(5-(дифлуорметил)піридин-2-іл)-3-метил-1H-піразол-5-іл)-7метилімідазо[5,1-f][1,2,4]триазин; 1-(5-(5-(4-(азетидин-1-іл)-7-метилімідазо[5,1-f][1,2,4]триазин-5-іл)-3-метил-1H-піразол-4іл)піридин-2-іл)етанон; 4-(азетидин-1-іл)-5-(4-(5-етилпіразин-2-іл)-3-метил-1H-піразол-5-іл)-7-метилімідазо[5,1f][1,2,4]триазин; 4-(азетидин-1-іл)-5-(4-(5-хлорпіримідин-2-іл)-3-метил-1H-піразол-5-іл)-7-метилімідазо[5,1f][1,2,4]триазин; 4-(азетидин-1-іл)-5-(4-(5,6-диметилпіридазин-3-іл)-3-метил-1H-піразол-5-іл)-7метилімідазо[5,1-f][1,2,4]триазин; 4-(азетидин-1-іл)-5-(4-(2,4-біс(трифлуорметил)піримідин-5-іл)-3-метил-1H-піразол-5-іл)-7метилімідазо[5,1-f][1,2,4]триазин; 4-(азетидин-1-іл)-5-(1-(4-флуор-2-метилпіримідин-5-іл)-2-метил-1H-імідазол-5-іл)-7метилімідазо[5,1-f][1,2,4]триазин; або її фармацевтично прийнятної солі. Представлений винахід, крім того, стосується композицій, що містять сполуку формули I або її прийнятну сіль (наприклад, фармацевтичні композиції). Відповідно, в одному втіленні, винахід 15 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 55 60 стосується фармацевтичної композиції, що містить сполуку формули I, необов'язково включає фармацевтично прийнятний носій та, необов'язково, щонайменше, один додатковий медичний або фармацевтичний агент. В одному втіленні, додатковим медичним або фармацевтичним агентом є агентом проти шизофренії, як описано нижче. Фармацевтично прийнятний носій може включати будь-який традиційний фармацевтичний носій або наповнювач. Прийнятні фармацевтичні носії включають інертні розріджувачі або наповнювачі, воду та різні органічні розчинники (такі як гідрати та сольвати). Фармацевтичні композиції можуть, якщо бажано, містити додатклві інгредієнти, такі як ароматизатори, зв'язувальні речовини, наповнювачі, тощо. Таким чином, для перорального введення, таблетки, які містять різні наповнювачі, такі як лимонна кислота, можуть бути застосовані разом з різними розпушувачами, такими як крохмаль, альгінова кислота та певні комплексні силікати та зі зв'язуючими агентами, такими як сахароза, желатин та аравійська камедь. Крім того, для здійснення таблетування часто корисними є змащувальні агенти, такі як стеарат магнію, лаурилсульфат натрію та тальк. Тверді композиції подібного типу також можуть бути застосовані в м'яких та твердих заповнених желатиновихкапсулах. Необмежуючі приклади речовин, вваслідок цього, включають лактозу або молочний цукор та високомолекулярні поліетиленгліколі. У випадку, коли бажаними є водні суспензії або еліксири для перорального введення, активна сполука в них може комбінуватися з різними підсолоджувачами або смаковими агентами, фарбуючими речовинами або барвниками та, якщо необхідно, емульгуючими агентами або суспендуючими агентами, разом з розріджувачами, такими як вода, етанол, пропіленгліколь, гліцерин або їх комбінації. Фармацевтична композиція, наприклад, може бути в формі прийнятній для перорального введення у вигляді таблетки, капсули, гранули, порошку, складу з уповільненим вивільненням, розчину або суспензії, для парентерального ін'єкційного введення у вигляді стерильного розчину, суспензії або емульсії, для місцевого введення у вигляді мазі або крему або для ректального введення у вигляді супозиторіїв. Ілюстративні форми для парентерального введення включають розчини та суспензії активних сполук в стерильних водних розчинах, наприклад, водних розчинах пропіленгліколю або декстрози. Такі дозовані форми, якщо необхідно, можуть містити відповідний буфер. Фармацевтична композиція може бути в одиничних дозованих формах, прийнятних для одноразового введення певного дозування. Кваліфікований фахівець в даній галузі прийняв би до уваги, що композиція може бути сформульована в суб-терапевтичному дозуванні так, щоб передбачити багаторазові дози. В одному переважному втіленні композиція містить терапевтично ефективну кількість сполуки формули I та необов'язково включає фармацевтично прийнятний носій. Інше втілення за винаходом включає спосіб лікування шизофренії або психозів у ссавців, переважно людини, за яким згаданому ссавцю (переважно людині) вводять терапевтично ефективну кількість сполуки формули I або її фармацевтично прийнятної солі. Інше втілення за винаходом включає спосіб лікування розладу, опосередкованого PDE2, за яким згаданому ссавцю (переважно людині), що потребує цього, вводять кількість сполуки формули I, ефективну для інгібування PDE2; більш переважно, вводять кількість сполуки формули I ефективну для селективного інгібування PDE2. Інше втілення за винаходом передбачає спосіб лікування неврологічних розладів (таких як мігрень; епілепсія; хвороба Альцгеймера; хвороба паркенсона; черепно-мозкова травма; інсульт; порушення мозкового кровообігу (включаючи артеріосклероз судин головного мозку, церебральна амілоїдна ангіопатія, спадкова церебральна геморагія та мозкова гіпоксія-ішемія); когнітивних розладів (включаючи амнезію, сенільну деменцію, деменцію, пов'язану з ВІЛ, деменцію, пов'язану з хворобою Альцгеймера, деменцію, пов'язану з хворобою Гентінгтона, деменцію з тільцями Леві, судинну деменцію, деменція пов'язана з лікарськими засобами, марення та помірні когнітивні порушення); розумової недостатності (включаючи синдром Дауна та синдром Мартіна-Белла ламкої Х-хромосоми); розладів сну (включаючи гіперсомнію, розлад циркадного ритму сну, безсоння, порушень сну та позбавлення сну) та психіатричних розладів (таких як тривога, включаючи гострий стресовий розлад, генералізований тривожний розлад, соціальний тривожний розлад, панічний розлад, пост-травматичний стресовий розлад та обсесивно-компульсивний розлад); симулятивний розлад (включаючи істеричне сутінкове потьмарення свідомості); розладів імпульсивного контролю (включаючи компульсивний потяг до азартних ігор та розлад епізодичного порушення контролю); розлади настрою (включаючи біполярний розлад I, біполярний розлад II, манію, змішаний афективний стан, глибоку депресію, хронічну депресію, сезонну депресію, психотичну депресію і післяпологову депресію); психомоторні розлади; психотичні розлади (включаючи шизофренію, шизоаффективний розлад, 16 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 55 60 шізофреноформний розлад та маячний розлад); залежності від лікарських засобів (включаючи наркотичну залежність, алкоголізм, амфетамінову залежність, кокаїнову залежність, нікотинову залежність та синдром відміни препарату); розлади харчової поведінки (включаючи анорексію, булімію, компульсивне переїдання, гіперфагію та пагофагію); та дитячих психічних розладів (включаючи синдром дефіциту уваги, розлад дефіциту уваги/гіперактивності, кондуктивний розлад та аутизм) у ссавців, переважно людини, за яким згаданому ссавцю вводять терапевтично ефективну кількість сполуки формули І або її фармацевтично прийнятної солі. Інше втілення за винаходом включає спосіб лікування шизофренії. Інше втілення за винаходом включає спосіб лікування порушення когнітивних функцій, пов'язаних з шизофренією. Термін "терапевтично ефективна кількість", як використано в даному документі, стосується такої кількості сполуки, що вводять, яка буде полегшувати до деякої міри один або більше симптомів розладу, що лікують. Посилаючись на лікування шизофренії, терапевтично ефективна кількість стосується такої кількості, яка призводить до ефекту полегшення до деякої міри (або, переважно, усунення) одного або більше симптомів, пов'язаних з шизофренією. Термін "лікування", як використано в даному документі, якщо не зазначене інше, означає повернення, полегшення, затримка прогресування, або попередження розладу або стану, до якого цей термін застосовується, або одного або більше симптомів такого розладу або стану. Термін "лікування", як використано в даному документі, якщо не зазначене інше, стосується дії лікування, як "лікування", яке визначене безпосередньо вище. Термін "лікування" також включає адьювантне та неоадьювантне лікування суб'єкта. Введення сполук формули I може бути ефективним, використовуючи будь-який спосіб, що забезпечує доставку сполук до місця дії. Дані способи включають пероральні способи, інтраназальні способи, інгаляційні способи, інтрадуодентальні способи, парентеральні ін'єкції (включаючи внутрішньовенну, пудшкірну, внутрішньом'язову, вгутрішньосудинну або інфузію), місцеве та ректальне введення. В одному втіленні за представленим винаходом, сполуки формули I переважно можуть бути ефективними при пероральних способах введення. Схеми прийому лікарського засобу можуть бути скореговані для забезпечення оптимальної бажаної відповіді. Наприклад, можуть вводити одиничний болюс, можуть вводити декілька розділених доз протягом певного часу або дозу можуть пропорційно зменшувати або збільшувати, як показано за гострої необхідності терапевтичної ситуації. Особливо переважним є формулювання парентеральних композицій в дозованій одиничній формі для легкого введення та одноманітності дозування. Дозована одинична форма, як використано в даному документі, стосується фізично дискретних одиниць, прийнятних як одиничних доз для суб'єктівссавців, що підлягають лікуванню; кожна одиниця містить завчасно встановлену кількість активної сполуки, розраховану для одержання необхідного терапевтичного ефекту в поєднанні з необхідним фармацевтичним носієм. Специфікація для дозованих одиничних форм за винаходом продиктована та безпосередньо залежить від (a) унікальних характеристик хіміотерапевтичного агенту та конкретного терапевтичного або профілактичного ефекту, який повинен бути досягнутий, та (b) обмежень, властивих в даній галузі формулювання такої активної сполуки для лікування чутливості у суб'єктів. В одному втіленні за представленим винаходом, сполуки формули I переважно можуть бути застосовані для лікування людей. Слід зазначити, що дозовані значення можуть варіювати від типу та жорсткості умови, щоб призвести до полегшення, та можуть включати одиничну або багаторазові дози. Крім того, слід розуміти, що для будь-якого конкретного суб'єкта, конкретні схеми дозування повинні корегуватися протягом часу, відповідно до індивідуальної необхідності та професійного процесу введення суб'єкту або нагляду за введенням композицій, та такі дозовані діапазони, запропоновані в даному документі, є тільки ілюстративними та не призначені для обмеження меж або здійснення на практиці заявленої композиції. Наприклад, дози можуть корегуватися, ґрунтуючись на фармакокінетичних або фармакодинамічних параметрах, які можуть включати клінічні ефекти, такі як токсичні ефекти та/або лабораторні значення. Таким чином, представлений винахід охоплює підвищення дози у пацієнтів, як визначено кваліфікованим фахівцем. Визначення відповідних дозувань та схем введення хіміотерапевтичного агенту є добре відомою з відповідного рівня техніки, та слід розуміти, що вони охоплюються кваліфікованими фахівцями за умови забезпечення ідей, розкритих в даному документі. Кількість введеної сполук формули I буде залежати від суб'єкту, що піддається лікуванню, тяжкості розладу або стану, швидкості введення, характеру сполуки та розділення призначеного лікарем. Однак, ефективне дозування знаходиться в діапазоні від приблизно 0,01 до приблизно 50 мг на кг маси тіла на деньper, переважно від приблизно 0,01 до приблизно 5 мг/кг/день, в 17 UA 106692 C2 5 10 15 20 25 30 35 одиничній або розділених дозах. Для людини масою 70 кг, ця кількість становила б від приблизно 0,7 мг до приблизно 3500 мг/день, переважно, від приблизно 5 мг до приблизно 2000 мг/день. В деяких випадках, рівні дозувань нижчі нижнього обмеження вищезгаданого діапазону можуть бути більшими, ніж достатні, тоді як в інших випадках ще більші дози можуть застосовуватися без спричинення будь-якого шкідливого побічного ефекту, що забезпечується тим, що більші дози спочатку поділяють на декілька маленьких доз для введення протягом дня. Як використано в даному документі, термін "комбінована терапія" стосується введення сполуки формули I разом з, щонайменше, одним додатковим фармацевтичним або медичним агентом (наприклад, агентом проти шизофренії), або послідовно, або одночасно. Як зазначено вище, сполуки формули I можуть застосовуватися в комбінації з одним або більше додатковими агентами проти шизофренії, які описуються нижче. Коли застосовують комбіновану терапію, один або більше додаткових агентів проти шизофренії можуть вводити послідовно або одночасно зі сполукою за винаходом. В одному втіленні, додатковий агент проти шизофренії вводять ссавцю (наприклад, людині) перед введенням сполуки за винаходом. В іншому втіленні, додатковий агент проти шизофренії вводять ссавцю після введення сполуки за винаходом. В іншому втіленні, додатковий агент проти шизофренії вводять ссавцю (наприклад, людині) одночасно з введенням сполуки за винаходом. Крім того, винахід стосується фармацевтичної композиції для лікування шизофренії у ссавців, включаючи людину, яка містить кількість сполуки формули I, як зазначено вище (включаючи гідрати, сольвати та поліморфи згаданої сполуки або її фармацевтично прийнятної солі), в комбінації з одним або більше (переважно від одного до трьох) агентами проти шизофренії, такими як зипразидон, рисперидон, оланзапін, кветіапін, арипіпразол, азенапін, блонансерин або ілоперидон, де кількості активного агенту та комбінації, коли взяті, як ціле є терапевтично ефективними для лікування шизофренії. Детальний опис винаходу Сполуки формули I можуть бути одержані відповідно до наступних схем реакцій та 1 8 супроводжуючого їх обговорення. Якщо не зазначене інше, з R по R , A та n, та структурна формула I є такими, як визначено вище в схемах реакції та обговоренні, наведеному далі. Загалом сполуки за даним винаходом можуть бути одержані за процесами аналогічними до відомих в хімії з рівня техніки, зокрема, в світлі опису, включеному в даний документ. Конкретні процеси для виробництва сполук за даним винаходом передбачаються як додаткові особливості винаходу та є ілюстративними за наступними схемами реакцій. Інші процеси можуть бути описані в експериментальному розділі. Схема 1 Схема 2 Схема 3 40 Схема 4 18 UA 106692 C2 Схема 5 Схема 6 5 Схема 7 19 UA 106692 C2 Схема 1 стосується одержання сполуки формули I. Звертаючись до схеми 1, сполуки 5 формули I, в яких R є зв'язаним з атомом карбону в групі A, одержують зі сполуки формули II, де "A-X" є 5 10 або та X є H, Cl, Br, I або трифлат, шляхом реакції сполучення, яка каталізується паладієм, 5a 5g використовуючи реагент формули R – R : або 20 UA 106692 C2 5 10 15 20 25 30 35 40 В залежності від типу реакції, що застосовують, Z може представляти собою Br, B(OH) 2 або 5 B(OR)2 або фрагмент триалкілолова. Наприклад, коли X є галогеном або трифлатом та R реагент є бороновою кислотою або бороновим естером, можуть застосовувати реакцію Судзукі [A. Suzuki, J. Organomet. Chem. 1999, 576, 147-168; N. Miyaura and A. Suzuki, Chem. Rev. 1995, 95, 2457-2483; A. F. Littke et al., J. Am. Chem. Soc. 2000, 122, 4020-4028]. Більш конкретно, гетероароматичний йодид, бромід або трифлат формули II змішують з 1-3 еквівалентами арилабо гетероарил- боронової кислоти або боронового естера та прийнятною основою, такою як 25 еквівалентів карбонату натрію, в прийнятному органічному розчиннику, такому як етанол. Додають паладієвий каталізатор, такий як 0,01 еквівалентів тетра(трифенілфосфін)паладію(0), та реакційну суміш нагрівають до температур в діапазоні від 60 до 100 °C протягом від 1 до 24 годин. В деяких випадках переважним може бути застосування 1-2 еквівалентів купруму(І) хлориду та 1-2 еквівалентів калію броміду в реакція Судзукі, в 1,2-диметоксіетані, як розчиннику. Альтернативно, реакцію сполучення можуть виконувати шляхом взаємодії сполуки 5 формули II, де X є H та Z є Br, з 1-3 еквівалентами реагенту (R )-Br, в присутності від 0,01 до 0,5 еквівалентів димеру алілпаладію хлориду та прийнятної основи, такої як 2-4 еквіваленти карбонату калію, в прийнятному органічному розчиннику, такому як 1,4-діоксан. Реакцію можуть проводити при температурах в діапазоні від 100 до 160 ºC протягом від 24 до 72 годин. Коли X є галогеном або трифлатом та Z є триалкілоловом, можуть застосовувати сполучення Стілла [V. Farina et al., Organic Reactions 1997, 50, 1-652]. Більш конкретно, сполуку формули II, де X є 5 бромідом, йодидом або трифлатом, можуть змішувати з 1,5-3 еквівалентами R станану в присутності паладієвого каталізатору, такого як 0,05 еквівалента дихлорбіс(трифенілфосфін)паладію(II), в прийнятному органічному розчиннику, такому як толуол, та реакційну суміш можуть нагрівати до температури в діапазоні від 100 до 130 ºC протягом від 12 до 36 годин. Коли X є Br, I або трифлатом та Z є Br або I, можуть застосовувати сполучення Негіші [E. Erdik, Tetrahedron 1992, 48, 9577-9648]. Більш конкретно, сполука формули II, в якій X є бромідом, йодидом або трифлатом, може бути переметальованою шляхом обробки від 1 до 1,1 еквівалентів реагенту алкіл літію, після чого обробляють розчином 1,2 – 1,4 еквіваленти хлориду цинка у відповідному розчиннику, такому як тетрагідрофуран, при температурі в діапазоні від -80 до -65 ºC. Після нагрівання до температури від 10 до 30 ºC, 5 реакційну суміш можуть обробляти реагентом R -Z, та нагрівають при від 50 до 70 ºC з додаванням каталізатору, такого як тетра(трифенілфосфін)паладію(0). Реакцію можуть проводити протягом діапазонк часу від 1 до 24 годин. Жодна з даних реакцій не обмежується застосуванням розчинника, основи або каталізатору, описаного вище, також можуть зостосовувати багато інших умов. Альтернативно, звертаючись до схеми 1, направленність реакції сполучення з AX1 або AX3 5a 5g з будь-яким з R – R може бути зворотньою. В такому випадку, X група AX1 або AX3 є 5a 5g бороновою кислотою, боронатом або фрагментом-триалкілолово, та Z група R – R є Cl, Br, I або трифлатом. Застосовані хімічні перетворення для створення зв'язку карбон-карбон, є такими ж як ті, що описані вище. 5 Звертаючись до схеми 1, додаткові сполуки формули I, в яких R є приєднаним до атому нітрогену в групі A, одержують зі сполуки формули II, в якій "A-X" є 5a 45 50 5g та X є H, шляхом сполучення, що каталізується купрумом, з реагентом формули з R по R , де Z є групою боронової кислоти або Z є Cl або Br, відповідно до способу P. Y. S. Lam et al., Tetrahedron Lett. 1998, 39, 2941-2944 або способу Z. Xi et al., Tetrahedron 2008, 64, 4254-4259. Схема 2 стосується альтернативного одержання сполуки формули I. Звертаючись до схеми 2 3 3 2, сполуку формули I, в якій R є N(R )2 або HNR , можуть одержувати зі сполуки формули III, в якій L є триазоло або хлором, за реакцією з 1,1-4 еквівалентами первинного або вторинного 3 3 аміну, H2NR або HN(R )2, необов'язково в присутності основи, такї як карбонат цезію, у відповідному органічному розчиннику, такому як дихлорметан або N, N-диметилформамід. Прийнятні температури для згаданих вище реакцій становлять від 0 ºC до 100 ºC. Прийнятний 2 час реакції становить від 20 хвилин до 48 годин. Альтернативно, сполуку формули I, в якій R є арилом або гетероарилом, можуть одержувати зі сполуки формули III, за реакцією з відповідним 21 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 арил- або гетероарил- йодидом, бромідом, похідною триалкілолова, похідною цинку, бороновою кислотою або бороновим естером, як описано для перетворення формули II у формулу I на 2 схемі 1, щоб одержати сполуки формули I. Альтернативно, сполуку формули I, в якій R є алкілом, можуть одержувати зі сполуки формули III, в якій L є хлором, за реакцією з відповідним реагентом цинку в реакції Негіші, як описано вище для перетворення формули II у формулу I на схемі 1. (Дивись також: R. T. Hendricks et al., Bioorg. Med. Chem. Lett. 2009, 19, 410-414.) 2 Альтернативно, сполуку формули I, в якій R є алкілом, циклоалкілом або гетероциклілом, можуть одержувати зі сполуки формули III, в якій L є хлором, за реакцією з відповідним реагентом Гріньяру в присутності ацетиацетонату феруму(III), як описано L.K. Ottesen et al., Organic Lett. 2006, 8, 1771-1773. 2 9 8 Звертаючись до схеми 2, сполуку формули I, в якій R є -O-(C1-C6)алкіл-R або –OR , можуть безпосередньо одержувати зі сполуки формули IV через алкілування з відповідним галогенідом, або за реакцією Міцунобу з необхідним спиртом. Дивись S. B. Bodendiek et al., Eur. J. Med. Chem. 2009, 44, 1838-1852; A. F. Khattab et al., Synth. Commun. 2006, 36, 2751-2761; G. Smith et al., J. Med. Chem. 2008, 51, 8057-8067. Сполуки формули III, в яких L є хлором або 1H-1,2,4-триазол-1-ілом можуть одержувати зі сполуки формули IV обробкою оксихлоридом фосфору, необов'язково в присутності 1H-1,2,4триазолу. Більш конкретно, від 2 до 4 еквівалентів оксихлориду фосфору та від 8 до 11 еквівалентів 1H-1,2,4-триазолу, у відповідному органічному розчиннику, такому як ацетонітрил або дихлорметан, при температурі від -10 до 5 ºC, обробляли 12-15 еквівалентами триетиламіну або N, N-діізопропілетиламіну. Після додавання 1 еквіваленту імідазотриазинону формули IV, реакційну суміш можуть витримувати при температурах в діапазоні від 25 ºC до температури кипіння від 2 до 24 годин, одержуючи сполуку формули III, в якій L є 1H-1,2,4триазолом. Якщо 1H-1,2,4-триазол виключають з реакції, яку, в даному випадку, можуть проводити в толуолі, як розчиннику, продуктом є сполука формули III, в якій L є хлором. Якщо немає необхідності, в усіх випадках не виділяють проміжну сполуку формули III, яка може безпосередньо реагувати з відповідним амінним реагентом. Сполуки формули III, в яких L є три флатом, можуть одержувати зі сполуки формули IV за стандартними способами; дивись B. T. Shireman et al, Bioorg. Med. Chem. Lett. 2008, 18, 2103-2108. Дані реакції не обмежуються застосуванням розчинника або основи, описаних вище, а також багато інших умов можуть бути застосовані. 2 3 3 Схема 3 стосується одержання сполук формули II, в яких R є HNR або N(R )2. Сполуки формули II можуть бути перетворені в сполуки формули I відповідно до способів зі схеми 1. Звертаючись до схеми 3, сполуку формули II можуть одержувати зі сполуки формули V за способами аналогічними до тих, за якими здійснюють перетворення сполуки формули III у сполуку формулу I на схемі 2. Сполуки формули V, в яких L є хлором або 1H-1,2,4-триазол-1ілом, можуть одержувати зі сполук формули VI, в яких X є H, Cl, Br або I, за способами аналогічними до перетворень сполуки формули IV в III на схемі 2. 2 3 Схема 4 стосується альтернативного одержання сполук формули II, в яких R є HNR або 3 N(R )2 та X є H або Cl. Сполуки формули II можуть бути перетворені в сполуки формули I відповідно до способів зі схеми 1. Звертаючись до схеми 4, сполуки формули II можуть одержувати з бромвмісної сполуки формули VII за реакцією сполучення, яка каталізується паладієм, з відповідно заміщеної гетероароматичної сполуки формули ZAX: Сполука формули II, X є H в сполуках ZAX1 та ZAX3; в ZAX2, X може бути H або відповідна захисна група для нітрогену, добе відома кваліфікованому фахівцю в даній галузі з рівня техніки, така як Boc, п-метоксибензил, аліл або 2-(триметилсиліл)етокси]метил. Коли Z є B(OH) 2 або B(OR)2, сполучення зв'язку карбон-карбон можуть виконувати при умовах, описаних вище для реакції Судзукі. Кваліфікований фахівець в даній галузі розумітиме, що дана хімія також 5 буде ефективною, якщо X є R ; в даному випадку, продуктом буде сполука формули I. Сполуку 2 3 3 формули VII, в якій R є HNR або N(R )2 можуть одержувати зі сполуки формули VIII за способами аналогічними перетворенню сполук формули III в сполуки формули I на схемі 2. 22 UA 106692 C2 5 10 15 20 25 30 35 40 Сполуку формули VIII можуть одержувати зі сполуки формули IX за способами аналогічними перетворенню сполук формули IV в сполуки формули III на схемі 2. Схема 5 стосується одержання сполук формули IV. Сполуки формули IV можуть бути перетворені в сполуки формули I відповідно до способів зі схеми 2. Звертаючись до схеми 5, сполуку формули IV можуть одержувати зі сполуки формули VI, в якій X є H, Cl, Br, I, трифлатом, бороновою кислотою, боронатом або триалкілоловом за тим самим способом, як описано для перетворення сполуки формули II в сполуку формули I на схемі 1. Схема 6 стосується одержання сполук формули VI, в яких "A-X" є та X є H, Cl, Br, I, трифлатом, бороновою кислотою, боронатом або триалкілоловом. Сполука формули VI може бути перетворена в сполуку формули I, застосовуючи способи, описані в схемі 3, потім схемі 1 або схемі 5, потім схемі 2. Звертаючись до схеми 6, сполуку формули VI можуть одержувати зі сполуки формули X, дією від 1,1 до 3 еквівалентів 1,1’карбонілдіімідазолу або 1,1’-карбонілди(1,2,4-триазолу) в розчиннику, такому як 1,4-діоксан або тетрагідрофуран, при температурах в діапазоні від 40 до 70 ºC протягом від 1 до 4 годин. Сполуку формули X можуть одержувати зі сполуки формули XI обробкою від 2 до 5 еквівалентів формамідинацетату в розчиннику, такому як 2-бутанол, при температурах в діапазоні від 60 до 100 ºC протягом від 1 до 12 годин. Сполуку формули XI можуть одержувати 1 1 зі сполуки формули XII шляхом видалення захисної групи P , в яких P може бути –(C=O)арилом, -(C=O)-алкілом, -(C=O)O-(C1-C4)алкілом або іншою відповідною захисною групою, відомою кваліфікованому фахівцю в даній галузі з рівня техніки, шляхом основного гідролізу 1 амідної або карбаматної групи, або, у випадку, в якому P є –(C=O)O-трет-бутилои, реакцією з надлишком трифлуороцтової кислоти в дихлорметановому розчиннику, при температурі в діапазоні від 15 до 35 ºC. Сполуку формули XII можуть одержувати зі сполуки формули XIII, в якій X є H, Cl, Br, I, трифлатом, бороновою кислотою, боронатом або триалкілоловом, та в якій 1 LG є Cl, Br або I, за реакцією з 1,1-2 еквівалентами N-захищеної R -імідогідразидної сполуки формули XIX 1 в якій P є –(C=O)-арилом, -(C=O)-алкілом, -(C=O)O-(C1-C4)алкілом або іншоювідповідною захисною групою, відомою кваліфікованому фахівцю в даній галузі з рівня техніки. Дану реакцію можуть проводити в розчиннику, такому як 2-метилтетрагідрофуран та/або 1,2-диметоксіетан при температурах в діапазоні від 60 до 90 ºC, в присутності основи, такої як від 2 до 4 еквівалентів N, N-діізопропілетиламіну. Імідогідразидний реагент XIX можуть одержувати за реакцією необхідного ацилгідразину з відповідним іміноетером, відповідно до способу D. Hurtaud et al., Synthesis 2001, 2435-2440. Схема 7 стосується одержання сполук формули VI, в яких X є H або Cl. Сполуки формули VI можуть бути перетворені в сполуки формули I відповідно до способів, описаних на схемі 3, потім на схемі 1 або на схемі 5, потім на схемі 2. Сполуку формули IX можуть застосовувати для одержання сполуки формули I, як описано на схемі 4, потім на схемі 1. Звертаючись до схеми 7, сполуку формули VI можуть синтезувати зі сполуки формули IX за реакцією, що каталізується паладієм, з відповідно заміщеною гетероароматичною сполукою формули ZAX 23 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 В даному випадку, X є H або Cl в сполуках ZAX1 та ZAX3; в ZAX2, X може бути H або відповідною захисною групою для нітрогену, добре відомою кваліфікованому фахівцю в даній галузі з рівня техніки, такою як BOC, п-метоксибензил, аліл або 2-(триметилсиліл)етокси]метил; Z є B(OH)2 або B(OR)2. Реакцію сполучення карбон-карбон можуть проводити за подібним способом до того, який описаний для перетворення сполуки VII в сполуку формули II на схемі 4. 2 Сполуку формули IX можуть одержувати за реакцією сполуки формули XIV, в якій P є (C1C4)алкілом, з 1-30 еквівалентами формаміду, при температурах в діапазоні від 100 до 180 ºC протягом від 2 до 20 годин. Сполуку формули XIV можуть одержувати зі сполуки формули XV шляхом депротонування з основою, такою як літію біс(триметилсиліл)амід, та наступним амінуванням з реагентом, таким як O-(4-нітробензоїл)гідроксиламін або O(дифенілфосфініл)гідроксиламін. Обережно: O-(дифенілфосфініл)гідроксиламін є високо енергетичною речовиною, що показує здатність розкладатися з вибухом за умов навколишнього середовища. ЇЇ застосування повинно ретельно перевірятися. Сполуку формули XV можуть одержувати шляхом бромування сполуки формули XVI відповідно до способу T. L Grange et al., Tetrahedron Lett. 2007, 48, 6301-6303, застосовуючи бром в розчиннику, такому як N, Nдиметилформамід при температурах в діапазоні від 60 до 90 ºC, в присутності основи, такої як бікарбонат калію. Сполуки формули XVI можуть бути утворені шляхом циклізації сполуки формули XVII, виконаної, наприклад, при нагріванні в мікрохвильовому реакторі при 150 до 190 ºC протягом від 30 хвилин до 3 годин, у відповідному інертному розчиннику, такому як 1,4діоксан. Сполуки формули XVII одержують за реакцією пропінатного естеру з N'гідроксіімідаміду формули XVIII, яку можуть проводити при температурі кипіння зі зворотним холодильником в розчиннику, такому як метанол або етанол, протягом періоду від 2 до 24 годин. Сполуки формули XVIII легко одержують з відповідних нітрилів, як повідомлено в X. Yang et al., J. Med. Chem. 2010, 53, 1015-1022. Сполуки формули I, які мають хіральні центри, можуть існувати у вигляді стереоізомерів, таких як рацемати, енантіомери або діастереомери. Тадиційні методики одержання/виділення індивідуальних енантіомерів включають хіральний синтез з прийнятного оптично чистого прекурсору або розділення рацемату, використовуючи, наприклад, хіральну високоефективну рідинну хроматографію (ВЕРХ). Альтернативно, рацемат (або рацемічний прекурсор) можуть піддавати взаємодії з прийнятною оптично активною сполукою, наприклад, спиртом, або, у випадку, коли сполука містить кислотний або основний фрагмент, кислту або основу, таку як винну кислоту або 1-фенілетиламін. Одержану в результаті діастереомерна суміш може бути розділена, використовуючи хроматографію та/або фракційну кристалізацію та один або обидва діастереоізомери перетворюють у відповідний(і) чистий(і) енантіомер(и) способами, добре відомими кваліфікованому фахівцю в даній галузі з рівня техніки. Хіральні сполуки формули I (та їх хіральні прекурсори) можуть одержувати в енантіомерно-збагаченій формі, використовуючи хроматографію, як правило ВЕРХ, на асиметричних смолах з рухомою фазою, що складається з вуглеводню, як правило, гептану або гексану, що містить від 0 до 50 % ізопропанолу, як правило, від 2 до 20 %, та від 0 до 5 % алкіламіну, як правило 0,1 % діетиламіну. Концентрація елюату забезпечує збагачену суміш. Стереоізомерні конгломерати можуть розділяти за традиційними методиками, відомими кваліфікованому фахівцю в даній галузі з рівня техніки. Дивись, наприклад "Stereochemistry of Organic Compounds" by E. L. Eliel (Wiley, New York, 1994), розкриття якого включене в даний документ у вигляді посилання в повному об'ємі. Прийнятні стерео селективні методики є добре відомими кваліфікованому фахівцю в даній галузі з рівня техніки. Коли сполука формули I містить алкеніл або алкеніленову групу, геометричні цис/транс (або Z/E) ізомери є можливими. Цис/транс ізомери можуть бути розділені, використовуючи традиційні методики, добре відомі кваліфікованому фахівцю в даній галузі з рівня техніки, наприклад, хроматографію та фракційну кристалізацію. Солі за представленим винаходом можуть бути одержані відповідно до способів, відомих кваліфікованому фахівцю в даній галузі з рівня техніки. 24 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 55 60 Сполуки формули I, які в природі є основними, здатні до утворення широкої різноманітності солей з різними неорганічними та органічними кислотами. Хоча такі солі повинні бути фармацевтично прийнятними для введення тваринам, часто на практиці є необхідним спочатку виділити сполуку за представленим винаходом з реакційної суміші, як фармацевтично неприйнятну сіль, та потім легко перетворити останню назад у сполуку у вигляді вільної основи шляхом обробки лужним реагентом та наступного перетворення останньої вільної основи у фармацевтично прийнятну кислу адитивну сіль. Кислі адитивні солі основних сполук за даним винаходом можуть одержувати шляхом обробки основної сполуки, в значній мірі, еквівалентною кількістю вибраної мінеральної або органічної кислоти у водному середовищі розчинника або в прийнятному органічному розчиннику, такому як метанол або етанол. При випаровуванні розчинника, одержують бажану тверду сіль. Бажану кислу сіль також можуть осаджувати з розчину вільної основи в органічному розчиннику шляхом додавання до розчину мінеральної або органічної кислоти. Якщо заявлена сполука є основою, бажану фармацевтично прийнятну сіль можуть одержувати будь-яким прийнятним способом, доступним з рівня техніки, наприклад, обробкою вільної основи неорганічною кислотою, такою як гідрохлоридна кислота, гідробромідна кислота, сульфатна кислота, нітратна кислота, фосфорна кислота тощо, або органічною кислотою, такою як оцтова кислота, малеїнова кислота, бурштинова кислота, мигдалева кислота, фумарова кислота, малонова кислота, піровиноградна кислота, щавелева кислота, гліколева кислота, саліцилова кислота, ізонікотинова кислота, оцтова кислота, молочна кислота, пантотенова кислота, бівинна кислота, аскорбінова кислота, 2,5-дтгідроксибензойна кислота, фумарова кислота, глюконова кислота, цукрова кислота, мурашина кислота, мутансульфонова кислота, етансульфонова кислота, бензолсульфонова кислота, п-толуолсульфонова кислота та памоєві [тобто, 1,1’-метилен-біс-(2-гідрокси-3-нафтоат)] кислоти, піранозидилова кислота, така як глюкуронова кислота або галактуронова кислота, альфа-гідроксикислота, така як лимонна кислота або винна кислота, амінокислота, така як аспарагінова кислота або глутамінова кислота, ароматична кислота, така як бензойна кислота або корична кислота, сульфонова кислота, така як п-толуолсульфонова кислота або етансульфонова кислота, тощо. Дані сполуки формули I, які в природі є кислотними, здатні утворювати основні солі з різними фармакологічно прийнятними катіонами. Приклади таких солей включають солі лужних металів та лужно-земельних металів, та зокрема, соді натрію та калію. Всі дані солі одержують за традиційними методиками. Хімічні основи, які застосовують як реагенти для одержання фармацевтично прийнятних основних солей за винаходом, є такими, які утворюють нетоксичні основні солі з кислотними сполуками формули I. Такі солі можуть одержувати за будь-яким прийнятним способом, наприклад, обробкою вільної кислоти неорганічною або органічною основою, такою як амін (первинний, вторинний або третинний), гідроксидом лужного металу або гідроксидом лужно-земельного металу, тощо. Крім того, дані солі можуть одержувати обробкою відповідних кислотних сполук водними розчинами, що містять бажані фармакологічно прийнятні катіони, та потім випаровуванням отриманого в результаті розчину насухо, переважно при зниженому тиску. Альтернативно, крім того, їх можуть одержувати шляхом змішування разом розчинів кислотних сполук в нижчих спиртах та алкоксидів лужних металів, та наступним випаровуванням одержаного в результаті розчину насухо, за тим самим способом як і раніше. В іншому випадку, переважно застосовують стехіометричні кількості реагентів з метою забезпечення повноти проходження реакції та максимального виходу потрібного кінцевого продукту. Крім того, винахід включає ізотопно мічені сполуки формули I, в яких один або більше атомів замінені на атом, який має той самий атомний номер, але атомна маса або масове число відрізняється від атомної маси або масового числа, що зазвичай зустрічається в природі. Ізотопно мічені сполуки формули I, як правило, можуть одержувати за традиційними методиками, відомими кваліфікованому фахівцю в даній галузі з рівня техніки або за процесами аналогічними до тих, які описані в даному документі, застосовуючи відповідний ізотопно мічений реагент замість неміченого реагента в інших випадках застосування. В наступних прикладах та одержаннях "ДМСО" означає диметилсульфоксид, "N" означає нормальний, "M" означає молярний, "мл" означає мілілітр, "ммоль" означає мілімолі, "мкмоль" означає мікромолі, "екв.” означає еквівалент, "ºC" означає градуси за Цельсієм, "Pa" означає паскалі, "УФ" означає ультрафіолет, "Мгц" означає мегагерц. Експериментальні методики Експерименти, як правило, проводили в інертній атмосфері (азот або аргон), зокрема у випадках, коли застосовували оксиген- або волого-чутливі реагенти або проміжні сполуки. Комерційнодоступні розчинники та реагенти, як правило, застосовували без додаткової очистки, 25 UA 106692 C2 TM 5 10 15 20 25 30 35 40 45 50 включаючи безводні розчинники, де підходило (як правило, Sure-Seal продукти від фірми Aldrich Chemical Company, Milwaukee, Wisconsin). Продукти, як правило, сушили в вакуумі перед виконанням наступних реакцій або проведення біологічних досліджень. Дані мас-спектрометрії одержували або використовуючи рідинну хроматографію – мас-спектрометрію (РХ-МС), хімічну іонізацію при атмосферному тиску (ХІАТ) або газову хроматографію - мас-спектрометрію (ГХМС). Дані хімічних зсувів в ядерно-магнітному резонансі (ЯМР) представляли в мільйонних частках (м.ч., δ) по відношенню до залишкових піків дейтерованих розчинників, які застосовувались. Для синтезів за методиками, на які посилаються в інших прикладах або способах, умови реакції (тривалість реакції та температура) можуть змінюватися. Як правило, реакції проводили з наступною тонко-шаровою хроматографією або мас-спектрометрією, та піддавали обробці, коли необхідно. Очистки можуть змінюватися між експериментами: як правило, розчинники та співвідношення розчинників, яке використовують для елюєнтів/градієнтів, вибирали, щоб забезпечити відповідні Rf або час утримання. Приклад 1 4-(Азетидин-1-іл)-7-метил-5-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]імідазо[5,1f][1,2,4]триазин Стадія 1. Синтез 2-бром-1-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]етанону A. Одержання 1-метил-5-(4-метилфеніл)-1H-піразолу (1-Метил-1H-піразол-5-іл)боронову кислоту (2,0 г, 16 ммоль), 1-бром-4-метилбензол (1,96 мл, 15,9 ммоль), карбонат натрію (5,05 г, 47,6 ммоль) та дихлорбіс(трифенілфосфін)паладію(II) (557 мг, 0,794 ммоль) змішували в суміші з водою (20 мл) та 1,2-диметоксіетану (100 мл), та нагрівали при 80 ºC протягом 18 годин. Після того, як реакційну суміш охолоджували, її фільтрували через целіт, та концентрували в вакуумі. Залишок розподіляли між водою та етилацетатом, та водний шар екстрагували додатковим етилацетатом. Об'єднані органічні шари сушили над сульфатом магнію, фільтрували та концентрували під зниженим тиском. Хроматографія на силікагелі (Градієнт: від 0 % до 50 % етилацетат в гептані) давала продукт у 1 вигляді жовтої олії. Вихід: 1,15 г, 6,68 ммоль, 42 %, РХ-МС m/z 173,1 (M+1). H ЯМР (400 Мгц, CDCl3) δ 2,42 (с, 3H), 3,89 (с, 3H), 6,29 (д, J=2,0 Гц, 1H), 7,30 (ш AB квартет, J AB=8 Гц, ΔνAB=18 Гц, 4H), 7,51 (д, J=1,9 Гц, 1H). B. Одержання 4-йод-1-метил-5-(4-метилфеніл)-1H-піразолу N-Йодсукцинімід (95 %, 756 мг, 3,19 ммоль) додавали до розчину 1-метил-5-(4-метилфеніл)1H-піразолу (500 мг, 2,90 ммоль) в ацетонітрилі (15 мл), та реакції давали перемішуватися протягом 1 години при 85 ºC. Видалення розчинника в вакуумі давало залишок, який хроматографували на силікагелі (Градієнт: 20 % - 50 % етилацетат в гептані), даючи продукт у 1 вигляді коричневої олії. Вихід: 630 мг, 2,11 ммоль, 73 %. РХ-МС m/z 299,2 (M+1). H ЯМР (400 Мгц, CDCl3) δ 2,44 (ш с, 3H), 3,83 (с, 3H), 7,26-7,33 (м, 4H), 7,57 (с, 1H). C. Одержання 1-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]етанону Трибутил(1-етоксивініл)станан (95 %, 1,39 мл, 3,88 ммоль) додавали до суміші 4-йод-1метил-5-(4-метилфеніл)-1H-піразолу (768 мг, 2,58 ммоль), тетра(трифенілфосфін)паладію(0) (298 мг, 0,258 ммоль) та літію хлориду (98 %, 279 мг, 6,45 ммоль) в N, N-диметилформаміді (20 мл), та реакцію перемішували при 90 ºC протягом 18 годин. Після охолодження, суміш фільтрували через целіт, та концентрували в вакуумі; хроматографія на силікагелі (Градієнт: 10 % - 50 % етилацетат в гептані) давала продукт у вигляді безбарвної олії. Вихід: 460 мг, 2,15 1 ммоль, 83 %. РХ-МС m/z 215,3 (M+1). H ЯМР (400 Мгц, CDCl3) δ 2,17 (с, 3H), 2,45 (ш с, 3H), 3,69 (с, 3H), 7,28 (ш AB квартет, JAB=8 Гц, ΔνAB=28 Гц, 4H), 7,99 (с, 1H). D. Синтез 2-бром-1-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]етанону Бром (97 %, 0,104 мл, 1,97 ммоль) додавали до розчину 1-[1-метил-5-(4-метилфеніл)-1Hпіразол-4-іл]етанону (420 мг, 1,96 ммоль) в крижаній оцтовій кислоті (10 мл), та реакційну суміш енергійно струшували протягом 2 годин при 80 ºC. Після видалення розчинника під зниженим тиском, залишок розбавляли етилацетатом, промивали насиченим водним розчином 26 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 55 60 бікарбонату натрію, промивали насиченим розчином хлориду натрію та сушили над сульфатом натрію. Фільтрування та концентрування фільтрату в вакуумі давало залишок, який чистили, використовуючи хроматографію на силікагелі (Градієнт: 10 % - 30 % етилацетат в гептані), одержуючи продукт у вигляді безбарвної олії. Вихід: 353 мг, 1,20 ммоль, 61 %. РХ-МС m/z 293,1 1 (M+1). H ЯМР (400 Мгц, CDCl3) δ 2,46 (с, 3H), 3,71 (с, 3H), 3,97 (с, 2H), 7,31 (ш AB квартет, JAB=8 Гц, ΔνAB=23 Гц, 4H), 8,05 (с, 1H). Стадія 2. Синтез N'-етанімідоїлацетогідразиду Суміш гідроксиду натрію (2,59 г, 64,8 ммоль) в безводному етанолі (300 мл) перемішували протягом 20 хвилин при 50 ºC, щоб розчинився. Розчин охолоджували до 0 ºC, та поступово додавали етилетанімідоату гідрохлорид (8,0 г, 65 ммоль); осаджені солі видаляли фільтруванням, та фільтрат обробляли ацетогідразидом (4,80 г, 64,8 ммоль) при кімнатній температурі. Дану суміш нагрівали до 80 ºC протягом 10 хвилин, потім давали охолонути протягом 18 годин. Осад збирали фільтруванням та промивали діетиловим етером, одержуючи 1 продукт у вигляді твердої білої речовини. Вихід: 4,4 г, 38 ммоль, 59 %. H ЯМР (400 Мгц, ДМСОd6), характеристичні піки: δ 1,78 (с, 3H), 1,95 (с, 3H). Стадія 3. Синтез N-{2-метил-4-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]-1H-імідазол-1іл}ацетамід N'-Етанімідоїлацетогідразид (147 мг, 1,28 ммоль) та натрію бікарбонат (99 %, 181 мг, 2,13 ммоль) додавали до розчину 2-бром-1-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]етанону (250 мг, 0,853 ммоль) в ацетонітрилі (9 мл), та суміш нагрівали при 80 ºC протягом 3 годин. Реакційній суміші давали охолонути до кімнатної температури, та потім розбавляли дихлорметаном та фільтрували через целіт. Фільтрат концентрували в вакуумі, та залишок чистили, використовуючи хроматографію на силікагелі (елюєнт: 10 % метанол дихлорметані), одержуючи продукт у вигляді жовтої олії. Вихід: 236 мг, 0,763 ммоль, 89 %. РХ-МС m/z 310,5 1 (M+1). H ЯМР (400 Мгц, CDCl3), передбачається, що є сумішшю ротамерів: δ 2,10 та 1,77 (2 с, 3H), 2,25 та 2,36 (2 с, 3H), 2,44 та 2,46 (2 с, 3H), 3,69 та 3,72 (2 с, 3H), 6,21 (с, 1H), 7,22-7,33 (4H, м, передбачається; частково прихований піком розчинника), 7,96 (ш с, 1H). Стадія 4. Синтез 2-метил-4-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]-1H-імідазол-1-аміну Водну гідрохлоридну кислоту (1 N, 7,0 мл) додавали до розчину N-{2-метил-4-[1-метил-5-(4метилфеніл)-1H-піразол-4-іл]-1H-імідазол-1-іл}ацетаміду (236 мг, 0,763 ммоль) в метанолі (1,0 мл), та суміш нагрівали при кип'ятінні зі зворотним холодильником протягом 30 хвилин. Додавали додаткову кількість 1 N водної гідрохлоридної кислоти (2,0 мл), та нагрівання продовжували протягом додаткових 30 хвилин. Після охолодження, розчин підлужнювали 1 N водним розчином гідроксиду натрію, та суміш двічі екстрагували етилацетатом, що містить 1 % метанолу. Об'єднані органічні шари промивали насиченим водним розчином натрію хлориду, сушили над сульфатом натрію, фільтрували та концентрували в вакуумі, одержуючи продукт у вигляді жовтої твердої речовини. Вихід: 148,5 мг, 0,5555 ммоль, 73 %. РХ-МС m/z 268,5 (M+1). 1 H ЯМР (400 Мгц, CDCl3) δ 2,39 (с, 3H), 2,45 (ш с, 3H), 3,70 (с, 3H), 4,45 (ш с, 2H), 6,26 (с, 1H), 7,24-7,32 (м, 4H, передбачається, що частково прихований піком розчинника), 7,97 (с, 1H). Стадія 5. Синтез N-{2-метил-4-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]-1H-імідазол-1іл}імідоформаміду Етилімідоформату гідрохлорид (608 мг, 5,55 ммоль) додавали до розчину 2-метил-4-[1метил-5-(4-метилфеніл)-1H-піразол-4-іл]-1H-імідазол-1-аміну (148 мг, 0,554 ммоль) в етанолі (5 мл), та реакційну суміш нагрівали при 75 ºC протягом 66 годин. Додавали додатковий етилімідоформату гідрохлорид (300 мг, 2,74 ммоль), та нагрівання продовжували протягом 8 годин. Остаточно додавали етилімідоформату гідрохлорид (300 мг, 2,74 ммоль) після чого реакційну суміш витримували при 75 ºC протягом додаткових 18 годин. Реакційну суміш охолоджували, концентрували в вакуумі та розбавляли етилацетатом. Даний органічний шар промивали насиченим водним розчином бікарбонату натрію, промивали насиченим водним розчином хлориду натрію та сушили над сульфатом натрію. Фільтрування та видалення розчинника під зниженим тиском, з наступною очисткою, використовуючи хроматографію на силікагелі (елюєнт: 10 % метанол в дихлорметані), давали продукт у вигляді жовтої твердої 1 речовини. Вихід: 70 мг, 0,24 ммоль, 43 %. РХ-МС m/z 295.5 (M+1). H ЯМР (400 Мгц, CD3OD), передбачається, що це суміш ротамерів або таутомерів: δ 2,20 та 2,25 (2 с, 3H), 2,43 (ш с, 3H), 3,68 (с, 3H), 6,14 та 6,30 (2 с, 1H), 7,26-7,30 (м, 3H), 7,35 (ш д, J=8 Гц, 2H), 7,84 та 7,81 (2 с, 1H). Стадія 6. Синтез 7-метил-5-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]імідазо[5,1f][1,2,4]триазин-4(3H)-ону Натрію гідрид (60 % дисперсія в мінеральній олії, 24 мг, 0,60 ммоль) додавали до розчину N{2-метил-4-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]-1H-імідазол-1-іл}імідоформаміду (70 мг, 0,24 ммоль) в 1,4-діоксані (4,0 мл), та суміш нагрівали при 75 ºC протягом 10 хвилин. Реакційну 27 UA 106692 C2 5 10 15 20 25 30 35 40 45 50 суміш охолоджували, обробляли 1,1’-карбонілдіімідазолом (135 мг, 0,833 ммоль), давали перемішуватися при кімнатній температурі протягом 30 хвилин, та потім нагрівали до 100 ºC протягом 18 годин. Далі реакційну суміш охолоджували до кімнатної температури, гасили водою та розбавляли етилацетатом. Органічний шар промивали водою, потім насиченим водним розчином натрію хлориду, сушили над сульфатом натрію, фільтрували та концентрували в вакуумі. Хроматографія на силікагелі (Градієнт: 0 % - 10 % метанол в етилацетаті) давала продукт у вигляді твердої білої речовини. Вихід: 55 мг, 0,17 ммоль, 71 %. РХ-МС m/z 321,5 1 (M+1). H ЯМР (400 Мгц, ДМСО-d6) δ 2,34 (ш с, 3H), 2,36 (с, 3H), 3,71 (с, 3H), 7,22 (ш д, J=8 Гц, 2H), 7,30 (д, J=8,2 Гц, 2H), 7,79 (с, 1H), 7,95 (с, 1H). Стадія 7. Синтез 7-метил-5-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]-4-(1H-1,2,4-триазол1-іл)імідазо[5,1-f][1,2,4]триазину 1H-1,2,4-Триазол (162 мг, 2,34 ммоль) розтирали, змішували з дихлорметаном (4,0 мл) та охолоджували до 0 ºC. Додавали фосфору оксихлорид (58,2 мкл, 0,624 ммоль), потім через 1 хвилину по краплям додавали триетиламін (0,349 мл, 2,50 ммоль). Через 10 хвилин при 0 ºC видаляли крижану баню; через 5 хвилин додавали 7-метил-5-[1-метил-5-(4-метилфеніл)-1Hпіразол-4-іл]імідазо[5,1-f][1,2,4]триазин-4(3H)-он (50 мг, 0,16 ммоль). Реакційну суміш витримували при кімнатній температурі протягом 4 годин, потім охолоджували до 0 ºC та гасили водою, потім обробляли насиченим водним розчином бікарбонату натрію. Суміш екстрагували етилацетатом, та об'єднані органічні шари промивали водою, промивали насиченим водним розчином натрію хлориду, сушили над сульфатом натрію, фільтрували та концентрували в вакуумі. Дану сиру речовину безпосередньо використовували на наступній стадії. РХ-МС m/z 1 372,5 (M+1). H ЯМР (400 Мгц, ДМСО-d6) δ 2,27 (ш с, 3H), 2,70 (с, 3H), 3,73 (с, 3H), 6,86 (ш д, J=8,2 Гц, 2H), 7,06 (ш д, J=8,0 Гц, 2H), 7,37 (с, 1H), 8,14 (с, 1H), 8,53 (с, 1H), 8,84 (с, 1H). Стадія 8. Синтез 4-(азетидин-1-іл)-7-метил-5-[1-метил-5-(4-метилфеніл)-1H-піразол-4іл]імідазо[5,1-f][1,2,4]триазину Азетидин (27,0 мкл, 0,400 ммоль) та цезію карбонат (97 %, 202 мг, 0,601 ммоль) додавали до розчину 7-метил-5-[1-метил-5-(4-метилфеніл)-1H-піразол-4-іл]-4-(1H-1,2,4-триазол-1іл)імідазо[5,1-f][1,2,4]триазину (речовина з попередньої реакції,
ДивитисяДодаткова інформація
Назва патенту англійськоюImidazo[5,1-f][1,2,4]triazines for the treatment of neurological disorders
Автори англійськоюChappie, Thomas Allen, Humphrey, John Michael, Verhoest, Patrick Robert, Yang Eddie, Helal, Christopher John
Автори російськоюЧаппи Томас Аллен, Умфрей Джон Майкл, Вергоест Патрик Роберт, Янг Эдди, Гелал Кристофер Джон
МПК / Мітки
МПК: C07D 487/04, A61K 31/53, A61P 25/18
Мітки: імідазо[5,1-f][1,2,4]триазини, розладів, лікування, неврологічних
Код посилання
<a href="https://ua.patents.su/66-106692-imidazo51-f124triazini-dlya-likuvannya-nevrologichnikh-rozladiv.html" target="_blank" rel="follow" title="База патентів України">Імідазо[5,1-f][1,2,4]триазини для лікування неврологічних розладів</a>
Попередній патент: Спосіб виробництва здобного печива “цілюще зернятко”
Наступний патент: Оздоблювальний профіль для віконних і дверних прорізів
Випадковий патент: Підсилювач постійного струму