Сполука 1,1-діетилкарбокси-2-трифторметил-2-(5′-нітроуридил-1′-)-етилен з потенційними фізіологічними властивостями
Формула / Реферат
Сполука 1,1-діетилкарбокси-2-трифторметил-2-(5'-нітроуридил-1'-)-етилен з потенційними фізіологічними властивостями загальної формули:
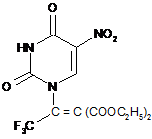 .
.
Текст
Реферат: Сполука 1,1-діетилкарбокси-2-трифторметил-2-(5'-нітроуридил-1'-)-етилен фізіологічними властивостями загальної формули: O NO2 HN N O F3 C С = С (СOOС2H5)2 . з потенційними UA 108908 U (54) СПОЛУКА 1,1-ДІЕТИЛКАРБОКСИ-2-ТРИФТОРМЕТИЛ-2-(5'-НІТРОУРИДИЛ-1'-)-ЕТИЛЕН ПОТЕНЦІЙНИМИ ФІЗІОЛОГІЧНИМИ ВЛАСТИВОСТЯМИ UA 108908 U UA 108908 U 5 10 15 20 25 30 35 40 45 50 55 Корисна модель належить до хімії гетероциклічних сполук, а саме до 1,1-діетилкарбокси-2трифторметил-2-(5'-нітроуридил-1'-)-етилен (далі сполука) з потенційними фізіологічними властивостями та високою реакційною здатністю, які можуть проявлятися за рахунок наявності в будові молекули спряженої системи: подвійних зв'язків гетероциклічного ядра, груп С=О у складі ефірних фрагментів, етиленового зв'язку та при електронегативному впливі на молекулу з боку атомів фтору та нітрогрупи. Структурні аналоги сполуки 1,1-діетилкарбокси-2-трифторметил-2-(5'-нітроуридил-1'-)етилен в літературі не описані, але різноманітні синтези нових похідних урацилу дозволили отримати оригінальні фізіологічно активні речовини, як свідчать літературні джерела. Після синтезу похідних урацилу, а особливо 5-фторурацилу та фторафуру, які продемонстрували високу протипухлинну активність, значно зросла кількість досліджень з цього напрямку. Стало відомо, що пухлини використовують молекули урацилу активніше, ніж нормальні клітини. Оскільки вандерваальсові радіуси водню та фтору близькі, можна очікувати, що 5фторурацил (або його похідне) буде виконувати роль субстрату та/або інгібітору ферментів і буде переважно поглинатися тканинами пухлини. З іншого боку, молекули 5-(6)-заміщеного та/або незаміщеного урацилу та його похідних, інших галогеновмісних гетероциклів, здатні виконувати роль фтор(галоген)вмісних синтонів в органічному синтезі з метою створення оригінальних біологічно активних молекул. Введення фтор(галоген)вмісних фармакофорів в гетероциклічну молекулу призводить до підвищення розчинності сполук в ліпідах та робить лікарські засоби ефективнішими у зв'язку із легкістю їх транспорту в організмі [1, 2]. Авторами роботи [3] описано метод введення при використанні доступного фторотану фармакофорної групи -CF2CHBrCl до аліфатичного ланцюга та ароматичного кільця з метою синтезу біологічно активних сполук з поліфторалкоксигрупами. В роботі [4] описано метод синтезу 1,1-диціано-2-хлор-2-трифторметилетилену, який за хімічною будовою подібний до сполуки корисної моделі, та синтезований реакцією ацилювання маломодинітрилу метиловим ефіром трифтороцтової кислоти в присутності метилату натрію з послідуючою обробкою продукту першої стадії реакції п'ятихлористим фосфором. Раніше, як описано в роботі [5], автором була синтезована оригінальна сполука - біс-аддукт 1,1'-(2"-бром-2"-хлоретеніл)-біс-(5-фторурацил) в умовах міжфазного каталізу дибензо-18-краун6-ефіром в лужному середовищі, яка має протипухлинну активність на моделях експериментального пухлинного зросту різного гістогенезу: Лімфосаркомі Пліса, Карциномі Герена, Саркоми 45. Даний модифікований метод синтезу перенесено нами на молекулу 5-нітроурацилу з метою отримання сполуки 1,1'-діетилкарбокси-2-трифторметил-2-(5'-нітроуридил-1'-)-етилен з потенційними фізіологічними властивостями. Сполука 1,1-діетилкарбокси-2-трифторметил-2-(5'-нітроуридил-1'-)-етилен синтезована з метою отримання нового поліфункціонального фторвмісного синтону для подальшого вивчення її фізико-хімічних та біологічних властивостей, а також дослідження можливості проходження хімічних реакцій між урацилами та фторвмісними реагентами, наприклад, з новим хімічно активним реагентом 1,1-діетилкарбокси-2-хлор-2-трифторметилетиленом. Сполука 1,1-діетилкарбокси-2-трифторметил-2-(5'-нітроуридил-1'-)-етилен поліфункціональна, містить в молекулі одночасно з атомами фтору, подвійний зв'язок, дві складноефірні групи, гетероциклічне ядро та нітрогрупу, тому здатна виконувати роль фтор(галоген)вмісних синтонів в органічному синтезі з метою створення оригінальних складних забудовою біологічно активних молекул. В основу корисної моделі поставлено хімічну будову молекули сполуки 1,1-діетилкарбокси2-трифторметил-2-(5'-нітроуридил-1'-)-етилен з потенційними фізіологічними властивостями, яка отримана реакцією нуклеофільного заміщення між 5-нітроурацилом, що виконує роль нуклеофільного реагенту, та 1,1-діетилкарбокси-2-хлор-2-трифторметилетиленом, в молекулі якого атом хлору активовано двома діетилкарбоксигрупами, в системі безводних розчинників (піридин-диметилформамід) в присутності триетиламіну безводного як галогенвіднімаючого агенту. 1,1-діетилкарбокси-2-хлор-2-трифторметилетилен синтезовано реакцією ацилювання діетилового ефіру малонової кислоти трифтороцтовою кислоти в присутності метилату натрію (продукт А) з послідуючою обробкою продукту І стадії реакції п'ятихлористим фосфором в дихлоретані з нагріванням реакційної суміші (продукт В, II стадія реакції) (схема 1): 1 UA 108908 U Схема 1 надл. CF3COOH , CH3ONa CH2(COOC2H5)2 CF3 - C = C(COOС2H5)2 - CH3OH , - H2O PCl5 -NaCl , - POCl3 ONa ( продукт А, І стадія реакції ) CF3 - C = C(COOC2H5)2 5 -NO2-uracile, Py - DMFA , t0 , N(C2H5)3 - N (C2H5)3 x HCl Cl 1,1 -діетилкарбокси -2-хлор-2 - трифторметилетилен (продукт В, ІІ стадія реакції ) O NO2 HN N O F3C С = С (СOOС2H5)2 1,1 -діетилкарбокси -2 -трифторметил - 2 - ( 5' - нітроуридил -1' -) -етилен ( продукт С, ІІІ стадія реакції ) 5 10 15 20 25 30 В ІЧ-спектрі синтезованої сполуки спостерігаються смуги поглинання, які характерні для -1 групи -CF3 в області 400, 415, 470, 560, 905, 995, 1180, 1230, 1295 см , для груп -ОСН3 та -1 ОС2Н5 в області 1050-1150 см . Частоти подвійних зв'язків С=С знаходяться в області 1315, -1 -1 -1 1600 см , -С=О в області 1710, 1750 см , NO2 в області 1370 см . -1 Положення смуг γС-С гетероциклу спостерігається в області 1300-1600 см , γС-Н в області -1 -1 3010-3080 см , а також сигнали в характерній області δСH при 600-800 см . В ПМР-спектрі синтезованої сполуки спостерігаються сигнали: у вигляді мультиплету при 1.005-1.355 м. ч., який відповідає шести протонам двох груп -СН3 складноефірних фрагментів молекули, мультиплету при 3,737-4,315 м. ч. чотирьох протонів в фрагментах -ОСH2 складноефірних груп молекули, триплету при 7,78 м. ч. протону групи -С(6)Н, синглету при 11.69 м. ч. протону групи -N(3)H. Таким чином, можна зробити висновок, що сполука з потенційними фізіологічними властивостями, аналогічно до відомих галоген(фтор)вмісних лікарських засобів може бути перспективною для подальшого вивчення як потенційно фізіологічно активна. Ознаки способу. Методика синтезу сполуки 1,1-діетилкарбокси-2-трифторметил-2-(5'-нітроуридил-1'-)-етилен Приготування розчину № 1 (1 Стадія реакції). 6.13 г натрію металевого (0,268 моль) розчиняють в 250 мл метанолу безводного, додають краплями через ділильну лійку 43.0 г діетилового ефіру малонової кислоти (40 мл, 0.268 моль) та 62.0 г трифтороцтової кислоти (40 мл, 0.543 моль) при перемішуванні реакційної суміші та нагріванні. Кип'ятять суміш протягом 6 годин, охолоджують до кімнатної температури, відганяють простою перегонкою розчинник. Залишок - скловидну масу білого кольору заливають діетиловим ефіром. Осад білого кольору (продукт А), що випадає фільтрують та використовують па наступній стадії реакції. Приготування розчину № 2 (II Стадія реакції). 8.0 г (0,0287 моль) продукту А розчиняють в 55 мл сухого дихлоретану при кімнатній температурі додають 6 г (0,0287 моль) п'ятихлористого фосфору. Реакційна суміш гріється та 2 UA 108908 U 5 10 15 20 25 30 35 40 набуває молочного забарвлення. Гарячий розчин перемішують з кип'ятінням 5 годин, охолоджують, осад, що утворився відфільтровують та промивають дихлоретаном, відганяють простою перегонкою розчинник. Залишок - масло, яке очищують перегонкою у вакуумі (продукт 25 В). Практичний вихід 6.31 г (80 %). Т. кип. 56-59 о С (25 мм рт. ст.), n D 1,3010. Приготування розчину № 3 (III Стадія реакції). До суміші 2.26 г (0.014 моль) 5-нітроурацилу розчиненого в суміші 200 мл піридину та 50 мл диметмлформаміду безводних та 1.42 г (2.5 мл, 0.014 моль) триетиламіну безводного додають по краплям 3.8 г (0.014 моль) продукту By 10 мл диметилформаміду безводного при перемішуванні реакційної суміші та нагріванні до 60-70 °C. Кип'ятять суміш протягом 10 годин (реакційна суміш темно-червоного забарвлення), фільтрують гарячий розчин та відділяють осад N(С2Н5)3 х НСl, відганяють розчинники у вакуумі. Залишок - масло жовтого забарвлення заливають гексаном та кип'ятять, зливають гексан декантацією, заливають ацетоном, осад блідо-жовтого забарвлення випадає із ацетону (продукт С). Практичний вихід 2.5 г (45 %). Тпл. 156-159 °C. Індивідуальність синтезованої сполуки контролювали методом тонкошарової хроматографії, склад підтверджували даними елементного аналізу. Спектр ПМР синтезованої сполуки записували на приладах "Bruker WP-200" (виробник "Bruker", Switzerland), "Varian T-60" (виробник "Varian", USA) з робочою частотою 200-132 МГц у виді розчину ДМСО-D6 (внутрішній стандарт ТМС). ІЧ-спектр записували на спектрофотометрі UR-20 (виробник "Charles Ceise Hena", Germany). ТШХ виконували на пластинах Silufol-254. ГРХ визначали на газорідинному хроматографі "Perkin Elmer'з УФ-детектором (виробник "Perkin", Germany). Хроматограму, ІЧ-, ПМР-спектри кінцевого продукту (Фіг.) ідентифікували у порівнянні з хроматограмами, ІЧ-, ПМР-спектрами вихідних сполук. Синтезована сполука - мілкокристалічний осад блідо - жовтого забарвлення. Дані елементного аналізу на С, Н, N синтезованої сполуки відповідають обчисленим значенням. В ІЧ-спектрі синтезованої сполуки ідентифіковано смуги поглинання, які характерні для -1 групи -CF3 в області 400, 415, 470, 560, 905, 995, 1180, 1230, 1295 см , для груп -ОСНз та -1 ОС2Н5 в області 1050-1150 см . Частоти подвійних зв'язків С=С знаходяться в області 1315, -1 -1 -1 1600 см , - С=O в області 1710, 1750 см , NO2 в області 1370 см Положення смуг С-С -1 -1 гетероциклу спостерігається в області 1300-1600 см С-Н в області 3010-3080 см , а також -1 сигнали в характерній області СH при 600-800 см . Співвідношення інтегральних інтенсивностей сигналів в ПМР-спектрі синтезованої сполуки підтверджує наявність в молекулі протонів двох груп -СН3 складноефірних фрагментів молекули у вигляді мультиплету при 1.005-1.355 м.д., чотирьох протонів в фрагментах -ОСН2 складноефірних груп молекули у вигляді мультиплету при 3.737 4.315 м. ч., протонів груп -С(6)Н при 7.78 м. ч. у вигляді триплету та групи -N(3)H у вигляді синглету при 11.69 м. ч. Фізико-хімічні характеристики та дані елементного аналізу синтезованої сполуки наведено в таблиці. Таблиця Фізико-хімічні характеристики та дані ej ементного аналізу сполуки. Знайдено, в% Бруттоформула Обчислено, в %, -1 ІЧ-спектр (КВr), см γ C-Hal, Alk, Heterocycl., С=О, С=С. С Н N С Н N 41,03,3511,09 C13H12O8N3F3 39,513,0510,63 400,415,470, 560 (CF3), 600800 (Heterocycl.), 905, 995, 1180, 1230, 1295 (CF3), 1050 -1150(OCH3). (OC2H5), 13001600 (Heterocycl.), 1315, 1600 (С-С), 1710, 1750 (ОО), 1370 (NO2),3010-3080 (Heterocycl.). 3 Спектр ПМР (ДМСО-D6 ТМС), , м. д. (J Гц) 1.005-1.355 (6Н, 3 м.,J Н.Н7,0 Гц, 2СН3), 3 3.737-4.315 (4Н, м., J Н.Н 7.0 Гц, 2ОСН2), 7.78 (1Н, 2 т., J Н.Н 10,0 Гц, С(6)Н (Heterocycl.)), 11.69 (1H, c.,N(3)H (Heterocycl.)). UA 108908 U Задачею корисної моделі є опис хімічної будови нової сполуки 1,1-діетилкарбокси-2трифторметил-2-(5'-нітроуридил-1’-)-етилен з потенційними фізіологічними властивостями, яка синтезована з метою отримання нового поліфункціонального фторвмісного синтону для подальшого вивчення її фізико-хімічних та біологічних властивостей. 5 10 15 Джерела інформації: 1. Ягупольский Л.М. //Ароматические и гетероциклические соединения с фторсо-держащими заместителями. - Киев: Наукова думка. 1988. - С. 90-105. 2. Соединения фтора. Синтез и применение. //Под ред. Н. Исикава. - М.: Мир. 1990. - Гл. 5. С. 183-265. 3. Герус И.И., Колычева М.Т., Ягупольский Ю.Л. Кухарь В.П. //ЖОрХ.-1989. - Т. 25, Вып. 9. С. 2020-2021. 4. Крохтяк В.П., Ильченко А.Я. //ЖОрХ.-1980, - Т. 16. Вып. 8. - С. 1694 1698. 5. Вельчинська О.В. Спосіб отримання речовини з протипухлинною активністю 1,1'-(2"-бром2"-хлоретеніл)-біс-(5-фторурацил). Деклараційний патент на корисну модель. 6893. C07D 239/553, С07С 21/18. 21/185. А61K 33/16. Дата прийняття рішення 16.05.2005. Бюл. № 5. С. 6893. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 20 Сполука 1,1-діетилкарбокси-2-трифторметил-2-(5'-нітроуридил-1'-)-етилен фізіологічними властивостями загальної формули: O NO2 HN N O F3 C С = С (СOOС2H5)2 . 4 з потенційними UA 108908 U Комп’ютерна верстка М. Мацело Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A61K 33/16, C07C 21/18, C07D 239/553, C07C 21/185
Мітки: 1,1-діетилкарбокси-2-трифторметил-2-(5'-нітроуридил-1'-)-етилен, потенційними, сполука, властивостями, фізіологічними
Код посилання
<a href="https://ua.patents.su/7-108908-spoluka-11-dietilkarboksi-2-triftormetil-2-5-nitrouridil-1-etilen-z-potencijjnimi-fiziologichnimi-vlastivostyami.html" target="_blank" rel="follow" title="База патентів України">Сполука 1,1-діетилкарбокси-2-трифторметил-2-(5′-нітроуридил-1′-)-етилен з потенційними фізіологічними властивостями</a>
Попередній патент: Сполука 1,1-діетилкарбокси-2-трифторметил-2-(уридил-1′-)-етилен з потенційними фізіологічними властивостями
Наступний патент: Сполука 1,1-діетилкарбокси-2-трифторметил-о-(4′-метоксипіримідиніл-2′)-етилен з потенційними фізіологічними властивостями
Випадковий патент: Вентиляційна головка торовця а. г. - солдатова в. б.











