Спосіб одержання 5,11,17,23-тетра(n,n-диметил-n-гідроксіетиламоніум)-метилен-25,26,27,28-тетраалкоксикалікс[4]аренів тетрахлоридів
Номер патенту: 72777
Опубліковано: 27.08.2012
Автори: Ів Мелі, Родік Роман Васильович, Климченко Андрій Сергійович, Кальченко Віталій Іванович
Формула / Реферат
Спосіб одержання 5,11,17,23-тетра(N,N-диметил-N-гідроксіетиламоніум)-метилен-25,26,27,28-тетраалкоксикалікс[4]аренів тетрахлоридів загальної формули:
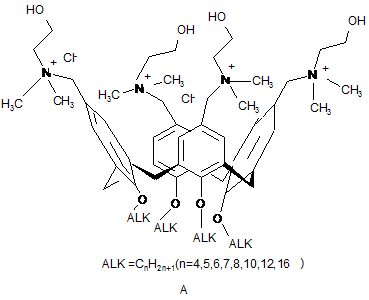 ,
,
який відрізняється тим, що Ν,Ν-диметилетаноламін кватернізують тетракисхлорометилтетраалкоксикаліксаренами в безводних органічних розчинниках при кип'ятінні.
Текст
Реферат: Спосіб одержання 5,11,17,23-тетра(N,N-диметил-N-гідроксіетиламоніум)-метилен-25,26,27,28тетраалкоксикалікс[4]аренів тетрахлоридів кватернізують тетракисхлорометилтетраалкоксикаліксаренами в безводних органічних розчинниках при кип'ятінні. UA 72777 U (54) СПОСІБ ОДЕРЖАННЯ 5,11,17,23-ТЕТРА(N,N-ДИМЕТИЛ-N-ГІДРОКСІЕТИЛАМОНІУМ)-МЕТИЛЕН25,26,27,28-ТЕТРААЛКОКСИКАЛІКС[4]АРЕНІВ ТЕТРАХЛОРИДІВ UA 72777 U UA 72777 U Корисна модель належить до органічної хімії, а саме до серії гомологічних 5,11,17,23тетра(N,N-диметил-N-гідроксіетиламоніум)-метилен-25,26,27,28-тетраалкоксикалікс[4]аренів тетрахлоридів А загальної формули: HO HO OH + Cl N H3 C CH3 Cl Cl H3 C OH N + N + CH 3 Cl O ALK O N+ CH3 CH3 CH3 CH3 O O ALK ALK ALK ALK =CnH2n+1(n=4,5,6,7,8,10,12,16 ) A 5 10 , які одночасно містять позитивно-заряджені гідрофільні холінові групи на верхньому вінці макроциклу та ліпофільні нерозгалужені алкільні групи на нижньому вінці макроциклу, і мають амфіфільну природу. Ці сполуки завдяки зв'язуванню з нуклеїновими кислотами (зокрема ДНК), яке супроводжується повною компенсацією та маскуванням від'ємного заряду останніх, можуть знайти застосування для промотування генної трансфекції у генотерапії. [1] Названі сполуки, їх властивості та застосування в патентних виданнях і науковій літературі не описані. Найближчими структурними аналогами сполук, які заявляються, є 5,11,17,23тетра(триметиламоніум)-метилен-25,26,27,28-тетрапропоксикалікс[4]арен тетрахлорид Б [2]; ClH3 C + N CH3 ClH3 C + N + CH 3 N CH3 CH3 O 20 CH3 H3C CH3 H7 C3 15 Cl Cl H3 C O C3H7 N+ CH3 CH3 O O C3 H 7 C3H7 Б . Каліксарен Б завдяки наявності чотирьох триметиламонійних груп на верхньому вінці макроциклу та чотирьох ліпофільних груп на протилежному нижньому вінці є водорозчинною амфіфільною сполукою. Наявність чотирьох позитивних зарядів надає здатність до зв'язування з аніонними гостями, а саме нуклеотидами, нуклеотиддифосфатами, нуклеотидтрифосфатами та ДНК [2]. Відомо, що каліксарен Б зв'язує аденозин, аденозинмонофосфат (АМФ), аденозиндифосфат (АДФ) та аденозинтрифосфат (АТФ), відповідні константи стійкості комплексів (К ст) та вільні енергії їх утворення (G) наведені в таблиці 1 [2] Таблиця 1 -1 Константи стійкості (Кст М ) та вільні енергії зв'язування (-G, кДж/моль) каліксарену Б з похідними аденозину Субстрат Аденозин 2АМФ 3АДФ 4АТФ -1 КстМ 9,6 3 1,3±0,1 10 3 2,7±0,5 10 3 11±4,8 10 25 1 -G, кДж/моль 5,6 17,7 19,6 23,0 UA 72777 U Каліксарен Б не має селективності дії щодо інших нуклеотидмонофосфатів: гуанозинмонофосфату (ГМФ), уридинмонофосфату (УМФ), цитозинмонофосфату (ЦМФ) та тимидинмонофосфату (ТМФ) (табл. 2) Таблиця 2 -1 Константи стійкості (Кст М ) та вільні енергії зв'язування (-G, кДж/моль) каліксарену Б з нуклеотидами [2] -1 Субстрат 2ГМФ 2УМФ 2ЦМФ 2ТМФ КстМ 3 0,31±0,06 10 3 0,47±0,1 10 3 1,4±0,2 10 3 0,9±0,2 10 -AG, кДж/моль 14,2 15,2 17,9 16,8 5 Також каліксарен Б ефективно зв'язується з полінуклеотидами. Дослідження по витисненню флуоресцентного барвника Етидіум броміду (приклад 2) наведені у таблиці 3 Таблиця 3 Концентрація (С50, мкМ), при якій відбувається 50% гасіння флюоресценції Етидіум броміду при додаванні каліксарену Б до розчину дезоксирибонуклеїнової кислоти та етидіум броміду [2] Поліаденінполітимін 0,56 Каліксарен 4+ Б , рН 7 10 15 20 ДНК з тимусу Полігуанінтеля поліцитидин 0,53 1,3 Поліаденіна поліуридин 21 досліджувалась рибонуклеїнова кислота. Задачею корисної моделі є спосіб отримання серії гомологічних 5,ll,17,23-тeтpa(N,Nдиметил-Н-гідроксіетиламоніум)-метилен-25,26,27,28-тетраалкоксикалікс[4]аренів тетрахлоридів загальної формули А. Введення на верхній вінець макроциклу чотирьох гідрофільних холінових груп, здатних до зв'язування з нуклеїновими кислотами за рахунок як електростатичних взаємодій, так і водневих зв'язків розширить комплексоутворюючі та гентрансфектуючі властивості цих сполук порівняно з каліксареном Б по відношенню до нуклеїнових кислот. Спосіб одержання сполук, які заявляється, складається з однієї стадії, згідно з наведеною нижче схемою. Тетрахлорометилтетраалкоксикалікс[4]арени В, отримані по літературним методикам [3, 4] при взаємодії з півторакратним надлишком Ν,Ν-диметилетаноламіну у безводних органічних розчинниках (ТГФ, ацетонітрил, діоксан) при температурах 60-100 °С утворюють 5,11,17,23тетра(N,N-диметил-N-гідроксіетиламоніум)-метилен-25,26,27,28-тетраалкоксикалікс[4]арени тетрахлориди А. HO HO OH Cl Cl Cl Cl + Cl N H3C CH3 ClH3C OH Cl + N + CH 3 N Cl CH3 CH3 N+ CH3 CH3 (CH3)2NCH2CH2OH O ALK 25 30 O ALK B O O ALK ALK O ALK O ALK O O ALK ALK ALK =CnH2n+1(n=4,5,6,7,8,10,12,16 ) A . Індивідуальність та структура 5,11,17,23-тетра(N,N-диметил-N-гідроксіетиламоніум)метилен-25,26,27,28-тетраалкоксикалікс[4]аренів тетрахлоридів А доведена спектрами ЯМР Ή, елементним аналізом та дослідженнями мас-спектроскопії. Так, згідно з даними ПМР спектроскопії калікс[4]арени А перебувають у розчині ДМСО-do у конформації конус, на що вказує різниця хімічних зсувів в ПМР спектрах між екваторіальними та аксіальними протонами метиленових спейсерів макроциклу (Δ 1,15-1,21 м.ч.) Корисна модель ілюструється методом отримання, фізико-хімічними характеристиками синтезованих сполук та результатами досліджень їх зв'язування з молекулами ДНК. 2 UA 72777 U Експерименти по дослідженню зв'язування полікатіонних каліксаренів з ДНК були проведені методом витиснення флуоресцентного катіонного барвника Етидіум Броміду (ЕБ). Даний метод дає кількісну інформацію про силу зв'язування каліксарену з ДНК та якісну інформацію про утворення агрегатів комплексів в цьому процесі. Br + N NH2 H2 N 5 10 15 20 25 30 35 40 45 Етидіум Бромід . Даний барвник має низьку флуоресценцію у водних середовищах. Завдяки електростатичним взаємодіям він легко зв'язується з поліаніонною ДНК. Його видовжена структура дозволяє йому розташовуватись у борозенках ДНК та не порушувати її геометрію. Після зв'язування флуоресценція ЕБ зростає у декілька разів і максимум її зміщується на 10-15 нм у синю область. При наступному додаванні іншого агенту, який також здатен зв'язуватись з ДНК, відбувається витиснення ЕБ із комплексу ДНК-ЕБ та згасання його флуоресценції. При додаванні розчинів каліксаренів А до розчину ТТ-ДНК, поміченої ЕБ (молярне співвідношення 50 нуклеотидів до 1 ЕБ), спостерігалось стрімке згасання флуоресценції та зсув її максимуму з 600 до 610-615 нм. Це пояснюється утворенням агрегатів каліксарен Α-ДНК та витисненням ЕБ з місць його неспецифічного зв'язування з ДНК. При концентрації каліксарену А 6-7,5 мкМ згасання флуоресценції ЕБ закінчувалось, тобто відбувалось повне зв'язування молекул ДНК каліксареном. Приклад 1. Загальний спосіб одержання 5,11,17,23-тетра(N,N-диметилN-гідроксіетиламоніум)-метилен25,26,27,28-тетраалкоксикалікс[4]аренів тетрахлоридів А. До розчину тетрахлорметилкаліксарену В [4] (1 ммоль) в ТГФ (20 мл) при перемішуванні додавали протягом 5 хв. розчин Ν,Ν-диметилетаноламіну (5 ммоль) в ТГФ (5 мл). Реакційну суміш кип'ятили при перемішуванні 16 год. Утворився безбарвний осад. Після охолодження реакційної суміші до кімнатної температури осад сполуки А відфільтровували. Сушили в вакуумі (0,05 мм. рт. ст., 20 °С) 4 год. 5,11,17,23-тетра(N,N-диметил-N-гідроксіетиламоніум)-метилен-25,26,27,28-тетрагексилоксикалікс[4]арен тетрахлорид, Alk = С6Н13 1 Безбарвна тверда речовина: вихід 75%. т. топл. 265 °С (розкл.). ЯМР H ((CD3)2S=O, 299,94 МГц), м.ч.: 0.90 τ (J=7,3 Гц, 12Н, О-СН2-СН2-СН3), 1,33-1,38 (уш. с, 24Н, О-СН2-СН2-(СН2)5-СН3), 1,91 (уш. с, 8Н, О-СН2-СН2-(СН2)5-СН3), 2,95 (с, 24Н, N-СН3), 3,29 (уш. с, 12Н, ArCHeqAr, N-CH2), 3,89 (уш. с, 16Н, О-CH2-СН2-СН3, СН2-ОН), 4,36 д (J=13,3 Гц, 4Н, АrСНахАr), 4,53 с (8Н, Ar-CH2N), 5,72 уш. с (4Н, ОН), 6,98 с (8Н, АrН). 5,11,17,23-тетра(N,N-диметил-N-гідроксіетиламоніум)-метилен-25,26,27,28тетраоктилоксикалікс[4]арен тетрахлорид, Alk = C8H17 1 Безбарвна тверда речовина: вихід 65%. т. топл. 260 °С (розкл.). ЯМР H ((CD3)2S=O, 299,94 МГц), м.ч.: 0,86 т (J=7,3 Гц, 12Н, О-СН2-СН2-СН3), 1,30-1,35 (уш.с, 40Н, О-СН2-СН2-(СН2)5-СН3), 1,89 (уш.с, 8Н, О-СН2-СН2-(СН2)5-СН3), 2,95 (с, 24Н, N-СН3), 3,30 (уш.с, 12Н, ArCHeqAr, N-CH2), 3,87 (уш. с, 16Н, О-СН2-СН2-СН3, СН2-ОН), 4,33 д (J = 13,3 Гц, 4Н, АrСНахАr), 4.54 с (8Н, Ar-CH2- 2+ N), 5,76 уш. с (4Н, ОН), 6,97 с (8Н, АrН). MS: (m/z) знайдено [М-2Сl ] /2 = 675,5 (розраховано 2+ - 2+ для C8oH136Cl2N4O8 ; [M-2Сl ] /2=675,5). Анал. розр. для C80H136Cl2N4O8, %: С 65,71; Η 7,54;. Знайдено, %: С 65,76; Η 7,52; 5,11,17,23-тетра(N,N-диметил-N-гідроксиетиламоніум)-метилен-25,26,27,28тетрадодецилокси-калікс[4]арен тетрахлорид, Alk = С12Н25 1 Безбарвна тверда речовина: вихід 55%. т. топл. 255 °С (розкл.). ЯМР Н ((CD3)2S=O, 5%(v/v) CDCI3, 299,94 МГц), м.ч.: 0,87 т (J = 7,3 Гц, 12Н, О-СН2-СН2-СН3), 1,25-1,45 (уш.с, 72Н, ОСН2СН2-(CH2)5-СН3), 1,91 (уш.с, 8Н, О-СН2-СН2-(СН2)5-СН3), 2,99 (с, 24Н, N-СН3), 3,35 (уш.с, 12Н, 3 UA 72777 U 5 10 15 20 25 30 ArCHeqAr, N-CH2), 3,92 (уш. с, 16Н, О-СН2-СН2-СН3, СН2-ОН), 4,39 д (J = 13,3 Гц, 4Н, АrСНахАr), 4,56 с (8Н, Ar-CH2-N), 5,62 уш. с (4Н, ОН), 6,99 с (8Н, АrН). Приклад 2. Дослідження зв'язування 5Д1Д7,23-тетра(N,N-диметил-N-гідроксіетиламоніум)-метилен25,26,27,28-тетраоктилоксикалікс[4]арену тетрахлориду A (Alk=C8H17) з ТТ-ДНК методом витиснення Етидіум броміду Для досліджень готували розчин, що містив 20 мкМ телячої тимусної (ТТ) ДНК (у перерахунку на концентрацію нуклеотидів), 0,4 мкМ ЕВ у 20 мМ Tris-буфері. Вимірювали інтенсивність флуоресценції в діапазоні 580-700 нм при збудженні 550 нм. Потім додавали зростаючі концентрації каліксаренів, витримували 1 хвилину та знов вимірювали інтенсивність флуоресценції. Використовували такі концентрації каліксаренів 1, 2, 2,5, 4, 5, 6, 7,5, 10, 20, 40 60 мкМ. Отримані криві флуоресценції наведені кресленні. Фіг 1. Залежність флуоресценції Етидіум броміду (0.4 мкМ) у присутності ТТ-ДНК (20 мкМ) від концентрації каліксарену A (Alk=C8H17) у 20 mM Tris-буфері. Після обробки даних була отримана залежність інтенсивності флуоресценції ЕБ від концентрації каліксарену A (Alk=C8H17). Фіг. 2. Залежність флуоресценції ЕБ (0,4 мкМ) у присутності ТТ-ДНК (20 мкМ) від концентрації тетракатіонного каліксарену A (Alk=C8H17) у 20 гаМ Tris-буфері. Тобто, при концентрації каліксарену A (Alk=C8H17) 6-7,5 мкМ згасання флуоресценції закінчилось, відбулось повне зв'язування молекул ДНК каліксареном. Ця концентрація є вищою всього на 20-50% точки повної нейтралізації зарядів ДНК каліксареном А і вказує на високу стійкість утворених комплексів. ЛІТЕРАТУРА 1 V. Bagnacani, F. Sansone, G. Donofrio, L. Baldini, A. Casnati and R. Ungaro, // Org. Lett. 2008,-Vol. 10,- Pages 3953-3958. 2 У. Shi and H. J. Schneider, // J. Chem. Soc, Perkin Trans. 2 - 1999, - Pages: 1797-1803 3 Nagasaki, Т., Sisido, K., Arimura, Т., Shinkai, S. // Tetrahedron - 1992 - Vol. 48. - P. 797-801 4 R. V. Rodik, A. S. Klymchenko, N. Jain, S. I. Miroshnichenko, L. Richert, V. I. Kalchenko Y. Mely // Chemistry - A European Journal - 2011 - Vol. 17, - Pages: 5526-5538. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 35 Спосіб одержання 5,11,17,23-тетра(N,N-диметил-N-гідроксіетиламоніум)-метилен-25,26,27,28тетраалкоксикалікс[4]аренів тетрахлоридів загальної формули: HO HO OH + Cl N H3 C CH3 H3 C N + O ALK + N CH3 Cl O OH N+ CH3 CH3 CH3 CH3 O O ALK ALK ALK ALK =CnH2n+1(n=4,5,6,7,8,10,12,16 ) A , який відрізняється тим, що Ν,Ν-диметилетаноламін кватернізують тетракисхлорометилтетраалкоксикаліксаренами в безводних органічних розчинниках при кип'ятінні. 4 UA 72777 U Комп’ютерна верстка І. Скворцова Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 5
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 5,11,17,23-tetra(n,n-dimethyl-n-hydroxyethylammonium)-methylene-25,26,27,28-tetraalkoxycalix[4]arene tetrachlorides
Автори англійськоюRodik Roman Vasyliovych, Kalchenko Vitalii Ivanovych, Yves Mely, Klymchenko Andrii Serhiiovych
Назва патенту російськоюСпособ получения 5,11,17,23-тетра(n,n-диметил-n-гидроксиэтиламмониум)-метилен-25,26,27,28-тетраалкоксикаликс[4]аренов тетрахлоридов
Автори російськоюРодик Роман Васильевич, Кальченко Виталий Иванович, Ив Мели, Климченко Андрей Сергеевич
МПК / Мітки
МПК: C07C 211/62, C07C 15/16
Мітки: одержання, спосіб, тетрахлоридів, 5,11,17,23-тетра(n,n-диметил-n-гідроксіетиламоніум)-метилен-25,26,27,28-тетраалкоксикалікс[4]аренів
Код посилання
<a href="https://ua.patents.su/7-72777-sposib-oderzhannya-5111723-tetrann-dimetil-n-gidroksietilamonium-metilen-25262728-tetraalkoksikaliks4areniv-tetrakhloridiv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання 5,11,17,23-тетра(n,n-диметил-n-гідроксіетиламоніум)-метилен-25,26,27,28-тетраалкоксикалікс[4]аренів тетрахлоридів</a>
Попередній патент: Спосіб ідентифікації т-хелперів 17 типу (th17)
Наступний патент: Спосіб автоматизованої діагностики порушень уродинаміки нижніх сечових шляхів
Випадковий патент: Засіб для реклами











