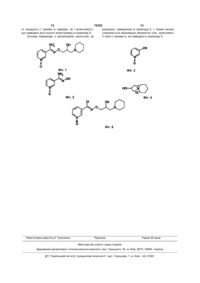
N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідин та спосіб його перетворення у фармацевтично ефективні сполуки
Номер патенту: 75353
Опубліковано: 17.04.2006
Автори: Етвьос Ласло, Тьомьошкьозі Іштван, Шнейдерне Барлаі Маріа, Сакачне Шмідт Аніко, Рейдер Ференцне, Єгешне Чакаі Зіта, Тот Йожеф, Грубер Лайош, Ірьогді Ласло
Формула / Реферат
1. N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідин та його кислотно-адитивні солі.
2. (R)-(-)-N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідин та його кислотно-адитивні солі.
3. (S)-(+)-N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідин та його кислотно-адитивні солі.
4. Застосування N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідину та його оптично активних енантіомерів для одержання N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксимідоїлхлориду та його оптично активних енантіомерів.
5. Спосіб одержання N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксимідоїлхлориду та його кислотно-адитивних солей, який включає:
a) діазотування N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідину шляхом взаємодії з нітритом лужного металу в присутності хлороводневої кислоти, або
b) діазотування N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідину шляхом взаємодії з нітритом лужного металу в присутності хлороводневої кислоти та перетворення одержаної основи в кислотно-адитивну сіль.
6. Спосіб одержання (R)-(+)-N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксимідоїлхлориду та (S)-(-)-N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксимідоїлхлориду та їх кислотно-адитивних солей, який включає:
а) діазотування (R)-(-)-N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідину або (S)-(+)-N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідину шляхом взаємодії з нітритом лужного металу в присутності хлороводневої
кислоти, або
b) розділення N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідину та діазотування одержаного оптично активного (R)-(-) енантіомера або (S)-(+) енантіомера в присутності хлороводневої кислоти шляхом взаємодії з нітритом лужного металу, або
c) діазотування N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідину в присутності хлороводневої кислоти шляхом взаємодії з нітритом лужного металу та виділення необхідного (R)-(+) або (S)-(-) енантіомера розділенням одержаного рацемічного N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксимідоїлхлориду, або
е) перетворення (R)-(+)-N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксимідоїлхлориду або (S)-(-)-N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксимідоїлхлориду, одержаного будь-яким із варіантів а) - с) способу, в кислотно-адитивну сіль.
Текст
1. N-[2-гідрокси-3-(1-піперидиніл) пропокси]піридин-1-оксид-3-карбоксамідин та його кислотно-адитивні солі. 2. (R)-(-)-N-[2-гідрокси-3-(1піперидиніл)пропокси]піридин-1-оксид-3карбоксамідин та його кислотно-адитивні солі. 3. (S)-(+)-N-[2-гідрокси-3-(1піперидиніл)пропокси]піридин-1-оксид-3карбоксамідин та його кислотно-адитивні солі. 4. Застосування N-[2-гідрокси-3-(1піперидиніл)пропокси]піридин-1-оксид-3карбоксамідину та його оптично активних енантіомерів для одержання N-[2-гідрокси-3-(1піперидиніл)пропокси]піридин-1-оксид-3карбоксимідоїлхлориду та його оптично активних енантіомерів. 5. Спосіб одержання N-[2-гідрокси-3-(1піперидиніл)пропокси]піридин-1-оксид-3карбоксимідоїлхлориду та його кислотноадитивних солей, який включає: a) діазотування N-[2-гідрокси-3-(1піперидиніл)пропокси]піридин-1-оксид-3карбоксамідину шляхом взаємодії з нітритом луж C2 2 (19) 1 3 75353 4 піперидиніл)пропокси]піридин-1-оксид-3карбоксімідоїлхлориду з високою чистотою та з карбоксамідин та її оптично активних енантіомерів, високим винаходом. (R)-(-)-N-[2-гідрокси-3-(1Базуючись на цьому спостереженні, даний випіперидиніл)пропокси]піридин-1-оксид-3нахід стосується N-[2-гідрокси-3-(1карбоксамідину та (S)-(+)-N-(2-гідрокси-3-(1піперидиніл)пропокси]піридин-1-оксид-3піперидиніл)пропокси]піридин-1-оксид-3карбоксамідину та його кислотно-адитивних солей. карбоксамідину. Більш того, винахід стосується Винахід також стосується оптично активних енанодержання N-[2-гідрокси-3-(1тіомерів вищезгаданої сполуки, (R)-(-)-N-[2піперидиніл)пропокси]піридин-1-оксид-3гідрокси-3-(1-піперидиніл)пропокси]піридин-1карбоксімідоїлхлориду, який може бути використаоксид-3-карбоксамідину та (S)-(+)-N-[2-гідрокси-3ний як активний інгредієнт лікарських засобів, та (1-піперидиніл)пропокси]піридин-1-оксид-3одержання оптично активних енантіомерів цієї карбоксамідину, та кислотно-адитивних солей цих сполуки з використанням сполук винаходу як просполук. міжних речовин. Далі, термін "оптично активний енантіомер" N-[2-Гідрокси-3-(1стосується сполуки, яка має оптичну чистоту, припіперидиніл)пропокси]піридин-1-оксид-3наймні, 80%, переважно, принаймні, 90%, найкарбоксімідоїлхлорид, разом із декількома спорідбільш переважно, принаймні, 96%, тобто, сполука неними сполуками, відомий з WO 97/16439 як містить, принаймні, таке масове співвідношення ефективний агент, придатний для підвищення ексконкретного оптично активного енантіомера. Терпресії шаперонів клітин. В цій публікації сполука мін "кислотно-адитивні солі" стосується солей, визначена як нова сполука, і також заявлені Nотриманих із сполук з мінеральними або органічоксидні похідні сполуки, але немає конкретних зганими кислотами за відомими методиками. дувань про N-[2-гідрокси-3-(1Як згадувалося вище, сполуки винаходу мопіперидиніл)пропокси]піридин-1-оксид-3жуть використовуватися як проміжні сполуки при карбоксімідоїлхлорид, і спосіб його одержання одержанні N-[2-гідрокси-3-(1також не описаний. піперидиніл)пропокси]піридин-1-оксид-3N-[2-Гідрокси-3-(1карбоксімідоїлхлориду. Таким чином, винахід стопіперидиніл)пропокси]піридин-1-оксид-3сується використання N-[2-гідрокси-3-(1карбоксімідоїлхлорид розкритий і заявлений як піперидиніл)пропокси]піридин-1-оксид-3нова сполука в WO 00/50403, і спосіб його одеркарбоксамідину та його оптично активних енантіожаний також описаний там. Сполуку одержують мерів для одержання N-[2-гідрокси-3-(1окисненням N-[2-гідрокси-3-(1піперидиніл)пропокси]піридин-1-оксид-3піперидиніл)пропокси]піридин-3карбоксімідоїлхлориду та його оптично активних карбоксімідоїлхлориду. У процесі окиснення перенантіомерів. кислотами біс-N-оксидна похідна окиснюється на Сполуку винаходу N-[2-гідрокси-3-(1N-атомах як піперидинового, так і піридинового піперидиніл)пропокси]піридин-1-оксид-3кільця, або переважно утворюється похідна піпекарбоксамідин переважно отримують наступним ридин-N-оксиду і, таким чином, окиснення за доспособом. помогою перкислот повинно здійснюватися в приЯк вихідну сполуку використовують 3сутності сильної кислоти для забезпечення ціанопіридин і 3-ціанопіридин-1-оксид формули (II), утворення похідної піридин-N-оксиду в процесі який відомий з літератури [J. Chem. Soc. 3680 реакції окиснення. Вихід у цьому процесі, однак, є (1959)] і може бути одержаний окисненням. Як незадовільним. Оптично активні енантіомери N-{2оксидант використовують перкислоту, переважно, гідрокси-3-(1-піперидиніл)пропокси]піридин-1м-хлорпербензойну кислоту. Одержаний таким оксид-3-карбоксімідоїлхлориду також описані в чином продукт може бути очищений кристалізаціWO 00/50403. Їх отримують способом, подібним до єю, але неочищений продукт також може викорисспособу одержання рацемічної сполуки, використовуватися в наступній стадії синтезу. товуючи відповідні оптично активні вихідні речовиВзаємодією 3-ціанопіридин-1-оксиду формули ни. (II) із гідроксиламіном отримують 3Приймаючи до уваги той факт, що N-[2піридинамідоксим-1-оксид формули (III). Реакцію гідрокси-3-(1-піперидиніл)пропокси]піридин-1проводять в придатному водному розчині при кімоксид-3-карбоксімідоїлхлорид та його оптично акнатній температурі шляхом взаємодії 3тивні енантіомери придатні не тільки для лікування ціанопіридин-1-оксиду з гідроксиламіном, який ускладнень діабету, первинної ретинопатії, нейрододають у надлишку і вивільнюють у воді in situ із патії та нефропатії, але й одночасно зменшують його гідрохлоридної солі за допомогою бікарбонахронічну резистентність до інсуліну, ці сполуки є ту натрію. Продукт осаджується і тому він легко корисними активними інгредієнтами фармацевтиможе бути виділений і очищений кристалізацією. чних продуктів. Однак, для того, щоб ці сполуки N-[2-Гідрокси-3-(1були корисними у фармацевтичній промисловості, піперидиніл)пропокси]піридин-1-оксид-3необхідно знати легкий спосіб їх одержання. карбоксамідин формули (I) отримують із 3Нами було виявлено, що N-гідрокси-3-(1піридинамідоксим-1-оксиду формули (III) взаємодіпіперидиніл)пропокси]піридин-1-оксид-3єю сполуки з реакційноздатним похідним 3-(1карбоксамідин формули (І), який є новою сполупіперидино)-2-гідроксипропану. Як реагент може кою, є придатною проміжною сполукою для розробути використане 1-гало- або 1,2-епоксипохідне, бки простого процесу одержання N-[2-гідрокси-3але повинно використовуватися переважно циклі(1-піперидиніл)пропокси]піридин-1-оксид-3чне похідне, галід 2-гідрокси-4 5 75353 6 азоніаспіро[3,5]нонан. Переважним реагентом є 2ятну кислотно-адитивну сіль. гідрокси-4--азоніаспіро[3,5]нонанхлорид формули Необхідні оптично активні енантіомери N-[2(IV). Реакцію проводять у лужному середовищі, гідрокси-3-(1-піперидиніл)пропокси]піридин-1використовуючи придатний спирт, переважно алоксид-3-карбоксімідоїлхлориду формули (V), одеканол з 1-3 атомами вуглецю, найбільш переважржаного діазотуванням, отримують розділенням ним розчинником є етанол. Реагенти можуть дорацемічної суміші сполук. Розділення здійснюють даватися у будь-якому порядку. Переважно, шляхом утворення діастереомерної пари солей, реакційноздатне похідне 3-(1-піперидино)-2переважно з дибензоїлвинною кислотою, викорисгідроксипропану застосовують у невеликому надтовуючи для солеутворення її придатну оптично лишку. Реакцію здійснюють при підвищеній темпеактивну форму. ратурі, переважно, при кипінні розчинника. Якщо здійснюють описане вище діазотування Отриману таким чином сполуку формули (I) оптично активного енантіомеру N-[2-гідрокси-3-(1або виділяють у вигляді основи і використовують піперидиніл)пропокси]піридин-1-оксид-3як проміжну сполуку при одержанні біологічно карбоксамідину формули (I), утворюється енантіоефективного N-[2-гідрокси-3-(1мер N-[2-гідрокси-3-(1піперидиніл)пропокси]піридин-1-оксид-3піперидиніл)пропокси]піридин-1-оксид-3карбоксімідоїлхлориду, або перетворюють и у кискарбоксімідоїлхлориду формули (V) достатньої лотно-адитивну сіль з мінеральною або органічоптичної чистоти, який обертає площину поляриною кислотою. Таким чином можуть бути одержані зації у зворотному напрямку. Таким чином, згідно з моно- або дигідрохлорид, малеат або будь-яка іншим варіантом способу даного винаходу оптично інша кислотно-адитивна сіль, яка є придатною для активний N-[2-гідрокси-3-(1використання у якості проміжної сполуки при одепіперидиніл)пропокси]піридин-1-оксид-3ржанні вищезгаданого кінцевого продукту. Однак, карбоксімідоїлхлорид формули (V) одержують немає необхідності виділяти N-[2-гідрокси-3-(1проведенням вищеописаного діазотування відпопіперидиніл)пропокси]піридин-1-оксид-3відного оптично активного енантіомеру N-[2карбоксамідин для використання його як проміжної гідрокси-3-(1-піперидиніл)пропокси]піридин-1сполуки. Наступна стадія в синтезі N-[2-гідрокси-3оксид-3-карбоксамідину формули (I). Одержану (1-піперидиніл)пропокси]піридин-1-оксид-3таким чином основу можна в подальшому, при карбоксімідоїлхлориду може бути проведена також необхідності, очистити або можна перетворити в без виділення сполуки формули (I). кислотно-адитивну сіль взаємодією з мінеральною Коли бажаним є отримання оптично активного або органічною кислотою. продукту, сполука формули (I) перед її перетвоПеревага винаходу полягає в тому, що шляренням може бути розчинена шляхом взаємодії її з хом використання сполуки формули (I) згідно з оптично активною кислотою, придатною для утвовинаходом як проміжної сполуки, можливо одеррення пари діастереомерних солей, добре відожання високочистого N-[2-гідрокси-3-(1мими способами розчинення. Коли сіль необхідної піперидиніл)пропокси]піридин-1-оксид-3оптичної чистоти отримана, оптично активна оснокарбоксімідоїлхлориду, який має корисні біологічні ва може бути вивільнена з неї. Після цього, якщо властивості. На відміну від способу, описаного в необхідно, з основи може бути одержана кислотзаявці WO 00/50403, згаданій у вступі, згідно з но-адитивна сіль взаємодією з мінеральною або яким дана сполука одержується окисненням N-[2органічною кислотою. Або основа або сіль потім гідрокси-3-(1-піперидиніл)пропокси]піридин-3можуть бути використані на наступній стадії спокарбоксімідоїлхлориду, в даному процесі утворенсобу згідно з винаходом. ня продуктів побічних реакцій не повинно приймаЗгідно з винаходом N-[2-гідрокси-3-(1тися до уваги. Згідно зі способом даного винаходу піперидиніл)пропокси]піридин-1-оксид-3основну форму N-{2-гідрокси-3-(1карбоксамідин формули (I) перетворюють в N-[2піперидиніл)пропокси]піридин-1-оксид-3гідрокси-3-(1-піперидиніл)пропокси]піридин-1карбоксімідоїлхлориду одержують із високою чисоксид-3-карбоксімідоїлхлорид діазотуванням у тотою. До теперішнього часу цього можливо було присутності хлористоводневої кислоти. Діазотудосягти лише тривалою очисткою або шляхом вання здійснюють звичайним способом при темвиділення основи з малеатної солі. пературі між -5°С та 0°С шляхом повільного додаЩе однією перевагою винаходу є те, що N-{2вання нітриту лужного металу, переважно нітриту гідрокси-3-(1-піперидиніл)пропокси]піридин-1натрію. У присутності хлористоводневої кислоти оксид-3-карбоксамідин згідно з винаходом може отримана таким чином діазонієва сіль розкладабути одержаний шляхом об'єднання стадій, описається при температурі діазотування з утворенням них вище, що ілюструється в наступних прикладах N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1більш детально, без виділення і/або очищення оксид-3-карбоксімідоїлхлориду формули (V). Потім кожного проміжного продукту, одержуючи задовіреакційну суміш при охолодженні підлуговують, і льну чистоту. Таким чином, одержання проміжного продукт виділяють у формі основи звичайним меN-{2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1тодом. Отримана основа, при необхідності, в пооксид-3-карбоксамідин стає можливим в умовах дальшому може бути очищена або перетворена в фармацевтичного виробництва, що робить можкислотно-адитивну сіль із мінеральною або органіливим промислове одержання біологічно ефектичною кислотою. Переважно зі сполуки формули (V) вного N-[2-гідрокси-3-(1утворюють малеат або цитрат, але вона також піперидиніл)пропокси]піридин-1-оксид-3може бути перетворена у гідрохлоридну, дигідрохкарбоксімідоїлхлориду. лоридну або будь-яку іншу фармацевтично прийнВинахід ілюструється наступними прикладами. 7 75353 8 Приклад 1. 3-(1-піперидиніл)пропокси]піридин-1-оксид-3Одержання 3-ціанопіридин-1-оксиду (сполука карбоксамідину. Температура плавлення 142формули II) 144,5°С. 1 86г (0,378моль) 76% м-хлорпербензойної кисН-ЯМР: (Розчинник ДМСО; внутрішній станлоти розчиняють у 730мл дихлорметану при 20дарт ДМСО; МГц 75,4) [ч./млн.]: 9,65 (шс, 1Н, + 25°С і додають 220мл розчину 38,3 г (0,378моль) ΝΗ ); 8,42 (с, 1Н, 2-піридин); 822 (д, 1Н, 6-піридин); 3-ціанопіридину в дихлорметані при 20-28°С. Реа7,58 (д, 1Н, 4-піридин); 7,42 (т, 1Н, 5-піридин); 6,50 кційну суміш перемішують при 20-24°С протягом (с, 2Н, NH2); 5,72 (д, 1Н, ОН); 4,24 (шм, 1Н, ОСН); 24 годин. В кінці реакції розчинник випарюють. 3,86 (м, 2Н, NOCH2); 3,42 (м, 2Н, 2 x NCHeq); 3,18 Залишок після випарювання розтирають з 430мл (м, 2Н, NCH2); 2,92 (м, 2Н, 2 x NCHax); 1,36-1,8 (м, метил-трет-бутилового естеру, осад відфільтро6Н, 3-, 4- та 5-піперидин). 13 вують, промивають і висушують. Одержують 59г С-ЯМР: (Розчинник ДМСО; внутрішній станнеочищеного продукту. дарт ДМСО; МГц 75,4) [ч./млн.]: 148,2 (CNO); Шляхом двічі проведеної перекристалізації 139,2(2-піридин); 135,9 (6-піридин); 131,8 (3неочищеного продукту з гарячого етанолу одерпіридин); 126,3 (5-піридин); 122,9 (4-піридин); 74,9 жують 36,6г (80%) чистого 3-ціанопіридин-1(СНОН); 63,6 (NOCH2); 58,9 (NCH2); 53,6 та 51,9 оксиду, який плавиться при 174-176,5°С [літерату(2С, 2 x піперидин NCH2); 22,1 (2С, 3- та 5рні дані: 174-175°С, J.Cherrt.Soc. - 3680 (1959)]. піперидин ); 21,2 (4-піперидин). Приклад 2. CI- вміст Згідно з методикою Mohi (розраховаОдержання 3-піридинамідоксим-1-оксиду (споно /отримано): 10,7/10:45 лука формули III) Приклад 4. 25,41г (0,366моль) гідрохлориду гідроксиламіа) Одержання N-[2-гідрокси-3-(1ну та 36,6г (0,305моль) 3-ціанопіридин-1-оксиду піперидиніл)пропокси]піридин-1-оксид-3розчиняють в 540мл води, потім невеликими поркарбоксімідоїлхлориду (Сполука формули V) ціями додають 30,72г (0,366моль) гідрокарбонату Розчин 6,1г (0,088моль) нітриту натрію в 40мл натрію. Реакційну суміш перемішують протягом 2 води додають по краплям при -5 - 0°С до розчину годин при 20-25°С. Суспензію відфільтровують, 20г (0,068моль) N-[2-гідрокси-3-(1осад промивають водою, висушують і перекристапіперидиніл)пропокси]піридин-1-оксид-3лізовують із суміші метанолу та води 9:1. Утворекарбоксамідину в 110мл 1М розчину хлороводнений при охолодженні осад відфільтровують, прової кислоти, охолодженої до -5°С. Реакційну суміш мивають і висушують. Отримують 37,3г (80%) перемішують протягом 1,5 годин при температурі указаної в заголовку сполуки, яка плавиться при між -5°С та 0°С і потім при інтенсивному охоло212-215°С з розкладанням. дженні (t
ДивитисяДодаткова інформація
Назва патенту англійськоюN-[2-hydroxy-3-(1-piperidinyl)propoxy]piridine-1-oxide-3-carboxamidine and a method for transformation thereof into pharmaceutically effective compounds
Назва патенту російськоюN-[2-гидрокси-3-(1-пиперидинил)пропокси]пиридин-1-оксид-3-карбоксамидин и способ его преобразования в фармацевтически эффективные соединения
МПК / Мітки
МПК: C07B 57/00, C07D 213/89
Мітки: фармацевтично, n-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідин, ефективні, перетворення, спосіб, сполуки
Код посилання
<a href="https://ua.patents.su/7-75353-n-2-gidroksi-3-1-piperidinilpropoksipiridin-1-oksid-3-karboksamidin-ta-sposib-jjogo-peretvorennya-u-farmacevtichno-efektivni-spoluki.html" target="_blank" rel="follow" title="База патентів України">N-[2-гідрокси-3-(1-піперидиніл)пропокси]піридин-1-оксид-3-карбоксамідин та спосіб його перетворення у фармацевтично ефективні сполуки</a>
Попередній патент: Штам бактерії bacillus circulans b-65 – продуцент цикломальтодекстринглюканотрансферази, спосіб його виділення та застосування для одержання b-циклодекстрину
Наступний патент: Спосіб одержання комбінованого профілю і комбінований профіль
Випадковий патент: Кристали похідних 6,7-ненасиченого 7-карбамоїлморфінану і спосіб їх отримання