Гідрохлориди діфенілпропіламіну, що мають антиангінальну активність
Номер патенту: 3466
Опубліковано: 27.12.1994
Автори: Д'юла Папп, Єва Удварі, Золтан Варгаі, Імре Бата, Каталін Мармароші, Віра Гергелі, Габор Ковач, Дежьо Корбонітш, Андрео Шанта, Петер Кьормеці, Пал Кішш, Шандор Віраг, Ласло Секереш, Ласло Тардош
Формула / Реферат
Пидрохлориды дифениппропиламина формулы
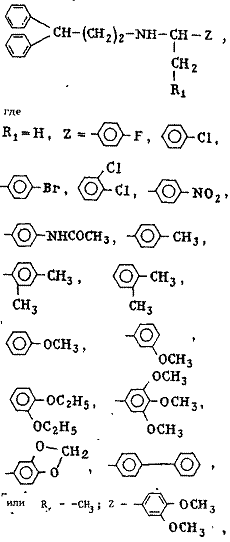
обладающие антиангинальной активностью.
Текст
Изобретение касается замещеннь-х диФенилпропилчмина, в частности их гидрохлоридов общей ф-лы I : (С^Н$-)2СН-(CH 2 ) l -NH-CHZ-CH l R 1 > где R, - Н при 2 - а ) 4 - F - C t H 4 ; 4-С1(нлн 4-Вг)~С 6 Н 4 ; 3,4-ди-С1-С 6 Н^; 4-NO^-CfcH4; 4-CH а Изобретение относится к новым с о е динениям - производным дифенилпропиламина, обладающим антиангиналь- • ной активностью. Цель изобретения - выявление в р я ду производных дифенилпропиламина но б) R, - С Н 3 при Z - 3,4-ди-СН э О-С с Н 5 , обладаюпаїх антиангинальной активностью, что может быть использовано в медицине. Цель - создание новых более активных веществ указанного класса. Синтез ведут, например, конденсацией 1-(3,4 -диметоксифенил)-!аминопропана с бенчальдегидом в присутствии пиридина в среде метанола с последующим восстановлением тетраборатом натрия, обработкой 2-хлорэтанолом в среде диметилформамида при 70°С и затем тионилхлоридом в среде хлороформа при нагревании (все промежуточные продукты выделяют). Новые соединения проявляют активность при э&фективной дозе ЭДу- = = 0,054 мг/кг против 1,5 для известного фендилина, при отсутствии кардиодепрессивного действия, наличии более длительного эффекта и меньшей токсичности. 2 табл. вых соединений с более высокой антиангинальной активностью П р и м е р 1. а. Смесь из 3,3дифенил-пропиламин? (84,5 г, 0,4 моль) к 3,4-димеіокси-ацетобенона (72,1 і , 0,4 моль) выдержива 00 1588740' * токси-адетофенона (18,0 г, 0,1 моль),, ют при перевешивании в течение 200 с м 3 этанола и 2 г 10%-ного палла10 ч при 90°С и под давлением 130— 160 Па, причем образующуюся воду дия на активном угле гидрируют под постоянно отгоняют. Масса ставшего давлением 1,0 МПа, После фильтрации, твердым после охлаждения сырого Nвыпаривания> солеобразования с соля^-метил-3,4-диметоксибенэилиден)нокислым этилацетатом и кристалли3,3-дифенил-прогшламина составляет зации из этанола получают 2 7,2 г 149,5 г (теоретический выход). Т.пл, 10,6 г бенэтанола и 2 г 10%-ного палладия на зчльдегида, 100 с м 5 метанола и ! капактивном у г л е , согласно примеру 1в. ли пиридина оставляют стоять в течение I дней при 20 С, затем в течение Получают 31,5 г (84%) KHL-8430. 30 чин к смеси добавляют 3,8 г тетрад . Смесь из 3,3-дифенил-пропиліидробората натрия и перемешивают в амина (21,1 г, 0,1 моль) ^3,4-диме 5 1538740 течение 3 ч . Растворитель отгоняют, прекращения газообразования). Оставшуюся после выпаривания соль растворяостаток разбавляют водой, экстрагируют п воде, при охлаждении льдом подщеют хлороформом, высушивают и хлоролачивают н экстрагируют эфиром. Эфирформ выпаривают. Таким образом полуный раствор сушат над сульфатом натченный 1-фенил-3-(3,4-диметоксиферия, отфильтровывают. После отгонки нил)-2-азабутан (27,1 г) можно неэфира получают в виде масла образопосредственно применять в описанном вавшийся l - ( N - ( 1- (3 5,4-диметок сифез примере 6 способе. нил) -этан-1 -ил) -:М-бенэил)-амино-2to П р и м е р 3 . К смеси из ! 8 , 1 г хлорэтан, 1-(3,4-диметоксифенил)~1-аминоэтана, 16,5 г этого сырого масла раство15 г карбоната калия и 100 см бутаряют в 100 см бензола и при пе^еменола при перемешивании и нагревании Етизании в течение 2 ч нагревают с в течение примерно 1 ч добавляют 9,7 г дифенилацетонитрила и 2,5 г 50 с м 3 бутанэльного раствора 23,7 г амида натрия * После охлаждения приме1-хлор-3,3-дифенилпропана и нагревашивают воду, отделяют беззольную фают далее вплоть до прекращения г а з о зу, отфильтровывают и выпаривают. образования. После охлаждения отфильтОстаток растворяют в дизтиловом эфировывают, выпаривают и получают с о г - 20 ре, полученный с помощью солянокисласно примеру 16 28,5 г KHL-8430, лого этанола 1,1-дифенил-1-циано-3' т . п л . которого составляет !71-173 С. (^-(1-(3,4-диметоксифенил)-этан-1-ил)П р и м е р а * Смесь из 21,0 г N-бензил)-аминопропангидрохлорид крис1-амино-3,3-дифекіил-пропана, 24,5 г таллизуют из э т а н о л а . 10 г таким 1-бром-1-(3,4-димстоксифенилэтана), 25 образом полученного гидрохлорида 15 г карбоната калия и 80 см диметилрастворяют в 100 с м 3 воды, при охлажформамида перемешивают в течение 15 ч дении подщелачивают, экстрагируют при 50°С и отфильтровывают. Раствори100 с м 3 бензола, сушат над суль&атель отгоняют при пониженном давлетом натрия и отфильтровывают. Фильтнии и остаток обрабатывают хлорофор30 рат вместе с 10,0 г амида натрия при мом. После солеобразования согласно перемешивании нагревают 2 ч , после примеру 16 и.двукратной кристаллизаохлаждения отфильтровывают и выпариции из водного этанола получают вают. Остаток растворяют в 50 см 24,0 г KHL-8430, т . п л . которого с о с концентрированной уксусной кислоты тавляет 17]-173°С. р и м е р 5. 180 с м 3 этанольио- 35 и гидрируют с помощью 0,1 г катализатора на основе оксида платины при го раствора 21,0 г 3,3-дифенилпропио70°С и давлении 0,4 МПа (примерно НОБОГО альдегида и 18,1 г 1-(3,4-ди~ в течение 5 ч ) . Смесь разбавляют метоксифенил)-1-аминоэтана нагревают 50 см метанола, отфильтровывают, выв течение 40 мин, затем смесь после 40 паривают, путем легкого нагревания с добавления 2 с м 3 воды при 33-35°С солянокислым этанолом получают с о л ь . в течение 30 мин вводят во взаимодейПосіє кристаллизации из водного э т а ствие с 4 г тетрагидробората натрия. нола получают 6,2 г KHL-8430, котоПосле отгонки спирта остаток обрабатырый плавится при 171-172 С. вают водой, экстрагируют хлороформом 45 П р и м е р ? . 15,1г* 1-фенил-1и хлороформный раствор обрабатывают окси-3-аминопропана и 19,0 г 3,4-дисогласно примеру 1 б. метоксиацетофенона перемешивают в Получают 30,0 г KHL-8430 с т . п п . течение 16 ч при 80 С и давлении 171—173°С (из водного э т а н о л а ) . 130-160 Па, затем охлаждают, смешиваП р и м е р 6. К 27,1 г 1-фенил-З50 ют со смесью 50 с м 3 метанола и 2 см 3 О,4-диметоксифенил)-2-азаГутана ( п о воды и вводят во взаимодействие с лучен согласно примеру 2б) в 80 с м 3 3,5 г тетрагидробората натрия при диметилформамида при 70 С при пере30-40 С в течение 2 ч . После отгонки мешивании в течение 1 ч прикапывают растворителя остаток растворяют в 7,! г 2-хлорэтанола, Перемешивают 55 еще 5 ч , затем отфильтровывают. Ф и л ь т Ю0 см* эфира и с помощью солянокис3 рат выпаривают, растворяют в 150 с м лого этанола получают соль. Таким хпороформа и нагревают в течение 1 ч образом полученный сырой I-фенил-13 с 20 см тионилхлорнда (вплоть ло OKCH-3-(N-3-(3,4-диметоксифешш) . 1588740 ч т і м - ! -ил)~нминонропанхлг>рид суспендирую'Е в 100 см бензола, при перемешивании в течение 40 мни добавляют чО см' тиокилхлорида, суспензию пере- ,мешивают еще следующий час при 40°С. Смесь выпаривают с помощью водоструйного -насоса (максимально при 40 С) остаток растворяют в 100 с м 3 бензола, вводят во взаимодействие при 55-60°С ю н течение 1 ч с хлоридом алюминия, затем при нагревании следующие 2 ч . После охлаждения смесь выливают в солянокислый л е д . Вензольную фазу отделяют и бензол вымывают водой. Объеди- 15 иенные водные фазы сильно подщелачивают при охлаждении льдом, э к с т р а г и руют эфиром, эфирную фазу высушивают над сульАатом натрия. Затем с помощью солянокислого этанола получа20 ют соль. Таким образом получают плавящийся при І 72-173°С KHL-8430. П р и м є р в . К 1 5 , 8 г основания 2,6,6-три&енил-3-азагексана (Фендилин) при охлаждении добавляют 5,9 г 98-100%-ной муравьиной кислоты, з а тем добавляют к полученному густому маслу в течение 5 мин 5,7 г 30%-ного водного раствора Формальдегида. Смесь выдерживают при 40 С вплоть до начала газовыделения, затем нагревание прекращают на 30 мин. После этого смесь перемешивают в течение 12 ч при 80 С и выпаривают, остаток растирают с 100 см 5%-ного раствора соляной кислоты, нагревают в течение 10 мин на водяной бане, при охлаждении подщелачивают. Основание э к с т р а гируют хлороформом, высушивают, отфильтровывают и выпаривают, остаток растворяют в эфире и с солянокислым эфиром получают с о л ь . Получают 14,2 г 3-метил-2,6,6-трифенил-3-азагексангндрохлорида, который плавится при 96°С. 25 8 8430, который имеет т . п л . 171-173"С (из водного э т а н о л а ) . П р и м е р 10. К смеси из 21,0 г 1,1-дифенил-З-амино-пропана и 10,5 г гидрокарбоната натрия в течение 2 ч при кипении и перемешивании прикапывают 30 см бутанольного раствора 24,5 г 1-бром-1-(3,4-диметоксифенил)э т а н а . Нагревают далее вплоть до прекращения газообразования, после охлаждения и фильтрации отгоняют р а с т воритель, и из остатка в эфирном растворе с помощью солянокислого этанола получают соль. Трижды кристаллизуют из водного этанола, получают 18,0 г KHL-843O, т . п л , которого 171~173°С. П р и м е р ы 11-52. С помощью описанных в примерах la и 16 способов и с таким же выходом можно получать указанные в табл.1 соединения общей формулы ( I ) (R, в каждом случае ^ атом водорода). Предлагаемые соединения обладают антиангинозным действием. Действие 2-(4-хлорфенил)-6,6-дифенил-3-азагексангидрохлорида при вызванной 30 вазопрессином острой коронарной н е достаточности у крыс чрезвычайно сильное. При внутривенном введении за 2 мин до возбуждения ангины за счет вазопрессина ЭД для этого соединения составляет 0,054 м г / к г . По срав35 нению с этим измеренное Э Д ^ - з н а ч е н и е фендилина (известного структурного аналога) в подобных условиях с о с т а в ляет 2,30 м г / к г . Указанное соединение в этих условиях примерно в 42 раза 40 активнее, чем фендилин» Соединения этого типа обладают не только характерным для фендилина более сильным и более продолжительным 45 антиангинозным действием, но и облаі дают неожиданно также другими предпочтительными в терапии заболеваний П р и м е р 9, Смесь из 30,0 г сердца действиями нового типа. 2 - ( 3 , 4 I,5,5-трифенил-З-азапентана, Диметоксифенил)-6,6-дифенил-З-азагек24,5 г 1-бром-1-(3,4-диметокснфснил)сан (обозначение для гидрохлорида этаиа, 15,0 г карбоната калия и 50 этого соединения в дальнейшем KHLъ 100 см диметилформамида перемешива8430) при вызванной вазопрессином ют в течение 16 ч при 70 С. Фильтруангине у крыс с о о т в е т с т в е н н о при ют , растворитель отгоняют, остаток 3 вызванных закупоркой коронарных сосув 100 см уксусной кислоты гидрируют дов (коронарной окклюзией) ишемичесс помощью 0,5 г оксида платины при 55 ких состояниях у собак превышает фенs 70 *С и давлении 0,4 Па, разбавляют s дії лин по силе и продолжительности 100 гм метанола и фильтруют, растволечебного действия, кроме т о г о , он ритель отгоняют. Из остатка согластакже при внутривенном и перорально примеру 16 получают 30,0 г KHL 1588740- 'О Ф о р м у л а и з о б р е т е н и я ном введении менее токсичен, чем Гидрохлориды дифениппролиламина стандартное вещество. формулы В случае вызванной вазопрессином ангины у крыс измеренная спустя 2 мин после внутривенного введения и соответственно спустя 60 мин после перорального введения антиангинозная активность, измеренные у крыс внутривенно и перорально значения острой токсичности, терапевтические индексы и относительность терапевтических индексов в отношении KHLгде 8430 и фендилина указаны в табл.2. 15 Соединения общей формулы (I) в противоположность фендилину и другим антагонистам кальция не обладают кардиодепрессивным действием, что представляет собой предпочтительное преимущество предлагаемых соединений. і . • Антиангинальная активность синтезированных соединений следующая*. Антиангинальная Пример активность Ы ) ^ , мг/кг i.V II 12 13 15 17 П 40 39 18 21 27 ІІ 21 36 1 50 52 Фендилин (соединение для сравнения) 1,46 0,054 0,48 1,15 0,78 1,40 25 30 осн 3 ОСН3 35 0,68 1,35 0,92 0,36 0,39 0,94 0,56 1,02 ос 2 н 5 сн2 осн 1,52 1,52 1,52 2.30 или Z обладающие антиангинальной активностью. 11 12 588740 Т а б л и ц а 1 • R Z 1 2 3 tl H неї 12 H неї 13 Н НС1 14 Н Мапеиновая 142 15 Н неї 188 16 Н НС1 197-198 17 Н НС1 22,7-228 Пример 8 . Кислота 4 -Q-C, . Температура плавления,0 С 5 176-178 78 Н -{[}-ОСЇІ3 НС1 194-196 19 Н HQ-OC 2 H 5 неї 186-188 20 Н 21 Н Н С 1 208-209 НС1 160-162 НС1 215-220 неї 186-188 неї 187-188 ОСН, 22 Н 23 Н -ГХ СИ, О v^n/ СН,0 ОСНз 1 ІЗ 1538740 25 Продолжение табл.I неї 178-182 неї 171-172 неї 149-15! неї 129-132 неї 182-184 неї 201-203 неї 198-200 неї 180-181 33 неї 188-189 34 неї 181-183 ЇТСІ 124-127 сн3о 26 Н 27 Н -Q-OC2H5 о"с 3 н 7 28 о"с 4 н 9 '19 о1с4н9 осн 3 (OVocHj осн3 ЗО ЗІ И осн, сн3о 32 осн3 сн, н 35 н з* Н 37 38 н н (2)з-СН3 103-112 НС1 . 202-205 НС1 199-201 неї 236-238 неї СЯз 226-227 сн, 39 ся, сн, 40 Н осн, S38740 Продолжение 2 _____ \ 41 табл.1 г 5 3 _ .. L Н НС1 212-214 неї 181-183 ос 2 н 5 42 Н -(ОУ- оск 3 сн3 43 Н "О" осн з неї 192-194 неї 228-229 С1 44 н С1 СИ, осн, 45 -С1 неї но 46 сн, 47 си. 48 сн. Калеиновая кислота 49 сн. неї 217-218 50 сн. неї 213 неї 140-142 неї 98-101 51 С1 Вт сн 5 2 Маленновая кислота НС1 141-143 200 !24-I26 Т а б л и ц а '1 Внутривенно Орально Соединение мг/кі * мг/кг 0,34 2,30 KHL-8430 Фендилнн 16,0 1?,2 Относительность индексов KHL-8430 фендилин зді0, 1 і 400 800 Относительность индексов" мг /кг 20,0 47,1 5,3 кг/кг 8,89 !66,7 40,0 4,17 Зака-ч 2515 ВНИИИИ Г о с у д а р с т и о н н о ї Составитель Л, Иоффе Техред Л.Олнинмк Корректор С. Шевкун Тираж 350 Редактор Н, Кпштулинеп Подписное о комитета ІП'-Гі, MuuMja, по іпоПрстсниям и открытиям Ж - З Ь , І ' а у і і ч к . і н н.»С»., П р о и з в о д с т в є н м о - и з д . 11 ^ ii.t м і й к о м б и н а т "Пліч* пі " . д. п р и ГКН'Г СССР і/5 І Л'лг'фол, ул . Г а г а р и н а , І')]
ДивитисяДодаткова інформація
Автори англійськоюKishsh Pal, Gabor Kovacs, Shandor Virah, Katalin Marmarosi, GERGELI VERA, VARGAI ZOLTAN
Автори російськоюПал Кишш, Габор Ковач, Шандор Вераг, Каталин Мармароши, Вера Гергели, Золтан Варгаи
МПК / Мітки
Мітки: гідрохлориди, активність, діфенілпропіламіну, мають, антиангінальну
Код посилання
<a href="https://ua.patents.su/8-3466-gidrokhloridi-difenilpropilaminu-shho-mayut-antianginalnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Гідрохлориди діфенілпропіламіну, що мають антиангінальну активність</a>
Попередній патент: Пристрій для очистки внутрішньої поверхні трубопроводу
Наступний патент: Пристрій для виявлення течі в підземних трубопроводах
Випадковий патент: Тензометричний датчик тиску












