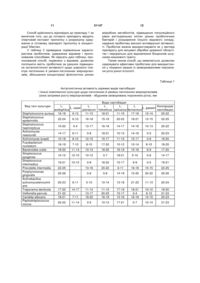
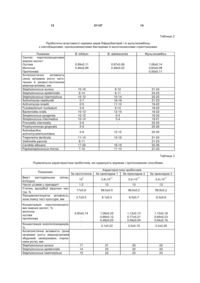
Спосіб одержання пробіотика “стомабакт” для лікування хворих із захворюваннями порожнини рота
Номер патенту: 51147
Опубліковано: 12.07.2010
Автори: Янковський Дмитро Станіславович, Широбоков Володимир Павлович, Димент Галина Семенівна
Формула / Реферат
1. Спосіб одержання пробіотика для лікування хворих із захворюваннями порожнини рота, що передбачає використання лактобацил і сорбенту, який відрізняється тим, що до складу пробіотика додатково вводять біфідобактерії видів Bifidobacterium adolescentis й В. bifidum, пропіоновокислі бактерії видів Propionibacterium freudenreichii ssp. shermanii і P. acidipropionici, молочнокислі стрептококи видів Lactococcus lactis й Streptococcus salivarius ssp. thermophilus, з лактобацил додатково вводять види Lactobacillus acidophilus, L. casei, L. helveticus, L. gasseri й L. salivarius, при цьому багатовидовий комплекс мікроорганізмів використовують у вигляді концентрованої біомаси мультикомпонентного симбіозу, а як сорбент використовують 5-6 %-й гель дрібнодисперсного бентоніту, з яким змішують біомасу пробіотичних бактерій у співвідношенні 1:2-1:3.
2. Спосіб за п. 1, який відрізняється тим, що до складу пробіотика додатково вводять спиртовий екстракт прополісу.
3. Спосіб за п. 1, який відрізняється тим, що до складу пробіотика додатково вводять йод у вигляді водного або спиртового розчину дрібнокристалічного йоду і йодиду калію.
4. Спосіб за п. 1, який відрізняється тим, що до складу пробіотика додатково вводять протимікозні препарати.
Текст
1. Спосіб одержання пробіотика для лікування хворих із захворюваннями порожнини рота, що передбачає використання лактобацил і сорбенту, який відрізняється тим, що до складу пробіотика додатково вводять біфідобактерії видів Bifidobacterium adolescentis й В. bifidum, пропіоновокислі бактерії видів Propionibacterium freudenreichii ssp. shermanii і P. acidipropionici, молочнокислі стрептококи видів Lactococcus lactis й Streptococcus salivarius ssp. thermophilus, з лакто U 2 (19) 1 3 захворювання верхніх і нижніх дихальних шляхів у багатьох випадках також прямо пов'язані із тривалим перебігом запальних процесів у порожнині рота. Розташування ротової порожнини поблизу головного мозку викликає ризик ураження центральної нервової системи патогенними мікроорганізмами при їхньому надлишковому розмноженні в ротоглотці з можливим розвитком менінгіту й інших небезпечних хвороб. Найнебезпечнішими для ротової порожнини збудниками інфекційно-запальних процесів є деякі представники родів Actinomyces, Bacteroides, Prevotella, Porphyromonas, Actinobacillus, Treponema, Peptostreptococcus, Veillonella, Candida, Aspergillus, а також патогенні види стафілококів і стрептококів. Лікування інфекцій, як правило, засновано на використанні етіотропних хіміопрепаратів, які здатні ще більше поглиблювати мікроекологічні порушення, що згодом приводить до розвитку численних рецидивів хвороби. В зв'язку з викладеним, особливу актуальність мають питання профілактики й лікування захворювань порожнини рота з використанням препаратів на основі натуральних інгредієнтів, що сприяють підтриманню й відновленню мікробної екологічної системи як ротової порожнини, так і всього організму. Останнім часом розширилося використання пробіотичних препаратів у комплексному лікуванні хворих з інфекційно-запальними захворюваннями слизової оболонки ротової порожнини, глотки й тканин пародонту, зокрема стоматиту, пародонтиту, гінгівіту й ін. Відомо бактеріальний препарат «Ацилакт», який використовують у комплексному лікуванні хворих пародонтитом (Пожарицька М.М., Морозова Л.В., Мельничук Г.М., Мельничук С.С. Застосування нового бактеріального біопрепарату «Ацилакт» у комплексному лікуванні пародонтиту // Стоматологія. - 1994. - №2. - С. 17-20). Пробіотик містить комплекс молочнокислих бактерій виду Lactobacillus acidophilus з високою антагоністичною активністю щодо ряду патогенних й умовно-патогенних мікроорганізмів, що забезпечує пригноблення збудників запального процесу й сприятливо позначається на стані тканин пародонту. Однак моновидовий пробіотик не може забезпечити стабільне відновлення біоценозів ротової порожнини й кишечнику й пригнічення широкого спектра патогенних й умовно-патогенних мікроорганізмів, у зв'язку із чим використання препарату не дозволяє попередити часті рецидиви хвороби. Відомий спосіб одержання препарату для лікування хворих запальними захворюваннями пародонту передбачає введення в розчин колагену суспензії клітин штаму молочнокислих бактерій Lactobacillus casei 37 з концентрацією клітин 108 КУО/мл і приготування препарату у вигляді лародонтальної пов'язки, що складається з живих клітин молочнокислих бактерій виду Lactobacillus casei і колагену (Воложин А.І., Ільїн В.К., Максимовський Ю.М. й ін. Розробка і застосування пародонтальної пов'язки з колагену й суспензії клітин Lactobacillus casei 37 у комплексному лікуванні запальних захворювань пародонта // Стоматол. 2004. - Т.83. - №6. - С. 6-11). 51147 4 Використання у складі препарату лактобацил виду Lactobacillus casei дозволяє знизити концентрацію окремих видів патогенних й умовнопатогенних мікроорганізмів, проліферуючих на слизовій оболонці порожнини рота хворих і зменшити запальну реакцію у пародонту. Введення до складу препарату колагену поліпшує репаративні процеси в тканинах. Однак використання одного штаму пробіотичних бактерій не забезпечує достатній лікувальний ефект. Найбільш близьким до способу, що заявляється, є спосіб одержання препарату «Лактобактерин, іммобілізований на колагені», що передбачає іммобілізацію суспензії клітин молочнокислих бактерій видів Lactobacillus plantarum або L. fermentum на стерильному іхтіоколі (колагені плавальних міхурів осетрових риб) і одержання колагенових пластин зі вмістом клітин життєздатних лактобацил не менш 107 КУО/пластину (Гаків А.І., Ільїн В.К., Істранов Л.П. та ін. Вплив короткострокового застосування пробіотика, що містить лактобактерії, на мікрофлору глотки здорових осіб // Вісник оториноларингологи. - 2008. - №5. - С. 51-53, прототип). Завдяки високій антагоністичній активності штамів лактобацил, які уводять до складу препарату, його застосування у лікуванні хворих запальними захворюваннями глотки дозволяє знизити титр умовно-патогенної мікрофлори, що колонізує слизову оболонку глотки, і зменшити інтенсивність запального процесу. Використання іммобілізованої форми клітинної суспензії із застосуванням як сорбенту-носія колагену дозволяє забезпечити пролонгований ефект пробіотика й поліпшити репаративні процеси в тканинах. Однак використання одно- або двуштамового пробіотика не дозволяє забезпечити достатню санацію ротової порожнини, пригнічення широкого спектра збудників інфекційно-запального процесу й відновлення нормобіозу ротоглотки, у зв'язку із чим високим залишається ризик частих рецидивів хвороби. За рахунок здатності колагену швидко розсмоктуватися в тканинах він не може забезпечити ефективне виконання функції сорбенту й виводити з біотопу шкідливі сполуки, зокрема токсини, канцерогени й інші речовини, які утворюються у значній кількості у патологічних умовах за рахунок метаболізму патогенної й умовно-патогенної мікрофлори й перебігу запальних процесів. Крім того, ряд патогенних мікроорганізмів синтезують активні колагенази і за рахунок цього швидко розщеплюють колаген, використовуючи його як білковий субстрат, внаслідок чого спостерігається посилена проліферація цих мікроорганізмів у біотопі й ускладнення хвороби. Низька концентрація клітин лактобацил у препараті є перешкодою для здійснення одночасного пробіотичного впливу на мікробні біоценози ротоглотки й шлунково-кишкового тракту, при цьому в організмі зберігається потужне вогнище мікроекологічних порушень, внаслідок чого неминучі рецидиви хвороби. Завданням корисної моделі є створення способу одержання пробіотика для лікування хворих із захворюваннями порожнини рота, у якому шляхом розширення складу пробіотичних мікрооргані 5 змів і використання гелю дрібнодисперсного бентоніту, забезпечується підвищення ефективності препарату й розширення сфери його застосування. Поставлене завдання вирішується тим, що в способі одержання пробіотика, що передбачає використання лактобацил і сорбенту, відповідно до корисної моделі, до складу пробіотика додатково вводять біфідобактерії видів Bifidobacterium adolescentis і В. bifidum, пропіоновокислі бактерії видів Propionibacterium freudenreichii ssp. shermanii й P. acidipropionici, молочнокислі стрептококи видів Lactococcus lactis й Streptococcus salivarius ssp. thermophilus, з лактобацил додатково вводять види Lactobacillus acidophilus, L. casei, L. helveticus, L. gasseri й L. salivarius, при цьому багатовидовий комплекс мікроорганізмів використовують у вигляді концентрованої біомаси мультикомпонентного симбіозу, а як сорбент використовують 5-6%-й гель дрібнодисперсного бентоніту, з яким змішують біомасу пробіотичних бактерій у співвідношенні 1:2-1:3. Крім того, для підвищення антагоністичної активності пробіотика щодо патогенної й умовно-патогенної мікрофлори до складу препарату вводять спиртовий екстракт прополісу, або йод, або протигрибкові препарати. Запропонований спосіб передбачає використання в складі пробіотика додаткових видів лактобацил: Lactobacillus acidophilus, L. casei, L. helveticus, L. gasseri й L. salivarius, а також введення біфідобактерій видів Bifidobacterium bifidum i Bifidobacterium adolescentis, пропіоновокислих бактерій видів Propionibacterium freudenreichii ssp. shermanii і P. acidipropionici, молочнокислих стрептококів видів Lactococcus lactis і Streptococcus salivarius ssp. thermophilus. Введення до складу препарату додаткових представників роду Lactobacillus дозволяє підвищити його антагоністичну активність щодо патогенних й умовно-патогенних мікроорганізмів. Антагоністичні властивості кожного зі штамів лактобацил, які використовуються у складі препарату, підсумовуються в комплексній культурі (консорціумі) із проявом синергізму (табл. 1). Біфідобактерії видів Bifidobacterium bifidum й Bifidobacterium adolescentis підсилюють антагоністичну активність пробіотика і його репаративні властивості щодо слизової оболонки ротової порожнини й шлунково-кишкового тракту. За рахунок здатності синтезувати лізоцим, коротколанцюгові жирні кислоти й високої щільності формованих клітинних популяцій, використовувані в способі біфідобактерії активно пригнічують ріст широкого спектра патогенних й умовно-патогенних мікроорганізмів. Молочна й оцтова кислоти, що накопичуються у результаті сахаролітичного метаболізму біфідобактерій, служать енергетичним і трофічним субстратом для епітеліальної тканини й прискорюють її відновлення. Використання у складі препарату біфідобактерій дозволяє не тільки підсилити пробіотичний вплив на слизову оболонку ротоглотки, але й сприяє ефективній нормалізації мікрофлори шлунково-кишкового тракту. Біфідобактерії, уведені до складу препарату, здатні досягти в активному стані області товстої кишки й реалізу 51147 6 вати в ній свій пробіотичний потенціал. Спеціально проведені дослідження встановили, що пробіотичні властивості біфідобактерій значно підсилюються в мультикомпонентному симбіозі з лактобацилами, пропіоновокислими бактеріями й молочнокислими стрептококами (табл. 2). Використання в складі пробіотика пропіоновокислих бактерій сприяє доповненню його кислотосинтезуючої функції продукцією пропіонової кислоти, що має виражену антимікозну дію. Завдяки присутності пропіоновокислих бактерій, пробіотик здобуває здатність синтезувати вітаміни, у тому числі вітамін В12, який виконує в організмі важливі фізіологічні функції. Антимікробними метаболітами пропіоновокислих бактерій є специфічні бактеріоцини - пропіоніни, що характеризуються широким спектром антибактеріальної, антимікозної й антивірусної дії. Молочнокислі стрептококи видів Lactococcus lactis і Streptococcus salivarius ssp. thermophilus конкурентно витісняють із біотопів патогенні й умовно-патогенні стрептококові клони. Крім того, ці мікроорганізми продукують полісахариди, що мають імуностимулюючі властивості, і активізують ріст інших складових мультикомпонентного симбіозу. Пропонований спосіб передбачає також змішування отриманої після культивування клітин багатовидового симбіозу в поживному середовищі біомаси з 5-6%-м гелем бентоніту. Бентоніт - це природний глинистий матеріал, що відноситься до класу алюмосилікатів і має високі вологоутримуючі, іонообмінні й адсорбційні властивості. Здатність бентоніту до набрякання й адсорбції стала підставою для широкого використання його у фармацевтичній промисловості, зокрема як основи для мазей. У пропонованому способі як сорбент використовують гель бентоніту, що є натрієвою формою дрібнодисперсної фракції бентоніту, яку одержують із сухого природного бентоніту шляхом обробки його вуглекислим натрієм й очищення від забруднюючих речовин і грубих часток. Використання як сорбенту гелю бентоніту не вимагає проведення операції з іммобілізації бактеріальних клітин, при якій губиться значна частина клітин. Гель бентоніту має високі адсорбційні властивості щодо вірусів, однак він не зв'язує бактеріальні клітини, тому має високу ефективність виведення з організму збудників вірусних інфекцій і різних токсинів, не порушуючи при цьому мікробного балансу в біотопах і не викликає метаболічих порушень. При змішуванні концентрованої біомаси з гелем бентоніту дрібнодисперсний сорбент зв'язується з поверхневими структурами бактеріальних клітин і покриває їх захисним шаром, охороняючи від впливу інгібуючих факторів й оптимізуючи умови для розвитку. Бентоніт є цінним джерелом макро- і мікроелементів. Завдяки здатності активно зв'язувати воду, набухати й формувати гелі, бентоніт, на відміну від багатьох інших сорбентів, не здатний впливати на слизові оболонки, а навпроти, сприяє зміцненню слизового бар'єра. У той же час здатність гелю бентоніту активно адсорбувати віруси дозволяє наділити 7 пробіотик високою антивірусною активністю. Велике значення має здатність гелю бентоніту санувати ротову порожнину за рахунок сорбції й виведення ферментів патогенності бактерій, токсинів, що утворюються в великій кількості під час перебігу інфекційно-запальних процесів і грають украй негативну роль, зокрема за рахунок перевантаження імунної системи й формування імунодефіцитних станів. У способі використовують гель, що містить 56% бентоніту. Зниження концентрації бентоніту менш 5% призводить до зменшення протекторної дії гелю бентоніту відносно пробіотичної мікрофлори й адсорбції вірусів і токсинів. Збільшення концентрації бентоніту в гелі вище 6% недоцільно, оскільки не сприяє помітному збільшенню захисних властивостей щодо мікрофлори пробіотика й антивірусної активності, але приводить до зайвого ущільнення консистенції препарату. Клітинну біомасу змішують із 5-6%-м гелем бентоніту у співвідношенні 1:2-1:3. Дане співвідношення є найбільш оптимальним. Як показали спеціально проведені дослідження, гель бентоніту в зазначеній концентрації має високі протекторні властивості щодо біомаси багатовидового симбіозу, що є бактеріальною основою пробіотика, оптимізує умови для розвитку пробіотичної флори. У присутності гелю бентоніту, одержаного спеціальним способом, значно краще зберігається бактеріальний склад й активність пробіотичної біомаси. Гель бентоніту відрізняється м'яким впливом на слизову оболонку, не здатний травмувати її або викликати метаболічні розлади, тому пробіотик з використанням гелю бентоніту можна використовувати тривалими курсами без небезпеки розвитку побічних реакцій. Зміна співвідношення убік зменшення частки гелю бентоніту призводить до зниження ефективності пробіотика. Збільшення кількості гелю бентоніту недоцільно, оскільки не сприяє поліпшенню пробіотичних властивостей, але приводить до зниження концентрації клітин у пробіотику і його активності. Одержуваний пропонованим способом препарат може використовуватись як для місцевої обробки слизової, так і у якості перорального пробіотика. Спосіб здійснюють таким чином. Як середовище культивування використовують знежирене молоко зі вмістом сухих речовин 45%, у яке додають 10% молока, гідролізованого панкреатином, або 5% гідролізату казеїну й 1-2% натрію лимоннокислого 3-заміщенного. Середовище стерилізують, охолоджують до температури культивування, інокулюють пробіотичним симбіозом і ферментують для накопичення біомаси, яку відокремлюють від культуральної рідини центрифугуванням. Для приготування інокуляту використовують мультикомпонентний симбіоз лактобацил, молочнокислих стрептококів, пропіоновокислих і біфідобактерій. Для створення симбіозу в оптимальних співвідношеннях з'єднують культури наступних видів 51147 8 пробіотичних бактерій: Bifidobacterium bifidum, Bifidobacterium adolescentis, Lactobacillus acidophilus, Lactobacillus casei, Lactobacillus fermentum, Lactobacillus plantarum, Lactobacillus helveticus, Lactobacillus gasseri, Lactobacillus salivarius, Lactococcus lactis, Streptococcus salivarius ssp. thermophilus, Propionibacterium freudenreichii ssp. shermanii й Propionibacterium acidipropionici. Отриманий симбіотичний комплекс штамів вносять у стерильне знежирене молоко зі вмістом сухих речовин 10%. Інокульоване молоко ферментують протягом 15-18 годин при температурі 3637°С. Спеціально проведеними дослідженнями встановлено, що при з'єднанні цих бактерій в оптимальних співвідношеннях вони формують стійкий мультикомпонентний симбіоз. Отриманий симбіоз використовують як посівний матеріал для одержання інокуляту, що використовують для нарощування клітин і накопичення біомаси. Біомасу клітин, відділену від культуральної рідини, змішують у співвідношенні 1:2-1:3 з 5-6%-м гелем бентоніту. Для одержання гелю бентоніту сухий природний бентоніт диспергують у воді з додаванням вуглекислого натрію, центрифугують. Осад суспендують у воді, центрифугують для відділення забруднюючих речовин і грубих часток бентоніту. Після багаторазового фракціонування одержують дрібнодисперсну фракцію бентоніту, яку суспендують у бідистильованій воді до одержання 5-6%ої суспензії гелеподібної консистенції, а потім стерилізують. Корисна модель пояснюється прикладами. Приклад 1. Одержання пробіотика для використання у комплексному лікуванні хворих пародонтитом. Для готування інокуляту до 25л стерильного знежиреного молока з 10% сухих речовин вносять 1,25л культури мультикомпонентного симбіозу лактобацил, молочнокислих стрептококів, пропіоновокислих і біфідобактерій наступного штамового складу й у зазначених нижче співвідношеннях: Bifidobacterium bifidum IMB В-7113 6 Bifidobacterium adolescentis IMB В-7148 4 Lactobacillus fermentum IMB В-7133 4 Lactobacillus salivarius IMB B-7134 2 Lactobacillus helveticus IMB B-7115 2 Lactobacillus acidophilus ВКПМ B-5863 1 Lactobacillus casei ВКПМ В-5724 5 Lactobacillus plantarum IMB B-7116 6 Lactobacillus gasseri IMB B-7135 3 Lactococcus lactis ВКПМ В-5725 1 Streptococcus salivarius ssp, thermophilus ВКПМ В-5388 2 Propionibacterium freudenreichii ssp. shermanii ВКПМ В-4544 7 P. acidipropionici ВКПМ B-5800 6. Інокульоване молоко ферментують протягом 18 годин при температурі 36°С. Готовий інокулят має густу в'язку консистенцію, кислотність 98 Т, рН 4,5, концентрація живих клітин - 8,6 108 КУО/см3. Для приготування середовища культивування 25кг сухого знежиреного молока розчиняють у 100л водопровідної води. До розчиненого молока 9 доливають воду (до 500л) з розрахунку одержання відновленого молока із вмістом сухих речовин 5%. Відновлене молоко стерилізують при температурі 121°С із витримкою протягом 25 хвилин; охолоджують до 37°С і зносять 25л (5%) інокуляту. Одночасно з інокулятом уводять 10% стерильного панкреатичного гідролізату молока й 1% натрію лимоннокислого 3-заміщенного (у вигляді стерильного 50%-го розчину). Процес культивування проводять 22 години при 37°С і рН 6,5. Концентрація життєдіяльних клітин наприкінці культивування становить 1,2 1010 КУО/см3. Клітинну біомасу відокремлюють центрифугуванням і змішують її в співвідношенні 1:2 з 5%-м гелем бентоніту. Характеристика отриманого пробіотика представлена в табл. 3. Приклад 2. Одержання пробіотика для використання у лікуванні хворих бактеріальним стоматитом. Для приготування інокуляту у 30л стерильного знежиреного молока з 10% сухих речовин вносять 1л культури мультикомпонентного симбіозу лактобацил, молочнокислих стрептококів, пропіоновокислих і біфідобактерій наступного штамового складу й у зазначених нижче співвідношеннях: Bifidobacterium bifidum ВКПМ В-5799 5 Bifidobacterium adolescentis IMB В-7112 4 Lactobacillus fermentum IMB В-7146 5 Lactobacillus salivarius IMB В-7134 2 Lactobacillus helveticus IMB B-7115 1 Lactobacillus acidophilus ВКПМ В-5254 1 Lactobacillus casei ВКПМ В-4542 6 Lactobacillus plantarum IMB B-7116 5 Lactobacillus gasseri IMB B-7145 3 Lactococcus lactis ВКПМ B-5387 1 Streptococcus salivarius ssp. thermophilus ВКПМ В-4741 1 Propionibacterium freudenreichii ssp. shermanii ВКПМ В-4545 6 P. acidipropionici ВКПМ В-5800 6. Інокульоване молоко ферментують протягом 20 годин при температурі 36°С. Готовий інокулят має густу в'язку консистенцію, кислотність 100°Т, рН 4,4, концентрація живих клітин - 9,9 108 КУО/см3. Для приготування середовища культивування 40кг сухого знежиреного молока розчиняють в 100л водопровідної води. До розчиненого молока доливають воду (до 1000л) з розрахунку одержання відновленого молока із вмістом сухих речовин 4%. Відновлене молоко стерилізують при температурі 121°С із витримкою протягом 35 хвилин. Охолоджують до температури 36°С і вносять 3% інокуляту. Одночасно з інокулятом уводять 10% стерильного панкреатичного гідролізату молока й 2% натрію лимоннокислого 3-заміщенного (у вигляді стерильного 50%-го розчину). Процес культивування проводять 24 години при 36°С і рН 6,6. Концентрація життєдіяльних клітин наприкінці культивування становить 1,3 1010 КУО/см3. Клітинну біомасу відокремлюють центрифугуванням і змішують її в співвідношенні 1:3 з 6%-м гелем бентоніту. Характеристика отриманого пробіотика представлена в табл. 3. 51147 10 Приклад 3. Одержання пробіотика для використання у лікуванні хворих гінгівітом. Для готування інокуляту до 50л стерильного знежиреного молока з 10% сухих речовин вносять 2л культури мультикомпонентного симбіозу лактобацил, молочнокислих стрептококів, пропіоновокислих і біфідобактерій наступного штамового складу й у зазначених нижче співвідношеннях: Bifidobacterium bifidum IMB В-7113 6 Bifidobacterium adolescentis IMB B-7148 5 Lactobacillus fermentum IMB B-7133 5 Lactobacillus salivarius IMB B-7134 3 Lactobacillus helveticus IMB B-71151 Lactobacillus acidophilus ЦМПМ B-2846 2 Lactobacillus casei ВКПМ B-3960 6 Lactobacillus plantarum IMB B-7116 4 Lactobacillus gasseri IMB B-7135 2 Lactococcus lactis ВКПМ В-5725 2 Streptococcus salivarius ssp. thermophilus ВКПМ В-5388 1 Propionibacterium freudenreichii ssp. shermanii ВКПМ В-4544 6 P. acidipropionici ВКПМ В-5723 5. Інокульоване молоко ферментують протягом 20 годин при температурі 36°С. Готовий інокулят характеризується густою в'язкою консистенцією, кислотністю 95°Т, рН 4,4, концентрацією живих клітин - 8,5 108 КУО/см3. Для приготування середовища культивування 45кг сухого знежиреного молока розчиняють в 150л водопровідної води. До розчиненого молока додають воду (до 1000л) з розрахунку одержання відновленого молока зі вмістом сухих речовин 4,5%. Відновлене молоко стерилізують при температурі 121°С із витримкою протягом 30 хвилин; охолоджують до 37°С і вносять 5% інокуляту. Одночасно з інокулятом уводять 10% стерильного панкреатичного гідролізату молока й 1,5% натрію лимоннокислого 3-заміщеного (у вигляді стерильного 50%-го розчину). Процес культивування проводять 23 години при температурі 37°С і рН 6,4. Концентрація життєдіяльних клітин наприкінці культивування становить 1,4 1010 КУО/см3. Клітинну біомасу відокремлюють центрифугуванням і змішують її в співвідношенні 1,0:2,5 з 5,5%-м гелем бентоніту. Характеристика отриманого пробіотика приведена в таблиці 3. Приклад 4. Одержання пробіотика для використання у лікуванні хворих стоматитом вірусної етіології. Спосіб здійснюють відповідно до прикладу 1 за винятком того, що до готового препарату уводять йод у вигляді водного або спиртового розчину дрібнокристалічного йоду і йодиду калію із розрахунку одержання в готовому препараті 0,5мг/мл йоду. Приклад 5. Одержання пробіотика для використання у лікуванні хворих кандидозом порожнини рота. Спосіб здійснюють відповідно до прикладу 1 за винятком того, що до готового препарату вводять міконазол. Приклад 6. Одержання пробіотика для використання у лікуванні хворих інфекційно-запальними захворюваннями глотки. 11 Спосіб здійснюють відповідно до прикладу 1 за винятком того, що до готового препарату вводять спиртовий екстракт прополісу з розрахунку одержання в готовому препараті прополісу в концентрації 30мг/мл. У таблиці 3 приведена порівняльна характеристика пробіотиків, одержаних відомим і пропонованим способами. Як свідчать дані таблиці, пропонований спосіб, порівняно з відомим, дозволяє поліпшити якість пробіотика за рахунок підвищення антагоністичної активності щодо широкого спектра патогенних й умовно-патогенних мікроорганізмів, збільшення концентрації фізіологічно цінних 51147 12 мікробних метаболітів, підвищення популяційного рівня життєдіяльних клітин цінних пробіотичних бактерій і розширення їхнього видового складу, надання пробіотику високої антивірусної активності. Пробіотик можна використовувати як у вигляді препарату для місцевої обробки ураженої області, так і перорально для відновлення біоценозів шлунково-кишкового тракту. Таким чином спосіб, що заявляється, дозволяє одержувати ефективні пробіотики для використання у лікуванні хворих із захворюваннями порожнини рота різної етіології. Таблиця 1 Антагоністична активність окремих видів лактобацил і їхньої комплексної культури щодо патогенних й умовно-патогенних мікроорганізмів (зона затримки росту мікроорганізмів - збудників захворювань порожнини рота), мм Види лактобацил L. L. L. L. L. Консорціум L. casei L. gasseri acidophilus plantarum helveticus salivarius fermentum лактобацил Staphylococcns aureus 16-18 9-13 11-13 18-21 11-15 17-19 10-14 20-22 Staphylococcus 22-24 6-10 16-18 15-19 20-22 18-21 12-15 22-25 epidermidis Staphylococcus 15-20 0-4 13-17 16-18 14-17 14-16 10-13 20-22 haemolyticus Actinomyces 14-17 6-11 0-8 18-21 10-13 14-16 0-5 20-23 naeslundii Actinomyces israelii 10-18 8-12 12-15 15-17 11-15 15-17 0-8 18-20 Fusobacterium 16-19 7-10 8-10 17-20 10-12 10-14 8-10 18-20 nucleatum Bacteroides oralis 18-20 11-14 10-13 18-20 16-19 15-18 6-9 17-20 Streptococcus 10-12 12-15 10-12 0-7 18-21 5-10 0-6 14-17 pyogenes Streptococcus 19-21 10-12 0-8 18-22 15-17 6-9 0-5 19-21 intermedius Prevotella intermedia 22-25 13-16 20-22 6-11 16-18 10-15 22-25 Porphyromonas 25-26 0-6 0-6 14-19 15-20 20-22 25-26 gingivalis Actinobacillus actinomycetemcomit 20-23 6-11 0-10 10-14 13-18 21-23 11-13 20-24 ans Treponema denticola 17-20 14-17 11-14 11-15 17-19 18-21 10-12 18-20 Veillonella parvula 21-22 13-17 20-23 15-17 0-4 9-12 21-23 Candida albicans 18-21 7-11 19-23 16-19 13-16 16-19 12-15 20-23 Peptostreptococcus 20-22 11-14 0-5 10-13 17-21 0-7 10-14 21-23 micros Вид тест-культури 13 51147 14 Таблиця 2 Пробіотичні властивості окремих видів біфідобактерій і їх мультисимбіозу з лактобацилами, пропіоновокислими бактеріями й молочнокислими стрептококами Показник Синтез коротколанцюгових жирних кислот: Оцтова Молочна Пропіонова Антагоністична активність (зона затримки росту патогенних й умовно-патогенних мікроорганізмів), мм: Staphylococcus aureus Staphylococcus epidermidis Staphylococcus haemolyticus Actinomyces naeslundii Actinomyces israelii Fusobacterium nucleatum Bacteroides oralis Streptococcus pyogenes Streptococcus intermedius Prevotella intermedia Porphyromonas gingivalis Actinobacillus actinomycetemcomitans Treponema denticola Veillonella parvula Candida albicans Peptostreptococcus micros B. bifidum B. adolescentis Мультисимбіоз 0,89±0,11 0,46±0,09 0,97±0,08 0,48±0,02 1,06±0,14 0,63±0,08 0,50±0,11 10-16 8-14 10-12 0-7 0-5 0-6 10-12 10-12 10-14 0-6 5-9 9-12 6-11 10-14 16-18 11-12 9-14 12-15 0-5 0-4 21-24 23-25 22-25 21-23 19-22 18-20 18-22 16-20 19-21 23-25 25-26 0-8 12-15 22-25 11-14 8-11 17-20 7-10 14-16 16-19 11-13 21-24 21-23 22-26 21-23 Таблиця 3 Порівняльна характеристика пробіотиків, які одержують відомим і пропонованим способами Показники Вміст життєдіяльних клітин, КУО/дозі Число штамів у препараті Ступінь адсорбції вірусних часток, % Лізоцимсинтезуюча активність, зона лізису тест-культури, мм Концентрація коротколанцюгових жирних кислот, %: молочна оцтова пропіонова Концентрація екзополісахаридів, % Антагоністична активність (зона затримки росту мікроорганізмів збудників захворювань порожнини рота), мм: Slaphylococcus aureus Staphylococcus epidermidis Slaphylococcus haemolyticus За прототипом 7 10 Характеристика пробіотиків За прикладом 1 За прикладом 2 11 3,8 10 11 3,0 10 За прикладом 3 3,4 1011 1-2 13 13 13 17±0,8 99,5±0,5 99,8±0,2 99,8±0,2 2,7±0,5 8,1±0,4 8,0±0,7 8,3±0,8 0,93±0,14 1,08±0,25 0,66±0,12 0,48±0,05 1,12±0,13 0,77±0,21 0,56±0,05 1,10±0,18 0,69±0,23 0,54±0,16 3,1±0,22 3,0±0,19 3,2±0,26 17 14 15 21 23 22 20 22 23 22 22 23 15 51147 16 Продовження таблиці 3 Actinomyces naeslundii Actinomyces israelii Fusobacterium nucleatum Bacteroides oralis Streptococcus pyogenes Streptococcus intermedius Prevotella intermedia Porphyromonas gingivalis Actinobacillus actinomycetemcomitans Treponema denticola Veillonella parvula Candida albicans Peptostreptococcus micros Вміст вітаміну В12, мкг/мл Комп’ютерна верстка М. Ломалова 10 7 8 15 22 20 23 21 23 21 24 25 22 21 23 23 19 20 22 22 8 10 17 10 23 20 24 22 0,93 23 20 22 23 0,91 22 23 22 23 0,89 Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for prepararion of “stomabakt” probiotic for treatment of patients with diseases of oral cavity
Автори англійськоюShyrobokov Volodymyr Pavlovych, Yankovskyi Dmytro Stanislavovych, Dyment Halyna Semenivna
Назва патенту російськоюСпособ получения пробиотика "стомабакт" для лечения больных с заболеваниями полости рта
Автори російськоюШиробоков Владимир Павлович, Янковский Дмитрий Станиславович, Димент Галина Семеновна
МПК / Мітки
МПК: A61K 35/74, C12N 1/20, A23C 9/12
Мітки: порожнини, стомабакт, лікування, рота, захворюваннями, хворих, спосіб, пробіотика, одержання
Код посилання
<a href="https://ua.patents.su/8-51147-sposib-oderzhannya-probiotika-stomabakt-dlya-likuvannya-khvorikh-iz-zakhvoryuvannyami-porozhnini-rota.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання пробіотика “стомабакт” для лікування хворих із захворюваннями порожнини рота</a>
Попередній патент: Спосіб використання регулятора росту “вермістим-д” в технології вирощування хмелю
Наступний патент: Спосіб одержання препарату із пробіотичними властивостями “симбітер космо” для застосування у косметології
Випадковий патент: Спосіб виробництва антифризів