Лікарський засіб для лікування або профілактики вірусної інфекції гепатиту в і спосіб лікування вірусної інфекції гепатиту в
Формула / Реферат
1. Применение производных 1-(2-гидроксиметил-1,3-оксатиолан-5-ил)цитозина общей формулы(І)
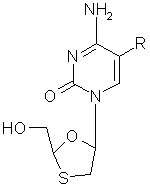 , (I)
, (I)
в которой R - водород или С1-С3 -алкил, или их физиологически функциональных производных для получения лекарственного средства для лечения или профилактики вирусной инфекции гепатита В.
2. Применение по пункту 1, отличающееся тем, что соединением формулы (І) является 1-(2-гидроксиметил-1,3-оксатиолан-5-ил)цитозин.
3. Применение по пункту 1, отличающееся тем, что соединением формулы (І) является (-)-цис-1-(2-гидроксиметил-1,3-оксатиолан-5-ил)цитозин.
4. Применение по пункту 1, отличающееся тем, что соединением формулы (І) является 1-(2-гидроксиметил-1,3-оксатиолан-5-ил)-5-метилцитозин.
5. Применение по пункту 1, отличающееся тем, что соединение формулы (І) представлено в форме цис-изомера.
6. Применение по пункту 1, отличающееся тем, что соединение формулы (І) представлено в форме (-)-цис-изомера.
7. Применение по пункту 1, отличающееся тем, что физиологически функциональными производными являются фармацевтически приемлемые соли или сложные эфиры соединения формулы (І).
8. Применение по любому из предыдущих пунктов, отличающееся тем, что лекарственный препарат находится в дозированной форме.
9. Применение по пункту 8, отличающееся тем, что дозированная форма содержит 10 - 1500 мг соединения формулы (I) или его физиологически функционального производного.
10. Применение по пункту 8 или 9, отличающееся тем, что дозированная форма является таблеткой или капсулой.
11. Способ лечения вирусной инфекции гепатита В, отличающийся тем, что инфицированным вводят эффективное количество производных 1-(2-гидроксиметил-1,3-оксатиолан-5-ил)цитозина общей формулы (I) или их физиологически функциональных производных.
12. Способ по пункту 11, отличающийся тем, что в качестве соединения формулы (I) используют 1-(2-гидроксиметил-1,3-оксатиолан-5-ил)-5-метилцитозин.
13. Способ по пункту 11, отличающийся тем, что в качестве соединения формулы (I) используют 1-(2-гидроксиметил-1,3-оксатиолан-5-ил)-5-цитозин.
Текст
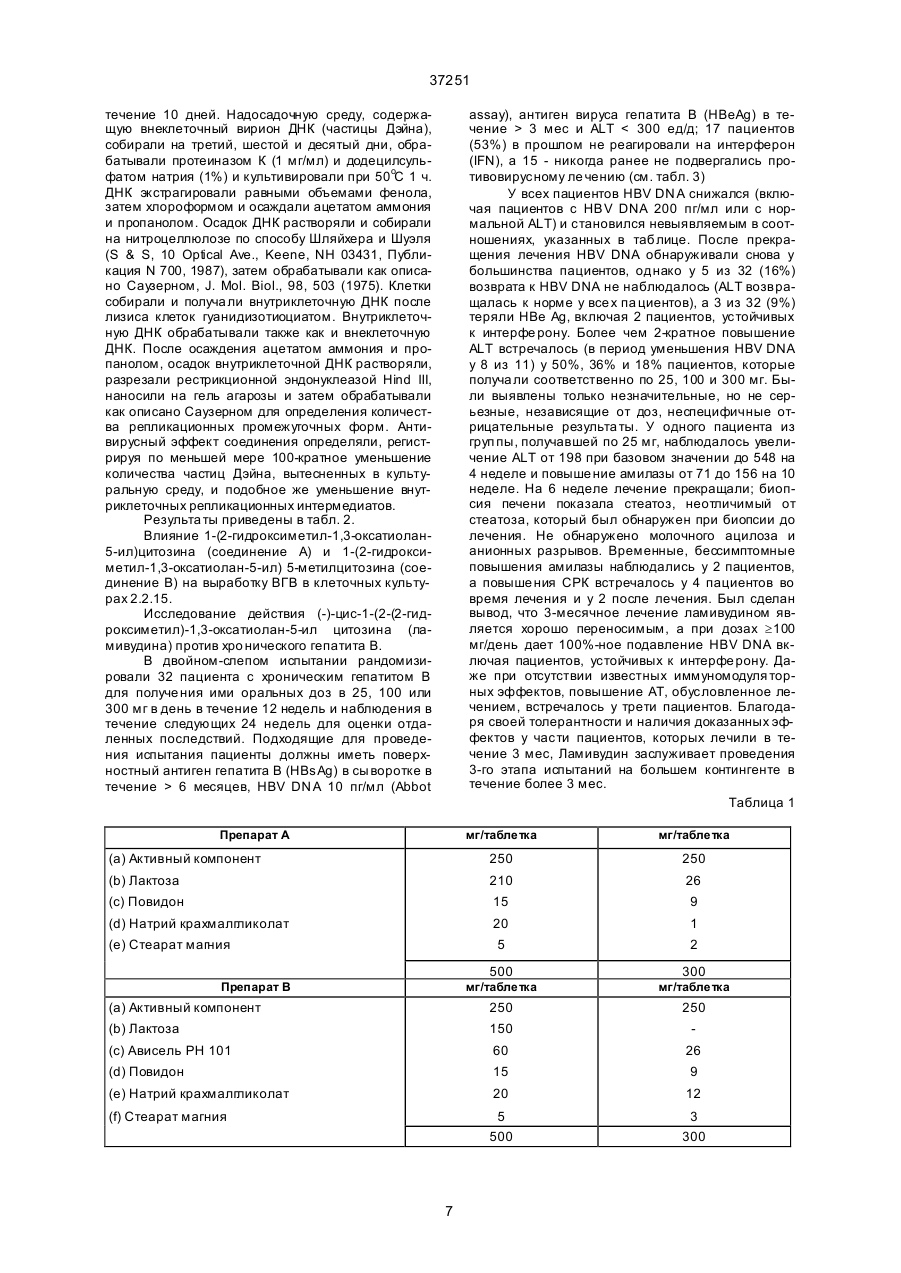
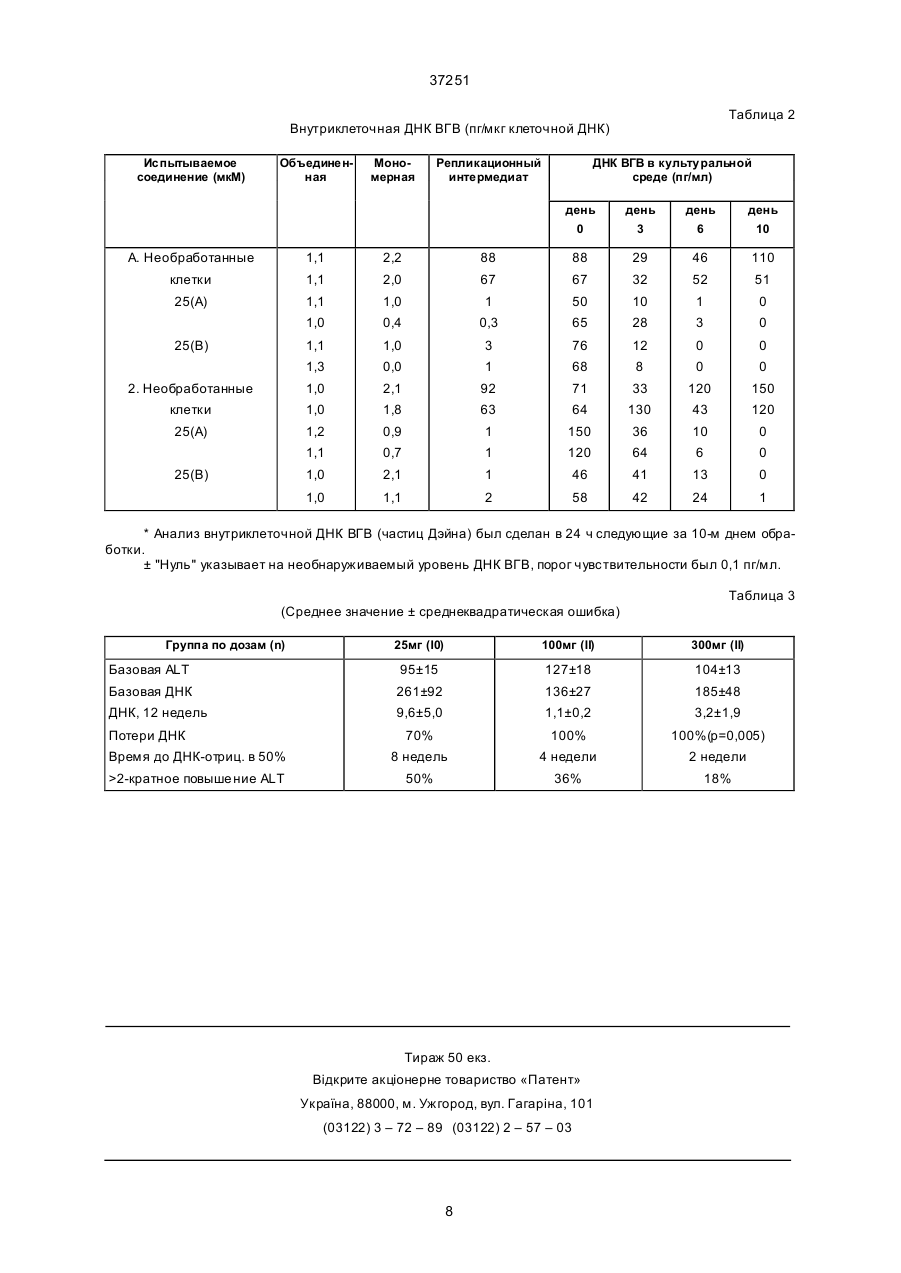
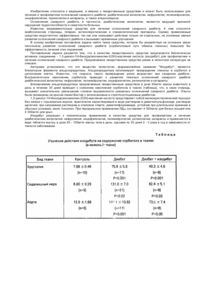
1. Применение производных 1-(2-гидроксиметил-1,3-оксатиолан-5-ил)цитозина общей формулы (I) NH2 C2 (54) ЛІКАРСЬКИЙ ЗАСІБ ДЛЯ ЛІКУВАННЯ АБО ПРОФІЛАКТИКИ ВІРУСНОЇ ІНФ ЕКЦІЇ ГЕП АТИТУ В І СПОСІБ ЛІКУВАННЯ ВІРУСНОЇ ІНФ ЕКЦІЇ ГЕП АТИТУ В ____________________ Настоящее изобретение относится к применению производных 1-(2-гидроксиметил-1,3-оксатиолан-5-ил)цитозина и их фи зиологически функциональных производных для ле чения инфекций вируса гепатита В. В.Ш. Вирус гепатита В (ВГВ) является всемирно известным вирусным патогенным микроорганизмом. ВГВ наиболее широко распространен в азиатских странах и в африканских странах южнее Сахары. Ви рус этио логически связан со злокачест 37251 венной гепатомой и, как полагают, вызывает 80% случаев рака печени в мире. В США каждый год госпитализируют больше 10 000 людей в связи с инфекцией ВГВ, в среднем 250 человек умирают в связи с быстрым развитием болезни. В США имеется около 500 000 - 1 млн носителей инфекции. Хронический активный гепатит развивается у более чем 25% носителей и часто переходит в цирроз. Согласно оценке около 5000 людей умирает от цирроза, связанного с ВГВ, каждый год в США и возможно 1000 умирает от рака печени, связанного с ВГВ. Даже в случае универсальной ВГВ вакцины, будет оста ваться необхо димость в эффективных анти-ВГВ соединениях. Большое количество постоянно инфицированных носителей, оцениваемое в 220 млн. человек во всем мире, не получи т пользы от вакцинации и будет пребывать в состоянии высокого риска заболеть болезнями печени, вызываемыми ВГВ. Популяция носителей служит источником инфекции восприимчивых индивидуумов, сохраняющи х случаи заболеваний, особенно в эндемических областях и гр уппах высокого риска, таких как злоупотребляющие лекарствами и гомосексуалисты. Та ким образом, существуе т необхо димость в эффективных антивирусных средствах как для борьбы с хроническими инфекциями, так и для снижения роста злокачественной гепатомы. Клинические проявления инфекции вирусом ВГВ включают го ловную боль, лихорадку, недомогание, тошноту, рво ту и боли в животе. Репликация вируса обычно регули руется иммунным ответом с продолжительностью периода выздоровления в недели или месяцы у людей, но инфекция может быть более серьезной, приводя к постоянной хронической болезни печени. В книге: Вирусные Инфекции Человека, (второе издание, ред. А.С.Э ванс, 1982, Пленум Паблишинг Корп., НьюЙорк), глава 12 описывает этиологию инфекции вирусным гепатитом. Европейский патент N 0382526 описывает некоторые 1,3-оксатиолановые аналоги нуклеозидов, ингибирующие репликацию вируса иммунодефицита че ловека (ВИЧ). Мы нашли, что производные 1-(2-гидроксиметил-1,3-оксатиолан-5-ил) цитозина формулы I Следуе т заметить, что соединения формулы I содержат два хиральных центра, и. следовательно, существуют в форме двух пар опти ческих изомеров, например энантиомеров, и их смесей, включая рацемические смеси. Таким образом, соединения формулы I могут быть либо цис- или транс-изомером, либо их смесью. Каждый цис- и транс-изомер может существовать в качестве одного из двух энантиомеров или их смеси, включая рацемические смеси. Все такие изомеры и их смеси, включая рацемические смеси, входят в предмет изобретения. Предпочтительным является цис-изомер соединения формулы I. Изобретение включает оптические и геометрические изомеры и все таутомерные формы соединений формулы I: из цис-изомеров (-)-изомер, т.е. (-)-цис-1-(2-гидроксиметил-1,3-оксатиолан-5-ил) - цитозин, особенно предпочтителен. Согласно одному аспекту настоящего изобретения мы предлагаем использовать соединения формулы I или их фи зиологически функциональные производные для лечения или профилактики инфекций вируса гепатита В. Согласно другому аспекту изобретения мы предлагаем использовать соединения формулы I или их фи зиологически функциональные производные для приготовления лекарственных препаратов для ле чения или профилактики инфекций вируса ге патита В. До полнительные аспекты настоящего изобретения включают способ лечения или профилактики инфекций вируса гепатита В у хо зяина, например, млекопитающего, такого как человек, который предусматривает введение хозяину терапевтически эффективного количества соединения формулы I или его фи зиологически функционального производного. "Физиологически функциональное производное" означает фармацевти чески приемлемую соль, сложный эфир или соль эфира соединения формулы I или любое другое соединение, которое после вве дения реципиенту, спо собно превращаться (прямо или непрямо) в соединения формулы Iили их активный метаболит или остаток. Предпочти тельные сложные эфиры в соответствии с изобретением включают эфиры карбоновых кислот, в которых некарбонильный остаток кислотной части эфира выбирают из нормального алкила или изоалкила, например, н-пропила, третбутила, н-бутила, алкоксиалкила (метоксиметил), арилалкила (бензил), арилоксиалкила (феноксиметил) и арила (фенил); эфиры сульфо кислот, такие как алкил- или арилсульфонил (метаносульфо нил); эфиры аминокислот, например, L-валил или L-изолейцил; эфиры дикарбоновых кислот, например, гемисукцинат; 51-моно-, ди- или трифосфатные эфиры, причем фосфатные эфиры могут быть этерифицированы, например, С1-С20спиртом или его реакционноспособным производным или 2,3-ди-С6-С24-ацилглицерином. Алкильный остаток сложного эфира содержит 1-18 атомов углерода, предпочти тельно 1-4 атома углерода. Арильный остаток такого сложного эфира предпочтительно представляет собой фе нил, возможно замещенный галогеном, С1-С4алкилом, C1-С4-алкокси- или нитрогруппой. В описанных выше сложных эфирах аминогруппа цитозина может присутствовать в амидной форме, например, NHCOR, где R - C1-С6-алкил NH2 R N N O , HO (I) O S (в которой R - водород или C1-С3-алкил) и их физически функциональные производные, имеющие высокую активность против ВГВ. Предпочти тельным соединением формулы I является соединение, где R - водород, т.е. 1-(2гидроксиметил-1,3-оксатиолан-5-ил)-цитозин. 2 37251 или арил, например, фенил, возможно замещенный галогеном, С1-С4-алкилом, С1-С4-алкокси-, нитро- или гидроксигруппой. Примеры фармацевти чески приемлемых солей в соответствии с изобретением включают соли с основаниями, например, производные соответствующи х оснований, такие как щелочнометаллические (натриевые), щелочноземельные (магнитные), аммониевые или четвертичные аммониевые соли NX4, где Х - С1-С4-алкил. Фармацевтически приемлемые аддиционные соли с кислотами включают соли органических карбоновых кислот, например, уксусной, молочной, винной, яблочной, изэтионовой, лактобиеновой и янтарной кислот; соли сульфо кислот, например, метансульфоновой, этансуль фоновой, бензолсульфо новой и п-толуолсуль фоновой кислоты; и соли неорганических кислот, например, соляной, серной, фосфорной и сульфаминовой кислот. Количество соединения формулы I (далее называемого также "активный компонент") или его фи зиологически функционального производного, которое необходимо для достижения желаемого эффекта, зависит от многих факторов, в особенности от специфического применения, природы отдельного соединения, способа введения и состояния пациента. В общем подхо дящая доза составляет 3,0 - 120 мг на кг массы тела реципиента в день, предпочти тельно 6-90 мг на кг массы тела в день и наиболее предпочтительно 15 - 60 мг на кг массы тела в день. Нужную дозу предпочти тельно разбивают на 2 - 6 или больше поддоз, вводимых через соответствующие интервалы времени в течение дня. Эти поддозы можно вводить в единых дозировочных формах, например, содержащих 10 - 1500 мг, предпочти тельно 20 - 1000 мг и наиболее предпочтительно 50 - 700 мг активного компонента на единую дозировочную форму. В идеальном случае активный компонент должен быть введен для достижения пиковой концентрации в плазме активного компонента 1 - 75 мкМ, предпочтительно 2-50 мкМ, наиболее предпочти тельно 3-30 мкМ. Это можно достичь, например, внутривенной инъекцией 0,1 - 5% раствора активного компонента, возможно в физиологическом растворе, или пероральным введением болюса, содержащего 1-100 мг/кг активного компонента. Желательный уровень в крови можно поддерживать непрерывным вливанием для обеспечения 0,01 - 5,0 мг/кг/ч или прерывными вливаниями, содержащими 0,4 - 15 мк/кг активного компонента. В технологии производства лекарственного препарата, да лее также называемого "препарат" соединения формулы I или их фи зиологически функциональные производные, "активный компонент", смешивают с одним или больше фар мацевтически приемлемым носителем или наполнителем и, возможно, другими терапевти ческими средствами. Применяют препараты, подхо дящие для перорального, ректального, назального, местного (включая чрезкожное, трансбукальное и подъязычное), вагинального или парентерального (включая подкожное, внутримышечное, внутривенное и внутрикожное) введения. Составы обычно могут иметь единую дозировочную фор му и могут быть получе ны любыми способами, хорошо известными в фармации. Такие способы включают ста дию смешивания активного компонента с носителем, который состоит из одного или больше дополнительного компонента. В общем составы получают однородным и тщательным смешиванием активного компонента с жидкими носителями или тонко измельченными твердыми носителями или с теми и другими и затем, если необхо димо, формованием продукта. Препараты настоящего изобретения, подходящие для перорального введения могут иметь форму отдельных единиц, та кую как капсулы, пакетики или таблетки, содержащие определенное количество активного компонента; порошки и гранулы; растворы или суспензии в водной или неводной жидкости; или жидкие эмульсии "масло в воде" или "вода в масле". Активный компонент также может быть помещен в болюс, кашку или пасту. Таблетки делают прессованием или формованием, возможно вместе с одним или больше вспомогательными компонентом. Прессованные таблетки делают прессованием в соответствующем аппарате активного компонента в свободно-текучей форме, например, в форме порошка или гранул, возможно смешанного со связующим (повидон, желатин, гидроксипропилметилцеллюлоза), смазочным средством, инертным разбавителем, консервантом, дезинтегрантом (натрийгликолат крахмала, сшитый повидон, сшитая карбоксиметилцеллюлоза), поверхностно-активным или диспергирующим средством. Формованные таблетки делают формованием в соответствующем аппарате смеси порошковых сое динений, увлажненных инертным жидким разбавите лем. Таблетки можно покрыть, можно пригото вить состав таким образом, чтобы обеспечить медленное или регули рованное выделение активного компонента, используя, например, гидроксиметилцеллюлозу в различных пропорциях для достижения желаемого профиля освобождения активного компонента. Таблетки можно покрыть анте росолюбильной оболочкой для выделения активного компонента вне желудка. Пероральные препараты могут включать буферные средства, предназначенные для нейтрализации желудочной кислотности. Та кие буферы выбирают из различных органических или неорганических средств, таких как слабые кислоты или основания, смешанные с их сопряженными солями. Препараты для местного вве дения во рту включают лепешки, содержащие активный компонент на вкусовой основе, обычно в сахарозе и акации или астрагале; пастилки, содержащие активный компонент в инертной основе, такой как желатин или глицерин, или сахароза и акация; жидкость для полоскания рта, содержащую активный компонент в подхо дящем жидком носителе. Препараты для ректального введения могут быть представлены суппозиториями с подходящей основой, состоящей, например, из масла какао или салицилата. Препараты для вагинального введения могут быть представлены пессариями, тампонами, кремами, гелями, пастами, пенами или разбрызги 3 37251 вающимися препаратами, содержащими вместе с активным компонентом известный носитель. Препараты для парентерального вве дения включают водные и неводные изотонические стерильные инъекционные растворы, возможно содержащие антиоксиданты, буферы, бактериостатические средства и растворенные вещества, делающие препараты изотоническими по отношению к крови предполагаемого реципиента; водные или неводные стерильные суспензии, возможно включающие суспендирующие средства и загустители, а также липосомы или другие системы микрочастиц, нацеливающие соединения на компоненты крови одного или нескольких органов. Препараты предполагаются в однодозовых или многодозовых сосудах, например, ампулах и пробирках, и могут храниться в лиофилизированном состоянии, требующем только добавления стерильного жидкого носителя, например, воды для инъекций, непосредственно перед использованием. Инъекционные растворы для немедленного применения могут быть приготовлены из стерильных порошков, гранул и таблеток, описанных ранее. Предпочти тельными препаратами являются те, которые содержат дневную дозу, дневную дозу или соответствующую часть дозы активного компонента. Следует понимать, что в дополнение к отдельно упомянутым компонентам препараты этого изобретения могут вк лючать другие средства, имеющие отношение к типу препарата, например, пероральные препараты могут включать такие дополнительные средства, как подслащивающие средства, загустители и вкусовые вещества. Соединения формулы I можно получать, например, по способу, описанному в ЕР 0382526 или по аналогичному способу. Таким образом соединения формулы I можно получать, например: а) реакцией необязательно замещенного 5R-цитозина, где R определен выше, с производными 1,3-оксатиолана формулы IIА урацила в аминогруппу, любые оставшиеся защитные группы удаляют, например, кислотным или ще лочным гидролизом. В способе (а) защитные радикалы для гидроксигруппы выбирают из ацила (например, ацетила), арилацила (например, бензоила или замещенного бензоила), тритила или монометокситритила, бензила или замещенного бензила, триалкилсилила (например, диметил-трет-бутилсилила) или дифенилметилсилила. 5-R-Цитозин может быть защищен силилом, например, триметилсилилом. Такие группы можно удалять обычными способами. Уходящая группа L - это ти пичная в нуклеозидной химии уходящая группа, например, галоген (хлор или бром), алкоксигруппа (метоксиили этоксигруппа) или ацил (ацетил или бензолил). Реакцию в способе (а) можно проводить в органическом растворителе, например, 1,2-дихлорэтане или ацетонитриле, в присутствии кислоты Льюиса, например, хлорида олова (IV) или триметилсилилтрифлата. Соединения формулы ІІА можно получать из защи щенного 2-гидроксиацетальдегида формулы R1OCH2CHO (III), где R1 определен выше, как описано в Can. J. Research, 8, 129 (1933) и ЕР 0382526. Реакция соединений формулы III с известным (Сhеm. Веr 85, 924 - 932 (1952)) меркаптоацеталем HSCH2(OR)2, где R - С1-С4-алкил, например, HSCH2CH(OC2H5)2, приводит к соединениям формулы IIА, где L-группа ОР, например, метокси- или этокси-группа. Альтернативно, соединения формулы ІІА, где L-алкоксигруппа, можно превратить в соединения формулы IIА, где L-галоген или ацил, известными методами химии углеводов. Соединения формулы III можно получать из 1,2-O-изопропилиденглицерина введением R1, например, тризамещенного силила, бензила или тритила, и удалением изопропилидена мягкой кислотой, например, водными муравьиной или уксусной кислотами, или бромидом цинка в ацетонитриле с последующим окислением спиртовой группы водным периодатом. В способе (б) соединения формулы IIB преимущественно обрабатывают 1,2,4-триазолом вместе с 4-хлорфенилдихлорфосфа том. Образующееся 4-(1,2,4-триазолил)-ьное производное превращают в 4-аминоцитидин по реакции с, например, метанолом. Исходные соединения формулы IIB получают, например, реакцией соответствующего (воз можно защищенного) основания с соединениями формулы IIА, способом аналогичным описанному в способе (а). R 1O L , (IIA) S где R1 - водород или защитный радикал для гидроксигруппы и L-уходящая гр уппа, или б) реакцией соединений формулы IIВ O R HN N O , R 1O Разделение (±)-цис и (±)-транс-изомеров, например, в защи щенной форме, может быть выполнено хро матографически на силикагеле смесью органических растворителей, таких как этилацетат/метанол, этилацетат/гексан или дихлорметан/метанол. Любые защитные группы затем можно удалить, используя соответствующий реагент для каждой группы. Расщепление (±)-энантиомеров может быть выполнено ферментативным способом с применением эстеразы, такой как эстераза печени свиньи (Сигма Кемикал Ко, Сент Луис, МО 63178), причем один энантиомер 51-ацилпроизводного соедине (IIB) O S где R и R1 определены выше, с реагентом, превращающим оксогруппу в положении 4 кольца 4 37251 ния формулы I диэтерифицируется. После разделения оставшееся этерифицированное соединение формулы I может быть подвергнуто реакции в основных условиях, например, NН3 в метаноле или NaOMe в метаноле, с получе нием индивидуальных (+)- и (-)-энантиомеров. Альтернативно, (±)-цис или (±)-транс-изомеры соединений формулы I можно ввести в реакцию с фосфорилирующим реагентом, например, оксихлоридом фосфо ра, в инертном растворителе, таком как триэтилфосфат, ацето нитрил или 1,3-диметил-3,4,5,6тетрагидро-2(1Н)-пиримидинон с образованием 51монофосфатного производного или его соли. Обработка 51-монофосфатного производного ферментом, таким как 51-нуклеотидаза яда змеи, приводит предпочтительно к гидролизу одного из энантиомеров. Отделение и последующее дефосфо рилирование другого 51-монофосфатного энантиомера приводит к индивидуальным (+)- или (-)энантиомерам соединений формулы I. Соединения формулы I можно превратить в фармацевтически приемлемые эфиры реакцией с соответствующим этерифи цирующим реагентом, например, ацилгалогенидом или ангидридом. Соединения формулы I можно превратить в фармацевти чески приемлемые соли обычным способом, например, в результате обработки основанием. Эфиры и соли соединений формулы I можно превратить в исходное соединение, например, гидролизом. Для лучшего понимания изобретения приведены следующие примеры. (±)-цис и (±)-транс-2-бензоилоксиметил-5(тимин-N-ил)-1,3-оксатиолан получают и разделяют на (±)-цис- и (±) -транс-изомеры как описано в ЕР 0382526. (+)-цис-изомер вводят в реакцию с уксусным ангидридом в пиридине при комнатной температуре с образованием 2-ацетата. Растворитель удаляют в вакууме при < 30oС. 2-Ацетат растворяют в СНСl3, промываютводным бикарбонатом, отделенный органический слой сушат в СНСl3 удаляют в вакууме. Превращение тиминового основания в 5-метилцитозиновое основание выполняют через стадию получе ния 4-(1,2,4-триазол-1-ил)ьного производного по методу К.В.Ри са и В.Л.Санга (см. ссылки в предыдущей методике), используя 1,2,4-триазoл и 2 эквивалента 4-хлорфе нилдихлорфосфата в сухом пиридине при комнатной температуре. Гидролиз 2-ацетата выполняют насыщенным раствором аммиака в метаноле при 0°С и получают (±)-цис-1-(2-гидроксиметил1,3-оксатиолан-5-ил)-5-метилцитозин. Фармацевти ческие препараты. В последующи х примерах препаратов "активный компонент" - это 1-(2-гидроксиметил-1,3оксатиолан-5-ил)-цитозин. Пример 3. Таблетированные препараты. Следующие препараты А, В и С получают мокрым гранулированием компонентов с раствором повидона, последующим добавлением стеарата магния и прессованием (см. табл. 1). Следующие препараты D и Е получают прямым прессованием смеси компонентов. Лактоза в препарате Е - это лактоза типа прямого прессования (Дэйри Крэст - "Зе па-рокс"). Препарат D мг/таблетка Активный компонент 250 Предварительно желатинизированный крахмал 150 Всего 400 Препарат Е мг/таблетка Активный компонент 250 Лактоза 150 Ависель 100 Всего 500 Препарат F (Препарат с контролированным выделением активного компонента). Препарат получают мокрым гранулированием компонентов (ниже) с раствором повидона, последующим добавлением стеарата магния и прессованием. Препарат F мг/таблетка (a) Активный компонент 500 (b) Гидроксипропилметилцеллюлоза 112 (c) Лактоза 53 (d) Повидон 28 (e) Стеарат магния 7 Всего 700 Выделение активного компонента происходит в течение 6 - 8 ч и завершается после 12 ч. Пример 1. 1-(2-Гидроксиметил-1,3-оксатиолан-5-ил) цитозин. Способ А: (±)-цис и (±)-транс-2-бензоилoксимeтил-5-(N 4-этилцитозин-1-ил)-1 ,3-ок сатио лан получают и разделяют на (±)-цис- и (±)-трансизомеры как описано в ЕР 0382526. N4-ацетил и 2бензоил удаляют диметиламином в этаноле и продукт, (±)-цис-1-(2-гидроксиметил-1,3-оксатиолан-5ил) цитозин, выделяют. Способ Б: (±)-цис- и (±)-транс-2-бензоилоксиметил-5-(урацил-1-ил)-1,3-оксатиолан и получают как описано в ЕР 0382526. После удаления защиты 2-гидроксигруп пы насыщенным раствором аммиака в метаноле изомеры разделяют на силиканеле с применением смеси этилацетат/метанол в качестве элюента (ЕР 0382526). (±)-цисИзомер вводят в реакцию с ук сусным ангидридом в пиридине при комнатной температуре с образованием 2-ацетата. Растворитель удаляют в вакууме при 6 месяцев, HBV DN A 10 пг/мл (Abbot assay), антиген вируса гепатита В (HBeAg) втечение > 3 мес и ALT 2-кратное повыше ние ALT 50% 36% 18% Потери ДНК Тираж 50 екз. Відкрите акціонерне товариство «Патент» Україна, 88000, м. Ужгород, вул. Гагаріна, 101 (03122) 3 – 72 – 89 (03122) 2 – 57 – 03 8 37251 9
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstance for treatment and prevention of viral hepatitis b and method for treating viral hepatitis b
Автори англійськоюFurman Phillip Allen, PEJNTER DZHORDZH Robert
Назва патенту російськоюЛекарственное средство для лечения или профилактики вирусной инфекции гепатита в и способ лечения вирусной инфекции гепатита в
Автори російськоюФурман Филлип Аллен, Пейнтер Джордж Роберт
МПК / Мітки
МПК: C07D 411/00, C07D 239/02, A61K 31/505, A61P 31/12, A61K 31/70, A61P 1/16
Мітки: лікарський, засіб, профілактики, вірусної, спосіб, інфекції, гепатиту, лікування
Код посилання
<a href="https://ua.patents.su/9-37251-likarskijj-zasib-dlya-likuvannya-abo-profilaktiki-virusno-infekci-gepatitu-v-i-sposib-likuvannya-virusno-infekci-gepatitu-v.html" target="_blank" rel="follow" title="База патентів України">Лікарський засіб для лікування або профілактики вірусної інфекції гепатиту в і спосіб лікування вірусної інфекції гепатиту в</a>
Попередній патент: Магнітна плита
Наступний патент: Жалюзі з ручним управлінням
Випадковий патент: Спосіб отримання рідкого біопалива з технічних тваринних жирів