1,4-дигідропіридинконденсовані гетероцикли, спосіб їх одержання, застосування і композиція, що містить їх
Номер патенту: 98928
Опубліковано: 10.07.2012
Автори: Філош-Ромм Брюно, Б'єргард Кірстен, Ма Ніна, Міну Ерве, Комбо Сесіль, Наір Аніл, Клерк Франсуа, Міньяні Серж, Каррі Жан-Крістоф, Шио Лоран, Може Жак, Ангуйан-Боніфас Оділь
Формула / Реферат
1. Сполука, що відповідає загальній формулі (І):
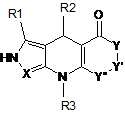 , (І)
, (І)
де:
R1 являє собою Н або метил;
R2 являє собою заміщений арил або заміщений гетероарил;
R3 являє собою Н або R4;
X являє собою N або CR7;
Y, Y' і Y":
(і) кожний, незалежно, являє собою замісник, вибраний з СН2, CHR5, CR5R6, С=О, О, S, NH і NR7; або
(іі) разом являють собою замісник, вибраний з ланцюгових фрагментів -СН2-О-(С=О)-, -(СН2)4- і -(СН2)2-;
кожний з R4 і R7, незалежно, являє собою замісник, вибраний з: R8, -COOR8, COR8 і CONHR8;
кожний з R5 і R6, незалежно, являє собою R8;
R8 являє собою Н або необов'язково заміщений: -алкіл, -алкілалкілен, -алкілен, -гетероциклоалкіл, -циклоалкіл, -арил, -гетероарил, -алкілгетероциклоалкіл, -алкілциклоалкіл, -алкіларил або -алкілгетероарил, -алкіл-NRaRb, причому кожний з Ra і Rb, незалежно, являє собою Н або алкіл,
за умови, що R1 являє собою Н, коли X являє собою N, і Y' являє собою CR5R6.
2. Сполука за п. 1, де R1 являє собою Н.
3. Сполука за п. 1, де R3 являє собою Н.
4. Сполука за п. 1, де Y" і Y являють собою СН2.
5. Сполука за п. 1, де Y' вибирають з СН2, СНСН3, С(СН3)2, СН-арилу, СН-гетероарилу, СН-(заміщений арил), СН-(заміщений гетероарил), NH і NR7, причому R7 такий, як визначено у п. 1.
6. Сполука за п. 1 формули (Іа)
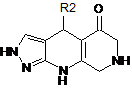 , (Іа)
, (Іа)
де R2 являє собою заміщену арильну групу.
7. Сполука за п. 1 формули (Іа), як визначено у п. 6, де R2 являє собою заміщену гетероарильну групу.
8. Сполука за п. 1 формули (I'а)
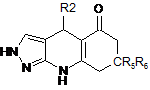 , (I'а)
, (I'а)
де R5 і R6 є такими, як визначено у п. 1, де R2 являє собою заміщену арильну групу.
9. Сполука формули (I'а), як визначено у п. 8, де R2 являє собою заміщену гетероарильну групу.
10. Сполука за п. 1 формули (Іb)
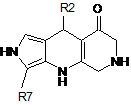 , (Ib)
, (Ib)
де R7 с таким, як визначено у п. 1, де R2 являє собою заміщену арильну групу.
11. Сполука формули (Іb), як визначено у п. 10, де R2 являє собою заміщену гетероарильну групу.
12. Сполука за п. 1 формули (I'b)
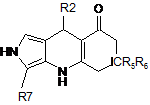 , (I'b)
, (I'b)
де R5, R6 і R7 є такими, як визначено у п. 1, де R2 являє собою заміщену арильну групу.
13. Сполука формули (Іb), як визначено у п. 12, де R2 являє собою заміщену гетероарильну групу.
14. Сполука формули (Іа) або (Іb) за будь-яким з попередніх пунктів, де R2 являє собою заміщену фенільну або гетероарильну групу; причому є присутніми від одного до чотирьох замісників, вибраних з галогену, алкілу, ОН, OR8, СН2-OR8, SH, SR8, NH2, NHR8, CONHR8, CONHCH2R8, NHCOR8, NHCONHR8, SO2NHR8, фенілу, незаміщеного або заміщеного алкілом, ОН або галогеном, де R8 є таким, як визначено у п. 1.
15. Сполука за п. 14, де R8 вибирають з фенілу і гетероарилу, незаміщеного або заміщеного одним-чотирма замісниками, незалежно вибраними з F, Сl, Вr, ОН, SH, CF3, OCF3, OCH3, SCF3, SCH3, OCHF2, OCH2F, SCH2F, (С1-С6)-алкілу, О-алілу, фенілу і фенілу, заміщеного галогеном.
16. Сполука формули (I'а) або (I'b) за будь-яким з попередніх пунктів, де R2 являє собою заміщений гетероарил; де є присутніми від одного до чотирьох замісників, вибраних з галогену, алкілу, ОН, OR8, CH2-OR8, SH, SR8, NH2, NHR8, CONHR8, CONHCH2R8, NHCOR8, NHCONHR8, SO2-NHR8, фенілу, незаміщеного або заміщеного алкілом, ОН або галогеном, де R8 є таким, як визначено у п. 1.
17. Сполука за п. 16, де R8 являє собою феніл або гетероарил, незаміщений або заміщений одним-чотирма замісниками незалежно вибраними з F, Сl, Вr, ОН, SH, CF3, OCF3, ОСН3, SCF3, SCH3, OCHF2, OCH2F, SCH2F, (С1-С6)-алкілу, О-алілу, фенілу і фенілу, заміщеного галогеном.
18. Сполука за будь-яким з пп. 1-17, де R2 являє собою феніл або гетероарил, заміщений SR8, при цьому R8 є таким, як визначено у пп. 1, 15 або 17.
19. Сполука за п. 18, де R2 являє собою фурил або тієніл, заміщений SR8, при цьому R8 є таким, як визначено у пп. 1, 15 або 17.
20. Сполука за пп. 1-19, де R2 являє собою фурил або тієніл, заміщений SR8, де R8 являє собою бензімідазоліл або імідазоліл, незаміщений або заміщений одним-чотирма замісниками, незалежно вибраними з F, Сl, Br, OH, SH, CF3, OCF3, ОСН3, SCF3, SCH3, OCHF2, OCH2F, SCH2F, (С1-С6)-алкілу, О-алілу, фенілу і фенілу, заміщеного галогеном.
21. Сполука формули (І), (I'а) і (I'b) за попередніми пунктами, де R5 і R6 обидва являють собою водень або обидва являють собою метил.
22. Сполука формули (І), (I'а) і (I'b) за попередніми пунктами, де R5 являє собою водень, і R6 являє собою заміщений або незаміщений (С1-С6)-алкіл або заміщений або незаміщений феніл.
23. Сполука формули (І), (Ib) і (I'b) за попередніми пунктами, де R7 являє собою групу -CO2Et.
24. Сполука за будь-яким з попередніх пунктів у вигляді рацемічної форми, збагаченої одним енантіомером, збагаченої одним діастереомером, у вигляді її таутомерів, проліків і фармацевтично прийнятних солей.
25. Сполука формули (І) за п. 1, що являє собою:
4-(4-гідрокси-3-метилфеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-хлорфенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-1,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7,7-диметил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-(2-фторфеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-(4-феноксифеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(3,5-дихлорфенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-трет-бутилфенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-трифторметилфенілокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-метоксифенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-(3-п-толілоксифеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(3,4-дихлорфенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-(3-феноксифеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-хлорфенокси)феніл]-3-метил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[2-(4-хлорфенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(4-хлорфеніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(2-трифторметилфеніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(3-трифторметилфеніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(3,4-дихлорфеноксиметил)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-(2-алілоксифеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-хлорфенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(3-хлорфеніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(3,4-дихлорфеноксиметил)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(3-трифторметилфеніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(2-трифторметилфеніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(4-хлорфеніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-метил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-феніл-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-6,6-диметил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-ізопропіл-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-(4-метоксифеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-(2,4-дихлорфеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-фуран-2-іл-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
7-бензо[1,3]діоксол-5-іл-4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-(3,4-диметоксифеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-пентил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-(2-фторфеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-(2-метоксифеніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(піридин-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-4,6,7,8,9,10-гексагідро-2Н-1,2,10-триазациклогепта[f]інден-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,7,8-тетрагідро-6-окса-1,2,8-триаза-s-індацен-5-он;
4-[3-(4-хлорфенокси)феніл]-6,8-диметил-2,4,8,9-тетрагідро-1,2,6,8,9-пентааза-циклопента[b]нафталін-5,7-діон;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-(трет-бутилоксикарбоніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-(2-гідрокси-3-піперидин-1-ілпропіл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-хлорфенокси)феніл]-7-(2-гідрокси-3-морфолін-4-ілпропіл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-9-(2-гідрокси-3-морфолін-4-ілпропіл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-хлорфенокси)феніл]-7-(3,5-диметилізоксазол-4-карбоніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-хлорфенокси)феніл]-7-(ізоксазол-5-карбоніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-хлорфенокси)феніл]-7-(4-метил-[1,2,3]тіадіазол-5-карбоніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[3-(4-хлорфенокси)феніл]-7-(6-хлорпіридин-2-карбоніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
7-ацетил-4-[3-(4-хлорфенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
9-ацетил-4-[3-(4-хлорфенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-9-метил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
3-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)-N-(4-трифторметоксибензил)бензамід;
3-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)-N-(3-трифторметоксибензил)бензамід;
4-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)-N-(3-трифторметоксифеніл)бензамід;
3-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)-N-(4-трифторметоксифеніл)бензамід;
3-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)-N-(3-трифторметоксифеніл)бензамід;
4-хлор-N-[3-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)феніл]бензамід;
4-хлор-N-[5-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)тіазол-2-іл]бензамід;
1-(4-хлорфеніл)-3-[3-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)феніл]сечовина;
4-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)-N-(4-трифторметоксифеніл)бензолсульфонамід;
N-(4-хлорфеніл)-4-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-4-іл)-бензолсульфонамід;
4-[5-(5-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
7,7-диметил-4-[5-(5-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-хлорбензотіазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-хлорбензотіазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(5-хлорбензотіазол-2-ілсульфаніл)фуран-2-іл]-7,7-диметил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-дифторметокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(6-метокси-1Н-бензімідазол-2-ілокси)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(4-метил-1Н-імідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-метокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-метокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(5-метокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7,7-диметил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(1-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
7,7-диметил-4-[5-(1-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5,6-дихлор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5,6-дихлор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(5,6-дихлор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7,7-диметил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-хлорбензоксазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
етиловий ефір 9-[5-(5-гідрокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
4-[5-(5-хлорбензоксазол-2-ілсульфаніл)фуран-2-іл]-7,7-диметил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
7,7-диметил-4-[5-(4-метил-1Н-імідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-{5-[5-(4-хлорфеніл)-1-метил-1Н-імідазол-2-ілсульфаніл]фуран-2-іл}-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-{5-[5-(4-хлорфеніл)-1-метил-1Н-імідазол-2-ілсульфаніл]фуран-2-іл}-7,7-диметил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-{5-[5-(4-хлорфеніл)-1-метил-1Н-імідазол-2-ілсульфаніл]фуран-2-іл}-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(5-трифторметил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-1,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-трифторметил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-7,7-диметил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-трифторметил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(4,5-диметил-1Н-імідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(4,5-диметил-1Н-імідазол-2-ілсульфаніл)фуран-2-іл]-7,7-диметил-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(4,5-диметил-1Н-імідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
4-[5-(5-метил-1Н-бензімідазол-2-ілсульфаніл)тіофен-2-іл]-1,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
7,7-диметил-4-[5-(5-метил-1Н-бензімідазол-2-ілсульфаніл)тіофен-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
4-[5-(5-метил-1Н-бензімідазол-2-ілсульфаніл)тіофен-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он;
етиловий ефір 9-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
етиловий ефір 9-[5-(1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 9-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-6,6-диметил-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 10-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-9-оксо-2,4,5,6,7,8,9,10-октагідро-2,4-діазациклогепта[f]інден-3-карбонової кислоти;
етиловий ефір 9-[5-(5-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 6,6-диметил-9-[5-(5-метил-1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 9-[5-(5-метокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 9-[5-(5-метокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b][1,7]нафтиридин-3-карбонової кислоти;
етиловий ефір 9-[5-(3Н-імідазо[4,5-b]піридин-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 9-[5-(3Н-імідазо[4,5-b]піридин-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b][1,7]нафтиридин-3-карбонової кислоти;
етиловий ефір 9-[5-(5,6-дифтор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 9-[5-(5,6-дифтор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b][1,7]нафтиридин-3-карбонової кислоти;
етиловий ефір 9-[5-(5,6-дихлор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 9-[5-(3Н-імідазо[4,5-с]піридин-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 9-[2-(1Н-бензімідазол-2-ілсульфаніл)тіазол-5-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір (+)-9-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір (-)-9-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
(+)-4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
(-)-4-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
етиловий ефір 9-[5-(6,7-дифтор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 8-оксо-9-[5-(4,5,6-трифтор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
гідрохлорид етилового ефіру 9-[5-(5-гідрокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
9-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-6,6-диметил-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонова кислота;
9-[5-(1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-6,6-диметил-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбоксамід;
етиловий ефір 9-[5-(5-дифторметокси-1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 6-трет-бутилокси-9-[5-(5-дифторметокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-2,4,5,7,8,9-гексагідропіроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
гідрохлорид етилового ефіру 9-[5-(5-дифторметокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
етиловий ефір 9-[5-(5-хлор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 6-трет-бутилокси-9-[5-(5-хлор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-2,4,5,7,8,9-гексагідропіроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
гідрохлорид етилового ефіру 9-[5-(5-хлор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
етиловий ефір 8-оксо-9-[5-(5-трифторметил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 9-[5-(5-хлор-6-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 6-трет-бутилокси-9-[5-(5-хлор-6-метил-1H-бензімідазол-2-ілсульфаніл)-фуран-2-іл]-8-оксо-2,4,5,7,8,9-гексагідропіроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
гідрохлорид етилового ефіру 9-[5-(5-хлор-6-метил-1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
етиловий ефір 9-[5-(5-хлор-7-метил-1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 6-трет-бутилокси-9-[5-(5-хлор-7-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-2,4,5,7,8,9-гексагідропіроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
гідрохлорид етилового ефіру 9-[5-(5-хлор-7-метил-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
етиловий ефір 9-[5-(2,2-дифтор-5Н[1,3]діоксоло[4",5",4,5]бензо[1,2-d]імідазол-6-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
етиловий ефір 6-трет-бутилокси-9-[5-(2,2-дифтор-5Н-[1,3]діоксоло[4',5':4,5]бензо[1,2-d]імідазол-6-ілсульфаніл)фуран-2-іл]-8-оксо-2,4,5,7,8,9-гексагідропіроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
гідрохлорид етилового ефіру 9-[5-(2,2-дифтор-5Н-[1,3]діоксоло[4',5':4,5]бензо[1,2-d]імідазол-6-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
етиловий ефір 9-[5-(4,6-дифтор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
гідрохлорид етилового ефіру 9-[5-(5,7-дифтор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
4-[5-(5,7-дифтор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]хінолін-5-он;
гідрохлорид 4-[5-(5,7-дифтор-1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-2,4,6,7,8,9-гексагідропіразоло[3,4b]-1,7-нафтиридин-5-ону;
етиловий ефір 9-[5-(6-хлор-5-фтор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
гідрохлорид етилового ефіру 9-[5-(6-хлор-5-фтор-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
етиловий ефір 9-[5-(5-фтор-1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
гідрохлорид етилового ефіру 9-[5-(5-фтор-1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-8-оксо-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]-1,7-нафтиридин-3-карбонової кислоти;
етиловий ефір 8-оксо-9-[5-(5-трифторметокси-1Н-бензімідазол-2-ілсульфаніл)фуран-2-іл]-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b]хінолін-3-карбонової кислоти;
гідрохлорид етилового ефіру 8-оксо-9-[5-(5-трифторметокси-1H-бензімідазол-2-ілсульфаніл)фуран-2-іл]-4,5,6,7,8,9-гексагідро-2Н-піроло[3,4-b][1,7]нафтиридин-3-карбонової кислоти;
або адитивні солі з неорганічними і органічними кислотами або з неорганічними і органічними основами зазначених продуктів формули (І).
26. Спосіб одержання сполук формули (І), як визначено у пп. 1-24, який відрізняється тим, що
а/ похідне амінопіразолу (X=N) або амінопіролу (X=CR7) формули (II)
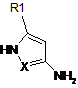 ,
,
b/ альдегід формули
R2-CHO (III)
і
с/ похідні дикетону формули (IV)
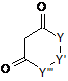 ,
,
де R1, R2, R7, Y, Y', Y" є такими, як визначено у пункті 1,
змішують у спиртовому розчиннику при температурі кипіння, одержуючи неочищену сполуку формули (І), яку потім необов'язково переводять на стадію зняття захисної групи і/або стадію очищення, і/або стадію солеутворення.
27. Сполука формули (І) за будь-яким з пп. 1-24 для застосування як лікарський засіб.
28. Фармацевтична композиція, що містить продукт за будь-яким з попередніх пунктів у поєднанні з фармацевтично прийнятним ексципієнтом.
29. Застосування сполуки за п. 1 як агента, що інгібує кіназу Aurora.
30. Застосування за п. 29 як агента, що інгібує проліферацію пухлинних клітин.
31. Застосування сполуки за п. 1 для одержання лікарського засобу для застосування при лікуванні патологічного стану.
32. Застосування за п. 31, де патологічний стан вибирають з раку, псоріазу, лейкемії і вовчака.
33. Застосування за п. 32, де патологічний стан являє собою рак.
Текст
Реферат: Винахід стосується 1,4-дигідропіридинконденсованих гетероциклів, способу їх одержання, застосування і композицій, що містять їх. Винахід стосується заміщених дигідропіридинконденсованих гетероциклів, які можна використовувати для лікування ракового захворювання, особливо для запобігання поділу ракових клітин. Дані сполуки діють як інгібітори кіназ Aurora А і/або В. Формула (І) R2 R1 O Y HN X N R3 Y'' Y' (І) UA 98928 C2 5 10 15 20 25 30 35 40 45 50 55 Даний винахід стосується нових хімічних сполук, зокрема, нових заміщених дигідропіридинконденсованих гетероциклів, композицій, що містять їх, і їх застосування як лікарських засобів. Більш конкретно, винахід стосується визначених, частково насичених конденсованих з піролом або піразолом 5-оксо-гексагідронафтиридинів або 5-оксо-гексагідрохінолінів, які проявляють протиракову активність за допомогою модулювання активності білків, зокрема, кіназ. До нашого часу більшість комерційно доступних сполук, використовуваних у хіміотерапії, являють собою цитотоксичні агенти, для яких характерні значні проблеми, пов'язані з побічними діями і переносимістю пацієнтами. Такі дії можна обмежити, якщо використовувані лікарські засоби будуть діяти селективно на ракові клітини, виключаючи здорові клітини. Отже, одне з рішень проблеми обмеження несприятливої дії хіміотерапії може полягати у застосуванні лікарських засобів, які діють на метаболічні шляхи або складові елементи таких шляхів, що експресуються головним чином у ракових клітинах, і які експресувалися б у незначному ступені або не експресувалися б здоровими клітинами. Протеїнкінази являють собою сімейство ферментів, що каталізують фосфорилування гідроксильних груп залишків специфічних білків, таких як залишки тирозину, серину або треоніну. Таке фосфорилування може широко модифікувати функцію білків; так, протеїнкінази відіграють важливу роль у регулюванні великого числа клітинних процесів, включаючи, зокрема, метаболізм, проліферацію клітин, диференціацію клітин, міграцію клітин і життєздатність клітин. Серед різних клітинних функцій, до яких залучена активність протеїнкінази, деякі процеси являють собою привабливі мішені для лікування пов'язаних з раком захворювань, а також інших захворювань. Таким чином, одна з задач даного винаходу полягає у створенні композицій, які володіють протираковою активністю, зокрема, впливають на кінази. Серед кіназ, модулювання активності яких розглядається, переважними є Aurora А і В. Огляд застосування інгібіторів кінази Aurora як протиракових агентів був зроблений нещодавно в "Aurora kinase inhibitors as anticancer agents". N. Keen and S. Taylor, Nature Reviews 2004, 4, 927-936. Багато білків, залучених до сегрегації хромосом і утворення веретена, було виявлено у дріжджах і дрозофілах. Дезорганізація функції даних білків веде до відсутності сегрегації хромосом і утворення монополярного або дезорганізованого веретена. Серед даних білків деякі кінази, включаючи Aurora і Ipl1, що мають походження з дрозофіли і S. cerevisiae, відповідно, необхідні для сегрегації хромосом і відділення центросоми. Людський аналог Ipl1 дріжджів нещодавно був клонований і охарактеризований у різних лабораторіях. Дана кіназа, називана Aurora2, Aurora A, STK15 або BTAK, належить до сімейства серин/треонінових кіназ. Bischoff et al. показали, що Aurora2 є онкогенною і поширена у клітинах раку прямої і ободової кишки (EMBO J, 1998, 17, 3052-3065). Подібні приклади також були показані на інших видах раку, включаючи пухлини епітелію, такі як рак молочної залози. Заслуговує на увагу той факт, що однією з переваг даного винаходу є розробка дійсно селективних сполук. Дійсно, дані сполуки звичайно не інгібують кінази, залучені до клітинної транскрипції, що може приводити до серйозних побічних дій і/або більш високої токсичності стосовно клітин у фазі спокою. У результаті, сполуки відповідно до винаходу звичайно не інгібують CDK7 і/або CDK9 кінази, або принаймні співвідношення інгібування складається на користь кінази Aurora. Наведені нижче публікації автори даної заявки вважають найближчими знайденими аналогами сполук формули (I) і (II) відповідно до винаходу: Drizin, Irene; Holladay, Mark W.; Yi, Lin; Zhang, Henry Q.; Gopalakrishnan, Sujatha; Gopalakrishnan, Murali; Whiteaker, Kristi L.; Buckner, Steven A.; Sullivan, James P.; Carroll, William A. "Structure-Activity studies for a novel series of tricyclic dihydropyrimidines as KATP channel openers (KCOs)". Bioorganic & Medicinal Chemistry Letters (2002), 12(11), 1481-1484. Quiroga, J. et al. Tetrahedron (2001) 57(32), 6947-6953 "Regioselective synthesis of 4,7,8, 9tetrahydro-2H-pyrazolo [3,4-b]quinolin5(6H)-ones". Drizin, Irene; Altenbach, Robert J.; Carroll, William A. "Preparation of tricyclic dіhуdrоруrаzоlоnе and tricyclic dihydroisoxozolone as potassium channel openers". Публікація заявки на патент США 2002007059 A1, WO 2001066544 A2. "New substituted benzimidazole derivatives are C-JUN N-terminal kinase inhibitors useful in the prevention and/or treatment of e.g. inflammatory diseases, autoimmune diseases, destructive bone disorders and neurodegenerative diseases". WO 200499190 A1. Gross, Rene; Lajoix, Anne-Dominique; Ribes, Gerard. "Novel methods for screening inhibitors of the interaction of rat neuronal nitric oxide synthase and its cognate inhibitor". WO02/083936 A2. 1 UA 98928 C2 5 10 15 Kohara, T; Fukunaga K, Fujimura M, Hanano T; Okabe H.: "Dihydropirazolopyridine compounds and pharmaceutical use thereof". WO02/72795 A2. Olsson L., Naranda T "Affinity small molecules for the EPO receptor" WO2004/005323 A2. Drees, BE; Chakravarty L.; Prestwich GD; Dorman; Kavecz M; Lukacs A; Urge L.; Darvas F; Rzepecki PW; Fergusson CG "Compound having inhibiting activity of phosphatidylinositol 3-kinase and methods of use thereof". WO2005/016245 A2. Kada, Rudolf; Knoppova, Viera; Kovac, Jaroslav; Cepec, Pavel. "Reaction of 2-cyano-3-(4,5dibromo-2-furyl)-2-propenenitrile and methyl 2-cyano-3-(4,5-dibromo-2-furyl)-2-propenenitrile and methyl 2-cyano-3-(4,5-dibromo-2-furyl)-2-propenoate with nucleophiles". Collection of Czechoslovak Chemical Communications (1984), 49(4), 984-91. Kada, Rudolf; Kovac, Jaroslav. "Furan derivatives. Part CXV. Condensation reactions of 5arylthio-and 5-heteroarylthio-2-furaldehydes with nitromethane". Collection of Czechoslovak Chemical Communications (1978), 43(8), 2037-40. У даний момент, неочікувано, і відповідно до першого аспекту даного винаходу, було встановлено, що продукти, які відповідають наведеній нижче загальній формулі (I), становлять особливий інтерес для інгібування кінази Aurora: , 20 25 30 35 40 45 де: R1 являє собою H, алкіл, арил, гетероарил, заміщений алкіл, заміщений арил, або заміщений гетероарил; R2 являє собою заміщений арил або заміщений гетероарил; R3 являє собою H або R4; X являє собою N або CR7; Y, Y' і Y": (i) кожний, незалежно, являє собою замісник, вибраний з CH 2, CHR5, CR5R6, C=O, O, S, NH, і NR7; або (ii) разом являють собою замісник, вибраний з ланцюжкових фрагментів -CH2-O-(C=O)-, (CH2)4- і -(CH2)2-; кожний з R4 і R7, незалежно, являє собою замісник, вибраний з: R8, -COOR8, COR8, і CONHR8; кожний з R5 і R6, незалежно, являє собою R8; R8 являє собою H або необов'язково заміщений: -алкіл, -алкіл-алкілен, -алкілен, гетероциклоалкіл, -циклоалкіл, -арил, -гетероарил, -алкіл-гетероциклоалкіл, -алкіл-циклоалкіл, алкіл-арил або -алкіл-гетероарил, -алкіл-NRaRb. Ra і Rb кожний, незалежно, являє собою H або алкіл, за умови, що R1 являє собою H, коли X являє собою N і Y' являє собою CR5R6. Формула (I) включає всі можливі таутомерні форми. Переважно, об'єктом винаходу є сполука формули (I), де R1 являє собою H. Переважно, об'єктом винаходу є сполука формули (I), де R3 являє собою H. Переважно, об'єктом винаходу є сполука формули (I), де Y і Y'' являють собою CH 2. Переважно, об'єктом винаходу є сполука формули (I), де Y' вибирають з CH 2, CHCH3, C(CH3)2, CH-арилу, CH-гетероарилу, CH-(заміщений арил), CH-(заміщений гетероарил), NH і NR7. Переважно, об'єктом винаходу є сполука формули (I), де R2 являє собою заміщений гетероарил, коли X являє собою N, і Y' являє собою CR5R6. Переважно, об'єктом винаходу є сполука формули (Ia): 2 UA 98928 C2 , 5 що відповідає сполуці формули (I), в якій X=N, R1=H, R3=H, Y=Y''=CH 2, і Y' = NH, де R2 являє собою заміщений арил. Більш переважно, об'єктом винаходу є сполука формули (Ia), як визначено вище, де R2 являє собою заміщену гетероарильну групу. Переважно, об'єктом винаходу є сполука формули (I'a): , 10 що відповідає сполуці формули (I), в якій X=N, R1=H, R3=H, Y=Y"=CH 2, і Y' = CR5R6, R5 і R6 є такими, як визначено вище, де R2 являє собою заміщену арильну групу. Більш переважно, об'єктом винаходу є сполука формули (I'a), як визначено вище, де R2 являє собою заміщену гетероарильну групу. Переважно, об'єктом винаходу є сполука формули (Ib): , 15 що відповідає сполуці формули (I), в якій X=CR7, R1=H, R3=H, Y=Y"=CH 2, і Y' = NH, R7 є таким, як визначено вище, де R2 являє собою заміщену арильну групу. Більш переважно, об'єктом винаходу є сполука формули (Ib), як визначено вище, де R2 являє собою заміщену гетероарильну групу. Переважно, об'єктом винаходу є сполука формули (I'b): , 20 25 що відповідає сполуці формули (I), в якій X=CHR7, R1=H, R3=H, Y=Y"=CH2, і Y' = CR5R6, R5, R6 і R7 є такими, як визначено вище, де R2 являє собою заміщену арильну групу. Найбільш переважно, об'єктом винаходу є сполука формули (I'b), як визначено вище, де R2 являє собою заміщену гетероарильну групу. Більш конкретно, об'єктом винаходу є сполука формули (Ia) або (Ib), де R2 являє собою заміщену фенільну або гетероарильну групу; де є присутнім від одного до чотирьох замісників, вибраних з галогену, алкілу, OH, OR8, CH 2-OR8, SH, SR8, NH2, NHR8, CONHR8, CONHCH2R8, 3 UA 98928 C2 5 10 15 20 25 30 35 40 45 50 55 NHCOR8, NHCONHR8, SO2-NHR8, фенілу, незаміщеного або заміщеного алкілом, OH або галогеном, де R8 є таким, як визначено вище. Більш конкретно, R8 вибирають з фенілу і гетероарилу, незаміщеного або заміщеного одним-чотирма замісниками, незалежно вибраними з F, Cl, Br, OH, SH, CF3, OCF3, OCH3, SCF3, SCH3, OCHF2, OCH2F, SCH2F, (C1-C6)-алкілу, O-алілу, фенілу, і фенілу, заміщеного галогеном. Більш конкретно, об'єктом винаходу є сполука формули (I'a) або (I'b), де R2 являє собою заміщену гетероарильну групу; де є присутнім від одного до чотирьох замісників, вибраних з галогену, алкілу, OH, OR8, CH2-OR8, SH, SR8, NH2, NHR8, CONHR8, CONHCH2R8, NHCOR8, NHCONHR8, SO2 NHR8, фенілу, незаміщеного або заміщеного алкілом, OH або галогеном, де R8 є таким, як визначено вище. Більш конкретно R8 являє собою феніл або гетероарил, незаміщений або заміщений однимчотирма замісниками, незалежно вибраними з F, Cl, Br, OH, SH, CF 3, OCF3, OCH3, SCF3, SCH3, OCHF2, OCH2F, SCH2F, (C1-C6)-алкілу, O-алілу, фенілу і фенілу, заміщеного галогеном. Більш конкретно, об'єктом винаходу є сполука формули (I), (Ia), (Ib), (I'a) і (I'b), де R2 являє собою гетероарил, заміщений SR8. Більш конкретно, об'єктом винаходу є сполука формули (I), (Ia), (Ib), (I'a) і (I'b), де R2 являє собою фурил або тієніл, заміщений SR8. Більш конкретно, R8 являє собою бензімідазоліл або імідазоліл, незаміщений або заміщений одним-чотирма замісниками, незалежно вибраними з F, Cl, Br, OH, SH, CF 3, OCF3, OCH3, SCF3, SCH3, OCHF2, OCH2F, SCH2F, (C1-C6)-алкілу, O-алілу, фенілу і фенілу, заміщеного галогеном. Більш конкретно, об'єктом винаходу є сполука формули (I), (I'a) і (I'b), де обидва R5 і R6 являють собою водень, або обидва являють собою метил. Більш конкретно, об'єктом винаходу є сполука формули (I), (I'a) і (I'b), де R5 являє собою водень, і R6 являє собою (C1-C6)-алкіл, заміщений або незаміщений, або феніл, заміщений або незаміщений. Більш конкретно, об'єктом винаходу є сполука формули (I), (Ib) і (I'b), де R7 являє собою групу -CO2Et. Більш конкретно, об'єктом винаходу є сполука, одержана відповідно до прикладів наведеної далі експериментальної частини. Сполука відповідно до першого аспекту винаходу може являти собою рацемічну форму, збагачену одним енантіомером, збагачену одним діастереомером, свої таутомери, свої проліки і свої фармацевтично прийнятні солі. У продуктах формули (I), як визначено вище і далі, алкільні, циклоалкільні, гетероциклоалкільні, арильні, гетероарильні, аралкільні або гетероаралкільні радикали необов'язково можуть бути заміщеними одним або декількома радикалами, що можуть бути однаковими або різними, вибраними з атомів галогену; і наступними радикалами: гідроксил; циклоалкіл, що містить не більше 6 кільцевих членів, ацил, що містить не більше 7 атомів вуглецю; ціано; нітро; вільний, солетворний і складноефірний карбоксил; тетразоліл; -NH2, NH(alk), -N(alk)(alk); SO2-NH-CO-NH-алкіл; SO2-NH-CO-NH-феніл; -C(O)-NH2; -C(O)-NH(alk); C(O)-N(alk)(alk), -NH-C(O)-(alk), -N(alk)-C(O)-(alk); тієніл; феніл, алкіл, алкілтіо, алкокси і фенокси, які самі необов'язково можуть бути заміщеними одним або декількома радикалами, вибраними з атомів галогену і гідроксилу, алкокси, алкільного, -NH2, -NH(alk) і -N(alk)(alk) радикалів. Більш конкретно, у продуктах формули (I), як визначено вище і далі, алкільний, циклоалкільний, гетероциклоалкільний, арильний, гетероарильний, аралкільний або гетероаралкільний радикали необов'язково можуть бути заміщеними одним або декількома радикалами, що можуть бути однаковими або різними, вибраними з атомів галогену; і наступних радикалів: гідроксил; вільний, солетворний і складноефірний карбоксил; -NH2, -NH(alk), N(alk)(alk); феніл, алкіл і алкокси, що самі необов'язково можуть бути заміщеними одним або декількома радикалами, вибраними з атомів галогену і гідроксилу, алкокси, алкільного, -NH2, NH(alk) і -N(alk)(alk) радикалів. Ще більш конкретно, у продуктах формули (I), як визначено вище і далі, алкільний, алкенільний, алкінільний, циклоалкільний, гетероциклоалкільний, арильний, гетероарильний, аралкільний або гетероаралкільний радикали необов'язково можуть бути заміщеними одним або декількома радикалами, що можуть бути однаковими або різними, вибраними з атомів галогену, гідроксилу і алкоксильних радикалів. У продуктах формули (I) і далі зазначені терміни мають наступне значення: - термін "галоген" стосується атомів фтору, хлору, брому, йоду, і переважно атомів фтору, хлору або брому; 4 UA 98928 C2 5 10 15 20 25 30 35 40 45 50 55 - термін "алкільний радикал" стосується лінійного або розгалуженого радикала, що містить не більше 12 атомів вуглецю, вибраного з метильного, етильного, пропільного, ізопропільного, бутильного, ізобутильного, втор-бутильного, трет-бутильного, пентильного, ізопентильного, втор-пентильного, трет-пентильного, неопентильного, гексильного, ізогексильного, вторгексильного і трет-гексильного радикалів, і також гептильного, октильного, нонільного, децильного, ундецильного і додецильного радикалів, а також їх лінійних і розгалужених ізомерів положення. Більш конкретно зазначимо алкільні радикали, що містять не більше 6 атомів вуглецю, і зокрема, метильний, етильний, пропільний, ізопропільний, н-бутильний, ізобутильний, трет-бутильний, лінійний або розгалужений пентильний, лінійний або розгалужений гексильний радикали; - термін "алкоксильний радикал", що може бути представлений, наприклад, OR, стосується лінійного або розгалуженого радикала, що містить не більше 12 атомів вуглецю, і переважно не більше 6 атомів вуглецю, вибраний, наприклад, з метокси, етокси, пропокси, ізопропокси, лінійного, вторинного або третинного бутокси, пентокси, гексокси або гептокси радикалів, а також з лінійних або розгалужених ізомерів положення; - термін "алкілтіо" або "алкіл-S-", що може бути представлений, наприклад, SR3, стосується лінійного або розгалуженого радикала, що містить не більше 12 атомів вуглецю, і, зокрема, метилтіо, етилтіо, ізопропілтіо і гептилтіо радикалів. У радикалах, що містять атом сірки, атом сірки може бути окиснений до SO або S(O)2 радикала; - термін "ацильний радикал" (COR) стосується лінійного або розгалуженого радикала, що містить не більше 12 атомів вуглецю, в якому радикал R являє собою атом водню або алкільний, циклоалкільний, циклоалкенільний, циклоалкільний, гетероциклоалкільний або арильний радикал, дані радикали мають зазначені вище значення і необов'язково є заміщеними, як зазначено; зазначимо, наприклад, формільний, ацетильний, пропіонільний, бутирильний або бензоїльний радикали, або ще валерильний, гексаноїльний, акрилоїльний, кротонільний або карбамоїльний радикали; - термін "циклоалкільний радикал" стосується моноциклічного або біциклічного карбоциклічного радикала, що містить від 3 до 10 членів кільця і стосується, зокрема, циклопропільного, циклобутильного, циклопентильного і циклогексильного радикалів. - термін "циклоалкілалкільний радикал" стосується радикала, в якому циклоалкіл і алкіл вибрані з їх значень, зазначених вище; таким чином, даний радикал стосується, наприклад, циклопропілметильного, циклопентилметильного, циклогексилметильного і циклогептилметильного радикалів; - термін "ацилокси радикал" призначений для позначення ацил-О-радикалів, в яких ацил має зазначені вище значення; зазначимо, наприклад, ацетокси або пропіонілокси радикали; - термін "ациламіно радикал" призначений для позначення ацил-N-радикалів, в яких ацил має зазначені вище значення; - термін "арильний радикал" стосується ненасичених карбоциклічних радикалів, що є моноциклічними або включають конденсовані кільця. Як приклади таких арильних радикалів можна зазначити, фенільний, нафтильний, антренільний і фенантренільний радикали; більш конкретно слід зазначити фенільний радикал; - термін "арилалкіл" призначений для позначення радикалів, які є результатом комбінації зазначених вище алкільних радикалів, що необов'язково є заміщеними, і арильних радикалів, також зазначених вище, які необов'язково є заміщеними; зазначимо, наприклад, бензильний, фенілетильний, 2-фенетильний, трифенілметильний або нафталінметильний радикали; - термін "гетероциклічний радикал" стосується насиченого (гетероциклоалкіл) або ненасиченого (включаючи гетероарил) (не всі ненасичені гетероарили обов'язково є ароматичними, наприклад, хроманіл, тетрагідрохіноліл) карбоциклічного радикала, що включає не більше 6 кільцевих членів, які перериваються одним або декількома однаковими або різними гетероатомами, вибраними з атомів кисню, азоту або сірки. Як гетероциклічні радикали, конкретно можна зазначити діоксолановий, діоксановий, дитіолановий, тіооксолановий, тіооксановий, оксиранільний, оксоланільний, діоксоланільний, піперазинільний, піперидильний, піролідинільний, імідазолідинільний, піразолідинільний, морфолінільний, тетрагідрофурильний, тетрагідротієнільний, хроманільний, дигідробензофурильний, індолінільний, піперидильний, пергідропіранільний, піридолінільний, тетрагідрохінолінільний, тетрагідроізохінолінільний, бензоксазинільний або тіоазолідинільний радикали, усі з який необов'язково є заміщеними. Серед гетероциклічних радикалів конкретно можна зазначити необов'язково заміщений піперазинільний, необов'язково заміщений піперидильний, необов'язково заміщений 5 UA 98928 C2 5 10 15 20 25 30 35 40 45 50 55 60 піролідинільний, імідазолідинільний, піразолідинільний, морфолінільний або тіоазолідинільний радикали. - Термін "гетероциклоалкілалкільний радикал" призначений для позначення радикалів, в яких гетероциклоалкільний і алкільний залишки мають вказані вище значення; - серед гетероарильних радикалів з 5 членами кільця, можна зазначити фурильні радикали, такі як 2-фурил і 3-фурил, тієнільні радикали, такі як 2-тієніл і 3-тієніл, і піролільний, діазолільний, тіазолільний, тіадіазолільний, тіатриазолільний, ізотіазолільний, оксазолільний, оксадіазолільний, 3- або 4-ізоксазолільний, імідазолільний, піразолільний та ізоксазолільний, триазолільний, триазинільний і тетразолільний радикали. Серед гетероарильних радикалів з 6 членами кільця можна зазначити особливо піридильні радикали, такі як 2-піридил, 3-піридил і 4-піридил і піримідильний, піримідинільний, піридазинільний і піразинільний радикали. Як конденсовані гетероарильні радикали, що містять принаймні один гетероатом, вибраний з сірки, азоту і кисню, можна зазначити, наприклад, бензотієніл, такий як 3-бензотієніл, бензофурил, бензотіазоліл, індоліл, бензімідазоліл, бензоксазоліл, тіонафтил, індоліл, ізоіндоліл, індазоліл, піридопіроліл, піридопіразоліл, нафтімідазоліл, імідазохіноліл, бензизотіазоліл, бензизоксазоліл, пуриніл, хінолініл, ізохінолініл і нафтиридиніл. Серед конденсованих гетероарильних радикалів більш конкретно можна зазначити бензотієніл, бензофураніл, індоліл або хінолініл, бензімідазоліл, бензотіазоліл, індолізиніл, ізохінолініл, хіназолінільну групу, дані радикали необов'язково є заміщеними, як зазначено для гетероарильних радикалів. Адитивні солі з неорганічними або органічними кислотами продуктів формули (I) можуть, наприклад, являти собою солі, утворені хлористоводневою кислотою, бромистоводневою кислотою, йодистоводневою кислотою, азотною кислотою, сірчаною кислотою, фосфорною кислотою, пропіоновою кислотою, оцтовою кислотою, трифтороцтовою кислотою, мурашиною кислотою, бензойною кислотою, малеїновою кислотою, фумаровою кислотою, бурштиновою кислотою, винною кислотою, лимонною кислотою, щавлевою кислотою, гліоксалевою кислотою, аспарагіновою кислотою, аскорбіновою кислотою, алкілмоносульфоновими кислотами, такими як, наприклад, метансульфонова кислота, етансульфонова кислота або пропансульфонова кислота, алкілдисульфоновими кислотами, такими як, наприклад, метандисульфонова кислота або альфа, бета-етандисульфонова кислота, арилмоносульфоновими кислотами, такими як бензолсульфонова кислота, і арилдисульфоновими кислотами. Відповідно до другого аспекту даний винахід стосується фармацевтичної композиції, що включає продукт відповідно до першого аспекту винаходу, у поєднанні з фармацевтично прийнятним ексципієнтом. Отже, даний винахід також стосується терапевтичних композицій, що містять сполуку відповідно до винаходу у поєднанні з фармацевтично прийнятним ексципієнтом в залежності від вибраного шляху введення. Фармацевтична композиція може бути у твердій або у рідкій або формі у вигляді ліпосом. Серед твердих композицій можна зазначити порошки, желатинові капсули і таблетки. До числа пероральних форм також можуть бути включені тверді форми, захищені від кислого середовища шлунку. Носії, використовувані для твердих форм, складаються, зокрема, з мінеральних носіїв, таких як або фосфати або карбонати, органічних носіїв, таких як лактоза, целюлоза, крохмаль або полімери. Рідкі форми включають розчини, суспензії або дисперсії. Вони містять як диспергуючий носій або воду, або органічний розчинник (етанол, НМП або тому подібні), або суміші поверхнево-активних речовин і розчинників, або комплексоутворювальних речовин і розчинників. Рідкі форми переважно будуть формами, призначеними для ін'єкцій, і, відповідно, будуть мати рецептурний склад, прийнятний для такого застосування. Прийнятні шляхи введення за допомогою ін'єкцій включають внутрішньовенний, внутрішньоочеревинний, внутрішньом'язовий і підшкірний шляхи введення, де внутрішньовенне введення є переважним. Доза сполук за винаходом, що вводиться, буде підібрана лікуючим лікарем в залежності від шляху введення пацієнту і стану зазначеного пацієнта. Сполуки за даним винаходом можна вводити самостійно або у вигляді суміші з іншими протираковими агентами. До можливих комбінацій, які можна зазначити, належать: - алкілуючі агенти і, особливо, циклофосфамід, мелфалан, іфосфамід, хлорамбуцил, бусульфан, тіотепа, преднімустин, кармустин, ломустин, семустин, стептозотоцин, декарбазин, темозоломід, прокарбазин і гексаметилмеламін; - похідні платини, особливо такі як цисплатин, карбоплатин або оксаліплатин; 6 UA 98928 C2 5 10 15 20 25 30 35 40 45 50 - антибіотики, особливо такі як вінбластин, вінкристин, віндезин або таксоїди (паклітаксел і доцетаксел); - антрацикліни, особливо такі як доксорубіцин, даунорубіцин, ідарубіцин, епірубіцин, мітоксантрон або лозоксантрон; - топоізомерази групи I і IІ, такі як етопозид, теніпозид, амсакрин, іринотекан, топотекан і томудекс; - фторпіримідини, такі як 5-фторурацил, UFT або флоксуридин; - аналоги цитидину, такі як 5-азацитидин, цитарабін, гемцитабін, 6-меркаптомурин або 6тіогуанін; - аналоги аденозину, такі як пентостатин, цитарабін або флударабін фосфат; - метотрексат і фолієва кислота; - різні ферменти і сполуки, такі як L-аспарагіназа, гідроксисечовина, транс-ретиноєва кислота, сурамін, дексразоксан, аміфостин, герцептин і гормони естроген і андроген; - протисудинні агенти, такі як комбретастатин, або похідні колхіцину і їх проліки. Також можна комбінувати сполуки за даним винаходом з променевою терапією. Таке лікування можна застосовувати одночасно, роздільно або послідовно. Лікування буде підібрано практикуючим лікарем для визначеного пацієнта, який піддається лікуванню. Відповідно до третього аспекту винахід стосується застосування продукту відповідно до його першого аспекту, як лікарського засобу. Отже, продукт відповідно до даного винаходу можна використовувати для одержання лікарського засобу, який можна використовувати для лікування патологічного стану, зокрема, раку. Відповідно до третього аспекту винахід стосується застосування продукту відповідно до його першого аспекту, як агента, що інгібує кіназу Aurora. Відповідно до третього аспекту винахід стосується застосування продукту відповідно до його першого аспекту, як агента, що інгібує проліферацію пухлинних клітин. Відповідно до четвертого аспекту винахід стосується застосування продукту відповідно до його першого аспекту для одержання лікарського засобу для застосування при лікуванні патологічного стану, особливо ракового стану. Як інгібітор проліферації пухлинних клітин зазначену сполуку можна використовувати для запобігання і лікування лейкозів, як первинних, так і метастатичних щільних пухлин, карцином і різних видів раку, зокрема, раку молочної залози; раку легенів; раку тонкого кишечнику; раку прямої і ободової кишки; раку дихальних шляхів, ротової частини глотки і підглотівника; раку стравоходу; раку печінки, раку шлунку, раку жовчних проток, раку жовчного міхура, раку підшлункової залози; раку сечовивідних шляхів, включаючи нирки, сечоводи і сечовий міхур; раку жіночих статевих шляхів, включаючи рак матки, шийки матки, яєчників, хоріокарциному і трофобластичну пухлину; раку чоловічих статевих шляхів, включаючи рак передміхурової залози, сім'яних пухирців, яєчок, рак зародкових клітин, рак ендокринних залоз, включаючи рак щитовидної залози, рак слизових залоз, рак надниркових залоз; раку шкіри, включаючи гемангіоми, меланоми, саркоми, включаючи саркому Капоші; пухлини мозку, нервів, очей, менінгеальних оболонок, включаючи астроцитоми, гліоми, гліобластоми, ретинобластоми, нейриноми, нейробластоми, шваноми, менінгіоми, злоякісні гематопоетичні пухлини; лейкемії (гостра лімфоцитна лейкемія (ALL), гостра мієлоїдна лейкемія (АМ), хронічна мієлоїдна лейкемія (СМ), хронічна лімфоцитна лейкемія (CLL)), хлорлейкоз, плазмоцитоми, лейкоз Т або В клітин, лімфоми не Ходжкінського типу і лімфоми Ходжкіна, мієломи і різні злоякісні гемопатії. Відповідно до п'ятого аспекту винахід стосується способу одержання трициклічного дигідропіридину формули (I) відповідно до наведеного нижче загального способу: Суміш 1 еквівалента піразолу або піролу (X=N або CR7), 1 еквівалента альдегіду R2-CHO і 1 еквівалента дикетопохідного нагрівають при температурі кипіння зі зворотним холодильником у спирті, такому як етанол або 1-бутанол протягом від ½ години до декількох годин. Розчин охолоджують до кімнатної температури. Цільову сполуку або виділяють фільтруванням, або розчинник видаляють у вакуумі. За необхідності, неочищений продукт очищають на силікагелі або з використанням препаративної високоефективної рідинної хроматографії (ВЕРХ). 7 UA 98928 C2 Коли Y' являє собою N-Boc, проводять зняття захисної групи у продукті з використанням розчину трифтороцтової кислоти у дихлорметані (50/50) або розчину хлористоводневої кислоти у діоксані. 5 10 15 Таким чином, винахід також стосується способу одержання сполук формули (I), який відрізняється тим, що а/ похідне амінопіразолу (X=NH) або амінопіролу (X=CR7) формули (II) b/ альдегід формули (III) R2-CHO і c/ похідне дикетону формули (IV) , де R1, R2, R7, Y, Y', Y" є такими, як визначено у пункті 1 формули винаходу, змішують у спиртовому розчиннику при температурі кипіння, одержуючи неочищену сполуку формули (I), яку потім необов'язково переводять на стадію зняття захисної групи і/або стадію очищення, і/або стадію солеутворення. A/ Загальний спосіб одержання N-заміщених трициклічних дигідропіридинів 8 UA 98928 C2 5 10 15 20 Трициклічну сполуку I у розчині дихлорметану (ДХМ) обробляють 2 еквівалентами бензилоксикарбонілхлориду, 2 еквівалентами діізопропілетиламіну (DIEA) і каталітичною кількістю 4-диметиламінопіридину (DMAP) при кімнатній температурі протягом 24 годин. Реакційну суміш виливають у 10 %-ний розчин гідросульфату калію і екстрагують ДХМ. Органічну фазу промивають водою, сушать над сульфатом магнію (MgSO 4) і концентрують у вакуумі. Неочищений продукт очищають на силікагелі, одержуючи Cbz-захищене похідне III. Boc-захисну групу видаляють при обробці сполуки III сумішшю трифтороцтової кислоти (ТФОК) і ДХМ (50/50) при кімнатній температурі протягом 1 години. Після упарювання розчинника неочищений продукт очищають на силікагелі, одержуючи IV. Ацильні похідні загальної формули V одержують у 2 стадії. Сполуки формули IV спочатку ацилюють різними ацилхлоридами у ДХМ з використанням DIEA і каталітичної кількості DMAP. Реакційну суміш перемішують протягом ночі при кімнатній температурі і виливають у воду. Суміш екстрагують ДХМ. Органічну фазу промивають водою, сушать над MgSO 4 і концентрують у вакуумі. Сполуки V очищають з використанням препаративної ВЕРХ. Алкільні похідні загальної формули VІ одержують зі сполук IV з використанням відповідних епоксидів в етанолі. Розчин або нагрівають при температурі кипіння зі зворотним холодильником протягом 2 годин, або піддають мікрохвильовому опроміненню при 110C протягом 10 хвилин. Суміш виливають у воду і екстрагують ДХМ. Розчин у ДХМ промивають водою, сушать над MgSO4 і концентрують. Одержаний продукт гідрують з використанням Pd/C в атмосфері водню. Після фільтрування через целіт® і упарювання неочищений продукт очищають з використанням препаративної рідинної хроматографії у поєднанні з масспектрометрією (РХ/МС). 9 UA 98928 C2 5 10 15 20 25 Ацильні похідні загальної формули VII одержують прямим ацилюванням I ацилхлоридами, як описано для III або ангідридами кислот у ДХМ з використанням DIEA протягом 2 годин при кімнатній температурі. Суміш виливають у 10 %-ний розчин гідросульфату калію і екстрагують ДХМ. Органічний розчин промивають водою, сушать над MgSO 4 і концентрують. Неочищений продукт безпосередньо обробляють розчином ТФОК/ДХМ (50/50) протягом 1 години при кімнатній температурі. Неочищені продукти очищають з використанням препаративної РХ/МС, одержуючи VII. Алкільні похідні загальної формули VIII одержують обробкою у приладі для мікрохвильового опромінення при 150 °C сполуки I відповідним епоксидом у N, N-диметилформаміді (ДМФ). Проміжну сполуку очищають з використанням препаративної ВЕРХ. Захисну групу в одержаному похідному знімають з використанням розчину ТФОК/ДХМ (50/50). Неочищений продукт очищають з використанням препаративної РХ/МС. B/ Загальний спосіб одержання комерційно недоступних альдегідів R2-CHO формули (III) - альдегіди загальної будови IХ: Суміш 1 еквівалента формілбензойної кислоти і 1 еквівалента похідного аніліну або бензилaміну в етилацетаті (AcOEt) обробляють дициклогексилкарбодіімідом (DCC) при 60C протягом декількох годин. Суміш виливають в 1н HCl. Органічну фазу збирають і послідовно промивають водою, розчином бікарбонату натрію і насиченим розчином солі. Розчин сушать над MgSO4 і концентрують. Неочищені продукти за необхідності очищають на силікагелі. - альдегіди загальної будови Х: Суміш 1 еквівалента амінобензальдегіду і 1 еквівалента похідного бензоїлхлориду у ДМФ обробляють 2 еквівалентами DIEA при мікрохвильовому опроміненні при 110C протягом 10 хвилин. Сполуки X звичайно випадають в осад, і їх збирають фільтруванням. - альдегіди загальної будови XI: 10 UA 98928 C2 5 10 Суміш 1 еквівалента амінобензальдегіду і 1 еквівалента похідного фенілізоціанату у ДМФ обробляють при мікрохвильовому опроміненні при 110C протягом 10 хвилин. Сполуки XІ звичайно випадають в осад, і їх збирають фільтруванням. - альдегіди загальної будови XII; Суміш 1 еквівалента хлорсульфонілбензальдегіду і 1 еквівалента похідного аніліну у дихлор-1,2-етані (DCE) обробляють надлишком піридину протягом декількох годин. Суміш виливають у 10 %-ний розчин HCl і екстрагують ДХМ. Органічну фазу промивають насиченим розчином солі, сушать над MgSО4 і концентрують. Неочищені продукти очищають на силікагелі, одержуючи альдегіди XII. 11 UA 98928 C2 - альдегіди загальної будови XV і XVI: або або 5 10 До розчину 1 еквівалента сполуки загальної формули XIII або XIV у сухому тетрагідрофурані (ТГФ) додають від 1 до 1,5 еквівалентів суспензії NaН при кімнатній температурі. Суміш перемішують при кімнатній температурі до припинення виділення газу і необов'язково нагрівають при 80C протягом 30 хвилин. Реакційну суміш охолоджують до кімнатної температури і додають розчин 1 еквівалента 5-нітро-фуральдегіду у ТГФ. Реакційну суміш перемішують до моменту завершення реакції і потім виливають у воду і екстрагують етилацетатом. Органічну фазу промивають насиченим розчином солі, сушать над MgSO 4 і концентрують. За необхідності неочищені продукти очищають колонковою хроматографією на силікагелі або перекристалізацією, одержуючи сполуки формули XV або XVI. - альдегіди загальної будови XVII і XVIII: 12 UA 98928 C2 5 10 15 Суміш 1 еквівалента 5-бромтіофен-2-карбоксальдегіду, 1 еквівалента сполуки загальної формули XIII або XIV і 2 еквівалентів карбонату калію нагрівають при 120C до завершення реакції. Потім реакційну суміш виливають у воду і екстрагують етилацетатом. Органічну фазу промивають насиченим розчином солі, сушать над MgSO 4 і концентрують. Неочищені продукти за необхідності очищають на силікагелі, одержуючи сполуки XVII або XVIII. - альдегіди загальної будови XIX: До розчину 1 еквівалента сполуки загальної формули XIIIa у сухому ТГФ додають від 1 до 1,5 еквівалентів суспензії NaН при кімнатній температурі. Суміш перемішують при кімнатній температурі до припинення виділення газу. Додають розчин 1 еквівалента 2-хлор-1,3-тіазол-5карбальдегіду у ТГФ. Реакційну суміш перемішують до завершення реакції і потім виливають у воду і екстрагують етилацетатом. Органічну фазу промивають насиченим розчином солі, сушать над MgSO4 і концентрують. Альтернативний спосіб обробки реакційної суміші може включати фільтрування реакційної суміші. Тверду речовину потім розбавляють водою і екстрагують етилацетатом і дихлорметаном. Органічні екстракти об'єднують, сушать над MgSO 4 13 UA 98928 C2 5 10 15 20 25 30 35 40 45 50 55 60 і концентрують. За необхідності неочищені продукти очищають колонковою хроматографією на силікагелі або перекристалізацією, одержуючи сполуки формули XIX. Експериментальна частина Методи: Аналітична РХ/МС, спосіб A: Аналізи методом аналітичної РХ/МС проводили з використанням насоса для ВЕРХ Shimadzu LC-10AD; планшетного автоматичного 215-ямкового пробовідбірника Gilson; УФ детектора Shimadzu SPD-10A; мас-спектрометра моделі PE Sciex API 100LC на основі YMC основної колонки S5 при елююванні з градієнтом ацетонітрилу (ACN), що містить 0,1 % ТФОК, у воді при швидкості потоку 0,1 мл/хв., подробиці градієнту наведені для кожного прикладу. Сполуки, елюйовані з колонки, виявляли методом мас-спектроскопії з електророзпиленням (МС EI). Аналітична РХ/МС, спосіб B: Аналіз проводили на мас-спектрометрі Waters моделі ZQ, що працює у режимі електророзпилення позитивних і негативних іонів (діапазон мас - 100-1200 атомних одиниць маси), встановленому на ВЕРХ приладі Agilent HP1100. Розділення проводили на колонці Waters Xbridge C18 (3×50 мм, діаметр частинок 2,5 мкм), підтримуваній при температурі 60 °C при елююванні градієнтом ацетонітрилу у воді, що містить 0,1 % (об./об.) мурашину кислоту при швидкості потоку 1,1 мл/хв. Форма градієнта була наступною: від 5 до 100 % ацетонітрилу протягом 5 хвилин, підтримка 100 % ацетонітрилу протягом 0,5 хвилини, потім знову до 5 % ацетонітрилу протягом 1 хвилини. Загальний час проходження складає 7 хвилин. Крім масспектрометрії здійснювали УФ детектування масиву при довжинах хвиль від 210 до 400 нM і розсіювання світла у парах проводили з використанням приладу Sedere Sedex 85. Аналітична РХ/МС, спосіб C: Аналіз проводили на мас-спектрометрі Waters моделі ZQ, що працює у режимі електророзпилення позитивних і негативних іонів (діапазон мас - 100-1200 атомних одиниць маси), встановленому на приладі Waters Acquity UPLC. Розділення проводили на колонці Waters UPLC BeН C18 (2,1×50 мм, діаметр частинок 1,7 мкм), підтримуваній при температурі 55 °C при елююванні градієнтом ацетонітрилу у воді, що містить 0,1 % (об./об.) мурашину кислоту при швидкості потоку 1,2 мл/хв. Форма градієнта була наступною: від 5 до 100 % ацетонітрилу протягом 3 хвилин, потім знову до 5 % ацетонітрилу протягом 1 хвилини. Загальний час проходження складає 4,5 хвилини. Крім мас-спектрометрії здійснювали УФ детектування масиву при довжинах хвиль від 210 до 400 нM. Препаративна РХ/МС, спосіб A: Розділення методом препаративної РХ/МС проводили на приладах Waters HPLC: насос 515 HPLC; модуль бінарного градієнта 2525; 2487 DAD (детектор подвійного поглинання); пристрій для керування зразками 2767, з'єднаний з мас-спектрометром Micromass. Продукти розділяли на колонці YMC Combi Prep Pro C18, елююючи градієнтом ацетонітрилу, що містить 0,1 % ТФОК, у воді, що містить 0,1 % ТФОК, при швидкості потоку 32 мл/хв. Для кожного розділення програмування градієнта підбирали на основі аналітичної хроматограми РХ/МС зразка. Препаративна РХ/МС, спосіб B: Сполуки очищають за допомогою РХ/МС з використанням системи Waters FractionLynx, що складається з градієнтного насоса Waters, модель 600, регенеруючого насоса Waters, модель 515, насоса підживлення Waters Reagent Manager, автоінжектора Waters, модель 2700, двох перемикачів Rheodyne, модель LabPro, фотодіодного детектора масиву Waters, модель 996, мас-спектрометра Waters, модель ZMD, і збирача фракцій Gilson, модель 204. Прилад керується програмним забезпеченням Waters FractionLynx. На виході ділильної колонки потік розщеплюється у співвідношенні 1/1000 з використанням сплітера LC Packing AccuRate, 1/1000 частина потоку змішується з метанолом (швидкість потоку 0,5 мл/хв.) і надсилається до детекторів, даний потік знову розщеплюється: ¾ потоку надсилається на фотодіодний детектор масиву і ¼ - на мас-спектрометр, залишок на виході з колонки (999/1000) надсилається у колектор фракцій, де потік направляється звичайно у відходи, якщо очікуваний сигнал маси не детектується програмним забезпеченням FractionLynx. Програмне забезпечення FractionLynx містить молекулярні формули очікуваних сполук і запускає колекцію сполук, коли детектується + + сигнал маси, що відповідає [M+H] і [M+Na] . У деяких випадках (в залежності від результату ++ аналітичної РХ/МС, коли детектується [M+2H] як інтенсивний іон) програмне забезпечення FractionLynx додатково забезпечене розрахунком половини молекулярної маси (MW/2), у даних ++ ++ умовах коли детектується сигнал з масою, що відповідає [M+2H] і [M+Na+H] також запускається програма збирання зразка. Сполуки збирають у зважені скляні пробірки. Після збирання, розчинник упарюють на центрифуговому роторі Jouan, модель RC 10.10, і 14 UA 98928 C2 визначають масу сполуки, зважуючи пробірки після упарювання розчинника. Подробиці, що стосуються колонки і градієнта наведені у наступній частині для кожного прикладу. Приклад 1: 4-(4-Гідрокси-3-метил-феніл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 5 10 15 20 25 30 До суміші 213 мг N-Boc-3,5-дикетопіперидину (1 ммоль) (N-Boc-3,5-дикетопіперидин може бути одержаний відповідно до патенту WO 06003096 A1) і 83 мг 3-амінопіразолу (1 ммоль) в 5 мл етанолу додають 136,2 мг 4-гідрокси-3-метилбензальдегіду (1 ммоль). Суміш нагрівають при температурі кипіння зі зворотним холодильником протягом 2 годин і охолоджують до кімнатної температури. Осад збирають фільтруванням і промивають етанолом, одержуючи 316 мг блідожовтої твердої речовини (вихід = 80 %). Аналітична РХ/МС, спосіб A: час утримання (RT) = 3,8 + хв. (2-85 % ACN/H2O градієнт протягом 7 хвилин) EI MС ([M+H] ): 397. N-Boc-3,5-дикетопіперидин може бути одержаний відповідно до патенту WO 2006003096 A1. 100 мг виділеної сполуки розчиняють у 5 мл ДХМ і обробляють 5 мл ТФОК протягом 1 години при кімнатній температурі. Після упарювання розчинника неочищений продукт безпосередньо очищають з використанням препаративної ВЕРХ з оберненою фазою. 50 мг цільової сполуки виділяють після ліофілізації фракцій (вихід = 50 %). Аналітична РХ/МС, спосіб + A: (2-85 % ACN/H2O градієнт протягом 7 хвилин) МС EI ([M+H] ): 297. RT=2,31. 1 H ЯМР (D6-ДМСО) (300 МГц, прилад Brucker): 1,99 (с, 3H); 3,64 (AB1, 2H); 4,09 (AB, 2H); 4,97 (с, 1H); 6,52 (д, 1H); 6,76 (д, 1H); 6,80 (с, 1H); 7,31 (С, 1H); 10,4 (с, 1H). Приклад 2: 4-[3-(4-Хлор-фенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою До суміші 107 мг N-Boc-3,5-дикетопіперидину (0,5 ммоль) і 42 мг 3-амінопіразолу (0,5 ммоль) у 2,5 мл етанолу додають 0,116 мл 3-(4-хлорфенокси)бензальдегіду (0,5 ммоль). Суміш нагрівають при температурі кипіння зі зворотним холодильником протягом 1/2 години і охолоджують до кімнатної температури. Розчин концентрують у вакуумі. Одержаний маслянистий залишок розчиняють у 2,5 мл ДХМ і обробляють 2,5 мл ТФОК при кімнатній температурі протягом 1 години. Після упарювання розчинника, неочищений продукт безпосередньо очищають з використанням препаративної ВЕРХ з оберненою фазою, одержуючи 70 мг білої твердої речовини після ліофілізації фракцій (вихід = 31 %). Аналітична + РХ/МС, спосіб A: (2-85 % ACN/H2O градієнт протягом 7 хвилин) МС EI ([M+H] ): 393, RT=3,91. 1 H ЯМР (D6-ДМСО) (300 МГц, прилад Brucker): 3,70 (AB, 2H); 4,18 (AB, 2H); 5,17 (с, 1H); 6,65 (д, 1H); 6,94 (м, 4H); 7,22 (м, 1H); 7,45 (м, 3H); 9,80 (c, 2H); 10,4 (с, 1H). 15 UA 98928 C2 Приклад 3: 4-[5-(1H-Бензімідазол-2-ілсульфаніл)фуран-2-іл]-1,4,6,7,8,9гексагідропіразоло[3,4-b]хінолін-5-он 5 10 15 20 25 До суміші 225 мг 1,3-циклогександіону (2 ммоль) і 183 мг 3-амінопіразолу (2,2 ммоль) в етанолі додають 490 мг 5-(1H-бензімідазол-2-іл-сульфаніл)фуран-2-карбальдегіду (2 ммоль). Суміш нагрівають при температурі кипіння зі зворотним холодильником протягом 1/2 години і охолоджують до кімнатної температури. Осад збирають фільтруванням і промивають етанолом, одержуючи 460 мг блідо-жовтої твердої речовини (вихід = 58 %). + Аналітична РХ/МС, спосіб A: (2-85 % ACN/H2O градієнт протягом 7 хвилин) МС EI ([M+H] ): 404, RT=3,13 хв. 1 H ЯМР (D6-ДМСО) (300 МГц, прилад Brucker): 1,96 (м, 2H); 2,26 (м, 2H); 2,54 (м, 2H); 4,11 (с, 1H); 5,22 (с, 1H); 5,97 (с, 1H); 6,85 (с, 1H); 7,16 (м, 2H); 7,37 (м, 1H); 7,46 (с, 1H); 7,55 (м, 1H); 10,0 (с, 1H); 12,2 (с, 1H); 12,47 (с, 1H). Приклад 4: 4-[5-(1H-Бензімідазол-2-ілсульфаніл)фуран-2-іл]-7,7-диметил-2,4,6,7,8,9гексагідропіразоло[3,4-b]хінолін-5-он До розчину 156 мг димедону (1 ммоль) і 91 мг 3-амінопіразолу (1,1 ммоль) в 5 мл етанолу додають 244 мг 5-(1H-бензімідазол-2-ілсульфаніл)фуран-2-карбальдегіду (1 ммоль). Суміш нагрівають при кипінні зі зворотним холодильником протягом 1 години. Розчин охолоджують до кімнатної температури і концентрують у вакуумі. Неочищений продукт безпосередньо очищають на силікагелі з використанням суміші дихлорметан/метанол 98/2, потім 96/4 як елюенту. Після упарювання фракцій виділяють 250 мг блідо-жовтої твердої речовини (58 %). + Аналітична РХ/МС, спосіб A: (2-85 % ACN/H2O градієнт протягом 7 хвилин.) МС EI ([M+H] ): 432, RT=2,56 хв. 1 H ЯМР (D6-ДМСО) (300 МГц, прилад Brucker): 0,81 (с, 3H); 0,87 (с, 3H); 2,00 (AB, 2H); 2,29 (AB, 2H); 5,02 (с, 1H); 5,85 (с, 1H); 6,72 Наведені нижче приклади сполук були одержані з використанням такого ж способу, як описано у прикладі 1: 16 UA 98928 C2 Таблиця 1 Назва сполуки Молекулярна маса очікуваної сполуки МС EI + ([M+H] ) РХ/МС RT (хв.) 5 4-(2-Фтор-феніл)-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 284,11 285,32 2,67* 6 4-(4-Фенокси-феніл)2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 358,14 359,43 3,6* 7 4-[3-(3,5-Дихлорфенокси)феніл]-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 427,07 428,32 3,29 8 4-[3-(4-трет-Бутилфенокси)феніл]-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 414,21 415,54 3,5 9 4-[3-(4-трифторметилфенілокси)феніл]-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 426,13 427,43 3,2 10 4-[3-(4-Метоксифенокси)феніл]-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 388,15 389,45 2,79 11 4-(3-п-Толілокси-феніл)2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 372,16 373,45 2,99 12 4-[3-(3,4Дихлорфенокси)феніл]2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 427,07 428,32 3,28 Прикл. номер Структура 17 UA 98928 C2 Продовження таблиці 1 Назва сполуки Молекулярна маса очікуваної сполуки МС EI + ([M+H] ) РХ/МС RT (хв.) 13 4-(3-Фенокси-феніл)2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 358,14 359,43 2,79 14 4-[3-(4-Хлор-фенокси)феніл]3-метил-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 406,12 407,90 2,87 15 4-[2-(4-Хлор-фенокси)феніл]2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 392,10 393,87 2,87 16 4-[5-(4-Хлор-феніл)фуран-2іл]-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 366,09 367,83 2,6 17 4-[5-(2-трифторметилфеніл)фуран-2-іл]-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 400,11 401,39 2,7 18 4-[5-(3-трифторметилфеніл)фуран-2-іл]-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 400,11 401,39 2,85 19 4-[5-(3,4дихлорфеноксиметил) фуран-2-іл]-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 431,06 432,31 3,02 20 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 404,11 405,48 1,85 Прикл. номер Структура 18 UA 98928 C2 Продовження таблиці 1 Прикл. номер 21 5 Назва сполуки МС EI + ([M+H] ) РХ/МС RT (хв.) 4-(2-алілоксифеніл)2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою Структура Молекулярна маса очікуваної сполуки 322,14 323,39 2,21 Умови аналітичної РХ/МС: спосіб A - градієнт від 2 до 80 % ацетонітрилу протягом 7 хв. * Умови аналітичної РХ/МС: спосіб A - градієнт від 5 до 85 % ацетонітрилу протягом 7 хв. Наведені нижче приклади сполук були одержані з використанням тих самих способів, які описано у прикладах 3 і 4: Таблиця 2 Молекул. маса очікуваної сполуки МС EI + ([M+H] ) РХ/МС RT (хв.) 22 4-[3-(4-Хлорфенокси)феніл]2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 391,86 392,85 3,01 23 4-[5-(3-Хлорфеніл)фуран-2іл]-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 365 366 3,74 24 4-[5-(3,4Дихлорфеноксиметил) фуран2-іл]-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 430 431 4,06 25 4-[5-(3-Трифторметилфеніл) фуран-2-іл]-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 399 400 3,94 26 4-[5-(2-Трифторметилфеніл) фуран-2-іл]-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 399 400 3,68 Прикл. номер Структура Назва сполуки 19 UA 98928 C2 Продовження таблиці 2 Молекул. маса очікуваної сполуки МС EI + ([M+H] ) РХ/МС RT (хв.) 27 4-[5-(4-Хлорфеніл)фуран-2іл]-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 365 366 3,6 28 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 417 418 3,01 29 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-7феніл-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 479 480 3,66 30 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-6,6диметил-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 431 432 3,33 31 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-7ізопропіл-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 445 446 3,57 32 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-7-(4метоксифеніл)-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 509 510 3,67 33 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-7(2,4-дихлорфеніл)-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 548 549 4,27 Прикл. номер Структура Назва сполуки 20 UA 98928 C2 Продовження таблиці 2 Молекул. маса очікуваної сполуки МС EI + ([M+H] ) РХ/МС RT (хв.) 34 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-7фуран-2-іл-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 469 470 3,38 35 7-Бензо[1,3]діоксол-5-іл-4-[5(1Н-бензімідазол-2ілсульфаніл)фуран-2-іл]2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 523 524 3,61 36 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-7(3,4-диметоксифеніл)2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 539 540 3,38 37 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-7пентил-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 473 474 4,25 38 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-7-(2фторфеніл)-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 497 498 3,73 39 4-[5-(1Н-Бензімідазол-2ілсульфаніл)фуран-2-іл]-7-(2метоксифеніл)-2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 509 510 3,77 Прикл. номер Структура Назва сполуки 21 UA 98928 C2 Продовження таблиці 2 Молекул. маса очікуваної сполуки МС EI + ([M+H] ) РХ/МС RT (хв.) 40 4-[5-(Піридин-2ілсульфаніл)фуран-2-іл]2,4,6,7,8,9гексагідропіразоло[3,4b]хінолін-5-он; сполука з трифтороцтовою кислотою 364 365 2.75 41 4-[5-(1H-Бензімідазол-2ілсульфаніл)фуран-2-іл]4,6,7,8,9,10-гексагідро-2H1,2,10-триазациклогепта[f] інден-5-он; сполука з трифтороцтовою кислотою 417,13 418,13 2,95 42 4-[5-(1H-Бензімідазол-2ілсульфаніл)фуран-2-іл]2,4,7,8-тетрагідро-6-окса1,2,8-триаза-s-індацен-5-он; сполука з трифтороцтовою кислотою 391,07 392,07 2,58 43 4-[3-(4-Хлор-фенокси)феніл]6,8-диметил-2,4,8,9тетрагідро-1,2,6,8,9-пентаазациклопента[b]нафталін-5,7діон; сполука з трифтороцтовою кислотою 435,11 436,11 2,55* Прикл. номер Структура Назва сполуки Умови аналітичної РХ/МС: спосіб A - градієнт від 2 до 80 % ацетонітрилу протягом 7 хв. * Умови аналітичної РХ/МС: спосіб A - градієнт від 30 до 90 % ацетонітрилу протягом 7 хв. 22 UA 98928 C2 Приклад 44: 4-[5-(1H-Бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-(трет-бутилоксикарбоніл)2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он; сполука з трифтороцтовою кислотою 5 10 15 20 25 30 До суміші 443 мг N-Boc-3,5-дикетопіперидину (2,08 ммоль) і 173 мг 3-амінопіразолу (2,08 ммоль) у 10 мл етанолу додають 508 мг 5-(1H-бензімідазол-2-ілсульфаніл)фуран-2карбальдегіду (2,08 ммоль). Суміш нагрівають при температурі кипіння зі зворотним холодильником протягом 1 години і охолоджують до кімнатної температури. Розчин концентрують і неочищений продукт очищають на силікагелі з використанням ДХМ/MeOH (95/5) як елюенту. Виділяють 590 мг блідо-жовтої твердої речовини 44 (вихід = 56 %). Аналітична + РХ/МС, спосіб A: (2-85 % ACN/H2O градієнт протягом 7 хвилин.) МС EI ([M+H] ): 505; RT: 3,79 хв. Приклад 45: 4-[5-(1H-Бензімідазол-2-ілсульфаніл)фуран-2-іл]-7-(2-гідрокси-3-піперидин-1-ілпропіл)-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он; сполука з трифтороцтовою кислотою 300 мг твердої речовини 44 (0,59 ммоль) розчиняють у 4 мл ДХМ і додають 0,184 мл бензилхлорформіату (1,3 ммоль) з подальшим додаванням 0,385 мл DIEA (2,36 моль) і 20 мг DMAP (0,16 ммоль). Реакційну суміш струшують протягом ночі при кімнатній температурі і потім виливають у 80 мл 10 % (ваг./об.) розчин KH2SO4 і екстрагують двічі 40 мл етилацетату. Об'єднані органічні екстракти промивають насиченим розчином солі, сушать над MgSO 4 і концентрують. Залишок безпосередньо обробляють 10 мл розчину ТФОК/ДХМ (50/50) протягом 1 години при кімнатній температурі. Розчин концентрують у вакуумі. Половину одержаного залишку розчиняють у 2 мл етанолу і безпосередньо використовують у кінцевій стадії. Розчин обробляють при мікрохвильовому опроміненні надлишкомсвіжоодержаного 1оксиранілметилпіперидину (одержаний при перемішуванні 274 мг епібромгідрину (2 ммоль) і 0,198 мл піперидину (2 ммоль) у 10 мл метанолу протягом ночі при кімнатній температурі). Суміш опромінюють мікрохвильовим випромінюванням протягом 15 хвилин при 150C. Розчин концентрують і одержаний залишок очищають з використанням препаративної ВЕРХ. Виділяють 29 мг очікуваної сполуки 45 (вихід = 4 %). Аналітична РХ/МС, спосіб A: (2-85 % ACN/H2O + градієнт протягом 7 хвилин.) ([M+H] ): 546, RT: 2,67 хв. Приклади 46-50: 23 UA 98928 C2 4-[3-(4-Хлор-фенокси)феніл]-7-(2-гідрокси-3-морфолін-4-іл-пропіл)-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он; сполука з трифтороцтовою кислотою (приклад 50) 5 10 15 20 25 30 35 Сполуку 50 одержують з використанням такого ж способу, як у прикладі 45 з використанням 3-(4-хлорфенокси)бензальдегіду як альдегіду. До суміші 1,07 г N-Boc-3,5-дикетопіперидину (5 ммоль) і 415 мг 3-амінопіразолу (5 ммоль) у 10 мл етанолу додають 962 мг 3-(4хлорфенокси)бензальдегіду (5 ммоль). Суміш нагрівають при температурі кипіння зі зворотним холодильником протягом 1 години і охолоджують до кімнатної температури. Розчин концентрують і неочищений продукт очищають на силікагелі з використанням ДХМ/MeOH (95/5) як елюенту. Виділяють 1,33 г блідо-жовтої твердої речовини 46 (вихід = 54 %). Аналітична + РХ/МС, спосіб A: МС EI ([M+H] ): 493; RT: 3,28 хв. (градієнт від 30 до 90 % ацетонітрилу протягом 7 хвилин). 1,21 г вказаної вище твердої сполуки (2,46 ммоль) розчиняють у 20 мл ДХМ і додають 0,184 мл бензилхлорформіату (4,92 ммоль) з подальшим додаванням 1,6 мл DIEA (9,84 моль) і 20 мг DMAP (0,16 ммоль). Реакційну суміш струшують протягом ночі при кімнатній температурі і потім виливають у 80 мл 10 % (ваг./об.) розчин KH2SO4 і екстрагують двічі 40 мл етилацетату. Об'єднані органічні екстракти промивають насиченим розчином солі, сушать над MgSO 4 і концентрують. Неочищений продукт очищають на силікагелі з використанням розчину ДХМ/MeOH 98/2 як елюенту. Виділяють 1,6 г цільової сполуки 47 (кількісний вихід). Аналітична + РХ/МС, спосіб A: МС EI ([M+H] ): 627; RT: 4,52 хв. (градієнт від 30 до 90 % ацетонітрилу протягом 7 хвилин). Продукт 47 обробляють 20 мл розчину ТФОК/ДХМ (50/50) протягом 1 години при кімнатній температурі. Розчин концентрують у вакуумі. Одержаний продукт очищають на силікагелі з використанням ДХМ/MeOH 90/10 як елюенту. Виділяють 0,91 г очікуваної сполуки 48 (вихід = + 64 %). Аналітична РХ/МС, спосіб A: МС EI ([M+H] ): 527; Час утримування: 2,66 хв. (градієнт від 30 до 90 % ацетонітрилу протягом 7 хвилин). Розчин 53 мг 48 (0,1 ммоль) і 21 мг 4-оксиранілметил-морфоліну (0,15 ммоль) в 1 мл етанолу нагрівають при температурі кипіння зі зворотним холодильником протягом 2 годин. Після охолодження суміш виливають у 80 мл води і екстрагують двічі 50 мл ДХМ. Об'єднані органічні екстракти промивають 50 мл 0,5н HCl, насиченим розчином солі, сушать над MgSO 4 і концентрують. Залишок 49 безпосередньо гідрують в атмосфері водню з використанням 0,01 ммоль паладію-на-вугіллі. Реакційну суміш перемішують протягом ночі і потім фільтрують через целіт®. Фільтрат концентрують і неочищений продукт безпосередньо очищають з використанням препаративної РХ/МС, спосіб A. Виділяють 45 мг цільової сполуки 50 (Вихід = + 85 %). Аналітична РХ/МС, спосіб A: [M+H] ): 536, RT: 3,77 хв. (градієнт від 5 до 85 % ацетонітрилу протягом 7 хвилин). 24 UA 98928 C2 Приклади 51 і 52: 4-[5-(1H-Бензімідазол-2-ілсульфаніл)фуран-2-іл]-9-(2-гідрокси-3-морфолін-4-іл-пропіл)2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он; сполука з трифтороцтовою кислотою (приклад 52) 5 10 15 20 25 До розчину 50 мг сполуки 44 (0,1 ммоль) в 1 мл EtOH і 1 мл ДМФ додають 21 мг 4оксиранілметил-морфоліну (0,15 ммоль). Розчин нагрівають при 150 °C при мікрохвильовому опроміненні протягом 20 хвилин. Розчин концентрують і залишок очищають з використанням препаративної РХ/МС, спосіб A. Сполуку 51 потім обробляють 2 мл розчину ТФОК/ДХМ (50/50) протягом 1 години при кімнатній температурі. Кінцевий продукт очищають препаративною РХ/Мас-спектрометрією (спосіб A). Виділяють 19 мг сполуки 52 (Вихід = 29 %). Аналітична + РХ/МС, спосіб A: ([M+H] ): 548, RT: 2,58 хв. (градієнт від 5 до 85 % ацетонітрилу протягом 7 хвилин). Приклад 53: 4-[3-(4-Хлор-фенокси)феніл]-7-(3,5-диметил-ізоксазол-4-карбоніл)-2,4,6,7,8,9гексагідропіразоло[3,4-b]-1,7-нафтиридин-5-он; сполука з трифтороцтовою кислотою До розчину 26,3 мг (0,05 ммоль) сполуки 48 в 0,5 мл ДХМ послідовно додають 12 мг 3,5диметилізоксазол-4-карбонілхлориду (0,75 ммоль), 16 мкл DIEA (0,1 ммоль) і 5 мг DMAP (0,04 ммоль). Реакційну суміш перемішують протягом ночі і потім виливають у 20 мл води і екстрагують двічі 10 мл ДХМ. Об'єднані органічні екстракти промивають насиченим розчином солі, сушать над MgSO4 і концентрують. Одержаний залишок розчиняють у суміші 1 мл метанолу і 0,1 мл оцтової кислоти. Сполуку гідрують з використанням Pd/C в атмосфері водню. Після гідрування протягом 20 годин суміш фільтрують через целіт® і фільтрат концентрують у вакуумі. Неочищений продукт очищають препаративною РХ/Мас-спектрометрією (спосіб A), + одержуючи 2,3 мг продукту 53, (Вихід = 7,4 %). Аналітичний спосіб A [M+H] : 516, RT: 4,45 хв. (градієнт від 5 до 85 % ацетонітрилу протягом 7 хв). Наведені нижче сполуки були одержані таким же способом: 25 UA 98928 C2 Таблиця 3 Прикл. номер 54 55 56 5 10 15 Структура Назва сполуки 4-[3-(4-Хлорфенокси)феніл]-7(ізоксазол-5-карбоніл)2,4,6,7,8,9гексагідропіразоло[3,4-b]1,7-нафтиридин-5-он; сполука з трифтороцтовою кислотою 4-[3-(4-Хлорфенокси)феніл]-7-(4метил-[1,2,3]тіадіазол-5карбоніл)-2,4,6,7,8,9гексагідропіразоло[3,4-b]1,7-нафтиридин-5-он; сполука з трифтороцтовою кислотою 4-[3-(4-Хлорфенокси)феніл]-7-(6-хлорпіридин-2-карбоніл)2,4,6,7,8,9гексагідропіразоло[3,4-b]1,7-нафтиридин-5-он; сполука з трифтороцтовою кислотою Молекул. маса очікуваної сполуки МС EI + ([M+H] ) РХ/МС RT (хв.) 487,90 488 4,34 519 520 4,5 532 533 4,66 Умови аналітичної РХ/МС: спосіб A, градієнт від 5 до 85 % ацетонітрилу протягом 7 хвилин. Приклад 57: 7-Ацетил-4-[3-(4-хлор-фенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою До розчину 25 мг (0,048 ммоль) сполуки 48 в 1 мл ДХМ послідовно додають 6 мкл оцтового ангідриду (0,06 ммоль) і 16 мкл DIEA (0,1 ммоль). Розчин перемішують протягом ночі і виливають у 20 мл води. Суміш екстрагують двічі 15 мл ДХМ. Об'єднані органічні екстракти промивають 10 %-ним розчином дигідросульфату калію, водою, сушать над MgSO 4 і концентрують. Неочищений продукт безпосередньо гідрують в атмосфері водню з використанням Pd/C як каталізатора. Реакційну суміш перемішують протягом ночі і потім фільтрують через целіт®. Фільтрат концентрують у вакуумі і одержаний залишок очищають за допомогою препаративної РХ/МС (спосіб A). Виділяють 1,1 мг цільового продукту 57 (вихід = + 4 %). Аналітична РХ/МС, спосіб A: [M+H] ): 435, RT: 3,71 хв. (градієнт від 5 до 85 % ацетонітрилу протягом 7 хвилин). Приклад 58: 9-Ацетил-4-[3-(4-хлор-фенокси)феніл]-2,4,6,7,8,9-гексагідропіразоло[3,4-b]-1,7нафтиридин-5-он; сполука з трифтороцтовою кислотою 26 UA 98928 C2 5 10 15 20 25 До розчину 25 мг (0,048 ммоль) сполуки 46 в 0,5 мл ДХМ послідовно додають 11 мкл оцтового ангідриду (0,11 ммоль) і 33 мкл DIEA (0,2 ммоль). Розчин перемішують при кімнатній температурі протягом 2 годин і виливають у 20 мл води. Суміш екстрагують двічі 15 мл ДХМ. Об'єднані органічні екстракти промивають 10 %-ним розчином дигідросульфату калію, водою, сушать над MgSO4 і концентрують. Неочищений продукт безпосередньо обробляють 1 мл розчину ТФОК/ДХМ (50/50) при кімнатній температурі протягом 1 години. Суміш концентрують у вакуумі і одержаний залишок очищають за допомогою препаративної РХ/МС (спосіб A). + Виділяють 23 мг цільового продукту 58 (вихід = 52 %). Аналітична РХ/МС, спосіб A: [M+H] : 435, RT: 4,33 хв. (градієнт від 5 до 85 % ацетонітрилу протягом 7 хвилин). Приклад 59: 4-[5-(1H-Бензімідазол-2-ілсульфаніл)фуран-2-іл]-9-метил-2,4,6,7,8,9гексагідропіразоло[3,4-b]хінолін-5-он; сполука з трифтороцтовою кислотою До розчину 30 мг (0,075 ммоль) сполуки 3 і 14 мкл йодистого метилу (0,225 ммоль) в 1 мл ДМФ додають 31 мг карбонату калію (0,225 ммоль). Розчин перемішують протягом 20 годин при кімнатній температурі і виливають у 20 мл води. Суміш екстрагують двічі 15 мл ДХМ. Об'єднані органічні екстракти промивають насиченим розчином солі, сушать над MgSO 4 і концентрують. Неочищений продукт очищають за допомогою препаративної РХ/МС (спосіб A). Виділяють 2,2 + мг цільового продукту 59 (вихід = 6 %). Аналітична РХ/МС, спосіб A: [M+H] ): 418, RT: 2,54 хв. (градієнт від 5 до 85 % ацетонітрилу протягом 7 хвилин). Приклад 60: 3-(5-оксо-2,4,6,7,8,9-гексагідро-піразоло[3,4b]-1,7-нафтиридин-4-іл)-N-(4трифторметокси-бензил)бензамід; сполука з трифтороцтовою кислотою Одержання альдегіду: До розчину 300 мг 3-карбоксибензальдегіду (2 ммоль) і 382 мг 4(трифторметокси)бензилaміну (2 ммоль) в 5 мл ДХМ послідовно додають 540 мг 1гідроксибензотриазолу (HOBt) (4 ммоль) і 0,63 мг діізопропілкарбодііміду (DIC) (4 ммоль). Реакційну суміш перемішують протягом ночі при кімнатній температурі і потім виливають у 20 мл 10 %-ного розчину KH2SO4. Суміш екстрагують двічі 15 мл етилацетату. Об'єднані органічні 27 UA 98928 C2 5 10 15 20 25 30 екстракти промивають 20 мл води і 20 мл насиченого розчину солі, сушать над MgSO 4 і концентрують, одержуючи 670 мг 3-форміл-N-(4-трифторметокси-бензил)бензаміду (Вихід = + 85 %). Аналітична РХ/МС, спосіб A: ([M+H] ): 324, RT: 5,24 хв. (градієнт від 5 до 85 % ацетонітрилу протягом 7 хвилин). Сполуку 60 одержують, як описано у прикладі 2, виходячи з 21,3 мг N-Boc-3,5-дикетопіперидину (0,1 ммоль), 8,3 мг 3-амінопіразолу (0,1 ммоль) і 32,3 мг 3форміл-N-(4-трифторметокси-бензил)бензаміду (0,1 ммоль) у суміші 0,5 мл етанолу і 0,5 мл ДМФ, одержуючи 22,5 мг продукту 60 після очищення за допомогою препаративної РХ/МС + (спосіб A, вихід = 38 %). Аналітична РХ/МС, спосіб A: ([M+H] ): 484, RT: 2,51 хв. (градієнт від 2 до 80 % ацетонітрилу протягом 7 хвилин). Приклад 61: 3-(5-оксо-2,4,6,7,8,9-гексагідро-піразоло[3,4b]-1,7-нафтиридин-4-іл)-N-(3трифторметокси-бензил)бензамід; сполука з трифтороцтовою кислотою Сполуку 61 одержували з використанням такого ж способу, як описано для 60, виходячи з 3(трифторметокси)бензилaміну. За допомогою препаративної РХ/МС виділяли 25,5 мг цільової + сполуки (спосіб A, вихід = 43 %). Аналітична РХ/МС, спосіб A: [M+H] ): 484, RT: 2,47 хв. (градієнт від 2 до 80 % ацетонітрилу протягом 7 хвилин). Приклад 62: 4-(5-оксо-2,4,6,7,8,9-гексагідропіразоло[3,4b]-1,7-нафтиридин-4-іл)-N-(3трифторметокси-феніл)бензамід; сполука з трифтороцтовою кислотою Одержання альдегіду: До розчину 300 мг 4-карбоксибензальдегіду (2 ммоль) і 382 мг 3(трифторметокси)аніліну (2 ммоль) в 5 мл етилацетату додають 830 мг дициклогексилкарбодііміду (DCC) (4 ммоль). Реакційну суміш нагрівають при 60 °C протягом ночі і потім виливають у 60 мл 1н розчину HCl. Суміш екстрагують двічі 30 мл етилацетату. Об'єднані органічні екстракти промивають 50 мл води, 50 мл насиченого розчину бікарбонату натрію і насиченим розчином солі, сушать над MgSO4 і концентрують. Неочищений продукт очищають на силікагелі, одержуючи 233 мг 4-форміл-N-(3-трифторметокси-феніл)бензаміду + (Вихід = 38 %). Аналітична РХ/МС, спосіб A: ([M+H] ): 310, RT: 5,60 хв. (градієнт від 5 до 85 % ацетонітрилу протягом 7 хвилин). Виходячи з 30,9 мг вказаного вище альдегіду (0,1 ммоль) і з використанням такого ж способу, як у прикладі 2, одержують 22,3 мг продукту 62 після препаративної РХ/МС (спосіб A, + вихід = 43 %). Аналітична РХ/МС, спосіб A: ([M+H] ): 470, RT: 2,61 хв. (градієнт від 2 до 80 % ацетонітрилу протягом 7 хвилин). Наведені нижче приклади сполук були одержані з використанням такого ж способу: 28
ДивитисяДодаткова інформація
Назва патенту англійською1,4-dihydropyridine-fused heterocycles, process for preparing the same, use and compositions containing them
Автори англійськоюMauger, Jacques, Nair Anil, MaNina, Bjergarde Kirsten, Filoche-Romme Bruno, Angouillant-Boniface Odile, Mignani, Serge, Carry Jean-Christophe, Clerc Francois, Minoux Herve, Schio, Laurent, Combeau Cecile
Назва патенту російською1,4-дигидропиридинконденсированные гетероциклы, способ их получения, применения и композиция, которая содержит их
Автори російськоюМожет Жак, Наир Анил, Ма Нина, Бьергард Кирстен, Филош-Ромм Брюно, Ангуйан-Бонифас Одиль, Миньяни Серж, Карри Жан-Кристоф, Клерк Франсуа, Мину Эрве, Шио Лоран, Комбо Сесиль
МПК / Мітки
МПК: C07D 471/14, A61K 31/4162, C07D 471/04
Мітки: містить, 1,4-дигідропіридинконденсовані, композиція, спосіб, гетероцикли, застосування, одержання
Код посилання
<a href="https://ua.patents.su/92-98928-14-digidropiridinkondensovani-geterocikli-sposib-kh-oderzhannya-zastosuvannya-i-kompoziciya-shho-mistit-kh.html" target="_blank" rel="follow" title="База патентів України">1,4-дигідропіридинконденсовані гетероцикли, спосіб їх одержання, застосування і композиція, що містить їх</a>
Попередній патент: Антитіло або його фрагмент, яке зв’язується з склеростином
Наступний патент: Захисна система проти зламу для дверних та віконних рам
Випадковий патент: Спосіб лікування хворих з кохлео-вестибулярними порушеннями внаслідок легкої черепно-мозкової травми за методом зубкової о.в. та самосюка і.з.












