Похідні бензімідазолу, фармацевтична композиція, що їх містить, спосіб їх одержання та їх застосування
Номер патенту: 83832
Опубліковано: 26.08.2008
Автори: Янг Хуа, Волпоул Крістофер, Лю Зіпінг, Паже Даніель
Формула / Реферат
1. Сполука формули І або її фармацевтично прийнятна сіль:
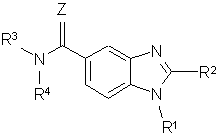 ,
,
де
Z вибрана з O= і S=;
R1 вибрана з С1-10алкілу, С2-10алкенілу, С2-10алкінілу, R5R6С1-6алкілу, R5О-С1-6алкілу, R5C(=O)N(-R6)-С1-6алкілу, R5R6NS(=O)2-С1-6алкілу, R5CS(=O)2N(-R6)-С1-6алкілу, R5R6NC(=O)N(-R7)-С1-6алкілу, R5R6NS(=O)2N(R7)-С1-6алкілу, С6-10арил-С(=О)-С1-6алкілу, С3-10циклоалкіл-С1-6алкілу, С4-8циклоалкеніл-С1-6алкілу, С3-6гетероцикліл-С1-6алкілу, С3-6гетероцикліл-С(=О)-С1-6алкілу, С1-10гідрокарбіламіно, R5R6N-, R5О-, R5C(=O)N(-R6)-, R5R6NS(=O)2-, R5СS(=O)2N(-R6)-, R5R6NC(=O)N(-R7)-, R5R6NS(=O)2N(R7)-, С6-10арилу, С6-10арил-C(=O)-, С3-10циклоалкілу, С4-8циклоалкенілу, С3-6гетероциклілу і С3-6гетероцикліл-С(=О)-; де зазначені С1-10алкіл, С2-10алкеніл, С2-10алкініл, С6-10арил-С1-6алкіл, С6-10арил-С(=О)-С1-6алкіл, С3-10циклоалкіл-С1-6алкіл, С4-8циклоалкеніл-С1-6алкіл, С3-6гетероцикліл-С1-6алкіл, С3-6гетероцикліл-С(=О)-С1-6алкіл, С1-10гідрокарбіламіно, С6-10арил, С6-10арил-С(=О)-, С3-10циклоалкіл, С4-8циклоалкеніл, С3-6гетероцикліл або С3-6гетероцикліл-С(=О)- у R1, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6,
R2 вибрана з групи, яку складають С1-10алкіл, С2-10алкеніл, С2-10алкініл, де зазначені С1-10алкіл, С2-10алкеніл, С2-10алкініл, використовувані у визначенні R2, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6;
де R5, R6 і R7 незалежно вибрані з -Н, С1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної С1-6групи, яка разом з іншими дивалентними R5, R6 або R7 утворює частину кільця; і
R3 і R4 незалежно вибрані з -Н, -ОН, аміно, R8 і -O-R8, де R8 незалежно вибрана з С1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної С1-6групи, яка разом з іншими дивалентними R8 утворює частину кільця, де R3 і R4 не є обидві -Н, а зазначені С1-6алкіл, С2-6алкеніл, С2-6алкініл або дивалентна С1-6група у R8, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, гідрокси, карбокси і -NR5R6; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6-членного кільця, причому зазначене кільце, як варіант, заміщене однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, гідрокси, карбокси і -NR5R6.
2. Сполука за п. 1, яка відрізняється тим, що у ній
Z є O=;
R1 вибрана з С1-6алкілу, С2-6алкенілу, С2-6алкінілу, R5R6N-С1-4алкілу, R5O-С1-4алкілу, R5С(=О)N(-R6)-С1-4алкілу, феніл-С(=О)-С1-4алкілу, С3-10циклоалкіл-С1-4алкілу, С4-6циклоалкеніл-С1-4алкілу, С3-6гетероцикліл-С1-4алкілу, С3-6гетероцикліл-С(=О)-С1-4алкілу, R5R6N-, R5O-, R5R6NS(=O)2-, С6-10арилу, С6-10арил-С(=О)-, С3-10циклоалкілу, С4-6циклоалкенілу, С3-6гетероциклілу і С3-6гетероцикліл-С(=О)-; де зазначені С1-6алкіл, С2-6алкеніл, С2-6алкініл, феніл-С1-4алкіл, феніл-С(=О)-С1-4алкіл, С3-10циклоалкіл-С1-4алкіл, С4-6циклоалкеніл-С1-4алкіл, С3-6гетероцикліл-С1-4алкіл, С3-6гетероцикліл-С(=О)-С1-4алкіл, С6-10арил, С6-10арил-С(=О)-, С3-10циклоалкіл, С4-6циклоалкеніл, С3-6гетероцикпіл або С3-6гетероцикліл-С(=О)- у R1, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6;
R2 вибрана з групи, яку складають С1-6алкіл, С2-6алкеніл, де зазначені С1-6алкіл або С2-6алкеніл, використовувані у визначенні R2, як варіант, заміщені одним або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6;
R3 і R4 незалежно вибрані з -ОН, аміно, С1-6алкілу і С1-6алкокси; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6-членного кільця, причому зазначене кільце, як варіант, заміщене групою, вибраною з гідрокси, карбокси, метилу і етилу; і
R5 і R6 незалежно вибрані з -Н, С1-6алкілу і С2-6алкенілу.
3. Сполука за п. 1, яка відрізняється тим, що у ній
Z є O=;
R1 вибрана з С1-6алкілу, С1-6алкенілу, R5R6N-С1-4алкілу, R5О-С1-4алкілу, R5C(=O)N(-R6)-С1-4алкілу, феніл-С(=О)-С1-4алкілу, С3-6циклоалкіл-С1-4алкілу, С4-6циклоалкеніл-С1-4алкілу, С3-6гетероцикліл-С1-4алкілу, С3-6гетероцикліл-С(=О)-С1-4алкілу, фенілу, С3-6циклоалкілу, С3-6гетероциклілу і С3-6гетероцикліл-С(=О)-; де зазначені С1-6алкіл, С2-6алкеніл, R5R6N-С1-4алкіл, R5O-С1-4aлкiл, R5C(=O)N(-R6)-С1-4алкіл, феніл-С1-4алкіл, феніл-С(=О)-С1-4алкіл, С3-6циклоалкіл-С1-4алкіл, С4-6циклоалкеніл-С1-4алкіл, С3-6гетероцикліл-С1-4алкіл, С3-6гетероцикліл-С(=О)-С1-4алкіл, феніл, С3-6циклоалкіл, С3-6гетероцикліл або С3-6гетероцикліл-С(=О)- у R1, як варіант, заміщені однією або більше групами, вибраними з галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6;
R2 є С1-6алкіл, як варіант, заміщений однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і R5R6N-;
R5 і R6 незалежно вибрані з -Н, С1-6алкілу і С2-6алкенілу; і
R3 і R4 незалежно вибрані з -ОН, аміно, С1-6алкілу і С1-6алкокси; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6-членного кільця, причому зазначене кільце, як варіант, заміщене групою, вибраною з гідрокси, метокси, етокси, метилу і етилу.
4. Сполука за п. 1, яка відрізняється тим, що у ній
Z є O=;
R1 вибрана з циклогексилметилу, циклопентилметилу, циклобутилметилу, циклопропілметилу, етилу, пропілу, адамантилу, адамантилметилу, алілу, ізопентилу, метоксіетилу, тетрагідропіранілметилу, тетрагідрофуранілметилу, циклогексилокси, циклогексиламіно, диметиламіноетилу, 4-піридилметилу, 2-піридилметилу, 1-піролілетилу, 1-морфоліноетилу, 4,4-дифлуорциклогексилметилу, циклогексилметилу, 2-піролідилметилу, N-метил-2-піролідилметилу, 2-піперидилметилу, N-метил-2-піперидилметилу, 3-тієнілметилу, (2-нітротіофен-5-іл)-метилу, (1-метил-1Н-імідазол-2-іл)метилу, (5-(ацетоксиметил)-2-фурил)-метилу, (2,3-дигідро-1Н-ізоіндол-1-іл)метилу і 5-(2-метилтіазоліл);
R2 вибрана з трет-бутилу, н-бутилу, 2-метил-2-бутилу, н-пентилу, ізопентилу, трифлуорметилу, 1,1-дифлуоретилу і 2-метокси-2-пропілу; і
R3 і R4 незалежно вибрані з метилу, етилу, гідрокси, метокси і стокси; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють групу, вибрану з ізоксазолідин-2-ілу, 4-гідроксіізоксазолідин-2-ілу, 4-гідрокси-4-метилізоксазолідин-2-ілу і N-морфолінілу.
5. Сполука, вибрана з групи сполук, яку утворюють
2-трет-бутил-N,N-діетил-1-{[(2R)-1-метилпіперидин-2-іл]метил}-1Н-бензімідазол-5-карбоксамід,
2-трет-бутил-1-(циклогексилметил)-N,N-діетил-1Н-бензімідазол-5-карбоксамід,
2-трет-бутил-1-(циклогексилметил)-N-метокси-N-метил-1Н-бензімідазол-5-карбоксамід,
1-(циклогексилметил)-2-(1,1-диметилпропіл)-N-метокси-N-метил-1Н-бензімідазол-5-карбоксамід,
1-(циклогексилметил)-2-{1,1-диметилпропіл)-N-метокси-N-метил-1Н-бензімідазол-5-карбоксамід,
1-(циклогексилметил)-2-(1,1-диметилпропіл)-N-морфолін-4-іл-1Н-бензімідазол-5-карбоксамід,
1-(циклогексилметил)-2-(1,1-диметилпропіл)-5-(морфолін-4-ілкарбоніл)-1Н-бензімідазол,
1-(циклогексилметил)-5-[(2,6-диметилморфолін-4-іл)карбоніл]-2-(1,1-диметилпропіл)-1Н-бензімідазол,
1-(циклогексилметил)-5-{[(2R,6S)-2,6-диметилморфолін-4-іл]карбоніл}-2-(1,1-диметилпропіл)-1Н-бензімідазол,
1-(циклогексилметил)-2-(1,1-диметилпропіл)-5-(ізоксазолідин-2-ілкарбоніл)-1Н-бензімідазол,
(4R)-2-{[1-(циклогексилметил)-2-(1,1-диметилпропіл)-1Н-бензімідазол-5-іл]карбоніл}-4-метилізоксазолідин-4-ол,
(4S)-2-{[1-(циклогексилметил)-2-(1,1-диметилпропіл)-1Н-бензімідазол-5-іл]карбоніл}-4-метилізоксазолідин-4-ол,
2-трет-бутил-1-(циклогексилметил)-N-метокси-1Н-бензімідазол-5-карбоксамід,
2-трет-бутил-1-(циклогексилметил)-N-етокси-1Н-бензімідазол-5-карбоксамід,
2-трет-бутил-1-(циклогексилметил)-N-етил-N-метил-1Н-бензімідазол-5-карбоксамід,
(4R)-2-{[2-трет-бутил-1-(циклогексилметил)-1Н-бензімідазол-5-іл]карбоніл}-ізоксазолідин-4-ол,
(4S)-2-{[2-трет-бутил-1-(циклогексилметил)-1Н-бензімідазол-5-іл]карбоніл}-ізоксазолідин-4-ол,
2-трет-бутил-1-(циклогексилметил)-5-(ізоксазолідин-2-ілкарбоніл)-1Н-бензімідазол,
(4R)-2-{[2-трет-бутил-1-(циклогексилметил)-1Н-бензімідазол-5-іл]карбоніл}-4-метилізоксазолідин-4-ол,
(4S)-2-{[1-(циклогексилметил)-2-(1,1-диметилпропіл)-1Н-бензімідазол-5-іл]карбоніл}-ізоксазолідин-4-ол,
2-трет-бутил-1-(циклогексилметил)-N-етокси-N-етил-1Н-бензімідазол-5-карбоксамід,
2-трет-бутил-N-метокси-N-метил-1-(тетрагідро-2Н-піран-4-ілметил)-1Н-бензімідазол-5-карбоксамід,
2-трет-бутил-5-(ізоксазолідин-2-ілкарбоніл)-1-(тетрагідро-2Н-піран-4-ілметил)-1Н-бензімідазол,
2-трет-бутил-1-[(4,4-дифлуорциклогексил)метил]-N-метокси-N-метил-1Н-бензімідазол-5-карбоксамід і
їх фармацевтично прийнятні солі.
6. Сполука згідно з будь-яким з пп. 1-5, призначена для використання як медикаменту.
7. Застосування сполуки за будь-яким з пп. 1-5 у виготовленні медикаменту, призначеного для лікування болю.
8. Застосування сполуки за будь-яким з пп. 1-5 у виготовленні медикаменту, призначеного для лікування розладу, пов'язаного з тривожністю.
9. Застосування сполуки за будь-яким з пп. 1-5 у виготовленні медикаменту, призначеного для лікування раку, множинного склерозу, хвороби Паркінсона, хореї Хантингтона, хвороби Альцгеймера, шлунково-кишкових розладів і серцево-судинних розладів.
10. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-5 і фармацевтично прийнятний носій.
11. Спосіб одержання сполуки формули II
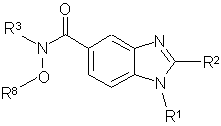 , II
, II
в якому проводять реакцію сполуки формули III
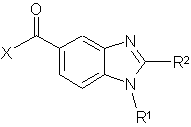 III
III
зі сполукою R3NHOR8 з одержанням сполуки формули II, в якій
X вибрана з Сl, Вr, І і ОН;
R1 вибрана з C1-10алкілу, C2-10алкенілу, C2-10алкінілу, R5R6C1-6алкілу, R5О-C1-6алкілу,R5C(=O)N(-R6)-C1-6алкілу, R5R6NS(=O)2-C1-6алкілу, R5СS(=O)2N(-R6)-C1-6алкілу, R5R6NC(=O)N(-R7)-C1-6алкілу, R5R6NS(=O)2N(R7)-C1-6алкілу, C6-10арил-C1-6алкілу, С6-10арил-С(=О)-C1-6алкілу, C3-10циклоалкіл-C1-6алкілу, С4-8циклоалкеніл-C1-6алкілу, C3-6гетероцикліл-C1-6алкілу, C3-6гетероцикліл-С(=О)-C1-6алкілу, C1-10гідрокарбіламіну, R5R6N-, R5O-, R5C(=О)N(-R6)-, R5R6NS(=O)2-, R5CS(=O)2N(-R6)-, R5R6NC(=O)N(-R7)-, R5R6NS(=O)2N(R7)-C6-10арилу, C6-10арил-С(=О)-, C3-10циклоалкілу, C4-8циклоалкенілу, C3-6гетероциклілу і C3-6гетероцикліл-С(=О)-; де зазначені C1-10алкіл, C2-10алкеніл, C2-10алкініл, C6-10арил-C1-6алкіл, C6-10арил-С(=О)-C1-6алкіл, C3-10циклоалкіл-C1-6алкіл, C4-8циклоалкеніл-C1-6алкіл, C3-6гетероцикліл-C1-6алкіл, C3-6гетероцикліл-С(=О)-C1-6алкіл, C1-10гідрокарбіламіно, C6-10арил, C6-10арил-С(=О)-, C3-10циклоалкіл, C4-8циклоалкеніл, C3-6гетероцикліл або C3-6гетероцикліл-С(=О)- у R1, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6;
R2 вибрана з групи, яку складають C1-10алкіл, C2-10алкеніл, C2-10алкініл, C3-8циклоалкіл, C3-8циклоалкіл-C1-6алкіл, C4-8циклоалкеніл-C1-6алкіл, C3-6гетероциклоалкіл-C1-6алкіл, C4-8циклоалкеніл, R5R6N-, C3-5гетероарил, C6-10арил і C3-6гетероциклоалкіл, де зазначені C1-10алкіл, C2-10алкеніл, C2-10алкініл, C3-8циклоалкіл, C3-8циклоалкіл-C1-6алкіл, C4-8циклоалкеніл-C1-6алкіл, C3-6гетероциклоалкіл-C1-6алкіл, C4-8циклоалкеніл, C3-5гетероарил, C6-10арил або C3-6гетероциклоалкіл у R2, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6;
де R5, R6 і R7 незалежно вибрані з -Н, C1-6алкілу, C2-6алкенілу, C2-6алкінілу і дивалентної C1-6групи, яка разом з іншими дивалентними R5, R6 або R7 утворює частину кільця;
R3 вибрана C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6групи, яка разом з дивалентною групою R8 утворює частину кільця;
R8 вибрана з -Н, C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6групи, яка разом з дивалентною групою R3 утворює частину кільця.
Текст
1. Сполука формули І або її фармацевтично прийнятна сіль: 2 3 83832 нітро, метокси, етокси, метилу, етилу, гідрокси і NR5R6; де R5, R6 і R7 незалежно вибрані з -Н, С1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної С 1-6гр упи, яка разом з іншими дивалентними R5, R6 або R7 утворює частину кільця; і R3 і R4 незалежно вибрані з -Н, -ОН, аміно, R8 і -OR8, де R8 незалежно вибрана з С1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної С 1-6гр упи, яка разом з іншими дивалентними R8 утворює частину кільця, де R3 і R4 не є обидві -Н, а зазначені С1-6алкіл, С2-6алкеніл, С2-6алкініл або дивалентна С1-6група у R8, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, гідрокси, карбокси і NR5R6; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6членного кільця, причому зазначене кільце, як варіант, заміщене однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, гідрокси, карбокси і -NR5R6. 2. Сполука за п. 1, яка відрізняється тим, що у ній Z є O=; R1 вибрана з С 1-6алкілу, С2-6алкенілу, С2-6алкінілу, R5R6N-С1-4алкілу, R5O-С1-4алкілу, R5С(=О)N(-R6)С1-4алкілу, феніл-С(=О)-С1-4алкілу, С3-10циклоалкілС1-4алкілу, С4-6циклоалкеніл-С 1-4алкілу, С3-6гетероцикліл-С1-4алкілу, С3-6 гетероциклілС(=О)-С1-4алкілу, R5R6N-, R 5 O-, R5R6NS(=O)2-, С6-10арилу, С 6-10арил-С(=О)-, С3-10циклоалкілу, С4-6циклоалкенілу, С3-6гетероциклілу і С3-6гетероцикліл-С(=О)-; де зазначені С1-6алкіл, С2-6алкеніл, С2-6алкініл, феніл-С 1-4алкіл, фенілС(=О)-С1-4алкіл, С3-10циклоалкіл-С 1-4алкіл, С4-6циклоалкеніл-С 1-4алкіл, С3-6гетероциклілС1-4алкіл, С3-6гетероцикліл-С(=О)-С1-4алкіл, С6-10арил, С6-10арил-С(=О)-, С3-10циклоалкіл, С4-6циклоалкеніл, С3-6гетероцикпіл або С3-6гетероцикліл-С(=О)- у R1, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6; R2 вибрана з групи, яку складають С 1-6алкіл, С2-6алкеніл, де зазначені С1-6алкіл або С 2-6алкеніл, використовувані у визначенні R2, як варіант, заміщені одним або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6; R3 і R4 незалежно вибрані з -ОН, аміно, С1-6алкілу і С1-6алкокси; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6членного кільця, причому зазначене кільце, як варіант, заміщене групою, вибраною з гідрокси, карбокси, метилу і етилу; і R5 і R6 незалежно вибрані з -Н, С1-6алкілу і С2-6алкенілу. 3. Сполука за п. 1, яка відрізняється тим, що у ній Z є O=; R1 вибрана з С 1-6алкілу, С1-6алкенілу, R5R6NС1-4алкілу, R5О-С1-4алкілу, R 5C(=O)N(-R 6)С1-4алкілу, феніл-С(=О)-С1-4алкілу, С3-6циклоалкілС1-4алкілу, С4-6циклоалкеніл-С 1-4алкілу, С3-6гетероцикліл-С1-4алкілу, С3-6 гетероциклілС(=О)-С1-4алкілу, фенілу, С3-6циклоалкілу, 4 С3-6гетероциклілу і С 3-6гетероцикліл-С(=О)-; де зазначені С1-6алкіл, С2-6алкеніл, R5R6N-С1-4алкіл, R5O-С1-4aлкiл, R5C(=O)N(-R 6)-С1-4алкіл, фенілС1-4алкіл, феніл-С(=О)-С1-4алкіл, С3-6циклоалкілС1-4алкіл, С4-6циклоалкеніл-С1-4алкіл, С3-6гетероцикліл-С1-4алкіл, С3-6гетероцикліл-С(=О)С1-4алкіл, феніл, С3-6циклоалкіл, С3-6гетероцикліл або С3-6гетероцикліл-С(=О)- у R1, як варіант, заміщені однією або більше групами, вибраними з галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6; R2 є С1-6алкіл, як варіант, заміщений однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і R5R6N-; R5 і R6 незалежно вибрані з -Н, С1-6алкілу і С2-6алкенілу; і R3 і R4 незалежно вибрані з -ОН, аміно, С1-6алкілу і С1-6алкокси; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6членного кільця, причому зазначене кільце, як варіант, заміщене групою, вибраною з гідрокси, метокси, етокси, метилу і етилу. 4. Сполука за п. 1, яка відрізняється тим, що у ній Z є O=; R1 вибрана з циклогексилметилу, циклопентилметилу, циклобутилметилу, циклопропілметилу, етилу, пропілу, адамантилу, адамантилметилу, алілу, ізопентилу, метоксіетилу, тетрагідропіранілметилу, тетрагідрофуранілметилу, циклогексилокси, циклогексиламіно, диметиламіноетилу, 4піридилметилу, 2-піридилметилу, 1-піролілетилу, 1-морфоліноетилу, 4,4дифлуорциклогексилметилу, циклогексилметилу, 2-піролідилметилу, N-метил-2-піролідилметилу, 2піперидилметилу, N-метил-2-піперидилметилу, 3тієнілметилу, (2-нітротіофен-5-іл)-метилу, (1метил-1Н-імідазол-2-іл)метилу, (5(ацетоксиметил)-2-фурил)-метилу, (2,3-дигідро1Н-ізоіндол-1-іл)метилу і 5-(2-метилтіазоліл); R2 вибрана з трет-бутилу, н-бутилу, 2-метил-2бутилу, н-пентилу, ізопентилу, трифлуорметилу, 1,1-дифлуоретилу і 2-метокси-2-пропілу; і R3 і R4 незалежно вибрані з метилу, етилу, гідрокси, метокси і стокси; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють групу, вибрану з ізоксазолідин-2-ілу, 4гідроксіізоксазолідин-2-ілу, 4-гідрокси-4метилізоксазолідин-2-ілу і N-морфолінілу. 5. Сполука, вибрана з групи сполук, яку утворюють 2-трет-бутил-N,N-діетил-1-{[(2R)-1метилпіперидин-2-іл]метил}-1Н-бензімідазол-5карбоксамід, 2-трет-бутил-1-(циклогексилметил)-N,N-діетил-1Нбензімідазол-5-карбоксамід, 2-трет-бутил-1-(циклогексилметил)-N-метокси-Nметил-1Н-бензімідазол-5-карбоксамід, 1-(циклогексилметил)-2-(1,1-диметилпропіл)-Nметокси-N-метил-1Н-бензімідазол-5-карбоксамід, 1-(циклогексилметил)-2-{1,1-диметилпропіл)-Nметокси-N-метил-1Н-бензімідазол-5-карбоксамід, 1-(циклогексилметил)-2-(1,1-диметилпропіл)-Nморфолін-4-іл-1Н-бензімідазол-5-карбоксамід, 1-(циклогексилметил)-2-(1,1-диметилпропіл)-5(морфолін-4-ілкарбоніл)-1Н-бензімідазол, 5 83832 1-(циклогексилметил)-5-[(2,6-диметилморфолін-4іл)карбоніл]-2-(1,1-диметилпропіл)-1Нбензімідазол, 1-(циклогексилметил)-5-{[(2R,6S)-2,6диметилморфолін-4-іл]карбоніл}-2-(1,1диметилпропіл)-1Н-бензімідазол, 1-(циклогексилметил)-2-(1,1-диметилпропіл)-5(ізоксазолідин-2-ілкарбоніл)-1Н-бензімідазол, (4R)-2-{[1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-іл]карбоніл}-4метилізоксазолідин-4-ол, (4S)-2-{[1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-іл]карбоніл}-4метилізоксазолідин-4-ол, 2-трет-бутил-1-(циклогексилметил)-N-метокси-1Нбензімідазол-5-карбоксамід, 2-трет-бутил-1-(циклогексилметил)-N-етокси-1Нбензімідазол-5-карбоксамід, 2-трет-бутил-1-(циклогексилметил)-N-етил-Nметил-1Н-бензімідазол-5-карбоксамід, (4R)-2-{[2-трет-бутил-1-(циклогексилметил)-1Нбензімідазол-5-іл]карбоніл}-ізоксазолідин-4-ол, (4S)-2-{[2-трет-бутил-1-(циклогексилметил)-1Нбензімідазол-5-іл]карбоніл}-ізоксазолідин-4-ол, 2-трет-бутил-1-(циклогексилметил)-5(ізоксазолідин-2-ілкарбоніл)-1Н-бензімідазол, (4R)-2-{[2-трет-бутил-1-(циклогексилметил)-1Нбензімідазол-5-іл]карбоніл}-4-метилізоксазолідин4-ол, (4S)-2-{[1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-іл]карбоніл}ізоксазолідин-4-ол, 2-трет-бутил-1-(циклогексилметил)-N-етокси-Nетил-1Н-бензімідазол-5-карбоксамід, 2-трет-бутил-N-метокси-N-метил-1-(тетрагідро-2Нпіран-4-ілметил)-1Н-бензімідазол-5-карбоксамід, 2-трет-бутил-5-(ізоксазолідин-2-ілкарбоніл)-1(тетрагідро-2Н-піран-4-ілметил)-1Н-бензімідазол, 2-трет-бутил-1-[(4,4-дифлуорциклогексил)метил]N-метокси-N-метил-1Н-бензімідазол-5-карбоксамід і їх фармацевтично прийнятні солі. 6. Сполука згідно з будь-яким з пп. 1-5, призначена для використання як медикаменту. 7. Застосування сполуки за будь-яким з пп. 1-5 у виготовленні медикаменту, призначеного для лікування болю. 8. Застосування сполуки за будь-яким з пп. 1-5 у виготовленні медикаменту, призначеного для лікування розладу, пов'язаного з тривожністю. 9. Застосування сполуки за будь-яким з пп. 1-5 у виготовленні медикаменту, призначеного для лікування раку, множинного склерозу, хвороби Паркінсона, хореї Хантингтона, хвороби Альцгеймера, шлунково-кишкових розладів і серцево-судинних розладів. 10. Фармацевтична композиція, яка містить сполуку за будь-яким з пп. 1-5 і фармацевтично прийнятний носій. 11. Спосіб одержання сполуки формули II 6 O R3 N R8 N O N R2 R1 , II в якому проводять реакцію сполуки формули III O N X R2 N R1 III зі сполукою R NHOR з одержанням сполуки формули II, в якій X вибрана з Сl, Вr, І і ОН; R1 вибрана з C1-10алкілу, C2-10алкенілу, C2-10алкінілу, R5R6C1-6алкілу, R5О-C1-6алкілу, R5C(=O)N(-R 6)-C1-6алкілу, R5R6NS(=O)2-C1-6алкілу, R5СS(=O)2N(-R6)-C1-6алкілу, R5R6NC(=O)N(-R 7)C1-6алкілу, R5R6NS(=O)2N(R7)-C1-6алкілу, C6-10арилC1-6алкілу, С6-10арил-С(=О)-C1-6алкілу, C3-10циклоалкіл-C1-6алкілу, С4-8циклоалкенілC1-6алкілу, C3-6гетероцикліл-C1-6алкілу, C3-6гетероцикліл-С(=О)-C1-6алкілу, C1-10гідрокарбіламіну, R5R6N-, R 5O-, R5C(=О)N(R6)-, R5R6NS(=O)2-, R5CS(=O)2N(-R6)-, 5 6 7 5 6 R R NC(=O)N(-R )-, R R NS(=O)2N(R7)-C6-10арилу, C6-10арил-С(=О)-, C3-10циклоалкілу, C4-8циклоалкенілу, C3-6гетероциклілу і C3-6гетероцикліл-С(=О)-; де зазначені C1-10алкіл, C2-10алкеніл, C2-10алкініл, C6-10арил-C1-6алкіл, C6-10арил-С(=О)-C1-6алкіл, C3-10циклоалкілC1-6алкіл, C4-8циклоалкеніл-C1-6алкіл, C3-6гетероцикліл-C1-6алкіл, C3-6гетероцикліл-С(=О)C1-6алкіл, C1-10гідрокарбіламіно, C6-10арил, C6-10арил-С(=О)-, C3-10циклоалкіл, C4-8циклоалкеніл, C3-6гетероцикліл або C3-6гетероцикліл-С(=О)- у R1, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6; R2 вибрана з групи, яку складають C1-10алкіл, C2-10алкеніл, C2-10алкініл, C3-8циклоалкіл, C3-8циклоалкіл-C1-6алкіл, C4-8циклоалкенілC1-6алкіл, C3-6гетероциклоалкіл-C1-6алкіл, C4-8циклоалкеніл, R5R6N-, C 3-5гетероарил, C6-10арил і C3-6гетероциклоалкіл, де зазначені C1-10алкіл, C2-10алкеніл, C2-10алкініл, C3-8циклоалкіл, C3-8циклоалкіл-C1-6алкіл, C4-8циклоалкенілC1-6алкіл, C3-6гетероциклоалкіл-C1-6алкіл, C4-8циклоалкеніл, C3-5гетероарил, C6-10арил або C3-6гетероциклоалкіл у R2, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6; де R5, R6 і R7 незалежно вибрані з -Н, C1-6алкілу, C2-6алкенілу, C2-6алкінілу і дивалентної C1-6гр упи, яка разом з іншими дивалентними R5, R6 або R7 утворює частину кільця; 3 8 7 83832 8 R3 вибрана C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6групи, яка разом з дивалентною групою R8 утворює частин у кільця; R8 вибрана з -Н, C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6групи, яка разом з дивалентною групою R3 утворює частин у кільця. Винахід стосується терапевтичних сполук - лігандів рецептора CB1, фармацевтичних композицій, які містять ці сполуки, процесів їх виготовлення і використання, зокрема, сполуки - агоністів рецептора CB1. Більш конкретно, винахід стосується сполук, які можуть бути ефективними проти болю, раку, множинного склерозу, хвороби Паркінсона, хореї Хантингтона, хвороби Альцгеймера, тривожних розладів, шлунково-кишкових розладів і серцево-судинних розладів. Боротьба з болем була важливим об'єктом досліджень протягом багатьох років. Добре відомо, що ліганди рецептора канабіноїду (наприклад, рецептора CB1, рецептора CB2), включаючи агоністи, антагоністи і зворотні агоністи полегшують біль у різних тваринних моделях, впливаючи на рецептори CB1 або CB2. Взагалі рецептори CB1 знаходяться переважно у центральній нервовій системі (ЦНС), а рецептори CB2 - у периферійній, головним чином, у клітинах і тканинах, пов'язаних з імунною системою. Якщо агоністи рецептора CB1, наприклад, D9тетрагідроканабінол (D9-ТНС) і анадамід є корисними у антиносисептичних моделях у тварин, вони схильні створювати небажані побічні явища у ЦНС, наприклад, психоактивність, схильність до зловживань, залежність від препаратів і толерантність до них тощо. Відомо, що ці небажані явища опосередковуються рецепторами CB1, розташованими у ЦНС. Існують дані, що вказують на те, що агоністи СВ1, які діють на периферії і обмежено у ЦНС, можуть полегшувати біль у людини або тварини з кращим загальним профілем in vivo. Отже, існує потреба у нових лігандах рецептора CB1, наприклад, агоністах, антагоністах або інверсних агоністах, які можуть полегшувати біль або лікувати інші пов'язані з болем симптоми або хвороб з меншою або мінімальною побічною діє на ЦНС. Винахід стосується лігандів рецептора CB1, які можуть бути використані у лікуванні болю і інших пов'язаних з ним симптомів і хвороб. Визначення Якщо не зазначено інше, номенклатура, використана у Прикладах, відповідає запропонованій у [Nomenclature of Organic Chemistry, Sections A, B, C, D, E, F, і H, Pergamon Press, Oxford, 1979], включеній в опис посиланням у випадках структурних термінів і правил найменування хімічних структур. Як варіант, імена сполук можна утворювати, використовуючи програму хімічних імен ACD/ChemSketch, Version 5,09/September 2001, Ad vanced Chemistry Development, Inc., Toronto, Canada. "Рецептори CB1/CB2" означає рецептори CB1 і/або CB2. Термін "Сm-n" або "Сm-nгрупа", використаний окремо або як префікс, стосується будь-якої групи з m-n атомами карбону і з 0-n мультивалентними гетероатомами, вибраними з O, S, N і P, де m і n дорівнюють 0 або є позитивними цілими, і n>m. Наприклад, "C1-6" означає хімічну групу з 1-6 атомами карбону і з 0-6 мультивалентними гетероатомами, вибраними з O, S, N і P. Термін "гідрокарбон", використаний окремо або як суфікс, або префікс, стосується будь-якої структури, що містить лише атоми карбону і гідрогену (до14 атомів карбону). Термін "гідрокарбоновий радикал" або "гідрокарбіл", використаний окремо або як суфікс, або префікс, стосується будь-якої структури, що є результатом видалення одного або більше гідрогенів з гідрокарбону. Термін "алкіл", використаний окремо або як суфікс, або префікс, стосується моновалентного лінійного або розгалуженого ланцюга гідрокарбонових радикалів, який містить від 1 до приблизно 12 атомів карбону. Якщо не визначено інше, "алкіл" взагалі включає як насичені, так і ненасичені алкіли. Термін "алкілен", використаний окремо або як суфікс, або префікс, стосується дивалентного лінійного або розгалуженого ланцюга гідрокарбонових радикалів, який містить від 1 до приблизно 12 атомів карбону і зв'язує дві стр уктури. Термін "алкеніл", використаний окремо або як суфікс, або префікс, стосується моновалентного лінійного або розгалуженого ланцюга гідрокарбонового радикалу, який містить щонайменше один карбон-карбоновий подвійний зв'язок і від щонайменше 2 до приблизно 12 атомів карбону. Термін "алкініл", використаний окремо або як суфікс, або префікс, стосується моновалентного лінійного або розгалуженого ланцюга гідрокарбонового радикалу, який має щонайменше один карбон-карбоновий потрійний зв'язок і від щонайменше 2 до приблизно 12 атомів карбону. Термін "циклоалкіл", використаний окремо або як суфікс, або префікс, стосується моновалентного гідрокарбонового радикалу, який містить кільце і має від щонайменше 2 до приблизно 12 атомів карбону. Термін "циклоалкеніл", використаний окремо або як суфікс, або префікс, стосується моновалентного гідрокарбонового радикалу, який містить кільце і має щонайменше один карбон-карбоновий подвійний зв'язок і від щонайменше 2 до приблизно 12 атомів карбону. Термін "циклоалкініл", використаний окремо або як суфікс, або префікс, стосується моновалентного гідрокарбонового радикалу, який містить кільце і має щонайменше один карбон-карбоновий потрійний зв'язок і від щонайменше 2 до приблизно 12 атомів карбону. Термін "арил", використаний окремо або як суфікс, або префікс, стосується моновалентного гідрокарбонового радикалу, який має одне або більше поліненасичених карбонових ароматичних 9 83832 кілець, (наприклад, має 4n+2 делокалізованих електронів) і від 5 до приблизно 14 атом карбону, причому радикал розташований на карбоні ароматичного кільця. Термін "неароматична група" або "неароматичний", використаний окремо, as суфікс або як префікс, стосується хімічної групи або радикалу без ароматичних кілець (наприклад, 4n+2 делокалізованих електронів). Термін "арилен", використаний окремо або як суфікс, або префікс, стосується дивалентного гідрокарбонового радикалу, який має одне або більше поліненасичених карбонових ароматичних кілець, (наприклад, має 4n+2 делокалізованих електронів) і від 5 до приблизно 14 атом карбону, і який зв'язує дві стр уктури. Термін "гетероцикл", використаний окремо або як суфікс, або префікс, стосується структури, що має кільце, або молекули з одним або більше мультивалентних гетероатомів, незалежно вибраних з N, O, P і S, як частини кільцевої структури, і включає від щонайменше 3 до приблизно 20 атомів у кільці(ях). Гетероцикл може бути насиченим або ненасиченим, з одним або більше подвійних зв'язків, і може містити більше одного кільця. Якщо гетероцикл має більше одного кільця, ці кільця можуть бути злитими або незлитими. Злитими кільцями звичайно є щонайменше два кільця з двома спільними атомами. Гетероцикл може бути ароматичним або неароматичним. Термін "гетероалкіл", використаний окремо або як суфікс, або префікс, стосується радикалу, який є результатом заміщення одного або більше атомів карбону алкілу одним або більше гетероатомами, вибраними з N, O, P і S. Термін "гетероароматичний", використаний окремо або як суфікс, або префікс, стосується структури, яка містить кільце, або молекули з одним або більше мультивалентними гетероатомами, незалежно вибраними з N, O, P і S, як частини кільцевої структур, і яка включає від щонайменше 3 до приблизно 20 атомів у кільці(ях), причому ця структура або молекула має ароматичний характер (наприклад, 4n+2 делокалізованих електронів). Термін "гетероциклічна група", "гетероциклічний компонент," "гетероциклічний" або "гетероцикло", використаний окремо або як суфікс, або префікс, стосується радикалу, отриманого з гетероциклу видаленням одного або більше гідрогенів. Термін "гетероцикліл", використаний окремо або як суфікс, або префікс, стосується моновалентного радикал, отриманого з гетероциклу видаленням одного гідрогену з карбонів кільця гетероциклу. Термін "гетероциклілен", використаний окремо або як суфікс, або префікс, стосується дивалентного радикал, отриманого з гетероциклу видаленням двох гідрогенів, який зв'язує дві структури. Термін "гетероарил", використаний окремо або як суфікс, або префікс, стосується гетероциклілу ароматичного характеру, де радикал гетероциклілу розташований на карбоні ароматичного кільця гетероциклілу. 10 Термін "гетероциклоалкіл", використаний окремо або як суфікс, або префікс, стосується неароматичного гетероциклілу. Термін "гетероарилен", використаний окремо або як суфікс, або префікс, стосується гетероциклілену ароматичного характеру. Термін "гетероциклоалкілен", використаний окремо або як суфікс, або префікс, стосується неароматичного гетероциклілену. Термін "6-членне" як префікс стосується групи з кільцем, яке має 6 кільцевих атомів. Термін "5-членне" як префікс стосується групи з кільцем, яке має 5 кільцевих атомів. 5-членним кільцевим гетероарилом є гетероарил з кільцем, яке має 5 кільцевих атомів і 1, 2 або 3 з цих атомів незалежно вибрані з N, O і S. Типовими 5-членними кільцевими гетероарилами є тієніл, фурил, піроліл, імідазоліл, тіазоліл, оксазоліл, піразоліл, ізотіазоліл, ізоксазоліл, 1,2,3триазоліл, тетразоліл, 1,2,3-тіадіазоліл, 1,2,3оксадіазоліл, 1,2,4-триазоліл, 1,2,4-тіадіазоліл, 1,2,4-оксадіазоліл, 1,3,4-триазоліл, 1,3,4тіадіазоліл і 1,3,4-оксадіазоліл. 6-членним кільцевим гетероарилом є гетероарил з кільцем, яке має 6 кільцевих атомів і 1,2 або 3 з цих атомів незалежно вибрані з N, O і S. Типовими 5-членними кільцевими гетероарилами є піридил, піразиніл, піримідиніл, триазиніл і піридазиніл. Термін "заміщений" як префікс стосується структури, молекули або групи, де один або більше гідрогенів заміщені однією або більше C 112гідрокарбоновими групами або однією або більше хімічними групами, що мають один або більше гетероатомів, вибраних з N, O, S, F, Cl, Br, І і P. Типові хімічні групи, що містять один або більше гетероатомів, включають гетероцикліл, -NO2, -OR, -Cl, -Br, -I, -F, -CF3, -C(=O)R, -C(=O)OH, -NH 2, -SH, NHR, -NR2, -SR, -SO3H, -SO 2R, -S(=O)R, -CN, -OH, C(=O)OR, -C(=O)NR 2, -NRC(=O)R, оксо(=О), іміно(=NR), тіо(=S) і оксіміно(=N-OR), де кожна "R" є C1-12гідрокарбілом. Наприклад, заміщеним фенілом може бути нітрофеніл, піридилфеніл, метоксифеніл, хлорфеніл, амінофеніл тощо, де нітро, піридил, метокси, хлор і аміногрупи можуть заміщати будь-який придатний гідроген на фенільному кільці. Термін "заміщений" як суфікс першої структури, молекули або групи, після яких стоять одне або більше імен хімічних гр уп, стосується другої структури, молекули або групи, які є результатом заміщення одного або більше гідрогенів першої структури, молекули або групи однією або більше пойменованими хімічними групами. Наприклад, "феніл, заміщений нітро" означає нітрофеніл. Термін "як варіант, заміщений" стосується груп, стр уктур, або молекул, заміщених і тих, що не заміщені. Гетероцикл включає, наприклад, моноциклічні гетероцикли, наприклад, азиридин, оксиран, тиїран, ацетидин, оксетан, тієтан, піролідин, піролін, імідазолідин, піразолідин, піразолін, діоксолан, сульфолан-2,3-дигідрофуран, 2,5-дигідрофуран, тіофан, піперидин, 1,2,3,6-тетрагідропіридин, піперазин, морфолін, тіоморфолін, піран, тіопіран, 2,3 11 83832 дигідропіран, тетрагідропіран, 1,4-дигідропіридин, 1,4-діоксан, 1,3-діоксан, діоксан, гомопіперидин, 2,3,4,7-тетрагідро-1Н-азепін, гомопіперазин, 1,3діоксепан, 4,7-дигідро-1,3-діоксепін і гексаметиленоксид. Крім того, гетероцикл включає ароматичні гетероцикли, наприклад, піридин, піразин, піримідин, піридазин, тіофен, фуран, фуразан, пірол, імідазол, тіазол, оксазол, піразол, ізотіазол, ізоксазол, 1,2,3-триазол, тетразол, 1,2,3-тіадіазол, 1,2,3оксадіазол, 1,2,4-триазол, 1,2,4-тіадіазол, 1,2,4оксадіазол, 1,3,4-триазол, 1,3,4-тіадіазол і 1,3,4оксадіазол. Гетероцикл також включає поліциклічні гетероцикли, наприклад, індол, індолін, ізоіндолін, хінолін, тетрагідрохінолін, ізохінолін, тетрагідроізохінолін, 1,4-бензодіоксан, кумарин, дигідрокумарин, бензофуран, 2,3дигідробензофуран, ізобензофуран, хромен, хроман, ізохроман, ксантен, феноксантен, тіантрен, індолізин, ізоіндол, індазол, пурин, фталазин, нафтиридин, хіноксалін, хіназолін, цинолін, птеридин, фенатридин, перимідин, фенантролін, феназин, фенотіазин, феноксазин, 1,2-бензізоксазол, бензотіофен, бензоксазол, бензотіазол, бензімідазол, бензотриазол, тіоксантин, карбазол, карболін, акридин, піролізидин і хінолізидин. Крім поліциклічних гетероциклів, описаних вище, гетероцикл включає поліциклічні гетероцикли, в яких кільцеве злиття двох або більше кілець включає більш, ніж один зв'язок, спільний для обох кілець, і більш, ніж два атоми, спільні для обох кілець. Прикладами таких з'єднаних містками гетероциклів є хінуклідин, діазабіцикло[2,2,1]гептан і 7оксабіцикло[2,2,1]гептан. Гетероцикліл включає, наприклад, моноциклічні гетероцикліли, наприклад, азаридиніл, оксираніл, тіїрагіл, ацетидиніл, оксетаніл, тієтаніл, піролщиніл, піролініл, імідазолідиніл, піразолідиніл, піразолініл, діоксоланіл, сульфоланіл, 2,3дигідрофураніл, 2,5-дигідрофураніл, тетрагідрофураніл, тіофаніл, піперидиніл, 1,2,3,6тетрагідропіридиніл, піперазиніл, морфолініл, тіоморфолініл, піраніл, тіопіраніл, 2,3-дигідропіраніл, тетрагідропіраніл, 1,4-дигідропіридиніл, 1,4діоксаніл, 1,3-діоксаніл, діоксаніл, гомопіперидиніл, 2,3,4,7-тетрагідро-1Н-азепініл, гомопіперазиніл, 1,3-діоксераніл, 4,7-дигідро-1,3-діоксепініл і гексаметиленоксиділ. Крім того, гетероцикліл включає ароматичні гетероцикліли або гетероарили, наприклад, піридиніл, піразиніл, піримідиніл, піридазиніл, тієніл, фурил, фуразиніл, піроліл, імідазоліл, тіазоліл, оксазоліл, піразоліл, ізотіазоліл, ізоксазоліл, 1,2,3триазоліл, тетразоліл, 1,2,3-тіадіазоліл, 1,2,3оксадіазоліл, 1,2,4-триазоліл, 1,2,4-тіадіазоліл, 1,2,4-оксадіазоліл, 1,3,4-триазоліл, 1,3,4тіадіазоліл, і 1,3,4-оксадіазоліл. Гетероцикліл включає також поліциклічні гетероцикліли (включаючи ароматичні або неароматичні), наприклад, індоліл, індолініл, ізоіндолініл, хінолініл, тетрагідрохінолініл, ізохінолініл, тетрагідроізохінолініл, 1,4-бензодіоксаніл, кумариніл, дигідрокумариніл, бензофураніл, 2,3дигідробензофураніл, ізобензофураніл, хроменіл, 12 хроманіл, ізохроманіл, ксантеніл, феноксатиїніл, тіантреніл, індолізиніл, ізоіндоліл, індазоліл, пуриніл, фталазиніл, нафтиридиніл, хіноксалініл, хіназолініл, цинолініл, птеридиніл, фенантридиніл, перимідиніл, фенантролініл, феназиніл, фенотіазиніл, феноксазиніл, 1,2-бензізоксазоліл, бензотіофеніл, бензоксазоліл, бензотіазоліл, бензімідазоліл, бензотриазоліл, тіоксантиініл, карбазоліл, карболініл, акридиніл, піролізидиніл і хінолізодиніл. Крім описаних вище поліциклічних гетероциклілів гетероцикліл включає поліциклічні гетероцикліли, в яких кільцеве злиття двох або більше кілець включає більш, ніж один зв'язок, спільний для обох кілець, і більш, ніж два атоми, спільні для обох кілець. Прикладами таких з'єднаних містками гетероциклів є хінукпідиніл, діазабіцикло[2,2,1]гептил і 7-оксабіцикло-[2,2,1]гептил. Термін "алкокси", використаний окремо або як суфікс, або префікс, стосується радикалів загальної формули -O-R, де -R є вибраним з гідрокарбонів радикалом. Типові алкокси включають метокси, етокси, пропокси, ізопропокси, бутокси, t-бутокси, ізобутокси, циклопропілметокси, алілокси і пропаргілокси. Термін "арилокси", використаний окремо або як суфікс, або префікс, стосується радикалів загальної формули -О-Ar, де -Ar є арилом. Термін "гетероарилокси", використаний окремо або як суфікс, або префікс, стосується радикалів загальної формули -О-Ar 1, де -Ar1 є гетероарилом. Термін "амін" або "аміно", використаний окремо або як суфікс, або префікс, стосується радикалів загальної формули -NRR', де R і R' незалежно вибрані з гідрогену або гідрокарбонових радикалів. "Ацил", використаний окремо, як префікс, або суфікс, означає -C(=O)-R, де -R, як варіант, заміщений гідрокарбілом, гідрогеном, аміно або алкокси. Ацильні групи включають, наприклад, ацетил, пропіоніл, бензоїл, фенілацетил, карбоетокси і диметилкарбамоїл. Галоген включає флуор, хлор, бром і йод. "Галогенований" як префікс групи означає, що один або більше гідрогенів групи заміщені одним або більше галогенами. "КT" або "кт" означає кімнатну температуру. Якщо перша кільцева група "злита" з другою кільцевою групою, це означає, що перше кільце і друге кільце мають щонайменше два спільні атоми. "Зв'язок" "зв'язаний" або "зв'язування," якщо не визначено інше, означають ковалентний зв'язок або з'єднання. Коли перша група, стр уктура або атом "безпосередньо зв'язані" з другою гр упою, структурою або атомом, щонайменше один атом першої групи, структури або атому утворює хімічний зв'язок з щонайменше одним атомом другої групи, стр уктури або атому. "Насичений карбон" означає атом карбону у структурі, молекулі або групі, де всі зв'язки, з'єднані з цим атом карбону є одиночними зв'язками, тобто відсутні подвійний або потрійний зв'язки, приєднані до цього атому карбону, і цей атом зви 13 83832 чайно приймає sp3-атомну орбітальну гібридизацію. "Ненасичений карбон" означає атом карбону у структурі, молекулі або групі, де щонайменше один зв'язок, з'єднаний з цим атомом карбону, не є одиночним зв'язком, тобто існує щонайменше один подвійний або потрійний зв'язок, з'єднаний з цим атомом карбону і цей атом карбону звичайно приймає sp- або sр3-атомну орбітальну гібридизацію. Термін "терапія" включає "профілактику", якщо не вказано інше. Термін "терапевтичний" і "терапевтично" інтерпретуються відповідно. Термін "терапія" також включає введення пацієнту ефективної кількості сполуки винаходу для полегшення загрозливого хворобливого стану, гострого або хронічного або поворотного стану. Це визначення також включає профілактичні терапії для відвернення поворотних станів і продовження терапії для хронічних розладів. Винахід включає сполуки формули І: де Z вибрана з O= і S=; R1 вибрана з C1-10алкілу, С2-10алкенілу, С2-10алкінілу, R5R6C1-6алкілу, R5О-С1-6алкілу, R5C(=O)N(-R 6)-C1-6алкілу, R5R6NS(=O)2-C1-6алкілу, R5СS(=O)1N(-R6)-C1-6алкілу, R5R6NC(=O)N(-R 7)C1-6алкілу, R5R6NS(=O)2N(R7)-C1-6алкілу, C6-10арил-С 1-6алкілу, C6-10арил-С(=О)C1-6алкілу, С3-10циклоалкіл-C1-6алкілу, С4-8циклоалкеніл-C1-6алкілу, С3-6гетероциклілС1-6алкілу, C3-6гетероцикліп-С(=О)-C1-6алкілу, C1-10гідрокарбіламіно, R5R6N-, R5O-, 5 6 S 6 5 R C(=O)N(-R )-, R R NS(=O)2, R CS(O)2N(-R6)-, R5R6NC(=O)N(-R 7)-, R5R6NS(=O)2N(R7)-, С6-10арилу, C6-10арил-С(=O)-, С3-10циклоалкілу, С4-8циклоалкенілу, С3-6гетероциклілу і С3-6гетероцикліл-С(=O)-; де зазначені C1-10алкіл, С2-10алкеніл, С2-10алкініл, C6-10арилС1-6алкіл, C6-10арил-C(=O)-С1-6алкіл, С3-10циклоалкіл-C1-6алкіл, С4-8циклоалкенілС1-6алкіл, С3-6гетероцикліл-С1-6алкіл, С3-6гетероцикліл-С(=О)-C1-6алкіл, C1-10гідрокарбіламіно, C6-10арил, C6-10арил-С(=О)-, С3-10циклоалкіл, C4-8циклоалкеніл, С3-6гетероцикліл або С3-6гетероцикліл-С(=O)- у R1, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NRSR6; R2 вибрана з групи, яку складають C1-10алкіл, С2-10алкеніл, С2-10алкініл, С3-8циклоалкіл, С3-8циклоалкіл-C1-6алкіл, С4-8циклоалкенілС1-6алкіл, С3-6гетероциклоалкіл-С1-6алкіл, C4-8циклоалкеніл, R5R6N-, С3-5гетероарил, C6-10арил і С 3-6гетероциклоалкіл, де зазначені C1-10алкіл, С2-10алкеніл, С2-10алкініл, С3-8циклоалкіл, С3-8циклоалкіл-С 1-6алкіл, С4-8циклоалкенілС1-6алкіл, С3-6гетероциклоалкіл-С1-6алкіл, 14 С4-8циклоалкеніл, С3-5гетероарил, C6-10арил або С3-6гетероциклоалкіл у R2, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6; де R5, R6 і R7 незалежно вибрані з -H, C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної С1-6групи, яка разом з іншими дивалентними R5, R6 або R7 утворює частину кільця; і R3 і R4 незалежно вибрані з -H, -OH, аміно, R8 і -O-R8, де R8 незалежно вибрана з C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6гр упи, яка разом з іншими дивалентними R8 утворює частину кільця, де R3 і R4 не є обидві -H, а зазначені C1-6алкіл, С2-6алкеніл, C2-6алкініл або дивалентна C1-6група у R8, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, гідрокси, карбокси і NR5R6; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6членного кільця, причому зазначені кільця, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, гідрокси, карбокси і -NR5R6. Винахід також включає стереоізомери, енантіомери, діастереомери, рацемати або їх суміші, здатні до гідролізу in vivo прекурсори і фармацевтично прийнятні солі сполуки формули 1, сольватовані або несольватовані форми сполуки формули 1, фармацевтичні композиції і рецептури, що містять їх, способи їх використання для лікування хвороб і станів окремо або у комбінації з іншими терапевтично активними сполуками або субстанціями, процеси і інтермедіати, потрібні для їх приготування, їх використання як медикаментів, їх використання у виготовленні медикаментів і їх використання для діагностики і аналізу. Згідно з одним з аспектів, винахід стосується сполуки формули І, її фармацевтично прийнятної солі, діастереомерів, енантюмерів або їх сумішей. де Z вибрана з O= і S=; R1 вибрана з C1-10алкілу, С2-10алкенілу, С2-10алкінілу, R5R6C1-6алкілу, R5O-C1-6алкілу, 5 6 5 6 R C(=O)N(-R )-C1-6алкілу, R R NS(=O)2-C1-6алкілу, R5CS(=O)2N(-R6)-C1-6алкілу, R5R6NC(=O)N(-R 7)C1-6алкілу, R5R6NS(=O)2N(R7)-C1-6алкілу, С6-10арилC1-6алкілу, С6-10арил-С(=О)-C1-6алкілу, C3-10циклоалкіл-С 1-6алкілу, С4-8циклоалкенілС1-6алкілу, С3-6гетероцикліл-C1-6алкілу, C3-6гетероцикліл-С(=О)-С1-6алкілу, C1-10гідрокарбіламіно, R5R6N-, R5O-, R5C(=O)N(R6)-, RSR6NS(=O)2-, R5CS(=O)2N(-R6)-, 5 6 7 5 6 R R NC(=O)N(-R )-, R R NS(=O)2N(R7)-, С6-10арилу, C6-10арил-С(=O)-, С3-10циклоалкілу, С4-8циклоалкенілу, С3-6гетероциклілу і С3-6гетероцикліл-С(=О)-; де зазначені C1-10алкіл, С2-10алкеніл, С2-10алкініл, C6-10арил-С 1-6алкіл, 15 83832 C6-10арил-С(=О)-C1-6алкіл, С3-10циклоалкілС1-6алкіл, С4-8циклоалкеніл-С1-6алкіл, С3-10гетероцикліл-С1-6алкіл, С3-6гетероциклілС(=О)-С1-6алкіл, C1-10гідрокарбіламіно, C6-10арил, C6-10арил-С(=О)-, С3-10циклоалкіл, C4-8циклоалкеніл, С3-6гетероцикліл або С3-6гетероцикліл-С(=O)- у R1, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NRSR6; R2 вибрана з групи, яку складають C1-10алкіл, С2-10алкеніл, С2-10алкініл, С3-6ациклоалкіл, С3-8циклоалкіл-С 1-6алкіл, С4-8циклоалкенілС1-6алкіл, С3-6гетероциклоалкіл-С1-6алкіл, C4-8циклоалкеніл, R5R6N-, С3-5гетероарил, C6-10арил і С 3-6гетероциклоалкіл, де зазначені C1-10алкіл, С2-10алкеніл, С2-10алкініл, С3-8циклоалкіл, С3-8циклоалкіл-С 1-6алкіл, С4-8циклоалкенілС1-6алкіл, C3-6гетероциклоалкіл-С1-6алкіл, С4-8циклоалкеніл, С3-5гетероарил, C6-10арил або С3-6гетероциклоалкіл у R2, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6; де R5, R6 і R7 незалежно вибрані з -H, C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6групи, яка разом з іншими дивалентними R5, R6 або R7 утворює частину кільця; і R3 і R4 незалежно вибрані з -H, -OH, аміно, R8 і -O-R8, де R8 незалежно вибрана з C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6гр упи, яка разом з іншою дивалентною R8 утворює частину кільця, де R3 і R4 не є обидві -H, а зазначені C1-6алкіл, С2-6алкеніл, С2-6алкініл або дивалентнаC1-6група у R8, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, гідрокси, карбокси і NR5R6; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6членного кільця, причому зазначене кільце, як варіант, заміщене однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, гідрокси, карбокси і -NR5R6. Зокрема, сполуками згідно з винаходом є сполуки формули І, де Z є O=; R1 вибрана з C1-6алкілу, С2-6алкенілу, С2-6алкінілу, R5R6N-C1-4алкілу, R5O-C1-4алкілу, 5 6 R C(=O)N(-R )-C1-4алкілу, феніл-C1-4алкілу, фенілС(=О)-C1-4алкілу, С3-10циклоалкіл-C1-4алкілу, С4-6циклоалкеніл-С 1-4алкілу, С3-6гетероциклілС1-4алкіл, С3-6гетероцикліл-С(=О)-С1-4алкілу, R5R6N-, R5O-, R5R6NS(=O)2-, C6-10арилу, C6-10арилС(=О)-, С3-10циклоалкілу, С4-6циклоалкеніл, С3-6гетероциклілу і С 3-6гетероцикліл-С(=О)-; де зазначені C1-6алкіл, С2-6алкеніл, С2-6алкініл, фенілС1-4алкіл, феніл-С(=О)-С1-4алкіл, С3-10циклоалкілС1-4алкіл, С4-6циклоалкеніл-С1-4алкіл, С3-6гетероцикліл-С1-4алкіл, С3-6гетероцикліл-С(=O)C1-4алкіл, C6-10арил, C6-10арил-С(=О)-, C3-10циклоалкіл, С4-6циклоалкеніл, С3-6гетероцикліл або С3-6гeтероцикліл-С(=О)- у R1, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6; 16 R2 вибрана з групи, яку складають C1-6 алкіл, С2-6алкеніл, С3-6циклоалкіл, С3-6циклоалкілС1-4алкіл, С4-6циклоалкеніл-С1-4алкіл, С3-6гетероциклоалкіл-С1-4алкіл, С4-6циклоалкеніл, C3-5гетероарил, R5R6N-, феніл і С3-6гетероциклоалкіл, де зазначені C1-6алкіл, С2-6алкеніл, C3-6циклоалкіл, С1-6циклоалкілС1-6алкіл, С1-6циклоалкеніл-С1-6алкіл, С3-6гетероциклоалкіл-C1-6алкіл, С4-6циклоалкеніл, С3-5гетероарил, феніл або С3-6гетероциклоалкіл у R2, як варіант, заміщені одним або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR 5R6; R3 і R4 незалежно вибрані з -OH, аміно, C1-6алкілу і C1-6алкокси або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6-членного кільця, причому зазначене кільце, як варіант, заміщене групою, вибраною з гідрокси, карбокси, метилу і етилу; і R5 і R6 незалежно вибрані з -H, C 1-6алкілу і С2-6алкенілу. Зокрема, сполуками винаходу є сполуки формули 1, в яких: Z є O=; R1 вибрана з C1-6алкілу, C1-6алкенілу, R5R6NC1-4алкілу, R5O-C1-4алкілу, R 5C(=O)N(-R 6)С1-4алкілу, феніл-С 1-4алкілу, феніл-С(=О)С1-4алкілу, С3-6циклоалкіл-С 1-4алкілу, C4-6циклоалкеніл-С 1-4алкілу, С3-6гетероциклілС1-4алкілу, С3-6гетероциклiл-С(=О)-С1-4алкілу, фенілу, С3-6циклоалкілу, С3-6 гетероциклілу і С3-6гетероцикліл-С(=O)-; де зазначені С1-6алкіл, C2-6алкеніл, R5R6N-C1-4алкіл, R5O-C1-4алкіл, 5 6 R С(=О)N(-R )-C1-4алкіл, феніл-С 1-4алкіл, фенілС(=О)-С1-4алкіл, С3-6циклоалкіл-С 1-4алкіл, С4-6циклоалкеніл-С 1-4алкіл, С3-6гетероциклілC1-4алкіл, С3-6гетероцикліл-С(=О)-С1-4алкіл, феніл, С3-6циклоалкіл, С3-6гетероцикліл або C3-6гетероцикліл-С(=О)- у R1, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NR5R6; R2 вибрана з групи, яку складають C 1-6алкіл, С3-6циклоалкіл, R5R6N-, С3-6циклоалкіл-С 1-4алкіл, С3-6гетероциклоалкіл-С1-4алкіл, С3-6гетероциклоалкіл, С3-6гетероарил і феніл, де зазначені C1-6алкіл, С3-6циклоалкіл, С3-6циклоалкілС1-4алкіл, С3-6гетероциклоалкіл-С1-4алкіл, C3-6гетероциклоалкіл, С3-5гетероарил і феніл у R2, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і аміно; R5 і R6 незалежно вибрані з -H, C 1-6алкілу і С2-6алкенілу; і R3 і R4 незалежно вибрані з -OH, аміно, C1-6алкілу і C1-6алкокси; або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють частину 5- або 6-членного кільця, причому зазначене кільце, як варіант, заміщене групою, вибраною з гідрокси, метокси, етокси, метилу і етилу. Зокрема, сполуками винаходу є сполуки формули І, де Z є O=; R1 вибрана з циклогексилметилу, циклопентилметилу, циклобутилметилу, циклопропілметилу, 17 83832 етилу, пропілу, адамантилу, адамантилметилу, алілу, ізопентилу, бензилу, метоксиетилу, тетрагідропіранілметилу, те трагідрофуранілметилу, циклогексилокси, циклогексиламіно, диметиламіноетилу, 4-піридилметилу, 2-піридилметилу, 1піролілетилу, 1-морфоліноетилу, 4,4дифлуорциклогексилметилу, циклогексилметилу, 2-піролідилметилу, N-метил-2-піролідилметилу, 2піперидилметилу, N-метил-2-піперидилметилу, 3тієнілметилу, (2-нітротіофен-5-іл)-метилу, (1метил-1Н-імідазол-2-іл)метилу, (5(ацетоксиметил)-2-фурил)метилу, (2,3-дигідро-1Нізоіндол-1-іл)метилу і 5-(2-метилтіазоліл); R2 вибрана з t-бутилу, n-бутилу, 2-метил-2бутилу, циклогексилу, циклогексилметилу, nпентилу, ізопентилу, трифлуорметилу, 1,1дифлуоретилу, N-піперидилу, диметиламіну, фенілу, піридилу, тетрагідрофуранілу, тетрагідропіранілу, N-морфолінілу і 2-метокси-2-пропілу; і R3 і R4 незалежно вибрані з метилу, етилу, гідрокси, метокси і етокси або R3 і R4 разом з нітрогеном, до якого вони приєднані утворюють частину 5- або 6-членного кільця, як варіант, заміщеного групою, вибраною з гідрокси, метокси, етокси, метилу і етилу. Більш конкретно, сполуками винаходу є сполуки формули І, де Z є O=; R1 вибрана з циклогексилметилу, циклопентилметилу, циклобутилметилу, циклопропілметилу, етилу, пропілу, адамантилу, адамантилметилу, алілу, ізопентилу, бензилу, метоксиетилу, тетрагідропіранілметилу, те трагідрофуранілметилу, циклогексилокси, циклогексиламіну, диметиламіноетилу, 4-піридилметилу, 2-піридилметилу, 1піролілетилу, 1-морфоліноетилу, 4,4дифлуорциклогексилметилу, циклогексилметилу, 2-піролідилметилу, N-метил-2-піролідилметилу, 2піперидилметилу, N-метил-2-піперидилметилу, 3тієнілметилу, (2-нітротіофен-5-іл)-метилу, (1метил-1Н-імідазол-2-іл)метилу, (5(ацетоксиметил)-2-фурил)метилу, (2,3-дигідро-1Нізоіндол-1-іл)метилу і 5-(2-метилтіазоліл); R2 вибрана з t-бутилу, n-бутилу, 2-метил-2бутилу, циклогексилу, циклогексилметилу, nпентилу, ізопентилу, трифлуорметилу, 1,1дифлуоретилу, N-піперидилу, диметиламіну, фенілу, піридилу, тетрагідрофуранілу, тетрагідропіранілу, N-морфолінілу і 2-метокси-2-пропілу; і R3 і R4 незалежно вибрані з метилу, етилу, гідрокси, метокси і етокси або R3 і R4 разом з нітрогеном, до якого вони приєднані, утворюють групу, вибрану з ізоксазолідин-2-ілу, 4гідроксиізоксазолідин-2-іл, 4-гідрокси-4-метилізоксазолідин-2-ілу і N-морфолінілу Якщо сполуки винаходу містять один або більше хіральних центрів, сполуки винаходу можуть існувати і бути ізольовані як енантіомерні або діастереомерні форми, або як рацемічні суміші. Винахід включає будь-які можливі енантіомери, діастереомери, рацемати сполуки формули І або їх суміші. Оптично активні форми сполуки винаходу можуть бути приготовлені, наприклад, хіральною хроматографічною сепарацією рацематів, синтезом з оптично активних вихідних матеріалів або 18 асиметричним синтезом на основі процедур, описаних нижче. Деякі сполуки винаходу можуть існувати як геометричні ізомери, наприклад E- і Z-ізомери алкенів. Винахід включає будь-які геометричні ізомери сполуки формули І, а також таутомери сполуки формули І. Деякі сполуки винаходу можуть існувати у сольватовані, наприклад, гідратованій, а також у несольватовані формах. Винахід включає всі такі сольватовані форми сполуки формули І. В об'єм винаходу входять також солі сполуки формули І. Взагалі фармацевтично прийнятні солі сполук винаходу можна отримати за стандартними процедурами, наприклад, введенням достатньо основної сполуки, наприклад, алкіламіну у реакцію з придатною кислотою, наприклад, HCI або оцтовою кислотою, з отриманням фізіологічно прийнятного аніону. Може виявитись можливим отримати сіль відповідного лужного металу (наприклад, натрію, калію або літію) або лужно-земельного металу (наприклад, кальцію), обробляючи сполуку винаходу, що має належний кислотний протон, наприклад, карбонову кислоту або фенол, одним еквівалентом гідроксиду лужного або лужноземельного металу, або алкоксидом (наприклад, етоксидом або метоксидом), або основним органічним аміном (наприклад, холіном або меглуміном) у водному середовищі, з подальшим очищенням звичайними методами. В одному з втілень, сполуку формули І можна перетворювати у її фармацевтично прийнятну сіль або сольват, зокрема, у кислотоадитивну сіль, наприклад, гідрохлорид, гідробромід, фосфат, ацетат, фумарат, малеат, тартрат, цитрат, метансульфонат або р-толуолсульфонат. Було виявлено, що сполуки винаходу є активними як фармацевтичні засоби, зокрема, як модулятори або ліганди, наприклад, агоністи, часткові агоністи, інверсні агоністи або антагоністи рецепторів CB1. Зокрема, сполуки винаходу виявляють селективну активність як агоністи рецепторів CB1 і можуть бути використані у терапії, наприклад, для полегшення різних болісних станів, зокрема, хронічного болю, нейропатичного болю, гострого болю, ракового болю, болю, викликаного ревматоїдним артритом, мігрені, внутрішнього болю тощо, причому цей перелік не є вичерпним. Крім того, сполуки винаходу можуть бути використані у випадках інших хворобливих станів, пов'язаних з дисфункцією рецептора CB1. Сполуки винаходу можуть бути використані у лікуванні раку, множинного склерозу, хвороби Паркінсона, хореї Хантингтона, хвороби Альцгеймера, тривожних розладів, шлунково-кишкових розладів і серцевосудинних розладів. Сполук винаходу можуть бути використані як імуномодулятори, зокрема при аутоімунних хворобах, наприклад, артриті, трансплантації шкіри і органів і для хірургічних потреб, при хворобах колагену, різних алергіях, як антипухлинний агент і антивірусний агент. Сполуки винаходу можуть бути використані у хворобливих станах, пов'язаних з дегенерацією або дисфункцією рецептора канабіноїду. Це може 19 83832 викликати застосування ізотопікальної версії сполуки винаходу для діагностики і застосуваннях, пов'язаних з одержанням зображень, наприклад, у позитроно-емісійній томографи. Сполуки винаходу можуть бути використані для лікування діареї, депресії, тривожності і стресових розладів, наприклад, посттравматичного стресового розладу, панічного стану, загальної тривожності, соціальної фобії і нав'язливих компульсивних розладів, нетримання сечі, передчасної еякуляції, різних психічних захворювань, кашлю, набряку легенів, різних шлунково-кишкових розладів, наприклад, запору, функціональних шлунковокишкових розладів, наприклад, синдрому подразнення кишечнику і функціональної диспепсії, хвороби Паркінсона і інших моторних розладів, травм мозку, інсульту, кардіозахисту після інфаркту міокарду, травм спини і залежностей, включаючи, залежність від спирту, нікотину, опіоїду тощо і інші зловживання, розладів симпатетичної нервової системи, наприклад, гіпертонії. Сполуки винаходу можуть бути використані як анальгетики при загальній анестезії і для нагляду при анестезії. Для досягнення балансу дій, необхідного для підтримання анестетичного стану (наприклад, амнезії, аналгезії, релаксації м'язів і заспокоєння) часто використовують комбінації агентів з різними властивостями. У таких комбінаціях можуть бути використані інгаляційні анестетики, гіпнотики, анксіотики, нейром'язові блокери і опіоїди. Винахід також включає використання будь-якої сполуки формули І у ви готовленні медикаменту для лікування будь-якого з зазначених вище станів. Ще одним аспектом винаходу є метод лікування будь-якого з зазначених вище станів, який включає введення пацієнту, що потребує такого лікування, ефективної кількості сполуки формули І. Отже, винахід стосується сполуки формули І або її фармацевтично прийнятної солі, або сольвату, визначених вище і призначених для застосування у терапії. Винахід також включає застосування сполуки формули І, або її фармацевтично прийнятної солі або сольвату, визначених вище, у виго товленні медикаменту для використання у терапії. Тут термін "терапія" включає також "профілактику", якщо не зазначено інше. Термін "терапевтичний" і "терапевтично" інтерпретуються відповідно. Термін "терапія", згідно з винаходом, включає введення пацієнту е фективної кількості сполуки винаходу для полегшення загрозливого хворобливого стану, гострого або хронічного або поворотного стану. Це визначення також включає профілактичні терапії для відвернення поворотних станів і продовження терапії для хронічних розладів. Сполуки винаходу можуть бути використані у терапії, зокрема, у терапії різних болісних станів, зокрема, хронічного болю, нейропатичного болю, гострого болю, ракового болю, болю у спині і внутрішнього болю. При лікуванні теплокровної тварини, наприклад, людини, сполуку винаходу можна вводити у формі звичайної фармацевтичної композиції будь 20 яким шляхом, а саме, перорально, внутрішньом'я зово, підшкірно, локально, через ніс, внутрішньочеревно, інтраторакально, внутрішньовенно, епідурально, інтратекапьно, інтрацеребровентрикулярно і ін'єкцією у суглоби. В одному з втілень винаходу, способом введення може бути пероральний, внутрішньовенний або внутрішньом'язовий. Дозування залежить від способу введення, важкості хвороби, віку і маси пацієнта і інших факторів, які беруться до уваги лікарем при визначенні ліків і доз для конкретного пацієнта. При приготуванні фармацевтичної композиції з сполуками винаходу інертними фармацевтично прийнятними носіями можуть бути як тверді, так і рідкі речовини. Тверді рецептури включають порошки, таблетки, гранули, капсули, каше і супозиторії. Твердим носієм можуть бути одна або більше речовин, які можуть також слугувати розріджувачами, смаковими агентами, солюбілізаторами, змащувачами, суспендуючими агентами, зв'язуючими, або дезінтеграторами таблетки; вони можуть бути також інкапсуляційним матеріалом. Порошковим носієм є тонкоподрібнена тверда речовина, яку змішують з тонкоподрібненою сполукою винаходу або активним компонентом. У таблетках активний компонент знаходиться у суміші з носієм, який має необхідні зв'язувальні якості, у належних пропорціях і у компактній формі бажаного розміру. Для приготування супозиторної композиції легкоплавкий віск, наприклад, суміш гліцеридів жирних кислот і масла какао спочатку розплавляють і диспергують у ній активний інгредієнт з перемішуванням. Розплавлену гомогенну суміш потім вливають у форми належного розміру і залишають охолонути і затвердіти. Придатними носіями є карбонат магнію, стеарат магнію, тальк, лактоза, цукор, пектин, декстрин, крохмаль, трагакант, метилцелюлоза, натрійкарбоксиметилцелюлоза, легкоплавкий віск, масло какао тощо. Термін "композиція" включає також рецептури активного компонента з інкапсуляційним матеріалом як носієм, який утворює капсулу, яка містить активний компонент (з іншим носієм або без нього). Це стосується також каше. Таблетки, порошки, каше і капсули можуть бути використані як тверді дозовані форми, придатні для перорального введення. Рідкі форми композицій включають розчини, суспензії і емульсії. Наприклад, стерильна вода або водний розчин пропіленгліколю і активної сполуки може бути рідким препаратом, придатним для парентерального введення. Рідкі композиції можуть мати форму розчину у воднополіетиленгліколевому розчині. Водні розчини для перорального введення можуть бути приготовлені розчиненням активного компонента у воді з доданням придатних забарвлювачів, смакових агентів, стабілізаторів і загущувачів. Водні суспензії для перорального введення можуть бути приготовлені диспергуванням тонкоподрібненого активного компонента у воді разом з 21 83832 в'язким матеріалом, наприклад, природною або синтетичною гумою, смолами, метилцелюлозою, натрійкарбоксиметилцелюлозою і іншими відомими фармацевтам суспендуючими агентами. Залежно від способу введення пацієнту фармацевтична композиція включає 0,05%-99% (за масою), бажано, 0,10%-50% (за масою) сполуки винаходу відносно повної маси композиції. Практична терапевтично ефективна кількість згідно з винаходом може бути визначена фахівцем за відомими критеріями, включаючи вік, масу і реакцію пацієнта, і інтерпретована з увагою до хвороби, що потребує лікування або профілактики. Винахід включає використання будь-якої сполуки формули І, визначеної вище, для виготовлення медикаменту. Винахід включає також використання будь-якої сполуки формули І, визначеної вище, для виготовлення медикаменту проти болю. Крім того, винахід включає використання будьякої сполуки формули І у виготовленні медикаменту для терапії різних болісних станів, включаючи, але без обмеження, хронічний біль, нейропатичний біль, гострий біль, раковий біль, біль у спині і внутрішній біль. Винахід включає також спосіб лікування пацієнта, що страждає від будь-якого з розглянутих вище станів, який включає введення ефективної кількості сполуки формули І пацієнту, що потребує такого лікування. Крім того, винахід включає фармацевтичну композицію, що містить сполуку формули І або її фармацевтично прийнятну сіль разом з фармацевтично прийнятним носієм. Зокрема, винахід включає фармацевтичну композицію, що містить сполуку формули І або її фармацевтично прийнятну сіль разом з фармацевтично прийнятним носієм і, зокрема, призначена для терапії болю. Винахід включає також фармацевтичну композицію, що містить сполуку формули І або її фармацевтично прийнятну сіль разом з фармацевтично прийнятним носієм і призначена для використання у будь-яких станах, зазначених вище. Згідно з ще одним аспектом, винахід включає спосіб приготування сполук винаходу. В одному з втілень винахід включає процес приготування сполуки формули II, який введення сполуки формули III, у реакцію з сполукою R3NHOR8 для отримання сполуки формули Il 22 де X вибрана з Cl, Br, І і OH; R1 вибрана з C1-10алкілу, С2-10алкенілу, С2-10алкінілу, R5R6C1-6алкілу, R5O-C1-6алкілу, 5 6 5 6 R C(=O)N(-R )-C1-6алкілу, R R NS(=O)2-C1-6алкілу, R5CS(=O)2N(-R6)-C1-6алкілу, R5R6NC(=O)N(-R 7)С1-6алкілу, R5R6NS(=O)2N(R7)-C1-6алкілу, C6-10арилС1-6алкілу, С6-10арил-С(=О)-С1-6алкілу, С3-10циклоалкіл-С 1-6алкілу, С4-8циклоалкенілС1-6алкілу, С3-6гетероцикліл-С1-6алкілу, C3-6гетероцикліл-С(=O)-С1-6алкілу, C1-10гідрокарбіламіну, R5R6N-, R 5O-, R5C(=O)N(R6)-, RSR6NS(=O)2-, R5CS(=O)2N(-R6)-, R5R6NC(=O)N(-R 7)-, R5R6NS(O)2N(R7)-, C6-10арилу, C6-10арил-С(=O)-, С3-10циклоалкілу, С4-8циклоалкенілу, С3-6гетероциклілу і С3-6гетероциклiл-С(=О)-; де зазначені C1-10алкіл, С2-10алкеніл, С2-10алкініл, C6-10арил-С 1-6алкіл, С6-10арил-С(=О)-С1-6алкіл, С3-10циклоалкілС1-6алкіл, С4-8циклоалкеніл-С1-6алкіл, С3-6гетероцикліл-С1-6алкіл, С3-6гетероцикліл-С(=О)С1-6алкіл, C1-10гідрокарбіламіно, C6-10арил, C6-10арил-С(=О)-, С3-10циклоалкіл, C4-8ациклоалкеніл, С3-6гетероцикліл або С3-6гетерофікліл-С(=О)- у R1 , як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і -NRSR6; R2 вибрана з групи, яку складають C1-10алкіл, С2-10алкеніл, С2-10алкініл, С3-8циклоалкіл, С3-8циклоалкіл-С 1-6алкіл, С4-8циклоалкенілС1-6алкіл, С3-6гетероциклоалкіл-С1-6алкіл, C4-8циклоалкеніл, R5R6N-, С3-5гетероарил, C6-10арил і С 3-6гетероциклоалкіл, де зазначені C1-10алкіл, С2-10алкеніл, С2-10алкініл, С3-8циклоалкіл, С3-8циклоалкіл-С 1-6алкіл, С4-8циклоалкенілС1-6алкіл, С3-6гетероциклоалкіл-С1-6алкіл, С4-8циклоалкеніл, С3-5гетероарил, C6-10арил або C3-6гетероциклоалкіл у R2, як варіант, заміщені однією або більше групами, вибраними з карбокси, галогену, ціано, нітро, метокси, етокси, метилу, етилу, гідрокси і аміно; де R5, R6 і R7 незалежно вибрані з -H, C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6групи, яка разом з іншими дивалентними R5, R6 або R7 утворює частину кільця; R3 вибрана C1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6групи, яка разом з дивалентною R8 утворює частину кільця; R8 вибрана з -H, C 1-6алкілу, С2-6алкенілу, С2-6алкінілу і дивалентної C1-6групи, яка разом з дивалентною R8 утворює частину кільця. Зокрема, винахід включає спосіб приготування сполуки формули II, в якій R1 вибрана з циклогексилметилу, циклопентилметилу, циклобутилметилу, циклопропілметилу, етилу, пропілу, адамантилу, адамантилметилу, алілу, ізопентилу, бензилу, метоксиетилу, тетрагідропіранілметилу, тетрагід 23 рофуранілметилу, циклогексилокси, циклогексиламіну, диметиламіноетилу, 4-піридилметилу, 2піридилметилу, 1-піролілетилу, 1-морфоліноетипу, 4,4-дифлуорциклогексилметилу, циклогексилметилу, 2-піролідилметилу, N-метил-2піролідилметилу, 2-піперидилметилу, N-метил-2піперидилметилу, 3-тієнілметилу, (2-нітротіофен-5іл)-метилу, (1-метил-1Н-імідазол-2-іл)метилу, (5(ацетоксиметил)-2-фурил)-метил), (2,3-дигідро-1Нізоіндол-1-іл)метил, і 5-(2-метилтіазоліл); 83832 24 R2 вибрана з t-бутилу, n-бутилу, 2-метил-2бутилу, циклогексилу, циклогексилметил, nпентилу, ізопентилу, трифлуорметилу, 1,1дифлуоретилу, N-піперидилу, диметиламіну, фенілу, піридилу, тетрагідрофуранілу, тетрагідропіранілу, 2-метокси-2-пропілу і N-морфолінілу; і R3 і R8 є незалежно C1-6алкілом. Сполуки винаходу можуть бути приготовлені згідно з Схемами 1-3 синтезу, використовуючи один або більше методів, описаних вище. 25 83832 26 27 83832 Біологічна оцінка Зв'язування рецептора hCB1 i hCB2 Мембрани рецептора CB1 людини від Receptor Biology (hCB1) або рецептора CB2 людини від BioSignal (hCB2) розморожували при 37°C, тричі проводили через голку калібру 25 з тупим кінцем, розбавили у канабіноїдному зв'язувальному буфері (50мМ Tris, 2,5мМ EDTA, 5мМ MgCI2 і 0,5мг/мл BSA без жирних кислот, рН 7,4) і аліквоти з відповідною кількістю протеїну розподілили у 96комірковому планшеті. IC50 сполуки винаходу для hCB1 і CB2 оцінювали на 10-точкових кривих залежності реакції від дози з використанням 3НСР55,940 при 20000-25000млн на комірку (0,170,21нМ) у кінцевому об'ємі 300мкл. Повне і неспецифічне зв'язування визначали у присутності і за відсутності 0,2мкМ HU210, відповідно. Планшети центрифугували і інкубували 60хвил. при кімнатній температурі, фільтрували через Unifilters GF/B (просочений 0,1% поліетиленіміну) з Tomtec або Packard harvester, використовуючи 3мл промивального буфера (50мМ Tris, 5мМ MgCI2, 0,5мг BSA, рН 7,0). Фільтри сушили 1год. при 55°C. Радіоактивність (імп./хвил.) відраховували у TopCount (Packard) після додання 65мкл/комірка сцинтиляційної рідини MS-20. Зв'язування GTPgS для hCB1 і hCB2 Мембрани рецептора CB1 людини від Receptor Biology (hCB2) або рецептора CB2 людини від BioSignal (hCB2) розморожували при 37°С, тричі проводили через голку калібру 25 з тупим кінцем і розбавляли у зв'язувальному буфері GTPgS (50мМ Hepes, 20мМ NaOH, 100мМ NaCI, 1мМ EDTA, 5мм MgCI2, рН 7,4, 0,1% BSA). The EC50 і Emax сполуки винаходу оцінювали на 10-точкових кривих залежності реакції для відповідної кількості протеїну мембрани при 100000-130000 1/млн GTPg35S на комірку (0,11-0,14нМ) в об'ємі 300мкл. Базове і максимальне стимульоване зв'язування визначали у присутності і за відсутності 1мкМ (hCB2) або 10мкМ (hCB1) Win 55,212-2, відповідно. Мембрани попередньо інкубували протягом 5хвил. з 56,25мкМ (hCB2) або 112,5мкМ (hCB1) GDP і потім розподіляли по планшетах (кінцеві дані - 15мкМ (hCB2) або 30мкМ (hCB1) GDP). Планшети центрифугували і інкубували 60хвил. при кімнатній температурі, фільтрували через Unifilters GF/B (просочений водою) з Tomtec або Packard harvester, використовуючи 3мл промивального буфера (50мМ Tris, 5мМ MgCI2, 0,5мг BSA, рН 7,0). Фільтри сушили 1год. при 55°С. Радіоактивність (імп./хвил.) відраховували у TopCount (Packard) після додання 65мкл/комірка сцинтиляційної рідини MS-20. Зворотний аналіз антагоніста проводили подібним чином, але а) криву залежності реакції від дози будували для постійної концентрації антагоніста, або (b) криву залежності реакції від дози будували для постійної концентрації агоніста. Базуючись на наведених аналізах, були визначені константа дисоціації (Ki) для сполуки винаходу відносно конкретного рецептора, з використанням рівняння: Ki=IC50/(1+[rad]/Kd), 28 де IC50 є концентрацією сполуки винаходу 50%-му спостереженому видаленні. [rad] - стандартна або еталонна концентрація радіоактивного ліганду на даний момент; Kd - константа дисоціації радіоактивного ліганду для даного рецептора. Описані аналізи показали значення Ki сполук винаходу відносно рецепторів CB1 людини від 36 до 5700нМ. Виміряні Ki сполук винаходу відносно рецепторів CB2 людини становили від 1,6 до 36нМ. Взагалі IC50 відносно рецептора CB1 для більшості сполук винаходу становило від 16,2 до 5655,7нМ. Приклади Винахід супроводжується наведеними далі Прикладами, якими ілюструються методи приготування, очищення, аналізу і біологічного тестування сполук винаходу і які не обмежують винаходу. Приклад 1 2-трет-бутил-N,N-дiетил-1-{[(2R)-1метилпіперидин-2-іл]метил}-1Н-бензімідазол-5карбоксамід Операція А. 2-трет-бутил-N,N-діетил-1-{[(2R)1-метилпіперидин-2-іл]-метил}-1Н-бензімідазол-5карбоксамід Трет-бутил-(2R)-2-[({2-аміно-4[(діетиламіно)карбоніл]феніл}амі-но)метил]піперидин-1-карбоксилат (75 rа г, 0,185ммоль) (див. опер В, C і D) розчиняють у 3мл DCE з TEA (0,058мл, 0,277ммоль). Додають краплями триметилацетилхлорид (0,025мл, 0,204ммоль) і розчин перемішують при кімнатній температурі 1год. Додають льодяну оцтову кислоту (1мл) і декілька крапель концентрованої HCI і розчин перемішують при 75°C 24год. Розчинник концентрують, залишок розчиняють у EtOAc і промивають 2М NaOH, розсолом і сушать над безводним MgSO4. Розчинник випарюють, продукт розчиняють у 5мл ТГФ з декількома краплями льодяної AcOH. Додають з надлишком 37% НСНО/воду (1мл), потім NaBH(OAc)3 (78мг, 0,370ммоль). Розчин перемішують при кімнатній температурі 30хвил., потім розбавляють EtOAc і промивають 2М NaOH, розсолом і сушать над безводним MgSO4. Розчинник випарюють, продукт очищають зворотно-фазовою ВЕРХ, використовуючи 10-50% CH3CN/H2O, і потім ліофілізу 29 83832 ють, отримуючи бажану сполуку як сіль TFA. Вихід: 42мг (46%). 1H ЯМР (400МГц, CD3OD) d 1,12 (m, 3H), 1,25 (m, 3H), 1,36 (m, 2H),1,65 (s, 9H), 1,79 (m, 2H), 1,87 (m, 1Н), 3,15 (s, 3H), 3,31 (m, 3H), 3,57 (m, 3H), 4,01 (m, 1Н), 4,85 (ra, 1H), 5,18 (m, 1Н), 7,50 (dd, J=1,56, 8,59Гц, 1Н), 7,72 (d, J=0,98Гц, 1Н), 7,93 (d, J=8,59Гц, 1Н); MS (ESI) (M+H)+ 385,3; Аналіз: обчислено для C23H36N40+3,0TFA: C, 47,94; H, 5,41; N, 7,71. Одержано: C, 48,06; H, 5,23;N, 7,85. Операція В. N,N-діетил-4-флуор-3нітробензамід 4-флуор-3-нітробензойну кислоту (5,0г, 27,0ммоль) витримують під зворотним холодильником у 2:1 суміші CH2CI2/SOCI2 (150мл) протягом ночі. Розчинник концентрують і залишок розчиняють у CH2CI2 (50мл). Розчин діетиламіну (3,35мл, 32,4ммоль) і триетиламіну (TEA) (7,5мл, 54ммоль) у CH2CI2 (50мл) додають краплями з перемішуванням до холодного розчину (0°C) кислотного хлориду. Розчин перемішують при кімнатній температурі 3год. Розчин промивають 5%-м розчином KHSO4, насиченим розчином NaHCO3, розсолом і сушать над безводним MgSO4. Сирий продукт очищають флеш-хроматографією використовуючи 1:1/гексани:EtOAc на силікагелі. Вихід: 5,39г (83%); 1 ЯМР (400МГц, ХЛОРОФОРМ-D) d 1,19 (b, 6H), 3,24 (b, 2H), 3,52 (b, 2Н), 7,33 (dd, J=10,45, 8,50Гц, 1Н), 7,66 (m, 1H), 8,09 (dd, J=7,03, 2,15Гц, 1Н). Операція C. Трет-бутил-(2R)-2-[({4[dіетиламіно)карбоніл]-2-нітрофеніл}аміно)метил]піперидин-1-карбоксилат 30 4,62 (m, 1H), 7,00 (m, J=8,79Гц, 1H), 7,57 (dd, J=8,79, 1,76Гц, 1H), 8,28(d, J=1,76Гц, 2H). Операція D. Трет-бутил-(2R)-2-[({2-аміно-4[(діетиламіно)карбоніл]феніл}аміно)метил]піперидин-1-карбоксилат Трет-бутил-(2R)-2-[({4-[(діетиламіно)карбоніл]2-нітрофеніл}аміно)метил]піперидин-1карбоксилат (380мг, 0,875ммоль) розчиняють у 35мл EtOAc з каталітичною кількістю 10% Pd/C. Розчин струшують у гідрогенаційному апараті Парра під H2 (40фунт/кв. дюйм (2,8ат)) при кімнатній температурі протягом ночі. Розчин фільтрують через целіт і розчинник концентрують. Продукт використовують у наступній операції без очищення. Вихід: 355мг (99%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D) d 1,17 (t, J=6,74Гц, 6Н), 1,46 (s,9H), 1,55 (d, J=1,72Гц, 1H), 1,65 (d, J=10,35Гц, 2H), 1,73 (m, 2H), 2,81 (t, J=12,50Гц, 1H), 3,09 (d, J=9,76Гц, 1H), 3,31 (m, 2H), 3,42 (m, 4H), 3,52 (m, 2H), 4,02 (m, 1H), 4,59 (m, 1H), 6,58 (d, J=8,01Гц, 1Н), 6,78 (d, J=1,56Гц, 1H), 6,86 (m, 1H), 7,26 (s, 1H). Приклад 2 2-трет-бутил-1-(циклогексилиетил-N,N-діетил1Н-бензімідазол-5-карбоксамід Операція А. 1-трет-бутил-1циклогексилметилJ-N,N-діетил-1Н-бензімідазол-Sкарбоксамід N,N-діетил-4-флуор-3-нітробензамід (210мг, 0,874ммоль) і трет-бутил-(2R)-2(амінометил)піперидин-1-карбоксилат (245мг, 1,14ммоль) перемішують у 15мл EtOH з TEA (0,185мл, 1,3 1ммоль) при 75°С протягом ночі. Розчинник концентрують, залишок розчиняють у EtOAc і промивають 5%-м розчином KHSO4, насиченим розчином NaHCO3, розсолом і сушать над безводним MgSO4. Сирий продукт очищають флеш-хроматографією використовуючи 1:1/гексани:EtOAc як елюент на силікагелі і отримують бажану сполуку. Вихід: 380мг (99%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D) d 1,22 (m, 6H), 1,47 (s, 9H), 1,55 (m, 1Н), 1,63 (m, 1H), 1,71 (d, J=12,89Гц, 4Н), 2,79 (m, 1H), 3,36 (dd, J=12,89, 6,25Гц, 1H), 3,43 (m, 4H), 3,61 (m, 1H), 4,07 (m, 1H), 3-аміно-4-[(циклогексилметил)амінo]-N,Nдіетилбензамід (124мг, 0,409ммоль) (див. опер. В і C) розчиняють у 3мл DCE з TEA (0,085мл, 0,614ммоль). Додають краплями триметилацетилхлорид (0,055мл, 0,450ммоль) і розчин перемішують при кімнатній температурі 1год. Додають льодяну AcOH (1мл) і декілька крапель концентрованої HCI і розчин перемішують при 75°С 48год. Розчинник концентрують, залишок розчиняють у EtOAc і промивають 2М водним 31 83832 NaOH, розсолом і сушать над безводним MgSO4. Розчинник випарюють. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 20-80% CH3CN/H2O, і потім ліофілізують, отримуючи бажану сполуку як сіль TFA. Ви хід: 64мг (32%). 1Н ЯМР (400МГц, CD3OD) d 1,12 (m, 3H), 1,23 (m, 7H), 1,67 (m, 14Н), 1,75 (m, 1H), 2,11 (m, 1Н), 3,28 (m, 2Н), 3,56 (m, 2Н), 4,48 (d, J=7,42Гц, 2Н), 7,58 (dd, J=1,46, 8,69Гц, 1Н), 7,73 (s, 1H), 7,99 (d, J=8,79Гц, 1Н); MS (ESI) (M+H)+ 370,2. Аналіз: обчислено для C23H35N3 O+2,1TFA+0,9H2O: C, 52,25; H, 6,27; N, 6,72. Отримано: C, 52,31; H, 6,24; N, 6,69. Операція В. 4-[(циклогексилметил)аміно]-N,Nдіетил-3-нітробензамід Згідно з процедурою Прикладу 1, опер. C, використовують N,N-діетил-4-флуор-3-нітробензамід (105мг, 0,437ммоль) і циклогексилметиламін (0,090мл, 0,656ммоль) у 5мл EtOH з TEA (0,135мл, 0,655ммоль). Продукт використовують у наступній операції після промивання. Вихід: 144мг (99%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D) d 1,06 (m, 2H), 1,22 (t, J=7,13Гц, 7Н), 1,30 (m, 2H), 1,71 (m, 2H), 1,79 (m, 2H), 1,86 (d, J=1,91Гц, 2H), 3,18 (m, 2H), 3,45 (m, 4Н), 6,88 (d, J=8,79Гц, 1Н), 7,55 (dd, J=8,88, 2,05Гц, 1H), 8,28 (d, J=1,95Гц, 1H), 8,31 (m, 1H). Операція С. 3-аміно-4-[(циклогексилметил)аміно]-N,N-діетилбензамід Згідно з процедурою Прикладу 1, опер. D, використовують 4-[(циклогексилметил)аміно]-N,Nдіетил-3-нітробензамід (140мг, 0,420ммоль) і каталітичну кількість 10% Pd/C у 15мл EtOAc. Розчин фільтрують через целіт і використовують у наступній операції. Вихід: 125мг (99%). MS (ESI) (М+Н)+: 304,2. Приклад 3 2-трет-бутил-1-(циклогексилметил)-N-метоксиN-метил-1Нr-бензімідазол-5-карбоксамід 32 Операція А. 2-трет-бутил-1(циклогексилметил)-N-метокси-N-метил-1Нбензімідазол-5-карбоксамід 2-трет-бутил-1-(циклогексилметил)-N-метоксиN-метил-1Н-бензімідазол-5-карбонову кислоту (див. опер. B-F) (58мг, 0,184ммоль), N,Oдиметилгідроксиламінгідрохлорид (25мг, 0,276ммоль) і HATU (77мг, 0,202ммоль) перемішують у 2мл ДМФ з DIPEA (0,080мл, 0,460ммоль) при кімнатній температурі протягом 3год. Розчинник концентрують. Залишок розчиняють у EtOAc і промивають насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4 . Розчинник випарюють і продукт очищають зворотно-фазовою ВЕРХ, використовуючи 20-80% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполук у як сіль TFA. Ви хід 29мг (33%). 1H ЯМР (400МГц, МЕТАНОЛ-D4) d 1,23 (m, 5H), 1,62 (s, 2H),1,65 (s, 9H), 1,75 (m, 2Н), 2,11 (m, 1Н), 3,38 (s, 3H), 3,56 (s, 3H), 4,45 (d, J=7,62Гц, 2Н), 7,82 (dd, J=8,69, 1,46Гц, 1H), 7,91 (m, 1H), 8,03 (d, J=0,78Гц, 1H), MS (ESI) (М+Н)+358,2; Аналіз: обчислено для C21H31N3 O2+1,2TFA+0,3H2 O: С, 56,24; H, 6,62; N, 8,41. Отримано: С, 56,28; H, 6,51; N, 8,48. Операція В. Метил 4-флуор-3-нітробензоат 4-флуор-3-нітробензойну кислоту розчиняють у 20мл суміші 5:1/толуол: MeOH при 0°C під нітрогеном. Краплями додають триметилсилілдіазометан (2М у гексанах, 1,6мл, 3,24ммоль) і розчин перемішують при кімнатній температурі 30хвил. Розчинник концентрують. Продукт очищають флеш-хроматографією на силікагелі з 4:1/гексани:EtOAc як елюентом і отримують бажану сполуку. Вихід 494мг (92%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D) d 3,98 (s, 3H) 7,39 (dd, J=10,06, 8,49Гц, 1H), 8,33 (ddd, J=8,69, 4,20, 2,15Гц, 1H), 8,75 (dd, J=7,23, 2,15Гц, 1H). Операція С. Метил 4[(циклогексилметил)аміно]-3-нітробензоат Згідно з процедурою Прикладу 1, опер. C, використовують метил-4-флуор-3-нітробензоат 33 83832 (225мг, 1,13ммоль) і циклогексилметиламін (0,175мл, 1,36ммоль) у 5мл EtOH з TEA (0,235мл, 1,70ммоль). Продукт використовують у наступній операції після промивання. Вихід: 329мг (99%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D) d 1,06 (m 2H), 1,26 (m, 3H), 1,72 (m, 3H), 1,72 (m, 2H), 1,84 (m, 1H), 1,87 (m, 1H), 3,20 (dd, J=6,64, 5,47Гц, 2Н), 3,90(s, 3H), 6,86 (d, J=8,98Гц, 1Н), 8,04 (ddd, J=9,03, 2,10, 0,78Гц, 1H), 8,47 (s, 1H), 8,89 (d, J=1,95Гц, 1H). Операція D. Метил-3-аміно-4[(циклогексилметил)аміно]бензоат Згідно з процедурою Прикладу 1, опер. D, використовують метил-4-[(циклогексилметил)аміно]3-нітробензоат (325мг, 1,11ммоль) у 25мл EtOAc. Суміш фільтрують через целіт і використовують в операції А. Вихід: 285мг (98%). MS (ESI) (М+Н)+: 263,0. Операція E. Метил-2-трет-бутил-1(циклогексилметил)-1Н-бензімідазол-5карбоксилат 34 Метил-2-трет-бутил-1-(циклогексилметил)-1Нбензімідазол-5-карбоксилат (165мг, 0,502ммоль) розчиняють у 10мл EtOH з 2мл 1M LiOH. Розчин витримують під зворотним холодильником протягом 3год. Розчин охолоджують до кімнатної температури і розчинник концентрують. Розчин нейтралізують 1M HCI і екстрагують ДХМ і EtOAc. Об'єднані органічні фази промивають розсолом і сушать над безводн. MgSO4. Органічні фази об'єднують і концентрують, отримуючи сиру бажану сполуку, яку використовують в операції А. Вихід: 140мг (87%). MS (ESI) (М+Н)+ 315,0. Приклад 4 1-(циклогексилметил)-2-(1,1-диметилпропіл)N-метокси-N-метил-1Н-бензімідазол-5-карбоксамід Операція А. 1-(циклогексилметил)-2-(1,1диметилпропіл)-N-метокси-N-метил-1Hбензімідазол-5-карбоксамід Метил 3-аміно-4[(циклогексилметил)аміно]бензоат (285мг, 1,09ммоль) розчиняють у 10мл ДХМ з D MAP (33мг, 0,272ммоль). Краплями додають триметилацетилхлорид (0,145мл, 1,20ммоль) і розчин перемішують при кімнатній температурі 2год. Розчинник концентрують, залишок розчиняють у 15мл льодяної AcOH і перемішують при 100°C 24год. Розчинник концентрують, залишок розчиняють у EtOAc і розчин промивають насиченим розчином NaHCO3, розсолом і сушать над безводним MgSO4. Продукт очищають флеш-хроматографією, використовуючи 7:3/гексани:EtOAc як елюент на силікагелі. Вихід: 170мг (47%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D) d 1,10 (m, 2H), 1,16 (m, 2H), 1,57 (s, 9H), 1,61 (m, 1H), 1,62 (m, 2H), 1,69 (m, 1H), 1,73 (m, 2H), 2,03 (m, 1H), 3,93 (s, 3H), 4,15 (d, J=7,62Гц, 2Н), 7,34 (d, J=8,59Гц, 1Н), 7,94 (dd, J=8,59, 1,56Гц, 1H), 8,47 (d, J=0,98Гц, 1H). Операція F. 2-трет-бутил-1(циклогексилметил)-1Н-бензімідазол-5-карбонова кислота Згідно з процедурою Прикладу 3, опер. А, використовують О,Nдиметилгідроксиламінгідрохлорид (36,6мг, 0,38ммоль), діізопропілетиламін (144 uL, 106,6мг, 0,83ммоль) і додають розчин 1(циклогексилметил)-2-(1,1-диметилпропіл)-1Нбензімідазол-5-карбонової кислоти (82,1мг, 0,250ммоль) у ДМФ (5мл) (див. операції В, C, D і E) при 0°C і потім HATU (114,1мг, 0,30ммоль). Суміш перемішують протягом ночі при кімнатній температурі, додають H2O (50мл) і екстрагують EtOAc (3´50мл). Бажану сполуку очи щають зворотнофазовою ВЕРХ (колонка С-18), використовуючи 20-70% CH3CN/H2O, і отримують 107,9мг (89%) білої твердої речовини. 1H ЯМР (400МГц, CD3OD) d 0,86 (t, J=7,52Гц, 3H), 1,26 (m, 5H), 1,67 (m, 3H), 1,69 (s, 6H), 1,78 (m, 2H), 2,04 (q, J=7,49Гц, 2H), 2,13 (m, 1H), 3,41 (s, 3H), 3,59 (s, 3H), 4,51 (d, J=7,81Гц, 2H), 7,90 (dd, J=8,79, 1,37Гц, 1H), 8,01 (d, J=8,79Гц, 1H), 8,08 (d, J=0,78Гц, 1H),. MS (ESI) (M+H)+=372,07. Операція В. 4-[(циклогексилметил)аміно]-3нітробензонітрил 35 83832 Циклогексилметиламін (3,12мл, 2,72г, 24,0ммоль) додають до суспензії 4-флуор-3нітробензонітрилу (3,22г, 20,0ммоль) і карбонату натрію (4,66г, 44,0ммоль) у EtOH (60мл) при кімнатній температурі. Реакційну суміш перемішують протягом ночі і розбавляють H2O (800мл). Жовтий твердий осад збирають, отримуючи бажаний продукт (5,25г, 100%). 1H ЯМР (400МГц, CDCI3): d 1,07 (m, 2H), 1,25 (m, 3H), 1,75 (m, 6H), 3,19 (dd, J=6,64, 5,47Гц, 2Н), 6,91 (d, J=8,98Гц, 1H), 7,59 (m, 1H), 8,50 (s broad, 1H), 8,51 (d, J=2,15Гц, 1Н). Операція C. 3-аміно-4[(циклогексилметил)аміно]-бензонітрил 4-[(циклогексилметил)аміно]-3нітробензонітрил (5,25г, 20,0ммоль) гідрогенують в етилацетаті (200мл) з каталізатором 10% Pd/C (0,8г) при 20-30фунт/кв. дюйм (1,4-2,1ат) H2 в апараті Парра протягом 2год. при кімнатній температурі. Після завершення реакції суміш фільтрують через целіт. Видалення розчинника дає бажану сполуку діамін (4,33г, 94%), яку використовують у наступній операції без очищення. 1H ЯМР (400МГц, CDCI3): d 1,02 (m, 2H), 1,24 (m, 3H), 1,62 (m, 1H), 1,76 (m, 5H), 3,00 (m, 2H), 3,27 (s broad, 2H), 4,05 (s broad, 1H), 6,56 (d, J=8,20Гц, 1H), 6,93 (d, J=1,76Гц, 1H), 7,16 (dd, J=8,20, 1,95Гц, 1H). MS (ESI) (M+H)+=229,90 (M+1)+. Операція D. 1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-карбонітрил 2,2-диметил бутурилхлорид (1,37г, 10,18ммоль) додають краплями з перемішуванням до розчину 3-аміно-4-[(циклогексилметил)аміно]бензонітрилу (1,83г, 7,98ммоль) і DMAP (387,8мг, 3,17ммоль) у ДХМ (70мл) при 0°C. Розчин перемішують протягом ночі при кімнатній температурі. Після випарювання розчинника, сирий продукт отримують як сіро-білу тверду речовину (3,51г, 100%). MS (ESI) (М+Н)+=328,03. Цей сирий продукт (773,9мг, 1,76ммоль) розчиняють у 1,2-дихлоретані (5´5мл) у 5 покритих 36 Тефлоном тест-пробірках. Судини опромінюють мікрохвилями 2год. при 190°C, потім розбавляють EtOAc (200мл), промивають 2N NaOM (10мл), насиченим NaCI (2´10мл) і сушать над безводн. Na2SO4. Після фільтрування і концентрування бажану сполуку отримують як білу тверду речовину (623,1мг, 100%). MS (ESI) (М+Н)+=310,02. Операція E. 1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-карбонова кислота Суміш 1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-карбонітрилу (623,1мг, 1,76ммоль) і гідроксиду калію (620,1мг, 11,05ммоль) у 20мл EtOH-Н2О (1:1) гріють 24год. під зворотним холодильником. Після випарювання етанолу водний розчин екстрагують етером (2´50мл) і підкислюють 2N HCI до рН 5-6. Бажану сполуку отримують як сіро-білу тверду речовину (541,2мг (94%). 1H ЯМР (400МГц, CD3OD) d 0,85 (t, J=7,52Гц, 3H), 1,26 (m, 5H), 1,65 (m, 3H), 1,69 (s, 6H), 1,78 (s, 2H), 2,04 (q, J=7,52Гц, 2H), 2,12 (m, 1H), 4,50 (d, J=7,62Гц, 2H), 7,99 (m, 1H), 8,24 (m, 1H), 8,42 (d, J=0,98Гц, 1H). MS (ESI) (M+H)+=372,07. Приклад 5 1-(циклогексилметил)-2-(14-диметилпропіл)-Nморфолін-4-іл-1Н-бензімідазол-5-карбоксамід Згідно з процедурою Прикладу 3, опер А, використовують морфолін-4-амін (30,6мг, 0,30ммоль), діізопропілетиламін (69,7мкл, 51,7мг, 0,40ммоль) і розчин 1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-карбонової кислоти (65,7мг, 0,20ммоль) у ДМФ (5мл) (див. Приклад 4, опер. E) при 0°C і потім HATU (91,3мг, 0,24ммоль). Суміш перемішують протягом ночі при кімнатній температурі, додають H2O (50мл) і екстрагують EtOAc (3´50мл). Бажану сполуку очищають зворотно-фазовою ВЕРХ (колонка С-18), використовуючи 10-50% CH3CN/H2O, і отримують 79,2мг (75%) білої твердої речовини. 1H ЯМР (400МГц, CD3OD): d 0,86 (t, J=7 ,52Гц, 3H), 1,26 (m, 5H), 1,64 (m, 3H), 1,70 (s, 6H), 1,78 (m, 2H), 2,04 (q, J=7,49Гц, 2H), 2,13 (m, 1H), 2,96 (m, 4H), 3,83 (m, 4H), 4,51 (d, J=7,62Гц, 2Н), 8,03 (m, 2H), 8,22 (m, 1H). MS (ESI) (M+H)+=413,3. Аналіз: обчислено для C24H36N4 O2+1,90TFA+1,30H2O+0,30MeCN (664,96): С, 51,30; H, 6,28; N, 9,06. Отримано: С, 51,33; H, 6,21; N, 9,08. 37 83832 Приклад 6 1-(циклогексилметил)-2-(1,1-диметилпропіл)-5(морфолін-4-ілкарбоніл)-1H-бензімідазол Згідно з процедурою Прикладу 3, опер. А, використовують морфолін (26,1мг, 0,30ммоль), діізопропілетиламін (69,7мкл, 51,7мг, 0,40ммоль) і розчин 1-(циклогексилметил)-2-(1,1-диметилпропіл)1Н-бензімідазол-5-карбонової кислоти (65,7мг, 0,20ммоль) (див. Приклад 4, опер. E) у ДМФ (5мл) при 0°C і потім HATU (91,3мг, 0,24ммоль). Суміш перемішують протягом ночі при кімнатній температурі, додають H2O (50мл) і екстрагують EtOAc (3´50мл). Бажану сполуку очи щають зворотнофазовою ВЕРХ (колонка С-18), використовуючи 10-50% CH3CN/H2O, і отримують 82,1мг (80%) білої твердої речовини. 1H ЯМР (400МГц, CD3OD): d 0,86 (t, J=7,42Гц, 3H), 1,27 (m, 5H), 1,65 (m, 3H), 1,69 (s, 6H), 1,78 (m, 2H), 2,04 (q, J=7,42Гц, 2H), 2,12 (m, 1H), 3,47 (m, 2H), 3,62 (m, 2H), 3,79 (m, 4H), 4,50(d, J=7,62Гц, 2H), 7,66 (dd, J=8,69, 1,46Гц, 1H), 7,82 (d, J=0,78Гц, 1H), 8,01 (d, J=8,79Гц, 1H),. MS (ESI) (M+H)+=398,3. Аналіз: обчислено для C24H35N3 O2+1,60TFA+1,10H2O+0,30MeCN (612,14): С, 54,55; H, 6,54; N, 7,55. Отримано: С, 54,61; H3 6,53; N, 7,51. Приклад 7 1-(циклогексилметил)-5-[(2,6-диметил морфолін-4-іл)карбоніл]-2-(1,1-диметилпропіл)-1Нбензімідазол Згідно з процедурою Прикладу 3, опер. А, використовують 2,6-диметилморфолін (34,6мг, 0,30ммоль), діізопропілетиламін (69,7мкл, 51,7мг, 0,40ммоль) і розчин 1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-карбонової кислоти (66,8мг, 0,203ммоль) (див. Приклад 4, опер. E) у ДМФ (5мл) при 0°C і потім HATU (91,3мг, 0,24ммоль). Суміш перемішують протягом ночі при кімнатній температурі, додають H2O (50мл) і екстрагують EtOAc (3´50мл). Бажану сполуку очищають ВЕРХ (гекс/EtOAc 1:1 як елюент, на силікагелі), отримуючи 76,0мг (89%) білої твердої речовини. 1H ЯМР (400МГц, CD3OD): d 0,86 (t, J=7,52Гц, 3H), 1,04 (m, 3H), 1,27 (m, 8H), 1,66 (m, 2H), 1,69 (s, 6H), 1,71 (m, 1H), 1,79 (m, 2H), 2,04 (q, J=7,55Гц, 2H), 2,13 (m, 1H), 2,63 (m, 1H), 2,92 (m, 1H), 3,59 (m, 3H), 4,50(d, J=7,81Гц, 2H), 4,54 (m, 1H), 7,65 (dd, J=8,69, 1,46Гц, 1H), 7,81 (d, J=0,78Гц, 1H), 8,01 (d, J=8,59Гц, 1H), MS (ESI) (M+H)+=426,2. Аналіз: обчислено для 38 C26H39N3 O2+1,70TFA+0,20H2O (623,06): С, 56,68; H, 6,65; N, 6,74. Отримано: С, 56,68; H, 6,59; N, 6,81. Приклад 8 1-(циклогексилметил)-5-{[(2R,6S)-2,6-диметил морфолін-4-іл]карбоніл}-2-(1,1-диметилпропіл-1Нбензімідазол Згідно з процедурою Прикладу 3, опер. А, використовують (2R,6S)-2,6-диметилморфолін (34,6мг, 0,30ммоль), діізопропілетиламін (69,7мкл, 51,7мг, 0,40ммоль) і розчин 1-(циклогексилметил)2-(1,1-диметилпропіл)-1Н-бензімідазол-5карбонової кислоти (65,9мг, 0,20ммоль) (див. Приклад 4, опер. E) у ДМФ (5мл) при 0°C і потім HATU (91,3мг, 0,24ммоль). Суміш перемішують протягом ночі при кімнатній температурі, додають H2O (50мл) і екстрагують EtOAc (3´50мл). Бажану сполуку очи щають ВЕРХ (гекс/EtOAc 1:1 як елюент, на силікагелі), отримуючи 75,7мг (89%) білої твердої речовини. 1H ЯМР (400МГц, CD3OD): d 0,86 (t, J=7,52Гц, 3H), 1,04 (m, 3H), 1,28 (m, 8H), 1,66 (m, 2H), 1,69 (s, 6H), 1,71 (m, 1Н), 1,79 (m, 2H), 2,04 (q, J=7,42Гц, 2H), 2,13 (m, 1H), 2,63 (m, 1H), 2,92 (m, 1H), 3,58 (m, 3H), 4,50 (d, J=7,62Гц, 2H), 4,55 (m, 1H), 7,65 (dd, J=8,69, 1,46Гц, 1H), 7,81 (d, J=0,78Гц, 1Н), 8,01 (d, J=8,79Гц, 1H). MS (ESI) (M+H)+=426,2. Аналіз: обчислено для C26H39N3 O2+1,60TFA+0,30H2O (613,46): C, 57,17; H, 6,77; N, 6,85. Отримано: C, 57,18; H, 6,69; N, 6,88. Приклад 9 1-(циклогексилметил)-2-(1,1-диметиллропіл)-5(ізоксазолідин-2-ілкарбоніл)-1H-бензімідазол Згідно з процедурою Прикладу 3, опер. А, використовують ізоксазолідингідрохлорид (29,5мг, 0,26ммоль), діізопропілетиламін (144мкл, 106,6мг, 0,83ммоль) і розчин 1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-карбонової кислоти (82,1мг, 0,25ммоль) (див. Приклад 4, опер. E) у ДМФ (5мл) при 0°C і потім HATU (114,0мг, 0,30ммоль). Суміш перемішують 4год. при кімнатній температурі і гасять доданням H2O (5мл). Після випарювання бажану сполуку очищають зворотнофазовою ВЕРХ (колонка С-18), використовуючи 20-50% CH3CN/H2O, і отримують 94,8мг (76%) білої твердої речовини. 1H ЯМР (400МГц, CD3OD): d 0,86 (t, J=7,42Гц, 3H), 1,27 (m, 5H), 1,66 (m, 3H), 1,69 (s, 6H), 1,79 (m, 2H), 2,04 (q, J=7,49Гц, 2H), 2,13 (m, 1H), 2,43 (m, 2H), 3,94 (m, 2H), 4,07 (t, J=6,74Гц, 2Н), 4,50(d, J=7,62Гц, 2H), 8,00 (m, 2H), 8,19 (s, 1H). MS (ESI) (M+H)+=384,2. Аналіз: обчислено для C23H33N3O2+1,40TFA+1,30H2O (566,59): 39 83832 С, 54,69; H, 6,58; N, 7,42. Отримано: С, 54,66; H, 6,50; N, 7,68. Приклад 10 (4R)-2-{[1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-іл]карбоніл}-4метилізоксазолідин-4-ол Згідно з процедурою Прикладу 3, опер. А, використовують гідрохлорид (4R)-4метилізоксазолідин-4-олу (36,0мг, 0,25ммоль), діізопропілетиламін (144мкл, 106,6мг, 0,83ммоль) і розчин 1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-карбонової кислоти (82,1мг, 0,25ммоль) (див. Приклад 4, опер. E) у ДМФ (5мл) при 0°C і потім HATU (114,0 мг,0,30ммоль). Суміш перемішують 4год. при кімнатній температурі, додають H2O (5мл). Після випарювання бажану сполуку очищають зворотнофазовою ВЕРХ (колонка С-18), використовуючи 20-50% CH3CN/H2O, і отримують 90,5мг (69%) білої твердої речовини. [a]D: +16,6° (с 0,15, EtOH). 1H ЯМР (400МГц, CD3OD): d 0,86 (t, J=7,42Гц, 3H), 1,26 (m, 5H), 1,50 (s, 3H), 1,66 (m, 3H), 1,69 (s, 6H), 1,79 (m, 2H), 2,04 (q, J=7,49Гц, 2H), 2,13 (m, 1H), 3,82 (d, J=11,33Гц, 1H), 3,89 (d, J=8,40Гц, 1H), 3,97 (m, 2H), 4,50 (d, J=7,81Гц, 2H), 7,99 (m, 2H), 8,19 (s, 1H),. MS (ESI) (M+H)+=414,2. Аналіз: обчислено для C24H35N3O3+1,50 TFA+1,10H2O (604,42): C, 53,65; H, 6,45; N, 6,95. Отримано: C, 53,55; H, 6,44; N, 7,18. Приклад 11 (4S)-2-{[1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-іл]карбоніл}-4метилізоксазолідин-4-ол Згідно з процедурою Прикладу 3, опер. А, використовують гідрохлорид (4S)-4метилізоксазолідин-4-олу (36,8мг, 0,264ммоль), діізопропілетиламін (144мкл, 106,6мг, 0,83ммоль) і розчин 1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-карбонової кислоти (83,2мг, 0,253ммоль) (див. Приклад 4, опер. E) у ДМФ (5мл) при 0°C і потім HATU (114,0мг, 0,30ммоль). Суміш перемішують 4год. при кімнатній температурі і гасять доданням H2O (5мл). Після випарювання бажану сполуку очищають зворотнофазовою ВЕРХ (колонка С-18), використовуючи 20-50% CH3CN/H2O, і отримують 74,9мг (56%) білої твердої речовини. [a]D: -14,1° (с 0,17, EtOH). 1H ЯМР (400МГц, CD3OD): d 0,85 (t, J=7,52Гц, 3H), 1,27 (m, 5H), 1,50 (s, 3H), 1,66 (m, 3H), 1,69 (s, 6H), 1,79 (m, 2H), 2,04 (q, J=7,42Гц, 2H), 2,13 (m, 1H), 40 3,82 (d, J=11,33Гц, 1H), 3,89 (d, J=8,40Гц, 1H), 3,97 (m, 2H), 4,50 (d, J=7,62Гц, 2H), 7,99 (m, 2H), 8,18 (s, 1H). MS (ESI) (M+H)+=414,2. Аналіз: обчислено для C24H35N3 O3+1,30TFA+2,00H2O (597,83): C, 53,44; H, 6,79; N, 7,03. Отримано: C, 53,39; H, 6,64; N, 7,22. Приклад 12 2-трет-бутил-1-(циклогексилметил)-N-метокси1Н-бензімідазол-5-карбоксамід Згідно з процедурою Прикладу 3, опер. А, використовують 2-трет-бутил-1-(циклогексилметил)1Н-бензімідазол-5-карбонову кислоту (50мг, 0,159ммоль) (див. Приклад. 3, опер. В-F), карбоксамідметоксиламінгідрохлорид (26мг, 0,318ммоль) HATU (75мг, 0,191ммоль) і діізопропілетиламін (0,085мл, 0,318ммоль) у 5мл ДМФ. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 10-50% CH3CN/H2O на колонці С-18, і потім ліофілізують, і отримують бажану сполуку як сіль TFA. Вихід: 56мг (77%). 1H Я МР (400МГц, METAHОЛD4): d 1,24 (m, 5H), 1,62 (m, 2H), 1,68 (s, 10Н), 1,76 (m, 2H), 2,11 (m, 1Н), 3,83 (s, 3H), 4,48 (d, J=7,62Гц, 2Н), 7,93 (dd, J=8,79, 1,56Гц, 1H), 7,98 (m, 1H), 8,18 (dd, J=1,56, 0,78Гц, 1H); MS (ESI) (М+Н)+ 344,3; Аналіз: обчислено для C20H29N3 O2+1,6TFA+0,6H2 O: С, 51,92; H, 5,97; N, 7,83. Отримано: С, 51,85; H, 6,02; N, 7,78. Приклад 13 2-трет-бутил-1-(циклогексилметил)-N-етокси1Н-бензімідазол-5-карбоксамід Згідно з процедурою Прикладу 3, опер. А, використовують 2-трет-бутил-1-(циклогексилметил)1Н-бензімідазол-5-карбонову кислоту (сіль TFA) (100мг, 0,233ммоль) (див. опер. B-F y Прикладі 3), О-етилгідроксиламінгідрохлорид (35мг, 0,350ммоль) HATU (110мг, 0,280ммоль) і діізопропілетиламін (0,145мл, 0,816ммоль) у 5мл ДМФ. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 10-50% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як сіль TFA. Ви хід: 73мг (66%). 1H ЯМР (400МГц, МЕТАНОЛ-D4): 5 1,25 (m, 5H), 1,33 (t, J=7,03Гц, 3H), 1,64 (m, 2Н), 1,69 (s, 10Н), 1,78 (m, 2Н), 2,13 (m, 1Н), 4,06 (q, J=7,03Гц, 2Н), 4,50 (d, J=7,62Гц, 2H), 7,95 (dd, J=7,23, 1,56Гц, 1Н), 8,00 (m, 1H), 8,19 (d, J=0,78Гц, 1H); MS (ESI) (M+H)+ 358,3; Аналіз: обчислено для C21H31N3O2+1,5TFA+1,0H 2O: C, 52,74; H, 6,36; N, 7,69. Отримано: C, 52,74; H, 6,50; N, 7,54. 41 83832 42 Приклад 14 2-трет-бутил-1-(циклогексилметил)-N-етил-Nметил-1Н-бензімідазол-5-карбоксамід Згідно з процедурою Прикладу 3, опер. А, використовують 2-трет-бутил-1-(циклогексилметил)1Н-бензімідазол-5-карбонову кислоту (TFA salt) (47мг, 0,110ммоль) (див. опер. B-F y Прикладі 3), N-етилметиламін (0,015мл, 0,165ммоль), HATU (50мг, 0,132ммоль) і діізопропілетиламін (0,030мл, 0,165ммоль) у 5мл ДМФ. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 20-80% CH3CN/H2O на колонці С-18 і потім ліофілізують, отримуючи бажану сполуку як сіль TFA. Вихід: 45мг (87%). 1H ЯМР (400МГц, МЕТАНОЛ-D4): d 1,17 (t, J=0,93Гц, 2Н), 1,26 (m, 8H), 1,66 (m, 2H), 1,70 (s, 9H), 1,79 (m, 2H), 2,14 (m, 1H), 2,99 (s, 1H), 3,12 (s, 1H), 3,33 (d, J=7,03Гц, 1H), 3,63 (q, J=7,03Гц, 1H), 4,50(d, J=7,62Гц, 2H), 7,63 (t, J=8,01Гц, 1H), 7,79 (d, J=4,49Гц, 1H), 8,00 (d, J=8,59Гц, 1Н); MS (ESI) (M+H)+ 356,3; Аналіз: обчислено для C22H33N3O+1,2TFA+0,5H2 O: С, 58,45; H, 7,08; N, 8,38. Отримано: С, 58,44; H, 7,09; N, 8,39. Приклад 15 (4S)-2-{[трет-бутил-1-(циклогексилметил)-1Нбензімідазол-5-іл]карбоніл}-ізоксазолідин-4-ол Згідно з процедурою Прикладу 3, опер. А, використовують 2-трет-бутил-1-(циклогексилметил)1Н-бензімідазол-5-карбонову кислоту (літієву сіль) (50мг, 0,156ммоль) (див. опер. B-F y Прикладі 3), гідрохлорид (4R)-ізоксазолідин-4-олу (21мг, 0,172ммоль), HATU (71мг, 0,187ммоль) і діізопропілетиламін (0,065мл, 0,390ммоль) у 2мл ДМФ. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 20-80% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як відповідну сіль TFA. Ви хід: 56мг (72%). 1H ЯМР (400МГц, МЕТАНОЛ-D4): d 1,26 (m, 5H), 1,66 (m, 2Н), 1,70 (s, 10H), 1,79 (m, 2Н), 2,14 (m, 1Н), 3,84 (d, J=11,91Гц, 1Н), 4,00(d, J=8,20Гц, 1H), 4,07 (m, 2H), 4,51 (d, J=7,62Гц, 2H), 4,82 (m, 1H), 8,00 (m, 2H), 8,20(s, 1H); MS (ESI) (М+Н)+ 386,2; Аналіз: обчислено для C22H31N3O3+1,5TFA: С, 53,95; H, 5,89; N, 7,55. Отримано: С, 53,93; H, 5,74; N, 7,60. Приклад 16 (4S)-2-{[2-трет-бутил-1-(циклогексилметил)-1Нбензімідазол-5-л]карбоніл}-ізоксазолідин-4-ол Згідно з процедурою Прикладу 3, опер. А, використовують 2-трет-бутил-1-(циклогексилметил)1Н-бензімідазол-5-карбонову кислоту (літієву сіль) (50мг, 0,156ммоль) (див. опер. B-F y Прикладі 3), гідрохлорид (4S)-ізоксазолідин-4-олу (21 г, 0,172ммоль), HATU (71мг, 0,187ммоль) і діізопропілетиламін (0,065мл, 0,390ммоль) у 2мл ДМФ. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 20-80% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як відповідну сіль TFA. Ви хід: 58мг (74%). 1H ЯМР (400МГц, МЕТАНОЛ-D4): 5 1,26 (m, 5H), 1,66 (m, 2H), 1,70(s, 10Н), 1,79 (m, 2Н), 2,15 (m, 1H), 3,84 (d, J=12,11Гц, 1H), 3,99 (d, J=8,01Гц, 1H), 4,07 (m, 2H), 4,51 (d, J=7,62Гц, 2H), 4,82 (m, 1H), 8,00 (m, 2H), 8,19 (m, 1H); MS (ESI) (M+H)+ 386,2; Аналіз: обчислено для C22H31N3O3+1,3TFA+0,8H 2O: C, 53,90; H, 6,23; N, 7,67. Отримано: C, 53,86; H, 6,30; N, 7,65. Приклад 17 Трет-бутил-1-(циклогексилметил)-5(ізоксазолідин-2-ілкарбоніл)-1Н-бензімідазол Згідно з процедурою Прикладу 3, опер. А, використовують 2-трет-бутил-1-(циклогексилметил)1Н-бензімідазол-5-карбонову кислоту (літієву сіль) (50мг, 0,156ммоль) (див. опер. B-F y Прикладі 3), ізоксазолідингідрохлорид (19мг, 0,172ммоль), HATU (71мг, 0,187ммоль) і діізопропілетиламін (0,065мл, 0,390ммоль) у 2мл ДМФ. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 20-80% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як відповідну сіль TFA. Ви хід: 72мг (95%). 1H ЯМР (400МГц, МЕТАНОЛ-D4): 5 1,26 (m, 5H), 1,65 (m, 1Н), 1,67 (m, 1Н), 1,70 (s, 9H), 1,79 (m, 2Н), 2,14 (m, 1Н), 2,43 (m, 2Н), 3,93 (m, 2Н), 4,07 (t, J=6,74Гц, 2Н), 4,51 (d, J=7,62Гц, 2Н), 8,00 (m, 2H), 8,19 (s, 1H); MS (ESI) (М+Н)+ 370,2; Аналіз: обчислено для C22H3IN3O 2+1,7TFA+0,6 H2O: С, 53,14; H, 5,95; N, 7,32. Отримано: С, 53,19; H, 5,95; N, 7,41. Приклад 18 (4R)-2-{[2-трет-бутил-1-(циклогексилметил)1Н-бензімідазол-5-іл]карбоніл}-4метилізоксазолідин-4-ол 43 83832 Згідно з процедурою Прикладу 3, опер. А, використовують 2-трет-бутил-1-(циклогексилметил)1Н-бензімідазол-5-карбонову кислоту (літієву сіль) (50мг, 0,156ммоль) (див. опер. B-F y Прикладі 3), гідрохлорид (4R)-4-метилізоксазолідин-4-олу (24мг, 0,172ммоль), HATU (71мг, 0,187ммоль) і діізопропілетиламін (0,065мл, 0,390ммоль) у 2мл ДМФ. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 20-80% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як відповідну сіль TFA. Ви хід: 63мг (79%). 1H ЯМР (400 МГц, МЕТАНОЛ-D4): d 1,26 (m, 5H), 1,50 (s, 3H), 1,65 (m, 3H), 1,70 (s, 9Н), 1,79 (m, 2Н), 2,14 (m, 1Н), 3,82 (d, J=11,33Гц, 1Н), 3,89 (d, J=8,40Гц, 1Н), 3,97 (m, 2Н), 4,51 (d, J=7,62Гц, 2H), 7,99 (m, 2H), 8,19 (s, 1H); MS (ESI) ( М+Н)+ 400,2; Аналіз: обчислено для C23H33N3 O3+1,5TFA+0,7H2 O: C,53,55; H, 6,20; N, 7,21. Отримано: С, 53,51; H, 6,21; N, 7,29. Приклад 19 (4S)-2-{[1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5іл]карбоніл}ізоксазолідин-4-ол Згідно з процедурою Прикладу 4, опер. А, використовують 1-(циклогексилметил)-2-(1,1диметилпропіл)-1Н-бензімідазол-5-карбонову кислоту (50мг, 0,152ммоль) (див. опер. В, C, D і E у Прикладі 4) гідрохлорид (4S)-ізоксазолідин-4-олу (21мг, 0,167ммоль), HATU (69мг, 0,182ммоль) і діізопропілетиламін (0,066мл, 0,380ммоль) у 2мл ДМФ. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 20-80% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як відповідну сіль TFA. Ви хід: 74мг (95%). 1H ЯМР (400МГц, МЕТАНОЛ-D4): 8 0,86 (t, J=7,52Гц, 3H), 1,26 (m, 5H), 1,65 (m, 2H), 1,69 (s, 7H), 1,79 (m, 2H), 2,04 (q, J=7,42Гц, 2H), 2,13 (m, 1H), 3,84 (d, J=11,91Гц, 1H), 4,00(d, J=8,01Гц, 1Н), 4,07 (m, 2H), 4,51 (d, J=7,62Гц, 2H), 4,82 (m, 1H), 8,00 (m, 2H), 8,20 (m, 1H); MS (ESI) (M+H)+ 400,2; Аналіз: обчислено для C23H33N3 O3+1,7TFA+1,5H2 O: С, 51,11; H, 6,13; N, 6,77. Отримано: С, 51,12; H, 6,00; N, 7,03. Приклад 20 2-трет-бутил-1-(циклогексилметил)-N-етоксиN-етил-1Н-бензімідазол-5-карбоксамід 2-трет-бутил-1-(циклогексилметил)-1Нбензімідазол-5-карбонову кислоту (літієву сіль) (100мг, 0,312ммоль) (див. Приклад 3, опер. В-F), О-етилгідроксиламінгідрохлорид (36мг, 44 0,374ммоль), HATU (140мг, 0,374ммоль) і діізопропілетиламін (0,135мл, 0,780ммоль) перемішують у 3мл ДМФ при кімнатній температурі протягом 2год. Розчинник концентрують, залишок розчиняють у EtOAc і промивають насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4. Розчинник випарюють. Сирий продукт розчиняють у 4мл ДМФ і потім додають краплями з перемішуванням до холодного (0°С) розчину (1мл) NaH у ДМФ (60%-на дисперсія в олії) (15мг, 0,374ммоль). Додають етилйодид (0,050мл, 0,624ммоль) і розчин перемішують при кімнатній температурі протягом ночі. Реакційну суміш гасять при 0°C доданням насиченого водного розчину NH4CI і розчинник концентрують. Залишок розчиняють у EtOAc, промивають насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4. Продукт очищають зворотнофазовою ВЕРХ, використовуючи 20-80% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як відповідну сіль TFA. Вихід: 68мг (44%). 1H Я МР (400МГц, МЕТАНОЛD4І): d 1,03 (t, J=7,03Гц, 3H), 1,27 (m, 5H), 1,33 (t, J=7,13Гц, 3H), 1,66 (m, 2H), 1,70(s, 10Н), 1,79 (m, 2H), 2,15 (m, 1H), 3,84 (m, 4H), 4,51 (d, J=7,62Гц, 2H), 7,88 (dd, J=8,79, 1,56Гц, 1H), 8,00 (dd, J=8,79, 0,59Гц, 1H), 8,06 (d, J=0,78Гц, 1H); MS (ESI) (М+Н)+ 386,2; Аналіз: обчислено для C23H35N3 O2+1,2TFA+0,7H2 O: С, 57,03; H, 7,08; N, 7,85.Отримано: С, 56,99; H, 7,00; N, 7,80. Приклад 21 2-трет-бутил-N-метокси-N-метил-1 (тетрагідро-2Н-піран-4-ілметил)-1H-бензімідазол5-карбоксамід Операція А. 2-тpeт-бyтил-N-мeтoкcи-N-мeтил1-(тeтpaгiдpo-2H-пipaн-4-iлмeтил)-1Hбензімідазол-5-карбоксамід 2-трет-бутил-1-(тетрагідро-2Н-піран-4ілметил)-1Н-бензімідазол-5-карбонову кислоту (літієву сіль) (див. опер. B-E) (50мг, 0,155ммоль), N,О-диметилгідроксиламінгідрохлорид (17мг, 0,171ммоль) і HATU (70мг, 0,186ммоль) перемішують у 3мл ДМФ з діізопропілетиламіном (0,040мл, 0,233ммоль) при кімнатній температурі протягом 2год. Розчинник концентрують і продукт очищають зворотно-фазовою ВЕРХ, використовуючи 10-50% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як відпо 45 83832 відну сіль TFA. Ви хід: 55мг (75%). 1H ЯМР (400МГц, МЕТАНОЛ-D4): d 1,55 (m, 3H), 1,61 (m, 1H), 1,69 (s, 9Н), 2,40(m, 1H), 3,35 (m, 2H), 3,40 (s, 3H), 3,57 (s, 3H), 3,92 (d, J=3,12Гц, 1H), 3,95 (m, 1H), 4,56 (dd, J=7,42Гц, 2H), 7,88 (dd, J=8,79,1,37Гц, 1H), 8,01 (d, J=8,79Гц, 1H), 8,07 (m, J=1,37Гц, 1H); MS (ESI) (М+Н)+ 360,3; Аналіз: обчислено для C20H29N3O3+1,6TFA+1,1H 2O: C, 49,61; H, 5,89; N, 7,48. Отримано: C, 49,63; H, 5,89; N, 7,53. Операція В. Метил-3-нітро-4-[(тетрагідро-2Нпіран-4-ілметил)аміно]бензоат Метил-4-флуор-3-нітробензоат (400мг, 2,01ммоль) (див. Приклад 3, опер. В) і 4амінометилтетрагідропіран (280мг, 2,41ммоль) перемішують у 5мл EtOH з триетиламіном (0,420мл, 3,02ммоль) при 75°С протягом 4год. Розчинник концентрують, залишок розчиняють у EtOH і промивають розчином 5% КSO4, насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4. Сирий продукт очищають флешхроматографією, використовуючи 2:1/гексани:EtOAc як елюент на силікагелі, і отримують бажану сполуку. Вихід: 545мг (92%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D): d 1,39-1,51 (m, 2H), 1,74 (d, J=1,76Гц, 1Н), 1,78 (d, J=1,95Гц, 1H), 1,93-2,03 (m, 1H), 3,28 (m, J=6,83, 5,66Гц, 2H), 3,43 (td, J=11,86, 2,05Гц, 2Н), 3,91 (s, 3H), 4,02 (d, J=3,91Гц, 1H), 4,05 (d, J=3,91Гц, 1H), 6,87 (d, J=8,98Гц, 1H), 8,06 (ddd, J=9,08, 2,05, 0, 78Гц, 1H), 8,42-8,49 (m, 1H), 8,89 (d, J=2,15Гц, 1H). Операція С. Метил-3-аміно-4-[(тетрагідро-2Нпіран-4-ілметил)аміно]бензоат Метил-3-нітро-4-[(тетрагідро-2Н-піран-4ілметил)аміно]бензоат (540мг, 1,83ммоль) розчиняють у 50мл EtOAc з каталітичною кількістю 10% Pd/C. Розчин струшують у гідрогенаційному апараті Парра під гідрогеном при 45фунт/кв. дюйм (3ат) при кімнатній температурі протягом 6год. Розчин фільтрують через целіт і розчинник концентрують. Вихід: 455мг (94%); MS (ESI) (М+Н)+ 264,93. Операція D. Метил-3-аміно-4-[(тетрагідро-2Нпіран-4-ілметил)аміно]бензоат 46 Метил-3-аміно-4-[(тетрагідро-2Н-піран-4ілметил)аміно]бензоат (455мг, 1,72ммоль) і каталітичну кількість DMAP розчиняють у 25мл ДХМ. Краплями додають триметилацетилхлорид (0,230мл, 1,89ммоль) і розчин перемішують при кімнатній температурі протягом 2год. Розчин промивають насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4. Розчинник випарюють, залишок розділяють на 3 частини і кожну розчиняють у 4мл льодяної оцтової кислоти у герметичній пробірці. Кожний розчин нагрівають при 175°С у мікрохвильовому інструменті Smithsynthesizer (Personal Chemistry) протягом 1год. Зразки об'єднують і розчинник концентрують. Залишок розчиняють у EtOAc і промивають насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4. Сирий продукт очищають флешхроматографією, використовуючи 2:1/гексани:ацетон як елюент на силікагелі, і отримують бажану сполуку. Вихід: 237мг (42%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D): d 1,51 (m, 3H), 1,55 (m, 1Н), 1,58 (в, 9Н), 2,29 (m, 1H), 3,31 (m, 2Н), 3,93 (s, 3H), 3,96 (m, 1Н), 3,99 (t, J=3,03Гц, 1Н), 4,23 (d, J=7,42Гц, 2H), 7,35 (d, J=8,59Гц, 1H), 7,96 (dd, J=8,59, 1,56Гц, 1H), 8,47 (d, J=0,98Гц, 1H). Операція E: 2-трет-бутил-1-(тетрагідро-2Нпіран-4-ілметил)-1Н-бензімідазол-5-карбонова кислота Метил 2-трет-бутил-1-(тетрагідро-2Н-піран-4ілметил)-1Н-бензімідазол-5-карбоксилат (230мг, 0,696ммоль) розчиняють у 5мл EtOH. Додають 1М LiOH (0,765мл, 0,766ммоль) і розчин витримують під зворотним холодильником протягом 3год. Розчинник концентрують і продукт ізолюють як літієву сіль і використовують у наступній операції. Вихід: 240мг (99%). MS (ESI) (М+Н)+317,23. Приклад 22 2-трет-бутил-5-(ізоксазолідин-2-ілкарбоніл)-1(тетрагідро-2Н-піран-4-ілметил)-1Н-бензімідазол Згідно з процедурою Прикладу 3, опер. А, використовують 2-трет-бутил-1-(тетрагідро-2Н-піран4-ілметил)-1Н-бензімідазол-5-карбонову кислоту 47 83832 (літієву сіль) (50мг, 0,156ммоль), ізоксазолідингідрохлорид (19мг, 0,172ммоль), HATU (70мг, 0,187ммоль) і діізопропілетиламін (0,040мл, 0,233ммоль) у 3мл ДМФ. Продукт очищають зворотно-фазовою ВЕРХ, використовуючи 10-50% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як відповідну сіль TFA. Вихід: 57мг (76%). 1H Я МР (400МГц, МЕТАНОЛD4): d 1,55 (m, 3H), 1,60 (m, 1Н), 1,69 (s, 9H), 2,40 (m, 3H), 3,34 (dt, J=11,67, 2,44Гц, 2Н), 3,93 (m, 4Н), 4,05 (t, J=6,74Гц, 2Н), 4,55 (d, J=7,42Гц, 2H), 7,98 (m, 2H), 8,17 (m, 1H); MS (ESI) (М+Н)+ 372,3; Аналіз: обчислено для C21H29N3O 3+1,4TFA+0,8H2O: С, 52,40; H, 5,91; N, 7,70. Отримано: С, 52,37; H, 5,97; N, 7,65. Приклад 23 2-трет-бутил-1-[(4,4дифлуорциклогексил)метил]-N-метокси-N-метил1Н-бензімідазол-5-карбоксамід 48 C21H29N3 O2F 2+1,2TFA+0,7H2O: C, 51,77; H, 5,87; N, 7,74. Отримано: C, 51,72; H, 5,63; N, 8,14. Операція В. Трет-бутил-[(4,4дифлуорциклогексил)метил]карбамат 4-N-Вос-амінометилциклогексанон (500мг, 2,2ммоль) розчиняють у 20мл ДХМ при 0°C під нітрогеном. Краплями додають DAST (0,580мл, 4,4ммоль) і розчин перемішують при кімнатній температурі 2год. Розчин промивають 5%-м розчином KHSO4, насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4. Сирий продукт очищають флеш-хроматографією, використовуючи 3:1/гексани:EtOAc як елюент на силікагелі, і отримують бажану сполуку. Вихід: 221мг (40%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D): d 1,28 (m, 2H), 1,44 (s, 9Н), 1,54 (m, 1H), 1,68 (m, 1H), 1,77 (m, 3H), 2,09 (m, 2H), 3,03 (t, J=6,54Гц, 2Н), 4,62 (m, 1H). Операція C. [(4,4дифлуорциклогексил)метил]амінгідрохлорид Операція А. 2-трет-бутил-1-[(4,4дифлуорциклогексил)метил]-N-метокси-N-метил1H-бензімідазол-5-карбоксамід Метил-2-трет-бутил-1-[(4,4дифлуорциклогексил)метил]-1Н-бензімідазол-5карбоксилат (33мг, 0,0905ммоль) (див. опер. B-F) витримують під зворотним холодильником у 1:1 суміші EtOH:Н2О з 1М LiOH (0,100мл, 0,0996ммоль) протягом 3год. Розчинник випарюють, залишок розчиняють у 5мл ДМФ і HATU (41мг, 0,0996ммоль) і додають N,Oдиметилгідроксиламінгідрохлорид (11мг, 0,109ммоль) і діізопропілетиламін (0,024мл, 0,149ммоль). Розчин перемішують при кімнатній температурі 1год. Розчинник випарюють, залишок розчиняють у EtOAc і промивають насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4 . Продукт очи щають зворотно-фазовою ВЕРХ, використовуючи 10-50% CH3CN/H2O на колонці С-18, і потім ліофілізують, отримуючи бажану сполуку як відповідну сіль TFA: Ви хід: 32мг (70%). 1H ЯМР (400МГц, МЕТАНОЛ-D4): 5 1,54-1,65 (m, 2H), 1,70 (s, 9Н), 1,74-1,84 (m, 4Н), 2,03-2,12 (m, 2Н), 2,24-2,34 (m, 1Н), 3,41 (s, 3H), 3,58 (s, 3H), 4,59 (d, J=7,42Гц, 2Н), 7,90 (dd, J=8,79, 1,37Гц, 1H), 8,02 (d, J=8,79Гц, 1H), 8,08 (s, 1H); MS (ESI) ( М+Н)+ 394,2; Аналіз: обчислено для Трет-бутил-[(4,4дифлуорциклогексил)метил]карбамат (215мг, 0,862ммоль) перемішують у 3мл 1M НСІ/АсОН при кімнатній температурі 1год. Розчинник концентрують і залишок промивають етером і сушать у вакуумі. Вихід: 135мг (85%); 1H ЯМР (400МГц, МЕТАНОЛ-D4): 5 1,34 (m, 2Н), 1,76 (m, 2Н), 1,85 (m, 2Н), 1,88 (m, 2Н), 2,09 (m, 2Н), 2,86 (d, J=7,03Гц, 2Н). Операції D. Метил-4-{[(4,4дифлуорциклогексил)метил]аміно}-3-нітробензоат Метил-4-флуор-3-нітробензоат (50мг, 0,251ммоль) (див. Приклад 3, опер. В) і [(4,4дифлуорциклогексил)метил]амінгідрохлорид (55мг, 0,301ммоль) перемішують у 3мл EtOH з триетиламіном (0,052мл, 0,376ммоль) при 75°С протягом 4год. Розчинник концентрують, залишок розчиняють у EtOAc і промивають 5%-м розчином KHSO4, насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4. Сирий продукт очи 49 83832 щають флеш-хроматографією, використовуючи 4:1/гексани: EtOAc як елюент на силікагелі, і отримують бажану сполуку. Ви хід: 84мг (99%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D): d 1,43 (ddd, J=12,99, 12,64, 3,51Гц, 2Н), 1,67-1,75 (m, 1H), 1,75-1,86 (m, 2H), 1,91-1,95 (m, 1H), 1,95-1,99 (m, 1H), 2,12-2,22 (m, 2H), 3,29 (dd, J=6,83, 5,66Гц, 2H), 3,91 (s, 3H), 6,86 (d, J=8,98Гц, 1Н), 8,07 (ddd, J=9,03, 2,00, 0,68Гц, 1H), 8,42-8,51 (m, 1H), 8,90 (d, J=2,15Гц, 1Н). Операція Е. Метил-3-аміно-4-{[(4,4дифлуорциклогексил)метил]аміно}бензоат Метил-4-{[(4,4дифлуорциклогексил)метил]аміно}-3-нітробензоат (80мг, 0,244ммоль) розчиняють у 20мл EtOAc з каталітичною кількістю 10% Pd/C. Розчин струшують у гідрогенаційному апараті Парра під гідрогеном (45фунт/кв. дюйм (3ат)) при кімнатній температурі протягом 5год. Розчин фільтрують через целіт і розчинник концентрують. Вихід: 73мг (99%); MS (ESI) (М+Н)+ 299,21. Операція F. Метил-2-трет-бутил-1-[(4,4дифлуорциклогексил)метил]-1Н-бензімідазол-5карбоксилат Комп’ютерна в ерстка О.Гапоненко 50 Метил-3-аміно-4-{[(4,4дифлуорциклогексил)метил]аміно}бензоат (70мг, 0,235ммоль) і DMAP (5мг, 0,047ммоль) розчиняють у 5мл ДХМ. Додають краплями триметилацетилхлорид (0,031мл, 0,259ммоль) і розчин перемішують при кімнатній температурі 3год. Розчин промивають насиченим розчином NaHCO3 і розсолом і сушать над безводн. MgSO4 . Розчинник випарюють, залишок розчиняють у 3мл льодяної оцтової кислоти у герметичній пробірці. Розчин нагрівають при 175°С у мікрохвильовому інструменті Smithsynthesizer (Personal Chemistry) протягом 4´1год. Розчинник концентрують, залишок розчиняють у EtOAc і промивають насиченим розчином NaHCO3, розсолом і сушать над безводн. MgSO4 . Сирий продукт очищають флешхроматографією, використовуючи 2:1/гексани/EtOAc як елюент на силікагелі і отримують бажану сполуку. Ви хід: 33мг (39%). 1H ЯМР (400МГц, ХЛОРОФОРМ-D): d 1,44-1,54 (m, 2H), 1,56 (s, 9H), 1,59-1,67 (m, 1H), 1,66-1,73 (m, 3H), 2,07-2,18 (m, 3H), 3,92 (s, 3H), 4,23 (d, J=7,42Гц, 2Н), 7,31 (d, J=8,59Гц, 1Н), 7,95 (dd, J=8,59, 1,56Гц, 1H), 8,48 (s, 1H). Підписне Тираж 28 прим. Міністерство осв іт и і науки України Держав ний департамент інтелектуальної в ласності, вул. Урицького, 45, м. Київ , МСП, 03680, Україна ДП “Український інститут промислов ої в ласності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюBenzimidazole derivatives, compositions containing them, preparation thereof and uses thereof
Автори англійськоюLiu Ziping, Page Daniel, Walpole Christopher, Yang Hua
Назва патенту російськоюПроизводные бензимидазола, фармацевтическая композиция, которая их содержит, способ их получения и их применение
Автори російськоюЛю Зипинг, Паже Даниэль, Волпоул Кристофер, Янг Хуа
МПК / Мітки
МПК: A61P 25/00, C07D 401/06, C07D 235/08, C07D 405/06, A61K 31/4184
Мітки: похідні, фармацевтична, одержання, містить, композиція, спосіб, бензимідазолу, застосування
Код посилання
<a href="https://ua.patents.su/25-83832-pokhidni-benzimidazolu-farmacevtichna-kompoziciya-shho-kh-mistit-sposib-kh-oderzhannya-ta-kh-zastosuvannya.html" target="_blank" rel="follow" title="База патентів України">Похідні бензімідазолу, фармацевтична композиція, що їх містить, спосіб їх одержання та їх застосування</a>
Попередній патент: Спосіб детонаційного напилювання покриттів і пристрій для його здійснення
Наступний патент: Яс гідравлічний закритого типу
Випадковий патент: Спосіб виготовлення зразків для настроювання приладів контролю змін структури виробів під час шліфування поверхні












