Спосіб одержання бісфенолу a
Номер патенту: 103301
Опубліковано: 10.10.2013
Автори: Кулєша Каміль, Рдесінска-Цвік Тереза, Матия Станіслав, Іванейко Аліна, Бальцеровяк Войцех, Банас Божена, Крюгер Анджей, Майхжак Марія, Ткач Богуслав, Ясінкевіч Єжи
Формула / Реферат
1. Спосіб одержання бісфенолу А з фенолу і ацетону шляхом каталітичної конденсації, в присутності промотованих сульфонільованих іонообмінних смол, використовуючи фракційну кристалізацію для виділення п,п'-БФА (2,2-біс-(4-гідроксифеніл)пропан) ізомеру, де реакцію конденсації ацетону і фенолу проводять в багатостадійній реакційній системі з міжстадійним контролем температури реакції і концентрації ацетону і з контролем концентрації води перед останньою стадією реакційної системи шляхом рециклізації частини післякристалізаційних рідин з кристалізаційного розчинника до потоку, спрямованого до останнього реактора, безперервно подаючи до реакційної системи, що містить каталізатор, реакційну суміш, яка містить ацетон і фенол, і на наступній стадії, воду, ацетон і частину фенолу упарюють з реакційної суміші, яку змішують із стоком фракційної кристалізації, розчиненим в ізомеризаті, збагаченому о,п-ізомером бісфенолу А, одержаному в процесі ізомеризації частини потоку концентрованих рідин після кристалізації з розчинника, ізомеризацію проводять, використовуючи макропористу сульфонільовану іонообмінну смолу у водневій формі і з діаметром пор не менше, ніж 20 нм, як каталізатор, і одержуваний потік піддають кристалізації з розчинника, виділяючи аддукт бісфенолу А і фенолу і післякристалізаційних рідин, і далі розчини розділяють на дві частини: потік, що рециркулюють на останню стадію реакційної системи, і потік, що направляють на концентрування шляхом дистиляції, і потім одну частину післякристалізаційних рідин піддають ізомеризації, а частину концентрованих післякристалізаційних рідин, що залишилась, ректифікують з одночасним розкладом похідних фенолу, що містяться в потоці, де аддукт піддають термальному розкладанню з одержанням суміші ізомерів бісфенолу А, фенолу і побічних продуктів, де вміст ізомеру п,п'-бісфенолу А не менше ніж 90 сг/г, і суміш направляють на фракційну кристалізацію, на якій одержують чистий бісфенол А, в той час як фенол виділяють з технологічних потоків в процесі для концентрування шляхом відгонки, термічного розкладання аддукту бісфенол А/фенол і з ректифікації з одночасним розкладанням похідних фенолу, що включені в частину потоку концентрованих післякристалізаційних рідин, рециклізують до багатостадійної реакційної системи.
2. Спосіб одержання бісфенолу А за п. 1, де реакційна суміш, що містить ацетон, фенол і продукти їх конденсації, контактує з каталізатором в 2-5-стадійній реакційній системі при температурі 323-348 К, і параметри процесу вибирають так, що на виході стадії реакції І молекулярне співвідношення ізомеру о,п'-БФА (2-(2-гідроксифеніл)-2-(4-гідроксифеніл)пропан) до п,п'-БФА є не більше ніж 5/100, і на вході на останню стадію реакції молекулярне співвідношення ізомеру о,п'-БФА до п,п'-БФА не менше ніж 7/100.
3. Спосіб одержання бісфенолу А за п. 1, де відношення завантажуваних потоків до багатостадійної реакційної системи вибирають так, що молекулярне співвідношення води до ацетону в реакційній суміші, яка містить фенол, ацетон, воду, ізомери БФА і побічні продукти, і що контактує з каталізатором при температурі 323-348 К, не більше ніж 0,5 на вході стадії реакції І, і не більше ніж 1,2 на останній стадії реакції багатостадійної реакційної системи.
4. Спосіб одержання бісфенолу А за п. 1, де суміш дистильованих фенолів, виділених з технологічних потоків в результаті концентрування післяреакційної суміші з багатостадійної реакційної системи і післякристалізаційних рідин, також як і термічного розкладання аддукту БФА/фенол і з ректифікації з одночасним каталітичним розкладанням похідних фенолу, додають до свіжого фенолу і спрямовують на стадію І багатостадійної реакційної системи.
5. Спосіб одержання бісфенолу А за п. 1, де частину потоку післякристалізаційних рідин з кристалізації аддукту БФА/фенол, що рециклізують до багатостадійної реакційної системи, змішують на вході на останню стадію реакції з післяреакційною сумішшю з стадії реакції перед останньою стадією в пропорції 1:1 до 3:1.
6. Спосіб одержання бісфенолу А за п. 1, де не більше ніж 95 сг/г вихідного потоку рідин спрямовують на останню стадію багатостадійної реакційної системи, в той час як другий потік піддають концентруванню шляхом відгонки частини фенолу так, що масова фракція бісфенолу А в цьому потоці не менше ніж 12 сг/г, і потім, концентрований потік розділяють на дві частини, одну з яких ректифікують з одночасним каталітичним розкладанням похідних фенолу, а другу частину концентрованих післякристалізаційних рідин спрямовують на ізомеризацію.
7. Спосіб одержання бісфенолу А за п. 1, де концентрування післяреакційної суміші з багатостадійної реакційної системи проводять так, що вміст води в післякристалізаційних рідинах з кристалізації аддукту БФА/фенол не більше ніж 0,4 сг/г.
8. Спосіб одержання бісфенолу А за п. 1, де кристалізацію аддукту проводять так, що вміст ізомеру п,п'-БФА в фільтраті не більше ніж 12 сг/г, а співвідношення ізомеру о,п'-БФА до п,п'- БФА не менше ніж 10/100.
9. Спосіб одержання бісфенолу А за п. 1, де ректифікацію з одночасним розкладанням похідних фенолу з частини потоку концентрованих післякристалізаційних рідин проводять в присутності сильних неорганічних основ КОН або NaOH при температурі принаймні 443 К при пониженому тиску не вище ніж 200 гПа, і параметри ректифікації вибирають так, що фенол, одержуваний в цьому процесі і рециклізований до багатостадійної реакційної системи, містить не більше ніж 0,05 сг/г ізопропенілфенолу (ІПФ).
10. Спосіб одержання бісфенолу А за п. 1, де не більше ніж 85 сг/г потоку концентрованих післякристалізаційних рідин ізомеризують в присутності макропористого сульфонільованого іонообмінного каталізатора при температурі 328-353 К з часовою об'ємною швидкістю рідини 0,2-5 м3/(м3г), в той час як процес ізомеризації проводять так, що збільшення загального вмісту побічних продуктів в результаті ізомеризації не більше ніж 0,2 сг/г.
11. Спосіб одержання бісфенолу А за п. 1, де стік з фракційної кристалізації, збагачений о,п'-БФА ізомером, розчиняють в ізомеризаті при температурі не нижче ніж 353 К в пропорції від 1:5 до 1:20.
Текст
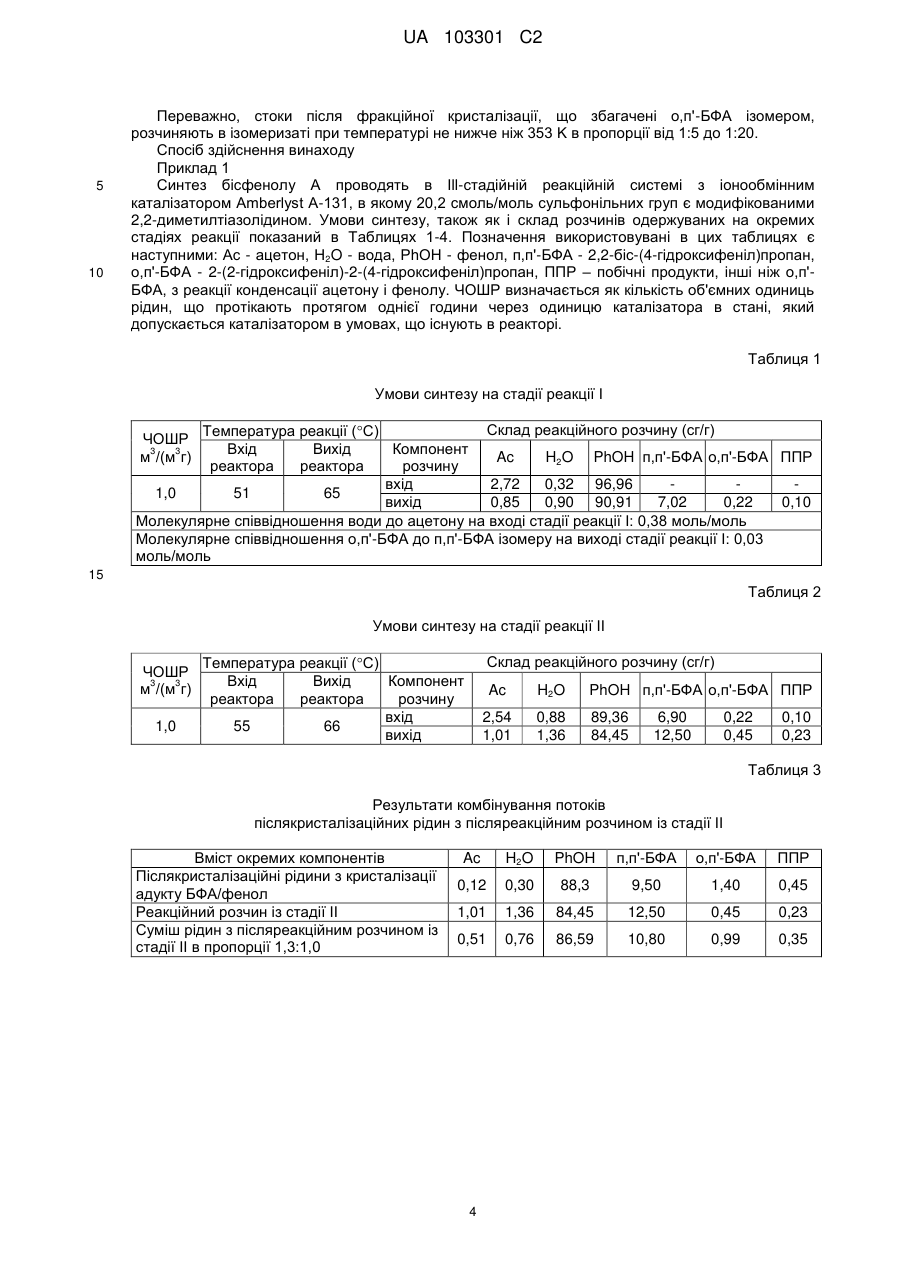
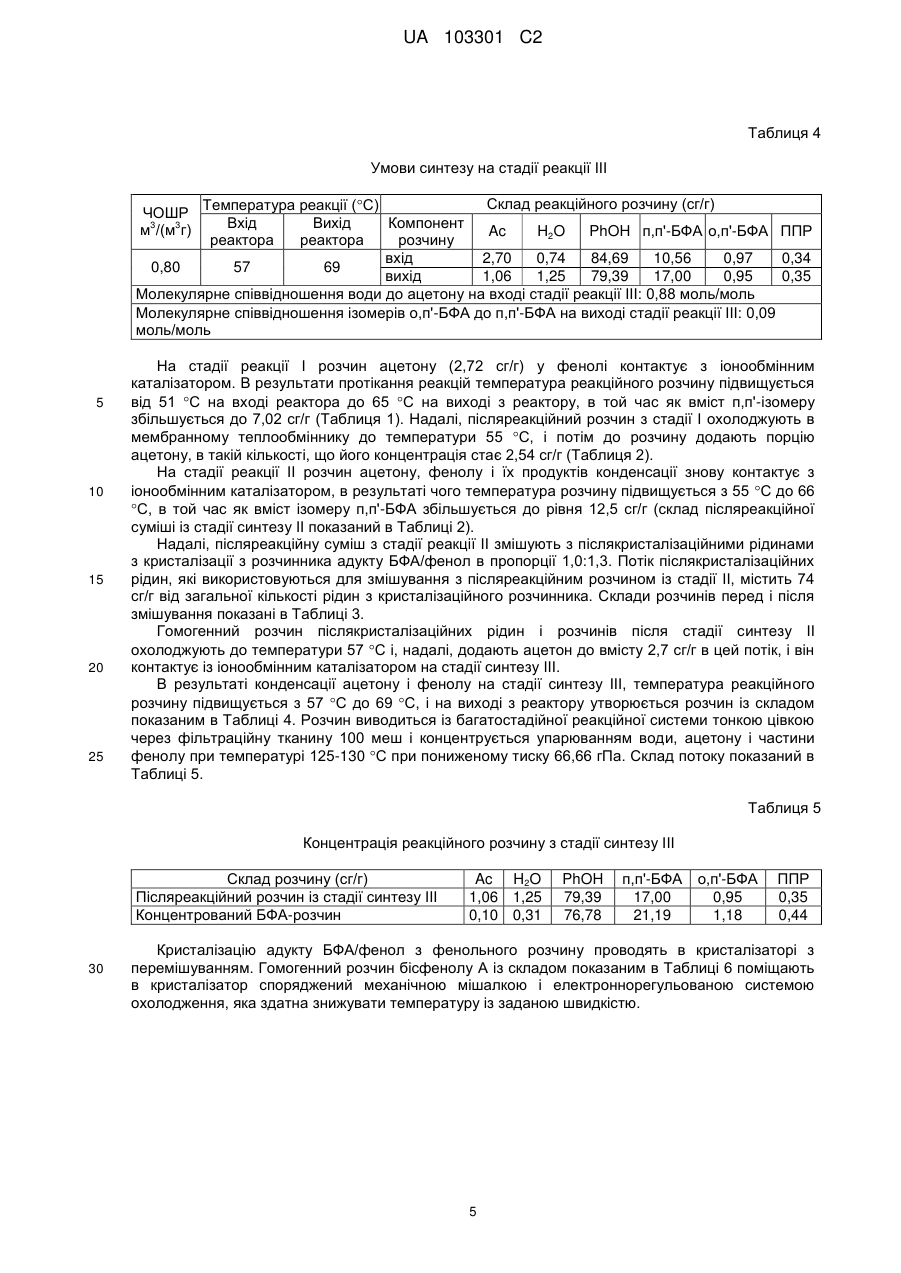
Реферат: Винахід стосується одержання бісфенолу А з фенолу і ацетону шляхом каталітичного конденсування в присутності промотованих сульфонільованих іонообмінних смол, використовуючи фракційну кристалізацію для виділення п,п'-БФА ізомеру. Реакцію конденсації ацетону і фенол проводять в багатостадійній реакційній системі з міжстадійним контролем температури реакції і концентрації ацетону, також як і з контролем концентрації води перед останньою стадією реакційної системи. Частину післякристалізаційних рідин з кристалізацій з розчинника рециклізують до останнього реактора. Воду і ацетон упарюють з післяреакційної суміші, яку надалі змішують із стоком з фракційної кристалізації, розчиненим в ізомеризаті, одержаному в процесі ізомеризації частини потоку концентрованих рідин після кристалізації з розчинника, одержаний потік піддають кристалізації з розчинника, виділений адукт бісфенол А/фенол піддають термічному розкладанню і одержаний сирий бісфенол А піддають фракційній кристалізації. UA 103301 C2 (12) UA 103301 C2 UA 103301 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь винаходу Представлений винахід стосується способу одержання бісфенолу A, сировини для одержання пластиків, зокрема, полікарбонатів. Передумови створення винаходу Бісфенол A (БФА), 2,2-біс-(4-гідроксифеніл)пропан, також має назву п,п'-БФА ізомер, використовується при виробництві пластиків, зокрема, полікарбонатів, їх сумішей і епоксисмол, також як і, але в менших кількостях, для одержання фенопластів, ненасичених поліестерних смол, полісульфонів, поліетерімідів і поліакрилових смол, також як і поліуретанів і добавок до пластиків, серед іншого, вогнезахисних складів, наприклад, тетрабромбісфенолу A і фенілфосфатів з БФА і термічних стабілізаторів для полівінілхлориду. В ході розвитку технології БФА було досліджено можливість його одержання реакцією алену, метилацетилену, 2-ізопропенілфенол, 4-ізопропенілфенолу і ізопропенілацетату з фенолом, також як і реакцією перегрупування гідроксиду кумену і його реакцією з фенолом. Жодна з цих реакцій не може конкурувати із способами одержання БФА за допомогою реакції конденсування фенолу з ацетоном. Було досліджено багато гомогенних каталізаторів, серед інших, BF3 і його адукти з H3PO4, (C2H5)2O, HCOOH, CH3COOH, C2H5COOH, CaF2, також як і HCl з BF3, AlCl3, SnCl4, SbCl5, SnF4 і SbF3 і багато інших каталітичних систем. Однак, спосіб одержання БФА за допомогою конденсації ацетону з фенолом в присутності сірчаної кислоти або хлориду водню, як каталізаторів, використовується в промислових масштабах. Альтернативним способом каталізу реакції одержання БФА є використання сильних кислотних іонообмінних смол (катіоніти), які частіше зустрічаються і краще досліджені, і, на кінець, замінювальні способи використовують H2SO4 або HCl, як каталізатори для реакцій конденсування. Також було рекомендовано використання сульфонільованих співполімерів стиролу і дивінілбензолу (ДВБ) і сульфонільованих фенол-формальдегідних смол, перший із згаданих типів каталізаторів широко використовується на сьогоднішній день в промислових масштабах. Спочатку, використовувались катіоніти із значним ступенем перехресного зв'язування, а надалі почали використовуватись гелькатіоніти з низьким ступенем перехресного зв'язування (2-4 сг/г ДВБ). Другим важливим аспектом пов'язаним з розробкою іонообмінних каталізаторів було використання так званих промоторів, які є тіоорганічними сполуками, які мають тіольну групу або здатні її утворювати за умов реакцій конденсації. Провели ряд тестів по використанню гомогенних промоторів. Однак, їх використання викликає проблеми пов'язані з одержанням продукту високої чистоти. З цієї причини, на сьогодні, все більше і більше популярними є іонообмінні смоли модифіковані тіоорганічними сполуками, які таким чином забезпечують їх приєднання сульфонільною групою, і головним чином використовується для приєднання до кінцевих аміногруп або гетероциклічних сполук, що містять атом(и) азоту основного характеру. Одне з втілень використовуваних для синтезу включає багатостадійну систему проточних реакторів з фіксованим шаром каталізатору, з'єднаних послідовно через теплообмінник, який здатен підтримувати необхідний температурний інтервал в наступних реакторах, індивідуальні втілення відрізняються один від одного подачею ацетону і післякристалізаційними рідинами одержаними в наступних стадіях виділення і очищення БФА. У випадку таких втілень, для реакційної системи відомі і описуються, серед іншого в патенті US 6414199, переваги одержувані від розділення протоку ацетону, що подається в реактори з'єднані послідовно, де переваги полягають, переш за все, у підвищенні часу життя каталізатора і селективності реакції конденсації, що обумовлено кращим розподіленням температури в шарі каталізатора, також як і кращою можливістю контролювати протікання реакцію синтезу БФА. Було протестовано або використано ряд способів по виділенню бісфенолу A, включаючи відгонку, принаймні, частини фенолу, води і ацетону (найбільш часто при пониженому тиску), вакуумну перегонку самого бісфенолу A або його кристалізацію як адукту бісфенол A/фенол, виділення кристалів адукту фільтруванням і наступне розкладання цього адукту вакуумною відгонкою фенолу і отпарювання або витіснення азотом або кристалізацію з різних розчинників. Був запатентований спосіб, що полягає в кристалізації розплаву сировинного бісфенолу A одержаного шляхом дистиляційного виділення ацетону, що непрореагував, води і фенолу з продуктів реакції конденсації. Описано ряд прикладів комбінування згаданих способів, а в WO 0035847 представлена суспензійна кристалізація адукту БФА/фенол, його відокремлення від маткового розчину фільтруванням, розкладання адукту вакуумною відгонкою фенолу і проведення фракційної кристалізації сирого БФА одержаного таким чином. Відомі переваги, які забезпечуються повторним використанням післякристалізаційних рідин, а у випадку повторного повернення до стадії кристалізації або стадії концентрування перед кристалізацією, перевага полягає у повторному використанні фенолу, що не прореагував, і 1 UA 103301 C2 5 10 15 20 25 30 35 40 45 50 55 60 некристалізації БФА, яка значно зменшує розхід сировини. Додаткова перевага, одержувана від рециклізації маткової рідини на стадію синтезу, полягає у обмеженні утворення 2-(2гідроксифеніл)-2-(4-гідроксифеніл)пропану (так званого o,п'-БФА ізомеру) тоді коли система приблизно більш близько наближається до стану рівноваги п,п'-БФА і o,п'-БФА ізомерів. У способах, в яких використовується багатостадійна система проточних реакторів з фіксованим шаром катіонообмінників, забезпечується можливість рециклізації маткового розчину декількома способами так що поповнюється перша стадія реакції конденсації або наступні стадії для проведення цієї реакції. Найбільша перевага полягає в обмеженні утворення o,п'-БФА ізомеру, що обумовлено рециклізації маткового розчину до першої стадії синтезу, ось чому патентна література включає, перш за все, втілення, що включають рециклізацію частини маткового розчину до наступних стадій синтезу тільки як необов'язкову можливість, без вказування на одержувані переваги (патент US 6858759). Рециклізація маткового розчину повністю не вирішує проблему побічних продуктів і вони накопичуються і один із способів вирішення цієї проблеми полягає у виведенні частини потоку одержаного після реакції з способу з ціллю підтримання його концентрації на прийнятному рівні. Навіть, коли фенол відганяється з цього потоку, цей необхідний процес має негативний вплив з точки зору економічних факторів способу одержання БФА. До способів зменшення впливу цього небажаного феномену, що описаний в патентній літературі, належить реакція ізомеризації o,п'БФА у п,п'-БФА, в якій використовується факт, що після кристалізації адукту БФА/фенол, концентрація o,п'-БФА ізомеру є вищою ніж в рівноважному стані, і що має місце процес каталітичного розкладання під впливом кислотного (WO 0040531) або основного (PL 181992) каталізаторів. Спосіб каталітичного розкладання побічних продуктів, що розглядається в патентній літературі як вступ до способу синтезу БФА з продуктів його розкладу, найбільш часто проводять в присутності макропористих іонообмінних смол, як каталізаторів. Реакція ізомеризація дозволяє перетворити o,п'-БФА у п,п'-БФА, також як і, згідно з декількома повідомленнями, також трисфеноли, перш за все, 2,4-біс-[2-(4-гідроксифеніл)ізопропіл]фенол (JP 08333290) присутній серед них в найбільш значних кількостях. Більшість видів побічних продуктів не зазнають змін за умов реакції ізомеризації. Однак, їх загальний внесок у побічні продукти, що утворюються під час реакції конденсування ацетону і фенолу в присутності модифікованих іонообмінних каталізаторів, не є значним. Приймаючи до уваги накопичення побічних продуктів в потоках способу, обов'язковим є відведення частини потоку способу. Недивлячись на незначну кількість побічних продуктів, економічний результат спостерігається, коли вміст п,п'-БФА в потоці, що виводиться з способу, буде значно більшим ніж загальна кількість побічних продуктів, що залишають спосіб. Однак, більш ефективним в цьому відношенні є спосіб каталітичного розкладання в комбінації з повторним синтезом БФА в макропористих катіонітах. У випадку рециклізації всіх летких продуктів розкладання, будуть зустрічатись нові види побічних продуктів, які обумовлюють складності одержання бісфенолу A високої якості. Опис винаходу Ціллю винаходу була розробка способу одержання прозорого і стабільно забарвленого бісфенолу A в рідкому стані, який характеризується доброю ефективністю і селективністю. Неочікувано було знайдено, що рециклізація маткового розчину до останньої стадії синтезу, порівняно із варіантом, в якому він рециклізується до реактору першої стадії, дозволяє обмежити кількість побічних продуктів, інших ніж o,п'-БФА ізомер, і одержати вищий ступінь конверсії, при тому ж самому загальному часі контактування з катіонообмінним каталізатором. У способі, в якому переважно використовується рециклізація маткового розчину на третю стадію реакції конденсації, і у випадку використання фракціонування продуктів каталітичного розкладання і рециклізації тільки фенолу до процесу, показники споживання сировинного матеріалу є незадовільними з огляду на факт, що o,п'-БФА ізомер, який утворюється в такому технологічному варіанті в значних кількостях, утворюється за умов каталітичного розкладання значної кількості ізопропенілфенолів і їх олігомерів, які видаляються з процесу. З цієї причини спосіб одержання бісфенолу A згідно з винаходом використовує ізомеризацію o,п'-БФА в п,п'БФА і рециклізацію ізомеризату до кристалізації, також як і каталітичне розкладання потоку післякристалізаційних рідин і фракціонування продуктів розкладання і наступну рециклізацію до процесу тільки фенолу одержаного з процесу розкладання. Це дозволяє уникнути проблем пов'язаних з новими видами побічних продуктів і в той же самий час гарантує високі показники перетворення сировини у бісфенол A. Сутність способу винаходу полягає у тому, що реакцію конденсації ацетону і фенолу проводять в багатостадійній реакційній системі з міжкаскадним контролем температури реакції і концентрації ацетону, також як і контролем концентрації води перед останньою стадією 2 UA 103301 C2 5 10 15 20 25 30 35 40 45 50 55 реакційної системи при рециклізації частини післякристалізаційних рідин з кристалізаційного розчинника до потоку спрямованого до останнього реактора, і в цей же час безперервним чином контролюючи систему реакторів, що містить каталізатор реакційної суміші, що містить ацетон і фенол. Далі, воду, ацетон і частину фенолу упарюють з одержаної реакційної суміші, яку змішують із стоком після фракційної кристалізації розчиненої в ізомеризаті одержаному в процесі ізомеризації частини потоку концентрованих розчинів після кристалізації з розчину, де процес проводять використовуючи макропористу сульфонільовану іонообмінну смолу, у водневій формі і діаметром пор не менше ніж 20 нм, як каталізатор, одержуваний потік піддають кристалізації з розчину, в якому виділяється адукт бісфенол A/фенол, де адукт піддають термічному розкладанню одержуючи суміш ізомерів бісфенолу A, фенолу і побічних продуктів, що містять п,п'-бісфенол A в кількості не менше ніж 90 сг/г, суміш піддають фракційній кристалізації, в якій одержують чистий бісфенол A, тоді як фенол виділяють з технологічних потоків в процесі дистиляційного концентрування, термічного розкладання адукту бісфенол A/фенол і ректифікації з одночасним розкладанням похідних фенолу, що містяться в частині потоку концентрованих післякристалізаційних рідин, рециклізують до багатостадійної реакційної системи. Переважно, коли реакційна суміш, що містить ацетон, фенол і продукти їх конденсації, контактує з каталізатором в 2-5-стадійній реакційній системі при температурі 323-348 K, крім того, параметри способу вибирають таким чином, що молекулярне співвідношення o,п'-БФА до п,п'-БФА ізомеру на виході першої стадії реакції не більше ніж 5/100 і молекулярне співвідношення o,п'-БФА до п,п'-БФА ізомеру на вході на останню стадію реакції не менше ніж 7/100. Переважно, пропорції завантаження потоків у багатостадійній реакційній системі вибирають таким чином, що молекулярне співвідношення води до ацетону в реакційній суміші, що містить фенол, ацетон, воду, БФА-ізомери і побічні продукти, які контактують з каталізатором при температурі 323-348 K, і не більше ніж 0,5 при потраплянні на першу стадію реакції і не менше ніж 1,2 на останній стадії реакції багатостадійної реакційної системи. Переважно, суміш перегнаних фенолів виділених з технологічних потоків в результаті концентрування післяреакційної суміші з багатостадійної реакційної системи і з післякристалізаційних рідин також як і з термічного розкладання адукту БФА/фенол і з ректифікації використовуючи одночасне каталітичне розкладання похідних фенолу, додають до свіжого фенолу і вводять на першу стадію багатостадійної реакційної системи. Переважно, коли частину потоку післякристалізаційної рідини з кристалізації адукту БФА/фенол, що рециклізують у багатостадійну реакційну систему, примішують на вході останньої стадії реакції з післяреакційною сумішшю із стадії реакції перед останньою в пропорції від 1:1 до 3:1. Переважно, післякристалізаційні рідини з кристалізації адукту БФА/фенол розподіляють на два потоки, завдяки чому більший потік містить не більше ніж 95 сг/г вихідного потоку рідин спрямованих на останню стадію багатостадійної реакційної системи, в той час як другий потік концентрують відгонкою частини фенолу, так що маса фракції бісфенолу A в цьому потоці не менше ніж 12 сг/г, концентрований потік розподіляють на дві частини, одна частина якого ректифікується використовуючи одночасне каталітичне розкладання похідних фенолу і друга частина післякристалізаційних рідин спрямовується на ізомеризацію. Переважно, концентрацію післяреакційної суміші з багатостадійної реакційної системи проводять таким чином, що вміст води в післякристалізаційних рідинах з кристалізації адукту БФА/фенол не більше ніж 0,4 сг/г. Переважно, кристалізацію адукту проводять таким чином, що вміст п,п'-БФА ізомеру у фільтраті не більше ніж 12 сг/г і співвідношення o,п'-БФА до п,п'-БФА ізомеру не менше ніж 10/100. Переважно, проводять ректифікацію з одночасним розкладанням похідних фенолу з частини потоку концентрованих післякристалізаційних рідин в присутності сильних неорганічних основ KOH або NaOH, при температурі принаймні 443 K при пониженому тиску не вище ніж 200 гПа, параметри ректифікації вибирають так, що фенол утворюваний в цьому процесі і рециклізуємий у багатостадійну реакційну систему містить не більше ніж 0,05 сг/г ізопропенілфенолу (ІПФ). Переважно, не більше ніж 85 сг/г потоку концентрованих післякристалізаційних рідин ізомеризується в присутності макропористого сульфонільованого іонообмінного каталізатора 3 3 при температурі 328-353 K із часовою об'ємною швидкістю рідини (ЧОШР) 0,2-5 м /(м г), процес ізомеризації проводять так, що збільшення загальної кількості побічних продуктів, одержуваних внаслідок ізомеризації, не більше ніж 0,2 сг/г. 3 UA 103301 C2 5 10 Переважно, стоки після фракційної кристалізації, що збагачені o,п'-БФА ізомером, розчиняють в ізомеризаті при температурі не нижче ніж 353 K в пропорції від 1:5 до 1:20. Спосіб здійснення винаходу Приклад 1 Синтез бісфенолу A проводять в Ill-стадійній реакційній системі з іонообмінним каталізатором Amberlyst A-131, в якому 20,2 cмоль/моль сульфонільних груп є модифікованими 2,2-диметилтіазолідином. Умови синтезу, також як і склад розчинів одержуваних на окремих стадіях реакції показаний в Таблицях 1-4. Позначення використовувані в цих таблицях є наступними: Ac - ацетон, H2O - вода, PhOH - фенол, п,п'-БФА - 2,2-біс-(4-гідроксифеніл)пропан, o,п'-БФА - 2-(2-гідроксифеніл)-2-(4-гідроксифеніл)пропан, ППР – побічні продукти, інші ніж o,п'БФА, з реакції конденсації ацетону і фенолу. ЧОШР визначається як кількість об'ємних одиниць рідин, що протікають протягом однієї години через одиницю каталізатора в стані, який допускається каталізатором в умовах, що існують в реакторі. Таблиця 1 Умови синтезу на стадії реакції І Склад реакційного розчину (сг/г) Температура реакції (С) Вхід Вихід Компонент Ac H2O PhOH п,п'-БФА o,п'-БФА ППР реактора реактора розчину вхід 2,72 0,32 96,96 1,0 51 65 вихід 0,85 0,90 90,91 7,02 0,22 0,10 Молекулярне співвідношення води до ацетону на вході стадії реакції І: 0,38 моль/моль Молекулярне співвідношення о,п'-БФА до п,п'-БФА ізомеру на виході стадії реакції І: 0,03 моль/моль ЧОШР 3 3 м /(м г) 15 Таблиця 2 Умови синтезу на стадії реакції ІІ ЧОШР 3 3 м /(м г) 1,0 Склад реакційного розчину (сг/г) Температура реакції (С) Вхід Вихід Компонент реактора реактора розчину вхід 55 66 вихід Ac H2O PhOH п,п'-БФА o,п'-БФА ППР 2,54 1,01 0,88 1,36 89,36 84,45 6,90 12,50 0,22 0,45 0,10 0,23 Таблиця 3 Результати комбінування потоків післякристалізаційних рідин з післяреакційним розчином із стадії II Вміст окремих компонентів Післякристалізаційні рідини з кристалізації адукту БФА/фенол Реакційний розчин із стадії ІІ Суміш рідин з післяреакційним розчином із стадії ІІ в пропорції 1,3:1,0 Ac H2O PhOH п,п'-БФА o,п'-БФА ППР 0,12 0,30 88,3 9,50 1,40 0,45 1,01 1,36 84,45 12,50 0,45 0,23 0,51 0,76 86,59 10,80 0,99 0,35 4 UA 103301 C2 Таблиця 4 Умови синтезу на стадії реакції ІІІ Склад реакційного розчину (сг/г) Температура реакції (С) Вхід Вихід Компонент Ac H2O PhOH п,п'-БФА o,п'-БФА ППР реактора реактора розчину вхід 2,70 0,74 84,69 10,56 0,97 0,34 0,80 57 69 вихід 1,06 1,25 79,39 17,00 0,95 0,35 Молекулярне співвідношення води до ацетону на вході стадії реакції ІІІ: 0,88 моль/моль Молекулярне співвідношення ізомерів о,п'-БФА до п,п'-БФА на виході стадії реакції ІІІ: 0,09 моль/моль ЧОШР 3 3 м /(м г) 5 10 15 20 25 На стадії реакції I розчин ацетону (2,72 сг/г) у фенолі контактує з іонообмінним каталізатором. В результати протікання реакцій температура реакційного розчину підвищується від 51 C на вході реактора до 65 C на виході з реактору, в той час як вміст п,п'-ізомеру збільшується до 7,02 сг/г (Таблиця 1). Надалі, післяреакційний розчин з стадії I охолоджують в мембранному теплообміннику до температури 55 C, і потім до розчину додають порцію ацетону, в такій кількості, що його концентрація стає 2,54 сг/г (Таблиця 2). На стадії реакції II розчин ацетону, фенолу і їх продуктів конденсації знову контактує з іонообмінним каталізатором, в результаті чого температура розчину підвищується з 55 C до 66 C, в той час як вміст ізомеру п,п'-БФА збільшується до рівня 12,5 сг/г (склад післяреакційної суміші із стадії синтезу II показаний в Таблиці 2). Надалі, післяреакційну суміш з стадії реакції II змішують з післякристалізаційними рідинами з кристалізації з розчинника адукту БФА/фенол в пропорції 1,0:1,3. Потік післякристалізаційних рідин, які використовуються для змішування з післяреакційним розчином із стадії II, містить 74 сг/г від загальної кількості рідин з кристалізаційного розчинника. Склади розчинів перед і після змішування показані в Таблиці 3. Гомогенний розчин післякристалізаційних рідин і розчинів після стадії синтезу II охолоджують до температури 57 C і, надалі, додають ацетон до вмісту 2,7 сг/г в цей потік, і він контактує із іонообмінним каталізатором на стадії синтезу III. В результаті конденсації ацетону і фенолу на стадії синтезу III, температура реакційного розчину підвищується з 57 C до 69 C, і на виході з реактору утворюється розчин із складом показаним в Таблиці 4. Розчин виводиться із багатостадійної реакційної системи тонкою цівкою через фільтраційну тканину 100 меш і концентрується упарюванням води, ацетону і частини фенолу при температурі 125-130 C при пониженому тиску 66,66 гПа. Склад потоку показаний в Таблиці 5. Таблиця 5 Концентрація реакційного розчину з стадії синтезу III Склад розчину (сг/г) Післяреакційний розчин із стадії синтезу ІІІ Концентрований БФА-розчин 30 Ac H2O 1,06 1,25 0,10 0,31 PhOH 79,39 76,78 п,п'-БФА 17,00 21,19 o,п'-БФА 0,95 1,18 ППР 0,35 0,44 Кристалізацію адукту БФA/фенол з фенольного розчину проводять в кристалізаторі з перемішуванням. Гомогенний розчин бісфенолу A із складом показаним в Таблиці 6 поміщають в кристалізатор споряджений механічною мішалкою і електроннорегульованою системою охолодження, яка здатна знижувати температуру із заданою швидкістю. 5 UA 103301 C2 Таблиця 6 Потоки використовувані для одержання розчину для кристалізації з розчинника і його склад Склад розчину (сг/г) Концентрований післяреакційний розчин із стадії синтезу ІІІ Стоковий розчин з фракційної кристалізації в ізомеризаті БФА-розчин для кристалізації з розчинника 5 10 15 Ac H2O PhOH п,п'-БФА o,п'-БФА ППР 0,10 0,31 76,78 21,19 1,18 0,44 0,01 76,34 21,40 1,53 0,72 0,08 0,25 76,71 21,23 1,24 0,49 Температуру БФА-розчину знижували із швидкістю 5 C/г з 80 C до 55 C і з швидкістю 1 C/г з 55 C до 50 C. Кристалізований адукт БФА/фенол виділяли з рідин фільтруванням при температурі 50 C, використовуючи вакуумну фільтрацію і без промивання кристалів адукту. Післякристалізаційні рідини, склад яких показаний в Таблиці 6, рециклізували до процесу згідно з попередньо приведеними методиками. Адукт БФA/фенол одержаний в результаті описаних операцій розплавляють при температурі 120 C і піддають термічному розкладанню. Розкладання адукту проводять у випарному апараті з рідиною, що падає плівкою, при температурі 165 C при пониженому тиску 26,66 гПа і, надалі, сирий бісфенол A з вмістом фенолу більше ніж 1,0 сг/г додатково піддають відпарюванню при температурі 170 C при тиску 20 гПа з ціллю зменшення вмісту фенолу до менше ніж 0,5 сг/г. Частину післякристалізаційних рідин в кількості 24 сг/г від загальної маси рідин концентрують дистиляцією при температурах 125-130 C при тиску 33,33 гПа. Потік рідин концентрують до вмісту ізомеру п,п'-БФA в розчині 15 сг/г. Склади потоків післякристалізаційної рідини до і після концентрування показані в Таблиці 7. Таблиця 7 Склад післякристалізаційних рідин до і після концентрування Склад розчину (сг/г) Післякристалізаційні рідини до концентрування Післякристалізаційні рідини після концентрування 20 25 30 35 Ac H2O PhOH п,п'-БФА o,п'-БФА ППР 0,12 0,30 88,23 0,50 1,40 0,45 0,00 0,01 82,07 15,00 2,21 0,71 Концентровані післякристалізаційні рідини розділяють на дві частини, потік 72,5 сг/г спрямовують на ізомеризацію, в той час як потік 27,5 сг/г піддають каталітичній деградації з одночасною ректифікацією продуктів розкладання похідних фенолу. Каталітичне розкладання похідних фенолу проводять в реактивній ректифікаційній колонці при температурі 190 C, при тиску 160 гПа, в присутності 0,1 сг/г гідроксиду натрію (NaOH). Дистилят з ректифікаційної колонки переганяють одержуючи, накінець, фенол із вмістом 4-ізопропенілфенолу (PIPH) менше ніж 0,01 сг/г. Перегнаний фенол з каталітичного розкладання похідних фенолу рециклізують на стадію реакції I. Частину потоку концентрованих рідин в кількості 72,5 сг/г ізомеризують при температурі 65 C. Концентровані рідини, склад яких показаний в Таблиці 7, контактують з макропористим каталізатором LEWATIT K2649, воднева форма, з середнім діаметром пор 65 нм і з ЧОШР 0,5 3 3 м /(м г). Стоки з фракційної кристалізації сирого бісфенолу A розчиняють в ізомеризаті, при температурі 87 C, в пропорції 1:12,7, і далі, одержаний розчин змішують з концентрованою післяреакційною сумішшю з стадії реакції III. Склад окремих потоків показаний в Таблиці 6. Очищення бісфенолу A проводять шляхом фракційної кристалізації одержуючи кінцевий продукт полікарбонатної чистоти і високої термічної стабільності. Характеристики бісфенолу A показані в Таблиці 8. 6 UA 103301 C2 Таблиця 8 Характеристики одержаного бісфенолу A Характеристичні параметри продукту Температура твердіння Вміст фенолу Вміст о,п'-БФА ізомеру Вміст принципового компоненту п, п'-БФА Вміст заліза Вміст золи Колір розчину, в метанолі (50 сг/г) Колір в розплавленому стані після нагрівання 2,5 години при 180 С Колір в розплавленому стані після нагрівання 2,5 години при 200 С Значення параметру 156,8 С 25 мкг/г 138 мкг/г 99,98 сг/г
ДивитисяДодаткова інформація
Автори російськоюTkacz, Boguslaw, Rdesinska-Cwik, Teresa, Kulesza, Kamil, Krueger, Andrzej, Matyja, Stanislaw, Majchrzak, Maria, Balcerowiak, Wojciech, Banas, Bozena, Iwanejko, Alina, Jasienkiewicz, Jerzy
МПК / Мітки
МПК: C07C 37/00
Мітки: бісфенолу, одержання, спосіб
Код посилання
<a href="https://ua.patents.su/10-103301-sposib-oderzhannya-bisfenolu-a.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання бісфенолу a</a>
Попередній патент: Спосіб визначення метаболічної стабільності тестованої речовини за метаболізму, який каталізує семікарбазид-чутлива аміноксидаза
Наступний патент: Спосіб виробництва реєстраторів аналогових та дискретних сигналів для електроенергетичних об’єктів
Випадковий патент: Біогазова установка