Спосіб одержання чотириядерного кластерного селеносульфідоброміду ренію re4se4s4br16
Номер патенту: 111360
Опубліковано: 10.11.2016
Автори: Волков Сергій Васильович, Демченко Павло Юрійович, Харькова Людмила Борисівна, Гладишевський Роман Євгенович, Ніколенко Андрій Сергійович, Суботін Владислав Володимирович, Янко Олег Георгієвич, Машкова Емілія Михайлівна
Формула / Реферат
1. Спосіб одержання чотириядерного кластерного селеносульфідоброміду ренію Re4Se4S4Br16, за яким вихідні реагенти завантажують у реактор Г-подібної форми, реакційну суміш нагрівають спочатку у нижній частині відкритого реактора на водяній бані, потім у запаяному реакторі у муфельній шафі при 200 °C, охолоджують до кімнатної температури, рідку фазу переливають у вільне коліно реактора, заморожують у зрідженому азоті, відокремлюють твердий продукт, відмивають його тетрахлорметаном ССl4, висушують у вакуумі, який відрізняється тим, що як вихідні реагенти використовують реній(УП) оксид Re2O7, монобромід сірки S2Br2 та монобромід селену Se2Br2 у мольному співвідношенні 1:8:6-1:12:8, причому спочатку реакційну суміш безперервно нагрівають у нижній частині відкритого реактора на водяній бані при температурі 95-100 °C упродовж 90-100 годин, а потім по всьому об'єму запаяного реактора у муфельній шафі при 200 °C упродовж 150-180 годин.
2. Спосіб за п. 1, який відрізняється тим, що отримують комплекс Re4Se4S4Br16, який проявляє каталітичні властивості у процесі гідрування m-нітробензойної кислоти в m-амінобензойну кислоту, і придатний як компонент каталітичних систем, напівпровідника, хімічного реактиву і препарату.
Текст
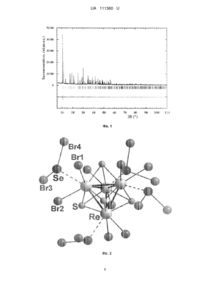
Реферат: Спосіб одержання чотириядерного кластерного селеносульфідоброміду ренію Re4Se4S4Br16, за яким вихідні реагенти завантажують у реактор Г-подібної форми, реакційну суміш нагрівають спочатку у нижній частині відкритого реактора на водяній бані, потім у запаяному реакторі у муфельній шафі при 200 °C, охолоджують до кімнатної температури, рідку фазу переливають у вільне коліно реактора, заморожують у зрідженому азоті, відокремлюють твердий продукт, відмивають його тетрахлорметаном ССl4, висушують у вакуумі. Як вихідні реагенти використовують реній(УП) оксид Re2O7, монобромід сірки S2Br2 та монобромід селену Se2Br2 у мольному співвідношенні 1:8:6-1:12:8. Спочатку реакційну суміш безперервно нагрівають у нижній частині відкритого реактора на водяній бані при температурі 95-100 °C упродовж 90-100 годин, а потім по всьому об'єму запаяного реактора у муфельній шафі при 200 °C упродовж 150-180 годин. UA 111360 U (12) UA 111360 U UA 111360 U 5 10 15 20 25 30 35 40 45 50 55 Корисна модель належить до фізико-хімічної галузі і може бути використана для одержання кластерних халькогенгалогенідів ренію, а саме селеносульфідоброміду ренію Re4Se4S4Br16, який можна застосувати у галузі хімічної промисловості як компонент каталітичних систем, як хімічний реактив і препарат, в сенсорній та мікроелектроніці як напівпровідник. Інтерес до дослідження халькогенгалогенідів ренію пояснюється різноманітністю їхньої будови та цінністю фізико-хімічних властивостей, що обумовлює широку сферу їхнього застосування. Так, гептасульфід ренію, Re2S- є каталізатором селективного гідрування арилзаміщених піридинів, ізохінолінів тощо, а також каталізатором N-алкілування у присутності спиртів для отримання гетероциклічних сполук [Ряшенцева М.А. Рений содержащие катализаторы в реакциях органических соединений // Успехи химии. - 1998. -Т. 66, № 2. -С. 175196). Каталізатори, які одержані на основі комплексних сполук ренію, мають значні переваги порівняно з каталізаторами, що одержують із бінарних сполук ренію: вони є більш дисперсними, демонструють більш високу каталітичну активність та селективність. Важливою перевагою застосування халькогенгалогенідних сполук у каталізі є їхня стійкість відносно до таких відомих отрут як селен та сірка, тому що до їхнього складу вже входять ці елементи. Відомий спосіб одержання кластерних халькогенгалогенідів ренію [Миронов Ю.В., Федоров В.Е. Четырехатомные кластерные халькогенгалогенидные комплексы рения с кубановым ядром. Синтез, строение и свойства. // Изв. АН. Серия хим. - 2002. - № 4. - С. 529-539] полягає у тому, що суміш ренію (V) галогеніду і елементарних халькогенів нагрівають при 350-550 °C у кварцовій ампулі упродовж двох годин та охолоджують до кімнатної температури. Недоліками цього аналога є: - по-перше, проведення твердофазного синтезу при досить високій температурі (до 550 °C) (в 2,5 рази вищій, ніж у запропоновану способі), і, як наслідок, - значно більші енергетичні витрати; - по-друге, неможливість отримати продукт синтезу у чистому вигляді (без елементарних халькогенів як другої фази) навіть при збільшенні часу реакції, що обумовлює непридатність даного продукту синтезу як об'єкта для подальших досліджень. Найближчим за технічною суттю аналогом до заявленої корисної моделі - прототипом є спосіб отримання триядерних кластерних тіоселенохлоридів ренію [Рыбаков В.Б., Янко О.Г., Асланов Л.А., Фокина З.А., Пехньо В.И., Волков С.В. Синтез и структура смешаных тиоселенохлоридных треугольных кластеров рения. // Коорд. химия. - 2000, - Т. 26, № 7. - С. 516-520], який полягає у тому, що у скляний реактор Г-подібної форми завантажують реній(VII) оксид Re2O7 і розчини селену (22 %) в монохлориді сірки S2Cl2 та сірки (18 %) в монохлориді селену Se2Cl2 при мольному співвідношенні вихідних реагентів 1:5:5-1:7:7. Суміш нагрівають при температурі 80-90 °C упродовж 80 годин у відкритому реакторі до повного виділення газоподібних продуктів реакції та в муфельній печі при 200 °C упродовж 100 годин, рідку фазу охолоджують до кімнатної температури, переливають у вільне коліно реактора, заморожують у зрідженому азоті, відокремлюють твердий продукт, відмивають його тетрахлорметаном ССl4, висушують у вакуумі. Причинами, що перешкоджають досягненню очікуваного результату при використанні найближчого аналога, є: - по-перше, проведення рідкофазного синтезу при мольному співвідношенні вихідних компонентів 1:5:5-1:7:7, що є занадто малим, якщо галогенід халькогену використовують не лише як середовище синтезу, але і як вихідний реагент, що призводить до одержання продукту з нижчим виходом та нижчим ступенем чистоти і потребує додаткової його очистки: - по-друге, використання розчинів селену в монохлориді сірки та сірки в монохлориді селену, що також призводить до одержання продукту з нижчим ступенем чистоти; - по-третє, нагрівання реакційної суміші у відкритому реакторі при 80-90 °C упродовж 80 годин та у запаяному реакторі при 200 °C упродовж 100 годин недостатньо для утворення чотириядерних кластерів ренію внаслідок нетривалого часу синтезу. В основу корисної моделі поставлено задачу одержання нової індивідуальної хімічної сполуки Re4Se4S4Br16 з установленою структурою, яка є чотириядерним кластерним комплексом, шляхом використання нових вихідних реагентів та умов синтезу, що дасть змогу одержати як технічний результат чисту речовину заданого складу і структури з високим виходом, яка проявляє каталітичні властивості, може проявляти напівпровідникові властивості і бути придатною як хімічний реактив і препарат. Поставлена задача вирішується так, що у способі одержання чотириядерного кластерного селеносульфідоброміду ренію Re4Se4S4Br16 синтез відбувається за наступною схемою: Re2O7+S2Br2+Se2Br2 → Re4Se4S4Br16↓+SО2↑+S. 1 UA 111360 U 5 10 15 20 25 30 35 40 45 50 55 60 Як вихідні реагенти використовують реній (VII) оксид Re2O7, монооромід сірки S2Br2 та монобромід селену Se2Br2 у мольному співвідношенні вихідних реагентів 1:8:6-1:12:8; безперервне нагрівання реакційної суміші проводять у нижній частині відкритого реактора на водяній бані при температурі 95-100 °C упродовж 90-100 годин, а потім по всьому об'єму запаяного реактора у муфельній шафі при 200 °C упродовж 150-180 годин; реактор охолоджують до кімнатної температури, переливають у вільне коліно реактора рідку фазу та заморожують її у зрідженому азоті; відмивають тверду фазу тетрахлорметаном ССl4, висушують у вакуумі. Суттєвими відмінностями від прототипу є збільшення мольного співвідношення вихідних реагентів до 1:8:6-1:12:8; заміна розчинів селену в монохлориді сірки та сірки в монохлориді селену на чисті монобромід сірки S2Br2 та монобромід селену Se2Br2; збільшення часу нагрівання реакційної суміші у нижній частині реактора (до 90-100 годин) на водяній бані при більш високій температурі (95-100 °C); та збільшення часу нагрівання реакційної суміші у муфельній шафі при 200 °C до 150-180 год. Одержують чистий, однофазний продукт синтезу - селеносульфідобромід ренію структурної формули Re4(μ3-S)4(SeBr2)4Br8. Корисна модель детальніше пояснюється кресленнями та конкретними прикладами. Фіг. 1. Експериментальна (кільця), теоретична (cуцільна, лінія) та різницева (унизу) дифрактограми селеносульфiдоброміду ренію Re4Se4S4Br16, разом із відмітками брегівських рефлексії: (вертикальні риски). Фіг. 2. Молекулярна структура селеносульфідоброміду ренію Re4Se4S4Br16 із виділеним тетраедром Re4. Фіг. 3. Загальна та орбітально-проектована густина станів (DOS) в сполуці Rе4Sе4S4Вr16 для примітивної комірки (28 атомів). Нуль шкали енергій відповідає розрахованому рівню Фермі (ЕF). Фіг. 4. Схема гідрування μ-нітробензойної кислоти в μ-амінобензойну кислоту з використанням як каталізатора Re4Se4S4Br16 (а) та вихід цільового продукту в залежності від середовища проведення реакції (б). Методи фізико-хімічного дослідження, що застосовують. Елементний склад сполуки Re4Se4S4Br16 встановлюють методом рентгенофлюоресцентної спектроскопії на спектрометрі "ЕlvaX Light" фірми Elva. Спектр комбінаційного розсіювання світла (КРС) записують у геометрії відбивання при кімнатній температурі за допомогою раманівського спектрометра "Т-64000" фірми Horiba JobinYvon, оснащеного охолоджуваним CCD детектором. Для збудження використовують лінію Аr-Кr іонного лазера з довжиною хвилі λ=514,5 нм, сфокусовану на зразку у пляму діаметрам ~ 1 мкм при потужності випромінювання близько 0,1 мВт. Масиви експериментальних інтенсивностей та кутів відбиті від досліджуваних зразків отримують на автоматичному дифрактометрі "STOE STADI Р" фірми STOE & Сіє GmbH [STOE WinXPOW, version 3.03. Darmstadt: Stoe & Сіє GmbH, 2010] з лінійним позиційно-прецизійним детектором PSD за схемою модифікованої геометрії Гіньє, метод на проходження (СuKα1випромінювання (λ=0,15406 нм); увігнутий Ge-монохроматор (111) типу Іоганна; 2θ/ωсканування, інтервал кутів 2θ 6,0002θ110,025°2θ з кроком 0,015°2θ; крок детектора 0,480°2θ, час сканування в кроці 300 с, температура при зйомці Т=25,00,1 °C, U=40 кВ, J=35 мА). Експериментальні лінійні коефіцієнти поглинання визначають шляхом логарифмічного відношення інтенсивності первинного променя до інтенсивності первинного променя після проходження крізь фоновий та робочий зразки. Кристалічну структуру сполуки розшифровують прямими методами за допомогою програми ЕХРО2013 [Altomare A., Cuocci C., Giacovazzo С., Moliternі A., Rizzi R., Corriero N., Falcicchio A. EXPO2013: a kit of tools for phasing crystal structures from powder data // J. Appl. Crystallogr. - 2013. Vol. 46, Pt. 4. - P. 1231-1235], уточнюють в ізотропному наближенні для параметрів зміщення атомів методом Рітвельда з використанням функції профілю pseudoVoigt за допомогою програми FullProf.2k (версія 5.60) [Rodriguez-Carvajal J. Recent developments of the program FULLPROF // Commission on Powder Diffraction (IUCr). Newslett. - 2001. - Vol. 26. P. 12-19], та візуалізують програмою DIAMOND [Brandenburg K. DIAMOND. Visual Crystal Structure Information System, Version 3.2g. Bonn: Crystal Impact, 2011]. Квантово-хімічні розрахунки електронної структури сполуки на основі структурних експериментальних даних проводять у рамках теорії функціонала густини (DFT) у наближенні повнопотенціального методу лінеаризованих приєднаних плоских хвиль (FP-LAPW) із узагальненою градієнтною апроксимацією (GGA) електронної густини обмінно-кореляційного функціонала PBEsol [Perdew J.P., Ruzsinszky A., Csonka G.I., Vydrov О.A., Scuseria G.E., Constantin L.A., Zhou X., Burke K. Restoring the density-gradient expansion for exchange in solids 2 UA 111360 U 5 10 15 20 25 30 35 40 45 and surfaces // Phys. Rev. Lett. - 2008. Vol. 100, Is. 13. - P. 136406-1-136406-4], із використанням програмного коду Elk [The Elk FP-LAPW Code (version 3.1.12); http://elk.sourceforge.net/]. Інтегрування зони Бріллюена у незвідній частині проводять сіткою 7×7×7 (88 k-точок), обмеження енергії для плоских хвиль становить 213 еВ, критерій збіжності для загальної енергії - 0,003 eВ. Як середовище для проведення процесу гідрування м-нітробензойної кислоти (м-НБК) в мамінобензойну (м-АБК) використовують воду або 5, 10, 20 % розчини соляної чи бромідної кислот. 0,1 г м-НБК розчиняють в 50 мл розчину, додають 0,1 г селеносульфідоброміду ренію Re4Se4S4Br16, нагрівають реакційну суміш до 80 °C, пропускають через неї водень при атмосферному тиску та постійному перемішуванні упродовж 2,5 годин. Після закінчення процесу гідрування каталізатор відділяють декантацією, розчин випарюють до сухих солей на водяній бані. Солі відмітають ацетоном від залишків (м-АБК), а по кількості утворених в процесі гідролізу солей м-АБКННаl (Hal: Сl, Вr) визначають ступінь перетворення м-НБК в, м-АБК. Приклад одержання чотириядерного кластерного селеносульфідоброміду ренію Re4Se4S4Br16. Як вихідні компоненти використовують реній(VІІ) оксид Re2O7, який синтезують відповідно до [Руководство по неорганическому синтезу: в 6 т. Т.2 / Под ред. Г. Брауэра. Пер. с нем. - М: Мир, 1985. - Т. 2. -338 с.], та моноброміди селену Se2Br2 та сірки S2Br2, які синтезують взаємодією стехіометричних кількостей елементарного селену (Se), селену (IV) оксиду (SeO2), елементарної сірки (S), сірки (IV) оксиду (SO2) та бромідної кислоти (НВr) шляхом поступового додавання концентрованої сульфатної кислоти (H2SO4) відповідно до реакцій: 3Se+SeO2+4HBr=2Se2Br2+2H2O S+SO2+4HBr=2S2Br2+2H2O. У Г-подібний скляний реактор із однією запаяною стороною поміщають 1 г Re2O7, 2 мл S;Br2 і 1 мл Se2Br2 (мольне співвідношення 1:11,2:5,4), безперервно нагрівають реакційну суміш спочатку у нижній частині відкритого реактора на водяній бані при температурі 100 °C упродовж 85 годин, а потім по всьому об'єму запаяного реактора у муфельній шафі при 200 °C упродовж 150 годин, охолоджують до кімнатної температури, переливають у вільне коліно реактора рідку фазу (S2Br2 і Se2Br2, що не прореагували, та інші нецільові продукти реакції) та заморожують у зрідженому азоті, відокремлюють твердий продукт, відмивають його тетрахлорметаном ССl4, висушують у вакуумі. Продукт синтезу - селеносульфідобромід ренію брутто-формули Re4Se4S4Br16 - кристалічний порошок сірувато-чорного кольору і складу (мас. %): Re - 32,28, Se - 8,86, S - 9,09, Br - 49,77. Теоретично розраховано (мас. %): Re - 30,19, Se - 12,80, S - 5,20, Br - 51,81. Вихід продукту 90 %. Чистота продукту підтверджена спектроскопічними та рентгендифракційними методами. Результати експерименту наведені у табл. 1-3 та представлені на Фіг. 1-4. Одержані дані підтверджують індивідуальність сполуки Re4Se4S4Br16. За результатами РСА (табл. 1-2, Фіг. 1) отриманий селеносульфідобромід ренію Re4Se4S4Br16 - чотириядерний кластерний комплекс будови Re4(μ3-S)4(SeBr2)4Br8 (Фіг. 2). Його основним структурним блоком є кубанове кластерне ядро Re4 з одинарними зв'язками Re-Re 2,698-2,738 Å (табл. 3). Кожна трикутна грань тетраедра Re4 координована містковими μ3-Sлігандами при довжині зв'язків Re-S 2,240-2,332 Å. Квантово-хімічні розрахунки електронної структури Re4Se4S4Br16 показали, що сполука є напівпровідником (Фіг. 3). Рівень Фермі розташований ближче до дна зони провідності, а ширина забороненої зони складає 1,47 еВ, що відповідає довжині фотона λ=844 нм і сіруваточорному кольору сполуки. Для наведеного інтервалу енергій домінуючий вклад в загальну густину станів у валентній зоні дають 4р-електрони брому, гібридизовані з 5d - електронами ренію і 4p - електронами селену, а в області 5 еВ - 3p - електрони сірки, гібридизовані з 5d електронами ренію, тоді як у зоні провідності переважаючою є 5d - зона ренію. 50 3 UA 111360 U Таблиця 1 Деталі експерименту та кристалографічні дані для Re4Se4S4Br16 Re4Se4S4Br16 /тетрареній тетраселен тетрасульфур гексадекабромід Формула / назва Просторова група - послідовність Вайкоффа / символ Пірсона Структурний тип Mr/Z Параметри елементарної комірки а, с (Å) 3 Об'єм комірки V(Å ) 3 Розрахована густина Dx (г/см ) -1 Коефіцієнт поглинання μ (СuKа) (мм ) Кількість виміряних рефлексів Кількість параметрів уточнення Параметри профілю η0, U, V, W Параметри асиметрії As1, As2 Нульове значення 2θ (°) Фактори достовірності: 7 І-4 (№ 82)-g /tI56 Re4Te4S4Cl16 2467,4/2 10,96292(12), 13,22261(16) 1589,17(3) 5156 60,35 545 38 0,545(5), 0,0598(18), -0,0358(12), 0,0173(2) 0,074(1), 0,0210(3) -0,0043(4) R1 Iobs Icalc / Iobs 0,0340 RF Fobs Fcalc / Fobs 0,0297 Rp yi yc,i / y i 0,0470 1/ 2 2 R wp wi yi yc,i / wi yi2 Rexp n p / wi yi2 0,0615 1/ 2 0,0310 2 Rwp / Rexp 2 3,94 Таблиця 2 Правильна система точок (ПСT), координати (х, у, z) та ізотропні параметри зміщення атомів (Biso) у структурі сполуки Re4Se4S4Br16 Атом Re Se S Br1 Br2 Вr3 Br4 ПСТ 8g 8g 8g 8g 8g 8g 8g x 0,02933(18} 0,2008(4) 0,4534(13) 0,0469(5) 0,1624(4) 0,2272(4) 0,3748(4) у 0,11952(17) 0,2810(5) 0,3402(9) 0,1494(4) 0,4408(4) 0,1198(5) 0,1779(3) Примітка. Нумерація атомів відповідає: Фіг. 2. 4 z 0,42574(14) 0,3730(3) 0,0953(8) 0,2326(3) 0,0879(4) 0,0165(3) 0,3205(3) 2 Biso(Å ) 0,64(4) 1,15(13) 2,3(3) 1,29(12) 1,96(15) 2,36(13) 1,73(11) UA 111360 U Таблиця 3 Міжатомні відстані (δ) та валентні кути (ω) у структурі сполуки Re4Se4S4Br16 Зв'язок Re-1S Re-1S Re-1S Re-1Br1 2,582(4) Re-1Br2 Re-1Se Re-1Re 2,587(5) 2,675(5) 2,698(3) Re-2Re 2,738(3) Se-1Br4 Se-1Br3 5 δ(Å) 2,240(14) 2,293(11) 2,332(12) 2,323(6) 2,325(6) ω (°) Re-Re-Re Re-Re-Re Re-Re-Se Re-Re-S Re-Re-S Re-Re-S Re-Re-Br1 Re-Re-Br2 Re-Re-Re Re-Re-Se Re-Re-S Re-Re-S Re-Re-S Re-Re-Br1 Re-Re-Br2 Re-Re-Se Re-Re-S Re-Re-S Re-Re-S Re-Re-Br1 Re-Re-Br2 ω (°) 60,48(10) 59,04(10) 109,1(2) 102,2(6) 52,0(4) 53,0(4) 139,3(2) 137,4(2) 60,48(10) 144,1(3) 55,4(4) 101,9(5) 52,3(4) 98,11(19) 143,9(2) 147,7(2) 53,7(4) 54,4(4) 99,7(5) 143,1(2) 99,2(2) Se-Re-S Se-Re-S Se-Re-S Se-Re-Br1 Se-Re-Br2 S-Re-S S-Re-S S-Re-Br1 S-Re-Br2 S-Re-S S-Re-Br1 S-Re-Br2 S-Re-Br1 S-Re-Br2 Brl-Re-Br2 Re-Se-Br3 Re-Se-Br4 Br3-Se-Br4 Re-S-Re Re-S-Re Re-S-Re 148,7(7) 94,0(5) 93,1(5) 66,8(2) 68,5(2) 105,5(8) 105,9(9) 89,5(6) 88,5(5) 102,5(7) 159,5(6) 85,5(5) 86,3(5) 160,7(6) 80,9(2) 109,6(3) 109,4(3) 101,1(3) 72,6(4) 72,3(4) 74,3(4) Селеносульфідобромід ренію Re4Se4S4Br16 проявляє каталітичні властивості у процесі гідрування μ-нітробензойної кислоти в μ-амінобензойну кислоту (Фіг. 4). Найкращі результати отримано у 10 % водному розчині соляної кислоти НСl. Вихід цільового продукту складає 28 %. Перелічені переваги та наведені дані підтверджують отримання очікуваного технічного результату. ФОРМУЛА КОРИСНОЇ МОДЕЛІ 10 15 20 25 1. Спосіб одержання чотириядерного кластерного селеносульфідоброміду ренію Re4Se4S4Br16, за яким вихідні реагенти завантажують у реактор Г-подібної форми, реакційну суміш нагрівають спочатку у нижній частині відкритого реактора на водяній бані, потім у запаяному реакторі у муфельній шафі при 200 °C, охолоджують до кімнатної температури, рідку фазу переливають у вільне коліно реактора, заморожують у зрідженому азоті, відокремлюють твердий продукт, відмивають його тетрахлорметаном ССl4, висушують у вакуумі, який відрізняється тим, що як вихідні реагенти використовують реній(УП) оксид Re2O7, монобромід сірки S2Br2 та монобромід селену Se2Br2 у мольному співвідношенні 1:8:6-1:12:8, причому спочатку реакційну суміш безперервно нагрівають у нижній частині відкритого реактора на водяній бані при температурі 95-100 °C упродовж 90-100 годин, а потім по всьому об'єму запаяного реактора у муфельній шафі при 200 °C упродовж 150-180 годин. 2. Спосіб за п. 1, який відрізняється тим, що отримують комплекс Re4Se4S4Br16, який проявляє каталітичні властивості у процесі гідрування -нітробензойної кислоти в -амінобензойну кислоту, і придатний як компонент каталітичних систем, напівпровідника, хімічного реактиву і препарату. 5 UA 111360 U 6 UA 111360 U 7 UA 111360 U Комп’ютерна верстка Л. Литвиненко Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 8
ДивитисяДодаткова інформація
МПК / Мітки
МПК: B01J 23/36, C01G 47/00
Мітки: селеносульфідоброміду, спосіб, чотириядерного, re4se4s4br16, кластерного, одержання, ренію
Код посилання
<a href="https://ua.patents.su/10-111360-sposib-oderzhannya-chotiriyadernogo-klasternogo-selenosulfidobromidu-reniyu-re4se4s4br16.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання чотириядерного кластерного селеносульфідоброміду ренію re4se4s4br16</a>
Попередній патент: Спосіб діагностики розвитку остеопорозу
Наступний патент: Прокатна кліть
Випадковий патент: Пристрій для запису і/або зчитування інформації