Поліморфи 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(r)-амінопіперидин-1-іл)ксантину
Номер патенту: 97244
Опубліковано: 25.01.2012
Автори: Нікола Томас, Кеммер Дірк, Зігер Петер, Ренц Мартін, Кольбауер Петер
Формула / Реферат
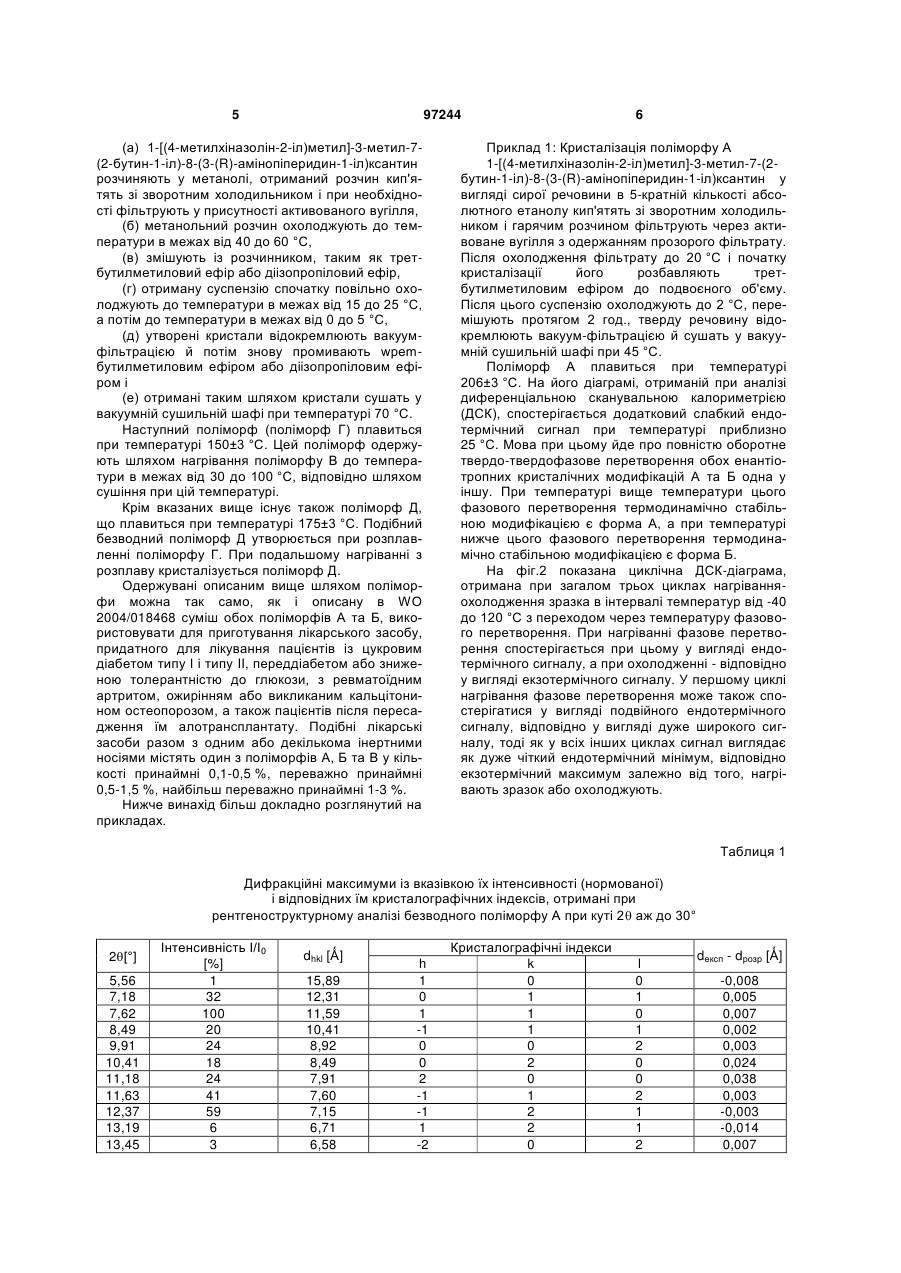
1. Безводний поліморф А 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину, який відрізняється тим, що він плавиться при температурі 206±3 °С.
2. Поліморф А за п. 1, який відрізняється тим, що на його рентгенівській порошковій дифрактограмі крім інших присутні характеристичні рефлекси, які відповідають значенням d, що дорівнюють 11,49 Ǻ, 7,60 Ǻ, 7,15 Ǻ, 3,86 Ǻ, 3,54 Ǻ і 3,47 Ǻ.
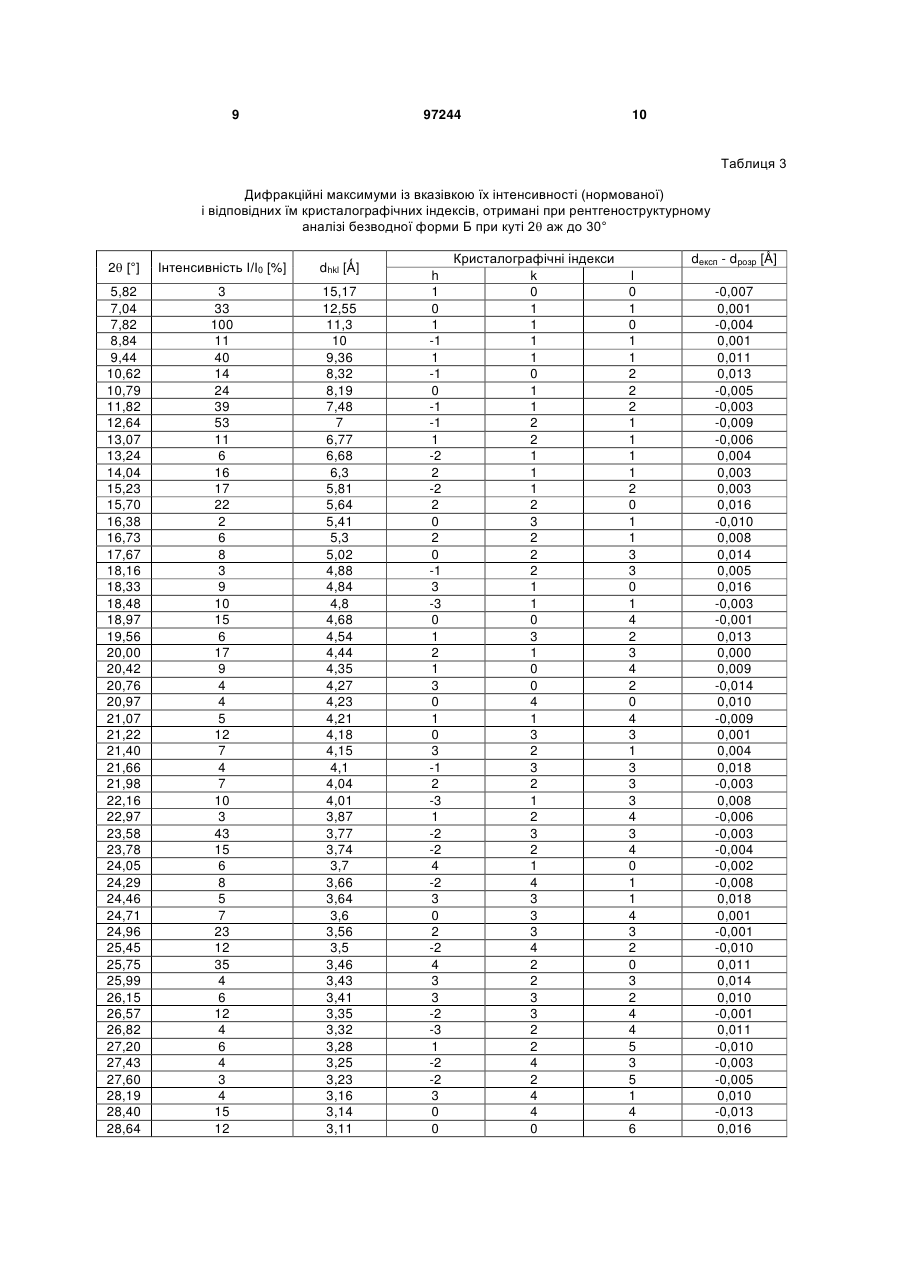
3. Безводний поліморф Б 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину, який відрізняється тим, що він при температурі в межах від 10 до 40 °С оборотно перетворюється в поліморф А за п. 1.
4. Поліморф Б за п. 3, який відрізняється тим, що на його рентгенівській порошковій дифрактограмі крім інших присутні характеристичні рефлекси, що відповідають значенням d, що дорівнюють 11,25 Ǻ, 9,32 Ǻ, 7,46 Ǻ, 6,98 Ǻ і 3,77 Ǻ.
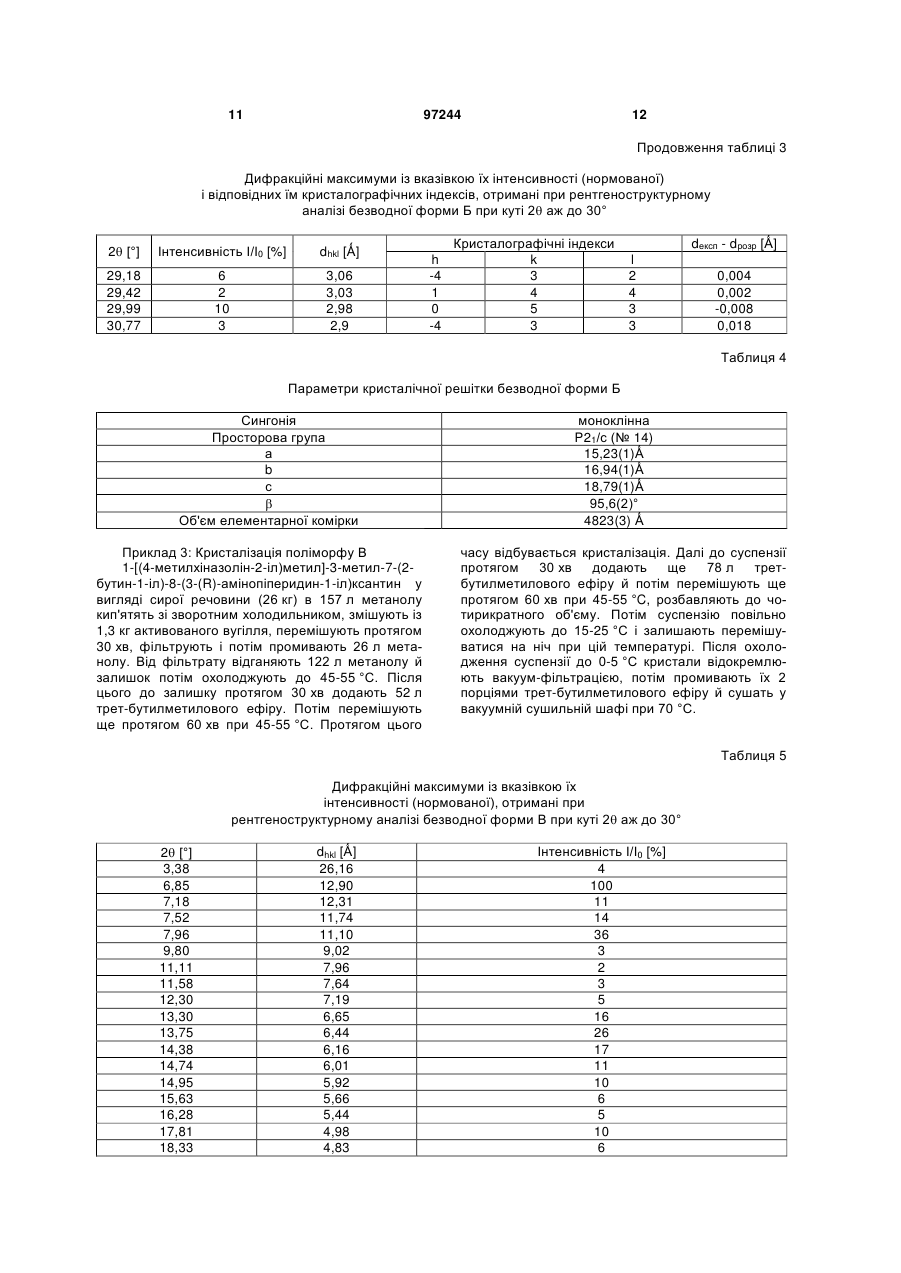
5. Поліморф В 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину, який відрізняється тим, що він при температурі в межах від 30 до 100 °С втрачає воду й на ДСК-діаграмі проявляє додаткові термічні ефекти при температурах приблизно 150 °С і 175 °С.
6. Поліморф В за п. 5, який відрізняється тим, що на його рентгенівській порошковій дифрактограмі крім інших присутні характеристичні рефлекси, які відповідають значенням d, що дорівнюють 12,90 Ǻ, 11,10 Ǻ, 6,44 Ǻ, 3,93 Ǻ і 3,74 Ǻ.
7. Спосіб одержання поліморфу В за п. 5, який відрізняється тим, що
(а) 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантин у метанолі кип'ятять зі зворотним холодильником,
(б) метанольний розчин охолоджують до температури в межах від 40 до 60 °С,
(в) змішують із розчинником, таким як трет-бутилметиловий ефір,
(г) отриману суспензію охолоджують спочатку до температури в межах від 15 до 25 °С, а потім до температури в межах від 0 до 5 °С,
(д) кристали відокремлюють вакуум-фільтрацією й
(є) сушать у вакуумі при температурі 70 °С.
8. Спосіб за п. 7, який відрізняється тим, що після завершення стадії (а) гарячий розчин фільтрують.
9. Лікарський засіб, який містить 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантин разом з одним або декількома інертними носіями й/або розріджувачами, який відрізняється тим, що він містить один з поліморфів А, Б та В у кількості принаймні 0,1-0,5 %.
10. Поліморф А за п. 2, на рентгенівській порошковій дифрактограмі якого по суті немає характеристичних рефлексів поліморфу Б за п. 4.
11. Поліморф Б за п. 4, на рентгенівській порошковій дифрактограмі якого по суті немає характеристичних рефлексів поліморфу А за п. 2.
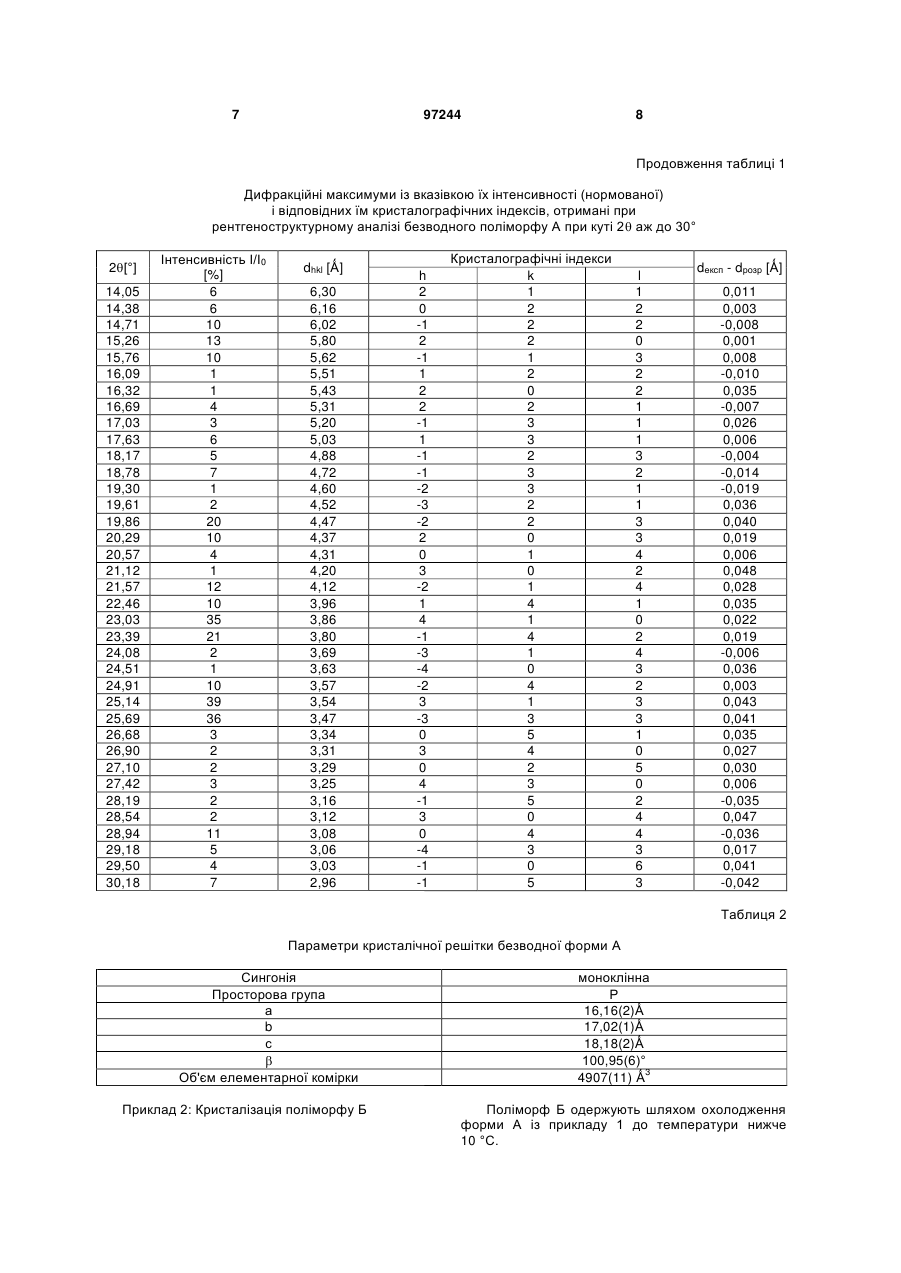
12. Безводний поліморф А 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину за п. 1, який відрізняється своїми параметрами кристалічної решітки
Сингонія
моноклінна
Просторова група
Р
a
16,16(2) Ǻ
b
17,02(1) Ǻ
c
18,18(2) Ǻ
β
100,95(6) °
Об’єм елементарної комірки
4907(11) Ǻ.
13. Безводний поліморф Б 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину за п. 3, який відрізняється своїми параметрами кристалічної решітки
Сингонія
моноклінна
Просторова група
Р21/с (№ 14)
a
15,23(1) Ǻ
b
16,94(1) Ǻ
c
18,79(1) Ǻ
β
95,6(2) °
Об’єм елементарної комірки
4823(3) Ǻ.
14. Поліморф А за п. 1, який відрізняється тим, що він по суті не містить поліморфу Б за п. 3.
15. Поліморф Б за п. 3, який відрізняється тим, що він по суті не містить поліморфу А за п. 1.
16. Застосування поліморфу А за п. 1 або 2 для одержання лікарського засобу.
17. Застосування поліморфу Б за п. 3 або 4 для одержання лікарського засобу.
Текст
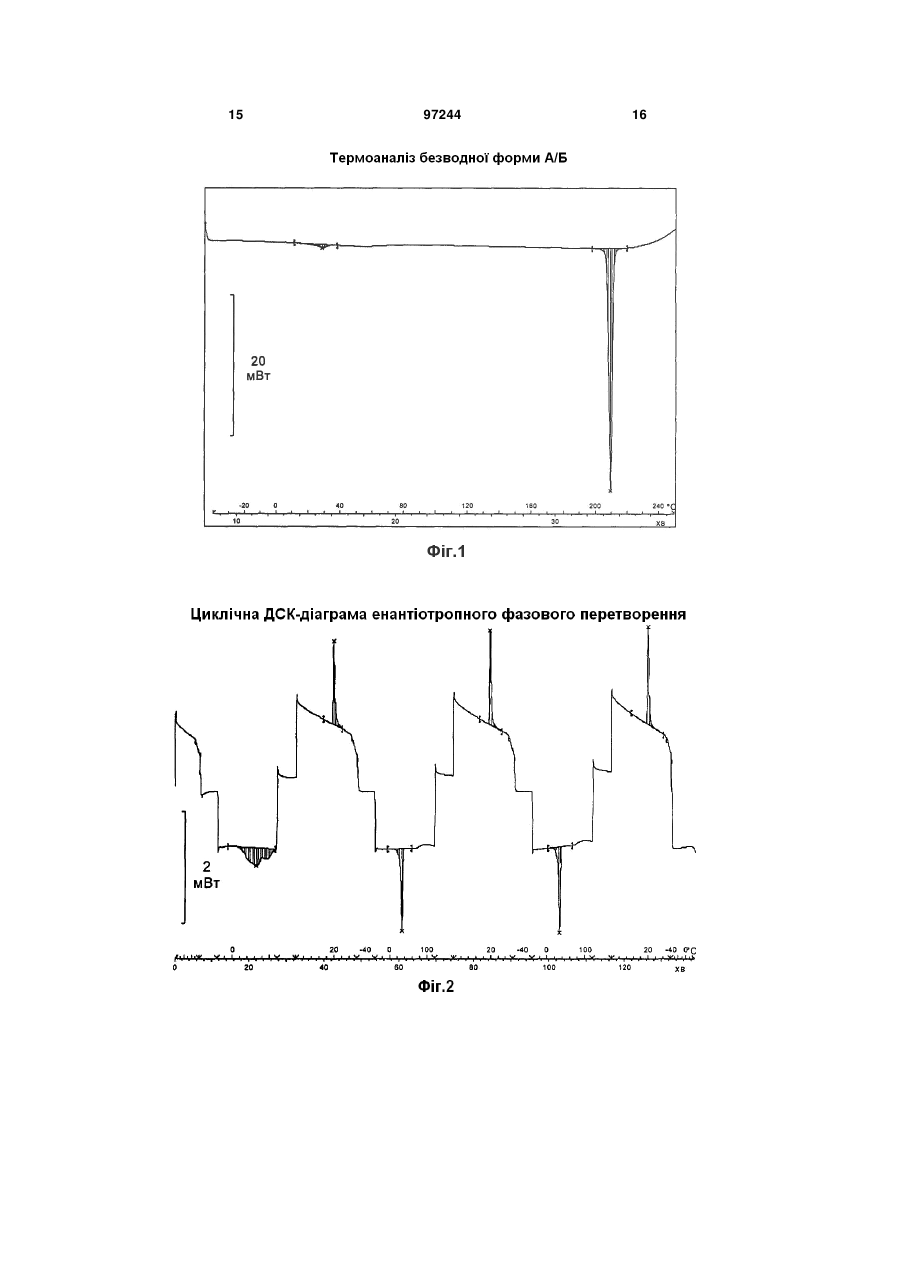
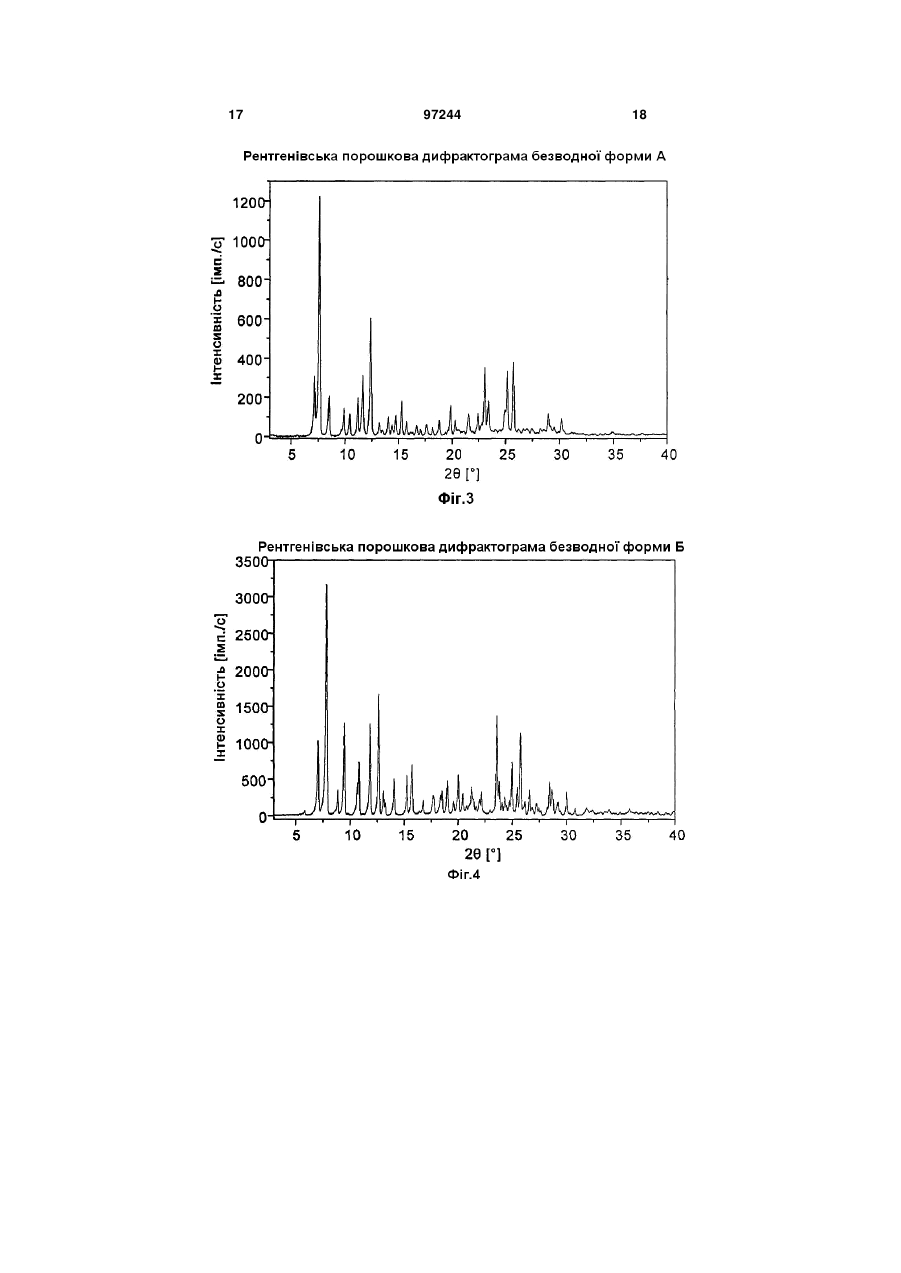
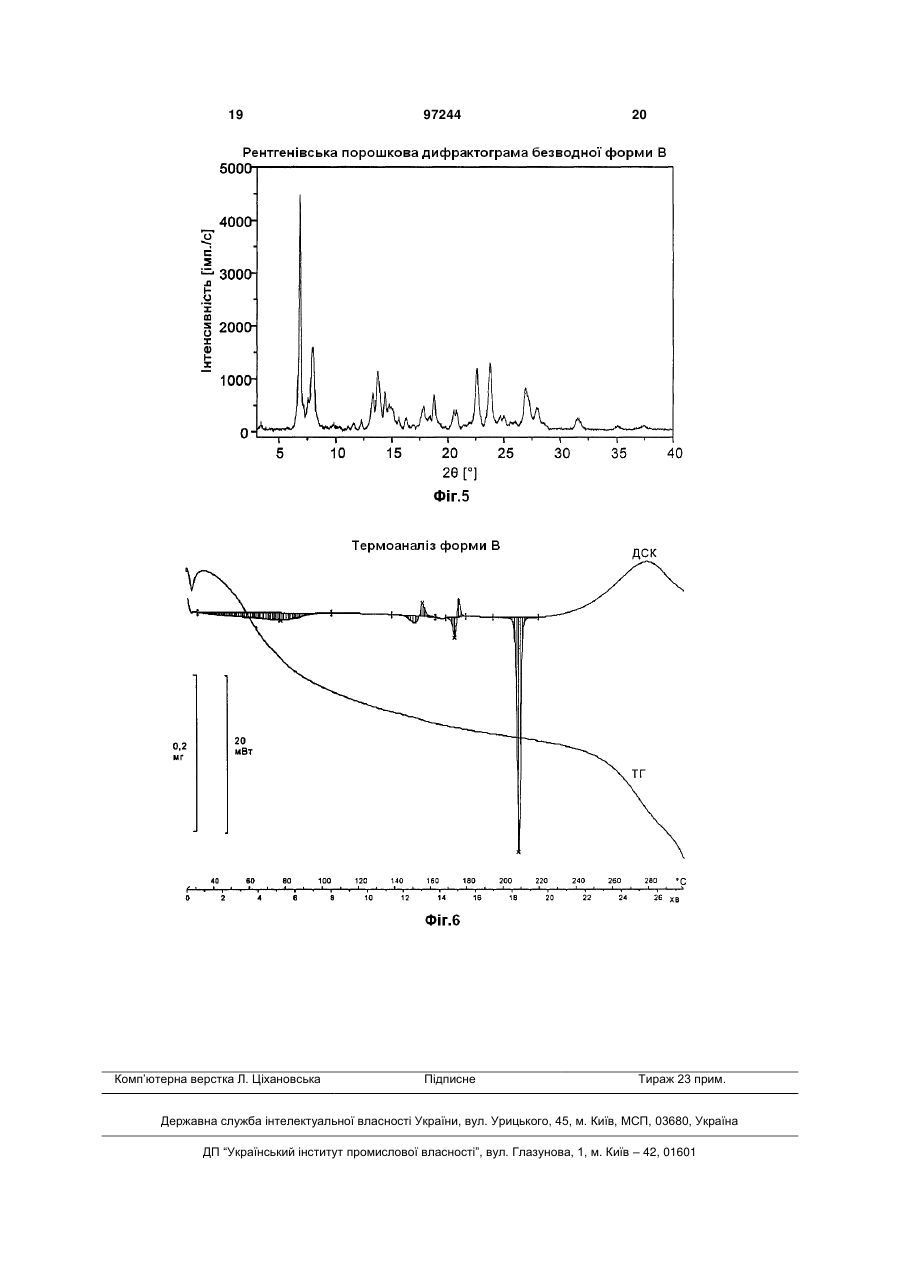
1. Безводний поліморф А 1-[(4метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1іл)-8-(3-(R)-амінопіперидин-1-іл)ксантину, який відрізняється тим, що він плавиться при температурі 206±3 °С. 2. Поліморф А за п. 1, який відрізняється тим, що на його рентгенівській порошковій дифрактограмі крім інших присутні характеристичні рефлекси, які відповідають значенням d, що дорівнюють 11,49 Ǻ, 7,60 Ǻ, 7,15 Ǻ, 3,86 Ǻ, 3,54 Ǻ і 3,47 Ǻ. 3. Безводний поліморф Б 1-[(4-метилхіназолін-2іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)амінопіперидин-1-іл)ксантину, який відрізняється тим, що він при температурі в межах від 10 до 40 °С оборотно перетворюється в поліморф А за п. 1. 4. Поліморф Б за п. 3, який відрізняється тим, що на його рентгенівській порошковій дифрактограмі крім інших присутні характеристичні рефлекси, що відповідають значенням d, що дорівнюють 11,25 Ǻ, 9,32 Ǻ, 7,46 Ǻ, 6,98 Ǻ і 3,77 Ǻ. 5. Поліморф В 1-[(4-метилхіназолін-2-іл)метил]-3метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1іл)ксантину, який відрізняється тим, що він при 2 (19) 1 3 Сингонія Просторова група a b c β Об’єм елементарної комірки 97244 моноклінна Р 16,16(2) Ǻ 17,02(1) Ǻ 18,18(2) Ǻ 100,95(6) ° 4907(11) Ǻ. 13. Безводний поліморф Б 1-[(4-метилхіназолін-2іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(R)амінопіперидин-1-іл)ксантину за п. 3, який відрізняється своїми параметрами кристалічної решітки Сингонія Просторова група моноклінна Р21/с (№ 14) Даний винахід стосується поліморфних кристалічних модифікацій інгібітора DPP-IV, їх одержання й їх застосування для приготування лікарського засобу. Фермент DPPIV (дипептидилпептидаза IV), відомий також за назвою CD26, представляє собою серинпротеазу, яка сприяє відщепленню дипептидів у білків із проліновим або аланіновим залишком на N-кінці. Тим самим інгібітори DPP IV впливають на рівень біоактивних пептидів, включаючи пептид GLP-1, у плазмі крові. Сполуки цього типу становлять інтерес як діючі речовини для профілактики або лікування захворювань або патологічних станів, які взаємозв'язані з підвищеною активністю ферменту DPPIV або які можна попередити або полегшити шляхом зниження активності ферменту DPPIV, насамперед цукрового діабету типу І або типу II, переддіабету або зниженої толерантності до глюкози. В публікації WO 2004/018468 описані інгібітори DPPIV з цінними фармакологічними властивостями. Як приклад описаних у цій публікації інгібіторів можна назвати 1-[(4-метилхіназолін-2-іл)метил]-3метил-7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1іл)ксантин. При створенні даного винаходу було встановлено, що 1-[(4-метилхіназолін-2-іл)метил]-3-метил7-(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1іл)ксантин може існувати в різних поліморфних кристалічних модифікаціях і що описана в WO 2004/018468 сполука при кімнатній температурі представлена у вигляді суміші двох енантіотропних поліморфів. Температура, при якій відбувається перетворення обох поліморфів один у інший, становить 25±15 °C (див. Фіг.1 і 2). Високотемпературна форма (поліморф А), яку можна одержати шляхом нагрівання суміші до температури понад 40 °C, плавиться при температурі 206±3 °C. На рентгенівській порошковій дифрактограмі цієї форми (див. фіг.3) присутні характеристичні рефлекси (дифракційні максимуми), що відповідають значенням d, що дорівнюють 11,49 Ǻ, 7,60 Ǻ, 7,15 Ǻ, 3,86 Ǻ, 3,54 Ǻ і 3,47 Ǻ (див. також таблиці 1 і 2). 4 a b c β Об’єм елементарної комірки 15,23(1) Ǻ 16,94(1) Ǻ 18,79(1) Ǻ 95,6(2) ° 4823(3) Ǻ. 14. Поліморф А за п. 1, який відрізняється тим, що він по суті не містить поліморфу Б за п. 3. 15. Поліморф Б за п. 3, який відрізняється тим, що він по суті не містить поліморфу А за п. 1. 16. Застосування поліморфу А за п. 1 або 2 для одержання лікарського засобу. 17. Застосування поліморфу Б за п. 3 або 4 для одержання лікарського засобу. Безводний поліморф А можна одержувати способом, при здійсненні якого (а) 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7(2-бутин-1-іл)-8-(3-(R) амінопіперидин-1-іл)ксантин в абсолютному етанолі кип'ятять зі зворотним холодильником і при необхідності фільтрують, (б) гарячий розчин, відповідно гарячий фільтрат охолоджують до початку кристалізації, (в) розбавляють розчинником, таким як третбутилметиловий ефір, (г) суміш розчинників відокремлюють шляхом вакуум-фільтрації й (д) поліморф А сушать у вакуумі при 45 °C. Низькотемпературну форму (поліморф Б) одержують шляхом охолодження суміші до температури нижче 10 °C. На рентгенівській порошковій дифрактограмі цієї форми (див. фіг.4) присутні характеристичні рефлекси, які відповідають значенням d, що дорівнюють 11,25 Ǻ, 9,32 Ǻ, 7,46 Ǻ, 6,98 Ǻ і 3,77 Ǻ (див. також таблиці 3 і 4). Безводний поліморф Б можна одержувати способом, при здійсненні якого (а) 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантин розчиняють в абсолютному етанолі, отриманий розчин кип'ятять зі зворотним холодильником і при необхідності фільтрують, (б) для кристалізації гарячий розчин, відповідно гарячий фільтрат охолоджують до температури 10 °C, (в) розбавляють розчинником, таким як третбутилметиловий ефір, (г) суміш розчинників відокремлюють шляхом вакуум-фільтрації й (д) поліморф Б сушать у вакуумі при температурі нижче 10 °C. Крім цього існує ще один поліморф (поліморф В), на рентгенівській порошковій дифрактограмі якого (див. фіг.5) присутні характеристичні рефлекси, що відповідають значенням d, що дорівнюють 12,90 Ǻ, 11,10 Ǻ, 6,44 Ǻ, 3,93 Ǻ і 3,74 Ǻ (див. також таблицю 5). Поліморф В одержують способом, при здійсненні якого 5 97244 (а) 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7(2-бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантин розчиняють у метанолі, отриманий розчин кип'ятять зі зворотним холодильником і при необхідності фільтрують у присутності активованого вугілля, (б) метанольний розчин охолоджують до температури в межах від 40 до 60 °C, (в) змішують із розчинником, таким як третбутилметиловий ефір або діізопропіловий ефір, (г) отриману суспензію спочатку повільно охолоджують до температури в межах від 15 до 25 °C, а потім до температури в межах від 0 до 5 °C, (д) утворені кристали відокремлюють вакуумфільтрацією й потім знову промивають wpemбутилметиловим ефіром або діізопропіловим ефіром і (e) отримані таким шляхом кристали сушать у вакуумній сушильній шафі при температурі 70 °C. Наступний поліморф (поліморф Г) плавиться при температурі 150±3 °C. Цей поліморф одержують шляхом нагрівання поліморфу В до температури в межах від 30 до 100 °C, відповідно шляхом сушіння при цій температурі. Крім вказаних вище існує також поліморф Д, що плавиться при температурі 175±3 °C. Подібний безводний поліморф Д утворюється при розплавленні поліморфу Г. При подальшому нагріванні з розплаву кристалізується поліморф Д. Одержувані описаним вище шляхом поліморфи можна так само, як і описану в WO 2004/018468 суміш обох поліморфів А та Б, використовувати для приготування лікарського засобу, придатного для лікування пацієнтів із цукровим діабетом типу І і типу II, переддіабетом або зниженою толерантністю до глюкози, з ревматоїдним артритом, ожирінням або викликаним кальцітонином остеопорозом, а також пацієнтів після пересадження їм алотрансплантату. Подібні лікарські засоби разом з одним або декількома інертними носіями містять один з поліморфів А, Б та В у кількості принаймні 0,1-0,5 %, переважно принаймні 0,5-1,5 %, найбільш переважно принаймні 1-3 %. Нижче винахід більш докладно розглянутий на прикладах. 6 Приклад 1: Кристалізація поліморфу А 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантин у вигляді сирої речовини в 5-кратній кількості абсолютного етанолу кип'ятять зі зворотним холодильником і гарячим розчином фільтрують через активоване вугілля з одержанням прозорого фільтрату. Після охолодження фільтрату до 20 °C і початку кристалізації його розбавляють третбутилметиловим ефіром до подвоєного об'єму. Після цього суспензію охолоджують до 2 °C, перемішують протягом 2 год., тверду речовину відокремлюють вакуум-фільтрацією й сушать у вакуумній сушильній шафі при 45 °C. Поліморф А плавиться при температурі 206±3 °C. На його діаграмі, отриманій при аналізі диференціальною сканувальною калориметрією (ДСК), спостерігається додатковий слабкий ендотермічний сигнал при температурі приблизно 25 °C. Мова при цьому йде про повністю оборотне твердо-твердофазове перетворення обох енантіотропних кристалічних модифікацій А та Б одна у іншу. При температурі вище температури цього фазового перетворення термодинамічно стабільною модифікацією є форма А, а при температурі нижче цього фазового перетворення термодинамічно стабільною модифікацією є форма Б. На фіг.2 показана циклічна ДСК-діаграма, отримана при загалом трьох циклах нагріванняохолодження зразка в інтервалі температур від -40 до 120 °C з переходом через температуру фазового перетворення. При нагріванні фазове перетворення спостерігається при цьому у вигляді ендотермічного сигналу, а при охолодженні - відповідно у вигляді екзотермічного сигналу. У першому циклі нагрівання фазове перетворення може також спостерігатися у вигляді подвійного ендотермічного сигналу, відповідно у вигляді дуже широкого сигналу, тоді як у всіх інших циклах сигнал виглядає як дуже чіткий ендотермічний мінімум, відповідно екзотермічний максимум залежно від того, нагрівають зразок або охолоджують. Таблиця 1 Дифракційні максимуми із вказівкою їхінтенсивності (нормованої) і відповідних їм кристалографічних індексів, отримані при рентгеноструктурному аналізі безводного поліморфу А при куті 2 аж до 30° 2[°] 5,56 7,18 7,62 8,49 9,91 10,41 11,18 11,63 12,37 13,19 13,45 Інтенсивність І/І0 [%] 1 32 100 20 24 18 24 41 59 6 3 dhkl [Ǻ] 15,89 12,31 11,59 10,41 8,92 8,49 7,91 7,60 7,15 6,71 6,58 h 1 0 1 -1 0 0 2 -1 -1 1 -2 Кристалографічні індекси k 0 1 1 1 0 2 0 1 2 2 0 l 0 1 0 1 2 0 0 2 1 1 2 dексп - dрозр [Ǻ] -0,008 0,005 0,007 0,002 0,003 0,024 0,038 0,003 -0,003 -0,014 0,007 7 97244 8 Продовження таблиці 1 Дифракційні максимуми із вказівкою їх інтенсивності (нормованої) і відповідних їм кристалографічних індексів, отримані при рентгеноструктурному аналізі безводного поліморфу А при куті 2 аж до 30° 2[°] 14,05 14,38 14,71 15,26 15,76 16,09 16,32 16,69 17,03 17,63 18,17 18,78 19,30 19,61 19,86 20,29 20,57 21,12 21,57 22,46 23,03 23,39 24,08 24,51 24,91 25,14 25,69 26,68 26,90 27,10 27,42 28,19 28,54 28,94 29,18 29,50 30,18 Інтенсивність І/І0 [%] 6 6 10 13 10 1 1 4 3 6 5 7 1 2 20 10 4 1 12 10 35 21 2 1 10 39 36 3 2 2 3 2 2 11 5 4 7 dhkl [Ǻ] 6,30 6,16 6,02 5,80 5,62 5,51 5,43 5,31 5,20 5,03 4,88 4,72 4,60 4,52 4,47 4,37 4,31 4,20 4,12 3,96 3,86 3,80 3,69 3,63 3,57 3,54 3,47 3,34 3,31 3,29 3,25 3,16 3,12 3,08 3,06 3,03 2,96 h 2 0 -1 2 -1 1 2 2 -1 1 -1 -1 -2 -3 -2 2 0 3 -2 1 4 -1 -3 -4 -2 3 -3 0 3 0 4 -1 3 0 -4 -1 -1 Кристалографічні індекси k 1 2 2 2 1 2 0 2 3 3 2 3 3 2 2 0 1 0 1 4 1 4 1 0 4 1 3 5 4 2 3 5 0 4 3 0 5 l 1 2 2 0 3 2 2 1 1 1 3 2 1 1 3 3 4 2 4 1 0 2 4 3 2 3 3 1 0 5 0 2 4 4 3 6 3 dексп - dрозр [Ǻ] 0,011 0,003 -0,008 0,001 0,008 -0,010 0,035 -0,007 0,026 0,006 -0,004 -0,014 -0,019 0,036 0,040 0,019 0,006 0,048 0,028 0,035 0,022 0,019 -0,006 0,036 0,003 0,043 0,041 0,035 0,027 0,030 0,006 -0,035 0,047 -0,036 0,017 0,041 -0,042 Таблиця 2 Параметри кристалічної решітки безводної форми А Сингонія Просторова група а b с Об'єм елементарної комірки Приклад 2: Кристалізація поліморфу Б моноклінна Р 16,16(2)Ǻ 17,02(1)Ǻ 18,18(2)Ǻ 100,95(6)° 3 4907(11) Ǻ Поліморф Б одержують шляхом охолодження форми А із прикладу 1 до температури нижче 10 °C. 9 97244 10 Таблиця 3 Дифракційні максимуми із вказівкою їх інтенсивності (нормованої) і відповідних їм кристалографічних індексів, отримані при рентгеноструктурному аналізі безводної форми Б при куті 2 аж до 30° 2 [°] Інтенсивність І/І0 [%] dhkl [Ǻ] 5,82 7,04 7,82 8,84 9,44 10,62 10,79 11,82 12,64 13,07 13,24 14,04 15,23 15,70 16,38 16,73 17,67 18,16 18,33 18,48 18,97 19,56 20,00 20,42 20,76 20,97 21,07 21,22 21,40 21,66 21,98 22,16 22,97 23,58 23,78 24,05 24,29 24,46 24,71 24,96 25,45 25,75 25,99 26,15 26,57 26,82 27,20 27,43 27,60 28,19 28,40 28,64 3 33 100 11 40 14 24 39 53 11 6 16 17 22 2 6 8 3 9 10 15 6 17 9 4 4 5 12 7 4 7 10 3 43 15 6 8 5 7 23 12 35 4 6 12 4 6 4 3 4 15 12 15,17 12,55 11,3 10 9,36 8,32 8,19 7,48 7 6,77 6,68 6,3 5,81 5,64 5,41 5,3 5,02 4,88 4,84 4,8 4,68 4,54 4,44 4,35 4,27 4,23 4,21 4,18 4,15 4,1 4,04 4,01 3,87 3,77 3,74 3,7 3,66 3,64 3,6 3,56 3,5 3,46 3,43 3,41 3,35 3,32 3,28 3,25 3,23 3,16 3,14 3,11 h 1 0 1 -1 1 -1 0 -1 -1 1 -2 2 -2 2 0 2 0 -1 3 -3 0 1 2 1 3 0 1 0 3 -1 2 -3 1 -2 -2 4 -2 3 0 2 -2 4 3 3 -2 -3 1 -2 -2 3 0 0 Кристалографічні індекси k 0 1 1 1 1 0 1 1 2 2 1 1 1 2 3 2 2 2 1 1 0 3 1 0 0 4 1 3 2 3 2 1 2 3 2 1 4 3 3 3 4 2 2 3 3 2 2 4 2 4 4 0 dексп - dрозр [Ǻ] l 0 1 0 1 1 2 2 2 1 1 1 1 2 0 1 1 3 3 0 1 4 2 3 4 2 0 4 3 1 3 3 3 4 3 4 0 1 1 4 3 2 0 3 2 4 4 5 3 5 1 4 6 -0,007 0,001 -0,004 0,001 0,011 0,013 -0,005 -0,003 -0,009 -0,006 0,004 0,003 0,003 0,016 -0,010 0,008 0,014 0,005 0,016 -0,003 -0,001 0,013 0,000 0,009 -0,014 0,010 -0,009 0,001 0,004 0,018 -0,003 0,008 -0,006 -0,003 -0,004 -0,002 -0,008 0,018 0,001 -0,001 -0,010 0,011 0,014 0,010 -0,001 0,011 -0,010 -0,003 -0,005 0,010 -0,013 0,016 11 97244 12 Продовження таблиці 3 Дифракційні максимуми із вказівкою їх інтенсивності (нормованої) і відповідних їм кристалографічних індексів, отримані при рентгеноструктурному аналізі безводної форми Б при куті 2 аж до 30° 2 [°] Інтенсивність І/І0 [%] dhkl [Ǻ] 29,18 29,42 29,99 30,77 6 2 10 3 3,06 3,03 2,98 2,9 h -4 1 0 -4 Кристалографічні індекси k 3 4 5 3 dексп - dрозр [Ǻ] l 2 4 3 3 0,004 0,002 -0,008 0,018 Таблиця 4 Параметри кристалічної решітки безводної форми Б Сингонія Просторова група а b с Об'єм елементарної комірки Приклад 3: Кристалізація поліморфу В 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2бутин-1-іл)-8-(3-(R)-амінопіперидин-1-іл)ксантин у вигляді сирої речовини (26 кг) в 157 л метанолу кип'ятять зі зворотним холодильником, змішують із 1,3 кг активованого вугілля, перемішують протягом 30 хв, фільтрують і потім промивають 26 л метанолу. Від фільтрату відганяють 122 л метанолу й залишок потім охолоджують до 45-55 °C. Після цього до залишку протягом 30 хв додають 52 л трет-бутилметилового ефіру. Потім перемішують ще протягом 60 хв при 45-55 °C. Протягом цього моноклінна P21/c (№ 14) 15,23(1)Ǻ 16,94(1)Ǻ 18,79(1)Ǻ 95,6(2)° 4823(3) Ǻ часу відбувається кристалізація. Далі до суспензії протягом 30 хв додають ще 78 л третбутилметилового ефіру й потім перемішують ще протягом 60 хв при 45-55 °C, розбавляють до чотирикратного об'єму. Потім суспензію повільно охолоджують до 15-25 °C і залишають перемішуватися на ніч при цій температурі. Після охолодження суспензії до 0-5 °C кристали відокремлюють вакуум-фільтрацією, потім промивають їх 2 порціями трет-бутилметилового ефіру й сушать у вакуумній сушильній шафі при 70 °C. Таблиця 5 Дифракційні максимуми із вказівкою їх інтенсивності (нормованої), отримані при рентгеноструктурному аналізі безводної форми В при куті 2 аж до 30° 2 [°] 3,38 6,85 7,18 7,52 7,96 9,80 11,11 11,58 12,30 13,30 13,75 14,38 14,74 14,95 15,63 16,28 17,81 18,33 dhkl [Ǻ] 26,16 12,90 12,31 11,74 11,10 9,02 7,96 7,64 7,19 6,65 6,44 6,16 6,01 5,92 5,66 5,44 4,98 4,83 Інтенсивність І/І0 [%] 4 100 11 14 36 3 2 3 5 16 26 17 11 10 6 5 10 6 13 97244 14 Продовження таблиці 5 Дифракційні максимуми із вказівкою їх інтенсивності (нормованої), отримані при рентгеноструктурному аналізі безводної форми В при куті 2 аж до 30° 2 [°] 18,75 20,51 20,77 21,47 21,96 22,59 23,76 24,68 25,01 25,57 25,96 26,93 27,22 27,92 dhkl [Ǻ] 4,73 4,33 4,27 4,14 4,05 3,93 3,74 3,60 3,56 3,48 3,43 3,31 3,27 3,19 Приклад 4: Кристалізація поліморфу Г Поліморф Г одержують нагріванням поліморфу В із прикладу 3 до температури в межах від 30 до 100 °C, відповідно сушінням при цій температурі. Приклад 5: Кристалізація поліморфу Д Безводний поліморф Д утворюється при розплавлюванні поліморфу Г. При подальшому нагріванні з розплаву кристалізується поліморф Д. На ДСК-діаграмі форми В спостерігається цілий ряд сигналів. Найбільш сильний сигнал припадає на температуру приблизно 206 °C, що відповідає температурі плавлення безводної форми А, яка утворюється в ході ДСК-експерименту. Перед сигналом, що відповідає температурі плавлення, спостерігається цілий ряд інших ендотермічних і екзотермічних сигналів. Так, наприклад, дуже широкий і слабкий ендотермічний сигнал спостерігається в інтервалі температур від 30 до 100 °C, що корелює з основним зменшенням маси зразка при його термогравіметричному (ТГ) аналізі. При спільному дослідженні зразка термограві Інтенсивність І/І0 [%] 15 8 8 3 4 26 29 6 7 4 4 18 13 10 метрією і ІЧ-спектрометрією можна одержати інформацію про те, що в цьому інтервалі температур із зразка видаляється тільки вода. На рентгенівській порошковій дифрактограмі, отриманій для термостатованого при 100 °C зразка, присутні рефлекси, відмінні від таких, які отримані для вихідного матеріалу, звідки можна зробити висновок про те, що форма В представляє собою гідратну фазу зі стехіометрією десь в ділянці гемігідрату або моногідрату. Вказаний термостатований зразок представляє собою іншу безводну модифікацію Г, яка, однак, стабільна тільки в безводних умовах. Форма Г плавиться при температурі приблизно 150 °C. З її розплаву кристалізується ще одна безводна кристалічна модифікація Д, яка при подальшому нагріванні плавиться при температурі приблизно 175 °C. З розплаву форми Д у кінцевому підсумку кристалізується форма А. Форма Д також представляє собою метастабільну кристалічну модифікацію, яка утворюється тільки при високих температурах. 15 97244 16 17 97244 18 19 Комп’ютерна верстка Л. Ціхановська 97244 Підписне 20 Тираж 23 прим. Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюPolymorphs of 1-((4-methyfquinazolin-2-yl)methyl)-3-methyl-7- (2-butyn-1-yl)-8-(3-(r)-aminopiperidin-l-yl)xanthine
Автори англійськоюSieger Peter, Kemmer Dirk, Kohlbauer Peter, Nicola Thomas, Renz Martin
Назва патенту російськоюПолиморфы 1-[(4-метилхиназолин-2-ил)метил]-3-метил-7-(2-бутин-1-ил)-8-(3-(r)-аминопиперидин-1-ил)ксантина
Автори російськоюЗигер Петер, Кеммер Дирк, Кольбауэр Петер, Никола Томас, Ренц Мартин
МПК / Мітки
МПК: C07D 473/04, A61K 31/522, A61P 3/10
Мітки: поліморфи, 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(r)-амінопіперидин-1-іл)ксантину
Код посилання
<a href="https://ua.patents.su/10-97244-polimorfi-1-4-metilkhinazolin-2-ilmetil-3-metil-7-2-butin-1-il-8-3-r-aminopiperidin-1-ilksantinu.html" target="_blank" rel="follow" title="База патентів України">Поліморфи 1-[(4-метилхіназолін-2-іл)метил]-3-метил-7-(2-бутин-1-іл)-8-(3-(r)-амінопіперидин-1-іл)ксантину</a>
Попередній патент: Кристалічна безводна форма (форма а) n-гідрокси-3-[4-[[[2-(2-метил-1н-індол-3-іл)етил]аміно]метил]феніл]-2e-2-пропенаміду
Наступний патент: Аміноглікозидні антибіотики
Випадковий патент: Високовольтний багатоканальний комутатор