Гідрати та поліморфи 4-[[(7r)-8-циклопентил-7-етил-5,6,7,8-тетрагідро-5-метил-6-оксо-2-птеридиніл]аміно]-3-метокси-n-(1-метил-4-піперидиніл)бензаміду, спосіб їх одержання (варіанти) та їх застосування як лікарських засобів
Номер патенту: 87865
Опубліковано: 25.08.2009
Автори: Кремер Герд Ф., Шмід Рольф, Зігер Петер, Хертер Рольф, Ралль Вернер, Лінц Гюнтер, Хоффманн Маттіас
Формула / Реферат
1. Гідрат сполуки формули (І)
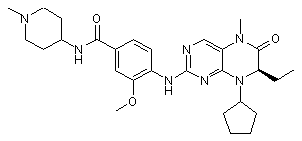 (I).
(I).
2. Гідрат сполуки формули (І) за п. 1, який відрізняється тим, що він являє собою моногідрат сполуки (І).
3. Гідрат сполуки формули (І) за п. 1, який відрізняється тим, що він являє собою тригідрат сполуки (І).
4. Ангідрат сполуки формули (І)
 (I).
(I).
5. Ангідрат за п. 4, який відрізняється тим, що він представлений у вигляді безводної форми І сполуки формули (І).
6. Ангідрат за п. 4, який відрізняється тим, що він представлений у вигляді безводної форми II сполуки формули (І).
7. Ангідрат за п. 4, який відрізняється тим, що він представлений у вигляді безводної форми III сполуки формули (І).
8. Фармацевтична композиція, яка відрізняється тим, що вона містить гідрат або ангідрат сполуки формули (І) за будь-яким з пп. 1, 2, відповідно за будь-яким з пп. 4-6, у терапевтично ефективній кількості та одну або декілька фармацевтично прийнятних допоміжних речовин.
9. Гідрат або ангідрат сполуки формули (І) за будь-яким з пп. 1, 2, відповідно за будь-яким з пп. 4-6, для застосування як лікарського засобу з антипроліферативною дією.
10. Спосіб одержання сполуки формули (І)
 , (I)
, (I)
який відрізняється тим, що сполуку формули 4
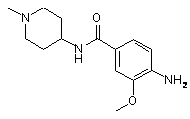 (4)
(4)
вводять у взаємодію зі сполукою формули 9
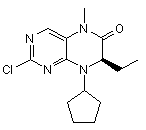 (9).
(9).
11. Спосіб одержання сполуки формули 9
 , (9)
, (9)
який відрізняється тим, що сполуку формули 8
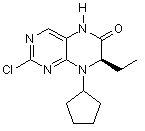 (8)
(8)
метилують диметилкарбонатом.
12. Сполука формули 3
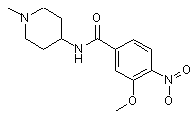 . (3)
. (3)
13. Сполука формули 4
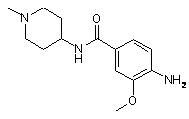 . (4)
. (4)
14. Спосіб одержання моногідрату сполуки формули (І) за п. 2, який полягає у тому, що
(а) приготовляють розчин сполуки формули (І) у суміші розчинників з 1-пропанолу або ізопропанолу та води,
(б) із суміші розчинників кристалізують моногідрат сполуки формули (І) та
(в) виділяють моногідрат сполуки формули (І).
15. Спосіб одержання моногідрату сполуки формули (І) за п. 14, де етап а) розчинення сполуки формули (І) проводять у суміші розчинників з 1-пропанолу та води.
16. Спосіб одержання безводної форми І сполуки формули (І) за п. 5, який полягає у тому, що
(а) приготовляють розчин сполуки формули (І) в етилацетаті та метил-трет-бутиловому ефірі,
(б) із суміші розчинників кристалізують безводну форму І сполуки формули (І) та
(в) виділяють безводну форму І сполуки формули (І).
17. Спосіб одержання безводної форми II сполуки формули (І) за п. 6, який полягає у тому, що
(а) приготовляють розчин сполуки формули (І) в етилацетаті,
(б) з етилацетату кристалізують безводну форму IІ сполуки формули (І) з наступним додаванням діетилового ефіру та
(в) виділяють безводну форму II сполуки формули (І).
Текст
1. Гідрат сполуки формули (І) C2 2 87865 1 3 N N Cl N 87865 4 N O (9). N O N H (4) NH2 O 11. Спосіб одержання сполуки формули 9 N N Cl N O (9) N , який відрізняється тим, що сполуку формули 8 H N N Cl N O (8) N метилують диметилкарбонатом. 12. Сполука формули 3 N O N H N O O (3) O . . 14. Спосіб одержання моногідрату сполуки формули (І) за п. 2, який полягає у тому, що (а) приготовляють розчин сполуки формули (І) у суміші розчинників з 1-пропанолу або ізопропанолу та води, (б) із суміші розчинників кристалізують моногідрат сполуки формули (І) та (в) виділяють моногідрат сполуки формули (І). 15. Спосіб одержання моногідрату сполуки формули (І) за п. 14, де етап а) розчинення сполуки формули (І) проводять у суміші розчинників з 1пропанолу та води. 16. Спосіб одержання безводної форми І сполуки формули (І) за п. 5, який полягає у тому, що (а) приготовляють розчин сполуки формули (І) в етилацетаті та метил-трет-бутиловому ефірі, (б) із суміші розчинників кристалізують безводну форму І сполуки формули (І) та (в) виділяють безводну форму І сполуки формули (І). 17. Спосіб одержання безводної форми II сполуки формули (І) за п. 6, який полягає у тому, що (а) приготовляють розчин сполуки формули (І) в етилацетаті, (б) з етилацетату кристалізують безводну форму IІ сполуки формули (І) з наступним додаванням діетилового ефіру та (в) виділяють безводну форму II сполуки формули (І). 13. Сполука формули 4 Даний винахід стосується нових гідратів і нових поліморфів 4-[[(7R)-8-циклопентил-7-етил5,6,7,8-тетрагідро-5-метил-6-оксо-2птеридиніл]аміно]-3-метокси-N-(1-метил-4піперидиніл)бензаміду, способів їх одержання та їх застосування як лікарських засобів. Передумови створення винаходу Сполука 4-[[(7R)-8-циклопентил-7-етил-5,6,7,8тетрагідро-5-метил-6-оксо-2-птеридиніл]аміно]-3метокси-N-(1-метил-4-піперидиніл)бензамід відіграє важливу роль як інгібітор Polo-подібної кінази (PLK, від англ. "Polo-like kinase") у регуляції клітинного циклу в еукаріот. Сполука 4-[[(7R)-8-циклопентил-7-етил-5,6,7,8тетрагідро-5-метил-6-оксо-2-птеридиніл]аміно]-3метокси-N-(1-метил-4-піперидиніл)бензамід має структуру, що відповідає наступній формулі (І) Аналогічні дигідроптеридинони описані в WO 03/020722. Докладний опис винаходу У даному винаході пропонуються нові гідрати та нові поліморфні форми сполуки формули (І) з антипроліферативною дією. Відповідно до цього винахід стосується гідратів сполуки формули (І) 5 87865 6 Кращим гідратом сполуки формули (І) є моногідрат. Іншим кращим гідратом сполуки формули (І) є тригідрат. Наступним об'єктом винаходу є ангідрат (безводна форма) сполуки формули (І). Так само кращий ангідрат сполуки формули (І), представлений у вигляді безводної форми І. Кращий також ангідрат сполуки формули (І), представлений у вигляді безводної форми II. Кращий далі ангідрат сполуки формули (І), шляхом метилування диметилкарбонатом за представлений у вигляді безводної форми III. присутності основи при підвищеній температурі (в Наступним об'єктом винаходу є фармацевтичінтервалі від 80 до 180°С), краще при температурі на композиція, яка містить один з описаних вище 130°С. Наступним об'єктом винаходу є сполука пропонованих у винаході гідратів і поліморфів формули 3 сполуки формули (І) у терапевтично ефективній кількості та одну або декілька фармацевтично прийнятних допоміжних речовин. Наступним об'єктом винаходу є пропоновані в ньому гідрати та поліморфи сполуки формули (І) для застосування як лікарських засобів з антипроліферативною дією. Наступним об'єктом винаходу є застосування Наступним об'єктом винаходу є сполука форпропонованих у ньому гідратів і поліморфів сполумули 4 ки формули (І) для одержання лікарського засобу, призначеного для лікування і/або профілактики раку, інфекційних, запальних і аутоімунних захворювань. Наступним об'єктом винаходу є застосування пропонованих у ньому гідратів і поліморфів сполуки формули (І) для одержання лікарського засобу, призначеного для інгібування Polo-подібної кінази. Краще застосування пропонованих у винаході Наступним об'єктом винаходу є спосіб одергідратів і поліморфів сполуки формули (І) для одежання моногідрату сполуки формули (І), який поржання лікарського засобу, призначеного для інгілягає у тому, що бування Polo-подібної кінази PLFC-1. (а) приготовляють розчин сполуки формули (І) Особливо краще застосування пропонованих у у суміші розчинників з ізопропанолу та води або винаході гідратів і поліморфів сполуки формули (І), ацетону та води, яке передбачає пероральне, ентеральне, внутріш(б) із суміші розчинників кристалізують моногіньовенне, перитонеальне введення діючої речодрат сполуки формули (І) і вини в організм або введення діючої речовини в (в) виділяють моногідрат сполуки формули (І). організм шляхом ін'єкції. Наступним об'єктом винаходу є спосіб одерНаступним об'єктом винаходу є спосіб одержання тригідрату сполуки формули (І), який поляжання сполуки формули (І), який відрізняється гає у тому, що моногідрат сполуки формули (І) тим, що сполуку формули 4 піддають витримуванню в атмосфері з вологістю повітря принаймні 70%. Наступним об'єктом винаходу є спосіб одержання безводної форми III сполуки формули (І), який полягає у тому, що (а) моногідрат сполуки формули (І) витримують у струмі сухого азоту або (б) моногідрат сполуки формули (І) витримують при температурі приблизно 70°С, краще при вводять у взаємодію зі сполукою формули 9 температурі в межах від 70 до 120°С, найкраще при температурі в межах від 70 до 90°С. Наступним об'єктом винаходу є спосіб одержання безводної форми І сполуки формули (І), який полягає у тому, що розплавляють безводну форму III сполуки формули (І) і потім розплав кристалізують при температурі принаймні 140°С, краще при температурі в межах від 140 до 160°С. Наступним об'єктом винаходу є спосіб одержання безводної форми І сполуки формули (І), Наступним об'єктом винаходу є спосіб одерякий полягає у тому, що жання сполуки формули 9 (а) приготовляють розчин сполуки формули (І) у суміші розчинників з етилацетату та метил-трет 7 87865 8 бутилового ефіру, краще при об'ємному співвідв) виділяють безводну форму II сполуки форношенні між етилацетатом і метил-трет-бутиловим мули (І). ефіром 3:5, або в суміші розчинників з метилізобуНаступним об'єктом винаходу є спосіб одертилкетону та циклогексану, жання безводної форми І сполуки формули (І), (б) із суміші розчинників кристалізують безвоякий полягає у тому, що дну форму І сполуки формули (І) і (а) розплавляють безводну форму II сполуки (в) виділяють безводну форму І сполуки форформули (І) і мули (І). (б) розплав кристалізують при температурі Наступним об'єктом винаходу є спосіб одерпринаймні 185°С, краще при температурі в межах жання безводної форми II сполуки формули (І), від 185 до 200°С. який полягає у тому, що Сполуки формули (І) можна одержувати опи(а) приготовляють розчин сполуки формули (І) саними нижче методами синтезу. Синтез сполуки в етилацетаті, формули (І) у загальному вигляді проілюстрований (б) з етилацетату кристалізують безводну фона схемі 1, що призначена тільки для пояснення рму II сполуки формули (І) з наступним додаванвинаходу і не обмежує його обсяг. ням діетилового ефіру та Одержання анілінового фрагмента 4 9 87865 10 Варіант 1А Суспензію 100г (0,507 моль) 3-метокси-4нітробензойної кислоти 2, 163г (0,508 моль) тетрафторборату О-(бензотриазол-1-іл)-N,N,N',N'тетраметилуронію та 192мл (1,1 моль) етилдіізопропіламіну в 1,2л дихлорметану перемішують протягом години при 25°С. До одержаного розчину додають 58г (0,508 моль) 1-метил-4амінопіперидину 1 і перемішують протягом 16год при 20°С. Потім розчин упарюють до об'єму 600мл і органічну фазу п'ятикратно промивають 80мл 1молярного розчину аміаку. Органічну фазу упарюють і залишок хроматографують на силікагелі, використовуючи суміш із дихлорметану, метанолу та конц. аміаку (у співвідношенні 15:1:0,1). Фракції, що містять продукт, поєднують, випарюють розчинник і продукт кристалізують із суміші етилацетату та метанолу. Таким шляхом одержують 123г продукту 3. Варіант 1Б 4,00кг (20,3 моль) 3-метокси-4-нітробензойної кислоти 2 додають в 54л толуолу. Далі при нормальному тиску відганяють 16л толуолу. Після цього суміш охолоджують до 105°С і додають 40мл диметилформаміду в 2л толуолу. При температурі сорочки 120°С протягом 30хв доливають 2,90кг (24,3 моль) тіонілхлориду та промивають 4л толуолу. Після цього реакційну суміш протягом 1 год перемішують при нагріванні зі зворотним холодильником. Потім при нормальному тиску відганяють 12л толуолу. Далі вміст реактора охолоджують. Потім при 55-65°С доливають розчин 2,55кг (22,3 моль) 1-метил-4-амінопіперидину 1 в 2л толуолу та 2,46кг (24,3 моль) триетиламіну в 2л толуолу. Після цього промивають 4л толуолу. Суспензію перемішують протягом 1год. Потім доливають 20л води та при 35-40°С додають 3,08кг (30,4 моль) конц. соляної кислоти (36%-вий). Далі промивають 2л води. При 35-40°С утворюються дві фази. Органічну фазу відокремлюють, а водну фазу, що містить продукт, знову завантажують у реактор. Після цього промивають 4л води. Потім при зниженому тиску та при 50°С відганяють 3,2л води. До розчину, що залишився, при 40°С доливають 4,87кг (60,9 моль) розчину гідроксиду натрію (50%вого). Після цього промивають 4 л води. Суспензії, що містить продукт, дають охолонути до 22°С і потім протягом 30хв перемішують при цій температурі. Суспензію фільтрують на нутчі й осад на фільтрі промивають 40л води. Продукт сушать у вакуумній сушильній шафі при 40°С. Таким шляхом одержують 5,65кг продукту. Варіант 2А Розчин 145г (0,494 моль) сполуки 3 в 2л метанолу гідрують за присутності 2г паладію на вугіллі (10%-вого) при тиску 4 бар. Після цього каталізатор відфільтровують і фільтрат упарюють. Таким шляхом одержують 128г продукту 4. Варіант 2Б До 5,00кг (17,0 моль) сполуки 3 і 600г активованого вугілля (технічного) додають 25л демінералізованої води. Після цього додають 2,05кг (34,1 моль) оцтової кислоти. Потім суспензію перемішують протягом 15хв при 22-25°С. Далі додають 500г паладію на вугіллі (10%-вого), збовтаного в 3л демінералізованої води, і потім промивають 2л демінералізованої води. Після цього вміст реактора нагрівають до 40°С і гідрують при цій темпера турі до припинення поглинання водню. Потім реакційну суміш фільтрують і осад на фільтрі промивають 10л демінералізованої води. Для кристалізації фільтрат переносять у реактор і транспортувальну ємність потім промивають 5л демінералізованої води. Вміст реактора нагрівають до 50°С. Далі додають суміш із 5,45кг (68,2 моль) розчину гідроксиду натрію (50%-вого, технічного) і 7л демінералізованої води. Після цього перемішують протягом 10хв при 45-50°С. Потім суспензію охолоджують до 20°С і перемішують при цій температурі протягом 1-1,5год. Продукт відфільтровують на нутчі, промивають 30л демінералізованої води та сушать у вакуумній сушильній шафі при 45°С. Таким шляхом одержують 4,13кг продукту 4. Одержання дигідроптеридинонового фрагмента 9 11 87865 12 Метиловий ефір 6а, етиловий ефір 6b і 2пропіловий ефір 6с одержують відомими з літератури методами, наприклад, згідно з WO 03/020722. трет-Бутиловий ефір 6d одержують переетерифікацією трет-бутилового ефіру оцтової кислоти за присутності перхлорної кислоти [J. Med. Chem., т.37, №20, 1994, с.3294-3302]. У наступній реакції нуклеофільного заміщення амінокислоти можна використовувати у вигляді основ або гідрохлоридів. Амід амінокислоти 6е одержують шляхом амінолізу метилового ефіру 6а 40%-вим водним розчином метиламіну при кімнатній температурі. Амід амінокислоти 6f одержують шляхом утворення аміду вільної амінокислоти взаємодією з взятим у п'ятикратному надлишку 2-молярним розчином диметиламіну в тетрагідрофурані за присутності тетрафторборату О-(бензотриазол-1-іл)-N,N,N',N'тетраметилуронію як агента сполучення. Одержання сполук 7 Одержання метилового ефіру 7 а Суспензію 457г (2,06 моль) метилового ефіру амінокислоти 6а і 693г (8,25 моль) подрібненого в порошок гідрокарбонату натрію в 10л циклогексану перемішують протягом 15хв при кімнатній температурі. Потім додають 440г (2,27 моль) 2,4-дихлор5-нітропіримідину 5 і 1,5л циклогексану та перемішують протягом 3 днів при кімнатній температурі. Протікання реакції контролюють за допомогою високоефективної рідинної хроматографії. Для переведення продукту, що викристалізувався, назад у розчин до суспензії додають 4л дихлорметану. Після додавання 335г сульфату магнію суспен зію фільтрують на нутчі та неорганічний осад на фільтрі потім промивають дихлорметаном. Фільтрат упарюють при зниженому тиску до маси 3,1кг і одержану суспензію нагрівають зі зворотним холодильником. Після цього розчину дають повільно охолонути й потім перемішують протягом години при 10-15°С. Суспензію фільтрують на нутчі й осад на фільтрі промивають циклогексаном. Продукт сушать у вакуумній сушильній шафі при 40°С. Таким шляхом одержують 582г сполуки 7а (X означає ОСН3) у вигляді темно-жовтої твердої речовини. 13 87865 14 Для досягнення високої регіоселективності при Аналогічно цій процедурі одержують сполуки нуклеофільному заміщенні в сполуці 5 найбільш 7b-7f. При перетворенні амідів амінокислот 7е, 7f придатні ліпофильні розчинники, такі, наприклад, для покращення розчинності додають невелику як циклогексан, метилциклогексан, толуол і їх сукількість більш полярного розчинника, наприклад, міші. етилацетату або дихлорметану. Свіжоприготовлену суспензію 560г (1,63 моль) сполуки 7а і 185г нікелю Ренея в 2,8л оцтової кислоти гідрують при 75°С. Після завершенні поглинання водню каталізатор відфільтровують і розчин для гідрування упарюють при зниженому тиску. До залишку додають 4л демінералізованої води та 4л етилацетату. Між фазами утворюється осад, який містить продукт. Водну фазу відокремлюють. До органічної фази додають 2л етилацетату та осад відфільтровують на нутчі. Осад суспендують в 600мл демінералізованої води, перемішують протягом 1год при кімнатній температурі, відфільтровують на нутчі та промивають демінералізованою водою. Таким шляхом одержують 110г вологого продукту А. Фільтрат тричі промивають розчином хлориду натрію. Органічну фазу упарюють. Таким шляхом одержують 380г червонясто-коричневого залишку Б, який поєднують із вологим продуктом А. Об'єднані сирі продукти А і Б при нагріванні зі зворотним холодильником розчиняють в 1,5л етанолу. Після цього розчин фільтрують до прозорого стану й фільтр потім промивають 150мл етанолу. Далі при нагріванні зі зворотним холодильником до розчину додають 550мл демінералізованої води. Потім розчину дають охолонути, після чого перемішують спочатку протягом 16год при кімнатній температурі, а потім протягом 3год при 0-5°С. Осад відфільтровують на нутчі та промивають спочатку сумішшю з демінералізованої води та метанолу (у співвідношенні 1:1), а потім демінералізованою водою. Продукт сушать у вакуумній сушильній шафі при 50°С. Таким шляхом одержують 266г продукту 8 у вигляді твердої речовини. Одержання сполуки 9 (варіант 3А) До розчину 264г (0,94 моль) сполуки 8 та 161г (1,13 моль) метилиодиду в 2л диметилацетаміду при 4-10°С порціями протягом години додають 38г (0,95 моль) гідриду натрію (60%-ва дисперсія в мінеральному маслі). Потім охолодну баню видаляють і суміші протягом 2год дають нагрітися до 20°С. Після цього охолоджують до 10°С і додають ще 0,38г (9,5 ммоль) гідриду натрію. Далі перемішують протягом 4год при 10-15°С. Потім до реак ційного розчину додають 100мл етилацетату та 1кг льоду. Суспензію, що утворилася, розбавляють 3л демінералізованої води. Після цього суспензію перемішують протягом 2год, осад відфільтровують на нутчі й осад на фільтрі промивають демінералізованою водою. Продукт сушать у вакуумній сушильній шафі при 50°С. Таким шляхом одержують 273г продукту 9 у вигляді безбарвних кристалів. 15 87865 16 Суспензію 100г (356 ммоль) сполуки 8 і 73,8г (534 ммоль) карбонату калію в 400мл диметилкарбонату нагрівають в автоклаві до 130°С з наступним витримуванням при цій температурі протягом 6год. Потім суміші дають охолонути та при перемішуванні додають 300мл демінералізованої води й 200мл етилацетату. Водну фазу разом з нерозчинними солями відокремлюють. Від органічної фази при тиску 180 мбар і при температурі нагрівальної бані 70°С відганяють 500мл розчинника. До залишку додають 600 мл демінералізованої води та при тиску 150 мбар і при температурі нагрівальної бані 80°С відганяють 100мл розчинника. До суспензії додають 350мл етанолу та нагрівають до 65°С. Потім розчину дають охолонути та додають затравку. Після цього охолоджують до 10°С, осад відфільтровують на нутчі та потім промивають сумішшю з демінералізованої води й етанолу (у співвідношенні 2,5:1). Продукт сушать у вакуумній сушильній шафі при 50°С. Таким шляхом одержують 95,5 г продукту 9. Суспензію 201г (1,06 моль) гідрату паратолуолсульфонової кислоти, 209г (706 ммоль) сполуки 9 та 183г (695 ммоль) сполуки 4 в 800мл 2-метил-4пентанолу кип'ятять зі зворотним холодильником. При цьому відганяють 100 мл розчинника. Після цього протягом 3год кип'ятять зі зворотним холодильником, додають 200мл 2-метил-4-пентанолу та відганяють 120мл розчинника. Після 2годинного кип'ятіння зі зворотним холодильником відганяють ще 280мл розчинника. Потім реакційному розчину дають охолонути до 100°С і додають до нього 1л демінералізованої води, а потім 0,5л етилацетату. Органічну фазу відокремлюють, а водну фазу ще раз промивають 0,5л етилацетату. До кислої водної фази додають 1,5л дихлорметану та 0,5л етилацетату. Значення рН водної фази встановлюють на 9,2 додаванням 260мл 6н. розчину їдкого натру. Водну фазу відокремлюють і органічні фази тричі промивають 1н. водним розчином гідрокарбонату натрію порціями по 1л. Органічну фазу сушать над сульфатом натрію, фільтрують і розчинник випарюють при зниженому тиску. Таким шляхом одержують 406г сирого продукту. Цей сирий продукт розчиняють в 1,5л етилацетату. Потім при температурі 50-55°С додають 2,5л метил-трет-бутилового ефіру. При 45°С додають затравку і перемішують протягом 16год при охолодженні до кімнатної температури. Далі су спензію перемішують протягом 3,5год при 0-5°С і осад відфільтровують на нутчі. Осад на фільтрі після цього промивають сумішшю метил-третбутилового ефіру й етилацетату (у співвідношенні 2:1), а потім метил-трет-бутиловим ефіром. Продукт сушать у вакуумній сушильній шафі при 50°С. Таким шляхом одержують 236г кристалічної сполуки формули (І) у вигляді безводної форми І. Кристалізація 46,5г описаної вище кристалічної безводної форми І сполуки формули (І) розчиняють в 310мл 1-пропанолу та розчин фільтрують до прозорого стану. Далі нагрівають до 70°С і додають 620мл демінералізованої води. Розчину дають охолонути до кімнатної температури, охолоджують до 0-10°С і додають кристали затравки. Суспензію, що утворилася, перемішують протягом 3год при 0-10°С. Після цього фільтрують на нутчі та промивають холодною сумішшю 1-пропанолу й демінералізованої води (у співвідношенні 1:2), а потім демінералізованої водою. Продукт сушать у вакуумній сушильній шафі при 50°С. Таким шляхом одержують 40,5г кристалічної сполуки формули (І) у вигляді моногідрату. Сирий продукт, одержаний при описаному вище хімічному перетворенні, можна також безпосередньо кристалізувати у вигляді кристалічного моногідрату із суміші 1-пропанолу та демінералізованої води. 17 87865 18 Гідрати та ангідрати сполуки формули (І) можтільки для пояснення винаходу без обмеження на одержувати описаними нижче методами. Ці його обсягу. методи проілюстровані на схемі 2 і призначені Характеристики пропонованих у винаході гідратів і ангідратів визначали за допомогою ДСК/ТГ (диференціальної сканувальної калориметрії/термогравіметрії) та за допомогою рентгенівської порошкової дифрактометрії (з одержанням рентгенівських порошкових дифрактограм) (таблиці 1-5, Фіг.1а-5а). Всі рентгенівські порошкові дифрактограми одержували відомими з рівня техніки методами, використовуючи рентгенівський порошковий дифрактометр (Bruker D8 Advanced). Дифрактограми одержували за наступних умов вимірювання: Кao випромінювання міді (l=1,5418 A ), 40кВ, 40мА. Для ДСК/ТГ-вимірювань використовували прилади фірми Mettler Toledo (DSC 821 і TGA 851). ДСК-вимірювання здійснювали на зразках масою від 2 до 10мг, а ТГ-вимірювання здійснювали на зразках масою від 10 до 30мг. Вимірювання здійснювали при швидкості нагрівання 10К/хв в атмосфері інертного газу (у струмі азоту). Таблиця 1 Дифракційні максимуми (рефлекси) та їх інтенсивність (нормована), виявлені при аналізі моногідрату сполуки формули (І) рентгенівською порошковою дифрактометрією за нормальних кімнатних умов 2q [°] o dhkl [ A ] Інтенсивність І/І0 [%] 1 6,07 8,06 9,11 12,23 12,93 13,81 14,29 14,94 16,29 17,01 17,8 18,29 18,6 19,71 19,94 20,43 2 14,54 10,96 9,7 7,23 6,84 6,41 6,2 5,92 5,44 5,21 4,98 4,85 4,77 4,5 4,45 4,34 3 62 15 100 24 50 13 76 18 18 15 8 69 32 18 13 7 19 87865 20 Продовження таблиці 1 1 20,76 21,8 22,64 23,21 23,67 24,38 25,4 25,98 27,01 27,78 28,49 30,41 2 4,27 4,07 3,92 3,83 3,76 3,65 3,5 3,43 3,3 3,21 3,13 2,94 3 17 5 65 29 22 7 14 2 3 27 11 9 Таблиця 2 Дифракційні максимуми (рефлекси) і їх інтенсивність (нормована), виявлені при аналізі тригідрату сполуки формули (І) рентгенівською порошковою дифрактометрією при кімнатній температурі та 90%-вій відносній вологості 2q [°] o dhkl [ A ] Інтенсивність І/І0 [%] 5,93 6,45 8,69 9,45 11,43 12,5 13,06 13,89 14,57 15,38 16,18 17,04 17,34 18,07 18,59 18,85 19,81 20,52 21,18 22,06 22,96 23,46 24,79 25,74 27,23 28,04 28,8 29,52 29,88 30,58 14,89 13,68 10,17 9,35 7,74 7,08 6,77 6,37 6,08 5,76 5,47 5,2 5,11 4,91 4,77 4,71 4,48 4,32 4,19 4,03 3,87 3,79 3,59 3,46 3,27 3,18 3,1 3,02 2,99 2,92 39 34 100 26 85 8 32 7 19 9 7 25 10 37 21 16 5 15 57 5 15 51 21 7 6 7 15 7 7 5 21 87865 22 Таблиця 3 Дифракційні максимуми (рефлекси) і їх інтенсивність (нормована), виявлені при аналізі безводної форми І сполуки формули (І) рентгенівською порошковою дифрактометрією за нормальних кімнатних умов 2q [°] o dhkl [ A ] Інтенсивність І/І0 [%] 5,48 6,47 7,88 8,93 9,5 10,74 11,06 13,06 13,81 14,95 15,86 16,71 16,94 18,27 18,65 19,14 20,12 21,32 21,81 22,57 23,44 23,78 24,66 25,28 25,55 27,21 28,03 29,35 30,04 16,11 13,65 11,21 9,89 9,31 8,23 7,99 6,78 6,41 5,92 5,58 5,3 5,23 4,85 4,75 4,63 4,41 4,16 4,07 3,94 3,79 3,74 3,61 3,52 3,48 3,27 3,18 3,04 2,97 22 51 31 100 5 22 5 19 9 4 14 10 17 5 20 9 29 5 4 11 4 7 3 7 4 8 2 3 3 Таблиця 4 Дифракційні максимуми (рефлекси) і їх інтенсивність (нормована), виявлені при аналізі безводної форми II сполуки формули (І) рентгенівською порошковою дифрактометрією за нормальних кімнатних умов 2q [°] o dhkl [ A ] Інтенсивність І/І0 [%] 1 4,76 6,64 7,92 9,03 9,51 11,29 12,39 13,41 14,31 17,1 17,58 18,72 19 2 18,55 13,3 11,15 9,79 9,29 7,83 7,14 6,6 6,18 5,18 5,04 4,74 4,67 3 50 100 1 3 39 1 37 2 16 1 1 3 7 23 87865 24 Продовження таблиці 4 1 19,23 20,04 20,39 21,15 21,57 22,18 23,07 23,54 24,2 24,65 25,37 26,28 26,74 27,01 27,95 28,13 2 4,61 4,43 4,35 4,2 4,12 4 3,85 3,78 3,67 3,61 3,51 3,39 3,33 3,3 3,19 3,17 3 17 5 2 4 2 1 4 1 3 1 2 1 1 2 1 1 Таблиця 5 Дифракційні максимуми (рефлекси) і їх інтенсивність (нормована), виявлені при аналізі безводної форми III сполуки формули (І) рентгенівською порошковою дифрактометрією при 100°С 2q [°] o dhkl [ A ] Інтенсивність І/І0 [%] 6,49 9,74 10,99 12,56 14,44 14,95 15,72 17,5 17,89 18,8 19,14 19,68 21,58 22,19 23,09 25,99 27,66 30,74 13,61 9,07 8,04 7,04 6,13 5,92 5,63 5,06 4,95 4,72 4,63 4,51 4,12 4 3,85 3,43 3,22 2,91 41 81 29 21 13 8 59 14 11 29 46 100 50 43 40 29 17 12 Пропоновані у винаході ангідрат І, ангідрат II і моногідрат сполуки формули (І) можуть застосовуватися індивідуально або в комбінації з іншими пропонованими у винаході діючими речовинами та необов'язково також у комбінації з фармакологічно активними діючими речовинами іншого типу. Як приклад лікарських форм, придатних для введення в організм у їх складі пропонованих у винаході сполук, можна назвати таблетки, капсули, супозиторії, розчини, насамперед розчини для ін'єкцій (підшкірних, внутрішньовенних, внутрішньом'язових) і інфузій, мікстури, емульсії та порошки, здатні диспергуватися. У таких лікарських формах на частку фармацевтично активної( их) сполуки(-ук) повинно припадати в кожному випадку від 0,01 до 90мас.%, краще від 0,1 до 50мас.%, від загальної маси препарату, тобто в подібних лікарських формах фармацевтично активна(-і) сполука(-и) повинна(-і) міститися в кількостях, достатніх для її(їх) введення в організм у дозуванні, що відповідає зазначеному нижче інтервалу значень. За потреби діюча(-і) речовина(и) можна вводити в організм у зазначені нижче дозах декілька разів на добу. Відповідні таблетки можна виготовляти, наприклад, змішанням діючої речовини або діючих речовин з відомими допоміжними речовинами, наприклад, інертними розріджувачами, такими як карбонат кальцію, фосфат кальцію або лактоза, 25 87865 26 розпушувачами, такими як кукурудзяний крохпорід (наприклад, каолін, глиноземи, тальк, креймаль або альгінова кислота, сполучними, такими да), синтетичне борошно гірських порід (наприяк крохмаль або желатин, змащувальними речоклад, високодисперсна кремнієва кислота та сивинами, такими як стеарат магнію або тальк, і/або лікати), цукри (наприклад, тростинний, молочний засобами для забезпечення депо-ефекту, такими та виноградний цукор), емульгатори (наприклад, як карбоксиметилцелюлоза, ацетофталат целюлігнін, сульфітний луг, метилцелюлоза, крохмаль лози або полівінілацетат. Таблетки можуть також і полівінілпіролідон) і змащувальні речовини (наскладатися з декількох шарів. приклад, стеарат магнію, тальк, стеаринова кисВідповідним чином можна виготовляти драже лота та лаурилсульфат натрію). нанесенням на одержані аналогічно таблеткам Пропоновані у винаході сполуки можна ввоядра покриттів зі звичайно застосовуваних у цих дити в організм звичайним шляхом, краще пероцілях матеріалів, наприклад, колідону або шеларально, шляхом ін'єкції або трансдермально. Для ку, гуміарабіку, тальку, діоксиду титану або цукру. прийому усередину можуть використовуватися Ядра драже для забезпечення депо-ефекту або таблетки, до складу яких крім вищевказаних носідля уникнення несумісності також можна виготоїв можна, як очевидно, включати також такі добавляти багатошаровими. Так само й оболонка вки, як, наприклад, цитрат натрію, карбонат кальдраже також може складатися для забезпечення цію та дикальційфосфат, разом з різного роду депо-ефекту з декількох шарів, для чого можна наповнювачами, такими як крохмаль, краще карвикористовувати допоміжні речовини, зазначені топляний крохмаль, желатин і т.п. Крім цього при вище для таблеток. виробництві таблеток можуть використовуватися До складу мікстур із пропонованими у винатакож змащувальні речовини, такі як стеарат маході діючими речовинами, відповідно комбінацій гнію, лаурилсульфат натрію та тальк. У випадку діючих речовин додатково можуть входити також водних суспензій діючі речовини крім вищеопипідсолоджувальна речовина, така як сахарин, саних допоміжних речовин можна також змішувацикламат, гліцерин або цукор, а також поліпшути з різного роду поліпшувачами смаку або барввач смаку, наприклад, ароматизатор, такий як никами. Для парентерального введення можна ванілін або апельсиновий екстракт. Крім цього використовувати розчини діючих речовин, одермікстури можуть містити суспендуючі допоміжні жувані із застосуванням придатних для цієї мети речовини або загусники, такі як натрійкарбоксирідких носіїв. метилцелюлоза, змочувачі, наприклад, продукти При внутрішньовенному введенні діючу реконденсації жирних спиртів з етиленоксидом, або човину вводять в організм у дозі, що становить захисні речовини (консерванти), такі як nвід 1 до 1000мг на годину, краще від 5 до 500мг гідроксибензоати. на годину. Однак у деяких випадках залежно від Розчини для ін'єкцій і інфузій приготовляють ваги тіла пацієнта, відповідно шляху введення за відомою технологією, наприклад, з додавандіючої речовини в організм, індивідуальної реакням агентів, що надають ізотонічності, консервації на лікарський засіб, типу його лікарської форнтів, таких як n-гідроксибензоати, або стабілізами та часу, відповідно інтервалу часу введення торів, таких як солі етилендіамінтетраоцтової лікарського засобу в організм доза діючої речокислоти з лужними металами, і за потреби із завини може відрізнятися від зазначених вище знастосуванням емульгаторів і/або диспергаторів, чень. Так, зокрема, іноді може виявитися достатпри цьому, наприклад, при застосуванні води як нім використовувати діючу речовину або діючі розріджувача за потреби можна використовувати речовини в дозі, меншій зазначеної вище нижньої органічні розчинники як гідротропні солюбілізатомежі, тоді як в інших випадках може знадобитися ри, відповідно допоміжні розчинники, і потім розвикористовувати діючу речовину або діючі речоливають по пляшках для ін'єкцій, ампулам або вини в дозі, що перевищує вищевказану верхню пляшкам для інфузії. межу. За потреби введення діючої речовини або Капсули, які містить одну або декілька діючих діючих речовин у більших дозах може виявитися речовин, відповідно комбінації діючих речовин, доцільним ділити їх на декілька більш дрібних доз можна виготовляти, наприклад, змішанням діюіз розрахунку на декілька прийомів на добу. чих речовин з інертними носіями, такими як лакНижче винахід проілюстрований на приклатоза або сорбіт, і розфасовуванням одержаної дах, у яких представлені склади деяких лікарсьсуміші в желатинові капсули. ких форм і які не обмежують його обсяг. Відповідні супозиторії можна виготовляти, Приклади лікарських форм (фармацевтичних наприклад, змішанням діючої речовини або діюкомпозицій) чих речовин з передбаченими для цієї мети носіями, такими як нейтральні жири або поліетиленгА) Таблетки ліколь, відповідно його похідні. Як приклад допоміжних речовин, які можна Вміст із розрахунку Компонент використовувати при приготуванні лікарських на одну таблетку форм, можна назвати воду, фармацевтично придіюча речовина 100 мг йнятні (нешкідливі) органічні розчинники, такі як лактоза 140 мг парафіни (наприклад, фракції мінерального маскукурудзяний крохмаль 240 мг ла), олії рослинного походження (наприклад, полівінілпіролідон 15 мг арахісова або кунжутна олія), моно- або поліфунстеарат магнію 5 мг кціональні спирти (наприклад, етанол або гліце500 мг рин), носії, такі як природне борошно гірських 27 87865 28 Тонкоподрібнену діючу речовину змішують із Тонкоподрібнену діючу речовину змішують із частиною від усієї передбаченої кількості кукурулактозою та частиною від усієї передбаченої кількості кукурудзяного крохмалю. Одержану суміш дзяного крохмалю, лактозою, мікрокристалічною целюлозою та полівінілпіролідоном, одержану просівають, після чого її зволожують розчином полівінілпіролідону у воді, місять, гранулюють у суміш просівають і разом з іншою кількістю кукурудзяного крохмалю та водою переробляють на вологому стані та сушать. Одержаний гранулят разом з іншою кількістю кукурудзяного крохмалю гранулят, який сушать і просівають. Далі додають та стеаратом магнію просівають і змішують між натрійкарбоксиметилкрохмаль і стеарат магнію, перемішують і з одержаної суміші пресують табсобою. З одержаної суміші пресують таблетки необхідної форми та розмірів. летки необхідних розмірів. Б) Таблетки В) Розчин в ампулах Вміст із розрахунку на одну таблетку діюча речовина 80 мг лактоза 55 мг кукурудзяний крохмаль 190 мг мікрокристалічна целюлоза 35 мг полівінілпіролідон 15 мг натрійкарбоксиметилкрохмаль 23 мг стеарат магнію 2 мг 400 мг діюча речовина хлорид натрію вода для ін'єкцій Компонент 50 мг 50 мг 5 мл Діючу речовину при її власному значенні рН або за потреби при рН 5,5-6,5 розчиняють у воді та змішують із хлоридом натрію як агентом, що надає ізотонічності. Від одержаного розчину відфільтровують пірогенні продукти та фільтрат в асептичних умовах розфасовують в ампули, які потім стерилізують і запаюють. Такі ампули можуть містити 5мг, 25мг або 50мг діючої речовини. 29 87865 30 31 87865 32 33 Комп’ютерна верстка В. Мацело 87865 Підписне 34 Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюHydrates and polymorphs of 4-[[(7r)-8-cyclopentyl-7-ethyl-5,6,7,8-tetrahydro-5-methyl-4-6-oxo-2-piperidinyl]amino]-3-methoxy-n-(1-methyl-4-piperidinyl)-benzamide, methods for the production thereof, and use thereof as medicaments
Автори англійськоюLints Gyunter, Sieger Peter, Kraemer Gerd F., Rall Werner, Herter Rolf, Hoffmann Matthias, Schmid Rolf
Назва патенту російськоюГидраты и полиморфы 4-[[(7r)-8-циклопентил-7-этил-5,6,7,8-тетрагидро-5-метил-6-оксо- 2-птеридинил]амино]-3-метокси-n-(1-метил-4-пиперидинил)бензамида, способ их получения (варианты) и их применение как лекарственных средств
Автори російськоюЛинц Гюнтер, Зигер Петер, Кремер Герд Ф., Ралль Вернер, Хертер Рольф, Хоффманн Маттиас, Шмид Рольф
МПК / Мітки
МПК: A61P 35/00, A61K 31/519, C07D 475/00, C07D 211/58
Мітки: застосування, варіанти, поліморфи, спосіб, одержання, засобів, гідрати, 4-[[(7r)-8-циклопентил-7-етил-5,6,7,8-тетрагідро-5-метил-6-оксо-2-птеридиніл]аміно]-3-метокси-n-(1-метил-4-піперидиніл)бензаміду, лікарських
Код посилання
<a href="https://ua.patents.su/17-87865-gidrati-ta-polimorfi-4-7r-8-ciklopentil-7-etil-5678-tetragidro-5-metil-6-okso-2-pteridinilamino-3-metoksi-n-1-metil-4-piperidinilbenzamidu-sposib-kh-oderzhannya-varianti-ta-kh-zast.html" target="_blank" rel="follow" title="База патентів України">Гідрати та поліморфи 4-[[(7r)-8-циклопентил-7-етил-5,6,7,8-тетрагідро-5-метил-6-оксо-2-птеридиніл]аміно]-3-метокси-n-(1-метил-4-піперидиніл)бензаміду, спосіб їх одержання (варіанти) та їх застосування як лікарських засобів</a>
Попередній патент: Спосіб неруйнівного контролю матеріалів і виробів і пристрій для його здійснення
Наступний патент: Перемикаючий пристрій кулачкового контролера двобічної дії
Випадковий патент: Машина для мінеральних добрив












