Сполука з властивостями вивільнювати гормон росту
Формула / Реферат
1. 2-аміно-N-[(1R)-2-[(3R)-3-бензил-3-(N,N',N'-триметилгідразинокарбоніл)піперидин-1-іл]-1-(1Н-індол-3-ілметил)-2-оксоетил]-2-метилпропіонамід
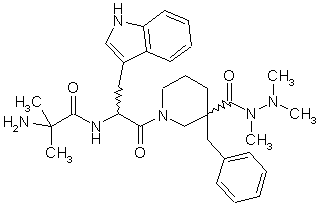
або його фармацевтично прийнятна сіль.
2. Фармацевтична композиція, яка містить як активний інгредієнт сполуку за п. 1 разом із фармацевтично прийнятним носієм або розріджувачем.
3. Фармацевтична композиція за п. 2 для стимулювання вивільнення гормону росту з гіпофізу.
4. Фармацевтична композиція за п. 2 або 3 для введення тваринам для збільшення швидкості та міри росту, для збільшення їх удійності та росту шерсті, або для лікування захворювань.
5. Спосіб стимулювання вивільнення гормону росту з гіпофізу ссавця, який включає введення вищезгаданому ссавцеві ефективної кількості сполуки за п. 1 або фармацевтичної композиції згідно з будь-яким з пп. 2-4.
6. Спосіб збільшення швидкості та міри росту, збільшення удійності та росту шерсті, або лікування захворювань, який включає введення суб'єктові, який цього потребує, ефективної кількості сполуки за п. 1 або фармацевтичної композиції згідно з будь-яким з пп. 2-4.
7. Застосування сполуки за п. 1 або її фармацевтично прийнятної солі для одержання медикаменту.
8. Застосування за п. 7 для одержання медикаменту для стимулювання вивільнення гормону росту з гіпофізу ссавця.
Текст
Даний винахід стосується нової сполуки, її фармацевтично прийнятних солей, композицій, що їх містять, та їх застосування для лікування захворювань, які є результатом дефіциту гормону росту. Гормон росту є гормоном, який стимулює ріст усіх тканин, які здатні рости. Крім того, відомо, що гормон росту має різний вплив на обмінні процеси, наприклад, стимуляцію синтезу білків та мобілізацію вільних жирних кислот, і викликає переключення енергетичного обміну речовин з вуглеводного на жирнокислотний обмін речовин. Дефіцит гормону росту може призводити до багатьох важких захворювань, наприклад, карликовості. Гормон росту вивільнюється з гіпофізу. Вивільнення прямо або непрямо жорстко контролюється багатьма гормонами та нейротрансмітерами. Вивільнення гормону росту може стимулюватися гормоном вивільнення гормону росту (GHRH) та інгібуватися соматостатином. В обох випадках гормони вивільнюються з гіпоталамусу, але їх дія опосередковується насамперед специфічними рецепторами, розташованими в гіпофізі. Було описано й інші сполуки, які стимулюють вивільнення гормону росту з гіпофізу. Наприклад, аргінін, L-3,4-дигідроксифенілаланін (L-Допа), глюкагон, вазопресин, РАСАР (пептид, який активує аденілілциклазу гіпофізу), агоністи мускаринового рецептора та синтетичний гексапептид, GHRP (пептид, який вивільнює гормон росту) вивільнюють ендогенний гормон росту або шляхом прямого впливу на гіпофіз, або впливаючи на вивільнення GHRH та/або соматостатину з гіпоталамусу. При захворюваннях або станах, коли вимагається підвищення рівня гормону росту, білковий характер гормону росту виключає будь-яке застосування, крім парентерального введення. До того ж, інші прямо діючі природні засоби, що посилюють секрецію, наприклад, GHRH та РАСАР, є довгими поліпептидами, через що перевагу віддають саме парентеральному введенню. Застосування певних сполук для підвищення рівня гормону росту у ссавців раніше пропонувалося, наприклад, у заявках ЕР 18072, ЕР 83864, WO 8302272, WO 8907110, WO 8901711, WO 8910933, WO 8809780, WO 9118016, WO 9201711, WO 9304081, WO 9413696, WO 9517423, WO 9514666, WO 9615148, WO 9622997, WO 9635713, WO 9700894, WO 9722620, WO 9723508, WO 9740023 та WO 9810653. Склад сполук, які вивільнюють гормон росту, є важливим для їх ефективності вивільнення гормону росту, а також їх біоакумуляції. Таким чином, задача даного винаходу полягає в забезпеченні нової сполуки з властивостями вивільнення гормону росту. Крім того, задача полягає в забезпеченні нової сполуки, яка вивільнює гормон росту (що посилює секрецію гормону росту), які є специфічними і/або селективними і не мають або практично не мають побічних ефектів, наприклад, вивільнення LH, FSH, TSH, АСТН, вазопресину, окситоцину, кортизолу та/або пролактину. Задача також полягає в забезпеченні сполуки, яка має добру біодоступність при пероральному введенні. Згідно з даним винаходом пропонується нова сполука, яка діє безпосередньо на клітини гіпофізу за нормальних умов експерименту in vitro для вивільнення з них гормону росту. Сполука, яка вивільнює гормон росту, може застосовуватись in vitro як унікальний дослідний засіб для розуміння, крім іншого, шляху регулювання секреції гормону росту на рівні гіпофізу. Крім того, сполука, яка вивільнює гормон росту, згідно з даним винаходом, також може вводитись in vivo для збільшення ендогенного вивільнення гормону росту. Відповідним чином, даний винахід стосується сполуки, яку одержують із застосуванням процедури, описаної у прикладі 1, або її фармацевтично прийнятної солі. Крім того, даний винахід стосується сполуки, яку одержують із застосуванням процедури, описаної у прикладі 1, і яка є 2-аміно-N-[(1R)2-[(3R)-3-бензил-3-(N,N'N'-триметилгідразинокарбоніл)піперидин-1-іл]-1-(1H-індол-3ілметил)-2-оксоетил]-2-метилпропіонамідом або її фармацевтично прийнятною сіллю. Крім того, даний винахід стосується сполуки 2-aміно-N-[(1R)2-[(3R)-3-бензил-3-(N,N',N'-триметилгідразинокарбоніл)піперидин-1-іл]-1-(1Н-індол-3ілметил)-2-оксоетил]-2-метилпропіонаміду або її фармацевтично прийнятної солі. Структуру сполуки, яку одержують із застосуванням процедури, описаної у прикладі 1, перевіряють, наприклад, шляхом рентгеноструктурного аналізу [наприклад, як описано у роботі Remington: The Science and Practice of Pharmacy, 19th Edition (1995), зокрема, сторінки 160 та 561-562]. Обсяг даного винаходу охоплює будь-яку можливу комбінацію двох або більшої кількості описаних авторами варіантів втілення. Процедура, застосована в цьому патенті, основана на з'єднанні пептидів, добре відомому спеціалістам, і ніяким чином не повинна розглядатись як така, що обмежує винахід. У цій процедурі перед з'єднанням амінокислотних або пептидних залишків добре відомими спеціалістам способами видаляють відповідну захисну групу, таку, як трет-бутилоксикарбоніл (Вос). Можна також уникнути застосування захисних груп. Відповідні амінокислоти можуть бути захищені і позбавлені захисту способами, відомими спеціалістам і описаними, наприклад, у роботі T.W. Green [Protective Groups in Органічн Synthesis, 2. Ed., John Wiley and Sons, New York 1991]. У Прикладі 1 процедуру описано детально. Після розділення рацемічної суміші 3-бензилпіперідин-1,3-дикарбонової кислоти 1-трет-бутилового естеру для одержання енантіомерних сполук, кінцевою сполукою, одержаною з застосуванням цієї процедури, є діастереомер 2-aміно-N-[(1R)2-[(3R)-3-бензил-3-(N,N',N'-триметилгідразинокарбоніл)піперидин-1-іл]-1-(1H-індол-3ілметил)-2-оксоетил]-2-метилпропіонамід замість суміші двох діастереомерів. Сполука даного винаходу виявляє посилений опір протеолітичному розщепленню ферментами, оскільки вона не є природною, зокрема, завдяки тому, що природні амідні зв'язки замінюються неприродними міметичними амідними зв'язками. Очікується, що збільшення опору сполуки винаходу протеолітичному розщепленню порівняно з відомими пептидами, що вивільнюють гормони, має поліпшити біоакумуляцію порівняно з біоакумуляцією пептидів, які пропонувалися в літературі раніше. Сполука даного винаходу необов'язково може бути у формі фармацевтично прийнятної солі, наприклад, у формі фармацевтично прийнятних кислотно-адитивних солей сполук даного винаходу, до яких належать солі, одержані шляхом реакції сполуки формули І з неорганічною або органічною кислотою, такою як соляна, гідробромнувата, сірчана, оцтова, фосфорна, молочна, малеїнова, мигдалева, фталева, лимонна, глутарова, глюконова, метансульфонова, саліцилова, бурштинова, винна, толуолсульфокислота, трифтороцтова, сульфамінова або фумарова кислота та/або вода. Сполука даного винаходу може вводитись у формі фармацевтично прийнятної кислотно-адитивної солі або, у певному випадку, у формі солі лужного металу або лужноземельного металу або нижчої алкіламонієвої солі. Вважають, що такі форми солей виявляють активність приблизно такого самого порядку, що й вільноосновні форми. В іншому аспекті даний винахід стосується фармацевтичної композиції, яка включає як" активний інгредієнт сполуку даного винаходу або її фармацевтично прийнятну соль разом із фармацевтично прийнятним носієм або розріджувачем. Фармацевтичні композиції, що містять сполуку даного винаходу, одержують традиційними способами, наприклад, як описано в роботі Remington's Pharmaceutical Sciences, 1985, або Remington: The Science and Practice of Pharmacy, 19th Edition (1995). Композиції можуть існувати у традиційних формах, наприклад, у формі капсул, таблеток, аерозолів, розчинів, суспензій або у формах для місцевого нанесення. Застосовуваний фармацевтичний носій або розріджувач може бути традиційним твердим або рідким носієм. Прикладами твердих носіїв є лактоза, каолін, цукроза, циклодекстрин, тальк, желатин, агар, пектин, гуміарабік, стеарат магнію, стеаринова кислота або нижчий алкіловий етер целюлози. Прикладами рідких носіїв є сироп, арахісова олія, оливкова олія, фосфоліпіди, жирні кислоти, аміни жирних кислот, поліоксіетилен або вода. Подібним чином, носій або розріджувач може включати будь-який відомий спеціалістам матеріал уповільненого вивільнення, такий як гліцерилмоностеарат або гліцерилдистеарат, окремо або змішаний з воском. Якщо для перорального введення застосовують твердий носій, композиція може бути таблетована, поміщена у тверду желатинову капсулу у формі порошку або гранул чи може бути у формі таблетки або пастилки. Кількість твердого носія може бути різною в широких межах, але зазвичай становить від приблизно 25мг до приблизно 1г м'якої желатинової капсули або стерильної рідини для ін'єкцій, такої як водна чи безводна рідка суспензія або розчин. Типова таблетка, яка може бути виготовлена традиційним способом таблетування, може містити: Ядро: Активна сполука (як вільна сполука або її сіль) 10мг Колоїдний діоксид кремнію (Aerosil) 1,5мг Целюлоза, мікрокрист. (Avicel) 70мг Модифікована целюлозна смола (Ac-Di-Sol) 7,5мг Стеарат магнію Покриття: НРМС приблизно 9мг *Mywacett 9-40 Τ approx. 0,9мг *Ацильований моногліцерид, застосований як пластифікатор для плівкоквого покриття. Для назального введення композиція може містити сполуку даного винаходу, розчинену або суспендовану в рідкому носії, зокрема, водному носії, для аерозольного розпилення. Носій може містити додатки, такі як солюбілізатори, наприклад, пропіленгліколь, поверхнево-активні речовини/ посилювачі абсорбції, такі як лецитин (фосфатидилхолін) або циклодекстрин, або консерванти, такі як парабени. Взагалі, сполуки даного винаходу відпускаються у формі одиничних доз, які містять 50-200мг активного інгредієнта разом із фармацевтично прийнятним носієм на одиничну дозу. Прийнятна доза для сполук згідно з даним винаходом становить 0,01-500мг/день, наприклад, від приблизно 5 до приблизно 50мг, скажімо, 10мг на дозу при введенні пацієнтові, наприклад, людині, як медикаменту. У ще одному аспекті даний винахід стосується фармацевтичної композиції у формі одиничної дози, яка включає як активний інгредієнт від приблизно 10 до приблизно 200мг сполуки загальної формули І або її фармацевтично прийнятної солі. Було продемонстровано, що сполука даного винаходу має здатність вивільнювати ендогенний гормон росту in vivo. Таким чином, ця сполука може бути застосована для лікування при станах, які вимагають підвищеного рівня гормону росту плазми, наприклад, у людей з дефіцитом гормону росту або у літніх пацієнтів чи худоби. Таким чином, в одному з аспектів даний винахід стосується фармацевтичної композиції для стимулювання вивільнення гормону росту з гіпофізу, композиції, яка включає як активний інгредієнт сполуку даного винаходу або її фармацевтично прийнятну сіль разом із фармацевтично прийнятним носієм або розріджувачем. У ще одному аспекті даний винахід стосується способу стимулювання вивільнення гормону росту з гіпофізу, способу, що включає введення суб'єктові, який цього потребує, ефективної кількості сполуки даного винаходу або її фармацевтично прийнятної солі. У ще одному аспекті даний винахід стосується застосування сполуки даного винаходу або її фармацевтично прийнятної солі для одержання медикаменту для стимулювання вивільнення гормону росту з гіпофізу. Спеціалістам добре відомо, що гормон росту застосовується і може застосовуватися найрізноманітнішими способами. Таким чином, сполука даного винаходу може вводитися з метою стимулювання вивільнення гормону росту з гіпофізу і в такому разі може мати практично такий самий вплив або застосування, що й сам гормон росту. Сполуки даного винаходу застосовують для стимуляції вивільнення гормону росту у літніх пацієнтів, запобігання катаболічним побічним ефектам глюкокортикоїдів, профілактики та лікування остеопорозу, лікування синдрому хронічної втоми (CFS), лікування синдрому гострої втоми та втрати м'язової маси після вибіркового хірургічного втручання, стимуляції імунної системи, прискорення загоєння ран, прискорення зростання кісток, прискорення при ускладнених переломах, наприклад, дистракційного остеогенезу, лікування виснаження внаслідок переломів, лікування затримки росту, лікування затримки росту в результаті ниркової недостатності, лікування кардіоміопатії, лікування виснаження у зв'язку з хронічними хворобами печінки, лікування тромбоцитопенії, лікування затримки росту у зв'язку з хворобою Крона, лікування синдрому короткого кишечнику, лікування виснаження у зв'язку з хронічною обструктивною легеневою хворобою (COPD), лікування ускладнень, пов'язаних із трансплантацією, лікування фізіологічної низькорослості, включаючи лікування дітей з дефіцитом гормону росту, та низькорослості, пов'язаної з хронічними захворюваннями, лікування ожиріння та затримки росту, пов'язаної з ожирінням, лікування анорексії, лікування затримки росту, пов'язаної з синдромом ПрадераВіллі та синдромом Тернера; прискорення росту у пацієнтів, які мають синдром часткової нечутливості до гормону росту, прискорення одужання та скорочення періоду госпіталізації опікових пацієнтів; лікування внутрішньоматкової затримки росту, дисплазії скелета, гіперкортицизму та синдрому Кушинга; викликання пульсуючого вивільнення гормону росту; заміни гормону росту у пацієнтів, що зазнали стресу, лікування остеохондродисплазії, синдрому Нунана, шизофренії, депресій, хвороби Альцгеймера, повільного загоєння ран та психосоціальної депривації, лікування катаболізму у зв'язку з легеневою дисфункцією та вентиляторною залежністю; лікування серцевої недостатності або пов'язаної з нею судинної дисфункції, лікування порушення серцевої функції, лікування або профілактики інфаркту міокарда, зниження кров'яного тиску, захисту від дисфункції шлуночка або профілактики реперфузії; лікування дорослих пацієнтів від хронічного діалізу; послаблення білкової катаболічної реакції після радикального хірургічного втручання, зменшення кахексії та втрати білків через такі хронічні захворювання, як рак або СНІД; лікування · гіперінсулінемії, включаючи незидіобластоз, допоміжного лікування для індукування овуляції; стимуляці розвитку тимуса та профілактики пов'язаного зі старінням зниження функції тимуса, лікування пацієнтів з пригніченим імунітетом; лікування саркопенії, лікування виснаження у зв'язку зі СНІДом; поліпшення сили та рухливості м'язів, підтримання товщини шкіри, метаболічного гомеостазу та ниркового гомеостазу у ослаблених пацієнтів літнього віку, стимуляції остеобластів, корекції кісток та росту хрящів; регуляції приймання їжі; стимуляції імунної систем у свійських тварин та лікування пов'язаних зі старінням порушень свійських тварин, сприяння ростові худоби та стимуляці росту шерсті овець, збільшення удійності худоби, лікування метаболічного синдрому (синдрому X), лікування резистентності до інсуліну, включаючи інсулінонезалежний цукровий діабет, у ссавців, наприклад, людини, лікування резистентності до інсуліну у ділянці серця, поліпшення якості сну та корекції відносного гіпосоматропізму при старінні через значне збільшення швидкого сну та зменшення латентності швидкого сну, лікування гіпотермії, лікування крихкості, пов'язаної зі старінням, лікування застійної серцевої недостатності, лікування переломів стегна, лікування імунодефіциту осіб зі зниженим співвідношенням Т4/Т8 клітин, лікування м'язової атрофії, лікування пошкодження скелетних м'язів літніх пацієнтів, підвищення активності білкової кінази В (РКВ), поліпшення загальної легеневої функції, лікування порушень сну, лікування затримки росту у зв'язку з астмою, лікування затримки росту у зв'язку з ювенільним ревматоїдним артритом та лікування затримки росту у зв'язку з кістозним фіброзом. Для вищезгаданих показань доза може бути різною залежно від способу введення та потрібної терапії. Однак зазвичай пацієнтам та тваринам вводять дозу на рівні від 0,0001 до 100мг/кг маси тіла на день для досягнення ефективного вивільнення ендогенного гормону росту. Крім того, сполука даного винаходу при введенні у вищевказаних дозах не має або практично не має побічних ефектів, таких як, наприклад, вивільнення LH, FSH, TSH, АСТН, вазопресину, окситоцину, кортизолу та/або пролактину. Як правило, дозовані форми, придатні для перорального, назального, пульмонального або крізьшкірного введення, включають від приблизно 0,0001мг до приблизно 100мг, в оптимальному варіанті — від приблизно 0,001мг до приблизно 50мг сполук даного винаходу, змішаних із фармацевтично прийнятним носієм або розріджувачем. Фармацевтична композиція винаходу необов'язково може включати сполуку даного винаходу у комбінації з однією або кількома сполуками, які виявляють різну активність, наприклад, антибіотиками або іншими фармакологічно активними матеріалами. Шлях введення може бути будь-яким шляхом, який ефективно переносить активну сполуку до підходящого або потрібного місця дії, наприклад, пероральним, назальним, пульмональним, крізьшкірним або парентеральним, причому перевагу віддають пероральному шляхові. Крім фармацевтичного застосування сполуки даного винаходу, корисними можуть бути in vitro засоби дослідження регуляції вивільнення гормону росту. Сполука даного винаходу також може бути корисною як in vivo засіб для оцінки здатності гіпофізу до вивільнення гормону росту. Наприклад, можуть бути піддані аналізові на гормон росту зразки сироватки, взяті до та після введення сполуки людині. Порівняння гормону росту в кожному зразку сироватки прямо визначає здатність гіпофізу пацієнта до вивільнення гормону росту. Сполука даного винаходу може вводитись тваринам, які мають промислове або сільського сподарське значення, для збільшення швидкості та міри їх росту, а також для підвищення удійності. Сполука даного винаходу також може застосовуватись у комбінації з іншими засобами, що поліпшують секрецію, такими як GHRP (2 або 6), GHRH та його аналоги, гормон росту та його аналоги або соматомедини, включаючи IGF-1 та IGF-2. Сполуку даного винаходу піддають in vitro аналізові на її ефективність та потенційну здатність вивільнювати гормон росту в первинних культурах гіпофізу щурів, і такий аналіз здійснюють описаним нижче способом. Виділення клітин гіпофізу щурів являє собою дещо змінений спосіб, описаний у роботі О. Sartor et al., Endocrinology 116. 1985, pp. 952-957. Самців-альбіносів щура Спрага-Долі (250 +/-25 грамів) закуповували у Mollegaard, Ulle Skensved, Данія. Щурів розсаджували по клітках групами (чотири тварини на клітку) і поміщували в кімнати з 12-годинним світловим циклом. Кімнатна температура становила від 19 до 24°С, а відносна вологість — від ЗО до 60%. Щурів декапітували і розрізали гіпофіз. Нейропроміжні частки видаляли, а решту тканини відразу поміщували в ізоляційний буфер при температурі льоду (середовище Гея (Gibco 041-04030) з 0,25% Dглюкози, 2% замінної амінокислоти (Gibco 043-01140) та 1% альбуміну сироватки великої рогатої худоби (BSA) (Sigma A-4503)). Тканину розрізали на дрібні фрагменти і переносили в ізоляційний буфер з 3,8мг/мл трипсину (Worthington #3707 TRL-3) та 330мг/мл ДНКази (Sigma D-4527). Цю суміш інкубували при 70об/хв протягом 35хв при 37°С в атмосфері 95/5% О2/СО2. Тканину після цього тричі промивали у вищезгаданому буфері. Застосовуючи стандартну пастерку, тканину після цього відсмоктували в окремі клітини. Після диспергування клітини фільтрували крізь нейлоновий фільтр (160мм) для видалення зайвої тканини. Суспензію клітин тричі промивали ізоляційним буфером з інгібітором трипсину (0,75мг/мл, Worthington #2829) і остаточно ресуспендували в культуральному середовищі; DMEM (Gibco 041-01965) з 25мМ HEPES (Sigma H-3375), 4мМ глутаміну (Gibco 043-05030H), 0,075% бікарбонату натрію (Sigma S-8875), 0,1% замінної амінокислоти, 2,5% ембріональної телячої сироватки (FCS, Gibco 011-06290), 3% конячої сироватки (Gibco 034-06050), 10% свіжої щурячої сироватки, 1нМ Т3 (Sigma Т-2752) та 40мг/л дексаметазону (Sigma D-4902) рН 7,3, до густини 2х105 клітин/мл. Клітини висівали у мікротитрувальні планшети (Nunc, Данія), 200мл/лунку, і культивували протягом 3 днів при 37°С та 8% СО2. Випробування сполуки Після культивування клітини двічі промивали стимуляційним буфером (збалансований сольовий розчин Хенкса (Gibco 041-04020) з 1% BSA (Sigma A-4503), 0,25% D-глюкози (Sigma G-5250) та 25мм HEPES (Sigma H-3375) рН 7,3) і попередньо інкубували протягом 1год при 37°С. Буфер замінювали на 90мл стимуляційного буфера (37°С). Додавали 10мл розчину випробуваної сполуки і планшети інкубували протягом 15хв при 37°С і 5% СО2. Середовище декантували і піддавали аналізові на вміст гормону росту (GH) у випробувальній системі rGH SPA. Сполуку випробували у дозах від 10пМ до 100мМ. Залежність реакції від дози вибудовували користуючись рівнянням Хілла (Fig P, Biosoft). Ефективність (максимальне вивільнення GH, Emax) виражали у % від Emax від GHRP-6. Потенційну здатність (ЕС50) визначали як концентрацію, що викликає половину від максимальної стимуляції вивільнення GH. Сполуки даного винаходу оцінюють на метаболічну стійкість, застосовуючи процедуру описану нижче: Сполуку розчиняють у концентрації 1мг/мл у воді. 25мл цього розчину додають до 175мл відповідного ферментного розчину (що в результаті дає співвідношення фермент:субстрат (маса/маса) приблизно 1:5). Розчин залишають до наступного дня при 37°С. 10мл розчинів різного ступеня розщеплення піддають аналізові порівняно з відповідним "нульовим" зразком, застосовуючи електророзпилювальну масспектрометрію (ESMS) з нагнітанням потоку при спостереженні за вибраним молекулярним іоном. Якщо сигнал послаблюється більше ніж на 20% порівняно з "нульвим" зразком, решту розчину піддають аналізові шляхом високоефективної рідинної хроматогрфії (HPLC) та мас-спектрометрії з метою точного визначення ступеня та місця (місць) розщеплення. Для випробування стійкості брали кілька стандартних пептидів (АСТН 4-10, ангіотензин 1-14 та глюкагон) з метою перевірки здатності різних розчинів до розщеплення пептидів. Стандартні пептиди (ангіотензин 1-14, АСТН 4-10 та глюкагон) закуповували у Sigma, МО, США) Усі ферменти (трипсин, хімотрипсин, еластазоамінопептидазу Μ та карбоксипептидазу Υ та В) закуповували у Boehririger Mannheim GmbH (Mannheim, Germany) Панкреатична ферментна суміш: трипсин, хімотрипсин та еластаза в 100мм амонійбікарбонату, рН 8,0 (концентрація в усіх випадках 0,025мг/мл). Карбоксипептидазна суміш: карбоксипептидаза Υ та В у 50мм амонійацетат, рН 4,5 (концентрація в усіх випадках 0,025мг/мл). Розчин амінопептидази М: амінопептидаза Μ (0,025мг/мл) у 100мм амонійбікарбонату, рН 8,0. Mac-спектрометричний аналіз здійснювали, застосовуючи два різні мас-спектрометри. Потрійний квадрупольний пристрій для LC-MS Sciex API III (Sciex instruments, Thomhill, Ontario), оснащений електророзпилювальним джерелом іонів, та часопролітний пристрій з плазмовим осадженням Bio-Ion 20 (Bio-Ion Nordic AB, Uppsala, Швеція). Визначення кількості сполуки (до та після розщеплення) здійснювали на пристрої API III, застосовуючи відстеження одиничного молекулярного іона з нагнітанням потоку аналіту. Потік рідини (МеОН:вода 1:1) зі швидкістю 100мл/хв контролювали за допомогою пристрою для HPLC АВІ 140В (Perkin-Elmer Applied Biosystems Divisions, Foster City, CA). Параметри пристрою встановлювали згідно зі стандартними робочими умовами, і відстеження SIM здійснювали, застосовуючи найбільш інтенсивний молекулярний іон (у більшості випадків він відповідає подвійно зарядженому молекулярному іонові). Крім того, ідентифікація продуктів розщеплення включала застосування мас-спектрометрії з десорбцією плазми (PDMS) з нанесенням зразків на вкриті нітроцелюлозою мішені та стандартними параметрами вимірювання. Точність визначених таким чином мас, як правило, є кращою за 0,1%. Відокремлення та виділення продуктів розщеплення здійснювали, застосовуючи HPLC-колонку HYTACH С-18 зі зворотною фазою, 4,6x105мм (Hewlett-Packard Company, Palo Alto, CA) зі стандартним ацетонітрилом: градієнт відокремлення TFA. Застосовуваною системою HPLC була НР1090М (HewlettPackard Company, Palo Alto, CA). Похідна пептиду Стандарти АСТН4-10 Глюкагон Інсулін (В23-29) Ангіотензин 1-14 GHRP-2 GHRP-6 Іон MW/SIM (amu) 1124,5/562,8 3483/871,8 859,1/430,6 1760,1/881,0 817,4/409,6 872,6/437,4 Карбокси-пептидазна суміш Панкр. ферментна суміш + +: Стійка (менше 20% послаблення сигналу SIM через 24год у розщеплювальному розчині) -: Нестійка (більше 20% послаблення сигналу SIM через 24год у розщеплювальному розчині) Сполуку даного винаходу піддають оцінці на її біодоступність при пероральному введенні, і таку оцінку здійснюють описаним нижче способом. Фармакокінетику сполуки досліджують на собаках породи бігль, яких утримують без їжі. Внутрішньовенне та пероральне введення випробуваної сполуки у 5% розчині глюкози здійснювали з тижневим інтервалом. Зразки крові забирали безпосередньо перед введенням ліків (початок відліку), а потім 0,08, 0,25, 0,50, 0,75, 1,0, 1,5, 2,0, 3,0, 4,0, 5,0 та 6,0 годин після введення. Зразки плазми до аналізу зберігали замороженими (
ДивитисяДодаткова інформація
Назва патенту англійськоюA compound having properties to release the growth hormone
Назва патенту російськоюСоединение со свойствами освобождения гормона роста
МПК / Мітки
МПК: A61P 5/00, A61K 31/454, C07D 401/06
Мітки: росту, властивостями, вивільнювати, гормон, сполука
Код посилання
<a href="https://ua.patents.su/11-73530-spoluka-z-vlastivostyami-vivilnyuvati-gormon-rostu.html" target="_blank" rel="follow" title="База патентів України">Сполука з властивостями вивільнювати гормон росту</a>
Попередній патент: Авіаційний ракетний комплекс для транспортування і запуску в повітрі ракети
Наступний патент: Спосіб сушіння деревини
Випадковий патент: Шарик опорно-поворотного пристрою












