Борати діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот
Номер патенту: 107774
Опубліковано: 10.02.2015
Автори: Гармашов Володимир Вікторович, Стріжков Олександр Генріхович
Формула / Реферат
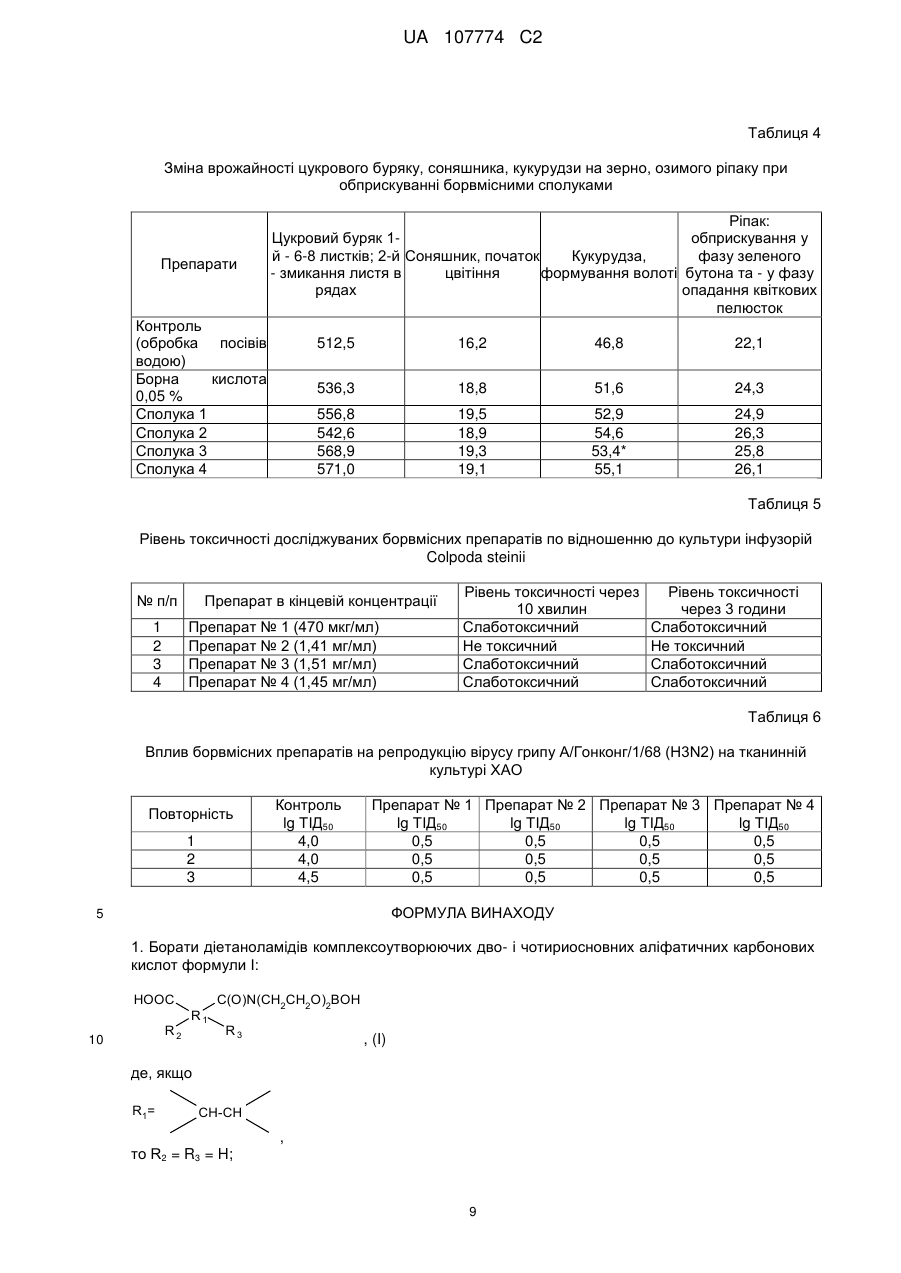
1. Борати діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот формули І:
![]() , (I)
, (I)
де, якщо
 ,
,
то R2 = R3 = H;
якщо
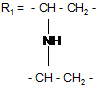 ,
,
то R2 = -COOH, R3 = C(O)N(CH2CH2O)2BOH;
якщо
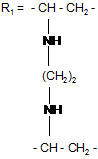 ,
,
то R2 = -COOH, R3 = C(O)N(CH2CH2O)2BOH;
якщо
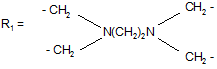 ,
,
то R2 = C(O)N(CH2CH2O)2BOH; R3 = -COOH.
2. Спосіб одержання боратів діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот формули І за п. 1, що передбачає взаємодію відповідної дво- або чотириосновної комплексоутворюючої аліфатичної карбонової кислоти з діетаноламіном і борною кислотою при 155-165 ºС і видалення води, що утворюється, за допомогою апарата Діна-Старка.
3. Спосіб за п. 2, який відрізняється тим, що як двоосновну комплексоутворюючу аліфатичну карбонову кислоту використовують бурштинову кислоту, а процес здійснюють при співвідношенні бурштинова кислота: діетаноламін: борна кислота, рівному 1:1: 1.
4. Спосіб за п. 2, який відрізняється тим, що як чотириосновну комплексоутворюючу аліфатичну карбонову кислоту використовують етилендіамінтетраоцтову або етилендіаміндибурштинову, або імінодибурштинову кислоту, а процес здійснюють при співвідношенні чотириосновна комплексоутворююча аліфатична карбонова кислота: діетаноламін: борна кислота, рівному 1:2: 2 відповідно.
5. Борати діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот формули І за п. 1 як рістрегулюючий, імуномоделюючий та противірусний засіб.
Текст
Реферат: Винахід належить до галузі органічної хімії, сільського господарства та медицини, а саме до боратів діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот, способу їх одержання та рістрегулюючого, імуномодулюючого та противірусного засобу. Заявлені сполуки мають структурну формулу І: HOOC R2 R1 C(O)N(CH2CH2O)2BOH R3 , (I) де, якщо R1= CH-CH , то R2 = R3 = H; якщо UA 107774 C2 (12) UA 107774 C2 R1 = - CH - CH2 NH - CH - CH2 , то R2 = -COOH, R3 = C(O)N(CH2CH2O)2BOH; якщо R1 = - CH - CH2 NH (CH2)2 NH - CH - CH2 , то R2 = -COOH, R3 = C(O)N(CH2CH2O)2BOH; якщо R1 = CH2 - CH2 N(CH2)2N - CH2 CH2 , то R2 = C(O)N(CH2CH2O)2BOH; R3 = -COOH. Отримують вказані сполуки шляхом взаємодії дво- або чотириосновної комплексоутворюючої аліфатичної карбонової кислоти з діетаноламіном і борною кислотою при температурі 155-165 °C і наступного видалення води, що утворюється, за допомогою апарата Діна-Старка. Запропонований винахід забезпечує одержання сполуки формули І в одну стадію з високим ступенем конверсії. Одержані сполуки можуть бути використані як рістрегулюючий, імуномодулюючий та противірусний засіб. UA 107774 C2 5 Винахід належить до галузі органічної хімії, сільського господарства та медицини, а саме до нових сполук - боратів діетаноламідів, комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот, способу їх одержання та рістрегулюючого, імуномодулюючого та противірусного засобу. Відома хімічна сполука (див. патент РФ № 2273637) із загальною формулою: DMP n MxByOz ( A )v m * WH 2O , n 10 15 де DMP означає N, N-диметилпіперидин (мепікват); M - необхідний метал, вибраний з ряду натрій, калій, магній, кальцій, цинк, марганець або мідь, водень або NH 4, B - означає бор, O кисень, A - хелатний або комплексоутворюючий фрагмент, зв'язаний з одним атомом бору, що являє собою (нижчі) алкілгліколі або цукри. Дана сполука має регулюючу ріст рослин дію. До її складу входить бор і можуть входити 3dметали, число яких дуже обмежено. Крім того, склад і структура сполуки, що зв'язує бор і метал, не є оптимальною для засвоєння рослинами, що призводить до необхідності збільшення доз речовини до 10 разів для досягнення фізіологічного ефекту. Що стосується рістрегулюючої здатності, то вона зводиться лише до уповільнення зростання бавовнику і деяких сортів пшениці. До недоліків описаної сполуки слід віднести і відсутність противірусної активності. Відома також сполука дицитроборат оксихінолінію, що проявляє антимікробні властивості (див. патент РФ № 2071477), зі структурною формулою: (+) O O C N O C O O C B C OH O *2 H2O 25 CH2 CH2 CH2 CH2 COOH 20 COOH COOH COOH . Дана сполука містить бор, здатна формувати комплексні сполуки з іонами металів та має бактерицидні, фунгіцидні властивості, але не є рістрегулятором та імуномодулятором, і не проявляє противірусної активності. Окрім того, відомий трис-2-оксіетиламонію фумарат (див. патент РФ № 2119384 від 27.09.1998), структурна формула: + HOOCCH = CH - COONH 30 O CCH2CH2C N OH 40 CH2CH2OH CH2CH2OH CH2CH2OH . Сполука має рістрегулюючу, імуномодулюючу активності, здатна взаємодіяти з іонами металів, але не є противірусною і не містить бор, що істотно обмежує галузь її використання. Найбільш близьким за активністю є N, N-біс-(2-гідроксилетил)сукцинамід, який синтезований, згідно патенту на винахід РФ № 2125040. Сполука має структурну формулу II: O 35 (-) CH2CH2OH CH2CH2OH . Дана речовина має рістрегулюючу та імуномодулюючу активності, взаємодіє з іонами металів, утворюючи комплекси, але не містить бор і не виявляє противірусну активність. З науково-технічної та патентної літератури заявнику невідомі борати діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот, що мають рістрегулюючу, імуномодулюючу та противірусну дію. В основу винаходу поставлено задачу - пошук нових борвмісних комплексоутворюючих речовин з класу аліфатичних карбонових кислот, розробка препаративно зручного ефективного способу їх одержання та рістрегулюючого, імуномодулюючого та противірусного засобу. Поставлена задача вирішена групою винаходів, об'єднаних єдиним винахідницьким задумом, а саме новою борвмісною органічною сполукою, способом її одержання та рістрегулюючим, імуномодулюючим та противірусним засобом. 1 UA 107774 C2 В першому винаході поставлена задача вирішена новими сполуками - боратами діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот, формули І: HOOC R2 5 R1 C(O)N(CH2CH2O)2BOH R3 , (I) де, R1= CH-CH якщо то R2=R3=H (сполука 1); , R1 = - CH - CH2 NH - CH - CH2 якщо R1 = - CH - CH2 , то R2 = -COOH, R3=C(O)N(CH2CH2O)2BOH (сполука 2); NH (CH2)2 NH - CH - CH2 якщо R1 = 15 20 25 CH2 - CH2 N(CH2)2N - CH2 10 , то R2 = -COOH, R3=C(O)N(CH2CH2O)2BOH (сполука 3); CH 2 якщо , то R2=C(O)N(CH2CH2O)2BOH; R3 = -COOH (сполука 4). В другому винаході поставлена задача вирішена в способі одержання боратів діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот формули І, що передбачає взаємодію відповідної двоабо чотириосновної комплексоутворюючої аліфатичної карбонової кислоти з діетаноламіном і борною кислотою при 155-165 °C і видалення води, що утворюється, за допомогою апарата Діна-Старка. Як двоосновну комплексоутворюючу аліфатичну карбонову кислоту використовують бурштинову кислоту, а процес здійснюють при співвідношенні бурштинова кислота: діетаноламін: борна кислота, рівному 1:0,1:0,1. Як чотириосновну комплексоутворюючу аліфатичну карбонову кислоту використовують етилендіамінтетраоцтову або етилендіаміндибурштинову, або імінодибурштинову кислоту, а процес здійснюють при співвідношенні чотириосновна комплексоутворююча аліфатична карбонова кислота: діетаноламін: борна кислота, рівному 1:2:2 відповідно. В третьому винаході поставлена задача вирішена боратами діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот формули І як рістрегулюючим, імуномодулюючим та противірусним засобом. Сполуки І, що заявляються, відрізняються від відомої сполуки ІІ наявністю однієї в складі 2гідрокси-1,3,6,2-діоксаазаборокан-6-іламідної групи (сполука 1) або двох 2-гідрокси-1,3,6,2діоксаазаборокан-6-іламідних груп і двох СООН груп, зв'язаних через структури: 2 UA 107774 C2 - CH - CH2 NH - CH - CH2 NH (CH2)2 CH2 CH2 NH N(CH2)2N - CH - CH2 5 CH2 - CH - CH CH 2 2 ; ; . Сполуки 2, 3 і 4, відповідно. Вказані відмінності в структурі сполук І і II призводять до появи у сполук І, що заявляються, нової біологічної властивості, а саме противірусної активності, а також до значного посилення рістрегулюючого та імуномодулюючого ефекту. Сполуки І, що заявляються, є похідними аліфатичних карбонових кислот і містять - C(O)N(CH CH O) BOH 10 15 20 25 2 2 2 структурний елемент . Об'єкти, що заявляються, відрізняються від сполуки II наявністю однієї (сполуки 1) або двох даних елементів і основністю (сполуки 2, 3, 4). Зазначена особливість призводить до появи у сполуки І нового типу противірусної активності, в той час як сполука II не має противірусної активності. Крім того, введення 2гідрокси-1,3,6,2-діоксаазаборокан-6-іл в структуру сполук істотно підсилює їх рістрегулюючу активність. Технічним результатом способу є одержання діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот в одну стадію без виділення діетаноламінбората або діетаноламіду з високим ступенем конверсії вихідних компонентів. Для досягнення технічного результату пропонується спосіб одержання діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот (сполуки формули І) при конденсації дво- і чотириосновних комплексоутворюючих аліфатичних карбонових кислот, діетаноламіну та борної кислоти при температурі 155-165 °C з видаленням води, що утворюється, апаратом Діна-Старка. Процес здійснюється в скляній колбі, забезпеченій термометром, механічною мішалкою і апаратом Діна-Старка. Після завантаження двоосновної карбонової кислоти, діетаноламіну і борної кислоти при молекулярному співвідношенні 1:1:1 або 1:2:2, у разі реакції чотириосновної кислоти та борної кислоти, діетаноламіну і підвищення температури до 120-130 °C відбувається розчинення карбонової кислоти в діетаноламіні з утворенням легкоплавкої, що збільшує термічну стійкість кислоти, моно- або діамонійної солі: a) HOOC- R1- COOH+NH(CH2CH2OH)2+t COOH б) HOOC R1 HOOC HOOC- R1-COONH2(CH2CH2OH)2 + 2NH(CH2CH2OH)2 COOH COOH HOOC + (HOCH2C H2)2NH2OC 30 t R1 + COONH2(CH2CH2OH) . Збільшення температури розплаву до 155-165 °C призводить до повного розчинення борної кислоти і початку конденсації з утворенням цільових продуктів. + в) HOOCR1COONH2(CH2CH2OH)+Р3ВО3+t HOOCR1C(O)N(СH2CH2O)2+ВОН+2Н2О 3 , UA 107774 C2 г) COOH HOOC R1 (HOCH2CH2)2NH2OОC + 2 Н3ВО3 C(O)N(СH2CH2O)2ВОН COOH HOOC R1 HOB(OCH2CH2)2N(O)C 5 10 15 20 25 30 35 40 45 50 t + C(O)N(СH2CH2O)2ВОН 4 H2O . Ефір борної кислоти, що утворюється, перешкоджає протіканню побічних реакцій і утворенню складних ефірів діетаноламіну та оксазолідинів, що підвищує чистоту і вихід цільових продуктів. Вода, що виділяється, в процесі конденсації виводиться з реакційної колби апаратом Діна-Старка. Час припинення виділення води є часом закінчення реакції. Принциповою відмінністю способу, що заявляється, є можливість одержання з високим виходом цільових сполук формули І, безпосередньою конденсацією компонентів, минаючи стадії синтезу проміжних сполук. Заявлений спосіб одержання сполук формули І є новим і здійснюється при конденсації двоабо чотириосновних комплексоутворюючих аліфатичних карбонових кислот, діетаноламіну і борної кислоти при температурі 155-165 °C з видаленням води, що утворюється, апаратом ДінаСтарка. Технічний результат способу, що заявляється, забезпечує сукупність суттєвих ознак, що оптимізують технологічний процес і підвищують його ефективність: високий вихід цільових продуктів; значне скорочення часу синтезу; скорочення трудовитрат. Винахід ілюструється прикладами конкретного виконання. Приклад 1. Одержання 4-(2-гідрокси-[1,3,6,2]-діоксаазаборакан-6-іл)-4-оксомасляної кислоти (сполука 1). В колбу, оснащену механічною мішалкою, термометром і апаратом Діна-Старка вміщують 11,8 г (0,1 м) бурштинової кислоти, 10,6 г (0,1 м) діетаноламіну (98,5 %) і 6,2 г (0,1 м) борної кислоти. Суміш поступово нагрівають до температури 160 °C. Після повного розчинення (розплавлення) компонентів і утворення жовтого прозорого розплаву проводять його плавне перемішування. Температура 160±5 °C підтримується протягом усього процесу і знижується до кімнатної, після припинення конденсації парів води апаратом Діна-Старка. Вихід продукту 21,2 г (92 % від теоретичного). Продукт реакції - тверда скловидна речовина світло-коричневого кольору, добре розчинна у воді. рН 10 % водного розчину 5,5. Склад одержаної сполуки підтверджений хімічним аналізом - визначено %: В - 4,51; С 41,42; Н - 5,91; N-5,86. Розраховано за формулою І у %: В - 4,68; С - 41,58; Н - 6,06; N-6,06. Приклад 2. Одержання {(2-{карбоксиметил-[2-(2-гідрокси-[1,3,6,2]-діоксаазаборокан-6-іл)-2оксоетил]-аміно}-етил)-[2-(2-гідрокси-[1,3,6,2]діоксаазаборокан-6-іл)-2-оксоетил]-аміно}-оцтової кислоти (сполука 2). В колбу, оснащену механічною мішалкою, термометром і апаратом Діна-Старка вміщають 29,2 г (0,1 м) етилендіамінтетраоцтової кислоти, 21,2 г (0,2 м) діетаноламіну (98,5 %) і 12,4 г (0,2 м) борної кислоти. Суміш поступово нагрівають до температури 160 °C. Після повного розчинення (розплавлення) компонентів і утворення жовтого прозорого розплаву проводять його плавне перемішування. Температура 160±5 °C підтримується протягом усього процесу і знижується до кімнатної, після припинення конденсації парів води апаратом Діна-Старка. Вихід продукту 46,5 г (~ 90 % від теоретичного). Продукт реакції - тверда скловидна речовина коричневого кольору, добре розчинна у воді. рН 10 % водного розчину ~ 4,4. 4 UA 107774 C2 5 10 15 20 25 30 35 40 45 50 55 60 Склад одержаної сполуки підтверджений хімічним аналізом - визначено %: В - 4,10; С 41,62; Н - 6,11; N-10,72. Розраховано за формулою І у %: В - 4,18; С - 41,71, Н - 6,18; N-10,81. Приклад 3. Одержання 2-{2-[1-карбокси-3-(2-гідрокси-[1,3,6,2]-діоксаазаборокан-6-іл)-3-оксопропіоламіно]-етиламіно}-4-[2-гідрокси-[1,3,6,2]діоксаазаборокан-6-іл)-4-оксомасляної кислоти (сполука 3). Процес відповідає процесу, описаному в прикладі 2. При заміні етилендіамінтетраоцтвої кислоти етилендіаміндибурштиновою кислотою в кількості 29,2 г (0,1 м). Вихід продукту 45,6 г (88 % від теоретичного). Продукт реакції - тверда скловидна речовина коричневого кольору, добре розчинна у воді. рН 10 % водного розчину ~ 4,5. Склад одержаної сполуки підтверджений хімічним аналізом, визначено %: В - 4,12; С - 41,58; Н - 6,10; N-10,65. Розраховано за формулою І у %: В - 4,18; С - 41,71; Н - 6,18; N-10,81. Приклад 4. Одержання 2-[1-карбокси-3-(2-гідрокси-[1,3,6,2]-діоксаазаборокан-6-іл)-3оксопропіоламіно]-етиламіно]-4-(2-гідрокси-[1,3,6,2]діоксаазаборокан-6-іл)-4-оксомасляної кислоти (сполука 4). Процес відповідає процесу, описаному в прикладі 2 при заміні етилендіамінтетраоцтової кислоти імінодибурштиновою кислотою в кількості 24,9 г (0,1 м). Вихід продукту 42,7 г (~ 90 % від теоретичного). Продукт реакції - тверда речовина коричневого кольору, добре розчинна у воді. рН 10 % водного розчину ~ 4,5. Склад одержаної сполуки доведений хімічним аналізом, визначено %: В - 4,51; С - 40,35; Н - 5,61; N-8,70. Розраховано за формулою І у %: В - 4,56; С - 40,45; Н - 5,69; N-8,85. Спосіб одержання заявлених речовин формули І є новим, препаративно зручним, заснованим на використанні продуктів основного органічного синтезу та борної кислоти. Нові препарати формули І розширюють арсенал високоефективних регуляторів росту, що підвищують стійкість рослин і тварин до вірусних захворювань. Використання борвмісних сполук передбачає їх розчинення у водних та/або інших розчинах. Дослідження швидкості розчинення сполук, що заявляються, у водних розчинах в порівнянні з бором в мінеральній формі показало їх суттєву перевагу (див. табл. 1). Для кожного з елементів є своя зона оптимальних значень рН, в якій цей елемент доступний для рослин. Бор краще засвоюється з слабокислою або близькою до нейтральної реакції середовища (див. Влияние рН на усвоение бора растениями Журнал "Зерно", апрель 2013). При рН нижче 4,5 і вище 7,5 доступність бору для рослин різко знижується. Якщо рН ґрунтового розчину складно контролювати, то рН розчину для листового підживлення легко підтримувати на оптимальному для засвоєння рослинами рівні. Більш того, в період ґрунтової посухи бор, що міститься в ґрунті, стає практично недоступним для рослин, оскільки доступним для рослин вважається лише водорозчинний бор. Ефективність позакореневих підживлень бором значно зростає, коли використовують борні добрива органічного походження на основі поліборатів і хелатуючих агентів основного типу. Вивчення значень рН розчинів та органічних борних добрив, що застосовуються у виробництві, показало переважне значення фізіологічно доступної для рослин форми сполук, що заявляються (табл. 2), де і далі 1 - борвмісна сполука бурштинової кислоти, 2 етилендіамінтетраоцтової, 3 - етилендіаміндибурштинової, 4 - імінодибурштинової кислот. Крім цього, зазвичай вода для приготування розчинів використовується жорстка, з високими показниками рН, тому доступність бору з лужних розчинів буде зниженою, а з кислих підвищеною. Борна кислота бактеріостатичну дію проявляє в 2-4 %-вих водних розчинах (див. Фридман Р.А. Технология косметики -М.: Пищевая промышленность, 1964. - 487 с. Технический словарь Том VII (8 826) http://www.ai08.org/index.php/index/7-tehnicheskiii-slovar-tom-vii.xhtmn. Для передпосівної обробки насіння застосовують розчини борної кислоти наступних концентрацій від 0,005 до 0,15 % (див. Миченкова В.Р. Справочник по удобрениям Издание 3. изд-во "Колос" - 1965. - С. 719, - 265 с). Вивчення дії сполук, що заявляються, на насінні озимої пшениці, озимого, ярого ячменю та озимого ріпаку показало (див. табл. 3), що препарати, які заявляються, індукують процеси проростання насіння. Борна кислота при обробці насіння не 5 UA 107774 C2 5 10 15 20 25 30 35 40 45 50 55 60 проявила бактеріостатичних властивостей, більше того спостерігалося слабке пригнічення насіннєвих достоїнств. Провідним критерієм оцінки того чи іншого прийому вирощування є продуктивність фотосинтетичних процесів, результатом якої є накопичення асимілянтів і зрештою господарсько-корисної частини врожаю. Дослідами встановлено, що препарати, які заявляються, при обприскуванні посівів цукрових буряків, соняшнику, кукурудзи на зерно та озимого ріпаку сприяли достовірному збільшенню врожаю (див. табл. 4). Проведено дослідження противірусної активності борвмісних препаратів. Перед визначенням противірусної активності борвмісних препаратів було досліджено токсичність препаратів з використанням культури інфузорій Colpoda steinii. Токсичність досліджуваних препаратів визначали за їхнім впливом на життєдіяльність культури інфузорій Colpoda stenii (див. патент України №15629. Спосіб оцінки ступеню цитотоксичності біологічно активних сполук і фармакологічних препаратів). Для проведення дослідів розкривали два флакони з сухою культурою Colpoda steinii і один флакон з живильним середовищем. У кожен флакон з Colpoda steinii додавали по 2 мл живильного середовищу флакони закривали пробками і вміщали в термостат при температурі 26-28 °C на 24 години. Перед дослідженням культуру Colpoda steinii витримували 15 хвилин на світлі, а потім розглядали під світловим мікроскопом методом висячої чи роздавленої краплі. Для підтвердження життєздатності культури (при збільшенні 80-150х) повинно бути не менше 6 клітин інфузорій, які активно рухаються в полі зору. У флакон з активною культурою вносили 2 мл досліджуваних розчинів препаратів і перемішували. В контрольний флакон з активною культурою Colpoda steinii вносили 2 мл живильного середовища. Критерієм визначення токсичності був час від початку впливу випробуваних препаратів на культуру інфузорій Colpoda steinii до загибелі більшості (90 % і більше) колпод, яка констатується на підставі повного припинення руху колпод і наявності їх розпаду. В контрольній пробі всі колподи повинні залишатися рухливими. Токсичними вважали ті речовини (об'єкти), при додаванні яких загибель інфузорій наступала в інтервалі до 10 хвилин спостереження. Слаботоксичні - до 3-х годин спостереження. Досліджувані препарати вважалися нетоксичними, якщо через 3 години спостереження всі найпростіші залишалися рухливими. У зв'язку з тим, що дослідження проводилися з використанням культури тканини, рівень рН підтримуючого глюкозо-желатинового середовища має становити 7,2-7,4 після додавання до нього досліджуваних препаратів. Перед проведенням експериментів необхідно перевірити рН досліджуваних препаратів і довести розчини препаратів до фізіологічного значення рН 7,2-7,4. Після доведення рН розчинів до фізіологічного значення визначали протигрипозну активність препаратів. Препарат № 1 (борвмісна похідна бурштинової кислоти), первинний рН якого становило 5,5. Цей препарат розводили (розведення в 54,72 рази) до кінцевої концентрації 870 мг/мл в якому доводили рН до 7,0. Препарат № 2 (борвмісна похідна етилендіамінтетраоцтової кислоти), первинне рН становило 4,4. Препарат розводили (розведення в 34013,61 разу) до первинної концентрації 1,47 мг/мл, в якому доводили рН до 7,0. Препарат № 3 (борвмісна похідна етилендіаміндибурштинової кислоти), первинне значення рН якого становило 4,5, розводили (розведення 32085,72 разу) до кінцевої концентрації 1,51 мг/мл, в якому доводили рН до 7,0. Препарат № 4 (борвмісна похідна імінодибурштинової кислоти) первинне значення рН якого становило 4,5, розводили (розведення 35164,21 разу) до кінцевої концентрації 1,45 мг мл, в якому доводили рН до 7,0. У цих концентраціях досліджували токсичну дію препаратів відносно до культури інфузорій в п'ятикратній повторності. Отримані дані, наведені в таблиці 5. Протигрипозну активність препаратів in vitro вивчали щодо вірусу грипу А/Гонконг/1/68 (H3N2), використовуючи культуру тканини хоріон-алантоїсних оболонок (ХАО) 11-12 добових курячих ембріонів, оскільки цю культуру можна вважати найбільш наближеною до рівня цілого організму, яким с курячий ембріон (див. Доклинические исследования лекарственных средств. Методические рекомендации: [ред. А.В. Стефанов]. -К.: Авиценна, 2002. - С. 395-420; Мальцева А.И. Репродукция вирусов гриппа в культуре ткани ХАО, прикрепленной к скорлупе/ А.И. Мальцева, В.Е. Аграновская, Я.С. Шварцман// Лаб. Дело. - 1973. - № 11. - С. 689-690]. Крім того, використання культури тканини ХАО є більш економічним методом порівняно з використанням курячих ембріонів для визначення противірусної дії препаратів. Накопичення вірусу грипу проводили в хоріон-алантоїсній оболонці 11-12-денних курячих ембріонів стандартним методом. Для проведення досліджень з вивчення противірусної дії 6 UA 107774 C2 5 10 15 20 25 30 препаратів відбирали вірусовмісну аллантоїсну рідину з великим вмістом вірусних частинок. При цьому вміст вірусу був не нижче 100 lg ТІД50. Визначення протигрипозної активності виконується в два етапи: 1 етап - протягом 24 годин препарати впливають на вірус в певних концентраціях при 37 °C; 2 етап - проводиться визначення вірусу після 24-х годинної дії препаратів. Для цього вірус розчиняється десятикратно, щоб визначити наскільки досліджувана доза препарату пригнічує репродукцію вірусів. У зв'язку з тим, що після дії досліджуваних препаратів вірусних частинок в досліді стало менше, то визначення їх вірусної репродукції проводять протягом 48 годин при 37 °C і потім визначають скільки вірусу залишилося в досліді в порівнянні з контролем. Після видалення фрагментів ХАО з лунок полістиролових панелей до вірусовмісної рідини додається 1 % розчин курячих еритроцитів для визначення гемаглютинації (ГА). Вплив препаратів на репродукцію вірусів грипу досліджували, розчиняючи препарати або хімічні сполуки в глюкозо-желатиновому підтримуючому середовищі. Вірусовмісну рідину з попередньо визначеним інфекційним титром, розводили в глюкозо-желатинову середовищі, що містить досліджуваний препарат (дослід), або не містить цей препарат (контроль). Розведення вірусу 10-1, 10-2, 10-3 робили на глюкозо-желатиновому підтримуючому середовищі ХАО, розведення вірусів 10-4, 10-5 робили на розчині препаратів в певній кінцевій концентрації, а розведення вірусу 10-6 робили на середовищі ХАО. Це розведення використовували для інфікування фрагментів ХАО (по 2 на кожен експеримент), які прикріплені до шкаралупи, і розміщені в лунках полістиролових панелей. Після термостатування 24 години при 37 °C (1-й етап) контрольні та дослідні зразки окремо з'єднувалися, і в них визначали титр інфекційного вірусу методом титрування в культурі тканини ХАО. Титрування вірусу грипу після впливу на вірус досліджуваного препарату проводили в культурі тканини ХАО, визначаючи найбільше розведення вірусовмісної рідини, при якому ще відбувається репродукція вірусу (2-й етап). Тобто, десятикратними розведеннями цих зразків інфікували фрагменти ХАО, які розміщені в лунки полістиролових панелей. Полістиролові панелі розміщували в термостаті при 37 °C. Після 48 годин термостатування визначали наявність вірусу в лунках за результатами реакції гемаглютинації (РГА). Розрахунок ТІД50 в експериментах in vitro проводили за методом Кербера в модифікації Ашмаріна (див. Ашмарин И.П. Вычисление ЭД50 при малом числе подопытных животных/ И.П. Ашмарин// Ж. микробиол. - 1959. - № 2. - С. 102-108) за формулою: lg TIД50 L d(S 0,5) , де L - первісне розведення в досліді; d - різниця між послідовними lg розведень; 35 40 S - сума пропорцій тест-об'єктів, які дали позитивний результат. Препарат № 1 досліджували в кінцевій концентрації 45 мкг/мл, препарат № 2 досліджували в кінцевій концентрації 312 мкг/мл, а препарати № 3 та № 4 в кінцевій концентрації 315 і 300 мкг/мл відповідно. Як видно з таблиці 6, борвмісні препарати в досліджуваній концентрації пригнічували на 3,54,0 lg ТІД50 (більш ніж 1000 разів) репродукцію вірусу грипу А/Гонконг/1/6 8 (H 3N2) в культурі тканини хоріон-алантоїсної оболонки (ХАО) 11-12 добових курячих ембріонів. В таблиці 6 наведено наявність інфекційного вірусу після 24-х годинного циклу репродукції вірусу грипу в присутності препаратів. Таблиця 1 Швидкість розчинення борвмісних сполук Концентрація розчину, % 1 %-ий розчин 2 %-ий розчин Сполука 1 Сполука 2 Сполука 3 Сполука 4 16 сек. 22 сек. 15 сек. 20 сек. 14 сек. 18 сек. 18 сек. 23 сек. 45 7 Борна кислота 410 сек. 450 сек. Бура 55 сек. 61 сек. UA 107774 C2 Таблиця 2 Залежність рН розчину від діючої речовини борвмісних сполук Досліджувані Сполука Сполука Сполука Сполука сполуки 1 2 3 4 рН 5,5 4,4 4,5 4,5 Квантум Бор- Бормоноетаноламін Динатрійоктаборат Актив 7,5+8,5 7,5+9,0 7,7+8,5 Таблиця 3 Вплив борвмісних сполук на фітоекспертні та насіннєві показники насіння озимої пшениці, озимого, ярого ячменю та озимого ріпаку Обробка насіння Зовнішня зараженість, кільк. спор на 100 Загальна зараженість на насінин 100 насінин Енергія гельмі пророста Схожість тв. альтерна гельмінто фузаріо альтер ння фузаріоз нтоспорі головня ріоз споріоз з наріоз оз Озима пшениця, сорт Антонівка Контроль (обробка насіння водою) Борна кислота 0,05 % Сполука 1 Сполука 2 Сполука 3 Сполука 4 Контроль (обробка насіння водою) Борна кислота 0,05 % Сполука 1 Сполука 2 Сполука 3 Сполука 4 Контроль (обробка насіння водою) Борна кислота 0,05 % Сполука 1 Сполука 2 Сполука 3 Сполука 4 Контроль (обробка насіння водою) Борна кислота 0,05 % Сполука 1 Сполука 2 Сполука 3 Сполука 4 11,1 2,0 26,7 38,7 62,7 89,0 5,6 7,0 108,3 44,4 2,7 2,8 2,5 66,7 13,9 0,7 5,6 3,5 57,8 8,3 0,7 5,6 2,7 52,2 11,1 0,8 2,8 4,2 44,4 16,7 1,1 Озимий ячмінь, сорт Достойний 28,7 28,0 18,7 42,7 48,7 36,7 22,0 14,7 20,7 21,0 54,7 77,7 87,2 94,7 86,7 88,0 90,6 92,7 97,3 90,7 5,6 2,0 40,0 30,0 82,0 94,3 2,8 77,8 13,9 1,9 2,8 55,6 8,3 1,5 2,8 66,7 11,1 1,3 0,0 19,4 8,3 0,0 0,0 50,0 8,3 0,7 Яровий ячмінь, сорт Адапт 38,7 16,7 14,7 18,7 27,3 29,3 18,0 19,3 12,0 20,2 82,0 94,7 92,0 94,0 63,3 93,7 96,7 97,3 96,3 97,0 24,0 194,6 96,7 97,3 13,9 0,0 36,1 16,7 4,7 111 0 33,3 2,8 0,7 8,3 0,0 63,9 2,8 0,7 5,6 0,0 105,5 5,6 0,0 0,0 0 36,1 0,0 9,3 Озимий ріпак, сорт Чемпіон України 19,3 1 80,0 18,7 106,0 22,0 112,7 20,0 88,6 22,7 90,7 89,3 90,7 70,0 7,3 45,3 98,0 94,7 88,7 19,3 76,7 13,9 5,6 130,6 8,3 6,2 46,2 12,0 55,6 78, 0 13,9 8,3 5,6 5,6 2,8 5,6 2,8 2,8 2,8 2,8 124,4 83,3 55,6 36,1 36,1 8,3 2,8 2,8 2,8 0,0 6,3 4,7 2,7 1,3 1,2 48,7 31,3 30 26 10,7 0,0 1,3 2,7 14,7 0,7 51,7 65,2 68,4 69,1 62,0 74,2 81,2 88,4 92,1 90,5 2,8 0 2,8 0,0 2,8 13,9 7,1 5,6 0,0 83,3 105,6 102,8 8 47,2 11,1 11,1 5,3 UA 107774 C2 Таблиця 4 Зміна врожайності цукрового буряку, соняшника, кукурудзи на зерно, озимого ріпаку при обприскуванні борвмісними сполуками Препарати Ріпак: Цукровий буряк 1обприскування у й - 6-8 листків; 2-й Соняшник, початок Кукурудза, фазу зеленого - змикання листя в цвітіння формування волоті бутона та - у фазу рядах опадання квіткових пелюсток Контроль (обробка посівів водою) Борна кислота 0,05 % Сполука 1 Сполука 2 Сполука 3 Сполука 4 512,5 16,2 46,8 22,1 536,3 18,8 51,6 24,3 556,8 542,6 568,9 571,0 19,5 18,9 19,3 19,1 52,9 54,6 53,4* 55,1 24,9 26,3 25,8 26,1 Таблиця 5 Рівень токсичності досліджуваних борвмісних препаратів по відношенню до культури інфузорій Colpoda steinii № п/п Препарат в кінцевій концентрації Препарат № 1 (470 мкг/мл) Препарат № 2 (1,41 мг/мл) Препарат № 3 (1,51 мг/мл) Препарат № 4 (1,45 мг/мл) 1 2 3 4 Рівень токсичності через 10 хвилин Слаботоксичний Не токсичний Слаботоксичний Слаботоксичний Рівень токсичності через 3 години Слаботоксичний Не токсичний Слаботоксичний Слаботоксичний Таблиця 6 Вплив борвмісних препаратів на репродукцію вірусу грипу А/Гонконг/1/68 (H3N2) на тканинній культурі ХАО Повторність 1 2 3 Контроль lg ТІД50 4,0 4,0 4,5 Препарат № 1 Препарат № 2 Препарат № 3 Препарат № 4 lg ТІД50 lg ТІД50 lg ТІД50 lg ТІД50 0,5 0,5 0,5 0,5 0,5 0,5 0,5 0,5 0,5 0,5 0,5 0,5 ФОРМУЛА ВИНАХОДУ 5 1. Борати діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот формули І: HOOC R2 10 R1 C(O)N(CH2CH2O)2BOH R3 , (I) де, якщо R1= CH-CH , то R2 = R3 = H; 9 UA 107774 C2 якщо R1 = - CH - CH2 NH - CH - CH2 , то R2 = -COOH, R3 = C(O)N(CH2CH2O)2BOH; якщо R1 = - CH - CH2 NH (CH2)2 NH 5 - CH - CH2 , то R2 = -COOH, R3 = C(O)N(CH2CH2O)2BOH; якщо R1 = N(CH2)2N - CH2 10 15 20 CH2 - CH2 CH2 , то R2 = C(O)N(CH2CH2O)2BOH; R3 = -COOH. 2. Спосіб одержання боратів діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот формули І за п. 1, що передбачає взаємодію відповідної двоабо чотириосновної комплексоутворюючої аліфатичної карбонової кислоти з діетаноламіном і борною кислотою при 155-165 ºС і видалення води, що утворюється, за допомогою апарата Діна-Старка. 3. Спосіб за п. 2, який відрізняється тим, що як двоосновну комплексоутворюючу аліфатичну карбонову кислоту використовують бурштинову кислоту, а процес здійснюють при співвідношенні бурштинова кислота:діетаноламін:борна кислота, рівному 1:1:1. 4. Спосіб за п. 2, який відрізняється тим, що як чотириосновну комплексоутворюючу аліфатичну карбонову кислоту використовують етилендіамінтетраоцтову або етилендіаміндибурштинову, або імінодибурштинову кислоту, а процес здійснюють при співвідношенні чотириосновна комплексоутворююча аліфатична карбонова кислота:діетаноламін:борна кислота, рівному 1:2:2, відповідно. 5. Борати діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот формули І за п. 1 як рістрегулюючий, імуномоделюючий та противірусний засіб. 25 Комп’ютерна верстка А. Крижанівський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 10
ДивитисяДодаткова інформація
МПК / Мітки
МПК: A01N 55/08, A61P 37/02, A61P 31/16, C07F 5/04
Мітки: чотириосновних, діетаноламідів, комплексоутворюючих, дво, борати, аліфатичних, карбонових, кислот
Код посилання
<a href="https://ua.patents.su/12-107774-borati-dietanolamidiv-kompleksoutvoryuyuchikh-dvo-i-chotiriosnovnikh-alifatichnikh-karbonovikh-kislot.html" target="_blank" rel="follow" title="База патентів України">Борати діетаноламідів комплексоутворюючих дво- і чотириосновних аліфатичних карбонових кислот</a>
Попередній патент: Спосіб отримання колоїдного розчину наночасток золота
Наступний патент: Сівалка навісна селекційно-насінницька снс-16ап
Випадковий патент: Підфуркальний провідник