Мезилат 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну та поліморфні форми
Формула / Реферат
1. 4-Аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну мезилат формули
.
2. Мезилатна сіль за п. 1, яка відрізняється тим, що в процесі диференціальної сканувальної калориметрії вона проявляє ендотермічний пік при приблизно 279°C .
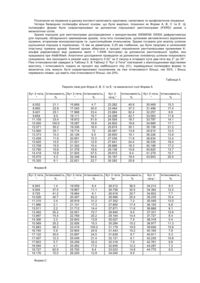
3. Мезилатна сіль за п. 1 або п. 2, яка характеризується порошковою рентгенограмою, отриманою при опроміненні рентгенівськими променями K-альфа1 радіоактивної міді з довжиною хвилі 1.5406Å, що має наступні головні піки:
Кут
2-тета °
Інтенсивність %
7.392
22.9
14.733
22.6
14.813
40.1
17.694
31
18.964
40.5
19.297
57.9
20.265
51
21.414
40
22.136
24
22.934
32.8
23.842
49.4
24.795
100
27.012
30.3
28.673
22.3
29.305
24.6
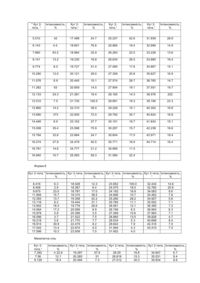
4. Безводна кристалічна форма вільної основи 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну (позначена як Форма E), зразок якої містить більш ніж 90% однієї поліморфної форми, яка відрізняється тим, що вона проявляє ендотермічний пік при приблизно 229°C та характеризується порошковою рентгенограмою, отриманою при опроміненні рентгенівськими променями K-альфа1 радіоактивної міді з довжиною хвилі 1.5406Å, яка має наступні головні піки:
Кут 2-тета °
Інтенсивність %
9.675
23.0
16.914
30.8
19.315
38.5
19.358
422
19.444
31.1
19.778
26.6
23.852
100.0
25.280
28.2
32.760
25.6
5. Форма вільної основи за п. 4, яка відрізняється тим, що зразок її містить більш ніж 90 % однієї поліморфної форми.
6. Фармацевтична композиція, яка містить 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі безводної вільної основи або мезилатної солі, як визначено в будь-якому з пунктів з 1 до 5, у суміші з фармацевтично прийнятним ад‘ювантом, розріджувачем або носієм.
7. 4-Аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі безводної вільної основи або мезилатної солі, за будь-яким з пунктів 1 - 5, для використання як фармацевтичного засобу.
8. Застосування 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну у формі безводної вільної основи або мезилатної солі, як визначено в будь-якому з пунктів з 1 до 5, у виробництві медикаменту для лікування доброякісної гіперплазії простати.
9. Спосіб лікування доброякісної гіперплазії простати, який полягає в уведенні терапевтично ефективної кількості 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну у формі безводної вільної основи або мезилатної солі, як визначено в будь-якому з пунктів з 1 до 5, пацієнту, який страждає від такого розладу.
10. Спосіб одержання мезилату 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну, як визначено у п. 1, який полягає в додаванні метансульфонової кислоти до суспензії або розчину 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну формули
в придатному розчиннику та збиранні осадженої твердої речовини.
11. Спосіб за п. 10, в якому розчин 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну підтримують при температурі, вище кімнатної температури, перед додаванням метансульфонової кислоти.
12. Спосіб за п. 10 або п. 11, в якому використовуваним розчинником є суміш бутанону та води.
13. Спосіб за будь-яким з пунктів 10, 11 та 12, в якому розчинником є суміш 10:1 за об‘ємом бутанону та води.
14. Спосіб за п. 12 або п. 13, в якому проводять стадії:
(a) нагрівання суспензії 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну в суміші бутанон/вода до кипіння;
(b) додавання суміші бутанон/вода до утворення розчину;
(c) охолодження розчину;
(d) додавання метансульфонової кислоти; та
(e) збирання отриманої твердої речовини фільтрацією.
15. Спосіб за будь-яким з пунктів з 10 до 14, в якому 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін використовують у Формі E, як визначено у п. 4 або п. 5.
Текст
Даний винахід стосується нових солей, придатних для лікування. Більш конкретно даний винахід стосується мезилату 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2піридил)хіназоліну, способів їх одержання, їх використання та композицій, що їх містять. Даний винахід також стосується нових негідратованих поліморфних форм вільної основи. Аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-Піридил)хіназолін має формулу і описаний в міжнародній заявці з номером публікації WO 98/30560 (див. Приклад 19) як придатний для лікування доброякісної гіперплазії простати. В загальних рисах заявка стосується to фармацевтично прийнятних солей і описує хлоридні, бромідні та фосфатні солі. На жаль, 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2піридил)хіназолін проявляє деякі несприятливі фізичні властивості. Зараз відомо, що він зустрічається в декількох різних формах. В деяких випадках його розчинність у воді є достатньо низькою і достатньо складно отримати його відтворювано в одній і тій же формі, яка інколи отримується у гідратованій формі. Крім того, було встановлено, що деякі форми вільної основи є достатньо гігроскопічними. Такі властивості є несприятливими для створення лікарської субстанції, тому що, зокрема, .матеріал повинен вироблятися з відтворюваною уніфікованою якістю для того, щоб задовольняти обов'язковим вимогам. На даний час отримана мезилатна сіль 4-аміно-6,7-диметокси-2-(5-Метансульфонамідо-1,2,3,4тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну, що має формулу Ця речовина має деякі неочікувані переваги над вільною основою і несподівано було виявлено, що вона має унікальну комбінацію властивостей, які роблять її ідеальною для розвитку як лікарської субстанції. Фахівцю буде зрозумілим, що "мезилат" є альтернативним терміном для "метансульфонату". Мезилатна сіль має високу температуру плавлення і є кристалічною твердою речовиною, яка не має будьяких гідратних або сольватних форм. Вона є ізоморфною, тобто, існує в одній поліморфній формі, і проявляє хорошу стабільність у широкому інтервалі умов, наприклад, при високій інтенсивності світла. Вона має прийнятну розчинність та характеристики розкладу і може бути економічно одержуватися та перероблятися, забезпечуючи придатні тверді дозовані форми лікарського засобу. її гігроскопічність є значно нижчою, ніж вільної основи (визначена як температура плавлення 198°С її поліморфа), в широкому інтервалі відносної вологості. Мезилатна сіль є мономорфною і не утворює гідратів; обидві ці риси, зокрема, представляють собою переважні властивості мезилатної солі. В Таблицях 1 - 3, представлених нижче, наведені фізичні властивості мезилату 4-аміно-6І7-диметокси-2(5-метансульфонамідо-1,2)3,4-тетрагідроізохінол-2-іл)-5-(2-йіридил)хіназоліну та деяких форм вільної основи. Таблиця 1 Фізичні властивості мезилатної солі Форма Мезилатна сіль Температура Гігроскопічність плавлення Кристалічність % (ваг./ваг.) (°С) при 90% ВВ 279 Кристалічна 1.1 Таблиця 2 Розчинність мезилатної солі та форм вільної основи (мікрограм/мл) Розчинник Вільна основа (т.пл. 198°С) Гідратна форма вільної основи Мезилатна сіль 420 12 880 36 4 120 Вода при 22°С 0.9% хлорид натрію при 22'С Таблиця З Гігроскопічність форм мезилатної солі та вільної основи Форма Вільна основа (т.пл. 198°С) Гідратна форма вільної основи Мезилатна сіль (т.пл. 279°С) Поглинання ваг./ваг.) при вологи (% 30°С та 45% ВВ 1.39 11.24 0.56 Велика кількість безводних кристалічних форм 4-аміно-6,7-диметокси-2-(5-іИЄтансульфонамідо-1,2,3,4тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну (вільної основи) описані в рамках цієї заявки. Ці безводні поліморфи позначені як Форма А, Форма В, Форма С та Форма Ε в Таблиці 4, наведеній нижче. Форма D, яку наведено для порівняння, є гідратною формою і існує як дигідрат. Таблиця 4 Поліморфні форми вільної основи Точка Гігроскопічність Форма плавлення Кристалічність % (ваг./ваг.) (°С) при 90% ВВ Форма 198 кристалічна 2.2 А Форма 218 кристалічна 0.27 В Форма 147 кристалічна С Форма 229 кристалічна 0.045 Ε Форма немає кристалічна 12.8 D При дегідратації гідратована форма (Форма D) стає аморфною. Безводні поліморфні форми даного винаходу також є значно менше гігроскопічними, ніж гідратована форма вільної основи. З цих причин Форми В та Ε мають високі температури плавлення і низьку гігроскопічність. Винахід охоплює Форму Е, зразок якої містить більш ніж 90% однієї поліморфної форми. Переважно зразок Форми Ε містить більш ніж 99% однієї поліморфної форми. ЗМІНЕНА СТОРІНКА Зараз вважається,що тверда форма 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну, яка була одержана спочатку відповідно до методики, описаної в WO 98/30560 (див. Приклад 19), була сумішшю Форм В та Е, можливо у співвідношенні 1:1 (на основі дослідження за допомогою диференціальної сканувальної калориметрії, в якій зареєстровано піки ендодерм при 220 та 227°С). Після створення найбільш стабільної Форми Ε у чистому вигляді цілком ймовірно, що в майбутньому переважно буде виготовлятися ця форма, коли буде повторено вищенаведене отримання 4аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну. Також у об'єм даного винаходу радіоактивно мічені похідні, інші ізотопні форми та таутомери 4-аміно-6,7диметокси-2-(5-метансульфонамщо-1,2,3,4-тетрапдро13ох1нол-2-т)-5-(2-піридил)хіназоліну у формі Форми Е, як визначено вище, або мезилатної солі. 4-Аміно-6,7-Диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено вище, або у формі мезилатної солі має фармакологічну активність по відношенню до тварин. Він може бути використаний для лікування цілого ряду стані у тому числі гіпертензії, інфаркту міокарду, чоловічої ректальної дисфункції, гіперліпідемії, кардіальної аритмії та доброякісної гіперплазії ірростати. Останній стан представляє найбільший інтерес. Таким чином, згідно з іншим аспектом винаходу, передбачується спосіб лікування доброякісної гіперплазії простати, який полягає в уведенні терапевтично ефективної кількості 4-аміно-6)7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол2-іл)-5-(2-піридил)хіназолін у формі Форми Ц, як визначено вище, або мезилатної солі пацієнту, який страждає від такого розладу. Згідно з подальшим аспектом винаходу, передбачується 4-аміно-6,7-диметокси-2-(f-метансульфонамідо1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі фрми Е, як визначено вище, або мезилатної солі для використання у фармацевтиці; та д|ія використання у лікуванні доброякісної гіперплазії простати. Згідно з подальшим аспектом винаходу, передбачується використання 4-аміно-6,7-:диметокси-2-(5метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну у формі Форми Е, як визначено вище, або мезилатної солі для виробництва медикаменту ідля лікування доброякісної гіперплазії простати. 4-Аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено вище, або мезилатної солі може вводитися лише сам, але загалом буде уводитися в суміші з придатним фармацевтичним екціпієнтом, розбавником або носієм, вибраним відносно призначеного шляху уведення та стандартної фармацевтичної практики. Таким чином, згідно з подальшим аспектом винаходу, передбачується фармацевтична композиція, яка містить 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-|,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено лище, або мезилатної солі у суміші з фармацевтично прийнятним адьювантом, ірзбавником або носієм. Композиція переважно буде містити менше ніж 50% за вагою 4-аміно-6,7-диметокси2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-г|іридил)хіназоліну як Форми Е, визначеної вище, або у формі мезилатної солі. Наприклад, 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2піридил)хіназолін у формі Форми Е, як визначено вище, або л|езилатної солі може бути уведений перорально, буккально або сублінгвально у формі таблеток, капсул, овул, еліксирів, розчинів або суспензій, які можуть містити смакові або забарвлювальні агенти, для застосування зі швидким, уповільненим або контрольованим вивільненням. Пероральне уведення представляє особливий інтерес. 4-Аміно-6,7-диметокси-2-(5метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено вище, мезилатної солі може також бути уведений шляхом інтракавернозної ін'єкції. Такі таблетки можуть містити екціпієнти, такі як мікрокристалічна целюлоза, лактоза, цитрат натрію, карбонат кальцію, двоосновний фосфат кальцію та гліцин, дезінтегранти, такі як крохмаль (переважно кукурудзяний, картопляний або тапіоковий крохмаль), натрію крохмальгліколят, кроскармелоза натрію та певні комплексні силікати, а також зв'язувальні агенти гранулювання, такі як полівінлпіролідон, гідроксипропілметилцелюлоза (НРМС), гідроксипропілцелюлоза (НРС), цукроза, желатин та гуміарабік. Крім того, можуть бути включені мастильні агенти, такі як стеарат магнію, стеаринова кислота, гліцерилбехенат і тальк. Тверді композиції подібного типу можуть також застосовуватися як наповнювачі в желатинових капсулах. В цьому випадку перевага надається таким екціпієнтам, як лактоза, крохмаль, целюлоза, молочний цукор або високомолекулярні-поліетиленгліколі. Для водних суспензій та/або еліксирів 4-аміно-6,7-диметокси-2-(5метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено вище, або мезилатної солі може бути скомбінований з різними підсоложувальними або смаковими агентами, забарвлювальними речовинами або барвниками, емульсифікаторами і/або суспендувальними агентами та розбавниками, такими як вода, етанол, пропіленгліколь та гліцерин, та їх комбінаціями. 4-Аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрапдроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено вище, або мезилатної солі може також бути уведений парентерально, наприклад, внутрішньовенно, внутрішньоартеріально, інтраперитонально, інтратекально, інтравентрикулярно, інтрастернально, інтракраніально, внутрішньом'язово або підшкірно, або може бути уведений шляхом інфузій. Найкраще використовувати його у формі стерильного водного розчину, який може містити інші речовини; наприклад, достатню кількість солей або глюкози для того, щоб зробити розчин ізотонічним з кров'ю. При необхідності до водних розчинів повинні додаватися буферні розчини (переважно до рН від 3 до 9). Одержання придатних парентеральних композицій в стерильних умовах легко проводиться за стандартними фармацевтичними методиками, добре відомими фахівцям даної галузі. Для перорального та парентерального уведення людям рівень денної дози 4-аміно-6,7-диметокси-2-(5метансульфонамідо-112,3)4-тетрагідроізохінол-2-іл)-5-(2-іііридил)хїназоліну у формі Форми Е, як визначено вище, або мезилатної солі зазвичай руде у межах від приблизно 0.01 до 10 мг/кг (в одиничній або розподілених дозах) і Переважно від приблизно 0.01 до 0.5 мг/кг, призначений від 1 до 4 разів на день. Таким чином, таблетки або капсули 4-аміно-6,7-Диметокси-2-(5-метансульфонамідо-1,2,3,4тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну у формі Форми Е, як визначено вище, або мезилатної солі можуть містити від приблизно 0.1 мг до 500 мг активної сполуки для одноразового уведення або дворазового, або більшої кількості уведень у разі необхідності. У будь-якому випадку лікар буде визначати фактичну дозу, яка буде найбільш прийнятною для конкретного пацієнта, і буде залежати від віку, ваги та реакції конкретного пацієнта. Вищенаведені дозування є прикладами фередньостатистичного випадку. Звичайно можуть бути окремі випадки, в яких заслуговують уваги вищі або нижчі інтервали доз, і такі інтервали лежать в межах цього винаходу. 4-Аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено вище, або мезилатної солі може також бути уведений інтраназально або шляхом інгаляцій і зручним чином доставляється за допомогою інгалятора з сухим порошком або аерозольного спрею з герметичного контейнеру, помпи, спрею або розпилювача з використанням придатного пропелента, наприклад, дихлордифторметану, трихлорфторметану, дихлортетрафторетану, гідррфторалкану, такого як 1,1,1,2-тетрафторетан (HFA 134A [торгова марка]) або 1,1,1,2,3,3,3-гептафторпропан (HFA 227EA [торгова марка]), діоксиду вуглецю або іншого придатного газу. У випадку герметичного аерозолю дозована одиниця може бути визначена шляхом застосування клапану для доставки дозованої кількості. Герметичний контейнер, помпа, спрей або розпилювач можуть містити розчин або суспензію активної сполуки, використовуючи, наприклад, суміш етанолу та пропеленту, такого як розчинник, який може додатково містити лубрикант, наприклад, триолеат сорбітану. Капсули та картриджі (зроблені, наприклад, з желатину) для використання в інгаляторі або Інсуфляторі можуть бути сформульовані таким чином, щоб вони містили порошкову суміш 4-аміно-6,7диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну у формі Форми Е, як визначено вище, або мезилатної солі та придатного порошкового носія, такого як лактоза або крохмаль. Аерозольні композиції або композиції у вигляді сухого порошку переважно скомпоновані таким чином, що кожна відміряна доза або "пуф" містить від 20 мкг до 4 мг 4-аміно-6,7-диметокси-2-(5-метансульфонамідо1,253,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну у формі Форми Е, як визначено вище, або мезилатної солі для доставки пацієнту. Загальна денна доза аерозолю буде у межах від 20мкг до 20мг, яка |ложе уводитися в одиничній дозі або, більш звичайно, у розподілених дозах протягом дня. Альтернативно, 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4Тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено вище, або мезилатної солі може уводитися у формі супозиторіїв або песаріїв, або можуть бути застосовані місцево у формі лосьйону, розчину, крему, мазі або пильного порошку. 4-Аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2І3,4тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено вище, або мезилатної солі може також уводитися трансдермально, використовуючи, наприклад, шкірний пластир. Він може також бути уведений окулярним шляхом, зокрема, для лікування очей. Для офтальмологічного використання, він може бути сформульований у вигляді мікронізованих суспензій в ізотонічному стерильному соляному розчині з необхідним рН або, переважно, у вигляді розчинів в ізотонічному стерильному соляному розчині з необхідним рН, при необхідності у комбінації з консервантами, такими як бензилалконійхлорид. Альтернативно, він може бути сформульований на мазевій основі, такій як вазелін. Для місцевого використання на шкірі 4-аміно-6,7-диметокси-2-(5-л|етансульфонамідо-1,2,3,4тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Ε, як визначено вище, або мезилатної солі може сформульований у вигляді придатної мазі, яка містить активну сполуку, суспендовану або розчинену, наприклад, у суміші однієї або декількох наступних речовин: мінеральне масло, рідкий петролатум, білий петролатум, пропіленгліколь, поліоксиетиленполіоксипропілен, здатний до емульгування віск та вода. Альтернативно, він може бути сформульований у вигляді придатного лосьйону або крему, суспендований або розчинений, наприклад, у суміші однієї або декількох наступних речовин: мінеральне масло, моностеарат сорбітану, поліетиленгліколь, рідкий парафін, полісорбат 60, цетілові естери парафіну, іртеарильний спирт, 2октилдодеканол, бензиловий спирт та вода. Винахід в подальшому охоплює спосіб одержання 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4тєтрагідроізохінол-2-їл)-5-(2-піридил)хіназолін мезилату, як визначено вище, який полягає у додаванні метансульфонової кислоти до суспензії або розчину 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну формули в придатному розчиннику та збиранні осадженої твердої речовини. Переважні умови процесу включають: (a) розчин 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2 Д4-тетрагідроізохінол-2-іл)-5-(2піридил)хіназоліну підтримують при температурі, вище кімнатної, перед додавання метансульфонової кислоти; та (b) використовуваний розчинник є сумішшю бутанону та води, наприклад суміш 10:1 (за об'ємом) бутанону та води. Більш конкретно процес може бути визначений як такий, що включає стадії: (a) нагрівання суспензії 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5(2-піридил)хіназоліну у суміші бутанон/вода до кипіння; (b) додавання суміші бутанон/вода до отримання розчину; (c) охолодження розчину; (d) додавання метанеульфонової кислоти; та (є) збирання одержаної твердої речовини фільтрацією, У вищенаведених процесах перевага надається випадку, коли 4-аміно-6»7-диметокси-2-(5метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін присутній у Формі Е, як визначено вище, хоча деякі з цільових продуктів повинні отримуватися незалежно від вихідної форми. Рецептурні композиції винаходу можуть також містити інгібітор людської 5-а редуктази [див. міжнародну патентну заявку WO-A-95/28397], або 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін у формі Форми Е, як визначено вище, або мезилатної солі може бути представлений у фармацевтичній упаковці, яка також містить інгібітор людської 5-а редуктази у вигляді комбінованого препарату для одночасного, окремого або послідовного застосування. Посилання на лікування в даному контексті включають куративне, паліативне та профілактичне лікування. Чотири безводних поліморфи вільної основи, що були виділені, позначені як Форми А, В, С та Е. Ці поліморфні форми були охарактеризовані за допомогою порошкової рентгенограми (PXRD) разом з мезилатною сіллю. Зразки порошків для рентгенограми досліджувалися з використанням SIEMENS D5000 дифрактометра для порошків, обладнаного замінювачем зразків, тета-тета гоніометром, щілинами автоматичного відхилення променя, вторинним монохроматором та .сцинтиляційним лічильником. Зразки готували для аналізу шляхом ущільнення порошка в порожнинах, 12 мм за діаметром, 0.25 мм глибиною, що були прорізані в силіконовій пластинці тримача зразків. Кожний зразок обертали в процесі опромінення рентгенівськими променями Кальфаі радіоактивної міді (довжини хвилі = 1.5406 Ангстрем) за допомогою рентгенівської трубки, яка працювала при 40кВ/40мА. Аналітичні дослідження проводили за допомогою гоніометру шляхом покрокового сканування, яке проходило в режимі шагу повороту 0.02° за 5 секунд в інтервалі кута два-тета від 2° до 55°. Піки інтенсивностей наведені в Таблиці 5. В Таблиці 5 "Кут 2-Тета" пов'язаний з міжплощинними відстанями кристалу, і інтенсивність подано як процент від найбільшого піку (І/І;). Індивідуальні поліморфні форми та мезилатна сіль можуть бути охарактеризовані посиланням на піки інтенсивності більші, ніж 50%, і більш переважно піками, що мають піки інтенсивності більші, ніж 20%. Таблиця 5 Перелік піків для Форм А, В, С та Е, та мезилатної солі Форма А Кут 2-тета, Інтенсивність, Кут 2-тета, Інтенсивність, ° % ° % 6.002 8.893 9.401 9.654 11.105 12.000 12.071 13.060 13.373 13.458 13.620 13.708 13.790 14.418 15.075 15.320 21.1 22.9 25.1 8.5 33.4 100.0 50.2 25.1 10.3 11.6 10.0 15.5 10.8 10.9 4.3 6.1 15.669 17.040 17.888 18.111 18.872 19.287 19.336 19.714 20.126 20.951 21.021 21.302 21.378 21.925 22.346 22.821 4.7 30.0 33.4 16.7 51.9 18.9 16.0 72 6.5 15.3 12.9 15.4 19.9 57.5 94.6 22.7 Кут 2тета,° 23.282 23.494 23.884 24.298 24.554 24.602 25.674 26.087 26.600 27.036 27.641 28.888 29.136 29.915 30.197 30.282 Інтенсивність, Кут 2-тета, Інтенсивність, % ° % 40.8 37.3 92.4 42.7 18.7 19.6 30.1 13.8 19.1 11.8 24.4 18.3 14.6 9.4 19.4 25.8 30.469 31.498 32.257 33.063 33.797 34.889 35.158 35.610 36.226 36.634 38.335 40.198 40.820 41.279 43.943 15.3 17.4 8.8 11.6 14.1 17.1 21.2 12.5 13.8 12.4 16.0 17.2 13.7 15.7 20.5 Кут 2тета,° Інтенсивність, % 34.214 34.382 34.602 35.235 35.449 36.193 36.668 37.331 37.727 38.318 38.977 39.646 40.165 40.911 42.235 42.761 44-287 44.775 9.3 12.2 7.7 10.4 13.0 6,8 8.1 12.6 8.4 5.4 11.3 15,8 7.8 5.3 10.8 9.8 7.2 9.5 Форма В Кут 2-тета, Інтенсивність, Кут 2-тета, Інтенсивність, Кут 2-тета, Інтенсивність, ° % ° % °ta° % 6.943 9.004 9.725 10.526 11.315 11.986 13.011 13.493 13.897 14.306 15.569 15.883 16.740 17.122 17.407 17.603 18.094 18.727 19.176 Форма С 1.4 37.5 41.2 40.7 3.4 2.1 2.2 30.2 74.4 3.3 25.2 48.3 5.9 30.0 12.3 5.7 4.1 62.9 10.0 19.559 19.867 19.964 20.407 20.919 21.101 21.712 22.551 22.769 22.843 22.926 23.418 23.904 23.997 25.049 25.209 25.462 25.700 26.205 8.4 11.1 6.1 62.2 31.2 17.3 14.4 72.7 20.2 13.9 15.3 100.0 24.9 24.5 21.4 32.4 17.0 8.4 12.9 26.512 26.758 26.918 26.989 27.302 27.800 27.871 28.945 29.164 30.027 30.284 31.179 31.443 31.629 32.121 32.318 32.845 33.023 34.045 36.5 30.5 20.7 25.4 7.2 17.4 11.6 9.5 14.4 7.5 10.2 19.9 10.2 8.7 8.1 7.9 12.2 14.8 9.5 * Кут 2тета, ° Інтенсивність, % Кут 2тета,° Інтенсивність, % Кут 2тета,° Інтенсивність, % Кут 2тета,° Інтенсивність, % 5.510 42 17.488 24.7 25.257 52.6 31.939 28.9 6.143 4.4. 18.601 76.6 25.885 19.4 32.689 14.9 7.860 63.2 18.964 32.9 26.283 22.0 33.228 13.6 8.141 13.2 19.230 16.8 26.634 28.5 33.880 16.4 9.774 8.0 19.727 51.4 27.085 17.6 34.867 15.1 10.290 12.0 20.121 29.0 27.309 20.8 35.627 16.9 11.076 6.9 20.440 10.1 27.574 28.7 36.765 14.7 11.262 63 20.859 14.5 27.904 19.1 37.551 19.7 12.133 24.3 21-261 19.4 28.165 14.3 38.576 202 12.510 7.5 21.730 100.0 28.891 19.3 39.190 23.3 12.860 14.2 22.310 39.0 29.226 15.1 40.302 16.8 13.690 373 22.830 72.0 29.792 30.7 40.824 16.8 14.446 8.5 23.102 27.7 30.101 19.7 41.643 15.1 15.008 35.4 23.598 75.9 30.287 15.7 42.238 16.6 15.794 32.6 23.884 24.7 30.604 17.0 42.971 19.4 16.274 27.9 24.479 50.5 30.771 16.9 44.714 16.4 16.781 14.6 24.777 21.2 30.995 11.5 16.940 10.7 25.093 59.3 31.590 22.4 Форма Е Кут 2-тета,° Інтенсивність, Кут 2-тета, Інтенсивність, Кут 2-тета, Інтенсивність, Кут 2-тета, Інтенсивність, % ° % ° % ° % 8.416 8.506 9.675 11.994 12.393 13.116 13.952 14.064 15.978 16.096 16.218 16.914 17.042 17.596 6.3 3.9 23.0 15.7 13.7 8.2 16.4 17.2 5.8 3.7 3.6 30.8 13.4 10.3 18.028 18.387 18.787 19.315 19.358 19.444 19.778 20.056 20.398 21.522 21.770 22.479 22.974 23.509 12.3 6.4 17.0 38.5 42.2 31.1 26.6 6.9 3.5 7.5 7.7 8.2 5.0 7.0 23.852 24.075 24.192 24.696 25.280 25.765 26.061 26.746 27.269 28.860 29.534 29.642 31.094 31.652 100.0 18.0 18.9 10.7 28.2 11.1 12.1 8.5 10.6 13.0 5.3 7.9 4.3 4.0 32.434 32.760 34.083 34.462 34.927 35.552 36.390 36.954 37.993 39.826 40.699 42.316 43.410 14.8 25.6 8.6 7.8 5.6 7.1 7.2 6.3 7.1 4.7 8.4 7.0 7.0 Мезилатна сіль Кут 2тета,° 7.392 7.56 9.129 Інтенсивність, Кут 2-тета, Інтенсивність, Кут 2-тета, Інтенсивність, Кут 2-тета, Інтенсивність, % ° % ° % ° % h 22.9 19.297 57.9 26.55 16.8 34.607 6.7 12.1 20.265 51 26.818 15.3 35.031 8.4 18.4 20.494 7.3 27.012 30.3 35.834 9.6 10.179 11.871 12.343 13.057 14.5 14.733 14.813 15.162 17.155 17.694 18.358 18.602 18.964 11 17.8 7.6 16.6 11.1 22.6 40.1 5.4 10.6 31 6.5 6.1 40.5 20.772 21.018 21.414 22.136 22.804 22.934 23.283 23.842 24.5 24.795 25.452 26.201 13.8 15.1 40 24 16.7 32.8 8.7 49.4 14.4 100 7.6 5.2 27.675 28.673 28.904 29305 29.627 29.93 30.327 30.663 30.999 31.297 31.841 32.844 15.9 22.3 16.3 24.6 9.1 9.3 14.91 16.8 16.7 12.8 6 16.5 36.125 36.418 37.675 38.92 40.614 41.061 41.65 42.03 42.65 42.878 44.003 44.817 9.2 9.3 10 6.3 5.9 8.8 133 10.4 10.1 8.9 7.7 9.3 Диференційну сканувальну калориметрія (DSC) проводили, використовуючи апарат Perkin Elmer DSC-7, обладнаний автоматичним змінювачем. Приблизно 2 мг кожного зразка обережно відвішували у 50 мікролітровий алюмінієвий стакан і його загнуті края закривали перфорованою кришкою. Зразки нагрівали зі швидкістю 20°С/хвил. в інтервалі від 40°С до 300°С з продувкою азотом. Результати термічного аналізу зведені у Таблиці 6 і можуть використані для характеристики форм вільної основи та мезилатної еолі. Таблиця 6 Дані термічного аналізу для Форм А, В, С, Ε та мезилатної солі Форма Форма А Форма В Форма С Форма Ε Мезилат Точка плавлення ( С) 198 218 147 229 279 Вміст води в гідратованій формі вільної основи (Форма D) в умовах навколишнього середовища загалом становить від 9 до 10% (ваг./ваг.). Це еквівалентно від 2.5 до 2.8 моль води на моль вільної основи. Було визначено, що вміст води при 90% RH був 12.8% (ваг./ваг.), це еквівалентно 3.6 моль води, тільки 2 моль якої, як було виявлено, представляють собою зв'язану воду. Перший моль втрачався нижче 5% RH, другий утримувався аж до 1% RH, див. фігуру 11. Ймовірно, що тривале зберігання гідратованої форми нижче приблизно 18% RH повинно приводити до гідратації. Більш того, видалення кристалічної води приводить до втрати кристалічної решітки, продукт стає переважно аморфним. Це висуває на перший план можливу проблему у використанні звичайної гидратованої форми для виготовлення фармацевтичних композицій. Зневоднення спостерігалося при термічному аналізі у вигляді широкої подвійної ендотерми при 97/113°С (Див. Фігура 8) Даний винахід ілюструється наступними малюнками, в яких: На Фігурі 1 представлено PXRD для мезилатної солі; На Фігурі 2 представлено DSC термограму для мезилатної солі; На Фігурі 3 представлено PXRD для усіх форм вільної основи А, В, С, D та Е; На Фігурі 4 представлено DSC термограму для Форми А; На Фігурі 5 представлено DSC термограму для Форми В; На Фігурі 6 представлено DSC термограму для Форми С; На Фігурі 7 представлено DSC термограму для Форми Е; На Фігурі 8 представлено DSC термограму для Форми D; На Фігурі 9 показано поглинання вологи мезилатної солі; На Фігурі 10 представлено поглинання вологи Форм А, В та Е; та На Фігурі 11 представлено поглинання вологи Форми D. Нижче даний винахід ілюструється прикладами, в яких можуть бути використані наступні абревіатури: хвил. - хвилина ЯМР - ядерний магнітний резонанс год. - година Приклад 1 Поліморфи вільної основи 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідро-2-ізохіноліл)5-(2-піридил)хіназолін (і) Форма А У атмосфері азоту при перемішуванні до суспензії 4-аміно-2-хлор-6,7-диметокси-5-(2-піридил)хіназоліну [див. WO 98/30560, Приклад 12(а), 97г, 0.31моль] та гідрохлориду N-(1,2,3,4-тетрагідро-5ізохіноліл)метансульфонамщу [див. WO 98/30560, Приклад 19(Ь), 89 г, 0.34 моль] в н-бутанолі (1.9 л) додавали триетиламін (161 мл, 1.16 моль). Реакційну суміш нагрівали до кипіння і кип'ятили зі зворотнім холодильником протягом ночі. Реакційну суміш охолоджували до кімнатної температури, концентрували у вакуумі і залишок суспендували у воді (1.5 л), після чого додавали гідрокарбонат натрію (15 г). Одержану суспензію перемішували протягом 3 ночей, фільтрували і тверду речовину промивали водою (500 мл) і висушували протягом ночі у вакуумі при 50°С з одержанням 158 г речовини. Основну частину речовини (156 г) об'єднували з подальшою частиною речовини (139 г), отриманою з використанням подібної методики, і об'єднані тверді речовини розчиняли у метанолі (3 л). Розчин фільтрували, концентрували у вакуумі і одержану тверду речовину висушували протягом ночі у вакуумі при 50°С з одержанням 287 г речовини. Основну частину речовини (285 г) суспендували протягом ночі в суміші ацетон/вода (4/1 за об'ємом, 1.4 л), фільтрували і тверду речовини промивали сумішшю ацетон/вода 4/1 (300 мл) і висушували протягом ночі у вакуумі при 50°С з одержанням 251 г речовини. Основну частину речовини просіювали через 500 мкМ сито з одержанням вказаної у заголовку сполуки (242 г). (ii) Форма В У атмосфері азоту при перемішуванні до суспензії 4-аміно-2-хлор-6,7-ДИМетокси-5-(2-піридил)хіназоліну (166 г, 0.53 моль) та гідрохлориду N-(1,2,3,4-тетрагідро-5-ізохіноліл)метансульфонаміду (152 г, 0.58 моль) в нбутанолі (2.0 л) додавали триетиламін (161 мл, 1.16 моль) і в подальшому н-бутанол (1.3 л). Реакційну суміш нагрівали до кипіння і перемішували при цій температурі протягом 11 годин. Реакційну суміш охолоджували до кімнатної температури, концентрували у вакуумі і залишок суспендували у воді (2.65 л), після чого додавали гідрокарбонат натрію (28.5 г). Одержану суспензію перемішували протягом ночі, фільтрували і тверду речовину промивали водою (500 мл). Одержану вологу тверду речовину додавали до метанолу (4 л) і одержану суспензію концентрували у вакуумі до отримання густої суспензії. Додавали додаткову кількість метанолу (150 мл) і одержану суспензію фільтрували і промивали метанолом (3 χ 50 мл). Одержану тверду речовину висушували протягом 3 ночей у вакуумі при 41°С. Висушену тверду речовину потім суспендували протягом ночі у суміші ацетон/вода (1/4 за об'ємом, 1250 мл), фільтрували, твердий осад промивали сумішшю ацетон/вода 1/4 (3 χ БО мл) і висушували протягом 2 ночей у вакуумі при 54°С з одержанням вказаної у заголовку сполуки (245 г). (ііі) Форма С До суміші 4-аміно-2-(5-метансульфонамід-1,2,3,4-тетрагідро-2-ізохіноліл)-6,7-диметокси-5-(2піридил)хіназоліну (0.1 г партії приблизно 90% чистоти, Форма D/аморфна суміш, 1.7 ммол) та адипінової кислоти (0.027 г, 1.8 ммоль) додавали ацетон (1.25 мл) і одержану суспензію перемішували при кімнатній температурі протягом 3 ночей. Одержану суспензію фільтрували і висушували у вакуумі протягом ночі при 48°С з одержанням великої кількості вказаної у заголовку сполуки. (іv) Форма Ε У атмосфері азоту при перемішуванні до суспензії 4-аміно-2-хлор-6,7-диметокси-5-(2^піридил)хіназоліну (105 г, 0.33 моль) в н-бутанолі (2.1 л) додавали гідрохлорід N-(1,2,3,4-тетрагідро-5ізохіноліл)метансульфонаміду (152 г, 0.37 моль) та триетиламін (106 мл, 0.73 моль). Реакційну суміш нагрівали до кипіння і перемішували при кип'ятінні протягом 6 годин, охолоджували до кімнатної температури і перемішували протягом ночі при кімнатній температурі. Потім суміш знову нагрівали до кипіння, перемішували при кип'ятінні протягом 6 годин, охолоджували до кімнатної температури і перемішували при кімнатній температурі протягом ночі. Потім реакційну суміш концентрували у вакуумі і залишок суспендували у воді (1.68 л) і додавали гідрокарбонат натрію (17.9 г). Одержану суспензію перемішували протягом ночі, фільтрували і вологу тверду речовину додавали до ацетонітрилу (1.16 л). Одержану суспензію нагрівали до кипіння, потім залишали охолоджуватися до кімнатної температури і перемішували при кімнатній температурі протягом ночі. Одержану суспензію фільтрували і промивали ацетонітрилом (2 х 100 мл). Вологу тверду речовину суспендували в суміші ацетон/вода (1/4 за об'ємом, 800 мл) протягом ночі при кімнатній температурі, фільтрували, тверду речовину промивали сумішшю ацетон/вода 1/4 (2 х 50 мл) і висушували протягом ночі у вакуумі при 45°С з одержанням 158 г речовини. Основну частину отриманої речовини з вищенаведеного препаративного приклада (155 г) об'єднували з подальшими порціями речовини (596 г), отриманої аналогічним чином і суспендованої в ацетонітрилі (5.28 л). Суспензію нагрівали до кипіння і перемішували при кип'ятінні протягом 90 хвил., нагрівали до кімнатної температури і перемішували при кімнатній температурі протягом ночі. Тверду речовину збирали фільтрацією, промивали ацетонітрилом (100 мл) і висушували протягом ночі у вакуумі при 50°С з одержанням вказаної у заголовку сполуки (734 г). Приклад 2 Аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназолін 1) Процес утворення солі, описаний нижче, використовували для перетворення вільної Основи Форми В в метансульфонатну сіль. У атмосфері азоту суспензію 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2)3)4-тетрагідроізохінол-2іл)-5-(2-піридил)хіназоліну Форми В (2.0 г) в суміші бутанон/вода (10/1 за об'ємом, 24 мл) нагрівали до кипіння протягом 20 хвилин. Додавали суміш бутанон/вода 10/1 доти, поки не отримували розчин (додавали зверх 3 мл, доводячи загальний об'єм розчинника до 27 мл). Розчин залишали охолоджуватися до 50°С і додавали по краплям метансульфонову кислоту (0.38 г, 4.0 ммоль) протягом 30 секунд. Додатково резервуар промивали сумішшю бутанон/вода 10/1 (2 х 0.25 мл) і промивний розчин додавали до реакційного резервуару. Отриману суспензію залишали охолоджуватися до кімнатної температури і потім перемішували при цій температурі протягом 2 годин. Тверду речовину збирали фільтрацією, промивали ацетоном (2x2 мл), залишали в ексикаторі протягом ЗО хвилин і висушували протягом ночі у вакуумі при 54°С з одержанням вказаної у заголовку сполуки (2.2 г) у вигляді твердої речовини білого кольору. 1 Н-ЯМР (300 МГц, ДМСО) δ : 2.30 (3Н, с), 2.99 (3Н, с), 3.04 (2Н, м), 3.44 (ЗН, с), 3.93 (2Н, мгл), 4.01 (ЗН, с), 4.91 (2Н, с), 7.15 (1Н, д), 7.28 (2Н, м), 7.44 (1Н, с), 7.57 (2Н, м), 8.02 (1Н, м), 8.77 (1Н,м), 9.19 (1Н,с). (іі) Наступну процедуру використовували для перетворення вільної основи Форми Ε у метансульфонатну сіль Суспензію 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідро-ізохінол-2-іл)-5-(2піридил)хіназоліну Форми Ε (1.0 г, 1.97 моль) в суміші ацетон/вода (12/7 за об'ємом, 9.5 мл) нагрівали до кипіння. Додавали однією порцією метансульфонову кислоту (0.19 г, 1.99 ммоль). Додатково резервуар промивали водою (1 мл) і одержаний розчин залишали охолоджуватися до кімнатної температури протягом ночі тверду речовину з одержаної суспензії збирали фільтрацією і висушували протягом ночі у вакуумі при 45 °С з одержанням вказаної у заголовку сполуки (1.14 г) у вигляді твердої речовини білого кольору. Приклад 3 Активність in vivo Щоденне пероральне уведення 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну мезилату самцям та самкам щурів лінії Sprague-Dawley у дозі 30мг/кг протягом 1 місяця викликало зміни, пов'язані з фармакологічною активністю сполуки, однак, не було виявлено побічних ефектів:
ДивитисяДодаткова інформація
Назва патенту англійською4-amino-6,7-dimethoxy-2-(5-methanesulfonamido-1,2,3,4-tetrahydroisoquinol-2-yl)-5-(2-pyridyl)quinazoline mesylate and polymorhic forms
Назва патенту російськоюМезилат 4-амино-6,7-диметокси-2-(5-метансульфонамидо-1,2,3,4-тетрагидроизохинол-2-ил)-5-(2-пиридил)хиназолина и полиморфные формы
МПК / Мітки
МПК: A61P 13/08, C07D 401/14, A61K 31/517
Мітки: мезилат, 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну, форми, поліморфні
Код посилання
<a href="https://ua.patents.su/13-72311-mezilat-4-amino-67-dimetoksi-2-5-metansulfonamido-1234-tetragidroizokhinol-2-il-5-2-piridilkhinazolinu-ta-polimorfni-formi.html" target="_blank" rel="follow" title="База патентів України">Мезилат 4-аміно-6,7-диметокси-2-(5-метансульфонамідо-1,2,3,4-тетрагідроізохінол-2-іл)-5-(2-піридил)хіназоліну та поліморфні форми</a>
Попередній патент: Спосіб переінсталяції системи контролю антигенного гомеостазу організму ссавця за кухарчуком-радченком-сірманом
Наступний патент: Просторовий блок покриття
Випадковий патент: Генераторний агрегат