Набір для виявлення вірусу гепатиту b
Номер патенту: 99793
Опубліковано: 25.09.2012
Автори: Суббарао Пілларісетті Венката, Джаганнатх Манджула, Наір Чандрасекхар Бхаскаран
Формула / Реферат
1. Набір, який містить олігонуклеотидний зонд, як зазначено в SEQ ID NO: 1, і відповідні праймери, як зазначено в SEQ ID NO: 3 і 4, для виявлення вірусу гепатиту В.
2. Набір за пунктом 1, де згаданий зонд являє собою подвійномічений зонд, який кон'югований з мітками, що виявляються, що має флуорофор на 5' кінці та агент для гасіння у внутрішній ділянці або на 3' кінці.
3. Набір за пунктом 1, де згаданий зонд SEQ ID NO: 1 спроектований для поверхневого гена вірусу гепатиту В.
4. Набір за пунктом 1, де згаданий праймер SEQ ID NO: 3 є смисловим праймером, а SEQ ID NO: 4 є антисмисловим праймером.
5. Суміш для реакції ПЛР для виявлення вірусу гепатиту В, яка містить реагенти для ампліфікації нуклеїнової кислоти, подвійномічений зонд, як визначено в SEQ ID NO: 1, відповідні праймери, як визначено в SEQ ID NO: 3 та 4, та тестовий зразок.
6. Суміш для реакції ПЛР за пунктом 5, де згаданий зразок вибирають з групи, що містить кров, сироватку та плазму; і згадана суміш використовується в ПЛР у реальному часі.
7. Спосіб виявлення вірусу гепатиту В, де згаданий спосіб включає стадії:
(а) формування реакційної суміші, що містить реагенти для ампліфікації нуклеїнових кислот, олігонуклеотидний зонд, як зазначено в SEQ ID NO: 1, з відповідними праймерами, як зазначено в SEQ ID NO: 3 та 4, тестовий зразок, і
(б) проведення ПЛР реакційної суміші з отриманням копій цільової послідовності, з наступним вимірюванням збільшення сигналу флуоресценції для виявлення вірусу гепатиту B.
8. Спосіб за пунктом 7, де згаданий зонд кон'югований з мітками, що виявляються, які мають флуорофор на 5' кінці і агентом для гасіння у внутрішній ділянці або на 3' кінці.
9. Спосіб за пунктом 7, де згаданий праймер SEQ ID NO: 3 є смисловим і SEQ ID NO: 4 є антисмисловим праймером.
10. Спосіб за пунктом 7, де згаданий досліджуваний зразок вибирають з групи, що містить кров, сироватку та плазму; і згадані реагенти для ампліфікації включають хлорид магнію, Taq-полімеразу і буфер для ампліфікації.
11. Спосіб за пунктом 7, де згадане виявлення носить якісний або кількісний характер.
12. Спосіб за пунктом 8, де згаданий флуорофор вибирають з групи, що містить флуоресцеїн і похідні флуоресцеїну FAM, VIC, JOE, 5-(2'-аміноетил)амінонафталін-1-сульфонову кислоту, кумарин та похідні кумарину, люцифер жовтий, техаський червоний, тетраметилродамін, 6-карбоксифлуоресцеїн, тетрахлор-6-карбоксифлуоресцеїн, 5-карбоксиродамін і ціанінові барвники, переважно 6-карбоксифлуоресцеїн; та зазначений агент для гасіння вибирають з групи, що включає тетраметилродамін [TAMRA], 4'-(4-диметиламінофенілазо)бензойну кислоту, 4-диметиламінофенілазофеніл-4'-малеїмід, тетраметилродамін, карбокситетраметилродамін і BHQ барвники, переважно тетраметилродамін на 3' кінці або "Black hole quencher 1" [BHQ1] у внутрішній ділянці або на 3' кінці.
13. Набір для виявлення вірусу гепатиту В, що містить подвійно мічений зонд, як зазначено в SEQ ID NO: 1; відповідні пари праймерів, як зазначено в SEQ ID NO: 3 і 4, і реагенти для ампліфікації.
14. Набір за пунктом 13, де згадані реагенти для ампліфікації включають хлорид магнію, Taq-полімеразу і буфер для ампліфікації.
Текст
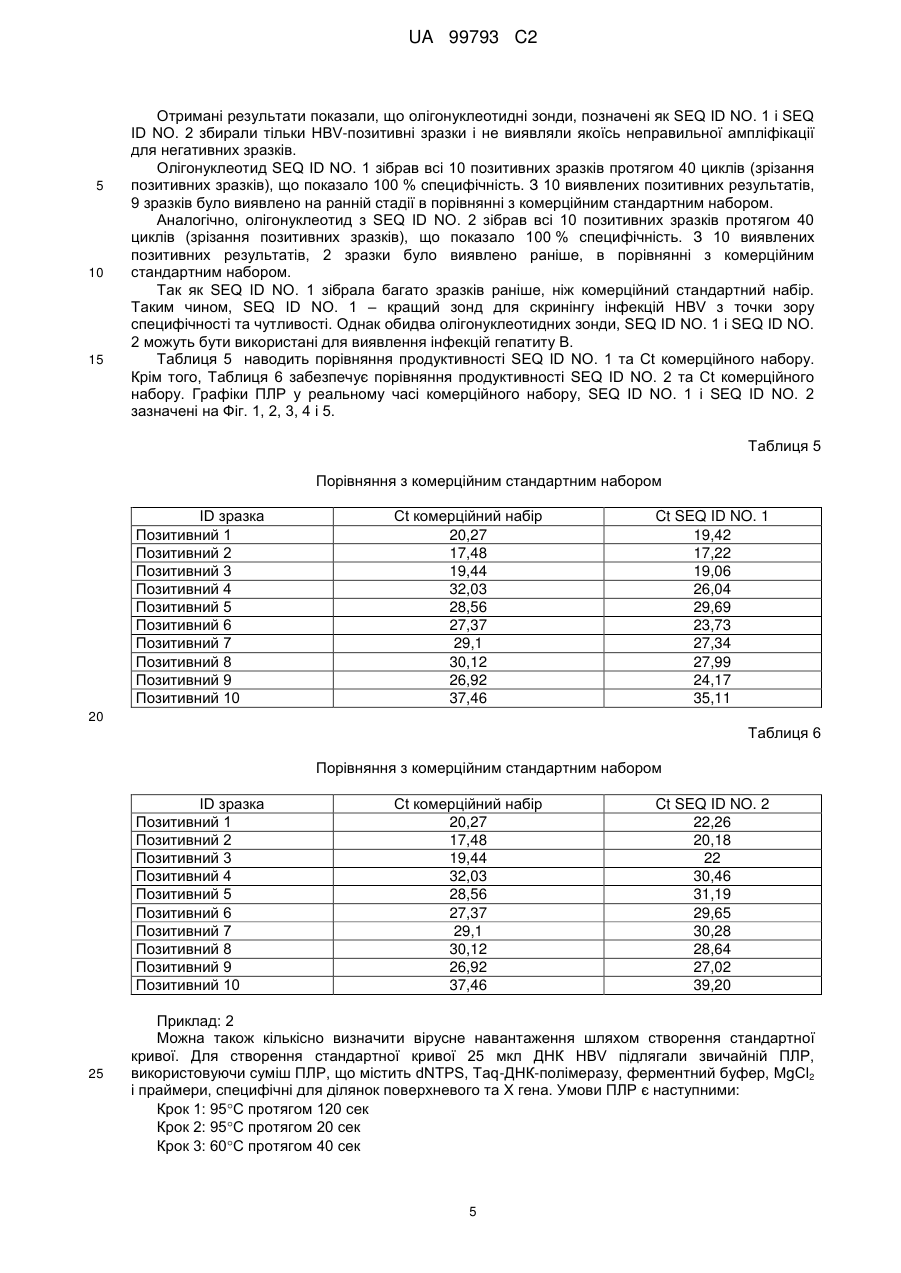
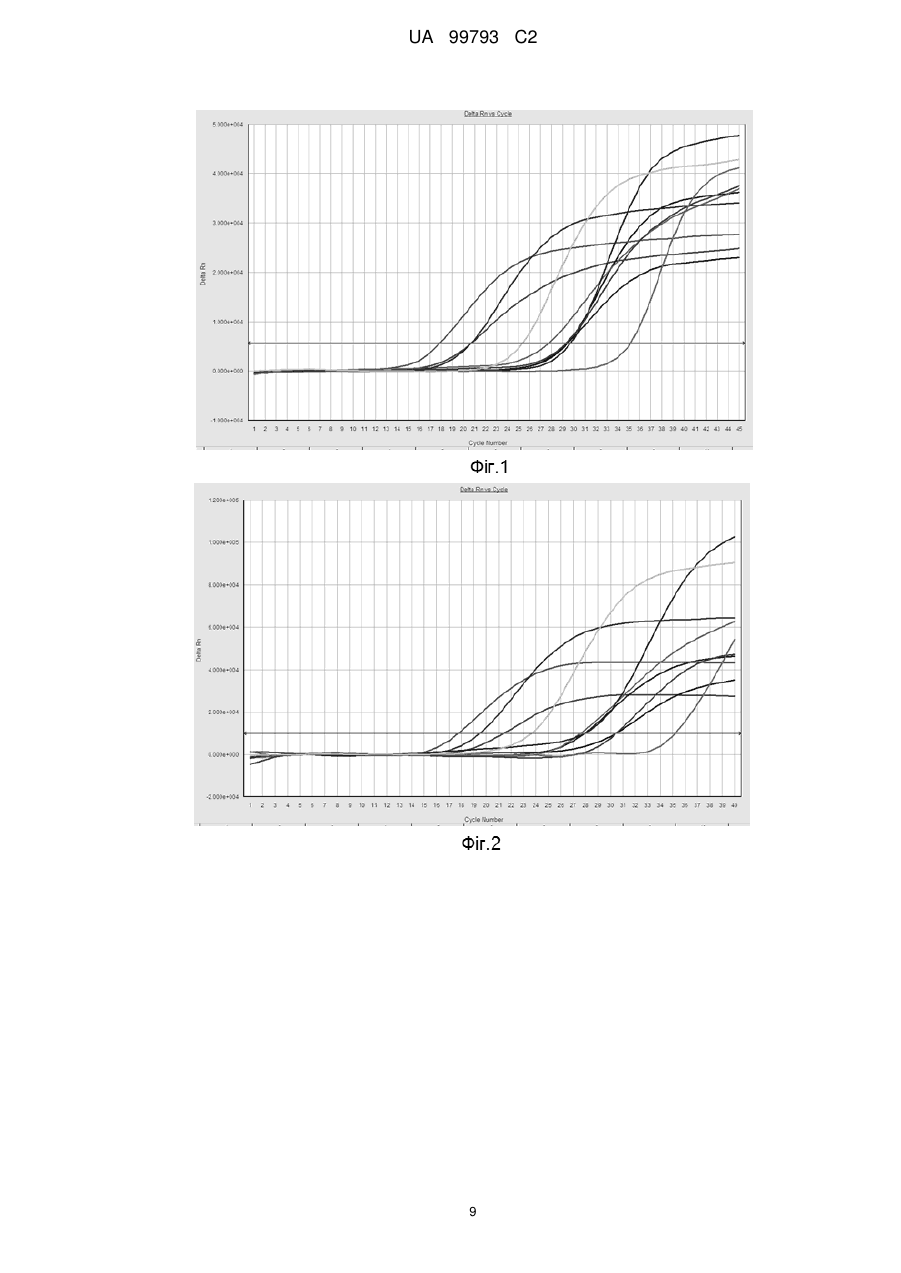
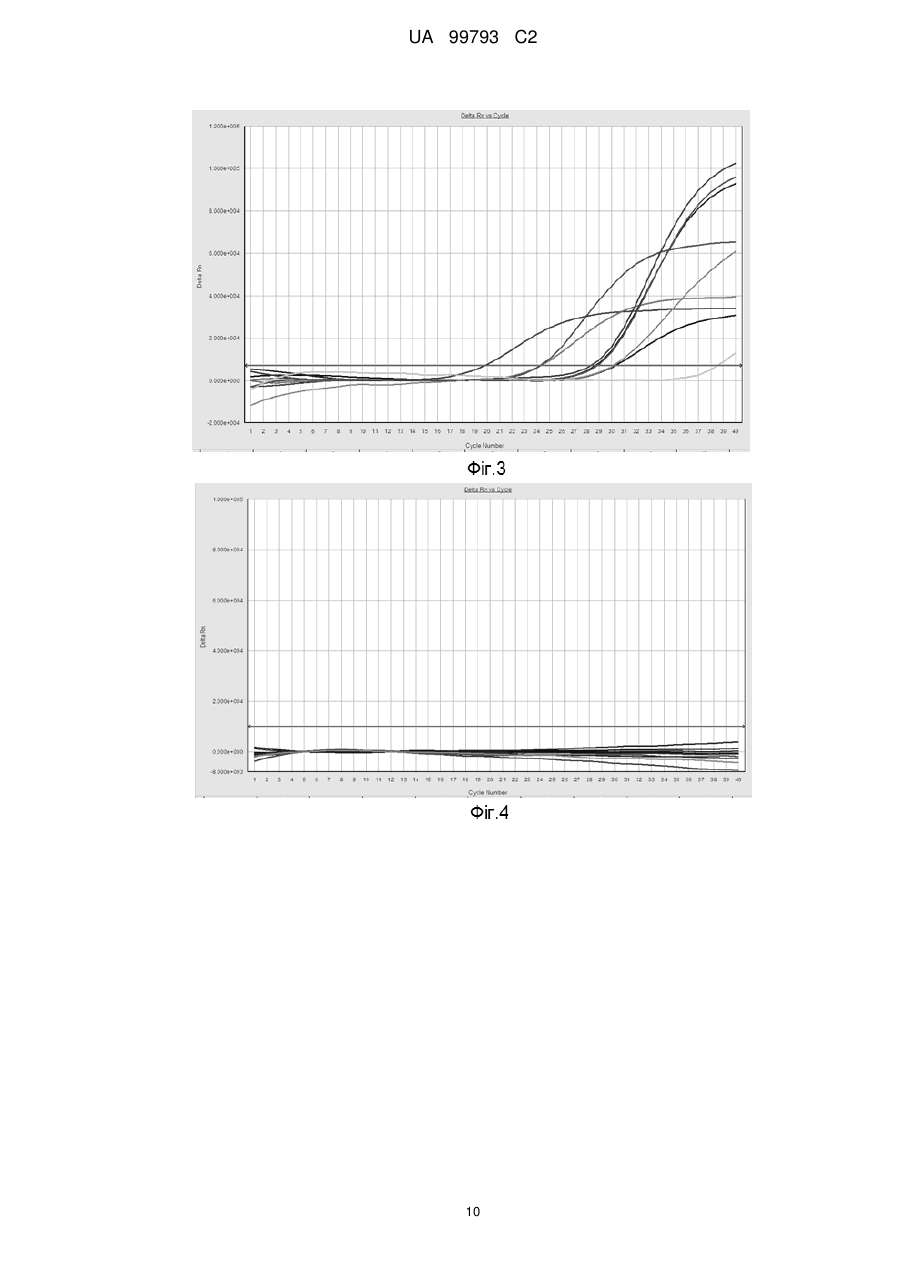
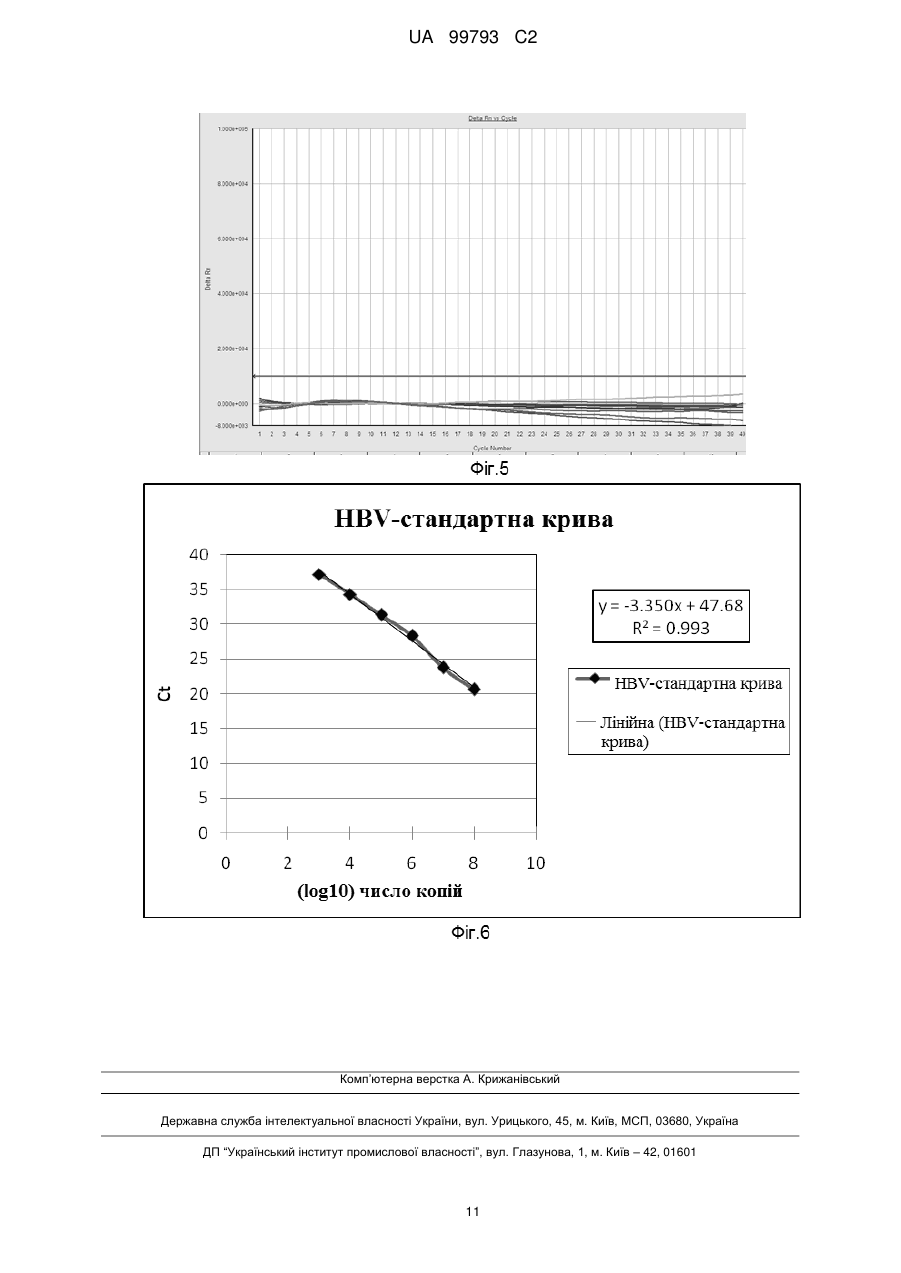
Реферат: Винахід належить до набору для виявлення вірусу гепатиту В, що містить олігонуклеотидний зонд та пару відповідних праймерів, суміші для ПЛР (полімеразної ланцюгової реакції) для виявлення вірусу гепатиту В, способу виявлення вірусу гепатиту В у зразку. UA 99793 C2 (12) UA 99793 C2 UA 99793 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь техніки Даний винахід стосується способу визначення присутності та кількісного визначення нуклеїнових кислот HBV (вірусу гепатиту В) в зразках. Передумови винаходу та попередній рівень техніки HBV викликає гострий і хронічний гепатит (гепатит типу В), а у важких випадках – цироз печінки і рак. Недавні дослідження показали, що в усьому світі число людей, інфікованих вірусом гепатиту В (HBV), становить приблизно 300 мільйонів. ПЛР аналізи для прямого виявлення нуклеїнових кислот HBV у крові/сироватці або плазмі інфікованого суб'єкту можуть забезпечити перевагу у визначенні точного вірусного навантаження інфікованого пацієнта, що буде корисним для лікаря з метою встановлення точної стадії інфекції. Це може також допомогти лікареві забезпечити належну терапію для пацієнта. Кількісне визначення точного вірусного навантаження також може допомогти у моніторингу перебігу антивірусної терапії. Використовувані в даний час методи діагностики HBV ґрунтуються на ELISA (імуноферментному аналізі - ІФА), який заснований на наявності сироваткових маркерів, таких як, HBeAg, HBsAg, або анти-HBc IgM, анти-HBe, анти-HBs, або анти-HBc IgG. Оскільки засновані на ELISA методи не можуть дати уявлення про точне вірусне навантаження потрібно шукати спосіб, який може надати кількісну міру вірусного навантаження. Існує необхідність в розробці ефективного способу з урахуванням вищезазначених проблем, пов'язаних з відомими методами виявлення, так, щоб один і той же спосіб можна було використати для виявлення HBV, що може дати якісний і кількісний показник вірусного навантаження. Задачі Перша задача даного винаходу полягає в забезпеченні способу, який дозволяє визначити наявність нуклеїнових кислот HBV в зразках. Друга задача даного винаходу полягає в забезпеченні зондів і праймерів для виявлення HBV. Третя задача даного винаходу полягає в забезпеченні суміші для реакції ПЛР для виявлення HBV. Четверта задача даного винаходу полягає в забезпеченні набору, що включає зонди і праймери для виявлення HBV. Короткий опис фігур, що додаються Фіг. 1 Реальний графік HBV-позитивних зразків з використанням комерційного набору Фіг. 2 Реальний графік HBV-позитивних зразків з використанням SEQ ID NO. 1 Фіг. 3 Реальний графік HBV-позитивних зразків з використанням SEQ ID NO. 2 Фіг. 4 Реальний графік HBV-негативних зразків з використанням SEQ ID NO. 1 Фіг. 5 Реальний графік HBV-негативних зразків з використанням SEQ ID NO. 2 Фіг. 6 HBV-стандартна крива Короткий опис винаходу Таким чином, даний винахід стосується олігонуклеотидних зондів SEQ ID NO. 1 і SEQ ID NO. 2; праймерів SEQ ID NO. 3, 4, 5 і 6; суміші для реакції ПЛР для виявлення вірусу гепатиту В, причому вказаної суміші, яка містить реагенти для ампліфікації нуклеїнових кислот, подвійні мічені зонди, викладені в SEQ ID NO. 1 і SEQ ID NO. 2, праймери SEQ ID NO. 3, 4, 5, 6 і досліджуваний зразок; способу виявлення вірусу гепатиту В, зазначеного способу, що включає наступні стадії: формування реакційної суміші, яка містить реагенти для ампліфікації нуклеїнових кислот, олігонуклеотидні зонди SEQ ID NO. 1 або SEQ ID NO. 2 з відповідними праймерами SEQ ID NO. 3 та 4 або SEQ ID NO. 5 і 6 відповідно, досліджуваний зразок, і використання реакційної суміші в ПЛР, щоб отримати копії цільової послідовності, що супроводжується вимірюванням збільшення сигналу флуоресценції для виявлення вірусу гепатиту B, а також набір для виявлення вірусу гепатиту B, вказаний набір, що включає подвійні мічені зонди SEQ ID NO. 1 і SEQ ID NO. 2, окремо або в комбінації; відповідну пару праймерів SEQ ID NO. 3, 4 і 5, 6, окремо або в комбінації і реагенти для ампліфікації. Детальний опис винаходу Даний винахід стосується олігонуклеотидних зондів SEQ ID NO. 1 і SEQ ID NO. 2. В одному з варіантів винаходу вказані зонди – подвійні мічені зонди. В одному з варіантів винаходу вказані зонди виявляють вірус гепатиту В. В одному з варіантів винаходу вказані зонди кон'юговані з мітками, що визначаються, з флуорофором на 5' кінці і агентом для гасіння у внутрішній ділянці або на 3' кінці. В одному з варіантів винаходу SEQ ID NO. 1 сконструйована для поверхневого гену вірусу гепатиту В, а SEQ ID NO. 2 - спроектована для ділянки X-гену вірусу гепатиту В. Даний винахід стосується праймерів SEQ ID NO. 3, 4, 5 і 6. 1 UA 99793 C2 5 10 15 20 25 30 35 40 45 В одному з варіантів винаходу вказані праймери SEQ ID NO. 3 та SEQ ID NO. 5 є смисловими, а SEQ ID NO. 4 і № 6 SEQ ID - антисмисловими праймерами, відповідно. В одному з варіантів винаходу вказані праймери SEQ ID NO. 3 та SEQ ID NO. 4 призначені для подвійного міченого зонду SEQ ID NO. 1, а праймери SEQ ID NO. 5 і № 6 SEQ ID – для подвійного міченого зонду SEQ ID NO. 2. Даний винахід стосується суміші для реакції ПЛР для виявлення вірусу гепатиту В, вказаної суміші, яка містить реагенти для ампліфікації нуклеїнових кислот, подвійні мічені зонди, викладені в SEQ ID NO. 1 і SEQ ID NO. 2, праймери SEQ ID NO. 3, 4, 5, 6 і досліджуваний зразок. В одному з варіантів винаходу зазначений зразок вибирається з групи, що складається з крові, сироватки та плазми. В одному з варіантів винаходу вказана ПЛР – ПЛР у реальному часі. Даний винахід стосується способу виявлення вірусу гепатиту В, що включає наступні стадії: (а) формування реакційної суміші, яка містить реагенти для ампліфікації нуклеїнових кислот, олігонуклеотидний зонд SEQ ID NO. 1 або SEQ ID NO. 2 з відповідними праймерами SEQ ID NO. 3 та 4 або SEQ ID NO. 5 і 6 відповідно, досліджуваний зразок, і (б) використання реакційної суміші для ПЛР для отримання копій цільової послідовності, що супроводжується вимірюванням збільшення сигналу флуоресценції для виявлення вірусу гепатиту B. В одному з варіантів винаходу вказані зонди кон'юговані з мітками, що визначаються, з флуорофором на 5' кінці і агентом для гасіння у внутрішній ділянці або на 3' кінці. В одному з варіантів винаходу вказані праймери SEQ ID NO. 3 та SEQ ID NO. 5 є смисловими, а SEQ ID NO. 4 і SEQ ID NO. 6– антисмисловими праймерами, відповідно. В одному з варіантів винаходу вказаний досліджуваний зразок вибирається з групи, що складається крові, сироватки та плазми. В одному з варіантів винаходу вказані реагенти для ампліфікації включають хлорид магнію, Taq-полімеразу і буфер для ампліфікації. В одному з варіантів винаходу вказане виявлення носить якісний або кількісний характер. В одному з варіантів винаходу вказаний флуорофор вибирається з групи, що складається з флуоресцеїну і похідних флуоресцеїну FAM, VIC, JOE, 5-(2'-аміноетил) амінонафтален-1сульфонової кислоти, кумарину та похідних кумарину, люциферу жовтого, техаського червоного, тетраметилродаміну, 6-карбоксифлуоресцеїну, тетрахлоро-6карбоксифлуоресцеїну, 5-карбоксиродаміну і ціанінових барвників. В одному з варіантів винаходу вказаний агент для гасіння вибирається з групи, що включає метилтетрародамін [TAMRA], 4'-(4-диметиламінофенілазо) бензойної кислоти, 4диметиламінофенілазофеніл-4'-малеіміду, тетраметилродаміну, карбокситетраметилродаміну і BHQ барвників. В одному з варіантів винаходу вказаний флуорофор – бажано 6-карбоксифлуоресцеїн на 5' кінці, а вказаний агент для гасіння – бажано тетраметилродамін на 3' кінці або "Black hole quencher 1" [BHQ1] у внутрішній ділянці або в 3'кінці. Даний винахід стосується набору для виявлення вірусу гепатиту В, вказаний набір, що включає подвійні мічені зонди SEQ ID NO. 1 і SEQ ID NO. 2, окремо або в комбінації; відповідні пари праймерів SEQ ID NO. 3, 4, 5, 6, окремо або в комбінації і реагенти для ампліфікації. В одному з варіантів винаходу вказані реагенти для ампліфікації включають хлорид магнію, Taq-полімеразу і буфер для ампліфікації. Список біологічних послідовностей винаходу SEQ ID NO. 1 і відповідні праймери 3 та 4 мають ідентифікаційні номери послідовності як показані в таблиці 1 нижче: Таблиця 1 ID НОМЕР ПОСЛІДОВНОСТІ SEQ ID No. 1 SEQ ID No. 3 SEQ ID No. 4 НУКЛЕОТИДНА ПОСЛІДОВНІСТЬ 5'– FAM – CCTCAGTCCGTTTCTCCTGGCTCAGTT – TAMRA – 3' або 5'–FAM-CCTCAGTCCGTT/iBHQ1T/CTCCTGGCTCAGTT-Phos– 3' 5' – TGCACCTGTATTCCCATCCC – 3' 5' – CCACATCATCCATATAACTGAAAGCC – 3' 50 2 UA 99793 C2 SEQ ID NO. 2 і відповідні праймери 5 і 6 мають ідентифікаційні номери послідовності, що показані в таблиці 2 Таблиця 2 ID НОМЕР ПОСЛІДОВНОСТІ SEQ ID No. 2 SEQ ID No. 5 SEQ ID No. 6 5 10 15 20 25 30 35 40 45 50 НУКЛЕОТИДНА ПОСЛІДОВНІСТЬ 5' – FAM – CCCCTTCTTCGTCTGCCGT – TAMRA – 3' або 5' – FAM – CCCCTTCTTCG/iBHQ1T/CTGCCGT – Phos-3' 5' – CGTCGGCGCTGAATCC – 3' 5' – GAAGCGAAGTGCACACGG – 3' Спроектовані "олігонуклеотидні" зонди можуть бути використані для виявлення нуклеїнових кислот HBV в інфікованих зразків за рахунок використання ПЛР у реальному часі. Режим виявлення – шляхом вимірювання збільшення флуоресценції при ПЛР. HBV база даних була ретельно досліджена для виявлення найбільш консервативних ділянок, характерних для геному HBV. Найбільш перспективні ділянки з консервативними ділянками були вибрані для розробки наборів праймерів і зондів. Консервативні ділянки з поверхневого і X генів були отримані і проаналізовані для проектування зондів і праймерів. Відповідно до цього винаходу SEQ ID NO. 1 разом з відповідними смисловими і антисмисловими праймерами SEQ ID NO. 3 та SEQ ID NO. 4 призначені для поверхневого гена геному HBV. Аналогічно, SEQ ID NO. 2 разом з відповідними смисловими і антисмисловими праймерами SEQ ID NO. 5 і SEQ ID NO. 6 призначені для X гена геному HBV. Відповідно до цього винаходу вказаний "олігонуклеотид" з SEQ ID NO. 1 і SEQ ID NO. 2, що має мітку, яка виявляється, з флуорофором на 5'кінці і агент для гасіння у внутрішній ділянці або на 3' кінці. Флуорофор вибирається з групи, що включає флуоресцеїн і похідні флуоресцеїну FAM, VIC, JOE, 5-(2'-аміноетил)амінонафтален-1-сульфонову кислоту, кумарин та похідні кумарину, люцифер жовтий, техаський червоний, тетраметилродамін, 6карбоксифлуоресцеїн, тетрахлоро-6-карбоксифлуоресцеїн, 5-карбоксиродамін і ціанінові барвники. У ще одному варіанті виконання цього винаходу вказаний агент для гасіння вибирається з групи, що включає тетраметилродамін, 4'-(4-диметиламінофенілазо)бензойну кислоту, 4диметиламінофенілазофеніл-4'-малеімід, тетраметилродамін, карбокситетраметилродамін і BHQ барвники. Вказаний флуорофор – бажано 6-карбоксифлуоресцеїн [FAM], і агент для гасіння – "Black hole quencher 1" [BHQ1], коли присутній внутрішньо, і тетраметилродамін [TAMRA] або "Black hole quencher 1" [BHQ1], коли присутній на 3'кінці. Даний винахід стосується способу виявлення вірусу гепатиту В, в якому зазначена ПЛР суміш, що складається з реагентів для ампліфікації нуклеїнової кислоти, "олігонуклеотидні" зонди, спроектовані як SEQ ID NO. 1 або SEQ ID NO. 2, разом з відповідними праймерами SEQ ID NO. 3, 4, 5 і 6, і досліджуваний зразок підлягає ампліфікації з використанням ПЛР у реальному часі для отримання копії цільової послідовності. Ампліфікація вимірюється з точки зору збільшення сигналу флуоресценції. "Олігонуклеотний" зонд має розмір 19-27 нуклеотидів. Спроектовані зонди мають флуорофор на 5кінці і агент для гасіння у внутрішній ділянці або на 3'кінці. Вказаний флуорофор – бажано 6-карбоксифлуоресцеїн [FAM], агент для гасіння – "Black hole quencher 1" [BHQ1], коли присутній внутрішньо, і тетраметилродамін [TAMRA] або "Black hole quencher 1" [BHQ1], коли присутній на 3'кінці. Даний винахід використовується для виявлення вірусу гепатиту В в крові/сироватці/плазмі крові. Спосіб, що використовується для виявлення – шляхом моніторингу збільшення флуоресценції при ПЛР. Відповідно до цього винаходу "олігонуклеотидний" зонд відноситься до короткої послідовності рибонуклеїнової кислоти (РНК) і дезоксирибонуклеїнової кислоти (ДНК). "Олігонуклеотидні" зонди можуть специфічно гібридизуватися з нуклеїновими кислотами з усіх генотипів вірусу гепатиту В (HBV). "Олігонуклеотидні" зонди відповідно до цього винаходу, як правило, приблизно 19-27 нуклеотидів в довжину. "Олігонуклеотидні" зонди, згадані авторами, специфічно гібридизуються з послідовністю нуклеїнової кислоти HBV, не виявляючи неспецифічну гібридизацію до не-HBV нуклеїнових кислот. Зонди "олігонуклеотидної" послідовності, що застосовуються авторами, дотримуються принципів хімії Taqman. TaqMan зонди, які також називають подвійні-барвникові олігонуклеотидні або подвійні мічені зонди, є найбільш широко використовуваним типом зондів. 3 UA 99793 C2 5 10 15 20 25 30 Вони були розроблені компанією Рош [Базель, Швейцарія] і ABI [Фостер-Сіті, США] на основі аналізу, в якому спочатку використовували радіомічений зонд, і складаються з одноланцюгової послідовності зонда, яка є комплементарною до одного з ланцюгів амплікону. Флуорофор при збудженні передає свою енергію через FRET (флуоресцентний резонансний перенос енергії), на агент для гасіння. Під час ПЛР у реальному часі зонд зв'язується з ампліконом протягом кожного етапу відпалу ПЛР. Коли Taq полімераза простягається від праймеру, зв'язаного з ампліконом, він витісняє 5" кінець зонда, який потім розкладається під активністю 5'3'екзонуклеазної Taq полімерази. Розщеплення триває до тих пір, поки залишок зонда не розтоплюється ампліконом. Цей процес вивільняє флуорофор і агент для гасіння в розчин, специфічно розділяючи їх, у порівнянні з тим, коли вони утримуються разом зондом. Цей процес призводить до необоротного збільшення флуоресценції флуорофору. "Олігонуклеотидні" зонди SEQ ID NO. 1 і № 2 відповідно до цього винаходу, таким чином, також пропонуються, в поєднанні з відповідними смисловими і антисмисловими праймерами SEQ ID NO. 3, 4, 5 і 6, відповідно, що можуть використовуватися для специфічної ампліфікації і виявлення послідовностей нуклеїнових кислот HBV в досліджуваному зразку шляхом ПЛР у реальному часі. Технологія даної заявки у подальшому розробляється за допомогою наступних прикладів. Тим не менш, приклади не повинні розглядатися як обмеження обсягу винаходу. Ефективність і чутливість олігонуклеотидних зондів SEQ ID NO. 1 і SEQ ID NO. 2 були проаналізовані в порівняні з комерційним стандартним набором. Однакові концентрації реагентів для ПЛР в режимі реального часу, шаблону і олігонуклеотидів були використані в кожному випадку, а умови циклізації також залишалися постійними для всіх реакцій. На підставі результату, отриманого з комерційного набору, олігонуклеотидні зонди з SEQ ID NO. 1 і 2 були проаналізовані на предмет їх чутливості та специфічності. Приклад: 1 ДНК була виділена з 10 HBV-позитивних і 10 HBV-негативних зразків сироватки з використанням комерційного набору. ПЛР реакції у реальному часі були проведені для всіх зразків з використанням олігонуклеотидних зондів, що позначається як SEQ ID NO. 1 і SEQ ID NO. 2, разом з відповідними праймерами SEQ ID NO. № 3, 4, 5 і 6 відповідно. Чутливість цих олігонуклеотидних зондів у збиранні інфікованих зразків порівнювали з комерційним стандартним набором. Ті ж концентрації в реагентів для ПЛР режимі реального часу, шаблону і праймерів використовували в кожному випадку, а умови циклізації також залишалися постійними для всіх реакцій. Композиція суміші ПЛР у реальному часі і умови ПЛР, як зазначені у Tаблиці 3 і 4. 35 Таблиця 3 ПЛР у реальному часі з преміксом Takara Композиція основної суміші ПЛР у реальному часі Премікс 5,0 мкл Прямий праймер 0,2 мкл (2 пікомоля) Зворотній праймер 0,2 мкл (2 пікомоля) Зонд 0,2 мкл (2 пікомоля) Зразок 2,0 мкл Сума 2,4 мкл Таблиця 4 Умови циклу ПЛР у реальному часі Крок 1 Крок 2 Крок 3 Програма ПЛР 95 °C протягом 60 сек 95 °C протягом 5 сек 60 °C протягом 34 сек Крок 2 і 3 будуть повторюватися 40 разів 4 UA 99793 C2 5 10 15 Отримані результати показали, що олігонуклеотидні зонди, позначені як SEQ ID NO. 1 і SEQ ID NO. 2 збирали тільки HBV-позитивні зразки і не виявляли якоїсь неправильної ампліфікації для негативних зразків. Олігонуклеотид SEQ ID NO. 1 зібрав всі 10 позитивних зразків протягом 40 циклів (зрізання позитивних зразків), що показало 100 % специфічність. З 10 виявлених позитивних результатів, 9 зразків було виявлено на ранній стадії в порівнянні з комерційним стандартним набором. Аналогічно, олігонуклеотид з SEQ ID NO. 2 зібрав всі 10 позитивних зразків протягом 40 циклів (зрізання позитивних зразків), що показало 100 % специфічність. З 10 виявлених позитивних результатів, 2 зразки було виявлено раніше, в порівнянні з комерційним стандартним набором. Так як SEQ ID NO. 1 зібрала багато зразків раніше, ніж комерційний стандартний набір. Таким чином, SEQ ID NO. 1 – кращий зонд для скринінгу інфекцій HBV з точки зору специфічності та чутливості. Однак обидва олігонуклеотидних зонди, SEQ ID NO. 1 і SEQ ID NO. 2 можуть бути використані для виявлення інфекцій гепатиту В. Таблиця 5 наводить порівняння продуктивності SEQ ID NO. 1 та Ct комерційного набору. Крім того, Таблиця 6 забезпечує порівняння продуктивності SEQ ID NO. 2 та Ct комерційного набору. Графіки ПЛР у реальному часі комерційного набору, SEQ ID NO. 1 і SEQ ID NO. 2 зазначені на Фіг. 1, 2, 3, 4 і 5. Таблиця 5 Порівняння з комерційним стандартним набором ID зразка Позитивний 1 Позитивний 2 Позитивний 3 Позитивний 4 Позитивний 5 Позитивний 6 Позитивний 7 Позитивний 8 Позитивний 9 Позитивний 10 Ct комерційний набір 20,27 17,48 19,44 32,03 28,56 27,37 29,1 30,12 26,92 37,46 Ct SEQ ID NO. 1 19,42 17,22 19,06 26,04 29,69 23,73 27,34 27,99 24,17 35,11 20 Таблиця 6 Порівняння з комерційним стандартним набором ID зразка Позитивний 1 Позитивний 2 Позитивний 3 Позитивний 4 Позитивний 5 Позитивний 6 Позитивний 7 Позитивний 8 Позитивний 9 Позитивний 10 25 Ct комерційний набір 20,27 17,48 19,44 32,03 28,56 27,37 29,1 30,12 26,92 37,46 Ct SEQ ID NO. 2 22,26 20,18 22 30,46 31,19 29,65 30,28 28,64 27,02 39,20 Приклад: 2 Можна також кількісно визначити вірусне навантаження шляхом створення стандартної кривої. Для створення стандартної кривої 25 мкл ДНК HBV підлягали звичайній ПЛР, використовуючи суміш ПЛР, що містить dNTPS, Taq-ДНК-полімеразу, ферментний буфер, MgCl2 і праймери, специфічні для ділянок поверхневого та X гена. Умови ПЛР є наступними: Крок 1: 95С протягом 120 сек Крок 2: 95С протягом 20 сек Крок 3: 60C протягом 40 сек 5 UA 99793 C2 5 Кроки 2 і 3 були повторені протягом 40 циклів Після ПЛР ампліфікований зразок був підданий електрофорезу на 3 % агарозному гелі і пофарбований бромідом етидію. Ампліконову смугу довжиною приблизно 1,2 kbp і яка відповідає ділянкам поверхневого і Х гена геному HBV, вирізали з гелю і очищали, використовуючи набор для екстракції гелю Qiaquick. Поглинання очищеної ДНК амплікону (2 мкл) оцінювали при 260 нм, використовуючи нанокраплю. Коефіцієнт екстинкції ДНК був розрахований з індивідуального коефіцієнта основи шляхом підсумовування. Наномолі амплікону були розраховані з використанням наступного рівняння: 1000 OD260(1см) 1мл (об' єм) Коефіцієнт екстинкції амплікону 10 Нмоль / мл 15 Число копій було розраховано за формулою: Число копій/мл = (молі/мл) число Авогадро. Розрахунки: OD 260=0,522 Коефіцієнт екст. = 33675,1 нмоль/мл = 0,015501068 12 Копії/мл = 9,34 × 10 20 8 3 З числа копій чистого амплікону була отримана стандартна крива, виконавши 10 10 розведень амплікону, використовуючи ПЛР у реальному часі. Композиція преміксу ПЛР у реальному часі і ПЛР програма зазначені в Таблиці 3 і 4. З Ct, отриманого із стандартної кривої, Фіг: 6, число копій може бути розрахована для невідомих зразків Фіг. 6 і таблиці 7. 25 Таблиця 7 Значення стандартної кривої щодо Ct Sl. № 1 2 3 4 5 6 30 35 Копії/мл 8 110 7 110 6 110 5 110 4 110 3 110 Ct 20,6 23,7 28,3 31,3 34,2 37,1 Висновок а) Жоден із негативних зразків не показав хибнопозитивного результату зі спроектованими олігонуклеотидними зондами, що позначаються як SEQ ID NO. 1 і SEQ ID NO. 2. б) Олігонуклеотид з SEQ ID NO. 1, який спроектований для поверхневого гена HBV, показав хорошу чутливість і специфічність (100 %). З 10 позитивних зразків 9 були зібрані раніше, ніж у випадку комерційного стандартного набору, Таблиця 5. в) Олігонуклеотид SEQ ID NO. 2, який спроектований для X гена HBV, також зібрав всі 10 позитивних зразків, показуючи 100 % специфічність. З 10 позитивних зразків 2 були зібрані раніше, ніж у випадку комерційного стандартного набору, Таблиця 6. г) На основі загальних оціночних досліджень, SEQ ID NO. 1 і SEQ ID NO. 2 були визнані кращими для виявлення HBV в порівнянні комерційними наборами. д) Нарешті, олігонуклеотидні зонди, позначені як SEQ ID NO. 1 і SEQ ID NO. 2, можуть бути використані для кількісного визначення вірусного навантаження в інфікованому зразку. 40 6 UA 99793 C2 7 UA 99793 C2 ФОРМУЛА ВИНАХОДУ 5 10 15 20 25 30 35 40 45 1. Набір, який містить олігонуклеотидний зонд, як зазначено в SEQ ID NO: 1, і відповідні праймери, як зазначено в SEQ ID NO: 3 і 4, для виявлення вірусу гепатиту В. 2. Набір за пунктом 1, де згаданий зонд являє собою подвійномічений зонд, який кон'югований з мітками, що виявляються, що має флуорофор на 5' кінці та агент для гасіння у внутрішній ділянці або на 3' кінці. 3. Набір за пунктом 1, де згаданий зонд SEQ ID NO: 1 спроектований для поверхневого гена вірусу гепатиту В. 4. Набір за пунктом 1, де згаданий праймер SEQ ID NO: 3 є смисловим праймером, а SEQ ID NO: 4 є антисмисловим праймером. 5. Суміш для реакції ПЛР для виявлення вірусу гепатиту В, яка містить реагенти для ампліфікації нуклеїнової кислоти, подвійномічений зонд, як визначено в SEQ ID NO: 1, відповідні праймери, як визначено в SEQ ID NO: 3 та 4, та тестовий зразок. 6. Суміш для реакції ПЛР за пунктом 5, де згаданий зразок вибирають з групи, що містить кров, сироватку та плазму; і згадана суміш використовується в ПЛР у реальному часі. 7. Спосіб виявлення вірусу гепатиту В, де згаданий спосіб включає стадії: (а) формування реакційної суміші, що містить реагенти для ампліфікації нуклеїнових кислот, олігонуклеотидний зонд, як зазначено в SEQ ID NO: 1, з відповідними праймерами, як зазначено в SEQ ID NO: 3 та 4, тестовий зразок, і (б) проведення ПЛР реакційної суміші з отриманням копій цільової послідовності, з наступним вимірюванням збільшення сигналу флуоресценції для виявлення вірусу гепатиту B. 8. Спосіб за пунктом 7, де згаданий зонд кон'югований з мітками, що виявляються, які мають флуорофор на 5' кінці і агентом для гасіння у внутрішній ділянці або на 3' кінці. 9. Спосіб за пунктом 7, де згаданий праймер SEQ ID NO: 3 є смисловим і SEQ ID NO: 4 є антисмисловим праймером. 10. Спосіб за пунктом 7, де згаданий досліджуваний зразок вибирають з групи, що містить кров, сироватку та плазму; і згадані реагенти для ампліфікації включають хлорид магнію, Taqполімеразу і буфер для ампліфікації. 11. Спосіб за пунктом 7, де згадане виявлення носить якісний або кількісний характер. 12. Спосіб за пунктом 8, де згаданий флуорофор вибирають з групи, що містить флуоресцеїн і похідні флуоресцеїну FAM, VIC, JOE, 5-(2'-аміноетил)амінонафталін-1-сульфонову кислоту, кумарин та похідні кумарину, люцифер жовтий, техаський червоний, тетраметилродамін, 6карбоксифлуоресцеїн, тетрахлор-6-карбоксифлуоресцеїн, 5-карбоксиродамін і ціанінові барвники, переважно 6-карбоксифлуоресцеїн; та зазначений агент для гасіння вибирають з групи, що включає тетраметилродамін [TAMRA], 4'-(4-диметиламінофенілазо)бензойну кислоту, 4-диметиламінофенілазофеніл-4'-малеїмід, тетраметилродамін, карбокситетраметилродамін і BHQ барвники, переважно тетраметилродамін на 3' кінці або "Black hole quencher 1" [BHQ1] у внутрішній ділянці або на 3' кінці. 13. Набір для виявлення вірусу гепатиту В, що містить подвійно мічений зонд, як зазначено в SEQ ID NO: 1; відповідні пари праймерів, як зазначено в SEQ ID NO: 3 і 4, і реагенти для ампліфікації. 14. Набір за пунктом 13, де згадані реагенти для ампліфікації включають хлорид магнію, Taqполімеразу і буфер для ампліфікації. 8 UA 99793 C2 9 UA 99793 C2 10 UA 99793 C2 Комп’ютерна верстка А. Крижанівський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 11
ДивитисяДодаткова інформація
Назва патенту англійськоюSet for determination of hepatitis b virus
Автори англійськоюJagannath, Manjula, Nair, Chandrasekhar, Bhaskaran, Subbarao, Pillarisetti, Venkata
Назва патенту російськоюНабор для определения вируса гепатита в
Автори російськоюДжаганнатх Манджула, Наир Чандрасекхар Бхаскаран, Суббарао Пилларисетти Венката
МПК / Мітки
МПК: G01N 33/576, C12Q 1/68
Мітки: набір, гепатиту, вірусу, виявлення
Код посилання
<a href="https://ua.patents.su/13-99793-nabir-dlya-viyavlennya-virusu-gepatitu-b.html" target="_blank" rel="follow" title="База патентів України">Набір для виявлення вірусу гепатиту b</a>
Попередній патент: Спосіб одержання розчинного композиційного добрива на основі карбаміду
Наступний патент: Спосіб виробництва композитної арматури і пристрій для його здійснення
Випадковий патент: Пристрій для закріплення фурми у кареткі