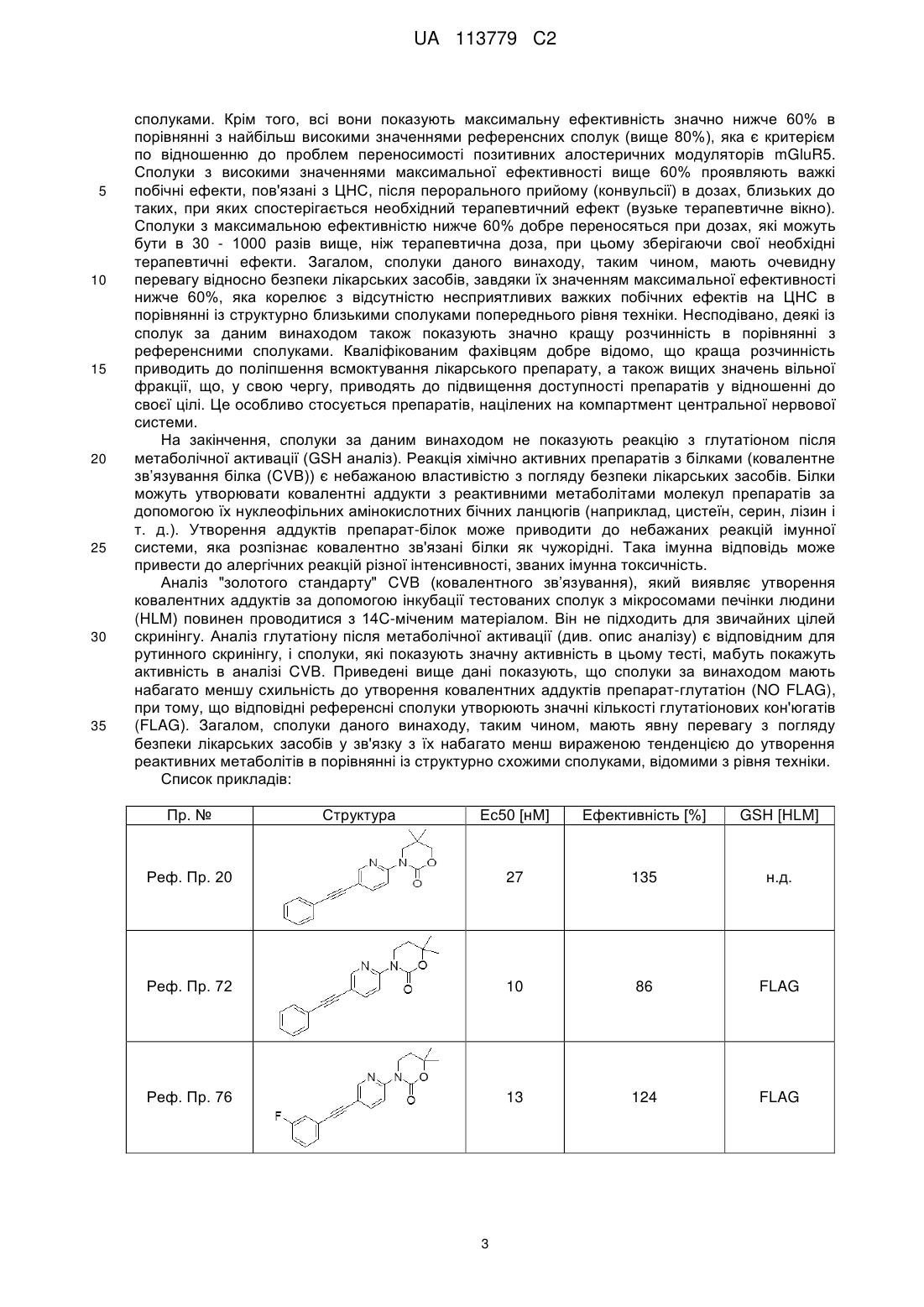
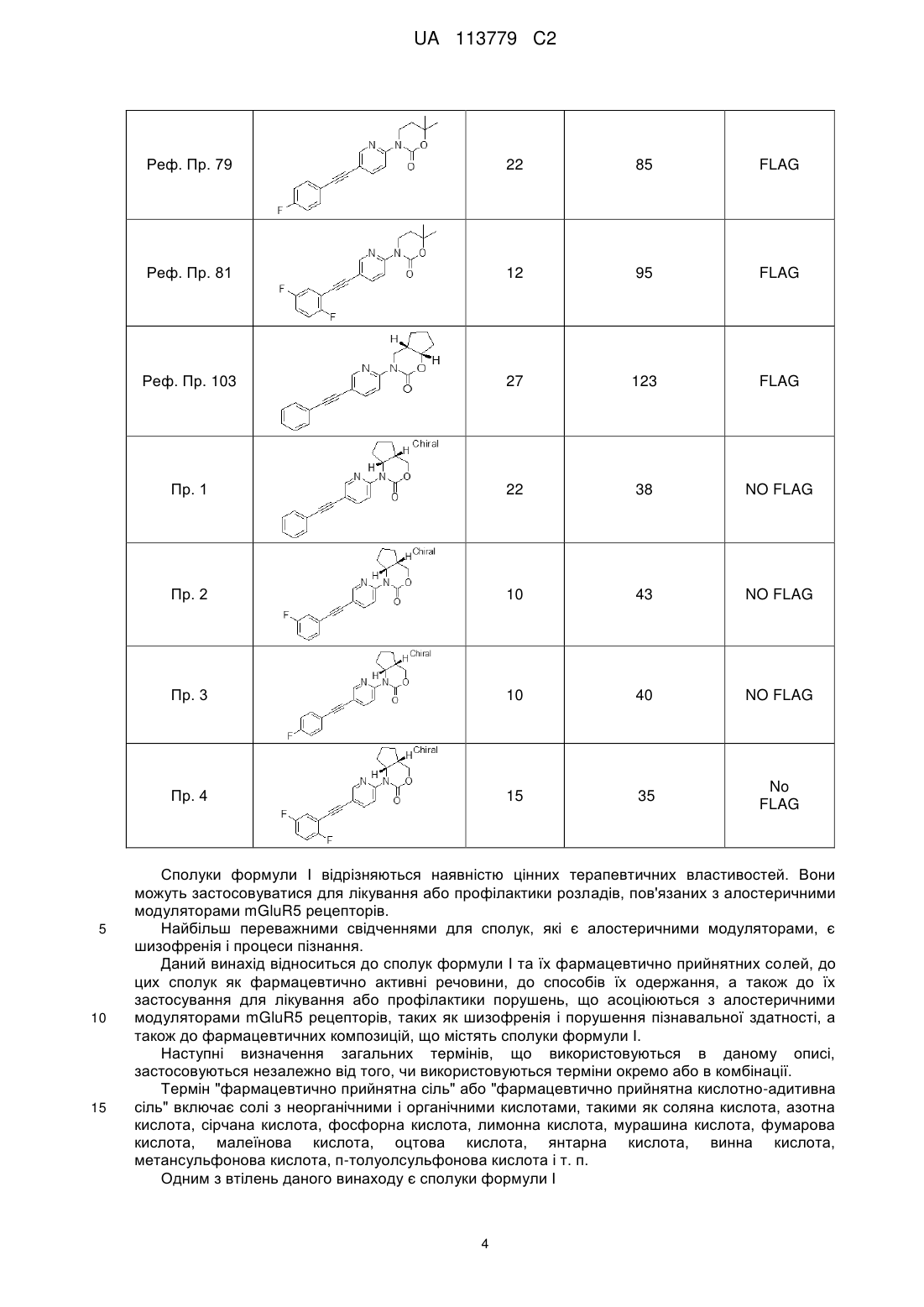
Похідні арилетинілу
Номер патенту: 113779
Опубліковано: 10.03.2017
Автори: Штадлєр Хайнц, Ліндеманн Лотар, Єшкє Гєорг, Віейра Ерік
Формула / Реферат
1. Етинілпохідна формули І
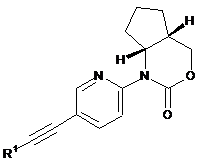 , I
, I
де
R1 позначає феніл, 3-фторфеніл, 4-фторфеніл або 2,5-дифторфеніл;
або фармацевтично прийнятна кислотно-адитивна сіль, в енантіомерно чистому вигляді.
2. Етинілпохідна формули І, де сполуки позначають
(4aS,7aR)-1-(5-Фенілетиніл-піридин-2-іл)-гексагідро-циклопента[d] [1,3]оксазин-2-он
(4аS,7аR)-1-[5-(3-фторфенілетиніл)-піридин-2-іл]-гексагідро-циклопента[d][1,3]оксазин-2-он
(4аS,7аR)-1-(5-((4-фторфеніл)етиніл)-піридин-2-іл)гексагідро-циклопента[d][1,3]оксазин-2(1Н)-он або
(4аS,7аR)-1-[5-(2,5-дифторфенілетиніл)-піридин-2-іл]-гексагідро-циклопента[d][1,3]оксазин-2-он.
3. Спосіб одержання сполуки формули І як описано в пункті 1, що містить варіанти:
а) взаємодія сполуки формули 3
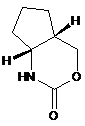 , 3
, 3
де сполука формули 3 є рацемічною сумішшю або знаходиться в енантіомерно чистому вигляді з відповідним арилацетиленовою сполукою галопіридину формули 4, де Υ позначає галоген, вибраний з фтору, брому або йоду
 4
4
з утворенням сполуки формули І в енантіомерно чистому вигляді або у вигляді рацемічної суміші, де енантіомери можуть бути розділені з використанням способів відомих кваліфікованим фахівцям,
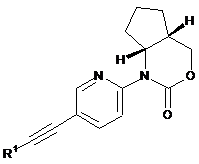 , I
, I
де заступники є такими, як визначено вище, або, якщо необхідно, конвертація одержаних сполук у фармацевтично прийнятні кислотно-адитивні солі, або
b) взаємодія сполуки формули II в енантіомерно чистому вигляді або у вигляді рацемічної суміші, де X позначає галоген, переважно йод або бром
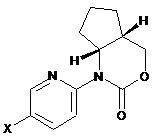 II
II
з ацетиленовою сполукою формули 5, де Q позначає водень або триалкілсилільну групу
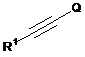 , 5
, 5
з утворенням сполуки формули І в енантіомерно чистому вигляді або у вигляді рацемічної суміші, яка може бути розділена з використанням способів відомих кваліфікованим фахівцям,
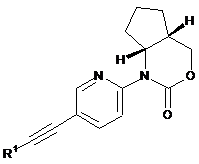 , I
, I
де заступники є такими, як описано в пункті 1, або, якщо необхідно, конвертація одержаних сполук у фармацевтично прийнятні кислотно-адитивні солі.
4. Сполука за будь-яким з пп. 1-2 для застосування як терапевтично активної речовини.
5. Фармацевтична композиція, яка містить щонайменше одну сполуку за будь-яким з пп. 1-2 або її фармацевтично прийнятну сіль.
6. Сполука за будь-яким з пп. 1-2, вживана у вигляді суміші енантіомерів, діастереомерів або в енантіомерно чистому вигляді; або її фармацевтично прийнятна сіль для застосування як лікарський засіб.
7. Застосування сполуки за будь-яким з пп. 1-2 або її фармацевтично прийнятної солі для виробництва лікарського засобу для лікування або профілактики захворювань, пов'язаних з алостеричними модуляторами рецепторів mGluR5.
8. Застосування сполуки за п. 7 для лікування або профілактики шизофренії, когнітивних захворювань, синдрому Мартіна-Белл або аутизму.
9. Сполука за будь-яким з пп. 1-2 для лікування або профілактики шизофренії, когнітивних захворювань, синдрому Мартіна-Белл або аутизму.
10. Спосіб лікування шизофренії, когнітивних захворювань, синдрому Мартіна-Белл або аутизму, який включає введення ефективної кількості сполуки за будь-яким з пп. 1-2.
Текст
Реферат: Даний винахід належить до етинілпохідних формули І H H N N O O R 1 ,І де 1 R позначає феніл, 3-фторфеніл, 4-фторфеніл або 2,5-дифторфеніл; або до фармацевтично прийнятної кислотно-адитивної солі, в енантіомерно чистому вигляді з абсолютною конфігурацією, як показано у формулі І. Несподівано було виявлено, що сполуки UA 113779 C2 (12) UA 113779 C2 загальної формули І є алостеричними модуляторами метаботропних глутаматних рецепторів підтипу 5 (mGluR5), які проявляють покращені біохімічні, фізико-хімічні і фармакодинамічні властивості, в порівнянні із сполуками, відомими з рівня техніки. UA 113779 C2 Даний винахід відноситься до етинілпохідних формули I H H N N O O 1 R 5 10 15 20 25 30 35 40 45 50 I, де 1 R позначає феніл, 3-фторфеніл, 4-фторфеніл або 2,5-дифторфеніл; або до фармацевтично прийнятної кислотно-адитивної солі, в енантіомерно чистому вигляді з абсолютною конфігурацією, як показано у формулі I. Несподівано було виявлено, що сполуки загальної формули I є алостеричними модуляторами метаботропних глутаматних рецепторів підтипу 5 (mGluR5), які проявляють покращені біохімічні, фізико-хімічні і фармакодинамічні властивості в порівнянні із сполуками, відомими з рівня техніки. У центральній нервовій системі (ЦНС) передача стимулів відбувається в результаті взаємодії нейромедіатора, який посилається нейроном, з нейрорецептором. Глутамат є основним збуджуючим нейромедіатором в головному мозку і відіграє унікальну роль в різних функціях центральної нервової системи (ЦНС). Глутамат-залежні стимулюючі рецептори розділені на дві основні групи. Перша основна група, а саме, іонотропні рецептори, утворює контрольовані лігандом іонні канали. Метаботропні рецептори глутамату (mGluR) відносяться до другої основної групи і, крім того, відносяться до сімейства G-білок зв'язаних рецепторів. В даний час відомо вісім різних членів цих mGluR і деякі з них навіть мають підтипи. За їх гомологією послідовностей, механізмом передачі сигналу і селективності агоністів, ці вісім рецепторів можуть бути підрозділені на три підгрупи: mGluR1 і mGluR5 належать до групи I, mGluR2 і mGluR3 відносяться до групи II, mGluR4, mGluR6, mGluR7 і mGluR8 і відносяться до групи III. Ліганди метаботропних глутаматних рецепторів, що належать до першої групи, можуть бути використані для лікування або профілактики гострих та/або хронічних неврологічних розладів, таких як психози, епілепсія, шизофренія, хвороба Альцгеймера, когнітивні розлади і порушення пам'яті, а також хронічному і гострому болю. У зв'язку з цим, іншими свідченнями для лікування є обмежена функція мозку, викликана операціями шунтування або пересадки, погане кровопостачання головного мозку, травми спинного мозку, травми голови, гіпоксія, викликана вагітністю, зупинка серця і гіпоглікемія. Також станами для лікування є ішемія, хорея Хантінгтона, бічний аміотрофічний склероз (ALS), склероз (TSC) туберози, недоумство, викликане СНІДом, травми очей, ретинопатія, ідіопатичний паркінсонізм або паркінсонізм, викликаний лікарськими засобами, а також стани, які ведуть до глутамат-дефіцитної функції, такі як, наприклад, м'язові спазми, судоми, мігрень, нетримання сечі, нікотинова залежність, опіатна залежність, тривога, блювота, дискінезія і депресії. Розладами, опосередкованими повністю або частково рецепторами mGluR5, є, наприклад, гострі, травматичні і хронічні дегенеративні процеси в нервовій системі, такі як хвороба Альцгеймера, старече недоумство, хвороба Паркінсона, хорея Гентінгтона, бічний аміотрофічний склероз і розсіяний склероз, психічні захворювання, такі як шизофренія і тривога, депресія, біль і наркотична залежність (Expert Opin. Ther. Patents (2002), 12 (12)). Новим напрямком для розробки селективних модуляторів є ідентифікація сполук, які діють за алостеричним механізмом, модулюючи рецептор шляхом пов'язування з сайтом, відмінним від високо консервативного ортостеричного сайту зв’язування. Алостеричні модулятори рецепторів mGluR5 з'явилися останнім часом як новий фармацевтичний засіб, що пропонує цю привабливу альтернативу. Позитивні алостеричні модулятори були описані, наприклад, в WO2008/151184, WO2006/048771, WO2006/129199, WO2005/044797 і, зокрема, WO2011/128279, а також в Molecular Pharmacology, 40, 333 - 336, 1991; The Journal of Pharmacology and Experimental Therapeutics, Vol 313, No. 1, 199-206, 2005; Nature, 480 (7375),63-68, 2012; Розкриті в рівні техніки модулятори є позитивними алостеричними модуляторами. Вони є сполуками, які безпосередньо не активують рецептори самі по собі, але значно підсилюють стимульовану агоністом відповідь, збільшуючи силу і максимум ефективності. Зв’язування цих 1 UA 113779 C2 5 10 15 20 25 30 35 40 45 50 55 60 сполук збільшує спорідненість агоністів глутаматних сайтів на їх позаклітинному N-кінцевому зв'язуючому сайті. Алостерична модуляція є, таким чином, привабливим механізмом для розширення відповідної фізіологічної активації рецептора. Існує брак виборчих алостеричних модуляторів рецепторів mGluR5. Звичайні модулятори mGluR5 рецепторів як правило не володіють безпекою лікарського засобу, що приводить до більшої кількості побічних ефектів лікарського засобу. Таким чином, існує потреба в сполуках, які б не мали ці недоліки і які були б ефективними селективними алостеричними модуляторами mGluR5 рецепторів. Даний винахід вирішує цю задачу, як показано далі: Порівняння сполук за даним винаходом і аналогічних сполук, відомих з рівня техніки: Структурно схожі сполуки, відомі з рівня техніки, розкриті в WO2011128279 (= Посилання 1, Hoffmann-La Roche) і найбільш близьких по структурі сполук цього патенту (приклади 20, 72, 76, 79, 81 і 103) показані для порівняння. Біологічні та фізико-хімічні аналізи і дані: 2+ Аналіз внутріклітинної мобілізації Ca Одержали моноклональну клітинну лінію HEK-293 стабільно трансфіковану cDNA, що кодує рецептори mGlu5a людини; для роботи з позитивними алостеричними модуляторами (PAM) mGlu5, відібрали клітинні лінії з низьким рівнем експресії і низькою конститутивною активністю рецепторів для того, щоб диференціювати активність агоністів від активності PAM. Клітини культивували згідно стандартним протоколам (Freshney, 2000) в середовищі Ігла, модифікованою за Дульбекко з високим вмістом глюкози і додаванням 1 мМ глутаміну, 10% (об./об.) інактивованої нагріванням бичачої сироватки, Пеніцилін/Стрептоміцин, 50 мкг/мл гідроміцину і 15 мкг/мл бластицидину (всі реагенти для культивування клітин і антибіотики були виробництва Invitrogen, Basel, Switzerland). Приблизно за 24 години перед експериментом, засівали 5x104 клітин/лунка в покриті полі-Dлізином чорні з прозорим дном 96-лункові планшети. Клітини нанесли з 2.5 мкМ Fluo-4AM в буфері для нанесення (1xHBSS, 20 мМ HEPES) протягом 1 години при 37 °C і промили 5 разів буфером для нанесення. Клітини перенесли в систему Functional Drug Screening System 7000 (Hamamatsu, Paris, France), і додали 11 напівлогарифмічних розведень тестованих сполук при 37 °C і клітини інкубували протягом 10-30 хвилин з онлайн записом флуоресценції. Після цієї передінкубаційної стадії, до клітин додали агоніст L-глутамат при концентрації, відповідною EC20 (зазвичай близько 80 мкМ) з онлайн записом флуоресценції; з метою порахувати денні зміни у відповідній реакції клітин, EC20 глутамату визначили безпосередньо перед кожним експериментом за допомогою запису повної кривої доза-відповідь для глутамату. Відповіді вимірювали як пік збільшення флуоресценції мінус базальний рівень (тобто флуоресценція без додавання L-глутамату), нормалізований по максимальному стимулюючому ефекту, одержаному з насичуючими концентраціями L-глутамату. Графіки будували у відсотках від максимальної стимуляції з використанням XLfit, програми, що будує криві, яка ітеративно наносить точки даних з використанням алгоритму Льовенберга - Марквардта. Використаним рівнянням одноточечного конкурентного аналізу було y = A + ((B-A)/(1+((x/C)D))), де у позначає % максимального стимулюючого ефекту, A позначає мінімум у, B позначає максимум у, C позначає EC50, x позначає log10 концентраціями конкуруючої сполуки і D позначає нахил кривої (коефіцієнт Хілла). З цих кривих були розраховані EC50 (концентрація при якій досягалася половина максимальної стимуляції), коефіцієнт Хілла, а також максимальна відповідь (=Ефективність) в % від максимального ефекту стимуляції, одержаного за допомогою насичуючих концентрацій L-глутамату. Позитивні сигнали, одержані протягом передінкубації з PAM тестовими сполуками (тобто до внесення EC20 концентрації L-глутамату) були індикативними для агоністичної активності, відсутність таких сигналів демонструвала відсутність агоністичної активності. Зниження сигналу, спостережуване після внесення EC20 концентрації L-глутамату, було індикативним для інгибіторної активності тестової сполуки. У списку прикладів нижче показані відповідні результати для сполук, які всі мають значення EC50 < 30 нМ. Аналіз додавання глутатіону (GSH) після метаболічної активації: Умови аналізу для детекції кон'югатів глутатіону відповідають методиці, описаній у C.M.Dieckhaus і соавт. у Chem.Res.Toxicol.,18, 630-638(2005). Зразки, для яких маса ковалентного аддукту з реактивним метаболітом була ясно виявлена, позначено як Flag (позитивний). Сполуки, для яких не було виявлено аддукту позначені як No Flag (негативний). Порівняння сполук за даним винаходом і референсних сполук Прикладів 20, 72, 76,79, 81 і 103 з документа WO2011128279: Всі сполуки даного винаходу мають аналогічну ефективність в порівнянні з референсними 2 UA 113779 C2 5 10 15 20 25 30 35 сполуками. Крім того, всі вони показують максимальну ефективність значно нижче 60% в порівнянні з найбільш високими значеннями референсних сполук (вище 80%), яка є критерієм по відношенню до проблем переносимості позитивних алостеричних модуляторів mGluR5. Сполуки з високими значеннями максимальної ефективності вище 60% проявляють важкі побічні ефекти, пов'язані з ЦНС, після перорального прийому (конвульсії) в дозах, близьких до таких, при яких спостерігається необхідний терапевтичний ефект (вузьке терапевтичне вікно). Сполуки з максимальною ефективністю нижче 60% добре переносяться при дозах, які можуть бути в 30 - 1000 разів вище, ніж терапевтична доза, при цьому зберігаючи свої необхідні терапевтичні ефекти. Загалом, сполуки даного винаходу, таким чином, мають очевидну перевагу відносно безпеки лікарських засобів, завдяки їх значенням максимальної ефективності нижче 60%, яка корелює з відсутністю несприятливих важких побічних ефектів на ЦНС в порівнянні із структурно близькими сполуками попереднього рівня техніки. Несподівано, деякі із сполук за даним винаходом також показують значно кращу розчинність в порівнянні з референсними сполуками. Кваліфікованим фахівцям добре відомо, що краща розчинність приводить до поліпшення всмоктування лікарського препарату, а також вищих значень вільної фракції, що, у свою чергу, приводять до підвищення доступності препаратів у відношенні до своєї цілі. Це особливо стосується препаратів, націлених на компартмент центральної нервової системи. На закінчення, сполуки за даним винаходом не показують реакцію з глутатіоном після метаболічної активації (GSH аналіз). Реакція хімічно активних препаратів з білками (ковалентне зв’язування білка (CVB)) є небажаною властивістю з погляду безпеки лікарських засобів. Білки можуть утворювати ковалентні аддукти з реактивними метаболітами молекул препаратів за допомогою їх нуклеофільних амінокислотних бічних ланцюгів (наприклад, цистеїн, серин, лізин і т. д.). Утворення аддуктів препарат-білок може приводити до небажаних реакцій імунної системи, яка розпізнає ковалентно зв'язані білки як чужорідні. Така імунна відповідь може привести до алергічних реакцій різної інтенсивності, званих імунна токсичність. Аналіз "золотого стандарту" CVB (ковалентного зв’язування), який виявляє утворення ковалентних аддуктів за допомогою інкубації тестованих сполук з мікросомами печінки людини (HLM) повинен проводитися з 14C-міченим матеріалом. Він не підходить для звичайних цілей скринінгу. Аналіз глутатіону після метаболічної активації (див. опис аналізу) є відповідним для рутинного скринінгу, і сполуки, які показують значну активність в цьому тесті, мабуть покажуть активність в аналізі CVB. Приведені вище дані показують, що сполуки за винаходом мають набагато меншу схильність до утворення ковалентних аддуктів препарат-глутатіон (NO FLAG), при тому, що відповідні референсні сполуки утворюють значні кількості глутатіонових кон'югатів (FLAG). Загалом, сполуки даного винаходу, таким чином, мають явну перевагу з погляду безпеки лікарських засобів у зв'язку з їх набагато менш вираженою тенденцією до утворення реактивних метаболітів в порівнянні із структурно схожими сполуками, відомими з рівня техніки. Список прикладів: Пр. № Структура Ec50 [нМ] Ефективність [%] GSH [HLM] Реф. Пр. 20 27 135 н.д. Реф. Пр. 72 10 86 FLAG Реф. Пр. 76 13 124 FLAG 3 UA 113779 C2 Реф. Пр. 79 12 95 FLAG 27 123 FLAG Пр. 1 22 38 NO FLAG Пр. 2 10 43 NO FLAG Пр. 3 10 40 NO FLAG Пр. 4 15 FLAG Реф. Пр. 103 10 85 Реф. Пр. 81 5 22 15 35 No FLAG Сполуки формули I відрізняються наявністю цінних терапевтичних властивостей. Вони можуть застосовуватися для лікування або профілактики розладів, пов'язаних з алостеричними модуляторами mGluR5 рецепторів. Найбільш переважними свідченнями для сполук, які є алостеричними модуляторами, є шизофренія і процеси пізнання. Даний винахід відноситься до сполук формули I та їх фармацевтично прийнятних солей, до цих сполук як фармацевтично активні речовини, до способів їх одержання, а також до їх застосування для лікування або профілактики порушень, що асоціюються з алостеричними модуляторами mGluR5 рецепторів, таких як шизофренія і порушення пізнавальної здатності, а також до фармацевтичних композицій, що містять сполуки формули I. Наступні визначення загальних термінів, що використовуються в даному описі, застосовуються незалежно від того, чи використовуються терміни окремоабо в комбінації. Термін "фармацевтично прийнятна сіль" або "фармацевтично прийнятна кислотно-адитивна сіль" включає солі з неорганічними і органічними кислотами, такими як соляна кислота, азотна кислота, сірчана кислота, фосфорна кислота, лимонна кислота, мурашина кислота, фумарова кислота, малеїнова кислота, оцтова кислота, янтарна кислота, винна кислота, метансульфонова кислота, п-толуолсульфонова кислота і т. п. Одним з втілень даного винаходу є сполуки формули I 4 UA 113779 C2 H H N N O O 1 R 5 10 15 20 25 I, де 1 R позначає феніл, 3-фторфеніл, 4-фторфеніл або 2,5-дифторфеніл; або фармацевтично прийнятна кислотно-адитивна сіль, в енантіомерно чистому вигляді з абсолютною конфігурацією, як показано у формулі I. Сполуки формули I є наступними: (4aS,7aR)-1-(5-Фенілетиніл-піридин-2-іл)-гексагідро-циклопента[d][1,3]оксазин-2-он (4aS,7aR)-1-[5-(3-Фторфенілетиніл)-піридин-2-іл]-гексагідро-циклопента[d][1,3]оксазин-2-он (4aS,7aR)-1-(5-((4-Фторфеніл)етиніл)-піридин-2-іл)гексагідро-циклопента[d][1,3]оксазин2(1H)-он (4aS,7aR)-1-[5-(2,5-Дифторфенілетиніл)-піридин-2-іл]-гексагідро-циклопента[d][1,3]оксазин-2он Одержання сполук формули I за даним винаходом може проводитися послідовним або конвергентним синтезом. Синтези сполук за винаходом показані на наведених нижче схемах 1 3. Навички, необхідні для проведення реакцій і очищення одержаних продуктів, відомі фахівцям в даній області. Заступники та індекси, використовувані в наступному описі методик, мають значення, зазначені тут раніше. Сполуки формули I можуть бути одержані способами, приведеними нижче, способами, наведеними в прикладах, або аналогічними способами. Відповідні умови реакції для окремих стадій реакції відомі фахівцеві в даній області. Послідовність реакцій не обмежується такою, яка зображена на схемах, проте, залежно від початкових матеріалів та їх реакційної здатності, послідовність стадій реакції можуть бути вільно змінені. Початкові речовини є або комерційно доступними, або можуть бути одержані способами, аналогічними способам, приведеним нижче, способами, описаними в посиланнях, наведених в описі або в прикладах, або способами, відомими в даній області техніки. Дані сполуки формули I та їх фармацевтично прийнятні солі можуть бути одержані способами, відомими в рівні техніки, наприклад, різними варіантами способу, описаного нижче, який включає а) взаємодію сполуки формули 3 H H HN 30 O O 3, де сполука формули 3 є рацемічною сумішшю або знаходиться в енантіомерно чистому вигляді, з відповідною арилацетиленовою сполукою галопіридину формули 4, де Y позначає галоген, переважно фтор, бром або йод N Y 1 R 35 4 з утворенням сполуки формули I в енантіомерно чистому вигляді або у вигляді рацемічної суміші, де енантіомери можуть бути розділені з використанням способів відомих кваліфікованим фахівцям, 5 UA 113779 C2 H H N N O O R 5 1 I де заступники є такими, як описано вище, або, якщо необхідно, конвертація одержаних сполук у фармацевтично прийнятні кислотно-адитивні солі або за допомогою b) взаємодії сполуки формули II в енантіомерно чистому вигляді або у вигляді рацемічної суміші, де X позначає галоген, переважно йод або бром H N H N O O X II з ацетиленовою сполукою формули 5, де Q позначає водень або триалкілсилільну групу Q R 10 1 5 з утворенням сполуки формули I в енантіомерно чистому вигляді або у вигляді рацемічної суміші, яка може бути розділена з використанням способів, відомих кваліфікованим фахівцям, H H N N O O 1 R 15 20 I де заступники є такими, як описано в пункті 1, або, якщо необхідно, конвертація одержаних сполук у фармацевтично прийнятні кислотно-адитивні солі. Одержання сполук формули I додатково детальніше описано на схемах 1 - 3 та в прикладах 1 - 4. Сполуку формули 3 може бути одержано з використанням як початкової речовини рацемічної або оптично чистої захищеної амінокислоти формули 1 за допомогою відновлення з алюмогідридом літію в ТГФ (THF) з утворенням спирту 2, який потім циклізують в лужному середовищі з одержанням біциклічного карбамату 3. Галопіридин-арилацетилен 4 синтезують за допомогою зв’язування Соногашири відповідної заміщеної похідної арилацетилену 5 (де Q позначає або in-situ захисну групу, що відщеплюється, таку як триалкілсилільна або діалкілсилільна група, переважно водень або триметилсиліл) з, наприклад, 2-фтор-5йодпіридином або 2-бром-5-йодпіридином. Каталізоване основою нуклеофільне заміщення 6 UA 113779 C2 (наприклад NaH/ДМФ; або Cs2CO3/Толуол) у разі, коли Y позначає фтор або при каталізі паладієм (Бухвальд), коли Y позначає бром, у присутності біциклічного карбамату 3 дає сполуки формули I (схема 1). 5 10 Альтернативно,взаємодія карбамату 3 з дигалопіридином, таким як 2-фтор-5-йодпіридин або 2-йод-5-бромпіридин, з використанням умов, описаних вище, також може утворювати сполуку формули II, де X позначає йод або бром (схема 2). Сполука II потім взаємодіє з відповідною заміщеною похідною арилацетилену 5 в умовах каналізованого паладієм зв'язування (реакція Соногашири) з утворенням сполук формули I. Альтернативно, ацетиленова часто може бути одержана за дві стадії за допомогою первинної взаємодії сполуки II з частково захищеною сполукою ацетилену, такою як, наприклад, триметилсилілацетилен з одержанням проміжної сполуки формули Ib з подальшою реакцією Соногашири (у присутності фториду для відщеплення in-situ захисної групи силілу) з відповідним заміщеним арилгалогенідом, де X позначає бром або йод, з утворенням сполуки формули I. (схема 3). 15 20 25 30 35 40 У разі використання рацемічної сполуки 3, енантіомери можуть бути розділені на будь-якій даній стадії протягом синтезу сполук формули I, з використанням методик, відомих кваліфікованим фахівцям. Переважно, сполуку формули I, як описано вище, а також її фармацевтично прийнятну сіль застосовують для лікування або профілактики психозу, епілепсії, шизофренії, хвороби Альцгеймера, когнітивних розладів і порушення пам'яті, хронічного і гострого болю, обмеженої функції мозку, викликаної шунтуванням або пересадкою, поганого кровопостачання головного мозку, травми спинного мозку, травми голови, гіпоксії, викликаною вагітністю, зупинки серця і гіпоглікемії, ішемії, хореї Гентінгтона, бічного аміотрофічного склерозу (ALS), недоумства, викликаного СНІДом, травми очей, ретинопатії, ідіопатичного паркінсонізму або паркінсонізму, викликаного лікарськими засобами, м'язових спазмів, конвульсій, мігрені, нетримання сечі, шлунково-кишкові рефлюкс розлади, пошкодження печінки або печінкова недостатність, викликані препаратами або захворюванням, синдрому Мартіна-Белл, синдрому Дауна, аутизму, нікотинової залежності, опіатної залежності, тривоги, блювоти, дискінезії, харчових розладів, зокрема, булімії або анорексії, і депресій, особливо для лікування і профілактики гострих та/або хронічних неврологічних розладів, тривоги, лікування хронічного і гострого болю, нетримання сечі та ожиріння. Переважними свідченнями є шизофренія і когнітивні розлади. Даний винахід також відноситься до застосування сполуки формули I, як описано вище, а також її фармацевтично прийнятної солі для виготовлення лікарського засобу, переважно для лікування і профілактики вищезазначених захворювань. Біологічні аналіз і дані: 2+ Аналіз внутріклітинної мобілізації Ca 2+ Аналіз внутріклітинної мобілізації Ca , як описано вище, використовувався для визначення значень EC50. У списку прикладів нижче показані відповідні результати для сполук, які всі мають значення EC50 менші або рівні 22 нМ. Список прикладів: 45 7 UA 113779 C2 Приклад 1 2 3 4 5 10 15 20 25 30 35 40 EC50 (нМ) mGlu5 PAM 22 10 10 15 Сполуки формули (I) та їх фармацевтично прийнятні солі можуть застосовуватися як лікарські засоби, наприклад у вигляді фармацевтичних препаратів. Фармацевтичні препарати можуть бути введені перорально, наприклад, у вигляді таблеток, таблеток з покриттям, драже, твердих і м'яких желатинових капсул, розчинів, емульсій або суспензій. Проте введення також може бути здійснене ректально, наприклад, у формі супозиторіїв, або парентерально, наприклад, у вигляді розчинів для ін'єкцій. Сполуки формули (I) та їх фармацевтично прийнятні солі можуть бути перероблені з фармацевтично інертними, неорганічними або органічними носіями для одержання фармацевтичних препаратів. Лактоза, кукурудзяний крохмаль або його похідні, тальк, стеаринова кислота або її солі і т. п. можуть бути використані, наприклад, як такі носії для таблеток, таблеток з покриттям, драже і твердих желатинових капсул. Відповідними носіями для м'яких желатинових капсул є, наприклад, рослинні олії, віск, жири, напівтверді і рідкі поліоли і т.п.; залежно від природи активної речовини ніяких носіїв, проте, зазвичай не потрібні у разі м'яких желатинових капсул. Відповідними носіями для одержання розчинів і сиропів є, наприклад, вода, поліоли, сахароза, інвертний цукор, глюкоза і т. п. Ад'юванти, такі як спирти, поліоли, гліцерин, рослинні олії і т. п., можуть бути використані для водних ін'єкційних розчинів на основі водорозчинних солей сполук формули (I), але, як правило, не є необхідними. Відповідними носіями для супозиторіїв є, наприклад, природні або отверджені масла, віск, жири, напіврідкі або рідкі поліоли і т. п. Крім того,фармацевтичні препарати можуть містити консерванти, солюбілізатори, стабілізатори, змочуючі агенти, емульгатори, підсолоджувачі, барвники, ароматизатори, солі для зміни осмотичного тиску, буфери, маскуючі агенти або антиоксиданти. Вони також можуть містити інші терапевтично цінні речовини. Як згадувалося раніше, лікарські засоби, що містять сполуку формули (I) або їх фармацевтично прийнятні солі і терапевтично інертний ексципієнт, також є об'єктом даного винаходу, так само як і спосіб одержання таких лікарських засобів, який включає приведення одної або більше сполук формули I або їх фармацевтично прийнятних солей і, при необхідності, одної або більше інших терапевтично цінних речовин в галенову лікарську форму разом з одним або більше терапевтично інертним носієм. Як також згадувалося раніше, застосування сполук формули (I) для одержання лікарських засобів для профілактики та/або лікування зазначених вище захворювань також є об'єктом даного винаходу. Дозування може варіюватися в широких межах і, звичайно, повинно відповідати індивідуальним вимогам у кожному конкретному випадку. Загалом, ефективне дозування для перорального або парентерального введення знаходиться в інтервалі 0,01-20 мг/кг/день, дозування 0,1-10 мг/кг/день є переважним для всіх описаних свідчень. Добова доза для дорослої людини вагою 70 кг, відповідно, знаходиться в інтервалі 0,7-1400 мг на день, переважно між 7 і 700 мг на день. Одержання фармацевтичних композицій, які містять сполуки за даним винаходом: Пігулки наступного складу були одержані звичайним способом: мг/таблетка Активна речовина 100 Порошкоподібна лактоза 95 Білий кукурудзяний крохмаль 35 Полівінілпіролідон 8 Na-карбоксиметилцелюлоза 10 Стеарат магнію 2 Вага таблетки 250 Приклад 1 (4aS,7aR)-1-(5-Фенілетиніл-піридин-2-іл)-гексагідро-циклопента[d][1,3]оксазин-2-он 8 UA 113779 C2 Стадія 1: ((1R,2S)-2-Гідроксиметил-циклопентил)-карбамінової кислоти трет-бутиловий ефір OH NH O 5 10 O До добре перемішаної суспензії 0.94 г (24.7 ммоль, 2 екв.) LiAlH4 в 30 мл ТГФ при 0 °C додали по краплях при 0 °C розчин (1S,2R)-метил 2-(трет-бутоксикарбоніламіно)циклопентанкарбоксилату (CAS: 592503-55-4) (3.0 г, 12.3 ммоль) (виділення газу, невелика екзотермічність). Через 15 хвилин при 0 °C реакційної суміші дали нагрітися до кімнатної температури і перемішували протягом 2 г. Суміш охолодили до 0 °C додали воду по краплях. Преципітовані неорганічні солі відфільтрували через целіт і промили етилацетатом. Фільтрат евапорували і залишок очистили за допомогою колоночної хроматографії на силікагелі з елюцією 0% - 50% етилацетатом в градієнті гептану з одержанням 1.99 г (75%) сполуки, зазначеної в заголовку, у вигляді а кристалічного білого осаду, який відразу використовували на наступній стадії. Стадія 2: (4aS,7aR)-Гексагідро-циклопента[d][1,3]оксазин-2-он H H HN 15 20 O O До розчину ((1R,2S)-2-гідроксиметил-циклопентил)-карбамінової кислоти трет-бутилового ефіру (1.6 г, 7.43 ммоль) в ТГФ (40 мл) додали трет-бутоксид калію (3.34 г, 29.7 ммоль, 4.0 екв.) при кімнатній температурі. Після перемішування протягом 1 г при 60 °C реакційної суміші дали нагрітися до кімнатної температури і після обробки етилацетатом/водою, сушки і концентрації під вакуумом, неочищену суміш матеріалу адсорбували на силікагелі і піддали хроматографії на попередньо заповненій колонці з силікагелем (50 г, 50% - 100% градієнт EtOAc в гептані) з одержанням 950 мг (91%) сполуки, зазначеної в заголовку, у вигляді білого осаду, який відразу використовували на наступній стадії. Стадія 3: 2-Фтор-5-фенілетиніл-піридин N F 25 30 35 40 45 У 100 мл 2-горлишковій круглодонній колбі під аргоном розчинили 2-фтор-5-йодпіридин (5.0 г, 22.4 ммоль, 1.0 екв.) в ТГФ (30 мл). Через 5 хвилин при кімнатній температурі додали біс(трифенілфосфін)паладій(II) хлорид (944 мг, 1.35 ммоль, 0.06 екв.), триетиламін (6.81 г, 9.32 мл, 67.3 ммоль, 3.0 екв.), фенілацетилен (2.75 г, 2.95 мл, 26.9 ммоль, 1.2 екв.) та йодид міді (I) (128 мг, 0.67 ммоль, 0.03 екв.). Коричневу суспензію охолодили водою (екзотермічна) до кімнатної температури і перемішували протягом ночі. Потім додали 200 мл діетилового ефіру, суміш відфільтрували, промили ефіром і сконцентрували під вакуумом з одержанням 5.7 г коричневого осаду, який адсорбували на силікагелі та піддали хроматографії в 2 порціях на 100 г попередньо заповненій колонці з силікагелем, елююючи 0-10% градієнтом етилацетату в гептані, з одержанням 3.99 г (91%) сполуки, зазначеної в заголовку, у вигляді світло+ коричневого осаду, MS: m/e = 198.1 (M+H ). Стадія 4: (4aS,7aR)-1-(5-Фенілетиніл-піридин-2-іл)-гексагідро-циклопента[d][1,3]оксазин-2-он У 10 мл круглодонній колбі розчинили (4aS,7aR)-гексагідро-циклопента[d]-[1,3]оксазин-2-он (80 мг, 0.57 ммоль,1.0 екв.) і 2-фтор-5-(фенілетиніл)піридин (112 мг, 0.57 ммоль, 1.0 екв.) в 2 м ДМФ. Додали гідрид натрію (60% суспензія) (29.5 мг, 0.74 ммоль, 1.3 екв.) і коричневу суспензію перемішували при кімнатній температурі протягом ночі. Реакційну суміш погасили водою і екстрагували двічі етилацетатом. Об'єднані органічні фази висушили, відфільтрували і сконцентрували. Неочищену речовину очистили за допомогою флеш-хроматографії на попередньо заповненій колонці з силікагелем, елююючи 0-50% градієнтом етилацетату в гептані, з одержанням 42.5 мг сполуки, зазначеної в заголовку, у вигляді безбарвного + аморфного осаду, MS: m/e = 319.1 (M+H ). 9 UA 113779 C2 Приклад 2 (4aS,7aR)-1-[5-(3-Фторфенілетиніл)-піридин-2-іл]-гексагідро-циклопента[d][1,3]оксазин-2-он Стадия 1: 2-Фтор-5-(3-фтор-фенілетиніл)-піридин F N F 5 10 15 Сполуку, зазначену в заголовку одержали відповідно до загального способу прикладу 1, стадія 3 з використанням 3-фторфенілацетилену замість фенілацетилену з одержанням + сполуки, зазначеної в заголовку, у вигляді а кристалічного білого осаду, MS: m/e = 216.2 (M+H ). Стадія 2: (4aS,7aR)-1-[5-(3-Фторфенілетиніл)-піридин-2-іл]-гексагідроциклопента[d][1,3]оксазин-2-он Сполуку, зазначену в заголовку одержали відповідно до загального способу прикладу 1, стадія 4 з використанням (4aS,7aR)-гексагідро-циклопента[d]-[1,3]оксазин-2-ону (66 мг, 0.47 ммоль) (Приклад 1, стадія 2) і 2-фтор-5-((3-фторфеніл)етиніл)піридину (100 мг, 0.47 ммоль) з одержанням 48 мг (31%) сполуки, зазначеної в заголовку, у вигляді світло-жовтого аморфного + осаду; MS: m/e = 337.3 (M+H ). Приклад 3 (4aS,7aR)-1-[5-(4-Фторфенілетиніл)-піридин-2-іл]-гексагідро-циклопента[d][1,3]оксазин-2-он Стадія 1: 2-Фтор-5-(4-фтор-фенілетиніл)-піридин N F 20 25 30 F Сполуку, зазначену в заголовку одержали відповідно до загального способу прикладу 1, стадія 3 з використанням 4-фторфенілацетилену замість фенілацетилену з одержанням + сполуки, зазначеної в заголовку, у вигляді світло-коричневого осаду, MS: m/e = 216.2 (M+H ). Стадія 2: (4aS,7aR)-1-[5-(3-Фторфенілетиніл)-піридин-2-іл]-гексагідроциклопента[d][1,3]оксазин-2-он Сполуку, зазначену в заголовку, одержали відповідно до загального способу прикладу 1, стадія 4 з використанням (4aS,7aR)-гексагідро-циклопента[d][1,3]оксазин-2-ону (66 мг, 0.47 ммоль) (Приклад 1, стадія 2) і 2-фтор-5-((3-фторфеніл)етиніл)піридину (100 мг, 0.47 ммоль) з одержанням 22 мг (14%) сполуки, зазначеної в заголовку, у вигляді безбарвного масла; MS: m/e + = 337.4 (M+H ). Приклад 4 (4aS,7aR)-1-[5-(2,5-Дифторфенілетиніл)-піридин-2-іл]-гексагідро-циклопента[d]-[1,3]оксазин2-он H N H N O O F F 35 Стадия 1: (рац)-(4aSR,7aRS)-Гексагідро-циклопента[d][1,3]оксазин-2-он 10 UA 113779 C2 H H HN O O 5 Сполуку, зазначену в заголовку одержали відповідно до аналогічних методик, описаних в прикладі 1, стадії 1 і 2, з використанням як початкової речовини рацемічного (1SR,2RS)-метил 2(трет-бутоксикарбоніламіно)-циклопентанкарбоксилату (CAS: 164916-42-1 ) з одержанням + сполуки, зазначеної в заголовку, у вигляді безбарвного масла; MS: m/e = 142.3 (M+H ). Стадія 2: 5-(2,5-Дифтор-фенілетиніл)-2-фтор-піридин F N F F 10 15 20 25 Сполуку, зазначену в заголовку одержали відповідно до загального способу прикладу 1, стадія 3 з використанням 2,5-дифторфенілацетилену замість фенілацетилену з одержанням + сполуки, зазначеної в заголовку, у вигляді жовтого осаду, MS: m/e = 234.4 (M+H ). Стадія 3: (рац)-(4aSR,7aRS)-1-[5-(2,5-Дифтор-фенілетиніл)-піридин-2-іл]-гексагідроциклопента[d][1,3]оксазин-2-он Сполуку, зазначену в заголовку, одержали відповідно до загального способу прикладу 1, стадія 4 з використанням (рац)-(4aSR,7aRS)-гексагідро-циклопента[d][1,3]оксазин-2-ону (30 мг, 0.21 ммоль) (приклад 4, стадія 2) і 5-(2,5-дифтор-фенілетиніл)-2-фтор-піридину (50 мг, 0.21 ммоль) з одержанням 33 мг (43%) сполуки, зазначеної в заголовку, у вигляді жовтого масла; + MS: m/e = 355.6 (M+H ). Стадія 4: (-)-(4aS,7aR)-1-[5-(2,5-Дифтор-фенілетиніл)-піридин-2-іл]-гексагідроциклопента[d][1,3]оксазин-2-он Рацемічну суміш (рац)-(+/-)-(rac)-(4aSR,7aRS)-1-[5-(2,5-дифтор-фенілетиніл)-піридин-2-іл]гексагідро-циклопента[d][1,3]оксазин-2-ону (Приклад 1) (33 мг) розділили за допомогою хіральної ВЕРХ: (Reprosil Chiral NR - 5 см x 50 см, 20 мкм; 40 % етанол/гептан, 35 мл/хв, 18 Бар). Одержали (+)-(4aR,7aS)-1-[5-(2,5-дифтор-фенілетиніл)-піридин-2-іл]-гексагідро+ циклопента[d][1,3]оксазин-2-он (15 мг) у вигляді світло-жовтого масла, MS: m/e = 355.6 (M+H ) і (-)-(4aR,7aS)-1-[5-(2,5-дифтор-фенілетиніл)-піридин-2-іл]-гексагідро+ циклопента[d][1,3]оксазин-2-он (14.9 мг) у вигляді світло-жовтого масла, MS: m/e = 355.6 (M+H ). ФОРМУЛА ВИНАХОДУ 30 1. Етинілпохідна формули І H H N N O O R 35 40 1 ,I де 1 R позначає феніл, 3-фторфеніл, 4-фторфеніл або 2,5-дифторфеніл; або фармацевтично прийнятна кислотно-адитивна сіль, в енантіомерно чистому вигляді. 2. Етинілпохідна формули І, де сполуки позначають (4aS,7aR)-1-(5-Фенілетиніл-піридин-2-іл)-гексагідро-циклопента[d] [1,3]оксазин-2-он, (4аS,7аR)-1-[5-(3-фторфенілетиніл)-піридин-2-іл]-гексагідро-циклопента[d][1,3]оксазин-2-он, (4аS,7аR)-1-(5-((4-фторфеніл)етиніл)-піридин-2-іл)гексагідро-циклопента[d][1,3]оксазин-2(1Н)-он або (4аS,7аR)-1-[5-(2,5-дифторфенілетиніл)-піридин-2-іл]-гексагідро-циклопента[d][1,3]оксазин-2-он. 3. Спосіб одержання сполуки формули І як описано в пункті 1, що містить варіанти: 11 UA 113779 C2 а) взаємодія сполуки формули 3 H H HN O O 5 ,3 де сполука формули 3 є рацемічною сумішшю або знаходиться в енантіомерно чистому вигляді з відповідним арилацетиленовою сполукою галопіридину формули 4, де Υ позначає галоген, вибраний з фтору, брому або йоду N R Y 1 4 10 з утворенням сполуки формули І в енантіомерно чистому вигляді або у вигляді рацемічної суміші, де енантіомери можуть бути розділені з використанням способів відомих кваліфікованим фахівцям, H H N N O O 15 20 R 1 ,I де заступники є такими, як визначено вище, або, якщо необхідно, конвертація одержаних сполук у фармацевтично прийнятні кислотно-адитивні солі, або b) взаємодія сполуки формули II в енантіомерно чистому вигляді або у вигляді рацемічної суміші, де X позначає галоген, переважно йод або бром H H N N O O X II з ацетиленовою сполукою формули 5, де Q позначає водень або триалкілсилільну групу 25 Q R 1 ,5 12 UA 113779 C2 з утворенням сполуки формули І в енантіомерно чистому вигляді або у вигляді рацемічної суміші, яка може бути розділена з використанням способів відомих кваліфікованим фахівцям, H H N N O O 5 10 15 20 R 1 ,I де заступники є такими, як описано в пункті 1, або, якщо необхідно, конвертація одержаних сполук у фармацевтично прийнятні кислотно-адитивні солі. 4. Сполука за будь-яким з пп. 1-2 для застосування як терапевтично активної речовини. 5. Фармацевтична композиція, яка містить щонайменше одну сполуку за будь-яким з пп. 1-2 або її фармацевтично прийнятну сіль. 6. Сполука за будь-яким з пп. 1-2, вживана у вигляді суміші енантіомерів, діастереомерів або в енантіомерно чистому вигляді; або її фармацевтично прийнятна сіль для застосування як лікарський засіб. 7. Застосування сполуки за будь-яким з пп. 1-2 або її фармацевтично прийнятної солі для виробництва лікарського засобу для лікування або профілактики захворювань, пов'язаних з алостеричними модуляторами рецепторів mGluR5. 8. Застосування сполуки за п. 7 для лікування або профілактики шизофренії, когнітивних захворювань, синдрому Мартіна-Белл або аутизму. 9. Сполука за будь-яким з пп. 1-2 для лікування або профілактики шизофренії, когнітивних захворювань, синдрому Мартіна-Белл або аутизму. 10. Спосіб лікування шизофренії, когнітивних захворювань, синдрому Мартіна-Белл або аутизму, який включає введення ефективної кількості сполуки за будь-яким з пп. 1-2. Комп’ютерна верстка Л. Бурлак Державна служба інтелектуальної власності України, вул. Василя Липківського, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут інтелектуальної власності”, вул. Глазунова, 1, м. Київ – 42, 01601 13
ДивитисяДодаткова інформація
Назва патенту англійськоюArylethynyl derivatives
Автори англійськоюJaeschke, Georg, Lindemann, Lothar, Stadler, Heinz, Vieira, Eric
Автори російськоюЕшке Георг, Линдеманн Лотар, Штадлер Хайнц, Виэйра Эрик
МПК / Мітки
МПК: C07D 413/04, A61K 31/444
Мітки: арилетинілу, похідні
Код посилання
<a href="https://ua.patents.su/15-113779-pokhidni-ariletinilu.html" target="_blank" rel="follow" title="База патентів України">Похідні арилетинілу</a>
Попередній патент: Багатоканальний датчик електроміограми
Наступний патент: Застосування 1-[4-(1-адамантил)-фенокси]-3-(n-бензил,n-диметиламіно)-2-пропанолхлориду як інгібітору утворення патогенних біоплівок
Випадковий патент: Спосіб захисту інформації у лініях зв`язку