Кристалічні моногідрати гідрохлориду ендо-2,3-дигідро-n-(8-метил-8-азабіцикло [ 3.2.1 ] окт-3-іл) -2-оксо-1н-бензимідазол-1-карбоксаміду та ендо-3-етил-2,3-дигідро-n-(8-метил-8-азабіцикло[3.2.1]окт-3-іл)-2-оксо
Номер патенту: 37179
Опубліковано: 15.05.2001
Автори: Антуан Ецхая, Марко Турконі, Грація Маффіоне, Енцо Череда, Енріка Дубіні
Формула / Реферат
1. Кристаллические моногидраты гидрохлоридов эндо-2,3-дигидро-N-(8-метил-8-азабицикло[3.2.1]окт-3-ил)-2-оксо-1Н-бензимидазол-1-карбоксамида и эндо-З-этил-2,3-дигидро-N-(8-метил-8-азабицикло[3.2.1]окт-3-ил)-2-оксо-1 Н-бензимидазол-1-карбоксамида формулы (I):
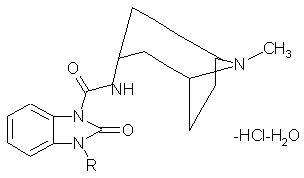 , (I)
, (I)
где:
R - атом водорода или этил, при этом производное карбоксамида, у которого R означает атом водорода, характеризуется следующими данными рентгеновской дифракции простого кристалла:
моноклинная решетка P21/C, а = 11,668 А, b = 11,714 А, с =13, 672 А, α=900, β=114,830, γ=900, а производное карбоксамида, у которого R означает этил, характеризуется следующими данными рентгеновской дифракции простого кристалла:
моноклинная решетка P21/C, а = 13,869 (2), b = 16,449 (2), с = 8,550(1)A, α=90°, β=97,64 (1)°, γ=90°, V = 1933,1 (5)A3, Z = 4.
2. Способ получения кристаллических моногидратов гидрохлоридов эндо-2,3-дигидро-N-(8-метил-8-азабицикло[3.2.1]окт-3-ил)-2-оксо-1Н-бензимидазол-1-карбоксамида и эндо-3-этил-2,3-дигидро-N-(8-метил-8-азабицикло[3.2.1]окт-3-ил)-2-оксо-1Н-бензимидазол-1-карбоксамида по пункту 1, отличающийся тем, что исходный эндо-2,3-дигидро-N-(8-метил-8-азабицикло[3.2.1]окт-3-ил)-2-оксо-1Н-бензимидазол-1-карбоксамид- или соответственно эндо-3-этил-2,3-дигидро-N-(8-метил-8-азабицикло[3.2.1]окт-3-ил)-2-оксо-1 Н-бензимидазол-1-карбоксамид растворяют в горячем водном алканоле и после добавления газообразного хлористого водорода раствор фильтруют и охлаждают до комнатной температуры с получением кристаллов соответствующего целевого соединения, которое обезвоживают под вакуумом при температуре от комнатной до 60°С.
3. Способ по п.2, отличающийся тем, что при получении соединения формулы (І), у которого R означает атом водорода, в качестве водного алканола используют 85 % водный этанол.
4. Способ по п.2, отличающийся тем, что при получении соединения формулы (І), у которого R означает этил, в качестве водного алканола используют 95 % водный изопропанол.
5. Фармацевтическая композиция, обладающая свойством антагониста 5-НТ рецепторов, содержащая активный компонент и фармацевтические носители или разбавители, отличающаяся тем, что в качестве активного компонента она содержит кристаллический моногидрат гидрохлорида эндо-2,3-дигидро-N-(8-метил-8-азабицикло[3.2.1]окт-3-ил)-2-оксо-1Н-бензимидазол-1-карбоксамида или соответственно гидрохлорида эндо-2,3-дигидро-N-(8-метил-8-азабицикло[3.2.1]окт-3-ил)-2-оксо-1Н-бензимидазол-1-карбоксамида в терапевтически эффективном количестве.
Текст
1. Кристаллические моногидраты гидрохлоридов эндо-2,3-дигидро-N-(8-метил-8-азабицикло [3.2.1]окт-3-ил)-2-оксо-1Н-бензимидазол-1-карбоксамида и эндо-З-этил-2,3-дигидро-N-(8-метил-8азабицикло[3.2.1]окт-3 -ил)-2-оксо-1 Н-бензимидазол-1 -карбоксамида формулы (I): C2 (54) КРИСТАЛІЧНІ МОНОГІДРАТИ ГІДРОХЛОРИДУ ЕНДО-2,3-ДИГІДРО-N-(8-МЕТИЛ-8-АЗАБІЦИКЛО [ 3.2.1 ] ОКТ-3-ІЛ) -2-ОКСО-1Н-БЕНЗИМІДАЗОЛ-1-КАРБОКСАМІДУ ТА ЕНДО-3-ЕТИЛ-2,3-ДИГІДРО-N-(8МЕТИЛ-8-АЗАБІЦИКЛО[3.2.1]ОКТ-3-ІЛ)-2-ОКСО-1Н-БЕНЗИМІДАЗОЛ-1-КАРБОКСАМІДУ, СПОСІБ ЇХ ОДЕРЖАННЯ ТА ФАРМАЦЕВТИЧНА КОМПОЗИЦІЯ 37179 а) пункт 1, касающийся соединения, у которого R означает водород; б) пункт 2, касающийся получения соединения по п. 1, у которого R означает водород; в) пункт 3; г) пункт 5, касающийся активного компонента по п. 1, у которого R означает водород. _______________________ Данное изобретение касается новых производных 2-оксо-1Н-бензимидазол-1-карбоксамида, обладающих ценными фармакологическими свойствами, в частности, кристаллических моногидратов гидрохлоридов эндо-2,З-дигидро-N-(8-метил-8-азабицикло[3,2,1]-октил-3)-2-оксо-1Н-бензимидазол-1-карбоксамида и эндо-З-этил-2,З-дигидро-N(8-метил-8-азабицикло-[3,2,1 ]-октил-3)-2-оксо-1Нбензимидазол-1-карбоксамида, способа их получения и фармацевтической композиции, содержащей эти соединения. Известны производные бензимидазолин-2оксо-1-карбоновой кислоты общей формулы (d) где р = 0 или 1; r = 0,1,2 или 3; R4 означает атом водорода или алкил С1-С4; R5 означает атом водорода, алкил С1-С6, циклоалкил С3-С8, (С3-С8)циклоалкил-(С1-С4)-алкил, алкил С1-С4, замещенный фенилом или R означает группу формулы -С = N-R7 R6 где R6 означает атом водорода, алкил С1-С4 или амино-группу, R7 означает атом водорода или алкил С1-С6, таутомеры этих соединений и соли присоединения кислот этих соединений, производные которых обладают ценными фармакологическими свойствами. Они особенно полезны как антагонисты 5-НТ-рецепторов (см.Европейскую патентную заявку 0 309 423 А2, С 07 Д 451/12, 1989). Безводные хлористоводородные соли эндо2,3-дигидро-N-(8-метил-8-азабицикло-[3,2,1]-октил3)-2-оксо-1Н-бензимидазол-1-карбоксамида (соединение А) и эндо-3-этил-2,3-дигидро-N-(8-метил-8азабицикло-[3,2,1]-октил-3)-2-оксо-1Н-бензимидазол1-карбоксамид-гидрохлорида (соединение В), разработанные в настоящее время как антагонисты рецепторов 5-НТ, являются полезными в качестве противорвотных и успокаивающих средств. где R означает атом водорода, алкил С1-С6, алкенил С1-С6, или алкинил С1-С6; R1 и R2 могут быть одинаковыми или различными и означают атом водорода или галогена, трифторметил, алкил С1С6, (С1-С6)-алкокси, (С1-С6)-алкилтио, ацил С1-С6, карбоксил, (С1-С6)-алкоксикарбонил, гидроксил, нитро-группу, аминогруппу, которая может быть Nмоно- или дизамещенной алкилом С1-С4, (С1-С6)ациламин, (С1-С6)-алкоксикарбониламино, карбамоил, который может быть N-моно- или дизамещен С1-С4, циано-группу, (С1-С6)-алкилтионил, (С1С6)-алкилсульфонил, аминосульфонил, который может быть N-моно- или дизамещен алкилом С1С4, аминосульфониламино-группу, N-моно- или дизамещенную алкилом С1-С4, аминосульфониламино-группу; Y означает кислород или группу NR3, где R3 - водород, алкил С1-С6 или бензил, который может быть замещен одной или несколькими (С1-С6)-алкокси-группами; А означает группу, выбранную из: × HCI (соединение A: R - Н) (соединение В: R - С2Н5) Из возможных видов употребления соединения А и В могут употребляться пациентами, как обычно, через рот в виде подходящих фармацевтических составов, таких как таблетки, таблетки с покрытием и капсулы, или ректально с использованием, например, суппозиториев. Такие виды употребления предпочтительны в сравнении, например, с парентеральным применением, поскольку не требуется присутствия доктора или того, кто мог бы сделать инъекцию. Хорошее производство указанных выше препаратов, полезных для орального употребления лекарственного вещества, обеспечивается различными параметрами, которые связаны с природой самого лекарственного вещества. Такими параметрами, например, являются стабильность (a) (b) (c) 2 37179 лекарственного исходного вещества в различных условиях окружающей среды, стабильность в процессе производства и стабильность в конечных фармацевтических композициях. Лекарственное вещество, используемое для приготовления указанных выше фармацевтических композиций, должно быть, насколько можно, чистым,и его стабильность при продолжительном хранении в различных условиях окружающей среды следует контролировать, чтобы избежать употребления деструктированного лекарственного вещества или лекарственного вещества с титром, который непредсказуемо ниже, чем требуется для процесса производства. В таких случаях содержание лекарственного вещества в отдельной таблетке или в капсуле должно быть непредсказуемо ниже, чем можно было ожидать. Абсорбция влаги понижает титр лекарственного вещества вследствие увеличения веса за счет содержания воды. Лекарственные вещества, способные абсорбировать влагу, следует защищать от влаги во время продолжительного хранения, например, добавлением подходящих осушителей или путем хранения лекарственного вещества в помещении, защищенного от влаги. Кроме того, абсорбция влаги может понижать титр лекарственного вещества в ходе процесса производства, если лекарственное вещество остается незащищенным при нормальных условиях без какой-либо защиты от влаги. Точное распределение веса лекарственного вещества в отдельных капсулах или таблетках является критическим фактором, в особенности если требуется низкая дозировка лекарства. Для достижения корректного распределения веса необходимо снизить размер частиц лекарственного вещества до подходящего значения, например, размалыванием. Действительно, частицы малого размера лучше распределяются при одном и том же количестве в массе каждой таблетки или капсулы. Поскольку при размалывании может происходить до некоторой степени разложение соединений А и Б из-за достаточно жестких условий, требуемых для процесса, высокая стабильность при размалывании является существенным преимуществом, так как позволяет изготовлять капсулы и таблетки, содержащие необходимое количество лекарственного вещества, избегая наличия продуктов разложения. Кроме того, во время размалывания продукта энергичное воздействие может вызвать образование полиморфных модификаций, аморфизацию, изменения в кристаллической решетке и форме поверхности твердого вещества. Эти модификации играют важную роль в различных последующих технологических процессах и в биофармацевтических характеристиках. Стабильность лекарственного вещества в фармацевтических композициях важна для определения периода действия фармацевтического начала; это период, в течение которого лекарственное средство можно употреблять без всякого риска, либо вызванного наличием избыточного количества потенциально опасных продуктов разложения, либо вызванного неприемлемо низким содержанием активного начала с точки зрения установленного количества. Высокая стабильность лекарственного вещества в указанных выше фарма цевтических препаратах при различных условиях хранения представляет собой поэтому дополнительное преимущество и для пациентов, и для производителя, так как нет необходимости в контроле условий хранения и в частой замене потерявшего активность лекарственного начала. По указанным выше причинам любая модификация твердофазного лекарственного вещества для орального употребления в форме капсул, таблеток или таблеток с покрытием, которая может улучшить его физическую или химическую стабильность, рассматривается как преимущественная по сравнению с менее стабильными формами того же самого лекарственного вещества. Не лимитирующие примеры таких модификаций включают различные кристаллические формы родственного лекарственного вещества, в том числе в виде различных или новых сольватов, и соли различных физиологически приемлемых кислот или оснований, если лекарственное вещество способно к образованию солей. Объектом данного изобретения является поэтому получение новых кристаллических форм соединений А и Б, которые не обладают указанными выше недостатками. Согласно изобретению предлагаются новые кристаллические моногидратные формы соединений А и Б, которые обладают преимуществами в сравнении с известными безводными формами. Действительно, оба заявляемых соединений не абсорбируют влагу ни во время хранения перед процессом производства капсул, таблеток и таблеток с покрытием при различных температурах и состояниях относительной влажности, ни во время самого процесса, кроме того, они более стабильны, чем соответствующие соединения А и Б на всех стадиях указанного выше процесса производства, особенно во время размалывания, и кроме того они более стабильны при хранении в форме капсул, таблеток и таблеток с покрытием при различных температурах и условиях относительной влажности. Более того, новые кристаллические формы обладают антагонистической активностью в отношении 5-НТ рецепторов. Соответственно вышесказанному согласно изобретению предлагаются соединения формулы × HCI H2O (при R = Н указано ниже как соединение 1 и при R= = С2Н5 указано ниже как соединение П), а также способ их получения и содержащая их фармацевтическая композиция. Соединения 1 и П можно получить растворением известных соединений А и Б, в виде свободных оснований, в горячем водном растворителе, предпочтительно в горячем водном спирте при добавлении требуемого количества газообразного хлористого водорода, фильтрованием полученного раствора и охлаждением до комнатной темпе 3 37179 тифицируемых химических и кристаллических структурах. В соединениях 1 и П молекулы воды прочно связаны с кристаллической решеткой и соотношение молекул лекарственного вещества и молекул воды составляет 1. Аналитическую характеристику соединений 1 и П можно осуществлять различными методами, такими как элементарный анализ, дифференциальная сканирующая калориметрия (ДСК), термо-гравиметрический анализ (ТГА), инфракрасная спектроскопия (ИКС), метод рентгеновской порошковой дифракции, рентгеновская дифракция простого кристалла. Дифференциальная сканирующая калориметрия (ДСК) Дифференциальная сканирующая калориметрия (ДСК) осуществляется с использованием системы Меттлера ТА 3000, снабженной процессором ТС 10А и 20 ячеек ДСК. Навеску соединения (3,5 мг) взвешивают в стандартном тигле из окиси алюминия. Его запечатывают гофрированной крышкой, в которой были три малых отверстия. Соединение 1 Образец нагревают в токе азота 40 мл/мин от 30oС до конечной температуры 320oС со скоростью 10oС/мин. Соединение 2а показало эндотермический пик, относящийся к десорбции кристаллизационной воды при 110°-160°С, со следующим эндотермическим пиком, относящимся к перестройке кристаллической решетки. В заключение соединение плавится при 295°С. Cоединение П Нагревание кристаллов соединения П в токе азота 40 мл/мин, начиная от 30oС до конечной температуры 270°С со скоростью 10oС/мин, приводит к десорбции кристаллизационной воды в области температур 70-160oС (отсутствие в термограмме соответствует безводной форме) с наиболее высоким пиком при 150oС, причем десорбция наблюдается по наличию эндотермического пика (см.рис.1). В заключение соединение плавится при 245oС. Термо-гравиметрический анализ (ТГА). Термо-гравиметрический анализ (ТГА) осуществляют с использованием системы Меттлера ТА 3000, снабженного процессором ТС 10А, печью ТГ50 и весами МЗ. Навеску исследуемого веществами 10 мг взвешивают в стандартном тигле из окиси алюминия. Соединение 1 Нагревание осуществляют в токе азота 200 мл/мин, начиная от 25oС до конечной температуры 295oС, со скоростью 10oС/мин. Соединение 1 показало потерю веса в соответствии с пиком, относящимся к десорбции кристаллизационной воды, составляющую 5,2%, что очень близко теоретическому значению 5,07%, соответствующему моногидрату. Соединение П Нагревание осуществляют в токе азота 200 мл/мин, начиная от 25oС до конечной температуры 255oС со скоростью 10oС/мин. Соединение П показало потерю веса в соответствии с пиком, относящимся к десорбциии кристализационной воды, составляющую 4,62%, что очень близко теоретическомy значению 4,70%, соответствующему моногидрату. ратуры. По предпочтительному варианту способа согласно изобретению соединение 1 получают при использовании, в качестве горячего водного спирта, горячего 85%-ного водного этанола. Кристаллы соединения 1 можно собирать путем вакуумной фильтрации и промывать небольшим количеством водного этанола. По предпочтительному варианту способа согласно данному изобретению соединение П получают при использовании, в качестве горячего водного спирта, горячего 95%-ного водного изопропанола. Кристаллы соединения П можно собирать путем вакуумной фильтрации и промывать небольшим количеством водного изопропанола. Полученные таким образом кристаллы соединений 1 и П могут быть осушены при температуре от комнатной до 60oС под вакуумом, наиболее предпочтительно при 40oС под вакуумом 0,1 мм рт.ст. в течение 24 часов без заметной потери содержания воды. Содержание воды можно измерить обычными методами, например анализом по Карлу Фишеру. Альтернативно, соединения 1 и П можно получать удобным образом путем растворения безводной формы соединений А и Б, в виде гидрохлорида, в горячем водном этаноле, предпочтительно в 85%-ном этаноле (соответственно, в горячем водном изопропаноле, предпочтительно в 95%-ном изопропаноле) и выдерживанием раствора до охлаждения до комнатной температуры; кристаллы соединения 1 (соответственно П), выделенные из охлажденного раствора, собирают вакуумной фильтрацией и обрабатывают как описано выше. По другому варианту соединения 1 и П можно также получать растворением соответствующих соединений А и Б, в виде свободных оснований, в безводном горячем спиртовом растворителе, предпочтительно безводном этаноле (соответственно безводном изопропаноле) и добавлением к профильтрованному раствору 37%-ной водной хлористоводородной кислоты. Кристаллы соединения 1 (или П) выделяют из охлажденного раствора, собирают путем вакуумной фильтрации и обрабатывают как описано вышe. По другому варианту соединения согласно изобретению можно получать путем выдержки соединений А и Б в увлажненной атмосфере, например, в воздухе или азоте при температуре от комнатной до 40oС, предпочтительно при комнатной температуре. Абсорбция воды может требовать различное время в соответствии, главным образом, с размером кристаллов исходных соединений и с величиной относительной влажности. Процесс завершен, когда не фиксируется дальнейшее повышение веса. Содержание воды можно постоянно регистрировать по методу Карла Фишера и для соединения 1 обычно составляет 5,07% ±0,5; для соединения П составляет 4,70 ± ±0,5, это содержание характеризует моногидрат. Соединения А и Б, используемые в форме свободного основания в качестве исходного вещества для получения соединений 1 и П, можно полyчать по методике, описанной в примерах 16, соотв. 14 Европейской патентной заявки 309423. Соединения 1 и П представляют собой новые кристаллические моногидратные формы соединений А и Б. Они имеют различные физико-химические свойства и существуют в хорошо иден 4 37179 Инфракрасная спeктроскопия Инфракрасные спектры соединений А, Б, 1 и П регистрируют на инфракрасном спектрофотометре Перкин-Элемер Mod 298. Соединения берут в твердой фазе и анализируют в виде пасты в нуйоле (расплавленном парафине). В инфракрасном спектре соединения 1 наблюдается сильная полоса при 3400 см-1, относящаяся к растяжению гидроксила воды. Эта полоса отсутствует в соответствующем спектре соединения А. Другие различия в высоте пиков и их относительной интенсивности наблюдаются при 2600, 1430-1390, 1350, 1240, 1170, 1110, 1050, 1000-900 и 850-750 см-1. Они показывают, что соединения А и 1 представляют собой различные кристаллические формы одного и того же соединения (см.рис.2). В инфракрасном спектре соединения П наблюдается сильная полоса при 3500 см-1, относящаяся к растяжению гидроксила воды. Эта полоса почти не проявляется в соответствующем спектре соединения В. Другие различия в высоте пиков и их относительной интенсивности наблюдаются при 2600-2500, 1680, 1630, 1480, 14001350, 1300-1200, 1160-1100, 1060, 1030, 950-900 и около 750 см-1. Это показывает, что соединения В и П являются различными кристаллическими формами одного и того же соединения (см. рис.3). Рентгеновская порошковая дифракция Анализ осуществляют на дифрактометре Филипса pW 1800/10, снабженном компьютером Дигитал Микровакс 2000, запрограммированным программой Филипс АРД 1700. Параметры регистрируют на дифрактометре, характеризующимся следующими параметрами: - гониометр -область развертки: 2on 5 2n -точность: 0,001° 2n -скорость развертки: 0,02o/секунда -тип развертки: непрерывно время анализа: 40 минут. - щели -щели Соллера -автоматическая дивергенция щелей -приемная щель: 0,3 мм детекторная щель: 0,8 мм - рентгеновские лучи -тип трубки: СU (длинный тонкий фокус) -длины волн (l ): К a1 = 1,54060А Кa2 = = 1,54439А - генератор -высокий вольтаж: 40 кв -ток в трубе: 20 ма стабилизация кв и ма: 0,0005% на % основных отклонений - общиe характеристики -длина облучаемого образца: 10 мм -монохроматор: кристалл графита -пропорциональный детектор -константа времени: 2. Наиболее важные параметры основных пиков, а именно углы дифракции (градусы), величины межплоскостных расстояний (Д), абсолютные (пик/расчет) и относительные (Y/Y макс) интенсивности даны в таблицах 1 и 2 для соединений А и 1 соответственно. Значительные различия между соединениями А и 1 особенно заметны, если сравнить пики, связанные с дифракционными углами 6,13 и 17,6-20 градусов для соединения А и 8, 15, 16, 8, 21, 26,1 и 26,3 градусов для соединения 1, как показано на рис.4. Таблица 1 Соединение А Пик, № Угол (градусы) Дмежпл. (углы) Пик (абсол.) Y/Y макс, (%) 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 18 19 20 21 22 23 6.6425 7.0300 11.3150 13.2800 15.0550 16.5550 16.9550 17.6150 18.3100 18.7525 19.3500 19.6425 19.9525 20.4825 21.5450 21.9850 22.7725 23.1850 23.6150 24.8125 25.3800 25.7275 26.2050 13.2961 12.5641 7.8138 6.6617 5.8801 5.3505 5.2252 5.0309 4.8414 4.7282 4.5835 4.5159 4.4464 4.3326 4.1212 4.0397 3.9018 3.8333 3.7645 3. 5854 3.5065 3.4599 3.3980 2440. 23. 98. 4761. 31. 388. 76. 1037. 376. 1576. 1892. 234. 102. 467. 380. 471. 751. 207. 480. 292. 222. 219. 713. 51.26 0.48 2. 06 100.00 0.66 8.15 1.59 21.78 7.91 33.10 39.74 4.92 2.14 9.80 7.99 9.89 15.77 4.36 10.07 6.14 4.66 4.60 14.97 Продолжение табл. 1 5 37179 Продолжение табл. 1 Пик, № Угол (градусы) Дмежпл. (углы) Пик (абсол.) Y/Y макс, (%) 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 50 51 52 53 54 55 56 26.7125 26.9050 27.4925 27.8325 28.1550 28.7925 29.2775 29.4950 30.1225 31.1900 31.6225 31.9350 32.3500 33.1125 33.5750 34.4900 35.0025 35.7225 36.8525 37.1650 38.0900 39.2350 39.7675 40.5000 41.2575 42.4050 43.1425 44.6975 45.1750 46.5625 47.6750 48.3575 49.4600 3.3346 3.3111 3.2417 3.2029 3.1669 3.0982 3.0480 3.0260 2.9644 2.8653 2.8271 2.8002 2.7652 2.7032 2.6670 2.5983 2.5615 2.5115 2.4370 2.4172 2.3606 2.2943 2.2648 2.2255 2.1864 2.1299 2.0952 2.0258 2.0055 1.9489 1.9060 1.8807 1.8413 790. 369. 188. 250. 353. 144. 299. 306. 121. 102. 266. 346. 219. 317. 590. 353. 506. 303. 204. 310. 228. 144. 159. 172. 166. 121. 151. 237. 121. 117. 202. 259. 177. 16.58 7.74 3.94 5.24 7.42 3.02 6.29 6.43 2.54 2.14 5.58 7.27 4.60 6.65 12.40 7.42 10.63 6.36 4.30 6.51 4.79 3.02 3.33 3.60 3.50 2.54 3.18 4.98 2.54 2.45 4.24 5.44 3.73 Таблица 2 Соединение 1 Пик, № Угол (градусы) D межпл. (углы) Пик (абс.) I/I max, (%) 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15 16 17 7.6775 8.2700 10.2450 11.1675 13.0450 13.9225 14.1635. 14.9850 15.9525 16.0700 16.8750 19.1650 19.2575 19.9475 20.8125 22.0550 22.2300 11.5058 10.6828 8.6274 7.9167 6.7812 6.3557 6.2485 5.9074 5.5512 5.5109 5.2498 4.6273 4.6053 4.4475 4.2646 4.0271 3.9958 40. 1505. 36. 76. 751. 106. 164. 1018. 190. 231. 2107. 392. 388. 310. 1998. 306. 335. 1.88 71.46 1.71 3.59 35.63 5.04 7.78 48.30 9.04 10.97 100.00 18.61 18.42 14.70 94.84 14.54 15.90 6 37179 Продолжение табл. 2 Пик, № Угол (градусы) D межпл. (углы) Пик (абс.) I/I max, (%) 18 19 20 21 22 23 24 25 26 27 28 29 30 31 32 33 34 35 36 37 38 39 40 41 42 43 44 45 46 47 48 49 22.5475 23.0250 23.7750 24.3300 25.7500 26.1500 26.3450 27.2225 27.4725 29.5325 29.9775 30.1725 30.5650 31.4925 32.3725 32.5925 32.9925 33.5200 33.9450 34.8125 36.3250 36.7950 37.1375 38.5925 39.0700 40.1000 40.6450 42.5125 43.2675 45.2500 46.3950 47.1150 3.9402 3.8596 3.7395 3.6554 3.4570 3.4050 3.3802 3.2732 3.2440 3.0223 2.9784 2.9596 2.9225 2.8385 2.7633 2.7452 2.7128 2.6713 2.6388 2.5750 2.4712 2.4407 2.4190 2.3310 2.3036 2.2468 2.2179 2.1247 2.0894 2.0023 1.9556 1.9273 454. 35. 67. 400. 207. 1505. 2098. 655. 1089. 74. 234. 324. 190. 650. 380. 462. 128. 146. 412. 784. 182. 210. 306. 900. 161. 193. 458. 121. 90. 177. 114. 324. 21.53 1.65 3.19 18.99 9.84 71.46 99.56 31.11 51.69 3.51 11.11 15.38 9.04 30.86 18.05 21.94 6.06 6.95 19.56 37.21 8.65 9.98 14.54 42.72 7.66 9.17 21.74 5.74 4.28 8.40 5.43 15.38 50 51 52 47.9125 48.9800 49.9000 1.8971 1.8582 1.8261 146. 299. 210. 6.95 14.21 9.98 I>3(I). Структуру определяли прямым методом (Мултан 80, Ксанаду). Рисунки выполнял Opmen II. Анализируемое соединение (формула С16H20N4O2 x x HCl×Н2O, мол.вес 354,84) обладает моноклинической решеткой Р21/С, а = 11,668 А, в = 11,714 А, с = 13,672 А, a= 90°, b= 114,83°, g= 90°. Молекула воды в кристаллической решетке соединения 1 находится в хорошо определяемом месте кристаллической решетки и связана водородной связью с незамещенным атомом азота в кольце бензимидазолона. Кроме того, та же молекула воды связана с двумя хлорид-ионами, относящимися к двум другим молекулам лекарственного вещества. Различие в кристаллических формах соединений Б и П также подтверждено результатами анализа методом рентгенoвской порошковой дифракции. Рентгеновская дифракция простого кристалла Анализ проводят на призматическом кристалле соединения 1 размером 0,41 х 0,23 х 0,08 мм. При этом использовали четырехцикловый дифрактометр Филипса Pw 1100, снабженный графитовым монохроматором. Для измерения параметров решетки использовали 48 рефлексий (2
ДивитисяДодаткова інформація
Назва патенту англійськоюCrystalline monohydrates of hydrochloride of endo -2,3-dihydro-n-(8-methyl-8-azabicyclo [3.2.1 ]oct-3-yl) -2-oxo-1h-benzimidazole-1-carboxamide and endo-3-ethyl-2,3-dihydro-n-(8-methyl-8- azabicyclo [3.2.1]oct-3-yl)-2-oxo-1h- benzimidazole-1-carboxamide, method for the preparation thereof and pharmaceutical composition
Автори англійськоюEnzo Cereda, Enrica Dubini, Antoine Ezhaya, Grazia Maffione, Marco Turconi
Назва патенту російськоюКристаллические моногидраты гидрохлорида эндо-2,3-дигидро-n-(8-метил-8-азабицикло [ 3.2.1 ] окт-3-ил) -2-оксо-1н-бензимидазол-1-карбоксамида и эндо-3-этил-2,3-дигидро-n-(8-метил-8-азабицикло[3.2.1]окт-3-ил)-2-оксо-1н-бензимидазол-1-карбоксамида, способ их получения и фармацевтическая композиция
Автори російськоюЭнцо Череда, Энрика Дубини, Антуан Эцхая, Грация Маффионе, Марко Туркони
МПК / Мітки
МПК: A61P 1/08, A61P 25/04, A61P 25/18, A61P 25/06, C07D 451/04, A61K 31/46, A61P 1/00, A61P 25/28
Мітки: ендо-2,3-дигідро-n-(8-метил-8-азабіцикло, кристалічні, моногідрати, 2-оксо-1н-бензимідазол-1-карбоксаміду, ендо-3-етил-2,3-дигідро-n-(8-метил-8-азабіцикло[3.2.1]окт-3-іл)-2-оксо, гідрохлориду, 3.2.1, окт-3-іл
Код посилання
<a href="https://ua.patents.su/16-37179-kristalichni-monogidrati-gidrokhloridu-endo-23-digidro-n-8-metil-8-azabiciklo-321-okt-3-il-2-okso-1n-benzimidazol-1-karboksamidu-ta-endo-3-etil-23-digidro-n-8-metil-8-azabiciklo321.html" target="_blank" rel="follow" title="База патентів України">Кристалічні моногідрати гідрохлориду ендо-2,3-дигідро-n-(8-метил-8-азабіцикло [ 3.2.1 ] окт-3-іл) -2-оксо-1н-бензимідазол-1-карбоксаміду та ендо-3-етил-2,3-дигідро-n-(8-метил-8-азабіцикло[3.2.1]окт-3-іл)-2-оксо</a>
Попередній патент: Терапевтичні гетероциклічні сполуки, спосіб їх одержання, спосіб профілактики та лікування, лікарський засіб та спосіб його одержання
Наступний патент: Багатошаровий папір
Випадковий патент: Оптоелектронна шкала