Спосіб одержання необов’язково 2-заміщених 1,6-дигідро-6-оксо-4-піримідинкарбонових кислот
Формула / Реферат
1. Спосіб одержання сполуки Формули 1
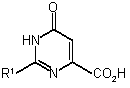 , 1
, 1
де R1 являє собою Н або необов'язково заміщений вуглецевий компонент;
який відрізняється тим, що здійснюють наступні стадії:
(1) реакцію суміші, що містить
(а) сполуку Формули 2а
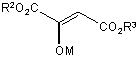 , 2a
, 2a
де М являє собою лужний метал, та R2 і R3 незалежно являють собою С1-С4алкіл,
(b) С1-С4алканол, та
(с) першу частину води, з розчином, що містить першу основу та другу частину води, зазначена основа знаходиться в кількості, достатній для одержання першого отриманого розчину, що має рН в діапазоні від приблизно 10 до приблизно 14, зазначений перший отриманий розчин містить сполуку Формули 2b
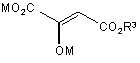 , 2b
, 2b
де М та R3 є такими, як визначено вище для Формули 2а;
(2) реакцію першого отриманого розчину, що містить сполуку Формули 2b, зі сполукою Формули 3 або її кислотною сіллю чи з розчином, що містить сполуку Формули 3 або її кислотну сіль
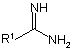 , 3
, 3
де R1 є таким, як визначено вище для Формули 1,
та другу основу в кількості, достатній для одержання другого отриманого розчину, що має рН в діапазоні від приблизно 9 до приблизно 12, зазначений другий отриманий розчин містить сіль сполуки Формули 1; та
(3) додавання кислоти до другого отриманого розчину, що містить сіль сполуки Формули 1, з одержанням сполуки Формули 1.
2. Спосіб за пунктом 1, де R1 являє собою необов'язково заміщений циклопропіл або необов'язково заміщений феніл.
3. Спосіб за пунктом 2, де R1 являє собою необов'язково заміщений циклопропіл.
4. Спосіб за пунктом 3, де R1 являє собою циклопропіл.
5. Спосіб за пунктом 1, де першою основою, яку додають на стадії (1), є гідроксид лужного металу.
6. Спосіб за пунктом 5, де гідроксидом лужного металу є гідроксид натрію або гідроксид калію.
7. Спосіб за пунктом 1, де рН першого отриманого розчину на стадії (1) підтримують в діапазоні від приблизно 11 до приблизно 13.
8. Спосіб за пунктом 1, де мольне співвідношення сполуки Формули 3 або її кислотної солі до сполуки Формули 2а підтримують в діапазоні від 0,7 до приблизно 0,9.
9. Спосіб за пунктом 1, де другою основою, яку додають на стадії (2) є гідроксид лужного металу.
10. Спосіб за пунктом 9, де як гідроксид лужного металу використовують гідроксид натрію або гідроксид калію.
11. Спосіб за пунктом 1, де рН другого отриманого розчину та стадії (2) підтримують в діапазоні від приблизно 10,5 до приблизно 11,5.
12. Спосіб за пунктом 1, де кислотою, яку додають на стадії (3), є мінеральна кислота.
13. Спосіб за пунктом 12, де кислотою є сірчана кислота або соляна кислота.
14. Спосіб одержання сполуки Формули 4
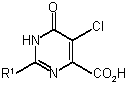 , 4
, 4
де R1 являє собою Н або необов'язково заміщений вуглецевий компонент,
який включає спосіб за пунктом 1 та додаткову стадію, в якій здійснюють реакцію сполуки Формули 1 з хлоруючим агентом.
15. Спосіб одержання сполуки Формули 6
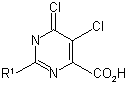 , 6
, 6
де R1 являє собою Н або необов'язково заміщений вуглецевий компонент,
який включає спосіб за пунктом 14 та додаткову стадію, в якій здійснюють реакцію сполуки Формули 4 з хлорзаміщуючим агентом.
16. Спосіб одержання сполуки Формули 7
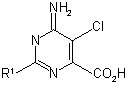 , 7
, 7
де R1 являє собою Н або необов'язково заміщений вуглецевим компонент,
який включає спосіб за пунктом 15 та додаткову стадію, в якій здійснюють реакцію сполуки Формули 6 з аміаком.
17. Спосіб одержання сполуки Формули 8
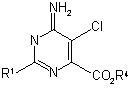 , 8
, 8
де R1 являє собою Н або необов'язково заміщений вуглецевий компонент; та R4 являє собою необов'язково заміщений вуглецевий компонент;
який включає спосіб за пунктом 16 та додаткову стадію, в якій здійснюють реакцію сполуки Формули 7 з R4-заміщуючим агентом.
18. Спосіб за пунктом 17, де R4 являє собою С1-С14алкіл, С2-С14алкоксіалкіл, С2-С14гідроксіалкіл або бензил.
19. Спосіб за пунктом 18, де R4 являє собою С1-C8алкіл або С2-C8алкоксіалкіл.
20. Спосіб за пунктом 19, де R4 являє собою С1-С4алкіл.
21. Спосіб за будь-яким з пунктів 1-20, де R1 являє собою циклопропіл.
Текст
1. Спосіб одержання сполуки Формули 1 1,6-ДИГІДРО-6-ОКСО-4 UA (54) СПОСІБ ОДЕРЖАННЯ ПІРИМІДИНКАРБОНОВИХ КИСЛОТ ОПИС (19) ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ 3 92171 13. Спосіб за пунктом 12, де кислотою є сірчана кислота або соляна кислота. 14. Спосіб одержання сполуки Формули 4 O Cl HN 4 де R1 являє собою Н або необов'язково заміщений вуглецевим компонент, який включає спосіб за пунктом 15 та додаткову стадію, в якій здійснюють реакцію сполуки Формули 6 з аміаком. 17. Спосіб одержання сполуки Формули 8 NH2 R1 N CO2H ,4 де R являє собою Н або необов'язково заміщений вуглецевий компонент, який включає спосіб за пунктом 1 та додаткову стадію, в якій здійснюють реакцію сполуки Формули 1 з хлоруючим агентом. 15. Спосіб одержання сполуки Формули 6 Cl N 1 Cl Cl N R1 N CO H 2 ,6 де R являє собою Н або необов'язково заміщений вуглецевий компонент, який включає спосіб за пунктом 14 та додаткову стадію, в якій здійснюють реакцію сполуки Формули 4 з хлорзаміщуючим агентом. 16. Спосіб одержання сполуки Формули 7 1 NH2 R1 N CO2R4 ,8 де R1 являє собою Н або необов'язково заміщений вуглецевий компонент; та R4 являє собою необов'язково заміщений вуглецевий компонент; який включає спосіб за пунктом 16 та додаткову стадію, в якій здійснюють реакцію сполуки Формули 7 з R4-заміщуючим агентом. 18. Спосіб за пунктом 17, де R4 являє собою С1С14алкіл, С2-С14алкоксіалкіл, С2-С14гідроксіалкіл або бензил. 19. Спосіб за пунктом 18, де R4 являє собою С1C8алкіл або С2-C8алкоксіалкіл. 20. Спосіб за пунктом 19, де R4 являє собою С1С4алкіл. 21. Спосіб за будь-яким з пунктів 1-20, де R1 являє собою циклопропіл. Cl N R1 N CO2H ,7 Розкрито новий спосіб одержання необов'язково 2-заміщених 1,6-дигідро-6-оксо-4піримідинкарбонових кислот. G. D. Daves, Jr. та інші. (J. Org. Chem., 1961, 26, 2755) описує одержання 1,6-дигідро-6-оксо-4піримідинкарбонової кислоти за допомогою циклоконденсації діетил оксалацетату з формамідином у водному NaOH. В цій методиці всі компоненти одночасно об'єднували без детального контролю рН з одержанням виходу 63%. В інших звітах відносно подібних конденсацій, використовуючи оксалацетатні діефіри, розкрито навіть нижчі виходи. Таким чином, існує потреба в нових способах для забезпечення вищих виходів, а також для надання низької вартості, високої ефективності та надійності. Даний винахід забезпечує спосіб одержання 1,6-дигідро-6-оксо-4-піримідинкарбонової кислоти Формули 1 1 де R1 являє собою Η або необов'язково заміщений вуглецевий компонент; який включає наступні стадії: (1) реакцію суміші, що містить (а) сполуку Формули 2а 2a де Μ являє собою лужний метал, та R2 і R3 незалежно являють собою С1-С4алкіл, (b) C1C4алканол, та (с) першу частину води, з розчином, що містить першу основу та другу частину води, зазначена основа знаходиться в кількості, достатній для одержання першого отриманого розчину, що має рН в діапазоні від приблизно 10 до приблизно 14, зазначений перший отриманий розчин містить сполуку Формули 2b 2b де Μ та R3 є такими, як визначено вище для Формули 2а; (2) реакцію першого отриманого розчину, що містить сполуку Формули 2b, зі сполукою Формули 3 або її кислотною сіллю чи з розчином, що містить сполуку Формули 3 або її кислотну сіль 3 5 92171 де R1 є таким, як визначено вище для Формули 1, та другу основу в кількості, достатній для одержання другого отриманого розчину, що має рН в діапазоні від приблизно 9 до приблизно 12, зазначений другий отриманий розчин містить сіль сполуки Формули 1; та (3) додавання кислоти до другого отриманого розчину, що містить сіль сполуки Формули 1, з одержанням сполуки Формули 1. Винахід також забезпечує спосіб одержання сполуки Формули 4 4 де R1 являє собою Η або необов'язково заміщений вуглецевий компонент, який включає описаний вище спосіб та додаткову стадію реакції сполуки Формули 1 з хлоруючим агентом. Винахід також забезпечує спосіб одержання сполуки Формули 6 6 де R1 являє собою Η або необов'язково заміщений вуглецевий компонент, який включає описаний вище спосіб та додаткову стадію реакції сполуки Формули 4 з хлор-замішуючим агентом. Винахід також забезпечує спосіб одержання сполуки Формули 7 7 де R1 являє собою Η або необов'язково заміщений вуглецевий компонент, який включає описаний вище спосіб та додаткову стадію реакції сполуки Формули 6 з аміаком. Винахід також забезпечує спосіб одержання сполуки Формули 8 8 де R1 являє собою Η або необов'язково заміщений вуглецевий компонент; та R4 являє собою необов'язково заміщений вуглецевий компонент; який включає описаний вище спосіб та додаткову стадію реакції сполуки Формули 7 з R4заміщуючим агентом. Відповідно, винахід також забезпечує спосіб одержання сполуки Формули 4, використовуючи сполуку Формули 1, який відрізняється тим, що сполуку Формули 1 одержують зі сполук Формул 2а та 3 за допомогою описаного вище способу. Винахід також забезпечує спосіб одержання сполуки Формули 6, використовуючи сполуку Формули 1, який відрізняється тим, що сполуку Формули 1 6 одержують зі сполук Формул 2а та 3 за допомогою описаного вище способу. Винахід також забезпечує спосіб одержання сполуки Формули 7, використовуючи сполуку Формули 1, який відрізняється тим, що сполуку Формули 1 одержують зі сполук Формул 2а та 3 за допомогою описаного вище способу. Винахід також забезпечує спосіб одержання сполуки Формули 8, використовуючи сполуку Формули 1, який відрізняється тим, що сполуку Формули 1 одержують зі сполук Формул 2а та 3 за допомогою описаного вище способу. У визначеннях в даній заявці, термін "вуглецевий компонент" відноситься до радикалу, що містить атом вуглецю, що зв'язує радикал із залишком молекули. Оскільки замісник R1 відокремлений від реакційного центру та R4 вводять наприкінці описаної послідовності стадій, R1 та R4 можуть включати велику множину груп на основі вуглецю, одержаних сучасними способами синтетичної органічної хімії. "Вуглецевий компонент", таким чином, включає алкіл, алкеніл та алкініл, які можуть бути прямо-ланцюговими або розгалуженими. "Вуглецевий компонент" також включає карбоциклічні та гетероциклічні кільця, які можуть бути насиченими, частково насиченими або повністю ненасиченими. Крім того, ненасичені кільця можуть бути ароматичними, якщо вони задовольняють правило Хюкеля. Карбоциклічні та гетероциклічні кільця у вуглецевому компоненті можуть утворювати поліциклічні кільцеві системи, які містять різні кільця, сполучені разом. Термін "карбоциклічне кільце" означає кільце, в якому атоми, що утворюють основу кільця, вибрані тільки з вуглецю. Термін "гетероциклічне кільце" означає кільце, в якому, принаймні, один з атомів, що утворюють основу кільця, є відмінним від вуглецю. "Насичене карбоциклічне" відноситься до кільця, що має основу, яка складається з атомів вуглецю, зв'язаних один з одним за допомогою простих зв'язків; якщо не визначено інше, валентності вуглеців, що залишилися, заповнюється атомами водню. Термін "ароматична кільцева система" означає повністю ненасичені карбоцикли та гетероцикли, в яких, принаймні, одне кільце в поліциклічній кільцевій системі є ароматичним. "Ароматичний" вказує, що кожний з кільцевих атомів знаходиться по суті в тій самій площині та має р-орбіталь, перпендикулярну до площини кільця, та в якому (4n+2) електрони, коли n складає 0 або позитивне ціле число, зв'язані з кільцем, щоб дотримуватися правила Хюкеля. Термін "ароматична карбоциклічна кільцева система" включає повністю ароматичні карбоцикли та карбоцикли, в яких, принаймні, одне кільце поліциклічної кільцевої системи є ароматичним. Термін "неароматична карбоциклічна кільцева система" означає повністю насичені карбоцикли, а також частково або повністю ненасичені карбоцикли, в яких жодне з кілець в кільцевій системі не є ароматичним. Терміни "ароматична гетероциклічна кільцева система" та "гетероароматичне кільце" включають повністю ароматичні гетероцикли та гетероцикли, в яких, принаймні, одне кільце поліциклічної кільцевої системи є ароматичним. Термін "неароматична гетероциклічна кільцева система" означає повністю насичені гетероцикли, а 7 також частково або повністю ненасичені гетероцикли, в яких жодне з кілець в кільцевій системі не є ароматичним. Термін "арил" означає карбоциклічне або гетероциклічне кільце чи кільцеву систему, в якій, принаймні, одне кільце, є ароматичним, та ароматичне кільце забезпечує приєднання до залишку молекули. Вуглецеві компоненти, вказані для R1 та R4, є необов'язково заміщеними. Термін "необов'язково заміщений" у зв'язку з цими вуглецевими компонентами відноситься до вуглецевих компонентів, які є незаміщеними, або мають, принаймні, один неводневий замісник. Так само, термін "необов'язково заміщений" у зв'язку з арилом та третинним алкілом відноситься до радикалів арилу та третинного алкілу, які є незаміщеними, або мають, принаймні, один неводневий замісник. Приклади необов'язкових замісників включають алкіл, алкеніл, циклоалкіл, циклоалкеніл, арил, гідроксикарбоніл, форміл, алкілкарбоніл, алкенілкарбоніл, алкінілкарбоніл, алкоксикарбоніл, гідрокси, алкокси, алкенілокси, алкінілокси, циклоалкокси, арилокси, алкілтіо, алкенілтіо, алкінілтіо, циклоалкілтіо, арилтіо, алкілсульфініл, алкенілсульфініл, алкінілсульфініл, циклоалкілсульфініл, арилсульфініл, алкілсульфоніл, алкенілсульфоніл, алкінілсульфоніл, циклоалкілсульфоніл, арилсульфоніл, аміно, алкіламіно, алкеніламіно, алкініламіно, ариламіно, амінокарбоніл, алкіламінокарбоніл, алкеніламінокарбоніл, алкініламінокарбоніл, ариламінокарбоніл, алкіламінокарбоніл, алкеніламінокарбоніл, алкініламінокарбоніл, ариламінокарбонілокси, алкоксикарбоніламіно, алкенілоксикарбоніламіно, алкінілоксикарбоніламіно та арилоксикарбоніламіно, кожний додатково необов'язково заміщений; та галоген, ціано та нітро. Необов'язкові додаткові замісники незалежно вибрані з груп, які подібні групам, проілюстрованим вище для замісників, надаючи додаткові замішуючі радикали для R1 та R4, такі як галоалкіл, галоалкеніл та галоалкокси. Як додатковий приклад, алкіламіно може бути, крім того, заміщений алкілом, надаючи діалкіламіно. Замісники також можуть бути сполучені разом фігурально шляхом видалення одного або двох атомів водню з кожного з двох замісників, або із замісника та основної молекулярної структури і приєднання радикалів з утворенням циклічних та поліциклічних структур, конденсованих або приєднаних до молекулярної структури, що містить замісники. Наприклад, сполучення разом сусідніх гідрокси та метокси груп, приєднаних, наприклад, до фенільного кільця, надає конденсовану діоксоланову структуру, що містить зв'язуючу групу -О-СН2О-. Сполучення разом гідрокси групи та молекулярної структури, до якої вона приєднана, може надати циклічні ефіри, включаючи епоксиди. Приклади замісників також включають кисень, який, коли він приєднаний до вуглецю, утворює карбонільну функцію. Так само, сірка, коли вона приєднана до вуглецю, утворює тіокарбонільну функцію. Як використовується в даній заявці, "алкіл", що використовується сам по собі або в складових словах, таких як "алкілтіо" або "галоалкіл", включає алкіл з прямим або розгалуженим ланцюгом, такий як метил етил, н-пропіл, і-пропіл або різні 92171 8 ізомери бутилу, пентилу або гексилу. "Алкеніл" включає алкени з прямим або розгалуженим ланцюгом, такі як етеніл, 1-пропеніл, 2-пропеніл та різні ізомери бутенілу, пентенілу та гексенілу. "Алкеніл" також включає полієни, такі як 1,2пропадієніл та 2,4-гексадієніл. "Алкініл" включає алкіни з прямим або розгалуженим ланцюгом, такі як етиніл, 1-пропініл, 2-пропініл та різні ізомери бутинілу, пентинілу та гексинілу. "Алкініл" також може включати компоненти, що містять різні потрійні зв'язки, такі як 2,5-гексадіїніл. "Алкокси" включає, наприклад, метокси, етокси, нпропілокси, ізопропілокси та різні ізомери бутокси, пентокси та гексилокси. "Алкоксіалкіл" включає, наприклад, СН3ОСН2, СН3ОСН2СН2, СН3СН2ОСН2, СН3СН2ОСН2СН2. Тідроксіалкіл" включає, наприклад, НОСН2СН2СН2, СН3СН(ОН)СН2СН2, СН3СН(ОН)СН2. "Алкенілокси" включає алкенілокси компоненти з прямим або розгалуженим ланцюгом. Приклади "алкенілокси" включають Н2С=СНСН2О, (СН3)2С=СНСН2О, (СН3)СН=СНСН2О, (СН3)СН=С(СН3)СН2О та СН2=СНСН2СН2О. "Алкінілокси" включає алкінілокси компоненти з прямим або розгалуженим ланцюгом. Приклади "алкінілокси" включають НC ССН2O, СН3C CСН2O та СН3С ССН2СН2О. "Алкілтіо" включає алкілтіо компоненти з прямим або розгалуженим ланцюгом, такі як метилтіо, етилтіо та різні ізомери пропілтіо, бутилтіо, пентилтіо та гексилтіо. "Алкілсульфініл" включає обидва енантіомери алкілсульфінільної групи. Приклади "алкілсульфінілу" включають CH3S(O), CH3CH2S(O), CH3CH2CH2S(O), (CH3)2CHS(O) та різні ізомери бутилсульфінілу, пентилсульфінілу та гексилсульфінілу. Приклади "алкілсульфонілу" включають CH3S(O)2, CH3CH2S(O)2, CH3CH2CH2S(O)2, (CH3)2CHS(O)2 та різні ізомери бутилсульфонілу, пентилсульфонілу та гексилсульфонілу. "Алкіламіно", "алкенілтіо", "алкенілсульфініл", "алкенілсульфоніл", "алкінілтіо", "алкінілсульфініл", "алкінілсульфоніл" та подібні визначені аналогічно до наведених вище прикладів. Приклади "алкілкарбонілу" включають С(О)СН3, С(О)СН2СН2СН3 та С(О)СН(СН3)2. Приклади "алкоксикарбонілу" включають СН3ОС(=О), СН3СН2ОС(=О), СН3СН2СН2ОС(=О), (СН3)2СНОС(=О) та різні ізомери бутокси- або пентоксикарбонілу. "Циклоалкіл" включає, наприклад, циклопропіл, циклобутил, циклопентил та циклогексил. Термін "циклоалкокси" включає ті ж самі групи, зв'язані через атом кисню, такі як циклопентилокси та циклогексилокси. "Циклоалкіламіно" означає, що атом азоту в аміно приєднаний до циклоалкільного радикалу і атому водню, та включає групи, такі як циклопропіламіно, циклобутиламіно, циклопентиламіно та циклогексиламіно. "(Алкіл)(циклоалкіл)аміно" означає циклоалкіламіно групу, де атом водню в аміно замінений на алкільний радикал; приклади включають групи, такі як (метил)(циклопропіл)аміно, (бутил)(циклобутил)аміно, (пропіл)циклопентиламіно, (метил)циклогексиламіно та подібні. "Циклоалкеніл" включає групи, такі як циклопентеніл та циклогексеніл, а також групи, що містять більше, ніж 9 один подвійний зв'язок, такі як 1,3- та 1,4циклогексадієніл. Термін "галоген", сам по собі або в складових словах, таких як "галоалкіл", включає фтор, хлор, бром або йод. Термін " 1-2 галогени" вказує, що одне або двоє з доступних положень для цього замісника можуть бути галогеном, який вибраний незалежно. Надалі, коли він використовується в складових словах, таких як "галоалкіл", зазначений алкіл може бути частково або повністю заміщений атомами галогену, які можуть бути однаковими або різними. Приклади "галоалкілу" включають F3C, ClCH2, CF3CH2 та CF3CCl2. Загальна кількість атомів вуглецю в заміщуючій групі вказана префіксом "Ci-Cj", де і тa j, наприклад, означають числа від 1 до 3; наприклад, C1С3алкіл означає метил, етил, пропіл. Хоча немає певного обмеження щодо розміру R1 та R4, необов'язково заміщені алкільні компоненти R1 звичайно включають 1-6 атомів вуглецю, більш звичайно 1-4 атоми вуглецю та найбільш звичайно 1-3 атоми вуглецю в алкільному ланцюгу. Необов'язково заміщені алкільні компоненти R4 звичайно включають 1-14 атомів вуглецю, більш звичайно 1-8 атомів вуглецю та найбільш звичайно 1-4 атоми вуглецю в алкільному ланцюгу. Необов'язково заміщені алкенільні та алкінільні компоненти R1 звичайно включають 2-6 атомів вуглецю, більш звичайно 2-4 атомів вуглецю та найбільш звичайно 2-3 атоми вуглецю в алкенільному або алкінільному ланцюгу. Необов'язково 4 заміщені алкенільні та алкінільні компоненти R звичайно включають 2-14 атомів вуглецю, більш звичайно 3-8 атомів вуглецю та найбільш звичайно 3-4 атоми вуглецю в алкенільному або алкінільному ланцюгу. Як вказано вище, вуглецеві компоненти R1 та R4 можуть бути ароматичним кільцем або кільцевою системою. Приклади ароматичних кілець або кільцевих систем включають фенільне кільце, 5або 6-членні гетероароматичні кільця, 3-8-членні насичені або ненасичені карбоциклічні кільцеві системи, ароматичні 8-, 9- або 10-членні конденсовані карбобіциклічні кільцеві системи та ароматичні 8-, 9- або 10-членні конденсовані гетеробіциклічні кільцеві системи, в яких кожне кільце або кільцева система необов'язково заміщені. Термін "необов'язково заміщений" у зв'язку з цими вуглецевими компонентами R1 та R4 відноситься до вуглецевих компонентів, які є незаміщеними або мають, принаймні, один неводневий замісник. Ці вуглецеві компоненти можуть бути заміщені стількома необов'язковими замісниками, скільки їх може бути приєднано шляхом заміни атома водню на неводневий замісник на будь-якому доступному атомі вуглеці або азоту. Звичайно, кількість необов'язкових замісників (коли вони присутні) знаходиться в діапазоні від одного до чотирьох. Як використовується в даній заявці, мається на увазі, що терміни "містить", "що містить", "включає", "включаючи", "має", "маючи" або будь-яка їх інша варіація відносяться до невиняткового включення. Наприклад, композиція, процес, спосіб, продукт або апарат, який включає перелік елементів, не обмежується обов'язково лише цими еле 92171 10 ментами, а він може включати інші елементи, не зазначені чітко в переліку або властиві такій композиції, процесу, способу, продукту або апарату. Надалі, якщо тільки не зазначено інше, "або" відноситься до включаючого "або" та до не виключаючого "або". Наприклад, умова А або В задовольняє будь-якому з наступного: А вірне (або присутнє) та В невірне (або відсутнє), А невірне (або відсутнє) та В вірне (або присутнє), та як А, так і В вірні (або присутні). Також, мається на увазі, що невизначені артиклі "а" та "an", що передують елементу або компоненту винаходу, необмежені щодо кількості прикладів (тобто випадків) елемента або компонента. Таким чином, потрібно читати, що "а" або "an" включають один або, принаймні, один, та однина елемента або компонента також включає множину, за винятком, коли число явно означає однину. Об'єднання хімічних речовин та додавання хімічних речовин відноситься до контактування хімічних речовин одна з одною. Цифрові діапазони є такими, що включають кожне та будь-яке ціле значення в межах діапазону. Фахівець в даній галузі техніки також визнає, що сполуки Формул 1 та 4 знаходяться в рівновазі з їх відповідними таутомерними аналогами Формул 1а та 4а, як показано в Ілюстрації 1. Якщо не заявлено інше, мається на увазі, що посилання на Формули 1 та 4 в даному описі та формулі винаходу включають всі таутомери, включаючи Формули 1а та 4а, відповідно. Атом азоту в сполуках Формул 1, 3, 4, 6, 7 та 8 (включаючи 1а та 4а) може бути протонований, дозволяючи зазначеним сполукам утворювати кислотно-адитивні солі з неорганічними або органічними кислотами, включаючи, але не обмежуючись, бромистоводневу кислоту, соляну кислоту, азотну кислоту, фосфорну кислоту, сірчану кислоту або 4-толуолсульфонову кислоту. Втілення даного винаходу включають: Втілення А1. Спосіб, який описано в Короткому 1 описі суті винаходу, де R являє собою необов'язково заміщений вуглецевий компонент. Втілення А2. Спосіб за Втіленням А1, де R1 являє собою необов'язково заміщений циклопропіл або необов'язково заміщений феніл. 11 Втілення A3. Спосіб за Втіленням А2, де R1 являє собою необов'язково заміщений циклопропіл. Втілення А4. Спосіб за Втіленням А2, де R1 являє собою необов'язково заміщений феніл. Втілення А5. Спосіб за Втіленням A3, де R1 являє собою незаміщений циклопропіл. Втілення А6. Спосіб за Втіленням А4, де R1 являє собою феніл, заміщений в пара-положенні та необов'язково заміщений в інших положеннях. Втілення А7. Спосіб за Втіленням А6, де R1 являє собою феніл, заміщений Вr або СІ в параположенні та необов'язково заміщений 1-2 галогенами в інших положеннях. Втілення А8. Спосіб за Втіленням А7, де R1 являє собою феніл, заміщений Вr або СІ в параположенні. Втілення А9. Спосіб, який описано в Короткому описі суті винаходу, де R4 являє собою С1С14алкіл. С2-С14алкоксіалкіл, С2-С14гідроксіалкіл або бензил. Втілення А10. Спосіб за Втіленням А9. де R4 являє собою С1-С14алкіл, С2-С14алкоксіалкіл або С2-С14гідроксі алкіл. Втілення A11. Спосіб за Втіленням А10, де R4 являє собою С1-С8алкіл, С2-С8алкоксіалкіл або С2С8гідроксіалкіл. Втілення А12. Спосіб за Втіленням A11, де R4 являє собою С1-С8алкіл або С2-C8алкоксіалкіл. Втілення А13. Спосіб за Втіленням А12, де R4 являє собою С1-С4алкіл. Втілення В1. Спосіб, який описано в Короткому описі суті винаходу, де алканол являє собою метанол або етанол. Втілення В2. Спосіб за Втіленням В1, де алканол являє собою етанол. Втілення В3. Спосіб, який описано в Короткому описі суті винаходу, де об'ємне співвідношення першої частини води до сполуки Формули 2а знаходиться в діапазоні від приблизно 10 до приблизно 0,01. Втілення В4. Спосіб за Втіленням В3, де об'ємне співвідношення першої частини води до сполуки Формули 2а знаходиться в діапазоні від приблизно 6 приблизно 1. Втілення В5. Спосіб за Втіленням В4, де об'ємне співвідношення першої частини води до сполуки Формули 2а знаходиться в діапазоні від приблизно 3 до приблизно 2. Втілення В6. Спосіб, який описано в Короткому описі суті винаходу, де об'ємне співвідношення першої частини води до алканолу знаходиться в діапазоні від приблизно 0,01 до приблизно 100. Втілення В7. Спосіб за Втіленням В6, де об'ємне співвідношення першої частини води до алканолу знаходиться в діапазоні від приблизно 1 до приблизно 50. Втілення В8. Спосіб за Втіленням В7, де об'ємне співвідношення першої частини води до алканолу знаходиться в діапазоні від приблизно 5 до приблизно 10. Втілення В9. Спосіб, який описано в Короткому описі суті винаходу, де перша основа являє собою гідроксид лужного металу. 92171 12 Втілення В10. Спосіб за Втіленням В9, де гідроксидом лужного металу є гідроксид натрію або гідроксид калію. Втілення В11. Спосіб за Втіленням В10, де гідроксидом лужного металу є гідроксид натрію. Втілення В12. Спосіб за Втіленням В9, демольне співвідношення першої основи до сполуки Формули 2а знаходиться в діапазоні від приблизно 0,5 до приблизно 2. Втілення В13. Спосіб за Втіленням В12, демольне співвідношення першої основи до сполуки Формули 2а знаходиться в діапазоні від приблизно 0,7 до приблизно 1,5. Втілення В14. Спосіб за Втіленням В13, демольне співвідношення першої основи до сполуки Формули 2а знаходиться в діапазоні від приблизно 0,9 до приблизно 1,2. Втілення В15. Спосіб, який описано в Короткому описі суті винаходу, де рН першого отриманого розчину знаходиться в діапазоні від приблизно 11 до приблизно 13. Втілення В16. Спосіб, який описано в Короткому описі суті винаходу, де стадію (1) проводять при температурі в діапазоні від приблизно 5 до приблизно 40°С. Втілення В17. Спосіб за Втіленням В16, де температура знаходиться в діапазоні від приблизно 20 до приблизно 30°С. Втілення С1. Спосіб, який описано в Короткому описі суті винаходу, де перший отриманий розчин, що містить сполуку Формули 2b, реагує зі сполукою Формули 3 або її кислотною сіллю. Втілення С2. Спосіб, який описано в Короткому описі суті винаходу, демольне співвідношення сполуки Формули 3 або її кислотної солі до сполуки Формули 2а знаходиться в діапазоні від приблизно 0,6 до приблизно 1,2. Втілення С3. Спосіб за Втіленням С2, демольне співвідношення сполуки Формули 3 або її кислотної солі до сполуки Формули 2а знаходиться в діапазоні від приблизно 0,6 до приблизно 1,0. Втілення С4. Спосіб за Втіленням С3, демольне співвідношення сполуки Формули 3 або її кислотної солі до сполуки Формули 2а знаходиться в діапазоні від приблизно 0,7 до приблизно 0,9. Втілення С5. Спосіб, який описано в Короткому описі суті винаходу, де друга основа являє собою гідрокcид лужного металу. Втілення С6. Спосіб за Втіленням С5, де гідроксидом лужного металу є гідроксид натрію або гідроксид калію. Втілення С7. Спосіб за Втіленням С6, де гідроксидом лужного металу є гідроксид натрію. Втілення С8. Спосіб за Втіленням С5, демольне співвідношення другої основи до сполуки Формули 3 знаходиться в діапазоні від приблизно 2 до приблизно 0,5. Втілення С9. Спосіб за Втіленням С8, демольне співвідношення другої основи до сполуки Формули 3 знаходиться в діапазоні від приблизно 1,2 до приблизно 0,8. Втілення С10. Спосіб, який описано в Короткому описі суті винаходу, де рН другого отриманого розчину знаходиться в діапазоні від приблизно 9 до приблизно 12. 13 Втілення С11. Спосіб за Втіленням С10, де рН знаходиться в діапазоні від приблизно 10,5 до приблизно 11,5. Втілення С12. Спосіб, який описано в Короткому описі суті винаходу, де стадію (2) проводять при першій температурі в діапазоні від приблизно 0 до приблизно 40°С, та потім температуру підвищують до другої температури в діапазоні від приблизно 10 до приблизно 70°С. Втілення С13. Спосіб за Втіленням С12, де перша температура знаходиться в діапазоні від приблизно 20 до приблизно 40°С, та друга температура знаходиться в діапазоні від приблизно 50 до приблизно 65°С. Втілення D1. Спосіб, який описано в Короткому описі суті винаходу, де кислота, яку додають на стадії (3), є мінеральною кислотою. Втілення D2. Спосіб за Втіленням D1, де кислотою є сірчана кислота або соляна кислота. Втілення D3. Спосіб, який описано в Короткому описі суті винаходу, де після додавання кислоти на стадії (3) другий отриманий розчин має рН в межах нижче приблизно 3. Втілення D4. Спосіб за Втіленням D3, де рН знаходиться в діапазоні від приблизно 1 до приблизно 2. Втілення D5. Спосіб, який описано в Короткому описі суті винаходу, де стадію (3) проводять при першій температурі в діапазоні від приблизно 30 до приблизно 55°С, та потім температуру знижують до другої температури в діапазоні від приблизно 0 до приблизно 20°С. Втілення D6. Спосіб за Втіленням D5, де перша температура знаходиться в діапазоні від приблизно 40 до приблизно 45°С, та друга температура знаходиться в діапазоні від приблизно 0 до приблизно 10°С. Втілення Е1. Спосіб, який описано в Короткому описі суті винаходу, в якому одержують сполуку Формули 4, де хлоруючий агент вибраний з групи, що включає хлор, гіпохлористу кислоту, сульфурил хлорид, гіпохлорид натрію, гіпохлорид кальцію та гіпохлорид калію. Втілення Е2. Спосіб, який описано в Короткому описі суті винаходу, в якому одержують сполуку Формули 6, де хлор-заміщуючий агент вибраний з групи, що включає оксихлорид фосфору, тіоніл хлорид, оксаліл хлорид, фосген, дифосген та трифосген. В наступних Схемах 1-6 визначення R1, R2, R3 та R4 в сполуках Формул 1-8 є такими, як визначено вище в Короткому описі суті винаходу та описі Втілень, якщо не вказано інше. Даний спосіб одержання необов'язково 2замішених 1,6-дигідро-6-оксо-4піримідинкарбонових кислот Формули 1, проілюстрований на Схемах 1 та 2. Як наведено на Схемі 1, на першій стадії, суміш, що містить сіль оксалацетатного ефіру Формули 2а, нижчий алканол (тобто С1-С4алканол) та воду, об'єднують з розчином, що містить основу, розчинену у воді. Основа присутня в достатній кількості, такій, що отриманий розчин, що містить сіль Формули 2b, має рН в діапазоні від приблизно 10 до приблизно 14. Вважають, що при цьому діапазоні рН ефірна група, гемінальна до 92171 14 ОМ на Формулі 2а, буде вибірково омилюватися з утворенням відповідної групи СО2М Формули 2b. де Μ являє собою лужний метал та R2 і R3 незалежно являють собою С1-С4алкіл. Звичайно суміш, що містить сіль оксалацетатного діефіру Формули 2, С1-С4алканол та воду, одержують шляхом додавання солі Формули 2а до суміші С1-С4алканолу та води, але можливі й інші порядки додавання. До того ж сіль оксалацетатного діефіру Формули 2а може бути одержана in situ шляхом об'єднання відповідного оксалацетатного діефіру з алканолом та/або водою, що містить приблизно один еквівалент гідроксиду або алкоксиду натрію або калію. Суміш, що містить сіль оксалацетатногодіефіру Формули 2а, С1-С4алканол та воду, звичайно присутня у вигляді розчину, в якому повністю розчинена сіль оксалацетатного діефіру, що має Формулу 2а, але залежно від кількостей алканолу та води суміш також може існувати у вигляді суспензії, в якій частина солі оксалацетатного діефіру Формули 2а залишається нерозчиненою. Оскільки сіль калію Формули 2а діє задовільно в цього способі, переважною є сіль натрію, оскільки її легко отримують з високим виходом. Хоча як R2 та R3 може бути використаний широкий ряд компонентів, що несуть вуглець, внаслідок вартості та придатності, найбільш прийнятними є нижчі алкільні (тобто С1-С4алкільні) групи, тобто метил, етил, н-пропіл, ізопропіл, н-бутил, втор-бутил або трет-бутил, та добре діють алкільні групи з коротким ланцюгом, такі як етил. С1-С4алканол вибраний з можливих С1С4алканолів, тобто метанолу, етанолу, нпропанолу, ізопропанолу, н-бутанолу, вторбутанолу, трет-бутанолу, та їх сумішей. Було знайдено, що етанол, який необов'язково містить денатуровані спирти, такі як ізопропанол, добре діє в цій реакції, але можуть бути використані й інші С1-С4алканоли, такі як метанол. Оскільки суміш містить воду, етанол придатно може бути використаний у вигляді його азеотропу 95% етанолу - 5% води. Звичайно об'ємне співвідношення води до сполуки Формули 2а в суміші перед додаванням основи знаходиться в діапазоні від приблизно 0,01 до приблизно 10, більш звичайно від приблизно 1 до приблизно 6, та найбільш звичайно від приблизно 2 до приблизно 3. Найбільш звичайно об'ємне співвідношення суміші вода-алканол до сполуки Формули 2а в суміші перед додаванням основи знаходиться в діапазоні від приблизно 2 до приблизно 6. Звичайно об'ємне співвідношення води до алканолу в суміші перед додаванням основи знаходиться в діапазоні від приблизно 0,01 до приблизно 100, більш звичайно від приблизно 1 до приблизно 50, та найбільш звичайно від приблизно 5 до приблизно 10. Коли, як С1-С4алканол, використовують етанол, добре діє приблизно 2,5 15 об'ємів суміші приблизно 15ваг.% етанолу у воді відносно сполуки Формули 2а. Суміш, що містить сіль оксалацетатного діефіру Формули 2а, С1-С4алканол та воду, об'єднують з розчином основи у воді. Переважно водний розчин основи додають до суміші, що містить сіль оксалацетатного діефіру Формули 2а, С1С4алканол та воду, оскільки цей порядок додавання запобігає тимчасовому впливові надлишку основи на сполуку Формули 2а. Основа повинна бути достатньо сильною, щоб забезпечити рН в діапазоні приблизно від 10 до 14. Найбільш придатною та недорогою основою є гідроксид лужного металу, такий як гідроксид натрію або калію. Звичайно використовують від приблизно 0,5 до приблизно 2, більш звичайно від приблизно 0,7 до приблизно 1,5, та найбільш звичайно приблизно від 0,9 до 1,2мольних еквівалентів основи щодо сполуки Формули 2а. Вважають, що ця кількість основи омилює сполуку Формули 2а з одержанням сполуки Формули 2b, забезпечуючи кінцевий рН в діапазоні приблизно від 10 до 14. Переважно кількість основи вибрана таким чином, що кінцевий рН знаходиться в діапазоні між приблизно 11 та 13. Основу додають у вигляді водного розчину до суміші, що містить сіль оксалацетатного діефіру Формули 2а, С1-С4алканол та воду. Звичайно водний розчин основи містить від приблизно 1 до 50ваг.% основи, більш звичайно від приблизно 10 до 40ваг.% основи, та найбільш звичайно від приблизно 20 до 30ваг.% основи. Протягом додавання водного розчину основи температуру реакційної суміші звичайно підтримують між приблизно 5 та 40°С, та більш звичайно між приблизно 20 та 30°С (наприклад, приблизно 25°С). В результаті способу Схеми 1 одержують суміш продукту гідролізу, що містить, в основному, моноалкіл оксалацетатну сіль сполуки Формули 2b, загалом у формі розчину. Цей розчин звичайно безпосередньо використовують в неочищеній формі на наступній стадії. Хоча проміжну моноалкіл оксалацетатну сіль сполуки Формули 2b звичайно не виділяють, базуючись на високих виходах для повного способу, обгрунтовано вважають, що виходи сполуки Формули 2b в результаті стадії, наведеної на Схемі 1, складають близько від 80 до 90%. Як наведено на Схемі 2, на наступній стадії сполуку Формули 1 одержують за допомогою реакції суміші продукту гідролізу, що містить сполуку Формулу 2b, отриманої на першій стадії, з карбоксимідамідом Формули 3. Використовують звичайно від приблизно 0,6 до приблизно 1,2, більш звичайно від приблизно 0,6 до приблизно 1, найбільш звичайно від приблизно 0,7 до приблизно 0,9мольних еквівалентів карбоксимідаміду Формули 3 щодо діалкілового 92171 16 ефіру Формули 2а, який використовують для одержання проміжної сполуки Формули 2Ь. Карбоксимідамід Формули 3 може знаходитися або у формі його вільної основи, або у формі солі, як наприклад його гідрохлоридна сіль. Хоча суміш продукту гідролізу може бути додана до карбоксимідаміду Формули 3, звичайно карбоксимідамід додають до суміші продукту гідролізу. Карбоксимідамід може безпосередньо контактувати із сумішшю продукту гідролізу, або він може бути доданий у вигляді розчину в прийнятному розчиннику, такому як вода або нижчий алканол. Звичайно карбоксимідамід Формули 3 реагує з сумішшю продукту гідролізу при температурі між приблизно 0 та приблизно 40°С, більш звичайно від приблизно 20 до приблизно 40°С, переважно від приблизно 20 до приблизно 30°С. Як описано нижче, температуру часто потім підвищують, щоб прискорити завершення реакції. На цій стадії реакції необхідно, щоб одержаний розчин мав рН в діапазоні від приблизно 9 до приблизно 12, переважно від приблизно 10 до приблизно 12, більш переважно від приблизно 10,5 до приблизно 11,5. Таким чином, щоб забезпечити цей діапазон рН додають достатню кількість основи. Якщо карбоксимідамід Формули 3 використовують у формі його вільної основи, кількість додаткової основи, необхідної, щоб досягти діапазону приблизно від 9 до 12, може складати нуль. Проте, якщо карбоксимідамід Формули 3 знаходиться у формі солі, як наприклад його гідрохлоридна сіль, щоб забезпечити необхідний діапазон рН, потрібна достатня кількість основи. Хоча основа може бути додана до солі карбоксимідаміду або його розчину перед додаванням карбоксимідаміду до суміші продукту гідролізу, або основа може бути додана до суміші продукту гідролізу перед додаванням солі карбоксимідаміду, переважно основу додають до суміші продукту гідролізу після додавання солі карбоксимідаміду. Основа повинна бути достатньо сильною, щоб забезпечити необхідний рН; в цьому випадку добре діє гідроксид лужного металу, такий як гідроксид натрію або калію. Коли карбоксимідамід Формули 3 знаходиться у формі солі,мольні еквіваленти основи щодо карбоксимідаміду знаходяться звичайно в діапазоні від приблизно 0,5 до приблизно 2, та більш звичайно в діапазоні від приблизно 0,8 до приблизно 1,2. Звичайно основу розчиняють в розчиннику, такому як вода, перед додаванням до реакційної суміші. Після того, як карбоксимідамід Формули 3 об'єднують з сумішшю продукту гідролізу разом з кількістю основи, необхідною, щоб забезпечити діапазон рН приблизно від 9 до 12 в реакційній суміші, реакційну суміш часто нагрівають, щоб прискорити завершення реакції. Для цієї мети температуру звичайно коректують від приблизно 10 до приблизно 70°С, та більш звичайно від приблизно 50 до приблизно 65°С. Реакційна суміш містить сполуку Формули 1 у вигляді її карбоксилатної солі, яку звичайно розчиняють в реакційній суміші. Для виділення сполуки Формули 1, реакційну суміш звичайно охолоджують до температури приблизно 55°С або нижче 17 (наприклад, між приблизно 30 та 55°С, часто прийнятно приблизно 45°С), та додають кислоту, щоб підкислити реакційну суміш та перетворити сполуку Формули 1 з її карбоксилатної солі на форму її вільної кислоти. Добре діють звичайні загальні мінеральні кислоти, такі як соляна кислота, сірчана кислота або фосфорна кислотна. Кислоту додають в кількості, достатній, щоб знизити рН реакційної суміші, нижче приблизно 3, звичайно в діапазоні від приблизно 1 до приблизно 2. Часто в цих умовах продукт Формули 1 буде кристалізуватися. Реакційну суміш потім переважно охолоджують до температури в діапазоні від приблизно 0 до приблизно 10°С, щоб сприяти кристалізації, та твердий продукт збирають фільтруванням, промивають та сушать. Якщо продукт Формули 1 утворюється у вигляді нетвердої речовини, він може бути виділений за допомогою екстракції реакційної суміші прийнятним розчинником, що не змішується з водою, таким як ефір, дихлорметан або етил ацетат, сушіння та випарювання розчиннику. Спосіб Схем 1 та 2 проілюстрований на Стадії В Прикладу 1. Карбоксимідамідні сполуки Формули 3 можуть бути одержані за допомогою способів, відомих з рівня техніки, включаючи поліпшені модифікації, викладені в патентах US 4,323,570 та 4,012,506. Одержання сполуки Формули 3 проілюстроване на Стадії А Прикладу 1. Таким чином, сполуки 1,6-дигідро-6-оксо-4піримідинкарбонових кислот Формули 1 можуть бути прийнятно одержані з високим виходом зі сполук Формули 2а та 3 відповідно до описаного вище способу. Сполуки 1,6-дигідро-6-оксо-4піримідинкарбонових кислот Формули 1, одержані цим способом, потім можуть бути перетворені, використовуючи додаткові стадії реакції на різноманітні необов'язково заміщені 4піримідинкарбонові кислоти та ефіри. За допомогою першої подальшої реакції, наведеної на Схемі 3, одержують сполуку Формули 4 за допомогою реакції сполуки Формули 1 з хлоруючим агентом. Цей спосіб залучає заміну водню в 4положенні 1,6-дигідро-6-оксо-4-піримідинільного кільця на хлор. Як відомо з рівня техніки, для цього типу перетворення можуть бути використані різні хлоруючі агенти (тобто реагенти, які замінюють атоми водню в органічних молекулах на хлор). Нижче описані приклади методик для способу, коли хлоруючим агентом є хлор, гіпохлориста кислота, сульфурил хлорид або неорганічні гіпохлорити, такі як гіпохлорит натрію, гіпохлорит кальцію та гіпохлорит калію. В одній методиці, сполуку Формули 1 суспендують в інертному розчиннику, звичайно приблизно від 3 до 6 об'ємах води, що необов'язково міс 92171 18 тить від 0,5 до 3,5мольних еквівалентів мінеральної кислоти, переважно соляної кислоти. При оптимальному перемішуванні при від приблизно 10 до приблизно 35°С додають від приблизно 0,95 до приблизно 1,2мольних еквівалентів хлоруючого агента, переважно хлору або гіпохлористої кислоти (НОСІ). Якщо використовують гіпохлористу кислоту, вона може бути синтезована in situ шляхом додавання, принаймні, 1мольного еквіваленту мінеральної кислоти до суспензії сполуки Формули 1 перед додаванням неорганічного гіпохлориту, переважно гіпохлориту натрію (NaOCl) звичайно у вигляді від 5 до 14% водного розчину. Надлишок хлоруючого агента може бути видалений за допомогою продувки інертним газом або за допомогою додавання відновника, такого як сульфіт натрію. Якщо продукт Формули 4 утворюється у вигляді твердої речовини, він може бути виділений за допомогою фільтрування. Якщо продукт Формули 4 утворюється у вигляді нетвердої речовини, він може бути виділений за допомогою екстракції водної реакційної суміші розчинником, що не змішується з водою, таким як ефір, дихлорметан або етил ацетат, сушіння та випарювання екстрагуючого розчиннику. Ця методика проілюстрована на стадії С1 Прикладу 1. В іншій методиці, сполуку Формули 1 розчиняють в інертному розчиннику, переважно від приблизно 1,5 до приблизно 4 об'ємах води, що необов'язково містить приблизно від 0 до 3,5мольних еквівалентів неорганічної основи, переважно гідроксиду натрію або гідроксиду калію. При оптимальному перемішуванні до реакційної суміші при приблизно від 0 до 70°С, звичайно приблизно від 10 до 35°С, додають від приблизно 0,95 до приблизно 1,2мольних еквівалентів хлоруючого агента, переважно хлору або гіпохлориту натрію (NaOCl, звичайно у вигляді від 5 до 14% водного розчину). Коли як хлоруючий агент використовують гіпохлорит натрію, кількість основи переважно складає приблизно від 0,85 до 1,2мольних еквівалентів щодо сполуки Формули 1. Надлишок хлоруючого агента може бути видалений за допомогою продувки інертним газом або за допомогою додавання відновника, такого як сульфіт натрію. Реакційну суміш потім підкисляють шляхом додавання мінеральної кислоти, такої як концентрована соляна кислота, щоб знизити рН до приблизно від 0,5 до 3, та одержують вільну кислотну форму сполуки Формули 4. Якщо продуктом Формули 4 є тверда речовина, вона може бути виділена за допомогою фільтрування. Якщо продукт Формули 4 утворюється у вигляді нетвердої речовини, він може бути виділений за допомогою екстракції водної реакційної суміші розчинником, що не змішується з водою, таким як ефір, дихлорметан або етил ацетат, сушіння та випарювання екстрагуючого розчиннику. Ця методика проілюстрована на Стадії С2 Прикладу 1. За допомогою другої додаткової реакції, наведеної на Схемі 4, одержують сполуку Формули 6 за допомогою реакції сполуки Формули 4 з хлорзаміщуючим агентом. 19 Цей спосіб залучає заміну 6-оксо функції на 1,6-дигідро-6-оксо-4-піримідинільному кільці на хлор. Як відомо з рівня техніки, для цього типу перетворення можуть бути використані різні хлорзаміщуючі агенти (тобто реагенти, які замінюють гідроксі компоненти в органічних молекулах на хлор). Оскільки гідроксильний компонент на функції карбонової кислоти також може бути заміщений на хлор, реакція з хлор-заміщуючими агентами часто приводить до утворення проміжних ацил хлоридів Формули 5, в яких R1 являє собою Η або необов'язково заміщений вуглецевий компонент, який гідролізується при контакті з водою протягом обробки реакційної суміші з одержанням сполук Формули 6. Нижче описані приклади методик для способу, коли хлор-заміщуючим агентом є оксихлорид фосфору, тіоніл хлорид, оксаліл хлорид, фосген, дифосген або трифосген. В одній методиці, сполуку Формули 4 об'єднують з від приблизно 2 до приблизно 4мольними еквівалентами хлор-заміщуючого агента, такого як оксихлорид фосфору. В реакційну суміш також необов'язково вводять приблизно від 0,05 до 1,0мольних еквівалентів Ν,Ν-диметилформаміду (DMF), звичайно без додавання розчиннику. Реакційну суміш утримують при температурі між приблизно 10 та приблизно 100°С, звичайно між приблизно 70 та приблизно 95°С. Надлишок оксихлориду фосфору може бути прийнятно видалений перегонкою при тиску приблизно від 6 до 30кПа. Реакційну суміш (вважають, що вона містить проміжний хлорангідрид кислоти Формули 5 та полімерні хлорфосфорні кислоти) потім обережно додають до води, що необов'язково містить приблизно від 20 до 40% органічного співрозчинника, що не змішується з водою, переважно третбутанолу. В суміші добре діє приблизно 25ваг.% трет-бутанолу. Якщо продукт Формули 6 являє собою тверду речовину, одержана суміш потім може бути розбавлена водою, щоб сприяти кристалізації. Суспензію кристалічного продукту Формули 6 потім відфільтровують, промивають водою та звичайно сушать. Якщо продукт Формули 6 утворюється у вигляді нетвердої речовини, він може бути виділений за допомогою екстракції реакційної суміші прийнятним розчинником, що не змішується з водою, таким як ефір, дихлорметан або етил ацетат, та сушіння розчину. Розчинник може бути випаруваний для виділення сполуки Формули 6, або, якщо розчинник є прийнятним для наступної реакції, розчин може бути використаний безпосередньо. Ця методика проілюстрована на Стадії D1 Прикладу 1. В іншій методиці, сполуку Формули 4 змішують з приблизно від 2 до 4 об'ємами апротонного органічного розчинника, такого як етил ацетат, тетрагідрофуран або 1,2-дихлоретан, необов'язково при 92171 20 близно від 0,02 до 0,2мольними еквівалентами Ν,Ν-диметилформаміду та від приблизно 2,0 до приблизно 3,0мольними еквівалентами хлорзамішуючого агента, переважно тіоніл хлориду, оксаліл хлориду або фосгену. Реакційну суміш утримують звичайно при приблизно 20-100°С, переважно при приблизно 50-70°С, протягом звичайно 2-12год. Реакційну суміш (вважають, що вона містить проміжний хлорангідрид кислоти Формули 5) потім обережно додають до води при перемішуванні. Продукт Формули 6 може бути виділений або одержаний у вигляді розчину, як описано для першої методики. Дана методика проілюстрована на Стадії D2 Прикладу 1. В результаті третьої подальшої реакції, наведеної на Схемі 5, одержують сполуку Формули 7 за допомогою реакції сполуки Формули 6 з аміаком. Цей спосіб залучає заміну хлору в 6-положенні піримідинільного кільця на аміно функцію. Як відомо з рівня техніки, цей тип перетворення загалом включає реакцію 6-хлорпіримідинових сполук з аміаком. Звичайно аміак забезпечують з резервуару зберігання, або у вигляді концентрованого розчину в розчиннику (наприклад, гідроксиду амонію), хоча аміак також може бути отриманий in situ за допомогою реакції солей амонію, таких як хлорид амонію або сульфат амонію, з основами. Нижче описаний приклад методики. В цій методиці, сполуку Формули 6 змішують з аміаком в розчиннику. Хоча стехіометично потрібно тільки приблизно 1мольний еквівалент аміаку, якщо присутня інша основа, звичайно аміак являє собою єдину основу, що присутня, та для отримання високої швидкості реакції використовують від 3 до 7мольних еквівалентів аміаку. Можуть бути використані різні інертні розчинники, включаючи воду, алканоли, такі як етанол, та ефіри, такі як тетрагідрофуран; вода є недорогою та часто діє добре. Реакційну суміш утримують при температурі в діапазоні приблизно від 0 до 100°С, звичайно приблизно від 80 до 90°С, та при тиску звичайно в діапазоні від приблизно 100 (тобто атмосферний тиск) до приблизно 500кПа. В цих умовах реакція звичайно завершується через приблизно 1-5 год. Продукт Формули 7 може бути виділений шляхом охолодження суміші, необов'язково видалення надлишкового тиску, перегонки, щоб видалити надлишковий аміак та розчинник, додавання 12мольних еквівалентів мінеральної кислоти, переважно водної соляної кислоти, щоб знизити рН до приблизно 2. Якщо продукт Формули 7 утворюється у вигляді твердої речовини, він може бути зібраний фільтруванням, промитий та висушений. Якщо продукт Формули 7 утворюється у вигляді нетвердої речовини, він може бути виділений за 21 допомогою екстракції реакційної суміші прийнятним розчинником, що не змішується з водою, таким як ефір, дихлорметан або етил ацетат, сушіння та випарювання розчиннику. Ця методика проілюстрована на Стадії Ε Прикладу 1. В результаті четвертої подальшої реакції, наведеної на Схемі 6, одержують сполуку Формули 8 за допомогою реакції сполуки Формули 7 з R4заміщуючим агентом. де R4 являє собою необов'язково заміщений вуглецевий компонент. Цей спосіб залучає перетворення групи карбонової кислоти (СО2Н) в сполуці Формули 7 на відповідну ефірну групу (CO2R4) в сполуці Формули 8. Перетворення карбонових кислот на ефіри є одним з найстаріших відомих перетворень в органічній хімії, та відома величезна різноманітність методик для цього перетворення. Для оглядів, див. наприклад, С. A. Buehler and D. E. Pearson, Survey of Organic Syntheses, Wiley-Interscience, New York, 1970, pp.802-827. Більшість безпосередніх методик залучає реакцію карбонових кислот зі спиртами (наприклад, R4OH) в присутності кислотного каталізатора або дегідратуючого агента сполучення, або реакцію зі сполуками, які надають спиртовий компонент та які також поглинають отриману воду (наприклад, ортоефіри, карбонати), також звичайно в присутності кислотного каталізатора, або реакцію карбонових кислот в присутності основи з хімічними сполуками типу алкілуючих агентів, в яких радикал R4 зв'язаний з нуклеофугом (наприклад, R4X, де X являє собою нуклеофільну групу, що відходить в реакції, також відому як нуклеофуг). Такі дегідратуючі агенти сполучення, як дициклогексил карбодіімід, N-(3диметиламінопропіл)-N'-етилкарбодіімід, циклічний ангідрид 1-пропанфосфорної кислоти та карбоніл діімідазол, добре відомі з рівня техніки, але зважаючи на їх вартість та потенційний вплив на аміно групу, кислотний каталіз є переважним способом одержання сполук Формули 8 зі сполук Формули 7 та спиртів формули R4ОН. В способі Схеми 6 сполуки, такі як спирти формули R4OH, ортоефіри (наприклад, (R4O)3CRa, в яких Ra являє собою Н, OR4 або необов'язково заміщений вуглецевий компонент), карбонати (наприклад, R4OC(O)OR4) та сполуки формули R4X є R4заміщуючими агентами, оскільки вони забезпечують компонент R4, необхідний для перетворення групи карбонової кислоти в сполуці Формули 7 на ефірну групу в сполуці Формули 8. Як визначено в даному описі та формулі винаходу, "R4заміщуючий агент" означає хімічну сполуку, здатну до переносу радикалу R4 до групи карбонової кис 92171 22 лоти (тобто СО2Н) або отриманого карбоксилатного кислотного аніону (тобто СО2Θ) з одержанням відповідного ефіру (тобто CO2R4). Реакції, каталізовані кислотою, спиртів формули R4ОН та відпо4 a відних ортоефірів формули (R O)3CR та карбона4 4 4 тів формули R OC(O)OR , як R -заміщуючиx агентів, діють найкраще, коли вони є рідкими при температурі реакції та коли вони мають порівняно помірну молекулярну складність та розмір (наприклад, молекулярні маси менші, ніж 200, переважно менші, ніж 150). Реакція з R4X, як R4-заміщуючим агентом, відбувається добре для груп R4 з як малим, так і великим структурним розміром та складністю. Нижче описані приклади методик для цього способу. В методиці, в якій використовується спирт формули R4OH, як R4-заміщуючий агент, з кислотним каталізатором, сполуку Формули 7 змішують із звичайно приблизно 2-10 об'ємами спирту формули R4OH та сильною кислотою як каталізатором. Сильні протоновмісні кислоти мають рKа менше, ніж 3. Приклади використовуваних сильних протоновмісних кислот включають фосфорну кислоту, сірчану кислоту, хлорид водню, трифтороцтову кислоту, р-толуолсульфонову кислоту, камфорсульфонову кислоту, метансульфонову кислоту та трифторметансульфонову кислоту. Кислоти переважно є концентрованими та містять так мало води, як припустимо. Хлорид водню переважно може бути синтезований шляхом додавання тіоніл хлориду до спирту. Використовувані сильні протоновмісні кислоти також включають тверді каталізатори, такі як сульфований полістирол та перфторовані іонообмінні смоли, такі як Nation®. Концентрована сірчана кислота є недорогою кислотою, що добре діє в цьому способі. Окрім протоновмісних кислот, як сильна кислота може бути використана кислота Льюїса, така як трифторид бору (наприклад, ефірат BF3). Звичайно використовують приблизно 2-4мольних еквівалентів кислоти щодо сполуки Формули 7, але можуть бути використані менші або більші кількості. Кислоту звичайно додають до реакційної суміші останньою. Додавання кислоти може бути надзвичайно екзотермічним, так що може бути потрібним охолодження реакційної суміші, щоб підтримувати бажану температуру реакції та запобігати надмірному закипанню спирту. Звичайно реакційну суміш утримують при температурі приблизно від 20 до 100°С, часто при приблизно 70°С. В цих умовах реакція звичайно досягає максимального перетворення через приблизно 2-24год. Швидкість реакції може бути збільшена та більш високе перетворення на ефір досягають за допомогою відгонки води, яка утворюється; може бути бажаним додавання більшої кількості спирту та/або кислотного каталізатору, щоб компенсувати складові, які відганяються з реакційної суміші разом з водою. Після завершення реакції суміш може бути концентрована, щоб видалити більшу частину спирту (R4ОН), якщо він має достатньо низьку температуру кипіння. При такому концентруванні також можуть бути видалені леткі кислоти, такі як хлорид водню. Полімерні кислотні каталізатори можуть бути відділені фільтруванням. Реакційну суміш 23 звичайно охолоджують до приблизно 0-35°С та розбавляють водою, звичайно 4-8 об'ємами. рН звичайно коректують до приблизно 5-10, найбільш звичайно до приблизно 7, за допомогою додавання основ (наприклад, гідроксидів лужних металів та лужноземельних металів та карбонатів, таких як гідроксид натрію, гідроксид кальцію та карбонат натрію), а також кислот (наприклад, оцтової кислоти, соляної кислоти, сірчаної кислоти), якщо потрібно титрують до конкретного рН. Якщо продукт Формули 8 утворюється у вигляді твердої речовини, він може бути виділений за допомогою фільтрування, промивання та сушіння. Якщо продукт Формули 8 утворюється у вигляді нетвердої речовини, він може бути виділений за допомогою екстракції розчинником, що не змішується з водою, таким як ефір, дихлорметан або етил ацетат, сушіння розчину та випарювання розчиннику. Вихідна сполука Формули 7, що не прореагувала, часто може бути відновлена шляхом підкислення водної суміші до приблизно рН2 та концентрування суміші, щоб викликати відокремлення сполуки Формули 7. Ця методика проілюстрована на Стадії F1 Прикладу 1. В методиці, в якій використовується ортоефір формули (R4O)3CRa або карбонат формули R4OC(O)OR4, як R4-заміщуючий агент, також звичайно використовують сильну кислоту як каталізатор. Найбільш звичайно ортоефірами є ортоформіати (тобто Ra являє собою Н) та ортоацетати (тобто Ra являє собою СН3). Стехіометрично потрібен, принаймні, одинмольний еквівалент ортоефіру формули (R4O)3CRa або карбонату формули R4OC(O)OR4 щодо карбонової кислоти Формули 7 для одержання ефіру за відсутності інших R4заміщуючиx агентів, але звичайно використовуються приблизно 2-8мольних еквівалентів, щоб швидко досягти високих виходів ефіру, та вони виступають як розчинник. До реакційної суміші також можуть бути включені інші розчинники, такі як ефіри, подібні тетрагідрофурану та р-діоксану, та спирти формули R4OH, які також можуть діяти, як R4-заміщуючi агенти, в умовах реакції. Якщо в реакційну суміш додатково включений розчинник, він звичайно присутній в кількості до приблизно 10 об'ємів щодо сполуки Формули 7. Загалом ті ж самі кислоти, які використовуються для естерифікації зі спиртами, також використовуються для естерифікації з ортоефірами та карбонатами. Звичайно використовують приблизно 2-4мольних еквівалентів кислоти щодо сполуки Формули 7, але можуть бути використані менші або більші кількості. Кислоту звичайно додають до реакційної суміші останньою. При додаванні кислоти може бути потрібне охолодження, щоб запобігти надмірним температурам. Реакційну суміш звичайно утримують при температурі між приблизно 20 та 100°С, найбільш звичайно між приблизно 70 та 80°С. В цих умовах реакція звичайно завершується через приблизно 4-24 год. Якщо температури кипіння дозволяють, надлишок ортоефіру, карбонату, спирту та/або кислотного каталізатору може бути видалений перегонкою або випарюванням з одержанням концентрованого залишку. Реакційна суміш може бути оброблена та ефірний продукт Формули 8 92171 24 виділяють, використовуючи способи, подібні описаним для попередньої методики, в якій як R4заміщуючий агент використовується спирт формули R4OH. Ця методика проілюстрована на Стадії F2 Прикладу 1. В методиці, в якій використовується сполука формули R4X як R4-заміщуючий агент, X являє собою нуклеофуг. На сполуки формули R4X часто посилаються як на алкілуючі агенти, хоча R4 може бути необов'язково заміщеними вуглецевими компонентами, окрім алкілу. Звичайно X являє собою основу, сполучену з кислотою. Загальні нуклеофуги включають галоген (наприклад, СІ, Вr, І), сульфати, такі як OS(O)2OR4 та сульфонати, такі як OS(O)2CH3 (метансульфонат), OS(O)2CF3, OS(O)2Ph-p-СН3 (р-толуолсульфонат). Проте, нуклеофуги, що використовуються для отримання ефірів, також включають пірокарбонати, силікати та фосфонати. Нуклеофуги також включають ефіри (наприклад, R4OR4), коли R4-заміщуючий агент являє собою сіль оксонію (наприклад, O(R4)3 BF4Θ). Сполука Формули 7 реагує зі сполукою формули R4X звичайно в полярному розчиннику, такому як ацетон, ацетонітрил або диметил сульфоксид (DMSO) та в присутності основи. Звичайно використовують приблизно 1-2 еквівалентів кожної зі сполуки формули R4X та основи щодо сполуки Формули 7. Прийнятні основи включають органічні аміни, такі як трибутиламін та Ν,Νдіізопропілетиламін, та неорганічні основи, такі як карбонати, оксиди, гідроксиди та фосфати лужних та лужноземельних металів (наприклад, Nа2СО3, K2СО3, LiOH, Li2O, NaOH, KОН, Na3PO4, K3РО4). Основа та сполука формули R4X можуть додаватися або послідовно, або одночасно. Звичайно реакційну суміш утримують при температурі між приблизно 0 та 120°С, більш звичайно між приблизно 10 та 80°С. Важливим є підтримання енергійного перемішування, особливо, якщо основа являє собою неорганічну основу, яка погано розчиняється в реакційному розчиннику. Швидкість реакції може істотно змінюватися залежно від умов, але звичайно реакція завершується через приблизно 1-24год. Для обробки реакційної суміші надлишок розчиннику, R4X та/або основи може бути видалений випарюванням під зниженим тиском або перегонкою, та надлишок основи може бути нейтралізований або видалений за допомогою екстракції кислотою. Якщо сполука Формули 8 являє собою тверду речовину, розбавлення реакційної суміші водою (наприклад, приблизно 4-10 об'ємами) часто приводить до кристалізації сполуки Формули 8, яка потім може бути зібрана фільтруванням, промита та висушена. Якщо сполука Формули 8 не кристалізується з водної суміші, її екстрагують, використовуючи розчинник, що не змішується з водою, такий як ефір, дихлорметан або етил ацетат, розчин сушать та розчинник випарюють, одержуючи сполуку Формули 8. Ця методика проілюстрована на Стадії F3 Прикладу 1. Було повідомлено, що сполуки Формул 7 та 8 мають біологічну активність. Зокрема, в публікації патентної заявки РСТ WO 2005/063721 описані сполуки Формул 7 та 8, де R1 являє собою, наприклад, циклопропіл або феніл, заміщений Вr або СІ 25 в пара-положенні фенільного кільця, та R4 являє собою, наприклад, С1-С14алкіл, С2-С14алкоксіалкіл, С2-С14гідроксіалкіл або бензил, які корисні як гербіциди. Без подальшого уточнення, вважають, що фахівець в даній галузі техніки, використовуючи попередній опис, може застосовувати даний винахід до його найширших меж. Таким чином, наступні Приклади наведено лише для ілюстрації та вони ні в якому випадку не обмежують розкриття. Стадії в наступних Прикладах ілюструють методику для кожної стадії в загальному синтетичному перетворенні, та вихідна речовина для кожної стадії могла не бути обов'язково одержана за допомогою специфічної серії одержання, методика якої описана в інших Прикладах або Стадіях. Спектри 1H ЯМР та 13 С ЯМР наведені в м.ч. нижче області тетраметилсилану; "s" означає синглет, "т" означає мультиплет, "br s" означає уширений синглет. Приклад 1 Одержання метил 6-аміно-5-хлор-2циклопропіл-4-піримідинкарбоксилату Стадія А: Одержання моногідрохлориду циклопропанкарбоксимідаміду 1-л реактор, постачений термопарою, зануреною трубкою подачі газу, резервуаром з хлоридом водню, рівноважним резервуаром та барботером азоту, наповнювали азотом та поміщали в нього циклопропанкарбонітрил (100г, 1,5моль), метанол (48г, 1,5моль) та толуол (400мл). Реакційну суміш утримували при 15°С під незначним позитивним тиском азоту, одночасно вводячи безводний хлорид водню (57г, 1,55моль) нижче поверхні реакційної суміші протягом 2 год. Потім реакційну суміш перемішували протягом 16год. при 23°С. Надлишковий хлорид водню видаляли барботуванням азоту нижче поверхні реакційної суміші та відводячи відхідний газ через водний газопромивач протягом 2год. Суміш охолоджували до 5°С та потім додавали розчин аміаку в метанолі (240мл 7Μ розчину, 1,7моль) протягом 10 хвилин, одночасно підтримуючи температуру нижче 25°С. Потім реакційну суміш утримували протягом 1год. та переганяли при зниженому тиску, щоб видалити надлишок метанолу. Продукт відфільтровували, промивали толуолом (100мл), та сушили вакуумним фільтруванням, одержуючи 170г (вихід 94%) зазначеної у заголовку сполуки у вигляді твердої речовини. 1H ЯМР (DMSO-d6) δ 8,8 (br s, 4H), 1,84 (m, 1H), 1,1 (m, 4H). Стадія В: Одержання 2-циклопропіл-1,6дигідро-6-оксо-4-піримідинкарбонової кислоти В 500-мл реактор, поміщений в кожух, постачений рН метром, датчиком температури та дозованою крапельною лійкою, поміщали денатурований етанол (що містив 5% 2-пропанолу, 30мл) та воду (150мл). Реакційну суміш перемішували, одночасно додаючи натрієву сіль діетил оксалацетату (70г, 0,33моль) протягом 10 хвилин. Розчин 25% водного NaOH (14г, 56мл, 0,35моль) дозували в приладі для струшування та перемішування протягом 1год., одночасно підтримуючи температуру в діапазоні від 25 до 30°С. Реакційну суміш перемішували протягом додаткових 30 хвилин при 30°С та додавали моногідрохлорид циклопропан 92171 26 карбоксимідаміду (32ваг.% розчин у воді, 32г, 0,267моль). Розчин 25% водного NaOH (31г, 0,19моль) додавали при температурі в діапазоні від 30 до 35°С протягом приблизно 1 год, таким чином, щоб підтримувати рН в діапазоні 10,5-11,5. Потім отриману оранжеву суміш поступово нагрівали до 60°С протягом 1год. та утримували при цій же температурі протягом додаткових 30 хвилин. Реакційну суміш охолоджували до 45-50°С та протягом 1год. при приблизно 45°С додавали соляну кислоту (37ваг.% у воді, 50мл, 0,60моль) (ОБЕРЕЖНО: вспінювання), поки рН досягне приблизно 1,5. Реакційну суміш охолоджували до 5°С та фільтрували. Отриманий вологий осад промивали водою (3 20мл), сушили вакуумним фільтруванням та сушили у вакуумній шафі при 70°С протягом 16 год, одержуючи 42г (вихід 85%) зазначеної у заголовку сполуки у вигляді бежевої твердої речовини (чистота 97% за допомогою аналізу ВЕРХ), яка розкладається при 235-236°С. 1 H ЯМР (DMSO-d6) δ 6,58 (s, 1H), 1,95 (m, 1H), 1,0 (m, 4H). 13 C ЯMP (DMSO-d6) δ 169,2, 169,0, 157,3, 116,8, 17,7, 14,1. Стадія С1: Одержання 5-хлор-2-циклопропіл1,6-дигідро-6-оксо-4-піримідин-карбонової кислоти У 2-л колбу Мортона з верхньою мішалкою, термопарою та крапельною лійкою поміщали 2циклопропіл-1,6-дигідро-6-оксо-4піримідинкарбонову кислоту (161г, 0,90моль), соляну кислоту (37ваг.% у воді, 300г, 250мл, 3моль) та воду (400мл). Реакційну суміш перемішували при 5-10°С та протягом 2год. додавали гіпохлорит натрію (14ваг.% водний розчин, 522г, 0,99моль). Реакційну суміш утримували при 10-12°С протягом 1год., поки тест на КІ-крохмальному папері, використовуючи сульфіт натрію, показав, що не залишилося гіпохлориту. Реакційну суміш охолоджували та фільтрували. Зібрану тверду речовину промивали холодною водою (160мл) та сушили до постійної маси у вакуумній шафі при 50°С, одержуючи 169г (вихід 88%) зазначеної у заголовку сполуки у вигляді твердої речовини, що плавиться при 189 -190°С. 1 Н ЯМР (DMSO-d6) δ 13,4 (br s, 1H), 1,95 (m, 1H), 1,0 (m, 4H). Стадія С2: Інший спосіб одержання 5-хлор-2циклопропіл-1,6-дигідро-6-оксо-4піримідинкарбонової кислоти У 500мл багато-горлу колбу з верхньою мішалкою, термопарою та крапельною лійкою поміщали 2-циклопропіл-1,6-дигідро-6-оксо-4піримідинкарбонову кислоту (36г, 0,20моль), воду (70мл) та 50ваг.% водний NaOH (14,4г, 0,18моль). Суміш перемішували при 10°С, та додавали 10,3% водного NaOCl (160г, 0,22моль) протягом 1,5год. з охолодженням, щоб утримувати реакційну суміш при 10°С. Суміш охолоджували до 5°С та додавали сульфіт натрію, поки КІ-крохмальний папір надавав негативні тестові результати. Додавали соляну кислоту (37ваг.% у воді, 44,3г, 0,443моль) при 5°С протягом приблизно 30 хвилин, щоб знизити рН до 0,8. Суміш фільтрували, та зібрану тверду речовину промивали охолодженою 1N НСl (20мл) та сушили до постійної маси у вакуумній шафі при 27 50°С, одержуючи 40,9г (вихід 95%) зазначеної у заголовку сполуки у вигляді твердої речовини, що плавиться при 189-190°С. Стадія D1: Одержання 5,6-дихлор-2циклопропіл-4-піримідинкарбонової кислоти Оксихлорид фосфору (363г, 221мл, 2,37моль) та 5-хлор-2-циклопропіл-1,6-дигідро-6-оксо-4піримідинкарбонову кислоту (169г, 0,79моль) поміщали в 1-л колбу та нагрівали при 90°С протягом 5год. Реакційну суміш охолоджували до 30°С та додавали протягом 60 хвилин до 2-л реактору, поміщеного в кожух, що містить добре перемішану суміш трет-бутанолу (280мл) та води (750мл), одночасно підтримуючи температуру при 5-10°С. Після того, як додавання реакційної суміші було завершено приблизно на 70%, у водну третбутанольну суміш вводили затравку, щоб викликати кристалізацію, та продовжували додавання реакційної суміші. В кінці додавання поступово додавали воду (750мл) при 10-15°С та суміш перемішували протягом додаткової 1год. Одержану суміш охолоджували до 5°С, фільтрували та зібрану тверду речовину промивали водою (3 χ 50мл). Одержаний вологий осад сушили у вакуумній шафі при 60°С, одержуючи 156г (вихід 85%) зазначеної у заголовку сполуки у вигляді твердої речовини, що плавиться при 126-127°С. 1 Н ЯМP (DMSO-d6) δ 2,23 (m, 1Н), 1,2 (m, 2H), 1,0 (m, 2H). Стадія D2: Інший спосіб одержання 5,6дихлор-2-циклопропіл-4-піримідинкарбонової кислоти У 500мл багато-горлу колбу з верхньою мішалкою, термопарою та холодильником поміщали 5хлор-2-циклопропіл-1,6-дигідро-6-оксо-4піримідинкарбонову кислоту (35,0г, 0,163моль), етил ацетат (105мл) та Ν,Ν-диметилформамід (1,19г, 0,016моль) при кімнатній температурі. Додавали тіоніл хлорид (48,5г, 0,408моль) при кімнатній температурі протягом 50 хвилин, та реакційну суміш нагрівали при 68°С протягом 7год. Реакційну суміш охолоджували до 25°С та додавали протягом 30 хвилин в 500-мл багато-горлу колбу, що містить воду (100мл), одночасно підтримуючи температуру при 10-20°С. Одержану суміш перемішували протягом додаткових 30 хвилин, та органічний шар відокремлювали від водного шару. Водний шар екстрагували додатковим етил ацетатом (20мл), та об'єднані органічні шари промивали водою. Органічний шар, що містить 35,0г (вихід 93%) зазначеного у заголовку продукту, безпосередньо переносили на наступну стадію. Стадія Е: Одержання 6-аміно-5-хлор-2циклопропіл-4-піримідинкарбонової кислоти У 3-л колбу поміщали 5,6-дихлор-2циклопропіл-4-піримідинкарбонову кислоту (280г, 1,2моль), аміак (28ваг.% у воді, 350г, 5,76моль) та воду (1,26л). Реакційну суміш нагрівали при 80°С протягом 5год., та надлишок води (приблизно 600мл) видаляли перегонкою при 50°С/9кПа. Після охолодження до 20°С реакційну суміш підкисляли до рН2 водною соляною кислотою (132г, 110мл, 1,32моль), охолоджували до 5°С та фільтрували. Відфільтрований вологий осад промивали водою (2 200мл) та сушили у вакуумній шафі при 55°С, 92171 28 одержуючи приблизно 270г зазначеної у заголовку сполуки у формі моногідрату, який містив 8,3ваг.% води, виміряної за допомогою титрування по методу Карла Фішера, та який розкладається при 152°С (після кристалізації з гарячого етанолу). 1 H ЯМР (DMSO-d6) δ 7,4 (br s, 3Н), 1,9 (m, 1H), 0,9 (m, 4H). 13 C ЯМР (DMSO-d6) δ 172,3, 169,5, 163,9, 158,5, 108,8, 21,1, 13,8. Стадія Fl: Одержання метил 6-аміно-5-хлор-2циклопропіл-4-піримідин-карбоксилату У 1-л колбу, постачену барботером азоту, сполученим з пасткою та газопромивачем, що містить каустичну соду, крапельною лійкою, зворотним холодильником та термопарою, поміщали моногідрат 6-аміно-5-хлор-2-циклопропіл-4піримідинкарбонової кислоти (144г, 0,62моль) та метанол (500мл). Додавали тіоніл хлорид (185г, 115мл, 1,58моль) протягом приблизно 30 хвилин з охолодженням та потім реакційну суміш нагрівали при 60°С протягом 12 год. Одержану суміш концентрували при 40-45°С/6кПа, щоб видалити надлишок метанолу (приблизно 300мл), та реакційну суміш розбавляли водою (580мл). Додавали фенолфталеїн (5 мг) та по краплям додавали 50% водний NaOH (80г, 1,0моль) з охолодженням при 10-25°С, щоб довести рН приблизно до 9, на що вказувала поява рожевого кольору. Потім, щоб погасити рожевий колір, додавали достатню для цього кількість 1N водної соляної кислоти. Отриману суспензію охолоджували до 5°С та фільтрували. Відфільтрований вологий осад промивали водою та сушили до постійної маси при 50°С/6кПа, одержуючи 123г (вихід 80%) зазначеної у заголовку сполуки з чистотою 98%, визначеною за допомогою ВЕРХ, у вигляді твердої речовини, яка плавиться при 147-148°С. 1 H ЯМР (DMSO-d6) δ 5,4 (br s, 2H), 3,97 (s, 3Н), 2,1 (m, 1H), 1,04 (m, 4H). Фільтрат, що залишився, підкисляли соляною кислотою (37ваг.% у воді), щоб довести рН приблизно до 2, та потім концентрували у вакуумі. Одержану суспензію фільтрували, промивали водою та сушили, одержуючи 14г 6-аміно-5-хлор-2циклопропіл-4-піримідинкарбонової кислоти, що не прореагувала, (вихід відновлення 10%). Стадія F2: Інший спосіб одержання метил 6аміно-5-хлор-2-циклопропіл-4-піримідинкарбоксилату У 500мл багато-горлу колбу, постачену барботером азоту, крапельною лійкою, зворотним холодильником та термопарою, поміщали моногідрат 6-аміно-5-хлор-2-циклопропіл-4піримідинкарбонової кислоти (47,8г, 0,206моль), метанол (32г) та диметил карбонат (94,5г, 1,05моль). Додавали концентровану сірчану кислоту (50,0г, 0,500моль) протягом приблизно 30 хвилин з охолодженням, щоб підтримувати температуру нижче 60°С, та потім реакційну суміш нагрівали при 70°С протягом 10год. Одержану суміш охолоджували до 15°С та розбавляли 250мл води. рН реакційної маси збільшували до 5-8 за допомогою додавання приблизно 42,7г (0,534моль) 50ваг.% водного NaOH протягом 30 хвилин з охолодженням, щоб підтримувати температуру в діа 29 пазоні 10-15°С. Одержану суспензію охолоджували до 5°С та фільтрували. Відфільтрований вологий осад промивали водою та сушили до постійної маси при 50°С, одержуючи 43,3г (вихід 93,5%) зазначеної у заголовку сполуки з чистотою 98%, яка плавилася при 147-148°С. Стадія F3: Інший спосіб одержання метил 6аміно-5-хлор-2-циклопропіл-4піримідинкарбоксилату У 200-мл реактор, постачений 10-мл крапельною лійкою, поміщеною в кожух, нижче пальчикового холодильника при -10°С, трубкою для введення азоту та верхньою мішалкою, поміщали трибутиламін (20,4г, 0,11моль) та DMSO (45мл). Суміш перемішували при 25°С, та порціями додавали моногідрат 6-аміно-5-хлор-2-циклопропіл-4піримідинкарбонової кислоти (23,1г, 0,1моль). Реакційну суміш перемішували при 30°С, одночасно бромметан (13,3г, 8мл, 0,14моль) конденсували у крапельній лійці, поміщеній в кожух, та потім його 92171 30 додавали до реакційної суміші протягом 30 хвилин. Суміш перемішували протягом додаткових 3год. та потім додавали протягом приблизно 30 хвилин до реактора, наповненого водою (200мл), при 25°С. Одержану суспензію охолоджували до 5°С та фільтрували. Відфільтрований осад промивали водою (2 30мл) та сушили при 60°С у вакуумній шафі протягом 16год., одержуючи 18,4г (вихід 81%) зазначеної у заголовку сполуки у вигляді не зовсім білої твердої речовини, яка плавиться при 147-148°С. За допомогою даного способу можуть бути одержані наступні сполуки, наведені в Таблицях 14. В Таблиці використовуються наступні скорочення: t означає третинний, i означає ізо, Me означає метил, Et означає етил, Рr означає пропіл, i-Рr означає ізопропіл, с-Рr означає циклопропіл, Вu означає бутил, i-Вu означає ізобутил та S(O)2Me означає метилсульфоніл. 31 Комп’ютерна верстка Т. Чепелева 92171 Підписне 32 Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюMethod for preparation of optionally 2-substituted 1,6-dihydro-6-oxo-4-pyrimidinecarboxylic acids
Автори англійськоюShapiro Rafael
Назва патенту російськоюСпособ получения необязательно 2-замещенных 1,6-дигидро-6-оксо-4-пиримидинкарбоновых кислот
Автори російськоюШапиро Рафаэль
МПК / Мітки
МПК: C07D 239/28, A61K 31/505
Мітки: 2-заміщених, необов'язково, кислот, одержання, спосіб, 1,6-дигідро-6-оксо-4-піримідинкарбонових
Код посилання
<a href="https://ua.patents.su/16-92171-sposib-oderzhannya-neobovyazkovo-2-zamishhenikh-16-digidro-6-okso-4-pirimidinkarbonovikh-kislot.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання необов’язково 2-заміщених 1,6-дигідро-6-оксо-4-піримідинкарбонових кислот</a>
Попередній патент: Лікарський засіб триметазидину у формі матриксної таблетки з пролонгованою дією (варіанти) та спосіб його одержання
Наступний патент: Пристрій для отримання дисперсних мінеральних продуктів
Випадковий патент: Статичний змішувач












