Заміщені 4-феніл-4-(1н-імідазол-2-іл)-піперидинові похідні та їх використання як селективних непептидних дельта-опіоїдних агоністів
Номер патенту: 76224
Опубліковано: 17.07.2006
Автори: Фернандес-Гадеа Франсіско Хавьєр, Леенартс Йозеф Елізабет, Гомес-Санчес Антоніо, Меерт Тео Франс, Янссенс Франс Едуард
Формула / Реферат
1. Сполука формули (І)
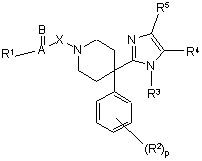 , (I)
, (I)
її фармацевтично прийнятні солі приєднання кислоти чи основи, її стереохімічно ізомерні форми, її таутомерні форми та її N-оксидні форми, у якій:
А=В означає бівалентний радикал з ![]() -зв'язками,
-зв'язками,
Х означає ковалентний зв'язок, -СН2- чи СН2СН2-,
R1 означає гідроген, алкілоксигрупу, алкілкарбонілоксигрупу, Аr-оксигрупу, Het-оксигрупу, Аr-карбонілоксигрупу, Het-карбонілоксигрупу, Аr-алкілоксигрупу, Het-алкілоксигрупу, алкіл, полігалоїдалкіл, алкілоксіалкіл, Аr-алкіл, Het-алкіл, Аr, Het, тіогрупу, алкілтіогрупу, Аr-тіогрупу, Het-тіогрупу чи NR9R10, де R9 та R10 кожний незалежно означає гідроген, алкіл, Аr, Аr-алкіл, Het, Het-алкіл, алкілкарбоніл, Аr-карбоніл, Het-карбоніл чи алкілоксикарбонілалкіл, або А=В та R1 разом утворюють необов'язково заміщений семіароматичний або ароматичний карбоциклічний чи гетероциклічний радикал Het2 чи Het3,
R2 означає гідроксильную групу, алкілоксигрупу, алкілкарбонілоксигрупу, фенілоксигрупу, фенілкарбонілоксигрупу, галоїд, ціаногрупу, алкіл, полігалоїдалкіл, алкілоксіалкіл, форміл, карбоксигрупу, алкілкарбоніл, алкілоксикарбоніл, амінокарбоніл, моно- чи діалкіламінокарбоніл, феніл, нітрогрупу, аміногрупу, моно- чи діалкіламіногрупу, тіогрупу чи алкілтіогрупу,
R3 означає алкіл, Аr, Аr-алкіл, Аr-алкеніл, Het, Het-алкіл чи Het-алкеніл,
R4, R5 кожний незалежно означають гідроген, алкіл, карбоксильну групу,
амінокарбоніл, алкілоксикарбоніл, галоїд чи гідроксіалкіл, р означає ціле число, яке дорівнює нулю, 1, 2 чи 3, алкіл означає лінійний чи розгалужений насичений вуглеводневий радикал, який містить від 1 до 6 атомів карбону, або циклічний насичений вуглеводневий (циклоалкільний) радикал, який містить від 3 до 7 атомів карбону, або циклічний насичений вуглеводневий радикал, який містить від 3 до 7 атомів карбону, приєднаний до лінійного чи розгалуженого насиченого вуглеводневого радикала, який містить від 1 до 6 атомів карбону, причому кожний атом карбону може бути необов'язково заміщений аміногрупою, нітрогрупою, тіогрупою, гідроксильною групою, оксогрупою, ціаногрупою, формілом чи карбоксильною групою, алкеніл означає алкільний радикал, який має один чи кілька подвійних зв'язків, Аr означає гомоциклічне ядро, вибране з групи фенілу та нафтилу, кожний з яких є необов'язково заміщеним одним чи кількома замісниками, причому кожний замісник незалежно вибирають з групи, що включає гідроксильну групу, алкілоксигрупу, фенілоксигрупу, фенілкарбонілоксигрупу, полігалоїдалкілоксигрупу, галоїд, ціаногрупу, алкіл, полігалоїдалкіл, алкілоксіалкіл, форміл, галоїдформіл, карбоксигрупу, алкілкарбоніл, алкілоксикарбоніл, амінокарбоніл, моно- чи діалкіламінокарбоніл, фенілалкіл, феніл, нітрогрупу, аміногрупу, моно- чи діалкіламіногрупу, тіогрупу, алкілтіогрупу чи SO2-CH3,
галоїд означає замісник, вибраний з групи флюору, хлору, брому та йоду, полігалоїдалкіл означає лінійний чи розгалужений насичений вуглеводневий радикал, який містить від 1 до 6 атомів карбону, або циклічний насичений вуглеводневий радикал, який містить від 3 до 7 атомів карбону, у якому один чи кілька атомів карбону є заміщеними одним чи кількома атомами галоїду, Het означає гетероциклічний радикал, вибраний з групи Het1, Het2 та Het3, Het1 означає аліфатичний моноциклічний гетероциклічний радикал, вибраний з групи піролідинілу, діоксолілу, імідазолідинілу, піразолідинілу, піперидинілу, діоксилу, морфолінілу, дитіанілу, тіоморфолінілу, піперазинілу та тетрагідрофуранілу,
Het2 означає семіароматичний моноциклічний гетероциклічний радикал, вибраний з групи 2Н-піролілу, піролінілу, імідазолінілу та піразолінілу,
Het3 означає ароматичний моноциклічний гетероциклічний радикал, вибраний з групи піролілу, піразолілу, імідазолілу, фуранілу, тієнілу, оксазолілу, ізоксазолілу, тіазолілу, ізотіазолілу, піридинілу, піримідинілу, піразинілу, піридазинілу та триазинілу, або ароматичний біциклічний гетероциклічний радикал, вибраний з групи хінолінілу, хіноксалінілу, індолілу, бензімідазолілу, бензоксазолілу, бензізоксазолілу, бензотіазолілу, бензізотіазолілу, бензофуранілу та бензотієнілу, причому кожний моноциклічний та біциклічний гетероциклічний радикал може необов'язково бути заміщеним на атомі карбону та/або гетероатомі галоїдом, гідроксильною групою, алкілоксигрупою, алкілом, Аr, Аr-алкілом чи піридинілом.
2. Сполука за п. 1, яка відрізняється тим, що А=В вибраний з групи С=O, C=N-R6, де R6 означає гідроген чи ціаногрупу, C=S, S=O, SO2 та C=CR7R8, де R7 та R8 кожний незалежно означає гідроген, нітрогрупу чи алкіл.
3. Сполука за будь-яким з пп. 1-2, яка відрізняється тим, що R1 вибраний з групи алкілоксигрупи, Аr-алкілоксигрупи, алкілу, полігалоїдалкілу, алкілоксіалкілу, Аr-алкілу, Het-алкілу, Аr, піперазинілу, піролілу, тіазолілу, піролідинілу та NR9R10, де R9 та R10 кожний незалежно означає гідроген, алкіл, Аr, Аr-алкіл, піридиніл чи алкілоксикарбонілалкіл.
4. Сполука за п. 1, яка відрізняється тим, що А=В та R1 разом утворюють радикал, вибраний з групи Het2 та Het3.
5. Сполука за п. 4, яка відрізняється тим, що А=В та R1 разом утворюють радикал, вибраний з групи бензоксазолілу, тіазолілу, бензотіазолілу, бензімідазолілу та піримідинілу.
6. Сполука за будь-яким з пп. 1-5, яка відрізняється тим, що Х означає ковалентний зв'язок.
7. Сполука за будь-яким з пп. 1-6, яка відрізняється тим, що R2 означає алкілоксигрупу чи галоїд.
8. Сполука за будь-яким з пп. 1-7, яка відрізняється тим, що R3 вибраний з групи фенілалкілу та нафтилу, кожний з яких є незалежно заміщеним щонайменше одним замісником, вибраним з групи галоїду, алкілоксикарбонілу, гідроксильної групи, алкілоксигрупи та діалкіламінокарбонілу.
9. Сполука за п. 1, у якій А=В означає С=O чи SO2, R1 означає алкілоксигрупу, алкілоксіалкіл, Аr чи NR9R10, де R9 та R10 кожний незалежно означає гідроген чи Аr, або А=В та R1 разом утворюють бензоксазолільний радикал, р дорівнює нулю, R3 означає бензил, необов'язково заміщений гідроксильною групою чи алкілоксикарбонілом, і кожний з R4 та R5 означає гідроген.
10. Сполука за п. 1, вибрана з групи:
1-етоксикарбоніл-4-феніл-4-[1-(фенілметил)-1H-імідазол-2-іл]піперидину,
1-пропілоксикарбоніл-4-феніл-4-[1-(фенілметил)-1H-імідазол-2-іл]піперидину,
1-етоксикарбоніл-4-феніл-4-[1-[(4-гідроксифеніл)метил]-1Н-імідазол-2-
іл]піперидину,
1-етоксикарбоніл-4-феніл-4-[1-(1-фенілетил)-1H-імідазол-2-іл]піперидину,
1-ізопропілоксикарбоніл-4-феніл-4-[1-(фенілметил)-1H-імідазол-2-іл]піперидину,
1-етоксикарбоніл-4-феніл-4-[1-[[4-(метоксикарбоніл)феніл]метил]-1H-імідазол-2-
іл]піперидину,
1-бензоїл-4-феніл-4-[1-(фенілметил)-1H-імідазол-2-іл]піперидину,
1-(метоксіацетил)-4-феніл-4-[1-(1-фенілетил)-1H-імідазол-2-іл]піперидину,
4-[[2-(1-бензоїл-4-феніл-4-піперидиніл)-1H-імідазол-1-іл]метил]метилбензоату,
4-[[2-[1-(2-бензоксазоліл)-4-феніл-4-піперидиніл]-1H-імідазол-1-іл]метил]-
метилбензоату,
1-бензоїл-4-феніл-4-[1-(1-фенілетил)-1H-імідазол-2-іл]піперидину,
1-етоксикарбоніл-4-феніл-4-[1-[1-[4-(етоксикарбоніл)феніл]етил]-1H-імідазол-2-
іл]піперидину та
N,4-дифеніл-4-[1-(фенілметил)-1H-імідазол-2-іл]-1-піперидинсульфонаміду.
11. Сполука, яка деградує in vivo з утворенням сполуки за будь-яким з пп. 1-10.
12. Сполука за будь-яким з пп. 1-11, призначена для використання як лікарський засіб.
13. Фармацевтична композиція, яка містить фармацевтично прийнятний носій та, як активний інгредієнт, терапевтично ефективну кількість сполуки за будь-яким з пп. 1-10.
14. Використання сполуки за будь-яким з пп. 1-10 чи фармацевтичної композиції за п. 13 для виробництва лікарського засобу, призначеного для застосування при лікуванні різних больових станів, таких як, зокрема, центрально медійований біль, периферично медійований біль, структурний біль чи біль, асоційований з ушкодженням м'яких тканин, біль, асоційований з прогресуючою хворобою, невропатичний біль та гострий біль, такий як спричинений гострим ушкодженням, травмою чи хірургічною операцією, і хронічний біль, такий як спричинений невропатичними станами, діабетичною периферичною невропатією, постгерпетичною невралгією, тригемінальною невралгією, післяінсультними больовими синдромами, гістаміновим головним болем чи мігренню, артритом, псоріазом, астмою, запальною хворобою кишечнику, розладом респіраторної функції, функціональною діареєю, неульцерогенною диспепсією, нетриманням та синдромом подразненого кишечнику (IBS).
15. Спосіб лікування людини, що страждає від будь-якого зі станів, згаданих у п. 14, який включає введення людині, що потребує такого лікування, терапевтично ефективної кількості сполуки за будь-яким з пп. 1-10 чи фармацевтичної композиції за п. 13.
16. Сполука за будь-яким з пп. 1-10 у ізотопно міченій формі.
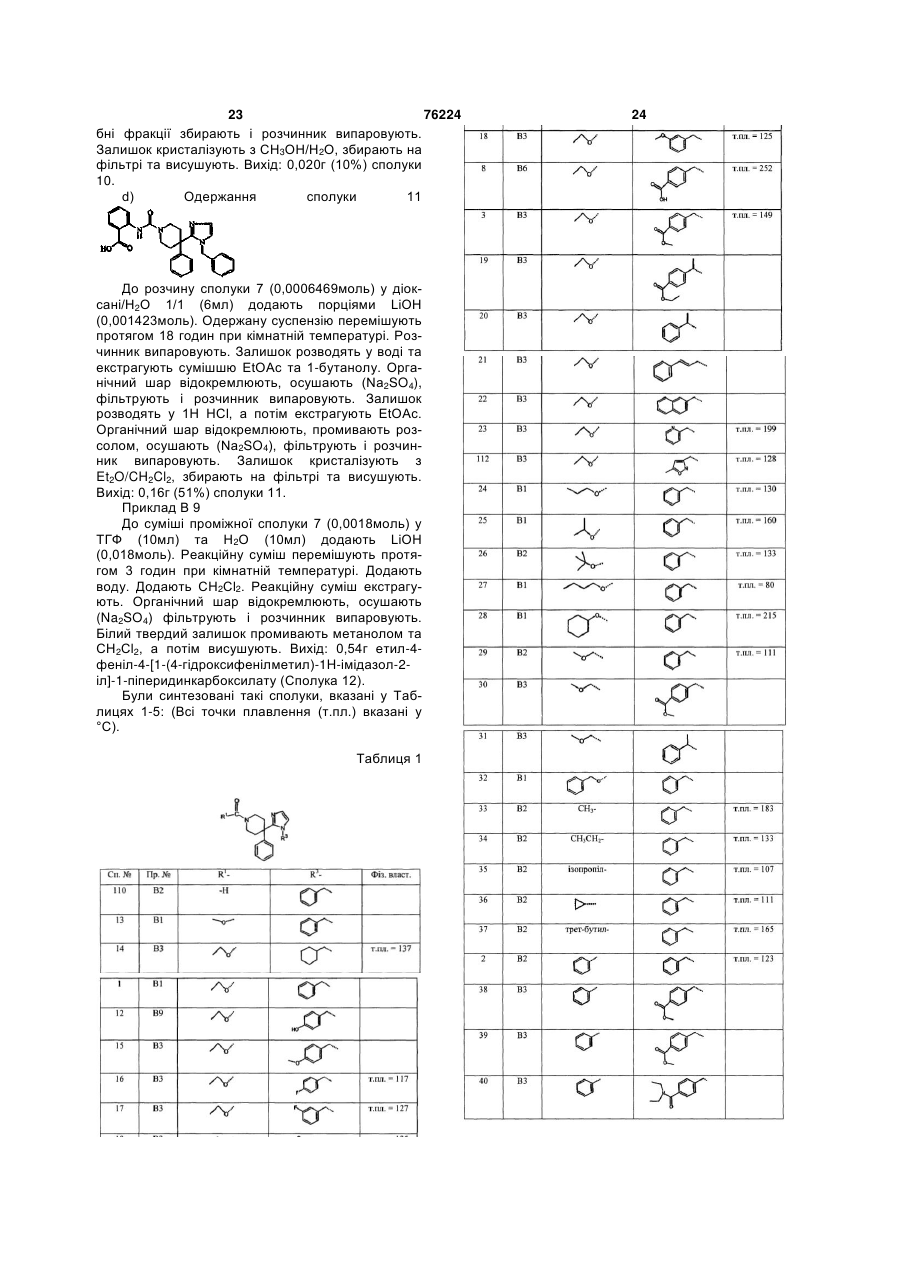
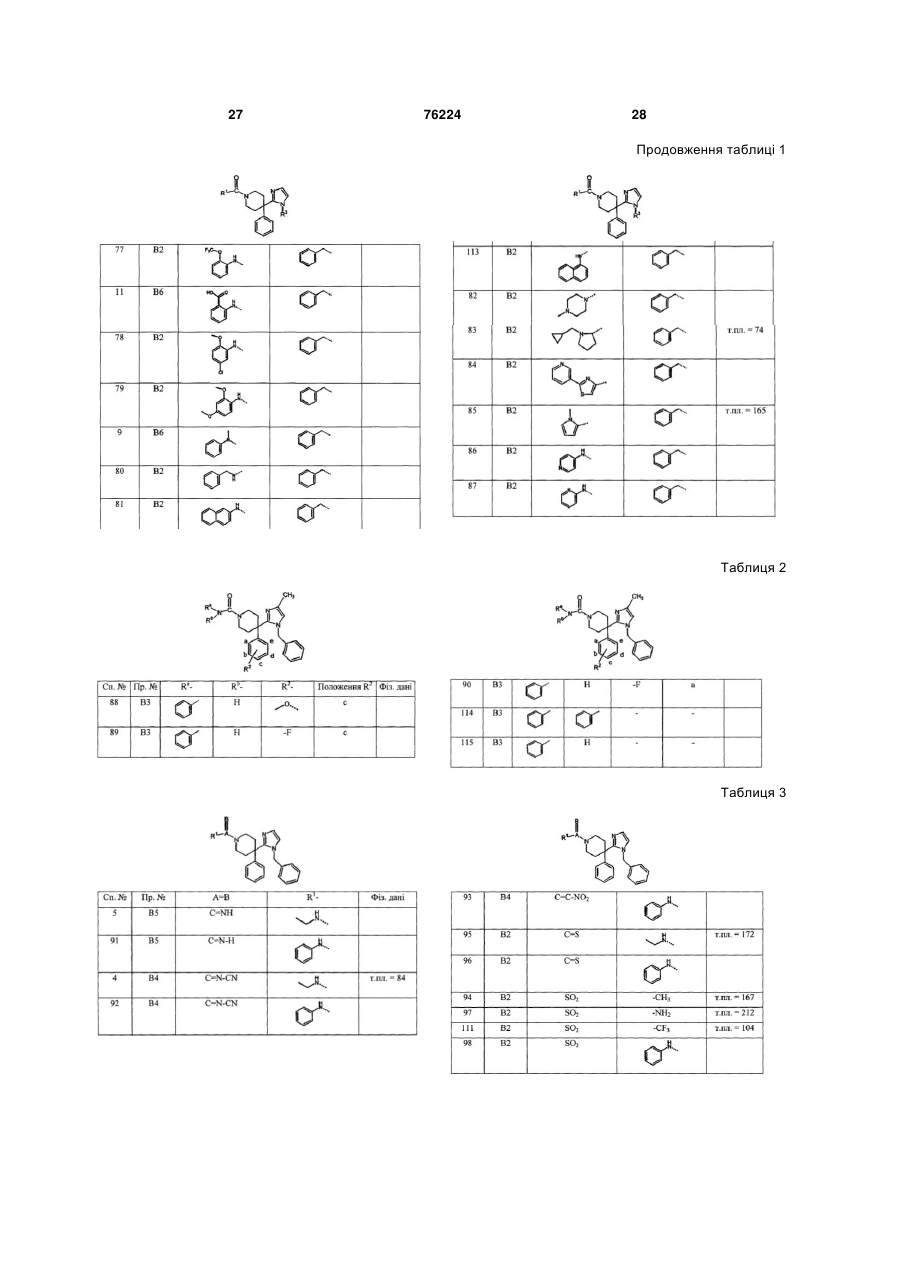
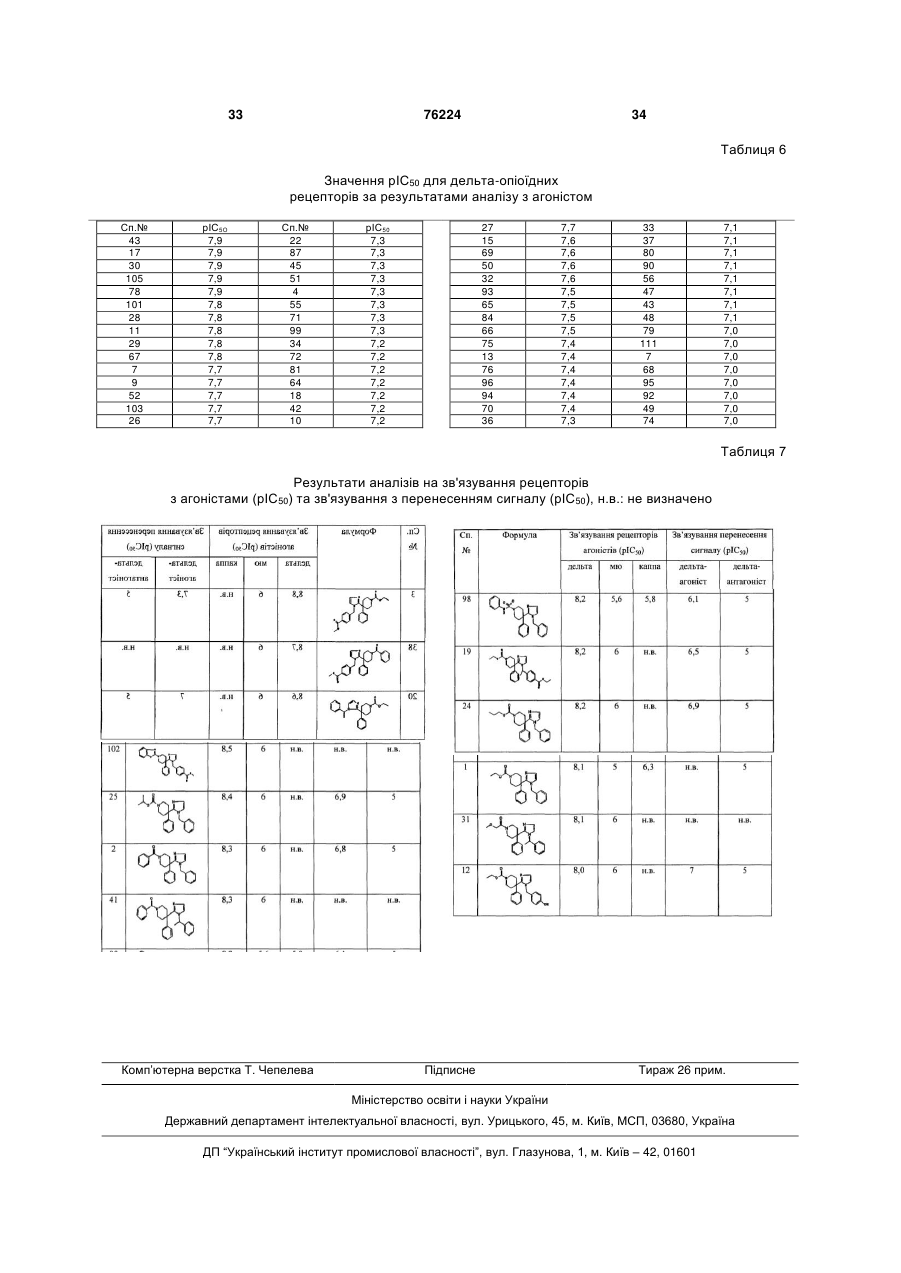
Текст
1. Сполука формули (І) 2 (19) 1 3 76224 4 ний вуглеводневий (циклоалкільний) радикал, який ролілу, тіазолілу, піролідинілу та NR9R10, де R9 та містить від 3 до 7 атомів карбону, або циклічний R10 кожний незалежно означає гідроген, алкіл, Аr, насичений вуглеводневий радикал, який містить Аr-алкіл, піридиніл чи алкілоксикарбонілалкіл. 4. Сполука за п.1, яка відрізняється тим, що А=В від 3 до 7 атомів карбону, приєднаний до лінійного чи розгалуженого насиченого вуглеводневого рата R1 разом утворюють радикал, вибраний з групи 2 3 дикала, який містить від 1 до 6 атомів карбону, Het та Het . 5. Сполука за п.4, яка відрізняється тим, що А=В причому кожний атом карбону може бути необов'язково заміщений аміногрупою, нітрогрупою, тіота R1 разом утворюють радикал, вибраний з групи групою, гідроксильною групою, оксогрупою, ціаногбензоксазолілу, тіазолілу, бензотіазолілу, бензімірупою, формілом чи карбоксильною групою, дазолілу та піримідинілу. 6. Сполука за будь-яким з пп.1-5, яка відрізняєтьалкеніл означає алкільний радикал, який має один ся тим, що Х означає ковалентний зв'язок. чи кілька подвійних зв'язків, Аr означає гомоциклі7. Сполука за будь-яким з пп.1-6, яка відрізняєтьчне ядро, вибране з групи фенілу та нафтилу, кося тим, що R2 означає алкілоксигрупу чи галоїд. жний з яких є необов'язково заміщеним одним чи 8. Сполука за будь-яким з пп.1-7, яка відрізняєтькількома замісниками, причому кожний замісник ся тим, що R3 вибраний з групи фенілалкілу та незалежно вибирають з групи, що включає гідроксильну групу, алкілоксигрупу, фенілоксигрупу, фенафтилу, кожний з яких є незалежно заміщеним нілкарбонілоксигрупу, полігалоїдалкілоксигрупу, щонайменше одним замісником, вибраним з групи галоїд, ціаногрупу, алкіл, полігалоїдалкіл, алкілокгалоїду, алкілоксикарбонілу, гідроксильної групи, сіалкіл, форміл, галоїдформіл, карбоксигрупу, алалкілоксигрупи та діалкіламінокарбонілу. кілкарбоніл, алкілоксикарбоніл, амінокарбоніл, 9. Сполука за п.1, у якій А=В означає С=O чи SO2, моно- чи діалкіламінокарбоніл, фенілалкіл, феніл, R1 означає алкілоксигрупу, алкілоксіалкіл, Аr чи нітрогрупу, аміногрупу, моно- чи діалкіламіногрупу, NR9R10, де R9 та R10 кожний незалежно означає тіогрупу, алкілтіогрупу чи SO2-CH3, гідроген чи Аr, або А=В та R1 разом утворюють галоїд означає замісник, вибраний з групи флюобензоксазолільний радикал, р дорівнює нулю, R3 ру, хлору, брому та йоду, полігалоїдалкіл означає означає бензил, необов'язково заміщений гідроклінійний чи розгалужений насичений вуглеводнесильною групою чи алкілоксикарбонілом, і кожний вий радикал, який містить від 1 до 6 атомів карбоз R4 та R5 означає гідроген. ну, або циклічний насичений вуглеводневий ради10. Сполука за п.1, вибрана з групи: кал, який містить від 3 до 7 атомів карбону, у 1-етоксикарбоніл-4-феніл-4-[1-(фенілметил)-1Hякому один чи кілька атомів карбону є заміщеними імідазол-2-іл]піперидину, одним чи кількома атомами галоїду, Het означає 1-пропілоксикарбоніл-4-феніл-4-[1-(фенілметил)1 гетероциклічний радикал, вибраний з групи Het , 1H-імідазол-2-іл]піперидину, Het2 та Het3, Het1 означає аліфатичний моноциклі1-етоксикарбоніл-4-феніл-4-[1-[(4чний гетероциклічний радикал, вибраний з групи гідроксифеніл)метил]-1Н-імідазол-2піролідинілу, діоксолілу, імідазолідинілу, піразолііл]піперидину, динілу, піперидинілу, діоксилу, морфолінілу, дитіа1-етоксикарбоніл-4-феніл-4-[1-(1-фенілетил)-1Hнілу, тіоморфолінілу, піперазинілу та тетрагідроімідазол-2-іл]піперидину, фуранілу, 1-ізопропілоксикарбоніл-4-феніл-4-[1Het2 означає семіароматичний моноциклічний ге(фенілметил)-1H-імідазол-2-іл]піперидину, тероциклічний радикал, вибраний з групи 2Н1-етоксикарбоніл-4-феніл-4-[1-[[4піролілу, піролінілу, імідазолінілу та піразолінілу, (метоксикарбоніл)феніл]метил]-1H-імідазол-2Het3 означає ароматичний моноциклічний гетероіл]піперидину, циклічний радикал, вибраний з групи піролілу, пі1-бензоїл-4-феніл-4-[1-(фенілметил)-1H-імідазолразолілу, імідазолілу, фуранілу, тієнілу, оксазолі2-іл]піперидину, лу, ізоксазолілу, тіазолілу, ізотіазолілу, піридинілу, 1-(метоксіацетил)-4-феніл-4-[1-(1-фенілетил)-1Hпіримідинілу, піразинілу, піридазинілу та триазиніімідазол-2-іл]піперидину, лу, або ароматичний біциклічний гетероциклічний 4-[[2-(1-бензоїл-4-феніл-4-піперидиніл)-1Hрадикал, вибраний з групи хінолінілу, хіноксалініімідазол-1-іл]метил]метилбензоату, лу, індолілу, бензімідазолілу, бензоксазолілу, бен4-[[2-[1-(2-бензоксазоліл)-4-феніл-4-піперидиніл]зізоксазолілу, бензотіазолілу, бензізотіазолілу, 1H-імідазол-1-іл]метил]бензофуранілу та бензотієнілу, причому кожний метилбензоату, моноциклічний та біциклічний гетероциклічний 1-бензоїл-4-феніл-4-[1-(1-фенілетил)-1H-імідазолрадикал може необов'язково бути заміщеним на 2-іл]піперидину, атомі карбону та/або гетероатомі галоїдом, гідрок1-етоксикарбоніл-4-феніл-4-[1-[1-[4сильною групою, алкілоксигрупою, алкілом, Аr, Аr(етоксикарбоніл)феніл]етил]-1H-імідазол-2алкілом чи піридинілом. іл]піперидину та 2. Сполука за п.1, яка відрізняється тим, що А=В N,4-дифеніл-4-[1-(фенілметил)-1H-імідазол-2-іл]-1вибраний з групи С=O, C=N-R6, де R6 означає гідпіперидинсульфонаміду. 7 8 роген чи ціаногрупу, C=S, S=O, SO2 та C=CR R , 11. Сполука, яка деградує in vivo з утворенням де R7 та R8 кожний незалежно означає гідроген, сполуки за будь-яким з пп.1-10. нітрогрупу чи алкіл. 12. Сполука за будь-яким з пп.1-11, призначена 3. Сполука за будь-яким з пп.1-2, яка відрізняєтьдля використання як лікарський засіб. ся тим, що R1 вибраний з групи алкілоксигрупи, Аr13. Фармацевтична композиція, яка містить фаралкілоксигрупи, алкілу, полігалоїдалкілу, алкілоксімацевтично прийнятний носій та, як активний інгалкілу, Аr-алкілу, Het-алкілу, Аr, піперазинілу, піредієнт, терапевтично ефективну кількість сполуки 5 76224 6 за будь-яким з пп.1-10. сультними больовими синдромами, гістаміновим 14. Використання сполуки за будь-яким з пп.1-10 головним болем чи мігренню, артритом, псоріазом, чи фармацевтичної композиції за п.13 для виробастмою, запальною хворобою кишечнику, розлаництва лікарського засобу, призначеного для задом респіраторної функції, функціональною діарестосування при лікуванні різних больових станів, єю, неульцерогенною диспепсією, нетриманням та таких як, зокрема, центрально медійований біль, синдромом подразненого кишечнику (IBS). периферично медійований біль, структурний біль 15. Спосіб лікування людини, що страждає від чи біль, асоційований з ушкодженням м'яких ткабудь-якого зі станів, згаданих у п.14, який включає нин, біль, асоційований з прогресуючою хворобою, введення людині, що потребує такого лікування, невропатичний біль та гострий біль, такий як спритерапевтично ефективної кількості сполуки за чинений гострим ушкодженням, травмою чи хірурбудь-яким з пп.1-10 чи фармацевтичної композиції гічною операцією, і хронічний біль, такий як сприза п.13. чинений невропатичними станами, діабетичною 16. Сполука за будь-яким з пп.1-10 у ізотопно міпериферичною невропатією, постгерпетичною ченій формі. невралгією, тригемінальною невралгією, післяін Даний винахід стосується нових 4-феніл-4-[1Hімідазол-2-іл]піперидинових похідних, способів їхнього одержання та їхнього використання у медицині, зокрема, як селективних непептидних dопіоїдних агоністів. Наявність щонайменше трьох популяцій опіоїдних рецепторів (загальновідомих як мю (μ), дельта (d) та каппа ( ) рецептори) зараз добре встановлена та документально підтверджена і всі три популяції, по-видимому, присутні у центральній та периферичній нервовій системі багатьох видів тварин, включаючи людину (Lord J.A.H. et al., Nature 1977, 267, 495). Модуляція одного чи кількох субтипів цих опіоїдних рецепторів може викликати різноманітні ефекти, що спостерігаються на тваринних моделях, обумовлюючи унікальний фармакологічний профіль кожного рецептора. Наприклад, dагоністи, по-видимому, виявляють аналгезивний ефект (як спінальний, так і супраспінальний) при різних больових станах у мишей, щурів, гризунів, приматів і навіть у людини (Moulin et al. Pain, 1985, 23, 213), збільшуючи вивільнення гормону росту та інгібуючи вивільнення допаміну, у той час як dантагоністи не мають аналгезивного ефекту та знижують вивільнення гормону росту (Goodman and Gilman, The Pharmacological Basis of Therapeutics, 9th Edition, McGraw-Hill, 1996, 525). Деякі експерименти також дозволяють припустити, що d-анальгетики можуть також не мати звичайних побічних ефектів, асоційованих з активацією μ-та -рецепторів (Galligan et al., J. Pharm. Exp. Ther. 1984, 229, 641). Тваринні моделі також продемонстрували, що агоністи d-опіоїдних рецепторів можуть мати прямий ефект на шлунково-кишковий тракт (наприклад, антидіарейний ефект) та дихальні шляхи (наприклад, стимулювальний ефект на дихальну активність). Крім того, було показано, що агоністи d-опіоїдних рецепторів можуть відігравати синергічну роль у різноманітних фармакологічних ефектах. Дійсно, вони позитивно модулюють центральну антиноцицептивну та протикашльову активність μ-агоністів, приводячи до зниження дозувань та уповільнюючи розвиток небажаних побічних ефектів, асоційованих з цими наркотичними лікарськими засобами. Цікаво, що імуностимулювальна активність деяких агоністів d-опіоїдних рецепторів може виявитися корисною при розробці терапевтичних стратегій лікування імунодефіцитних розладів у людини (Dondio et al. Review: Non-peptide d-opioid agonists and antagonists, Exp. Opin. Ther. Patents, 1997, 10, 1075). З урахуванням великої фармакологічної цінності, існує потреба в агоністах d-опіоїдних рецепторів, що виявляли б селективність у своїй дії як агоністи (не маючи чи маючи слабку антагоністичну дію) та по відношенню до d-рецепторів (не надаючи чи надаючи слабку перевагу μ- чи -субтипам опіоїдних рецепторів). Крім того, такі агоністи dопіоїдних рецепторів не повинні мати пептидної природи, оскільки такі сполуки є нестабільними при введенні системними шляхами. Відомі зараз непептидні агоністи дельтаопіоїдних рецепторів включають індоло- та бензофураноморфінани [US-5354863 (1994) на ім'я Searle & Co, WO-9531464 (1995) на ім'я Astra АВ], октагідроізохіноліни (наприклад, TAN-67 виробництва фірми Toray Inc., [опублікований у JP4275288 (1992) та WO-9710216 (1997)] на ім'я Smithkline Beecham SPA), піперазинові похідні (наприклад, BW373U86 та SNC 80 виробництва фірми The Welcome Foundation, [опубліковані у WO9315062 (1993)]), піролооктагідроізохіноліни ([WO9504734 (1995)] на ім'я Smithkline Beecham SPA), етиламінові похідні ([WO-9622276 (1996)] на ім'я Nippon Shinyaku Co. Ltd.), триазаспіродеканони ([WO 0146192 (2001)] на ім'я Meiji Seika Kaisha Ltd.) та похідні заміщених амінів ([ЕР-864559 (1998)] на ім'я Gruenenthal Gmbh). [WO-9828270 (1998) та WO-9828275 (1998)] на ім'я Astra AB розкривають піперидинові похідні з аналгезивною активністю. Вказані сполуки структурно не є спорідненими зі сполуками за даним винаходом. [ЕР 1038872 А1 (2000)] на ім'я Pfizer Products Inc. розкриває певні 4-феніл-4гетероарилпіперидинові похідні як ліганди опіоїдних рецепторів. Зазначені сполуки структурно відрізняються від сполук за даною заявкою, поміж іншого, природою піперидинільного заміщення нітрогену, у якому відсутнє заміщення бівалентним радикалом з -зв'язками. [У WO 00/37470 (2000)] на ім'я Jansson Pharmaceutica N.V. розкритий у загальних рисах шлях синтезу антигістамінових спіро-сполук з ви 7 76224 8 користанням деяких сполук за винаходом. Однак, клоалкільний) радикал, який містить від 3 до 7 у заявці відомого рівня техніки не наведені конкреатомів карбону; або позначає циклічний насичений тні приклади зазначених сполук, а також немає вуглеводневий радикал, який містить від 3 до 7 ніяких припущень про те, що вони можуть мати атомів карбону, приєднаний до лінійного чи розгавластивості агоністів d-опіоїдних рецепторів. луженого насиченого вуглеводневого радикала, Метою даного винаходу є створення нового який містить від 1 до 6 атомів карбону; причому класу високоселективних агоністів d-опіоїдних рекожний атом карбону може бути необов'язково цепторів на основі піперидинового фрагмента. заміщеним аміногрупою, нітрогрупою, тіогрупою, Іншою метою даного винаходу є створення агонісгідроксильною групою, оксогрупою, ціаногрупою, тів d-опіоїдних рецепторів, корисних як аналгезивні формілом чи карбоксильною групою. Краще, алкіл засоби, що мають зменшені побічні ефекти. Іншою позначає метил, етил, пропіл, ізопропіл, бутил, метою даного винаходу є створення агоністів dтрет-бутил, циклопропіл, циклопентил, циклогекопіоїдних рецепторів, які виявляють активність при сил, циклогексилметил та циклогексилетил. захворюваннях, медійованих d-опіоїдними рецепВ рамках цієї заявки, алкеніл позначає алкільторами. ний радикал як визначено вище, який має один чи Даний винахід стосується нових заміщених 4кілька подвійних зв'язків. Краще, алкеніл позначає феніл-4-[1H-імідазол-2-іл]піперидинових похідних етеніл та пропеніл. загальної формули (І) В рамках цієї заявки, Аr позначає гомоциклічне ядро, вибране з групи фенілу та нафтилу, кожний з яких є необов'язково заміщеним одним чи кількома замісниками, причому кожний замісник неза(І) лежно вибраний з групи, що складається з гідроксильної групи, алкілоксигрупи, алкілкарбонілоксигрупи, фенілоксигрупи, фенілкарбонілоксигрупи, галоїду, ціаногрупи, алкілу, поліїхніх фармацевтично прийнятних солей приєгалоїдалкілу, алкілоксіалкілу, формілу, галоїдфорднання кислоти чи основи, їхніх стереохімічно ізомілу, карбоксигрупи, алкілкарбонілу, мерних форм, їхніх таутомерних форм та їхніх Nалкілоксикарбонілу, амінокарбонілу, моно- чи діалоксидних форм, у яких: кіламінокарбонілу, фенілалкілу, фенілу, нітрогруА=В позначає бівалентний радикал з пи, аміногрупи, моно- чи діалкіламіногрупи, тіогрузв'язками; пи, алкілтіогрупи чи SO2-CH3. Краще, Аr позначає X позначає ковалентний зв'язок, -СН2- чи нафтил чи феніл, кожний з яких є необов'язково СН2СН2-; заміщеним гідроксильною групою, метилоксигру1 R позначає гідроген, алкілоксигрупу, алкілкапою, етилоксигрупою, фенілоксигрупою, тригалоїрбонілоксигрупу, Ar-оксигрупу, Het-оксигрупу, Аrдметилоксигрупою, галоїдом, метилом, трифлюокарбонілоксигрупу, Het-карбонілоксигрупу, Аrрметилом, хлорформілом, карбоксигрупою, алкілоксигрупу, Het-алкілоксигрупу, алкіл, полігаметилоксикарбонілом, етилоксикарбонілом, діетилоїдалкіл, алкілоксіалкіл, Аr-алкіл, Het-алкіл, Аr, ламінокарбонілом, фенілом, нітрогрупою, метилтіHet, тіогрупу, алкілтіогрупу, Аr-тіогрупу, Hetогрупою, трифлюорметилоксигрупою чи SО2-С1-39 10 9 10 тіогрупу чи NR R , де R та R кожний незалежно алкілом. позначають гідроген, алкіл, Аr, Аr-алкіл, Het, HetВ рамках цієї заявки, галоїд позначає замісник, алкіл, Аr-карбоніл, Het-карбоніл чи алкілоксикарвибраний з групи флюору, хлору, брому та йоду, а 1 бонілалкіл; або А=В та R разом утворюють неполігалоїдалкіл позначає лінійний чи розгалужений обов'язково заміщений семіароматичний або аронасичений вуглеводневий радикал, який містить матичний карбоциклічний чи гетероциклічний від 1 до 6 атомів карбону, або циклічний насиче2 3 радикал Het чи Het ; ний вуглеводневий радикал, який містить від 3 до 2 R позначає гідроксильну групу, алкілоксигру7 атомів карбону, у якому один чи кілька атомів пу, алкілкарбонілоксигрупу, фенілоксигрупою, фекарбону є заміщеними одним чи кількома атомами нілкарбонілоксигрупу, галоїд, ціаногрупу, алкіл, галоїду. Краще, галоїд позначає бром, флюор чи полігалоїдалкіл, алкілоксіалкіл, форміл, карбоксигхлор, а полігалоїдалкіл, краще, позначає трифлюрупу, алкілкарбоніл, алкілоксикарбоніл, амінокарорметил. боніл, моно- чи діалкіламінокарбоніл, феніл, нітроВ рамках цієї заявки, Het позначає гетероцикгрупу, аміногрупу, моно- чи діалкіламіногрупу, лічний радикал, вибраний з групи Het1, Het2 та тіогрупу чи алкілтіогрупу; Het3. Het1 позначає аліфатичний моноциклічний R3 позначає алкіл, Аr, Аr-алкіл, Ar-алкеніл, Аrгетероциклічний радикал, вибраний з групи піролікарбоніл, Het, Het-алкіл, Het-алкеніл чи Hetдинілу, діоксолілу, імідазолідинілу, піразолідинілу, карбоніл; піперидинілу, діоксилу, морфолінілу, дитіанілу, 4 5 R , R кожний незалежно позначають гідроген, тіоморфолінілу, піперазинілу та тетрагідрофурилу. алкіл, карбоксигрупу, амінокарбоніл, алкілоксикарHet2 позначає семіароматичний моноциклічний боніл, галоїд чи гідроксіалкіл; гетероциклічний радикал, вибраний з групи 2Нp позначає ціле число, яке дорівнює нулю, 1, 2 піролілу, піролінілу, імідазолінілу та піразолінілу. чи 3. Het3 позначає ароматичний моноциклічний гетеВ рамках цієї заявки, алкіл позначає лінійний роциклічний радикал, вибраний з групи піролілу, чи розгалужений насичений вуглеводневий радипіразолілу, імідазолілу, фурилу, тієнілу, оксазолікал, який містить від 1 до 6 атомів карбону; або лу, ізоксазолілу, тіазолілу, ізотіазолілу, піридинілу, позначає циклічний насичений вуглеводневий (ципіримідинілу, піразинілу, піридазинілу чи триазині 9 76224 10 лу; або ароматичний біциклічний гетероциклічний ізомерні форми, їхні таутомерні форми та їхні Nрадикал, вибраний з групи хінолінілу, хіноксалініоксидні форми, у яких А=В позначає С=О чи SO2, лу, індолілу, бензімідазолілу, бензоксазолілу, бенR1 позначає алкілоксигрупу, алкілоксіалкіл, Аr чи зізоксазолілу, бензотіазолілу, бензізотіазолілу, NR9R10, де R9 та R10 кожний незалежно позначабензофуранілу та бензотієнілу; причому кожний ють гідроген чи Аr; або А=В та R1 разом утворюмоноциклічний та біциклічний гетероциклічний ють бензоксазолільний радикал; p дорівнює нулю, радикал може необов'язково бути заміщеним на R3 позначає бензил, необов'язково заміщений гідатомі карбону та/або гетероатомі галоїдом, гідрокроксильною групою, алкілом чи алкілоксикарбонісильною групою, алкілоксигрупою, алкілом, Аr, Arлом, і кожний з R4 та R5 позначає гідроген. алкілом чи піридинілом. Більш конкретно, найкращими сполуками є таЦікавою групою сполук є такі сполуки формули кі: (І), їхні фармацевтично прийнятні солі приєднання 1-етоксикарбоніл-4-феніл-4-[1-(фенілметил)кислоти чи основи, їхні стереохімічно ізомерні фо1H-імідазол-2-іл]піперидин; рми, їхні таутомерні форми та їхні N-оксидні фор1-пропілоксикарбоніл-4-феніл-4-[1ми, у яких А=В вибраний з групи С=О, C=N-R6, де (фенілметил)-1H-імідазол-2-іл]піперидин; R6 позначає гідроген чи ціаногрупу, C=S, S=O, SO2 1-етоксикарбоніл-4-феніл-4-[1-[(4та OCR7R8, де R7 та Rs кожний незалежно познагідроксифеніл)метил]-1H-імідазол-2-іл]піперидин; чають гідроген, нітрогрупу чи алкіл. 1-етоксикарбоніл-4-феніл-4-[1-(1-фенілетил)Іншою цікавою групою сполук є такі сполуки 1H-імідазол-2-іл]піперидин; формули (І), їхні фармацевтично прийнятні солі 1-ізопропілоксикарбоніл-4-феніл-4-[1приєднання кислоти чи основи, їхні стереохімічно (фенілметил)-1H-імідазол-2-іл]піперидин; ізомерні форми, їхні таутомерні форми та їхні N1-етоксикарбоніл-4-феніл-4-[1-[[4оксидні форми, у яких R1 вибраний з групи, що (метоксикарбоніл)феніл]метил]-1H-імідазол-2складається з алкілоксигрупи, Ar-алкілоксигрупи, іл]піперидин; алкілу, полігалоїдалкілу, алкілоксигрупи, алкілу, 1-бензоїл-4-феніл-4-[1-(фенілметил)-1HАr-алкілу, Het-алкілу, Аr, піперазинілу, піролілу, імідазол-2-іл]піперидин; тіазолілу, піролідинілу та NR9R10, де R9 та R10 кож1-(метоксіацетил)-4-феніл-4-[1-(1-фенілетил)ний незалежно позначають гідроген, алкіл, Аr, Ar1H-імідазол-2-іл]піперидин; алкіл, піридиніл чи алкілоксикарбонілалкіл. 4-[[2-(1-бензоїл-4-феніл-4-піперидиніл)-1HІншою цікавою групою сполук є такі сполуки імідазол-1-іл]метил]метилбензоат; формули (І), їхні фармацевтично прийнятні солі 4-[[2-[1-(2-бензоксазоліл)-4-феніл-4приєднання кислоти чи основи, їхні стереохімічно піперидиніл]-1H-імідазол-1-іл]метил]ізомерні форми, їхні таутомерні форми та їхні Nметилбензоат; оксидні форми, у яких А=В та R1 разом утворюють 1-бензоїл-4-феніл-4-[1-(1-фенілетил)-1Hрадикал, вибраний з групи Het2 та Het3. Ще краще, імідазол-2-іл]піперидин; А=В та R разом утворюють радикал, вибраний з 1-етоксикарбоніл-4-феніл-4-[1-[1-[4групи бензоксазолілу, тіазолілу, бензотіазолілу, (етоксикарбоніл)феніл]етил]-1H-імідазол-2-іл]бензімідазолілу та піримідинілу. піперидин та Ще іншою цікавою групою сполук є такі сполуN,4-дифенш-4-[1-(фенілметил)-1H-імідазол-2ки формули (І), їхні фармацевтично прийнятні солі іл]-1-піперидинсульфонамід. приєднання кислоти чи основи, їхні стереохімічно Фармацевтично прийнятні солі приєднання киізомерні форми, їхні таутомерні форми та їхні Nслот визначені тут як такі, що включають терапевоксидні форми, у яких X позначає ковалентний тично активні нетоксичні сольові форми приєднанзв'язок чи фрагмент -СН2-. Краще, X позначає коня кислоти, які можуть бути утворені сполуками валентний зв'язок. формули (І). Вказані солі приєднання кислот моЩе іншою цікавою групою сполук є такі сполужуть бути одержані шляхом обробки основної фоки формули (І), їхні фармацевтично прийнятні солі рми сполук формули (І) відповідною кислотою, приєднання кислоти чи основи, їхні стереохімічно наприклад, неорганічними кислотами, наприклад, ізомерні форми, їхні таутомерні форми та їхні Nгалоїдводневою кислотою, зокрема, хлористоводоксидні форми, у яких R2 позначає алкілоксигрупу невою кислотою, бромистоводневою кислотою, чи галоїд. сірчаною кислотою, азотною кислотою та фосфоЩе іншою цікавою групою сполук є такі сполурною кислотою; органічними кислотами, наприки формули (І), їхні фармацевтично прийнятні солі клад, оцтовою кислотою, оксіоцтовою кислотою, приєднання кислоти чи основи, їхні стереохімічно пропіоновою кислотою, молочною кислотою, піроізомерні форми, їхні таутомерні форми та їхні Nвиноградною кислотою, щавлевою кислотою, маоксидні форми, у яких R3 вибраний з групи фенілалоновою кислотою, бурштиновою кислотою, малелкілу та нафтилу, кожний з яких є незалежно заїновою кислотою, фумаровою кислотою, яблучною міщеним щонайменше одним замісником, вибракислотою, винною кислотою, лимонною кислотою, ним з групи галоїду, алкілоксикарбонілу, мигдалевою кислотою, метансульфоновою кислогідроксильної групи, алкілоксигрупи та діалкіламітою, етансульфоновою кислотою, бензолсульфонокарбонілу. новою кислотою, п-толуолсульфоновою кислотою, Якщо R3 позначає алкіл, то алкіл, краще, є цицикламовою кислотою, саліциловою кислотою, пклогексилметилом. аміносаліциловою кислотою та памоєвою кислоЩе іншою цікавою групою сполук є такі сполутою. ки формули (І), їхні фармацевтично прийнятні солі Сполуки формули (І), які містять кислотні проприєднання кислоти чи основи, їхні стереохімічно тони, можуть також бути перетворені на їхні тера 11 76224 12 певтично активні нетоксичні сольові форми приєдгенний центр завдяки хіральному заміснику R1, R2, нання основ шляхом обробки відповідними органіR3, R4 чи R5. чними та неорганічними основами. Відповідні осТаутомерні форми сполук формули (І) мають новні сольові форми включають, наприклад, включати такі сполуки формули (І), у яких, наприамонієві солі, солі лужних та лужноземельних меклад, енольна група перетворюється на кето-групу талів, зокрема, солі літію, натрію, калію, магнію та (кето-енольний таутомеризм). кальцію, солі з органічними основами, наприклад, N-Оксидні форми сполук формули (І) мають бензатином, N-метил-D-глюкаміном, гібрамінові включати такі сполуки формули (І), у яких один чи солі та солі з амінокислотами, наприклад, аргінікілька атомів нітрогену окиснені до так званого Nном та лізином. оксиду, зокрема, такі N-оксиди, у яких окисненим є Навпаки, зазначені сольові форми приєднання нітроген піперидинільного фрагмента та/або імідакислоти чи основи можуть бути перетворені на золільного фрагмента. вільні форми шляхом обробки відповідною осноСполуки формули (І), одержані описаними нивою чи кислотою. жче методами, можуть бути синтезовані у формі Термін сіль приєднання в тому розумінні, що рацемічної суміші енантіомерів, які можуть бути використовується в рамках цієї заявки, включає розділені за допомогою відомих фахівцям методик також сольвати, які можуть утворювати сполуки розділення. Рацемічні сполуки формули (І) можуть формули (І), а також їхні солі. Такими сольватами бути перетворені на відповідні діастереомерні соє, наприклад, гідрати та алкоголяти. льові форми шляхом проведення реакції з придатТермін "стереохімічно ізомерні форми" у тому ною хіральною кислотою. Вказані діастереомерні значенні, що використовується тут, визначає усі сольові форми згодом розділяють, наприклад, можливі ізомерні форми, які можуть мати сполуки шляхом селективної чи фракційної кристалізації, і формули (І). Якщо не вказано чи зазначено інше, енантіомери вивільняють з них за допомогою лухімічна назва сполуки позначає суміш усіх можлигів. Альтернативний спосіб розділення енантіомевих стереохімічно ізомерних форм, причому вкарних форм сполук формули (І) включає рідинну зана суміш містить всі діастереомери та енантіохроматографію із застосуванням хіральної нерумери базової молекулярної структури. хомої фази. Вказані чисті стереохімічно ізомерні Конкретніше, стереогенні центри можуть мати Rформи можуть бути також одержані з відповідних чи S-конфігурацію; замісники на бівалентних цикчистих стереохімічно ізомерних форм відповідних лічних (частково) насичених радикалах можуть вихідних матеріалів, за умови, що реакція прохомати цис- чи транс-конфігурацію. Стереохімічно дить стереоспецифічно. Якщо потрібний конкретізомерні форми сполук формули (І) мають розгляний стереоізомер, то вказану сполуку краще синдатися як такі, що беззаперечно входять до обсягу тезують з використанням стереоспецифічних даного винаходу. методів. Ці методи краще використовують енантіЗгідно номенклатурним правилам CAS, якщо в омерно чисті вихідні матеріали. молекулі присутні два стереогенні центри з відоВинахід також включає похідні сполуки (які мою абсолютною конфігурацією, то дескриптором звичайно називають "проліками") фармакологічноR чи S позначають (на основі правила черговості активних сполук за винаходом, що розкладаються Кана-Інголда-Прелога) хіральний центр з найin vivo з утворенням сполук за винаходом. Проліки меншим порядковим номером, який є опорним звичайно (але не завжди) виявляють нижчу активцентром. Конфігурація другого стереогенного ність по відношенню до цільового рецептора, ніж центра вказується за допомогою відносних десполуки, до яких вони деградують. Проліки є особскрипторів [R*,R*] чи [R*S*], де R* завжди визначаливо корисними у тих випадках, коли потрібна ється як опорний центр, і [R*,R*] позначає центри з сполука має хімічні чи фізичні властивості, що рооднаковою хіральністю, a [R*,S*] позначає центри блять її введення складним чи неефективним. з різною хіральністю. Наприклад, якщо хіральний Наприклад, бажана сполука може бути малорозцентр з найменшим порядковим номером має чинною, вона може погано транспортуватися крізь конфігурацію S, а другий центр - R, то стереодескепітелій слизової, або вона може мати небажано риптор буде позначатися S-[R*,S*]. Якщо викорискороткий період напіввиведення з плазми. Додаткове обговорення проліків можна знайти [у Stella, товуються позначення " " та " ": положення старV.J. et al., "Prodrugs", Drug Deliveiy Systems, 1985, шого замісника на асиметричному атомі карбону у pp.112-176, та Drugs, 1985, 29, pp.455-473]. кільцевій системі, що має меншій номер кільця, Форми проліків фармакологічно-активних спозавжди довільно визначається як положення " " лук за винаходом є загалом сполуками формули середньої площі, утворюваної кільцевою систе(І), їхніми фармацевтично прийнятними солями мою. Положення старшого замісника на другому приєднання кислоти чи основи, їхніми стереохімічасиметричному атомі карбону у кільцевій системі но ізомерними формами, їхніми таутомерними по відношенню до положення старшого замісника формами та їхніми N-оксидними формами, що на опорному атомі позначається " ", якщо він знамають етерифіковану чи амідовану кислотну груходиться з того ж самого боку середньої площі, пу. Такі етерифіковані кислотні групи включають утворюваної кільцевою системою, або "β", якщо групи формули –COORx, де Rx позначає С1-6-алкіл, він знаходиться з іншого боку середньої площі, феніл, бензил чи одну з таких груп: утворюваної кільцевою системою. Ми відзначаємо, що заміщений атом карбону у положенні 4 піперидинільного фрагмента є ахіральним атомом; тому сполуки формули (І) можуть мати у своїй структурі щонайменше один стереоАмідовані групи включають групи формули 13 76224 14 CONRyRz, де Ry позначає Н, С1-6-алкіл, феніл чи активний інгредієнт, терапевтично ефективну кільбензил, і Rz позначає -ОН, Н, С1-6-алкіл, феніл чи кість сполуки за винаходом. Сполуки за винаходом бензил. можуть бути введені в композиції для виготовленСполуки за винаходом, які мають аміногрупу, ня різних фармацевтичних форм, призначених для можуть бути дериватизовані кетоном чи альдегівведення. Як відповідні композиції можна перелідом, таким як формальдегід, з утворенням основи чити всі композиції, що звичайно використовуютьМанніха. Така основа у водному розчині гідролізуся для системного введення лікарських засобів. ється за реакцією першого порядку. Для виготовлення фармацевтичних композицій за Несподівано було виявлено, що сполуки за даним винаходом, ефективну кількість конкретної винаходом є придатними для застосування у тесполуки, необов'язково, у формі солі приєднання рапії, особливо, для лікування різних больових кислоти, узятої як активний інгредієнт, поєднують з станів, таких як, зокрема, центрально-медійований утворенням однорідної суміші з фармацевтично біль, периферично медійований біль, структурний прийнятним носієм, який може мати різноманітні біль чи біль, асоційований з ушкодженням м'яких форми у залежності від форми препарату, бажаної тканин, біль, асоційований з прогресуючою хвородля введення. Бажано, такі фармацевтичні компобою, невропатичний біль та гострий біль, зиції мають вигляд дозованих лікарських форм, такий як спричинений гострим ушкодженням, придатних, зокрема, для введення шляхом парентравмою чи хірургічною операцією, і хронічний теральної ін'єкції чи інфузії. Наприклад, для вигобіль, такий як спричинений невропатичними статовлення композицій може бути використане будьнами, діабетичною периферичною невропатією, яке звичайне фармацевтичне середовище. Для постгерпетичною невралгією, тригемінальною непарентеральної композиції, носій буде звичайно вралгією, післяінсультними больовими синдромавключати, принаймні більшою частиною, стерильми та гістаміновим головним болем чи мігренню. ну воду, хоч можуть бути додані інші інгредієнти, Сполуки за винаходом можуть бути також занаприклад, для поліпшення розчинності. Можуть стосовані для лікування артриту, псоріазу, астми, бути одержані, наприклад, розчини для ін'єкцій, у запальної хвороби кишечнику, розладів респіратояких носій включає сольовий розчин, розчин глюрної функції, функціональної діареї, неульцерокози чи суміш сольового та глюкозного розчинів. генної диспепсії та нетримання. Таке застосування Можуть бути також виготовлені суспензії для ін'єкбуло також документоване [у WO/9852929] (Pfizer цій, у яких можуть бути використані відповідні рідкі Ltd., 1998). носії, суспендувальні агенти і т.п.Передбачаються Присутність дельта-опіоїдних рецепторів у також препарати у твердій формі, які незабаром ободовій кишці людини була також продемонстроперед використанням мають бути перетворені на вана дослідженнями зв'язування радіолігандів та препарати у рідкій формі. радіоавтографічними дослідженнями. Було визнаУ залежності від способу введення, фармацечено, що найбільша щільність зв'язування (80втична композиція, краще, включає від 0,05 до 90%) відноситься до нейронів м'язово-кишкового 99% мас, ще краще, від 0,1 до 70% мас, активного сплетіння, розташованого між круглими та поінгредієнта, і від 1 до 99,95% мас, ще краще, від 30 довжніми шарами гладких м'язів, причому шари до 99,9% мас, фармацевтично прийнятного носія, гладких м'язів мають низьку щільність розташоваде всі процентні частки вказані у розрахунку на них на них рецепторів. У функціональних дослікомпозицію в цілому. дженнях, дельта-опіоїдні агоністи мали здатність Фармацевтична композиція може додатково інгібувати як холінергічну, так і нехолінергічну збумістити різні інші інгредієнти, відомі фахівцям, наджувальну нейротрансмісію у ободовій кишці люприклад, стабілізатор, буферний агент, емульгудини. На основі цих спостережень можна очікувавальний агент, агент регулювання в'язкості, повети, що агоністи дельта-опіоїдних рецепторів рхнево-активну речовину чи консервант. будуть інгібувати рухливість ободової кишки у люДалі, даний винахід також стосується викорисдини. Було також показано, що селективний дельтання сполуки формули (І), її фармацевтично прита-опіоїдний агоніст UK-321130 периферичної дії йнятних солей приєднання кислоти чи основи, її виявляє сильне доза-зв'язане інгібування рухлистереохімічно ізомерних форм, її таутомерних вості ободової кишки у преклінічних моделях. Тому форм та її N-оксидних форм, а також будь-якої з її вважається, що сполуки за даним винаходом є вищезгаданих фармацевтичних композицій для також придатними для лікування синдрому подравиробництва лікарського засобу для лікування зненого кишечнику (IBS). різних больових станів, таких як, зокрема, центраТаким чином, даний винахід стосується сполульно медійований біль, периферично медійований ки формули (І), визначеної вище, її фармацевтичбіль, структурний біль чи біль, асоційований з но прийнятних солей приєднання кислоти чи осноушкодженням м'яких тканин, біль, асоційований з ви, її стереохімічно ізомерних форм, її прогресуючою хворобою, невропатичний біль та таутомерних форм та її N-оксидних форм, признагострий біль, такий як спричинений гострим ушкоченої для використання як лікарський засіб. дженням, травмою чи хірургічною операцією, і Дослідження in vitro рецепторів та трансдукції хронічний біль, такий як спричинений невропатичсигналів нейротрансміттерами можуть бути виконими станами, діабетичною периферичною неврористані для оцінки агоністичної активності дельта-, патією, постгерпетичною невралгією, тригемінальмю- та каппа-опіоїдних рецепторів, як буде описаною невралгією, післяінсультними больовими но далі в цій заявці. синдромами, гістаміновим головним болем чи мігВинахід також стосується композиції, яка ренню, артритом, псоріазом, астмою, запальною включає фармацевтично прийнятний носій та, як хворобою кишечнику, розладом респіраторної фу 15 76224 16 нкції, функціональною діареєю, неульцерогенною Реакція (f) проводиться у придатному розчиндиспепсією, нетриманням та синдромом подразнику, такому як дихлорметан, у присутності приданеного кишечнику (IBS). тної основи, такої як триетиламін, та при кімнатній Отже, в іншому аспекті винахід пропонує спотемпературі протягом приблизно від 30 до 120 сіб лікування людини, що страждає від будь-якого хвилин. з вищезгаданих станів, який включає введення Реакція (g) проводиться у придатному розчинособі, що потребує такого лікування, терапевтично нику, такому як ацетонітрил, при кипінні зі зворотефективної кількості сполуки чи фармацевтичної ним холодильником протягом 24 годин. композиції за винаходом. Реакція (h) проводиться в різних умовах, у заСполуки за даним винаходом в ізотопно мічележності від R1; наприклад, якщо R1=CF3, то реакній формі є придатними для використання як діагція проводиться у присутності триетиламіну у дихностичний агент. Таким чином, даний винахід талорметані при -78°С протягом 1 години. For кож стосується цих ізотопно мічених сполук, а R1=NH2, реакція проводиться у діоксані протягом також діагностичного способу з використанням 12 годин при температурі кипіння зі зворотним ізотопно мічених сполук за даним винаходом. холодильником. Для R1=СН3, реакція проводиться Сполуки за винаходом можуть загалом бути у дихлорметані при кімнатній температурі протяодержані шляхом проведення послідовних стадій, гом З годин у присутності триетиламіну. кожна з яких є відомою фахівцям в даній області. Реакція (і) проводиться у придатному розчинЗокрема, сполуки формули (I-а) можуть бути оденику, такому як ізопропанол, при температурі киржані шляхом проведення реакції проміжної спопіння зі зворотним холодильником протягом 12-36 луки формули (II) у відповідності до схеми реакції годин. (1), причому реакція проводиться у придатному Реакція (j) проводиться у придатному розчинінертному щодо реакції розчиннику, такому як тонику, такому як ацетонітрил, при температурі килуол, у присутності придатної основи, такої як трипіння зі зворотним холодильником протягом 24 етиламін. У схемі реакції (1), усі змінні мають знагодин. чення, визначені у формулі (І), a W1 разом з Схема 2 приєднаним до нього фрагментом дорівнює R1; прикладами W1 є алкіл, Аr чи Het. Прикладом W1OC(=O)Cl є хлорформіат. Схема 1 Сполуки формул (I-а), (І-b), (I-е), (I-d), (I-е), (I-f), (I-g) та (I-h) можуть бути одержані також шляхом проведення реакції проміжної сполуки формули (III) за будь-якою з реакцій, показаних на схемі реакції (2). У зазначених реакціях, всі змінні мають значення, визначені у формулі (І), a W1 разом з приєднаним до нього фрагментом дорівнює R1; прикладами W1 є алкіл, Аr чи Het. Реакція (а) проводиться у придатному розчиннику,такому як дихлоретан, та з використанням ВОС2О. Реакція зручно проводиться протягом кількох годин при кипінні зі зворотним холодильником. Реакція (b) проводиться у придатному розчиннику, такому як ТГФ. Реакція зручно проводиться протягом від однієї до кількох годин при кімнатній температурі. Реакція (с) проводиться у придатному розчиннику, такому як дихлорметан, у присутності придатної основи, такої як Et3N, при кімнатній температурі протягом однієї години. Реакція (d) проводиться у придатному розчиннику, такому як ТГФ чи ДМФ, при кімнатній температурі протягом кількох годин, причому використання основи непотрібне. Реакція (e) проводиться при кипінні зі зворотним холодильником в ацетоні чи ДМФ у присутності придатної основи, такої як карбонат калію, і може бути зручно проведена при 80°С. 17 76224 18 Сполуки формули (I-c) можуть бути також одещеного імідазолільного фрагмента. ржані шляхом проведення реакції проміжної споПроміжні сполуки формули (III) можуть бути луки формули (IV) з галогенідом. У вказаній реакодержані зі сполук формули (l-е) шляхом селектиції, всі змінні мають значення, визначені у формулі вного відновлення алкілоксикарбонільної групи (І). Реакція проводиться з основою, такою як NaH піперидинільного фрагмента у відповідності до (60% у мінеральному маслі) та у інертному щодо такої реакції: реакції розчиннику, такому як ДМФ чи ТГФ. Вихідний матеріал та проміжні сполуки формул (II), (III) та (IV) - це сполуки, які є комерційно доступними або можуть бути одержані у відповідності до методик проведення реакцій, загальновідомих в даній області техніки. Проміжні сполуки формули (II) можуть бути одержані у відповідності до наведеної нижче схеми реакції (4), де всі змінні мають значення, визначені у формулі (І): Схема 4 Схема реакції 4 включає стадію (а), на якій проводять реакцію ацилхлориду зображеного на схемі типу із заміщеним первинним аміном, наприклад, бензиламіном, у присутності придатної основи, такої як Et3N, та у придатному інертному щодо реакції розчиннику, такому як дихлорметан. Реакція може бути зручно проведена при кімнатній температурі. На наступній стадії (b) продукт приєднання, утворений на стадії (а), кип'ятять зі зворотним холодильником у SOCl2, після чого проводять реакцію одержаного продукту з відповідно заміщеним 2,2-диметоксіетиламіном у інертному щодо реакції розчиннику, такому як ДМФ, наприклад, при кімнатній температурі (стадія с). На стадії (d) циклізують продукт приєднання, одержаний на стадії (с), у вуглеводні (НС) з утворенням замі Реакція проводиться у присутності придатної основи, такої як КОН, у придатному інертному щодо реакції розчиннику, такому як 2-пропанол, та при температурі кипіння зі зворотним холодильником. Проміжні сполуки формули (IV) можуть бути одержані шляхом гідрування сполук формули (l-е) у відповідності до такої реакції: де всі змінні мають значення, вказані для формули (І). Реакція проводиться у присутності каталізатора, такого як Pd/C (10%) у метанолі при помірно підвищеній температурі. Зрозуміло, що у наведених вище та нижче реакціях продукти реакції можуть бути виділені з реакційного середовища і, якщо треба, далі очищені методами, загальновідомими фахівцям в цій області техніки, такими як екстракція, кристалізація та хроматографія. Далі, зрозуміло, що продукти реакції, які існують у більш ніж одній енантіомерній формі, можуть бути виділені з їхньої суміші відомими методами, зокрема, препаративною хроматографією, такою як препаративна ВЕРХ. Наведені далі приклади ілюструють даний винахід, не обмежуючи його. Експериментальна частина Для деяких сполук не було експериментально визначено абсолютну стереохімічну конфігурацію стереогенного атома (атомів) карбону, що входять до їхнього складу. У цих випадках стереохімічно ізомерну форму, яку було виділено першою, позначають "А", а другу - "В", без подальшого посилання на фактичну стереохімічну конфігурацію. Однак, вказані ізомерні форми "А" та "В" можуть бути однозначно охарактеризовані фахівцем в цій області техники за допомогою відомих в цій області техніки методів, таких як, наприклад, рентгенівська дифракція. Методика виділення детально описана нижче. Тут та надалі, "ДМФ" позначає Ν,Νдиметилформамід, "ТГФ" позначає тетрагідрофуран, і "DIPE" позначає простий діізопропіловий ефір. А. Одержання проміжних сполук Приклад А1 1-Метил-4-феніл-4-піперидинкарбонілхлорид 19 76224 20 (0,49моль) додають порціями при кімнатній темпедодають по краплях до розчину NaH, 60% у мінературі при перемішуванні до суміші бензолметаральному маслі (0,004моль), у ТГФ (10мл), перенаміну (0,49моль) та Ν,Ν-діетилетанаміну мішуваного при кімнатній температурі. Суміш пе(1,223моль) у СН2Сl2 (2500мл). Суміш перемішуремішують протягом однієї години при кімнатній ють при кімнатній температурі протягом 1 години. температурі. Потім додають по краплях розчин 4Додають K2СО3 (150мг) та Н2О. Суміш перемішу(ацетилокси)бензолметанолу (0,004моль) у ТГФ і ють та розділяють на шари. Водний шар екстрагуодержану реакційну суміш екстрагують СН2СІ2. ють СН2Сl2. Об'єднаний органічний шар осушають Відокремлений органічний шар осушають (MgSO4), фільтрують і розчинник випаровують. (Na2SO4), фільтрують і розчинник випаровують. Вихід: 144г (95%) 1-метил-4-феніл-NЗалишок очищають методом хроматографії на (фенілметил)-4-піперидинкарбоксаміду (проміжн. короткій відкритій колонці із силікагелем (елюент: сп.1). СН2СІ2/(СН3OН/NН3) 95/5). Чисті фракції збирають Приклад А2 і розчинник випаровують. Вихід: 1,33г етил-4Суміш проміжної сполуки 1 (0,47моль) у SOCl2 феніл-4-[1-((4-метилкарбокси)фенілметил)-1H(750мл) перемішують та нагрівають до кипіння зі імідазол-2-іл]-1-піперидинкарбоксилату (проміжн. зворотним холодильником протягом 1 години. Росп.7). зчинник випаровують. Двічі додають толуол та В. Одержання кінцевих сполук знов випаровують. Вихід: 190г (100%) N-[хлор-(1Приклад В1 метил-4-феніл-4Суміш проміжної сполуки 4 (0,05моль) та Ν,Νпіперидиніл)метилен]бензолметанаміну моногіддіетилетанаміну (0,15моль) у толуолі (750мл) перохлориду (проміжн. сп.2). ремішують при 100°С. Додають по краплях етилПриклад A3 хлорформіат (0,25моль) і реакційну суміш переміСуміш проміжної сполуки 2 (0,47моль) у ДМФ шують та нагрівають до кипіння зі зворотним (750мл) охолоджують на льодяній бані. Додають холодильником протягом 1 години, а потім охолопо краплях 2,2-диметоксіетанамін (0,54моль), розджують. Суміш виливають у водний розчин K2СО3 чинений у ДМФ. Суміш перемішують при кімнатній (35г K2СО3). Шари розділяють. Водний шар екстратемпературі протягом ночі. Розчинник випаровугують СН2Сl2. Відокремлений органічний шар осують. Вихід: 210г (100%) N-(2,2-диметоксіетил)-1шають (MgSO4), фільтрують та розчинник випарометил-4-феніл-N'-(фенілметил)-4вують. Залишок очищають на силікагелі на піперидинкарбоксімідаміду дигідрохлориду (проскляному фільтрі (елюент: СН2Сl2/С2Н5ОН 98/2). міжн. сп.3). Потрібні фракції збирають і розчинник випаровуПриклад А4 ють. Залишок кристалізують з CH3CN, збирають на Суміш проміжної сполуки 3 (0,47моль) у 6Н фільтрі та висушують. Вихід: 16,7г (86%) етил-4НСl (1500мл) перемішують до утворення мутного феніл-4-[1-(фенілметил)-1H-імідазол-2-іл]-1розчину, потім промивають СН2СІ2 (900мл), перепіперидинкарбоксилату (Сполука 1). мішують при 80°С протягом 1 години, охолоджуПриклад В2 ють, підлуговують за допомогою 50% розчину Одержання сполуки 2 NaOH та екстрагують СН2СІ2. Органічний шар відокремлюють, осушають (MgSO4), фільтрують і розчинник випаровують. Залишок кристалізують з CH3CN. Осад збирають на фільтрі та висушують. Вихід: 38,3г (25%) 1-метил-4-феніл-4-[1(фенілметил)-1H-імідазол-2-іл]піперидину (проміжн. сп.4). Бензоїлхлорид (0,0023моль) додають до суміПриклад А5 ші проміжної сполуки 6 (0,0019моль) та Ν,ΝСуміш сполуки 1 (0,089моль) у метанолі діетилетанаміну (0,0024моль) у СН2Сl (15мл), пе(250мл) гідрують при 50°С, використовуючи Pd/C ремішуваної при кімнатній температурі. Реакційну 10% (3г) як каталізатор. Після поглинання водню суміш перемішують протягом 30хв. при кімнатній (1екв.) каталізатор збирають на фільтрі та фільттемпературі. Додають воду. Шари розділяють. рат випаровують. Залишок кристалізують з Водний шар екстрагують СН2Сl2. Об'єднані органіCH3CN. Осад збирають на фільтрі та висушують. чні шари осушають (Na2SO4), фільтрують та розВихід: 23,89г (90%) етил-4-феніл-4-(1H-імідазол-2чинник випаровують. Залишок очищають хроматоіл)-1-піперидинкарбоксилату (проміжн. сп.5). графією на короткій відкритій колонці з Приклад А6 силікагелем (елюент: CH2Cl2/(CH3OH/NH3) 98/2). Суміш проміжної сполуки 5 (0,026моль) та Чисті фракції збирають і розчинник випаровують. KОН (0,26моль) у 2-пропанолі (150мл) перемішуЗалишок перекристалізовують з н-гексану, збирають та нагрівають до кипіння зі зворотним холодиють на фільтрі та висушують. Вихід: 0,42г (52%) льником протягом 10 годин. Розчинник випаровусполуки 2; т.пл. 122,7°С. ють. Залишок розводять у Н2О і суміш екстрагують Приклад В3 СН2СІ2. Органічний шар відокремлюють, осушають, фільтрують і розчинник випаровують. Вихід: 9,4г 4-феніл-4-[1-(фенілметил)-1H-імідазол-2Одержання сполуки 3 іл]піперидину (проміжн. сп.6). Приклад А7 Реакція під атмосферою N2. Суміш проміжної сполуки 5 (0,0033моль) у ДМФ (5мл) та ТГФ (5мл) Реакція під атмосферою N2. Розчин проміжної 21 76224 22 сполуки 5 (0,0054моль) у ДМФ (10мл) та ТГФ Приклад В7 (10мл) додають по краплях до NaH (0,00624моль) у ТГФ (30мл) і суміш перемішують при кімнатній температурі протягом 1 години. Потім додають по Одержання сполуки 7 краплях метил-4-(бромметил)бензоат (0,00624моль) у ТГФ (5мл) і реакційну суміш перемішують при 60°С протягом 3 годин. Додають воду Метил-2-ізоціанатобензоат (0,0007моль) доі суміш екстрагують СН2Сl2. Об'єднані органічні дають до проміжної сполуки 6 (0,0007моль) у ТГФ шари осушають (Na2SO4), фільтрують і розчинник (10мл) і реакційну суміш перемішують протягом 3 випаровують. Залишок очищають хроматографією годин при кімнатній температурі. Додають воду і на короткій відкритій колонці з силікагелем (елюцю суміш екстрагують СН2Сl2. Відокремлений орент: CH2Cl2/(CH3OH/NH3) 98/2). Потрібні фракції ганічний шар осушають (Na2SO4), фільтрують та збирають і розчинник випаровують. Залишок крисрозчинник випаровують. Залишок (0,4г) очищають талізують з DIPE, збирають на фільтрі та висушуметодом ВЕРХ на силікагелі (елюент: ють. Вихід: 1,7г (70%) сполуки 3; т.пл. 149,1°С. СН2Сl2/СН3ОН 98/2). Потрібні фракції збирають і Приклад В4 розчинник випаровують. Вихід: 0,2г (66%) сполуки 7. Приклад В 8 Одержання сполуки 4 а) Одержання сполуки 8 Суміш проміжної сполуки 6 (0,0059моль) та (0,0059моль) у CH3CN (70мл) перемішують та нагрівають до кипіння зі зворотним холодильником протягом 24 годин. Розчинник випаровують. Додають воду. Цю суміш екстрагують СН2Сl2. Відокремлений органічний шар осушають (Na2SO4, безводний), фільтрують і розчинник випаровують. Залишок кристалізують з DIPE, збирають на фільтрі та перекристалізовують з CH3CN, збирають на фільтрі та висушують. Вихід: 0,33г сполуки 4; т.пл. 84,2°С. Приклад В5 Одержання сполуки 5 Суміш сполуки 4 (0,0001моль) у 6Н НСl (22,8мл) перемішують та нагрівають до кипіння зі зворотним холодильником протягом 4 годин. Реакційну суміш підлуговують, а потім екстрагують СН2СІ2. Відокремлений органічний шар осушають (Na2SO4, безводний), фільтрують і розчинник випаровують. Залишок перекристалізовують з DIPE, збирають на фільтрі та висушують. Вихід: 0,24г (62%) сполуки 5. Приклад В6 Суміш сполуки 3 (0,002моль) та LiOH (0,02моль) у ТГФ (11мл) та Н2О (11мл) перемішують при кімнатній температурі протягом 24 годин. Додають Н2О. Суміш доводять до рН6, а потім екстрагують СН2Сl2. Органічний шар відокремлюють, осушають, фільтрують і розчинник випаровують. Залишок промивають СН2Сl2. Вихід: 0,72г (83%) сполуки 8; т.пл. 251,6°С. b) Одержання сполуки 9 Реакція під атмосферою N2. Розчин NaH 60% (0,000642моль) у ДМФ (2мл) перемішують при кімнатній температурі. Додають по краплях розчин сполуки 6 (0,000642моль) у ДМФ (8мл) і реакційну суміш перемішують протягом однієї години при кімнатній температурі. Додають СН3І (0,001284моль) і реакційну суміш перемішують при 60°С в апараті високого тиску Parr протягом 2 годин. Розчинник випаровують. Залишок очищають методом високоефективної рідинної хроматографії на силікагелі (елюент: СН2СІ2/СН3ОН 98/2). Потрібні фракції збирають і розчинник випаровують. Вихід: 0,14г (49%) сполуки 9. c) Одержання сполуки 10 Одержання сполуки 6 Ізоціанатобензол (0,0094моль) додають по краплях до проміжної сполуки 6 (0,0094моль) у ТГФ (50мл) і реакційну суміш перемішують протягом 30хв. при кімнатній температурі. Додають воду і цю суміш екстрагують СН2Сl2. Відокремлений органічний шар осушають (Na2SO4), фільтрують та розчинник випаровують. Твердий залишок промивають 2-пропаноном, збирають на фільтрі та висушують. Вихід: 2,7г (68%) сполуки 6. Додають по краплях 1М LiAlH4 у ТГФ (0,000444моль) до розчину сполуки 7 (0,000404моль) у ТГФ (5мл), перемішуваного при 0°С. Реакційну суміш перемішують протягом 30хв. при 0°С. Суміш обробляють 10% водним розчином NH4Cl і екстрагують EtOAc. Відокремлений органічний шар осушають (Na2SO4). фільтрують і розчинник випаровують. Залишок очищають методом протиточної ТШХ (CC-TLC) на пристрої Chromatotron (елюент: СН2Сl2/СН3ОН 96/4). Потрі 23 76224 бні фракції збирають і розчинник випаровують. Залишок кристалізують з СН3ОН/Н2О, збирають на фільтрі та висушують. Вихід: 0,020г (10%) сполуки 10. d) Одержання сполуки 11 До розчину сполуки 7 (0,0006469моль) у діоксані/Н2О 1/1 (6мл) додають порціями LiOH (0,001423моль). Одержану суспензію перемішують протягом 18 годин при кімнатній температурі. Розчинник випаровують. Залишок розводять у воді та екстрагують сумішшю ЕtOАс та 1-бутанолу. Органічний шар відокремлюють, осушають (Na2SO4), фільтрують і розчинник випаровують. Залишок розводять у 1Н НСl, а потім екстрагують ЕtOАс. Органічний шар відокремлюють, промивають розсолом, осушають (Na2SO4), фільтрують і розчинник випаровують. Залишок кристалізують з Et2O/CH2Cl2, збирають на фільтрі та висушують. Вихід: 0,16г (51%) сполуки 11. Приклад В 9 До суміші проміжної сполуки 7 (0,0018моль) у ТГФ (10мл) та Н2О (10мл) додають LiOH (0,018моль). Реакційну суміш перемішують протягом 3 годин при кімнатній температурі. Додають воду. Додають СН2Сl2. Реакційну суміш екстрагують. Органічний шар відокремлюють, осушають (Na2SO4) фільтрують і розчинник випаровують. Білий твердий залишок промивають метанолом та СН2Сl2, а потім висушують. Вихід: 0,54г етил-4феніл-4-[1-(4-гідроксифенілметил)-1H-імідазол-2іл]-1-піперидинкарбоксилату (Сполука 12). Були синтезовані такі сполуки, вказані у Таблицях 1-5: (Всі точки плавлення (т.пл.) вказані у °С). Таблиця 1 24 25 76224 26 Продовження таблиці 1 27 76224 28 Продовження таблиці 1 Таблиця 2 Таблиця 3 29 76224 30 Таблиця 4 Таблиця 5 С. Фармакологічні приклади Були проведені дослідження фармакологічних властивостей деяких сполук методами зв'язування радіоліганду, а також зв'язування GTP S, з клонованими -, - та μ-опіоїдними рецепторами людини, що експресуються у клітинних лініях ссавців. Вимірювали передачу сигналу вторинного месенджера на препаратах мембран шляхом стимулювання зв'язування [35S]GTP S. Цей функціональний аналіз досліджує агоністичні та антагоністичні властивості сполук. DPDPE ((О-Pen2,5)-енкефалін) використовували як еталонний агоніст, а налтриндол - як еталонний антагоніст -опіоїдного рецептора (Malatynska Ε., Wang Υ., Κηαρρ R.J., Santoro G, Li X., Waite S., Roeske W.R., Yamamura H.I.: Human δ opioid receptor: a stable cell line for functional studies ofopioids. NeuroReport 6, 613-616, 1995) і (Portoghese P.S., Sultana M., Takemori A.E.: Naltrindole, a highly selective and potent nonpeptide opioid receptor antagonist. Eur. J. Pharmacol. 146, 185-186, 1988), a U69593 та норбіналторфімін (нор-BNI) використовували як еталонні агоніст та антагоніст, відповідно, для опіоїдного рецептора. Для μ-опіоїдного рецептора як еталонний агоніст використовували морфін, а як еталонний антагоніст - налоксон (Alt Α., Mansour Α., Akil Η., Medzihradsky Κ, Traynor J.R., Woods J.H.: Stimulation of guanosine-5'-O-(3[35S]thio)triphosphate binding by endogenous opioids acting at a cloned Ми receptor. J. Pharmacol. Exp. Ther. 286, 282-288, 1998) та (Smart D., Hirst R.Α., Hirota K., Gramly O.K., Lambert D.G.: The effects of recombinant rat μ opioid receptor activation in CHO cells on phospholipase C, [Ca2+]I and adenylyl cyclase. Br. J. Pharmacol. 120, 1165-1171, 1997). Матеріали та методи Клітинна культура Клітини яєчників китайського хом'ячка (СНО), стабільно трансфековані -чи μ-опіоїдним рецептором, культивують у середовищі Ігла, модифікованому за Дульбекко (DMEM) / живильній суміші Ham's F12 (у співвідношенні 1:1) з добавкою 10% термоінактивованої сироватки плоду корови та розчину антибіотиків, що містить 100 МО/мл пеніциліну G, 100мкг/мл стрептоміцинсульфату, 110мкг/мл піровиноградної кислоти та 300мкг/мл L-глутаміну. Клітини гліоми С6, стабільно трансфековані -опіоїдним рецептором, потребували використання середовища DMEM, збагаченого 10% термоінактивованої сироватки плоду корови та розчину антибіотиків, як описано вище. Препарат мембран Мембрани одержують як загальні фракції мікрочастинок. Всі клітинні лінії культивують до ступеню злиття 90% на чашках Петрі діаметром 145мм і обробляють 5мМ бутиратом натрію за 24 години до збирання. Культуральне середовище видаляють і клітини промивають охолодженим на льоді фосфатно-сольовим буфером (PBS, який не містить Са2+ та Mg2+), зіскрібають з чашок у 50мМ трис-НСІ буфері, рН7,4, та збирають за допомогою центрифугування (10 хвилин, 16000об./хв., при 4°С). Клітинний осад ресуспендують у гіпотонічному 5мМ трис-НСІ буфері, рН7,4, та повторно гомогенізують за допомогою гомогенізатора Ultra Turrax. Гомогенат центрифу 31 76224 32 гують при 18000об./хв. протягом 20 хвилин при клітинних мембран гліоми С6, і 10мкМ GDP та 4°С. Кінцевий осад ресуспендують у 50мМ трис0,3мМ MgCl2 для -опіоїдних рецепторів мембран НСІ буфері, рН7,4, та зберігають у вигляді аліквот СНО. Суміші для проведення аналізу містять при -70°С. Визначення протеїну проводять за 10мкг мембранного протеїну. До розведених допомогою набору для аналізу на протеїн Biorad мембран додають ще 10мкг/мл сапоніну як пове(Bradford) з використанням альбуміну бичачої рхнево-активну речовину для збільшення пронисироватки (BSA) як стандарту (Bradford, M.M.: A кнення [35S]GTP S крізь мембрани. rapid and sensitive method for the quantification of Для аналізу на агоністичну активність, microgram quantities of protein utilizing the principle 175мкл розведених мембран попередньо інкубуof protein-dye binding. Analytical Biochem. 72: 248ють в описаному вище буфері разом з 25мкл бу254, 1976). фера та 25мкл різних концентрацій сполуки у Зв'язування радіоліганду загальному об'ємі 225мкл. Для аналізу антагонісБули проведені попередні експерименти зі тичної активності, замість добавки 25мкл буфера зв'язування радіолігандів для визначення оптидодають еталонний агоніст для визначення базомальних умов проведення аналізу для зазначевого титру після стимулювання. Для всіх трьох них субтипів опіоїдних рецепторів з відповідними клітинних ліній використовують концентрації мембранами клітин ссавців. DPDPE, U69593 та морфіну у300нМ для відпові3 Аналізи конкурентного інгібування [ H]DPDPE дних субтипів рецепторів. Після 20-хвилинного сполуками проводили при концентрації радіолігаперіоду попереднього інкубування при 37°С, донду 2нМ (Kd=1,7нМ) та різних концентраціях сподають 25мкл [35S]GTP S до кінцевої концентрації лук без паралельних дослідів, з охопленням що0,25нМ і суміші для аналізу інкубують далі протянайменше 3 порядків величини навколо значення гом 20 хвилин при 37°С. Зв'язаний та вільний pІС50. Для конкурентного зв'язування - та μ[35S]GTP S розділяють швидкою фільтрацією рецепторів використовували, відповідно, крізь UniFilter™-96 GF/B™ при зниженому тиску [3H]U69593 (Kd=0,4нМ) та [3H]DAMGO (Kd=0,6нМ) за допомогою пристрою Filtermate 196 (Packard). у концентрації 1нМ. Мембрани відтаювали на Кількість зв'язаної радіоактивності на фільтрі вильоді та розводили у 50мМ трис-НСІ буфері, значають після висушування фільтра та додарН7,4. Для -опіоїдних рецепторів, до цього бування сцинтилянта (Microscint-O; Packard) метофера для інкубування додавали 2мМ MgCl2, 1мМ дом підрахунку сцинтиляції. етиленглікольтетраоцтової кислоти (EGTA) та Базове зв'язування [35S]GTP S вимірюють 0,1% бичачого сироваткового альбуміну (BSA). шляхом проведення дослідів без використання Неспецифічне зв'язування вимірювали у присутсполук. Стимулювання агоністом обчислюють як ності 1мкМ налтриндолу, спірадоліну та декстропроцент збільшення показників над базовим рівмораміду для -, - та -опіоїдних рецепторів, нем. Сигмоїдальні криві концентраційної чутливідповідно. Було знайдено, що оптимальними вості агоніста для зростання зв'язування умовами аналізу конкурентного зв'язування для [35S]GTP S та криві інгібування антагоніста для всіх трьох субтипів рецепторів є інкубування проінгібування зв'язування, стимульованого еталонтягом 1 години при 25°С. Аналізи проводять у ним агоністом [35S]GTP S, аналізують методом кінцевому об'ємі 500мкл. Реакцію зупиняють нелінійної регресії з використанням комп'ютерної швидкою фільтрацією крізь фільтр UniFilter™-96, програми GraphPad Prism. Дані одержують шляGF/B™ при зниженому тиску за допомогою прихом проведення незалежних експериментів, а строю Filtermate 196 (Packard). Кількість зв'язаної для точок з різними концентраціями проводять по радіоактивності на фільтрі визначають після видва паралельні досліди. сушування фільтра та додавання сцинтилянта Усі сполуки за винаходом мають значення (Microscint-O; Packard) методом підрахунку сцинрІС50 не нижче 6 для дельта-опіоїдних рецепторів тиляції. і значення pIC50 не вище 6 для мю- або каппаЗв'язування [35S]GTP S рецепторів. Визначення зв'язування [35S]GTP S з GСполуки, вказані у Таблиці 6, мають значення протеїнами проводять за модифікованою меторІС50 від 7 до 8 для дельта-опіоїдних рецепторів і дикою Лазарено (Lazareno S.: Measurement of значення рІС50, що дорівнюють 6 чи менше, для agonist-stimulated [35S]GTP S binding to cell мю- або каппа-рецепторів. membranes. Meth. Molec. Biol. 106, 231-243, 1999). Сполуки, вказані у Таблиці 7, мають значення У попередніх експериментах на зв'язування рІС50, вищі за 8, для дельта-опіоїдних рецепторів, [35S]GTP S були оптимізовані умови проведення і значення рІС5о, що дорівнюють 6 чи менше, для аналізу, в результаті чого були вибрані такі бумю- або каппа-рецепторів. Коефіцієнт селективфери: 20мМ Hepes плюс 100мМ NaCl, який місності до дельта-опіоїдних рецепторів порівняно з тить 3мкМ гуанозиндифосфату (GDP) та 1мМ мю-опіоїдними рецепторами досягає 600. MgCl2 для μ-опіоїдних рецепторів мембран клітин яєчників китайського хом'ячка (СНО), або 10мкМ GDP та 1мМ MgCl2 для -опіоїдних рецепторів 33 76224 34 Таблиця 6 Значення рІС50 для дельта-опіоїдних рецепторів за результатами аналізу з агоністом Сп.№ 43 17 30 105 78 101 28 11 29 67 7 9 52 103 26 рІС5О 7,9 7,9 7,9 7,9 7,9 7,8 7,8 7,8 7,8 7,8 7,7 7,7 7,7 7,7 7,7 Сп.№ 22 87 45 51 4 55 71 99 34 72 81 64 18 42 10 рІС50 7,3 7,3 7,3 7,3 7,3 7,3 7,3 7,3 7,2 7,2 7,2 7,2 7,2 7,2 7,2 27 15 69 50 32 93 65 84 66 75 13 76 96 94 70 36 7,7 7,6 7,6 7,6 7,6 7,5 7,5 7,5 7,5 7,4 7,4 7,4 7,4 7,4 7,4 7,3 33 37 80 90 56 47 43 48 79 111 7 68 95 92 49 74 7,1 7,1 7,1 7,1 7,1 7,1 7,1 7,1 7,0 7,0 7,0 7,0 7,0 7,0 7,0 7,0 Таблиця 7 Результати аналізів на зв'язування рецепторів з агоністами (pIC50) та зв'язування з перенесенням сигналу (pIC50), н.в.: не визначено Комп’ютерна верстка Т. Чепелева Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюSubstituted 4-phenyl 4-[1h-imidazol-2-yl]-piperidine derivatives and use thereof as selective non-peptide delta-opioid agonists
Автори англійськоюJanssens, Frans, Eduard, Leenaerts Joseph Elisabeth
Назва патенту російськоюЗамещенные 4-фенил-4-(1н-имидазол-2-ил)-пиперидиновые производные и их применение как селективных непептидных дельта-опиоидных агонистов
Автори російськоюЯнссенс Франс Эдуард, Леенартс Йозеф Элизабет
МПК / Мітки
МПК: C07D 401/14, A61K 31/4178, A61P 1/12, A61P 1/14, A61P 11/06, C07D 233/10, C07D 233/12, A61P 17/06, C07D 401/04, A61P 19/02, A61P 25/06, A61P 25/04, A61K 31/4523, C07D 211/14
Мітки: похідні, непептидних, дельта-опіоїдних, 4-феніл-4-(1н-імідазол-2-іл)-піперидинові, агоністів, використання, заміщені, селективних
Код посилання
<a href="https://ua.patents.su/17-76224-zamishheni-4-fenil-4-1n-imidazol-2-il-piperidinovi-pokhidni-ta-kh-vikoristannya-yak-selektivnikh-nepeptidnikh-delta-opiodnikh-agonistiv.html" target="_blank" rel="follow" title="База патентів України">Заміщені 4-феніл-4-(1н-імідазол-2-іл)-піперидинові похідні та їх використання як селективних непептидних дельта-опіоїдних агоністів</a>
Попередній патент: Горілка “віче”
Наступний патент: Пристрій для очищення сипучим абразивним матеріалом поверхні дроту від забруднень
Випадковий патент: Самозаливний гідрозатвор