Таксоїди, cпосіб їх одержання та фармацевтична композиція на їх основі
Номер патенту: 61883
Опубліковано: 15.12.2003
Автори: Коммерсон Ален, Бушар Херве, Бурзат Жан-Домінік
Формула / Реферат
1. Таксоїди загальної формули (І):
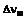
в якій:
Z означає атом водню або радикал загальної формули (II):
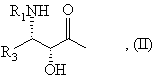
в якій:
R1 означає бензоїльний радикал, можливо, заміщений одним або декількома атомами або радикалами, однаковими або різними, що вибирають з атомів галогену та алкільних радикалів з 1-4 атомами вуглецю, алкоксильних радикалів з 1-4 атомами вуглецю або трифторметилу, теноїльний або фуроїльний радикал або радикал
![]()
в якому R2 означає:
- алкільний радикал з 1-8 атомами вуглецю, алкенільний радикал з 2-8 атомами вуглецю, алкінільний радикал з 3-8 атомами вуглецю, циклоалкільний радикал з 3-6 атомами вуглецю, циклоалкенільний радикал з 4-6 атомами вуглецю, біциклоалкільний радикал з 7-10 атомами вуглецю, причому ці радикали можуть бути заміщені одним або декількома замісниками, що вибирають з атомів галогену та гідроксильного радикалу, алкоксильного радикалу з 1-4 атомами вуглецю, діалкіламінорадикалу, кожна алкільна частина якого містить 1-4 атоми вуглецю, піперидино-, морфоліно-, піперазин-1-іл-радикалу (можливо, заміщеного в положенні 4 алкільним радикалом з 1-4 атомами вуглецю або фенілалкільним радикалом, алкільна частина якого містить 1-4 атоми вуглецю), циклоалкільного радикалу з 3-6 атомами вуглецю, циклоалкенільного радикалу з 4-6 атомами вуглецю, фенільного радикалу (можливо, заміщеного одним або декількома атомами або радикалами, що вибирають з атомів галогену та алкільних радикалів з 1-4 атомами вуглецю або алкоксильних радикалів з 1-4 атомами вуглецю), ціанорадикалу, карбоксильного радикалу або алкоксикарбонільного радикалу, алкільна частина якого містить 1-4 атоми вуглецю;
- фенільний або α- або β-нафтильний радикал, можливо, заміщений одним або декількома атомами або радикалами, які вибирають з атомів галогену і алкільних радикалів з 1-4 атомами вуглецю або алкоксильних радикалів з 1-4 атомами вуглецю, або ароматичний гетероциклічний п'ятичленний радикал, що вибирають переважно з фурильного та тієнільного радикалів;
- або насичений гетероциклічний радикал з 4-6 атомами вуглецю, можливо, заміщений одним або декількома алкільними радикалами з 1-4 атомами вуглецю;
R3 означає лінійний або розгалужений алкільний радикал з 1-8 атомами вуглецю, лінійний або розгалужений алкенільний радикал з 2-8 атомами вуглецю, лінійний або розгалужений алкінільний радикал з 2-8 атомами вуглецю, циклоалкільний радикал з 3-6 атомами вуглецю, фенільний або α- або β-нафтильний радикал, можливо, заміщений одним або декількома атомами або радикалами, що вибирають з атомів галогену та алкільних, алкенільних, алкінільних, арильних, аралкільних, алкоксильних, алкілтіо-, арилокси-, арилтіо-, гідроксильного, гідроксіалкільного, меркапто-, формільного, ацильного, ациламіно-, ароїламіно-, алкоксикарбоніламіно-, аміно-, алкіламіно-, діалкіламіно-, карбоксильного, алкоксикарбонільного, карбамоїльного, алкілкарбамоїльного, діалкілкарбамоїльного, ціано-, нітро- та трифторметильного радикалів; або ароматичний п'ятичленний гетероциклічний радикал, що містить один або декілька гетероатомів, однакових або різних, що вибирають з атомів азоту, кисню або сірки, та, можливо, заміщений одним або декількома замісниками, однаковими або різними, що вибирають з атомів галогену та алкільних, арильних, аміно-, алкіламіно-, діалкіламіно-, алкоксикарбоніламіно-, ацильного, арилкарбонільного, ціано-, карбоксильного, карбамоїльного, алкілкарбамоїльного, діалкілкарбамоїльного або алкоксикарбонільного радикалів, при умові, що в замісниках фенільного, α- або β-нафтильного та ароматичних гетероциклічних радикалів алкільні радикали та алкільні частини інших радикалів містять 1-4 атоми вуглецю та що алкенільні та алкінільні радикали містять 2-8 атомів вуглецю, та що арильні радикали являють собою фенільні або α- або β-нафтильні радикали;
R4 означає алкоксильний радикал з 1-6 атомами вуглецю в лінійному або розгалуженому ланцюгу, алкенілокси-радикал з 3-6 атомами вуглецю в лінійному або розгалуженому ланцюгу, алкінілокси-радикал з 3-6 атомами вуглецю в лінійному або розгалуженому ланцюгу, циклоалкілокси-радикал з 3-6 атомами вуглецю, циклоалкенілокси-радикал з 4-6 атомами вуглецю, причому ці радикали, можливо, заміщені одним або декількома атомами галогену або алкоксильними радикалами з 1-4 атомами вуглецю, алкілтіо-радикалом з 1-4 атомами вуглецю або карбоксильним радикалом, алкілоксикарбонільним радикалом, алкільна частина якого містить 1-4 атоми вуглецю, ціано-радикалом, карбамоїльним радикалом, N-алкілкарбамоїльним радикалом або N,N-діалкілкарбамоїльним радикалом, кожна алкільна частина якого містить 1-4 атоми вуглецю або разом з атомом азоту, з яким вона зв'язана, утворює насичений гетероциклічний п'яти- або шестичленний радикал, можливо, той, що містить другий гетероатом, що вибирають з атомів кисню, сірки або азоту, можливо, заміщений алкільним радикалом з 1-4 атомами вуглецю або фенільним радикалом, або фенілалкільним радикалом, алкільна частина якого містить 1-4 атоми вуглецю;
R5 означає алкоксильний радикал з 1-6 атомами вуглецю в лінійному або розгалуженому ланцюгу (можливо, заміщений алкокси-радикалом з 1-4 атомами вуглецю), алкенілокси-радикал з 3-6 атомами вуглецю, алкінілокси-радикал з 3-6 атомами вуглецю, циклоалкілокси-радикал з 3-6 атомами вуглецю, циклоалкенілокси-радикал з 3-6 атомами вуглецю, причому ці радикали, можливо, заміщені одним або декількома атомами галогену або алкоксильним радикалом з 1-4 атомами вуглецю, алкілтіо-радикалом з 2-4 атомами вуглецю або карбоксильним радикалом, алкілоксикарбонільним радикалом, алкільна частина якого містить 1-4 атоми вуглецю, ціано-радикалом, карбамоїльним радикалом, N-алкілкарбамоїльним або N,N-діалкілкарбамоїльним радикалом, кожна алкільна частина якого містить 1-4 атоми вуглецю або разом з атомом азоту, з яким вона зв'язана, утворює насичений гетероциклічний п'яти- або шестичленний радикал, можливо, той, що містить другий гетероатом, що вибирають з атомів кисню, сірки або азоту, можливо, заміщений алкільним радикалом з 1-4 атомами вуглецю або фенільним радикалом, або фенілалкільним радикалом, алкільна частина якого містить 1-4 атоми вуглецю.
2. Таксоїди за п. 1, які відрізняються тим, що Z означає атом водню або радикал загальної формули (II), в якій:
R1 означає бензоїльний радикал або радикал
![]()
в якому R2 означає трет-бутильний радикал; та R3 означає алкільний радикал з 1-6 атомами вуглецю, алкенільний радикал з 2-6 атомами вуглецю, циклоалкільний радикал з 3-6 атомами вуглецю, фенільний радикал, можливо, заміщений одним або декількома атомами або радикалами, однаковими або різними, що вибирають з атомів галогену та алкільних, алкоксильних, діалкіламіно-, ациламіно-, алкоксикарбоніламіно- або трифторметильного радикалів; або фур-2-ильний або фур-3-ильний радикал, тієн-2-ільний або тієн-3-ільний радикал або тіазол-2-, -4- або -5-ільний радикал; та R4 та R5, однакові або різні, кожний, означає лінійний або розгалужений алкілоксильний радикал з 1-6 атомами вуглецю.
3. Таксоїди за п. 1, які відрізняються тим, що Z означає атом водню або радикал загальної формули (II), в якій:
R1 означає бензоїльний радикал або радикал
![]()
в якому R2 означає трет-бутильний радикал, та R3 означає ізобутильний, ізобутенільний, бутенільний, циклогексильний, фенільний, фур-2-ильний, фур-3-ильний, тієн-2-ільний, тієн-3-ільний, тіазол-2-ільний, тіазол-4-ільний або тіазол-5-ільний радикал;
R4 та R5, однакові або різні, означають, кожний, метокси-, етокси- або пропокси-радикал.
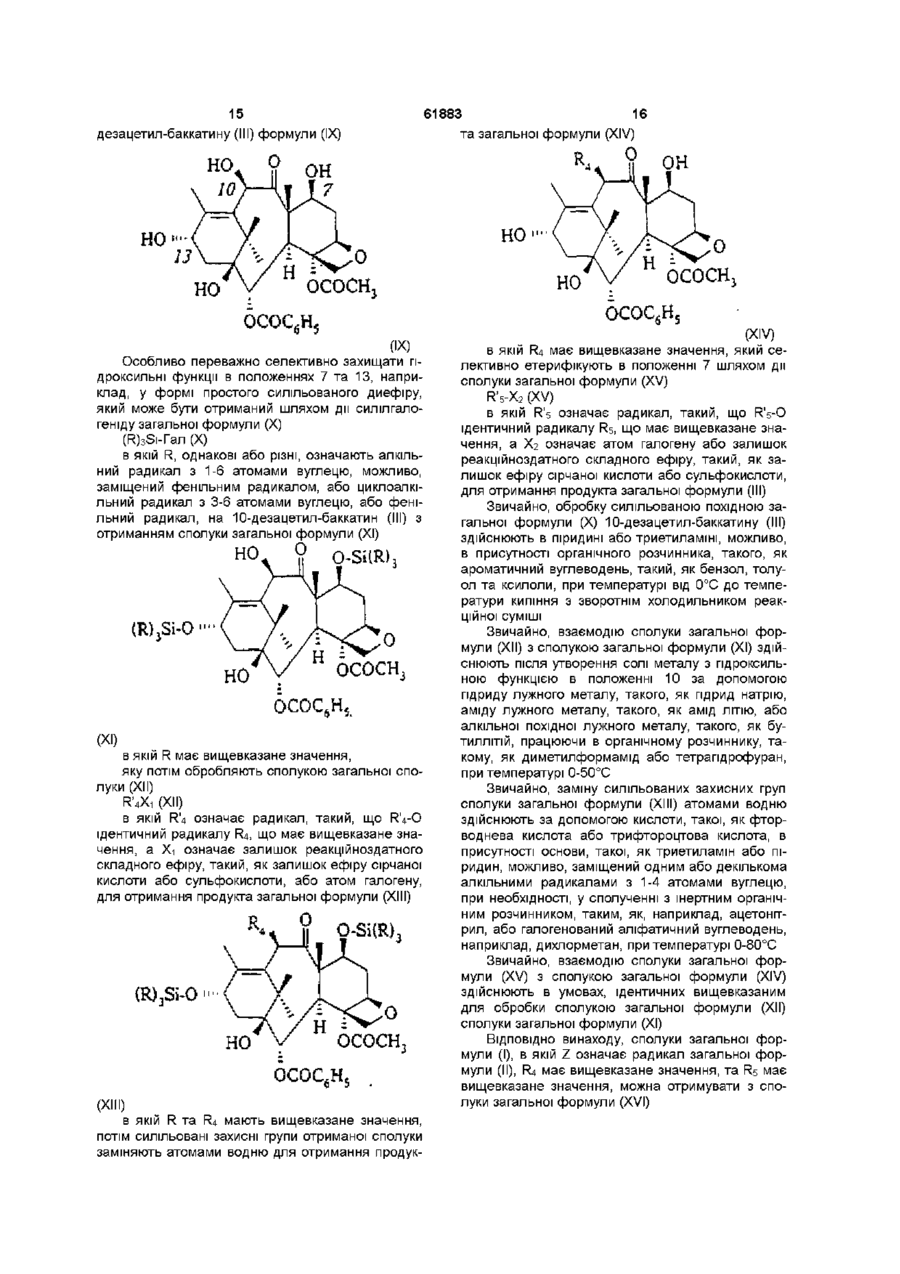
4. Спосіб одержання таксоїдів, що описані у будь-якому з пп. 1, 2 або 3, де Z означає радикал загальної формули (II), який відрізняється тим, що етерифікують сполуку загальної формули (ІІІ):
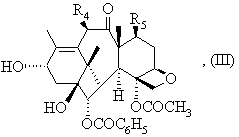
в якій R4 та R5 мають значення, що вказані у будь-якому з пп. 1, 2 або 3, за допомогою кислоти загальної формули (IV):
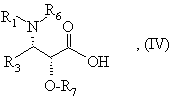
в якій R1 та R3 мають вищевказані значення, та або R6 означає атом водню, a R7 означає захисну для гідроксильної функції групу, або R6 та R7 разом утворюють насичений п'яти- або шестичленний гетероцикл, або за допомогою похідної цієї кислоти для отримання складного ефіру загальної формули (V):
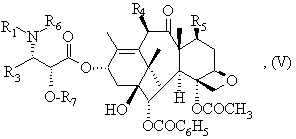
в якій R1, R3, R4, R5, R6 та R7 мають вищевказане значення, захисні групи якого, що позначені як R7 та/або R6 та R7, замінюють атомами водню.
5. Спосіб за п. 4, який відрізняється тим, що етерифікацію здійснюють за допомогою кислоти загальної формули (IV) в присутності агента конденсації та активуючого агента в органічному розчиннику при температурі від -10°С до 90°С.
6. Спосіб за п. 4, який відрізняється тим, що етерифікацію здійснюють за допомогою кислоти загальної формули (IV) у формі симетричного ангідриду, у присутності активуючого агента в органічному розчиннику та при температурі від 0°С до 90°С.
7. Спосіб за п. 4, який відрізняється тим, що етерифікацію здійснюють, використовуючи кислоту загальної формули (IV) у формі галоїдангідриду або у формі змішаного ангідриду з аліфатичною або ароматичною кислотою, можливо, того, що отримують in situ, в присутності основи, в органічному розчиннику при температурі від 0°С до 80°С.
8. Спосіб за п. 4, який відрізняється тим, що захисні групи R7 /та/або R6 та R7 замінюють атомами водню, в залежності від їх природи, таким чином:
1) коли R6 означає атом водню, а R7 означає захисну для гідроксильної функції групу, захисні групи замінюють атомами водню за допомогою неорганічної або органічної кислоти, що використовують індивідуально або у суміші, в органічному розчиннику, що вибирають з спиртів, простих ефірів, складних ефірів, аліфатичних вуглеводнів, галогенованих аліфатичних вуглеводнів, ароматичних вуглеводнів або нітрилів, при температурі від -10°С до 60°С, або за допомогою джерела фторид-іонів, такого як комплекс фтороводневої кислоти з триетиламіном, або шляхом каталітичного гідрування;
2) коли R6 та R7 разом утворюють насичений п'яти- або шестичленний гетероцикл загальної формули (VI):
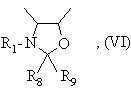
в якій:
R1 має вищевказане значення;
R8 та R9, однакові або різні, означають атом водню або алкільний радикал з 1-4 атомами вуглецю, або аралкільний радикал, алкільна частина якого містить 1-4 атоми вуглецю, а арильна частина переважно означає фенільний радикал, можливо, заміщений одним або декількома алкоксильними радикалами з 1-4 атомами вуглецю, або арильний радикал, переважно той, що означає фенільний радикал, можливо, заміщений одним або декількома алкоксильними радикалами з 1-4 атомами вуглецю, або
R8 означає алкоксильний радикал з 1-4 атомами вуглецю або тригалогенметильний радикал, такий як трихлорметильний радикал, або фенільний радикал, заміщений тригалогенметильним радикалом, таким як трихлорметильний радикал; та R9 означає атом водню; або R8 та R9 разом з атомом вуглецю, з яким вони зв'язані, утворюють 4-7-членний цикл,
захисну групу, що утворена R6 та R7, замінюють атомами водню, працюючи, в залежності від значень R1, R8 та R9, таким чином:
а) коли R1 означає трет-бутоксикарбонільний радикал, R8 та R9, однакові або різні, означають алкільний радикал або аралкільний радикал або арильний радикал, або R8 означає тригалогенметильний радикал або фенільний радикал, заміщений тригалогенметильним радикалом, та R9 означає атом водню, або R8 та R9 разом утворюють 4-7-членний цикл,
складний ефір загальної формули (V) обробляють неорганічною або органічною кислотою, можливо, в органічному розчиннику, такому як спирт, для отримання сполуки загальної формули (VII):
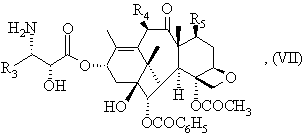
в якій R3, R4 та R5 мають вищевказане значення,
який ацилюють за допомогою бензоїлхлориду, в якому фенільне ядро, можливо, заміщене, теноїлхлориду, фуроїлхлориду або сполуки загальної формули (VIII):
R2-O-CO-X, (VIII)
в якій R2 має вищевказане значення, а Х означає атом галогену або залишок -O-R2 або -O-CO-O-R2, для отримання сполуки загальної формули (І), в якій Z означає радикал загальної формули (II);
б) коли R1 означає, можливо, заміщений бензоїльний радикал, теноїльний радикал або фуроїльний радикал або радикал
R2-O-CO-,
в якому R2 має вищевказане значення;
R8 означає атом водню або алкоксильний радикал з 1-4 атомами вуглецю або фенільний радикал, заміщений одним або декількома алкоксильними радикалами з 1-4 атомами вуглецю; та R9 означає атом водню,
захисну групу, що утворена R6 та R7, замінюють атомами водню у присутності неорганічної або органічної кислоти, що використовують індивідуально або у суміші, в стехіометричній або каталітичній кількості, в органічному розчиннику, що вибирають з спиртів, простих ефірів, складних ефірів, аліфатичних вуглеводнів, галогенованих аліфатичних вуглеводнів та ароматичних вуглеводнів, при температурі від -10°С до 60°С, переважно при 15-30°C.
9. Фармацевтична композиція, яка відрізняється тим, що вона містить принаймні одну сполуку за будь-яким з пп. 1, 2 або 3, в якій Z означає радикал загальної формули (II), у сполученні з одним або декількома фармацевтично прийнятними розчинниками або домішками.
10. Фармацевтична композиція за п. 9, яка відрізняється тим, що вона додатково містить принаймні одну або декілька сумісних та фармакологічно активних сполук.
Текст
1 Таксоїди загальної формули (І) FR, (І) Z-O' НО ососн, ОСОС 6 Н 5 в якій: Z означає атом водню або радикал загальної формули (II) О (П) R; он в якій RI означає бензоільний радикал, можливо, заміщений одним або декількома атомами або радикалами, однаковими або різними, що вибирають з атомів галогену та алкільних радикалів з 1-4 атомами вуглецю, алкоксильних радикалів з 1-4 атомами вуглецю або трифторметилу, теноільний або фуроільний радикал або радикал R2-O-CO- , в якому R2 означає - алкільний радикал з 1-8 атомами вуглецю, алкенільний радикал з 2-8 атомами вуглецю, алкінільний радикал з 3-8 атомами вуглецю, циклоалкільний радикал з 3-6 атомами вуглецю, циклоалкенільний радикал з 4-6 атомами вуглецю, біциклоалкільний радикал з 7-10 атомами вуглецю, причому ці радикали можуть бути заміщені одним або декількома замісниками, що вибирають з атомів галогену та гідроксильного радикалу, алкоксильного радикалу з 1-4 атомами вуглецю, діалкіламшорадикалу, кожна алкільна частина якого містить 1-4 атоми вуглецю, піперидино-, морфоліно-, піперазин-1-іл-радикалу (можливо, заміщеного в положенні 4 алкільним радикалом з 1-4 атомами вуглецю або фенілалкільним радикалом, алкільна частина якого містить 1-4 атоми вуглецю), циклоалкільного радикалу з 3-6 атомами вуглецю, циклоалкенільного радикалу з 4-6 атомами вуглецю, фенільного радикалу (можливо, заміщеного одним або декількома атомами або радикалами, що вибирають з атомів галогену та алкільних радикалів з 1-4 атомами вуглецю або алкоксильних радикалів з 1-4 атомами вуглецю), ціанорадикалу, карбоксильного радикалу або алкоксикарбонільного радикалу, алкільна частина якого містить 1-4 атоми вуглецю, - фенільний або а- або р-нафтильний радикал, можливо, заміщений одним або декількома атомами або радикалами, які вибирають з атомів галогену і алкільних радикалів з 1-4 атомами вуглецю або алкоксильних радикалів з 1-4 атомами вуглецю, або ароматичний гетероциклічний п'ятичленний радикал, що вибирають переважно з фурильноготатієнільного радикалів, - або насичений гетероциклічний радикал з 4-6 атомами вуглецю, можливо, заміщений одним або декількома алкільними радикалами з 1-4 атомами вуглецю, R3 означає ЛІНІЙНИЙ або розгалужений алкільний радикал з 1-8 атомами вуглецю, ЛІНІЙНИЙ або розгалужений алкенільний радикал з 2-8 атомами вуглецю, ЛІНІЙНИЙ або розгалужений алкінільний радикал з 2-8 атомами вуглецю, циклоалкільний радикал з 3-6 атомами вуглецю, фенільний або аабо р-нафтильний радикал, можливо, заміщений одним або декількома атомами або радикалами, що вибирають з атомів галогену та алкільних, алкенільних, алкінільних, арильних, аралкільних, О C O 00 00 (О 61883 діалкілкарбамоільним радикалом, кожна алкільна алкоксильних, алкілтю-, арилокси-, арилтю-, гідрочастина якого місить 1-4 атоми вуглецю або разом ксильного, пдроксіалкільного, меркапто-, форміль3 атомом азоту, з яким вона зв'язана, утворює наного, ацильного, ациламшо-, ароіламшо-, алкоксисичений гетероциклічний п'яти- або шестичленний карбоніламіно-, аміно-, алкіламшо-, діалкіламшо-, радикал, можливо, той, що містить другий гетерокарбоксильного, алкоксикарбонільного, карбамоіатом, що вибирають з атомів кисню, сірки або азольного, алкілкарбамоільного, діалкілкарбамоільноту, можливо, заміщений алкільним радикалом з 1го, ціано-, нітро- та трифторметильного радикалів, або ароматичний п'ятичленний гетероциклічний 4 атомами вуглецю або фенільним радикалом, або радикал, що містить один або декілька гетероатофенілалкільним радикалом, алкільна частина якомів, однакових або різних, що вибирають з атомів го містить 1-4 атоми вуглецю азоту, кисню або сірки, та, можливо, заміщений 2 Таксоїди за п 1, які відрізняються тим, що Z одним або декількома замісниками, однаковими означає атом водню або радикал загальної форабо різними, що вибирають з атомів галогену та мули (II), в якій алкільних, арильних, аміно-, алкіламшо-, діалкілаRi означає бензоільний радикал або радикал міно-, алкоксикарбоніламшо-, ацильного, арилкарR2-O-CO- , бонільного, ціано-, карбоксильного, карбамоільнов якому F 2 означає трет-бутильний радикал, та R3 ? го, алкілкарбамоільного, діалкілкарбамоільного означає алкільний радикал з 1-6 атомами вуглецю, або алкоксикарбонільного радикалів, при умові, алкенільний радикал з 2-6 атомами вуглецю, цикщо в замісниках фенільного, а- або р-нафтильного лоалкільний радикал з 3-6 атомами вуглецю, фета ароматичних гетероциклічних радикалів алкільнільний радикал, можливо, заміщений одним або ні радикали та алкільні частини інших радикалів декількома атомами або радикалами, однаковими містять 1-4 атоми вуглецю та що алкенільні та алабо різними, що вибирають з атомів галогену та КІНІЛЬНІ радикали містять 2-8 атомів вуглецю, та алкільних, алкоксильних, діалкіламшо-, ациламшощо арильні радикали являють собою фенільні або , алкоксикарбоніламшо- або трифторметильного а- або р-нафтильні радикали, радикалів, або фур-2-ильний або фур-3-ильний F 4 означає алкоксильний радикал з 1-6 атомами ? радикал, ТІЄН-2-ІЛЬНИЙ або тієн-3-ільний радикал вуглецю в лінійному або розгалуженому ланцюгу, або тіазол-2-, -4- або -5-ільний радикал, та R4 та алкенілокси-радикал з 3-6 атомами вуглецю в ліR5, однакові або різні, кожний, означає ЛІНІЙНИЙ нійному або розгалуженому ланцюгу, алкінілоксиабо розгалужений алкілоксильний радикал з 1-6 радикал з 3-6 атомами вуглецю в лінійному або атомами вуглецю розгалуженому ланцюгу, циклоалкілокси-радикал з 3-6 атомами вуглецю, циклоалкенілокси-радикал з 3 Таксоїди за п 1, які відрізняються тим, що Z 4-6 атомами вуглецю, причому ці радикали, можозначає атом водню або радикал загальної форливо, заміщені одним або декількома атомами мули (II), в якій галогену або алкоксильними радикалами з 1-4 Ri означає бензоільний радикал або радикал атомами вуглецю, алкілтю-радикалом з 1-4 атоR2-O-CO- , мами вуглецю або карбоксильним радикалом, алкілоксикарбонільним радикалом, алкільна частина в якому R2 означає трет-бутильний радикал, та R3 якого містить 1-4 атоми вуглецю, ціано-радикалом, означає ізобутильний, ізобутенільний, бутенількарбамоільним радикалом, N-алкілкарбамоільним ний, циклогексильний, фенільний, фур-2-ильний, радикалом або N.N-діалкілкарбамоільним радикафур-3-ильний, ТІЄН-2-ІЛЬНИЙ, тієн-3-ільний, тіазоллом, кожна алкільна частина якого містить 1-4 2-ільний, тіазол-4-ільний або тіазол-5-ільний радиатоми вуглецю або разом з атомом азоту, з яким кал, вона зв'язана, утворює насичений гетероциклічний R4 та R5, однакові або різні, означають, кожний, п'яти- або шестичленний радикал, можливо, той, метокси-, етокси- або пропокси-радикал що містить другий гетероатом, що вибирають з 4 Спосіб одержання таксоїдів, що описані у будьатомів кисню, сірки або азоту, можливо, заміщений якому з пп 1,2 або 3, де Z означає радикал загаалкільним радикалом з 1-4 атомами вуглецю або льної формули (II), який відрізняється тим, що фенільним радикалом, або фенілалкільним радиетерифікують сполуку загальної формули (III) калом, алкільна частина якого містить 1-4 атоми вуглецю, Rs означає алкоксильний радикал з 1-6 атомами вуглецю в лінійному або розгалуженому ланцюгу (можливо, заміщений алкокси-радикалом з 1-4 атомами вуглецю), алкенілокси-радикал з 3-6 атомами вуглецю, алкінілокси-радикал з 3-6 атомами вуглецю, циклоалкілокси-радикал з 3-6 атомами вуглецю, циклоалкенілокси-радикал з 3-6 атомами вуглецю, причому ці радикали, можливо, заміщені одним або декількома атомами галогену або алкоксильним радикалом з 1-4 атомами вуглецю, алкілтю-радикалом з 2-4 атомами вуглецю або карбоксильним радикалом, алкілоксикарбонільним радикалом, алкільна частина якого містить 1-4 атоми вуглецю, ціано-радикалом, карбамоільним радикалом, N-алкілкарбамоільним або N,N (III) 1 НО НО ососн, ОСОС 6 Н 5 в якій R4 та Rs мають значення, що вказані у будьякому з пп 1,2 або 3, за допомогою кислоти загальної формули (IV) 61883 (VI) (IV) ОН OR в якій Ri та R3 мають вищевказані значення, та або R6 означає атом водню, a R7 означає захисну для гідроксильної функції групу, або R6 та R7 разом утворюють насичений п'яти- або шестичленний гетероцикл, або за допомогою похідної цієї кислоти для отримання складного ефіру загальної формули (V) R N О (V) О' R, O-R, НО ососн, осос6н5 в якій R-і, R3, R4, R5, R6 та R7 мають вищевказане значення, захисні групи якого, що позначені як R7 та/або R6Ta R7, замінюють атомами водню 5 Спосіб за п 4, який відрізняється тим, що етерифікацію здійснюють за допомогою кислоти загальної формули (IV) в присутності агента конденсації та активуючого агента в органічному розчиннику при температурі від -10°С до 90°С 6 Спосіб за п 4, який відрізняється тим, що етерифікацію здійснюють за допомогою кислоти загальної формули (IV) у формі симетричного ангідриду, у присутності активуючого агента в органічному розчиннику та при температурі від 0°С до 90°С 7 Спосіб за п 4, який відрізняється тим, що етерифікацію здійснюють, використовуючи кислоту загальної формули (IV) у формі галоіданпдриду або у формі змішаного ангідриду з аліфатичною або ароматичною кислотою, можливо, того, що отримують in situ, в присутності основи, в органічному розчиннику при температурі від 0°С до 80°С 8 Спосіб за п 4, який відрізняється тим, що захисні групи R7 /та/або R6 таR7 замінюють атомами водню, в залежності від їх природи, таким чином 1) коли R6 означає атом водню, a R7 означає захисну для гідроксильної функції групу, захисні групи замінюють атомами водню за допомогою неорганічної або органічної кислоти, що використовують індивідуально або у суміші, в органічному розчиннику, що вибирають з спиртів, простих ефірів, складних ефірів, аліфатичних вуглеводнів, галогенованих аліфатичних вуглеводнів, ароматичних вуглеводнів або нітрилів, при температурі від 10°С до 60°С, або за допомогою джерела фторидюнів, такого як комплекс фтороводневої кислоти з триетиламіном, або шляхом каталітичного гідрування, 2) коли R6Ta R7 разом утворюють насичений п'ятиабо шестичленний гетероцикл загальної формули (VI) в якій RI має вищевказане значення, RsTa Rg, однакові або різні, означають атом водню або алкільний радикал з 1-4 атомами вуглецю, або аралкільний радикал, алкільна частина якого містить 1-4 атоми вуглецю, а арильна частина переважно означає фенільний радикал, можливо, заміщений одним або декількома алкоксильними радикалами з 1-4 атомами вуглецю, або арильний радикал, переважно той, що означає фенільний радикал, можливо, заміщений одним або декількома алкоксильними радикалами з 1-4 атомами вуглецю, або Rs означає алкоксильний радикал з 1-4 атомами вуглецю або тригалогенметильний радикал, такий як трихлорметильний радикал, або фенільний радикал, заміщений тригалогенметильним радикалом, таким як трихлорметильний радикал, та Rg означає атом водню, або Rs та Rg разом з атомом вуглецю, з яким вони зв'язані, утворюють 4-7членний цикл, захисну групу, що утворена R6 та R7, замінюють атомами водню, працюючи, в залежності від значень R-і, RsTa Rg, таким чином а) коли Ri означає трет-бутоксикарбонільний радикал, Rs та Rg, однакові або різні, означають алкільний радикал або аралкільний радикал або арильний радикал, або Rs означає тригалогенметильний радикал або фенільний радикал, заміщений тригалогенметильним радикалом, та Rg означає атом водню, або Rs та Rg разом утворюють 47-членний цикл, складний ефір загальної формули (V) обробляють неорганічною або органічною кислотою, можливо, в органічному розчиннику, такому як спирт, для отримання сполуки загальної формули (VII) (VII) ОН но н OOT C CL ОСОС6Н5 в якій R3, R4 та Rs мають вищевказане значення, який ацилюють за допомогою бензоілхлориду, в якому фенільне ядро, можливо, заміщене, теноілхлориду, фуроілхлориду або сполуки загальної формули (VIII) R2-O-CO-X, (VIII) в якій R2 має вищевказане значення, а X означає атом галогену або залишок -O-R2 або -O-CO-O-R2, для отримання сполуки загальної формули (І), в якій Z означає радикал загальної формули (II), б) коли Ri означає, можливо, заміщений бензоільний радикал, теноільний радикал або фуроільний радикал або радикал 61883 8 R2-O-CO-, чних вуглеводнів та ароматичних вуглеводнів, при температурі від -10°С до 60°С, переважно при 1530°С 9 Фармацевтична композиція, яка відрізняється тим, що вона містить принаймні одну сполуку за будь-яким з пп 1,2 або 3, в якій Z означає радикал загальної формули (II), у сполученні з одним або декількома фармацевтично прийнятними розчинниками або домішками 10 Фармацевтична композиція за п 9, яка відрізняється тим, що вона додатково містить принаймні одну або декілька сумісних та фармакологічно активних сполук Винахід відноситься до області синтезу біологічно активних речовин Більш конкретно, винахід відноситься до нових таксоїдів загальної формули (І) вуглецю, диалкіламіно-радикалу, кожна алкільна частина якого містить 1-4 атоми вуглецю, піперидино-, морфоліно-, піперазин-1-іл-радикала (можливо, заміщеного в положенні 4 алкільним радикалом з 1-4 атомами вуглецю або фенілалкільним радикалом, алкільна частина якого містить 1-4 атоми вуглецю), циклоалкенільного радикалу з 3-6 атомами вуглецю, циклоалкенільного радикалу з 4-6 атомами вуглецю, фенільного радикалу (можливо, заміщеного одним або декількома атомами або радикалами, що вибираються серед атомів галогену та алкільних радикалів з 1-4 атомами вуглецю або алкоксильних радикалів з 1-4 атомами вуглецю), ціано-радикала, карбоксильного радикала або алкоксикарбонільного радикала, алкільна частина якого містить 1-4 атоми вуглецю, - фенільний або а- або р-нафтильний радикал, можливо, заміщений одним або декількома атомами або радикалами, що вибираються серед атомів галогену та алкільних радикалів з 1 -4 атомами вуглецю або алкоксильних радикалів з 1-4 атомами вуглецю, або ароматичний гетероциклічний 5-членний радикал, що вибирається переважно серед фурильного та тиенільного радикалів, або насичений гетероциклічний радикал з 4-6 атомами вуглецю, можливо, заміщений одним або декількома алкільними радикалами з 1-4 атомами вуглецю, в якому F?2 має вищевказане значення, Rs означає атом водню або алкоксильнии радикал з 1-4 атомами вуглецю або фенільний радикал, заміщений одним або декількома алкоксильними радикалами з 1-4 атомами вуглецю, та Rg означає атом водню, захисну групу, що утворена R6 та R7, замінюють атомами водню у присутності неорганічної або органічної кислоти, що використовують індивідуально або у суміші, в стехіометричній або каталітичній КІЛЬКОСТІ, в органічному розчиннику, що вибирають з спиртів, простих ефірів, складних ефірів, аліфатичних вуглеводнів, галогенованих аліфати г-о осос6н5 (|) в якій Z означає атом водню або радикал загальної формули (II) 0 R . ОН в якій Ri означає бензоільний радикал, можливо, заміщений одним або декількома атомами або радикалами, однаковими або різними, що вибираються з атомів галогену та алькільних радикалів з 1 -4 атомами вуглецю, алкоксильних радикалів з 1-4 атомами вуглецю, алкоксильних радикалів з 1-4 атомами вуглецю або трифторметилу, теноільний або фуроільний радикал або радикал R2-O-COв якому R2 означає - алкільний радикал з 1-8 атомами вуглецю, алкенільний радикал з 2-8 атомами вуглецю, алкінільний радикал з 3-8 атомами вуглецю, циклоалкільний радикал з 3-6 атомами вуглецю, циклоалкенільний радикал з 4-6 атомами вуглецю, біциклоалкільний радикал з 7-10 атомами вуглецю, причому ці радикали можуть бути заміщені одним або декількома замісниками, що вибираються серед атомів галогену та гідроксильного радикалу, алкоксильного радикалу з 1-4 атомами R3 означає ЛІНІЙНИЙ або розгалужений алкільний радикал з 1-8 атомами вуглецю, ЛІНІЙНИЙ або розгалужений алкенільний радикал з 2-8 атомами вуглецю, ЛІНІЙНИЙ або розгалужений алкінільний радикал з 2-8 атомами вуглецю, циклоалкільний радикал з 3-6 атомами вуглецю, фенільний або аабо р-нафтильний радикал, можливо, заміщений одним або декількома атомами або радикалами, що вибираются серед атомів галогену та алкільних, алкенільних, алкінільних, арильних, аралкільних, алкоксильних, алкілтю-, арилокси-, арилтю-, гідроксильного, пдроксилалкільного, меркапто-, формільного, ацильного, ациламіно-, ароіламшо-, алкоксикарбоніламшо-, аміно-, алкіламіно-, диалкіламшо-, карбоксильного, алкоксикарбонільного, карбамоільного, алкілкарбамоільного, диалкілкарбамоільного, ціано-, нітро- та трифторметильного радикалів, або ароматичний 5-членний гетероциклічний радикал, що містить один або декілька ге 61883 10 лом з 1-4 атомами вуглецю або фенільним радикалом або фенілалкільним радикалом, алкільна частина якого містить 1-4 атоми вуглецю Переважно, арильними радикалами, які можуть бути представлені R3, є фенільні або а- або Р-нафтильні радикали, можливо, заміщені одним або декількома атомами або радикалами, що вибираються серед атомів галогену (фтор, хлор, бром, йод) та алкільних, алкенільних, алкінільних, арильних, арилалкільних, алкоксильних, алкілтю-, арилоксі-, арилтю-, гідроксильного, пдроксиалкільного, меркапто-, формільного-, ацильного, ациламшо-, ароіламіно, алкоксикарбоніламіно-, аміно, алкіламшо-, диалкіламшо-, карбоксильного, алкоксикарбонільного, карбамоільного, диалкілкарбамошьного, ціано-, нітро-та трифторметильного радикалів, при умові, що алкільні радикали та алкільні частини інших радикалів містять 1-4 атоми вуглецю, що алкенільні та алкінільні радикали місF 4 означає алкоксильний радикал з 1-6 ато? тять 2-8 атомів вуглецю та що арильні радикали мами вуглецю в лінійному або розгалуженому лапредставляють собою фенільні або а- або рнцюгу, алкенилоксі-радикал з 3-6 атомами вугленафтильні радикали цю в лінійному або розгалуженому ланцюгу, алкінилоксі-радикал з 3-6 атомами вуглецю в ліПереважно, гетероциклічні радикали, які монійному або розгалуженому ланцюгу, циклоалкижуть бути представлені R3, локсі-радикал з 3-6 атомами вуглецю, циклоалкепредставляють собою ароматичні гетероцикнилоксі-радикал з 4-6 атомами вуглецю, причому лічні п'ятичленні радикали, що містять один або ці радикали, можливо, заміщені одним або декільдекілька однакових або різних атомів, що вибиракома атомами галогену або алкоксильним радикаються серед атомів азоту, кисню або сірки, можлилом з 1-4 атомами вуглецю, алкілтю-радикалом з во, заміщені одним або декількома однаковими 1-4 атомами вуглецю або карбоксильним радикаабо різними замісниками, що вибираються серед лом, алкілоксикарбонільним радикалом, алкільна атомів галогену (фтор, хлор, бром, йод) та алкільчастина якого містить 1-4 атоми вуглецю, ціаноних радикалів з 1-4 атомами вуглецю, арильних радикалом, карбамоільним радикалом, Nрадикалів з 6-10 атомами вуглецю, алкоксильних алкілкарбамоільним радикалом або N, Nрадикалів з 1-4 атомами вуглецю, арилоксідиалкілкарбамоільним радикалом, кожна алкільна радикалів з 6-10 атомами вуглецю, амшочастина якого містить 1 -4 атоми вуглецю або рарадикалу, алкіламшо-радикалу з 1-4 атомами вугзом з атомом азоту, з яким вона зв'язана, утворює лецю, диалкіламшо-радикалу, кожна алкільна часнасичений гетероциклічний п'яти- або шестичлентина якого містить 1-4 атоми вуглецю, ациламшоний радикал, можливо той, що містить другий герадикалу, ацильна частина якого містить 1-4 атотероатом, який вибирається серед атомів кисню, ми вуглецю, алкоксикарбоніл-амшо-радикалу з 1-4 сірки або азоту, можливо, заміщений алкільним атомами вуглецю, ацильного радикалу з 1-4 аторадикалом з 1-4 атомами вуглецю або фенільним мами вуглецю, арилкарбонільного радикалу, арирадикалом або фенілалкільним радикалом, алкльна частина якого містить 6-10 атомів вуглецю, шьна частина якого містить 1-4 атоми вуглецю, ціано-, карбокси-, карбамоільного радикалу, алкілкарбамоільного радикалу, алкільна частина якого Rs означає алкоксильний радикал з 1-6 атомістить 1-4 атоми вуглецю, диалкілкарбамоільного мами вуглецю в лінійному або розгалуженому ларадикалу, кожна алкільна частина якого містить 1нцюгу (можливо, заміщений алкокси-радикалом з 4 атоми вуглецю, або алкоксикарбоншьного ради1-4 атомами вуглецю) алкенілокси-радикал з 3-6 калу, алкоксильна частина якого містить 1-4 атоми атомами вуглецю, алкінілокси-радикал з 3-6 атовуглецю мами вуглецю, циклоалкілокси-радикал з 3-6 атомами вуглецю, циклоалкенілокси-радикал з 3-6 Переважно, радикали R4 та Rs, однакові або атомами вуглецю, причому ці радикали, можливо, різні, означають ЛІНІЙНІ або розгалужені алкоксизаміщені одним або декількома атомами галогену льні радикали з 1-6 атомами вуглецю, можливо, або алкоксильним радикалом з 1-4 атомами вугзаміщені метокси-, етокси-, етилтю-, карбокси-, лецю, алкілтю-радикалом з 2-4 атомами вуглецю метоксикарбонільним, етоксикарбонільним, ціано-, або карбоксильним радикалом, алкоксикарбонількарбамоільним, N-метилкарбамоільним, Nним радикалом, алкільна частина якого містить 1-4 етилкарбамоільним, N.N-диметилкарбамошьним, атоми вуглецю, ціано-радикалом, карбамоільним N.N-диетилкарбамоільним, Nрадикалом, N-алкілкарбамоільним або N,Nпірролідшокарбонільним або Nдіалкілкарбамоільним радикалом, кожна алкільна піперідинокарбонільним радикалом частина якого містить 1-4 атоми вуглецю або раБільш переважно, даний винахід відноситься зом з атомом азоту, з яким вона зв'язана, утворює до продуктів загальної формули (І), в якій Z ознанасичений гетероциклічний 5- або 6-членний рачає атом водню або радикал загальної формули дикал, можливо той, що містить другий гетеро(II), в Ri означає бензоільний радикал або радикал атом, який вибирається серед атомів кисню, сірки R2-O-CO, в якому R2 означає трет -бутильний раабо азоту, можливо, заміщений алкільним радикадикал, та R3 означає алкільний радикал з 1-6 атотероатомів, однакових або різних, що вибираються серед атомів азоту, кисню або сірки, та, можливо, заміщений одним або декількома замісниками, однаковими або різними, що вибираються серед атомів галогену та алкільних, алкоксильних, арильних, арилоксильних, аміно-, алкіламшо-, диалкіламіно-, ациламшо-, алкоксикарбоніламшо-, ацильного, арил карбонільного, ціано-, карбоксильного, карбамоільного, алкілкарбамоільного, диалкілкарбамоільного або алкоксикарбонільного радикалів, при умовах, що у замісниках фенільного, а- або р-нафтильного та ароматичних гетероциклічних радикалів, алкільні радикали та алкільні частини інших радикалів містять 1-4 атоми вуглецю, та що алкенільні та алкінільні радикали містять 2-8 атомів вуглецю, та що арильні радикали представляють собою фенільні або а- або рнафтильні радикали, 12 11 61883 мами вуглецю, алкенільний радикал з 2-6 атомами вуглецю, циклоалкільний радикал з 3-6 атомами вуглецю, фенільний радикал, можливо, заміщений одним або декількома атомами або радикалами, однаковими або різними, що вибираються серед атомів галогену (фтор, хлор) та алкільних (метил), алкоксильних (метокси-), диалкіламшо- (диметиR ламіно-), ациламіно- (ацетиламшо-), алкоксикарбонідамшо(трет -бутоксикарбоніламшо-) або трифторметшіьного радикалів, або 2- або 3фурильний, 2- або 3-тиенільний або 2ОСОСН тиазолільний, 4-тиазолільний або 5-тиазолільний 6і'5 радикал, та R4 та Rs, однакові або різні, означають, кожний, ЛІНІЙНИЙ або розгалужений алкокси(V) льний радикал з 1-6 атомами вуглецю в якій R-і, R3, R4, R5, R6 та R7 мають вищевказані значення, з послідуючою заміною захисних Ще більш переважно, даний винахід відногруп, що означають як R7 та/або R6 та R7, атомами ситься до продуктів загальної формули (І), в якій Z водню означає атом водню або радикал загальної форЕтерифікацію до складного ефіру за допомомули (II), в якій Ri означає бензоільний радикал гою кислоти загальної формули (IV) можна здійсабо радикал R2-O-CO, в якому R2 означає третнювати в присутності агенту конденсації (карбодибутильний радикал, та R3 означає ізобутильний, ІМІД, реакційноздатний карбонат) та активуючого ізобутенільний, бутенільний, циклогексильний, агенту (амінопіридини) в органічному розчиннику фенільний, 2-фурильний, 3-фурильний, 2(прості ефіри, складні ефіри, кетони, нітрили, алітиенільний, 3-тиенільний, 2-тиазоільний, 4фатичні вуглеводні, галогеновані аліфатичні вугтиазолільний або 5-тиазолільний радикали, R4 та леводні, ароматичні вуглеводні) при температурі R5, однакові або різні, означають, кожний, метоксивід -10°С до90°С , етокси- або пропокси-радикал Етерифікацію також можна здійснювати, викоСполуки загальної формули (І), в якій Z ознаристовуючи кислоту загальної формули (IV) у фочає радикал загальної формули (II), володіє цінрмі симетричного ангідриду та працюючи в присуними протипухлинними та антилейкемічними влатності активуючого агенту (амінопіридини) в стивостями органічному розчиннику (прості ефіри, складні ВІДПОВІДНО даному винаходу, нові продукти заефіри, кетони, нітрили, аліфатичні вуглеводні, гагальної формули (І), в якій Z означає радикал залогеновані аліфатичні вуглеводні, ароматичні вуггальної формули (II), можуть бути отримані шлялеводні) при температурі від 0°С до 90°С хом етерифікації сполуки загальної формули (III) Етерифікацію також можна здійснювати, використовуючи кислоту загальної формули (IV) у формі галогеніду або змішаного ангідриду з аліфатичною або ароматичною кислотою, можливо, що отримується in situ, в присутності основи (третинний аліфатичний амін), працюючи в органічному розчиннику (прості ефіри, складні ефіри, кетони, НО нітрили, аліфатичні вуглеводні, галогеновані аліфатичні вуглеводні, ароматичні вуглеводні) при температурі від 0° С до 80°С Переважно, R6 означає атом водню, a R7 означає захисну групу гідроксильної функції, або ОСОС 6 Н 5 R6 та R7 разом утворюють насичений п'яти- або (III) шестичленний гетероцикл в якій R4 та Rs мають вищевказані значення, Коли R6 означає атом водню, R7 переважно за допомогою кислоти загальної формули (IV) означає метоксиметильний, 1-етоксиетильний, бензоілоксиметильний, триметилсилільний, триS N' O етилсилільний, р-триметилсилілетоксиметильний, бензоілоксикарбонільний або тетрапдропіранільний радикал ОН R. Коли R6 та R7 разом утворюють гетероцикл, то O-R, він представляє собою переважно оксазолідиновии цикл, можливо, монозаміщений або гем(IV) дизаміщений в положенні 2 в якій Ri та R3 мають вищевказані значення, Заміну захисних груп R7 та/або R6 та R7 атота або R6 означає атом водню, a R7 означає захисмами водню можна здійснювати, в залежності від ну групу гідроксильної функції, або R6 та R7 разом їх природи, слідуючим чином утворюють насичений п'яти- або шестичленний гетероцикл, або за допомогою похідної цієї кисло1) коли R6 означає атом водню, a R7 означає ти для отримання складного ефіру загальної форзахисну групу гідроксильної функції, заміну захисмули (V) них груп атомами водню здійснюють за допомогою неорганічної кислоти (соляна кислота, сірчана ки но 14 13 61883 слота, фтористоводнева кислота) або органічної кислоти (оцтова кислота, метансульфокислота, трифторметансульфокислота, птолуолсульфокислота), яку використовують індивідуально або у суміші, працюючи в органічному розчиннику, що вибирається серед спиртів, простих ефірів, складних ефірів, аліфатичних вуглеводнів, галогенованих аліфатичних вуглеводнів, ароматичних вуглеводнів або нітрилів, при температурі від -10°С до 60°С, або за допомогою джерела фторид-юнів, такого, як комплекс фторводOCOC6H5 невої кислоти з триетиламіном, або шляхом каталітичного гідрування, (VII) в якій F?3, R4 та Rs мають вищевказані значен2) коли F 6 або R7 разом утворюють насичений ? ня, який ацилюють за допомогою бензоілхлориду, п'ятичленний або шестичленний гетероцикл та в якому фенільне ядро, можливо, заміщено, теноіпереважно оксазолідиновий цикл загальної форлхлориду, фуроілхлориду або продукта загальної мули (VI) формули (VIII) R2-O-CO-X(VIII) в якій R2 має вищевказане значення, та X означає атом галогену (фтор, хлор) або залишок 0 O-R2 або -O-CO-O-R2, з отриманням продукта загальної формули (І), в якій Z означає радикал загальної формули (II) Rg R , Переважно, продукт загальної формули (V) (VI) обробляють мурашиною кислотою при температув якій Ri має вищевказане значення, a Rs та рі біля 20°С для отримання продукта загальної Rg, однакові або різні, означають атом водню або формули (VII) алкільний радикал з 1-4 атомами вуглецю або Переважно, ацилювання продукта загальної аралкільний радикал, алкільна частина якого місформули (VII) за допомогою бензоілхлориду, в тить 1-4 атоми вуглецю, а арильна частина переякому фенільне ядро, можливо, заміщено, теноілважно означає фенільний радикал, можливо, захлориду або фуроілхлориду або продукта загальміщений одним або декількома алкоксильними ної формули (VIII) здійснюють в інертному органічрадикалами з 1-4 атомами вуглецю, або арильний ному розчиннику, що вибирається серед складних радикал, переважно той, що означає фенольний ефірів, таких, як етилацетат, изопропілацетат або радикал, можливо, заміщений одним або декільн-бутилацетат, та галогенованих аліфатичних вугкома алкоксильними радикалами з 1-4 атомами леводнів, таких, як дихлорметан або 1,2вуглецю, або Rs означає алкоксильний радикал з дихлоретан, в присутності неорганічної основи, 1-4 атомами вуглецю, тригалогенметильний радитакої, як гідрокарбонат натрію, або органічної оскал, такий, як трихлорметильний, або фенільний нови, такої, як триетиламш Реакцію проводять радикал, заміщений тригалогенметильним радипри температурі 0-50°С, переважно біля 20°С, калом, таким, як трихлорметильний радикал, a Rg б) коли Rj означає бензоільний радикал, можозначає атом водню, або ж Rs та Rg разом з атоливо, заміщений, теноільний або фуроільний рамом вуглецю, з яким вони зв'язані, утворюють 4-7дикал або радикал членний цикл, тоді заміну захисної групи, що утвоR2O-COрена R6Ta R7, на атоми водню можна здійснювати, в якому R2 має вищевказане значення, Rs в залежності від значень Ri, Rs та Rg, слідуючим означає атом водню або алкоксильний радикал з чином 1-4 атомами вуглецю або фенільний радикал, заа) коли Ri означає трет-бутоксикарбонільний міщений одним або декількома алкоксильними радикал, Rs та Rg, однакові або різні, означають радикалами з 1-4 атомами вуглецю, та Rg означає алкільний радикал, або аралкільний радикал (бенатом водню, то заміну захисної групи, що утворена зил), або арильний радикал (феніл), або ж Rs R6Ta F?7, на атоми водню здійснюють в присутності означає тригалогенметильний радикал або фенінеорганічної кислоти (соляна кислота, сірчана кильний радикал, що заміщений тригалогенметильслота) або органічної кислоти (оцтова кислота, ним радикалом, та Rg означає атом водню, або Rs метансульфокислота, трифторметансульфокислота Rg разом утворюють 4-7-членний цикл, обробта, п-толуолсульфокислота), яку використовують ляють складний ефір загальної формули (V) неоріндивідуально або у суміші, в стехіометричній або ганічною або органічною кислотою, можливо, в каталітичній КІЛЬКОСТІ, працюючи в органічному органічному розчиннику, такому, як спирт, з отрирозчиннику, що вибирається серед спиртів, просманням продукту загальної формули (VII) тих ефірів, складних ефірів, аліфатичних вуглеводнів, при температурі від -10°С до 60°С, переважно при 15-ЗСГС ВІДПОВІДНО винаходу, продукти загальної формули (III), тобто продукти загальної формули (І), в якій 2означає атом водню, R4 та Rs мають вищевказані значення, можуть бути отримані з 10 683 18 15 дезацетил-баккатину (III) формули (IX) Q но. о н НО НО' ОСОСД осос б н 5 (IX) Особливо переважно селективно захищати гідроксильні функції в положеннях 7 та 13, наприклад, у формі простого силільованого диефіру, який може бути отриманий шляхом дії силілгалогеніду загальної формули (X) (RbSi-Гал (Х) в якій R, однакові або різні, означають алкільний радикал з 1-6 атомами вуглецю, можливо, заміщений фенільним радикалом, або циклоалкільний радикал з 3-6 атомами вуглецю, або фенільний радикал, на 10-дезацетил-баккатин (III) з отриманням сполуки загальної формули (XI) но о O-SUR) (R)3Si-O'"' OCOC.H, (XI) в якій R має вищевказане значення, яку потім обробляють сполукою загальної сполуки (XII) R'4Xi (XII) в якій RV означає радикал, такий, що RVO ідентичний радикалу R4, що має вищевказане значення, а Хі означає залишок реакційноздатного складного ефіру, такий, як залишок ефіру сірчаної кислоти або сульфокислоти, або атом галогену, для отримання продукта загальної формули (XIII) 0 0-SiflOj ОСОС 6 Н 5 (XIII) 1 6 та загальної формули (XIV) в якій R та R4 мають вищевказане значення, потім силільовані захисні групи отриманої сполуки заміняють атомами водню для отримання продук (XIV) в якій R4 має вищевказане значення, який селективно етерифікують в положенні 7 шляхом дії сполуки загальної формули (XV) RVX 2 (XV) в якій R^ означає радикал, такий, що R's-0 ідентичний радикалу Rs, що має вищевказане значення, а Хг означає атом галогену або залишок реакційноздатного складного ефіру, такий, як залишок ефіру сірчаної кислоти або сульфокислоти, для отримання продукта загальної формули (III) Звичайно, обробку силільованою похідною загальної формули (X) 10-дезацетил-баккатину (III) здійснюють в піридині або триетиламші, можливо, в присутності органічного розчинника, такого, як ароматичний вуглеводень, такий, як бензол, толуол та ксилоли, при температурі від 0°С до температури кипіння з зворотнім холодильником реакційної суміші Звичайно, взаємодію сполуки загальної формули (XII) з сполукою загальної формули (XI) здійснюють після утворення солі металу з гідроксильною функцією в положенні 10 за допомогою гідриду лужного металу, такого, як гідрид натрію, аміду лужного металу, такого, як амід ЛІТІЮ, або алкільної похідної лужного металу, такого, як буТИЛЛІТІЙ, працюючи в органічному розчиннику, такому, як диметилформамід або тетрапдрофуран, при температурі 0-50°С Звичайно, заміну силільованих захисних груп сполуки загальної формули (XIII) атомами водню здійснюють за допомогою кислоти, такої, як фторводнева кислота або трифтороцтова кислота, в присутності основи, такої, як триетиламш або піридин, можливо, заміщений одним або декількома алкільними радикалами з 1-4 атомами вуглецю, при необхідності, у сполученні з інертним органічним розчинником, таким, як, наприклад, ацетонітрил, або галогенований аліфатичний вуглеводень, наприклад, дихлорметан, при температурі 0-80°С Звичайно, взаємодію сполуки загальної формули (XV) з сполукою загальної формули (XIV) здійснюють в умовах, ідентичних вищевказаним для обробки сполукою загальної формули (XII) сполуки загальної формули (XI) ВІДПОВІДНО винаходу, сполуки загальної формули (І), в якій Z означає радикал загальної формули (II), R4 має вищевказане значення, та Rs має вищевказане значення, можна отримувати з сполуки загальної формули (XVI) 17 N 683 18 О О 0-R но OCOCSH5 (XVI) в якій R-i, R3, F?6 та R7 мають вищевказане значення, шляхом силілювання в положенні 7 за допомогою сполуки загальної формули (X) для отримання сполуки загальної формули (XVII) 1 8 яка після взаємодії з сполукою загальної формули (XV), приводить до сполуки загальної формули (V), захисні групи якої замінюють атомами водню, отримуючи продукт загальної формули (І), в якій Z означає радикал загальної формули (II) Реакції силілювання, функціоналізацм та заміни захисних груп атомами водню здійснюють в умовах, аналогічним вищеописаним Сполуки загальної формули (XVI) можна отримувати в умовах, описаних в європейському патенті 0 336 841 та міжнародних заявках 92/09589 та 94/07878, або з сполук загальної формули (XX) но. 9 R ОСОС 6 Н 5 но ( VI X I) (XX) осоед в якій R, R-i, R3, R6 та R7 мають вищевказане значення, яке функцюналізує в положенні 10 за допомогою сполуки загальної формули (XII) з отриманням сполуки загальної формули (XVIII) Rr O-SKR) N О в якій Ri та R3 мають вищевказане значення, ВІДПОВІДНО відомим способам захисту гідроксильної функції у бічному ланцюгу, не торкаючись остальної частини молекули ВІДПОВІДНО винаходу, сполуки загальної формули (І), в якій Z означає атом водню або радикал загальної формули (II), можна отримувати шляхом впливу активованим нікелем Ренея в присутності аліфатичного спирту з 1-3 атомами вуглецю або простого ефіру, такого, як тетрапдрофуран або диоксан, на сполуку загальної формули (XXI) 0 R 0-R, НО ОСОС6Н5 (XVIII) в якій R, R-i, R3, R6 та R7 мають вищевказане значення, силільовану захисну групу якого замінюють атомом водню для отримання сполуки загальної формули (XIX) Г\ГПГ Н N (XXI) 0 0 R. O-R. ОСОСН. ОСОС6Н5 (XIX) в якій R4 має вищевказане значення, R' та R", однакові або різні, означають атом водню або алкільний радикал з 1-6 атомами вуглецю, алкенільний радикал з 2-6 атомами вуглецю, алкінільний радикал з 2-6 атомами вуглецю, циклоалкільний радикал з 3-6 атомами вуглецю або циклоалкенільний радикал з 3-6 атомами вуглецю, можливо, заміщений, або ж R' та R" разом з атомом вуглецю, з яким вони зв'язані, утворюють циклоалкільний радикал з 3-6 атомами вуглецю 19 W 4 R (XXII) в якій R-i, R3, R6 та R7 мають вищевказане значення, отримують сполуку загальної формули (XXIII) ОСОС 6 Н 5 (XXIII) з наступною, коли Zi означає радикал загальної формули (XXII), тобто коли сполука загальної формули (XXIII) ідентична сполуці загальної формули (V), заміною захисних груп, що позначаються як R6 та/або R6 та R7, атомами водню в вищеописаних умовах Звичайно, активованим нікелем Ренея в присутності аліфатичного спирту або простого ефіру впливають при температурі від -10°С до 60°С ВІДПОВІДНО винаходу, сполука загальної формули (XXI), в якій Zi та R4 мають вищевказане значення, можна отримати шляхом взаємодії сульфоксиду загальної формули (XXIV) R' 20 61883 або циклоалкенільний радикал з 4-6 атомами вуглецю, Zi означає атом водню або радикал загальної формули (XXII) R1 (XXIV) в якій R' та R" мають вищевказане значення, з сполукою загальної формули (XIX) Звичайно реакцію сульфоксиду загальної формули (XXIV), переважно диметилсульфоксиду, з сполукою загальної формули (XIX) проводять в присутності суміші оцтової кислоти з оцтовим ангідридом або похідної оцтової кислоти, такої, як галогеноцтова кислота, при температурі 0-5 0°С, переважно біля 25°С Винахід відноситься також до 4а-ацетокси-2абензоілокси-5р, 20-епокси-1 р-пдрокси-7р, 10р-біс (метилтюметокси)-9-оксо-такс-11 -ен-1 За-іл /2R, 4S,5R/3-TpeT бутоксикарбоніл-2 (4-метоксифеніл)4-феніл-1,3-оксазолідин-5-карбоксилату, що використовується в якості проміжного продукту для отримання диметоксипохідної таксомеру, а саме 4а-ацетокси-2а-бензоілокси-5р-20-епокси-ірпдрокси-7р, 10р-диметокси-9-оксо-такс-11-ен-13аin-(2R, 3S)-3-TpeT -бутоксикарбоніламшо-2пдрокси-Зфеніл-пропюнату Винахід відноситься також до способу отримання 4а-ацетокси-2а-бензоілокси-5р, 20-епоксиір-пдрокси-7р, 10р-диметокси-9-оксо-такс-11-ен13a-in-(2R,3S)-3-TpeT -бутокси-карбоніламшо-2пдрокси-3-феніл-прошонату, що заклинається в тому, що на першому етапі 4а-ацетокси-2абензошокси-5р, 20-епокси-1р 7р, 10р-трипдрокси9-OKCO-TaKC-11-eH-13a-in-(2R,4S,5R)-3-TpeTбутоксикарбоніл-2-(4-метоксифеніл)-4-феніл-1,3 оксазолідин-5-карбоксилат оборобляють диметилсульфоксидом у присутності оцтової кислоти, на другому етапі отриманий 4а-ацетокси-2абензоілокси-5р, 20-епокси-1 р-пдрокси-7р, 10р-біс (метилтюметокси)-9-оксо-такс-11 -ен-1 За-іл(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(4метоксифеніл)-4-феніл-1,3-оксазолідин-5карбоксилат піддають взаємодії з етанольною суспензією нікеля Ренея, та на третьому етапі отриманий 4а-ацетокси-2а-бензоілокси-5р, 20-епоксиір-пдрокси-7р, 10р-диметокси-9-оксо-такс-11-ен13a-in-(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(4метоксифеніл-4-феніл-1,3-оксазолідин-5карбоксилат піддають взаємодії з етанольним розчином соляної кислоти Нові сполуки загальної формули (І), що отримуються шляхом здійснення способів ВІДПОВІДНО винаходу, можуть бути очищені відомими методами, такими, як кристалізація або хроматографія Продукти загальної формули (І), в якій Z означає радикал загальної формули (II), володіють чудовими біологічними властивостями Оцінка антипроліферативних властивостей Концентрацію лікарського засобу, що дає 50% інгібування росту (ICso), визначали з двох або трьох окремих експериментів в 96-лунковому планшеті для мікрокультивування КЛІТИННІ ЛІНІЇ, що ВИСІЯНІ при Зх104-Зх105клітин/мл (0,2мл/лунка), вирощували на протязі 96-120 годин в присутності різних концентрацій лікарського засобу (кожна точка повторювалась чотири рази) Потім клітини шкубували на протязі 16 годин з 0,02% нейтральним червоним Клітини промивали та піддавали лізису з 1% SDS Включення барвника, що відображує клітинний ріст та життєздатність, оцінювали шляхом виміру оптичної густини для кожної лунки при 540 та 346нм, використовуючи Titertec багатолунковий спектрофотометр У дослідженнях шанування KB клітини людського епідермоідного раку в експоненційному рості оброблювали на протязі 1 години у рідкому середовищі, потім промивали та виливали з Noble Difco Адаг в чашки Петрі (4 чашки/концентрація), як описано раніше КІЛЬКІСТЬ КЛІТИННИХ КЛОНІВ (>60 КЛІТИН) вимірювали після 15 днів після інкубації при 37°С у повлажненій атмосфері з 5% СОг Результати приведені в таблиці 1 FU Я 8, ЙДН Z-OOCOCHj % - Н или Я 21 22 61883 Таблиця 1 Пример Ri R3 R4 R5 1 і2 3 4 t-BuO-CO t-BuO-CO t-BuO-CO СєНб СєНб СєНб СНзО СН3СН2О СН3СН(СНз)О СНзО СНзО СНзО В тесті in vitro визначення біологічної активності здійснюють натубулині, вилученому з головного мозку свині, по методу М L Shelanski та співроб , Ргос Natl Acad Sci USA, 70, 765-768 (1973) Вивчення деполімеризації мікротрубочок до тубулину здійснюють по методу G Chauviere та співроб , С R Acad Sci, 293, серія II, 501-503 (1981) При цьому дослідженні продукти загальної формули (І), в якій Z означає радикал загальної формули (II), є принаймні такими же активними, як таксол та таксотер В тесті in vivo продукти загальної формули (І), в якій Z означає радикал загальної формули (II), показали себе активними в тесті з мишами, якій трансплантували меланому В16, в дозах, що складають від 1 до 10 мг/кг при штраперитональному введенні, а також у випадку рідких або твердих пухлин Нові продукти володіють протипухлинними властивостями, більш конкретно, володіють актив СІ50 мкг/мл клетки KB 0 029 0 006 0 150 містять тільки цільовий продукт, об'єднують та концентрують досуха при зниженому тиску (0 27кПа) при 40°С на протязі двох годин Таким чином отримують 271 8мг 4а-ацетокси-2абензоілокси-5р, 20-епокси-1 р-пдрокси-7р, 10рflHMeTOKCH-9-OKCO-TaKC-11-eHa-13a-in-(2R,4S,5R)-3трет -бутоксикарбоніл-2-(4-метоксифеніл)-4-феніл1,3-оксазолідин-5-карбоксилата у вигляді твердої речовини білого кольору, характеристики якої слідуючі (DOX), яка експресує ген mdr 1 - 1 Н-ЯМР-спектр (400МГц, дейтерохлороформ з декількома краплинами дейтерованого метанолу, хімздвиги 5 в м д (МІЛЬЙОННІ частки), константи зв'язування J в Гц) 1 02 (с, 9Н С(СН 3 )з), 1 10 (с, ЗН СНз), 1 17 (с, ЗН СНз), 1 63 (с, ЗН СН 3 ), 1 651 85 та 2 60 (2м, 1Н кожний С Н 2 в положенні 6), 1 78 (масив, ЗН СН 3 ), 2 02 та 2 15 (2 дд, J = 14 та 9, 1Н кожний С Н 2 в положенні 14), 2 14 (с, ЗН СНз), 3 22 та 3 35 (2 с, ЗН кожний ОСН 3 ), 3 64 (д, J = 7, 1Н Н в положенні 3), 3 37 (м, 1Н Н в положенні 7), 3 7 6 ( с , ЗН АЮСНз), 4 06 та 4 16 (2 д, J = 8 5, 1Н кожний С Н 2 в положенні 20), 4 53 (д, J=5, 1Н Н в положенн 2'), 4 67 (с, 1Н Н в положенні 10), 4 85 (уш д, J=10, 1 H H в положенні 5),5 36 (м, 1 Н Н в положенні 3'),5 52 (д, J=7, 1 H H в положенні 2), 6 07(м, 1 Н Н в положенні 13), 6 33 (масив, 1 Н Н в положенні 5 і ), 6 88 (д, J=8,2H ароматичні Н в ортоположенні до ОСНз), 7 25-7 40 (м, 7Н ароматичні Н в положенні 3' та ароматичні Н в мета-положенні до ОСНз), 7 43 (т, J=7 5,2Н ОСОС 6 Н 5 - Н в параположенні), 7 58 (т, J=7 5,1Н ОСОС6Н5-Н в параположенні), 7 96 (д, J=7 5,2Н ОСОС 6 Н 5 - Н в ортоположенні Слідуючі приклади ілюструють даний винахід Приклад 1 До суспензії, що містить 217 8мг 4а-ацетокси2а-бензоілокси-5р, 20-епокси-1р,13а-дипдрокси7р, Юр-диметокси-9-оксо-такс-И-ена, 200мг (2R, 4S, 5R)-3-TpeT -бутоксикарбоніл-2-(4метоксифеніл)-4-феніл-1,3-оксазолідин-5карбонової кислоти та 50мг молекулярного решета 4 А у вигляді порошка в 2см3 етилацетату, при температурі біля 20°С послідовно додають 126мг дициклогексикарбодиіміду, потім 14мг 4-N.N'диметилоамшо-піридину Отриману суспензію перемішують при температурі біля 20°С і в атмосфері аргону на протязі 16 годин, потім концентрують досуха при зниженому тиску (0 27кПа) при температурі біля 40°С Отриманий залишок очищають шляхом хроматографії при атмосферному тиску при використанні 50г диоксиду кремнію (0 0630 2мм), що містить в колонці диаметром 2см (градієнт елюювання суміш етилацетату з дихлорметаном у співвідношенні) від 10 90 до 40 60 по об'єму), збираючи фракції по 10см Фракції, що Розчин 446 Змг 4а-ацетокси-2а-бензоілокси5р, 20-епокси-ір-пдрокси-7р, 10р-диметокси-9OKCO-TeKC-11-eH-13a-in-(2R,4S,5R)-3-TpeT бутоксикарбоніл-2-(4-метоксифеніл)-4-феніл-1,3оксазолідин-5-карбоксилата в 11 6см 3 0 1н розчину хлороводню в етанолі витримують при перемішувнні та при температурі біля 0°С на протязі 16 годин в атмосфері аргону Реакційну суміш потім розбавляють за допомогою 40см 3 дихлорметану та 5см 3 дистильованої води Після декантації, водну фазу екстрагують за допомогою 5см 3 дихлорметану Органічні фази об'єднують, сушать над сульфатом магнію, фільтрують через фільтр з фритованого скла, потім концентрують при зниженому тиску (0 27кПа) при температурі біля 40°С Таким чином отримують 424,2мг твердої речовини блідожовтого кольору, яку очищають шляхом препаративної тонкошарової хроматографії (12 препаративних пластин фірми Мерк, силікагель 60F254, товщина 1мм, нанесення у вигляді розчину у суміші метанолу з дихлорметаном (у об'ємному співвідношенні 5 95)) Після елюювання зони, що відповідає ністю у відношенні пухлин, які СТІЙКІ до таксолу® або таксотеру® Такі пухлини включають пухлини ободової кишки, які мають високу експресію гену mdr 1 (ген СТІЙКОСТІ до багаточисленних лікарських засобів) Термін "СТІЙКІСТЬ ДО багаточисленних лі карських засобів" представляє собою загальноприйнятий термін, що означає СТІЙКІСТЬ пухлин до різних продуктів різних структур та різних механіз мів дії Таксоїди взагалі ВІДОМІ ТИМ, ЩО ВОНИ у ви сокому ступені розпізнаються експериментальними пухлинами, такими, як P388/DOX, ЛІНІЯ КЛІТИН, що вибирається по и СТІЙКОСТІ ДО доксорубицину 23 61883 основному продукту, сумішшю метанолу з дихлорметаном (в об'ємному співвідношенні 15 85), фільтрації через фільтр з фритованого скла, потім випарювання розчинників при зниженому тиску (0 27кПа) при температурі біля 40°С, отримують 126мг 4а-ацетокси-2а-бензоілокси-5р, 20-епоксиір-пдрокси-7р, Юр-диметокси-Э-оксо-такс-И-ен13a-in-(2R,3S)-3-TpeT -бутоксикарбоніламшо-2пдрокси-3-феніл-пропюната у вигляді повітряної маси кольору слонової кістки, характеристики якого слідуючі - обертальна здатність ао20=-32 9° (с=0 5, метанол) -1Н-ЯМР-спектр (400МГц, дейтерохлороформ, хімздвиги 5 в м д , константи зв'язування J в Гц) 1 23 (с, ЗН СНз), 1 25 (с, ЗН СН3), 1-39 (с, 9Н С(СНз)з), 1 70 (с, 1Н ОН в положенні 1), 1 75 (с, ЗН СНз), 1 82 та 2 72 (2 м, 1Н кожний СН 2 в положенні 6), 1 91 (с, ЗН СНз), 2 31 (АВ обмежений, 2Н СН 2 в положенні 14), 2 39 (с, ЗН СОСН3), 3 33 та 3 48 (2 с, ЗН кожний ОСН3), 3 48 (м, 1Н ОН в положенні 2'), 3 85 (д, J = 7, 1Н Н в положенні 3), 3 88 (дд, J = 11 та 7, 1Н Н в положенні 7), 4 20 та 4 33 (2 д, J = 8 5, 1Н кожний СН 2 в положенні 20), 4 65 (м, 1Н Н в положенні 2% 4 83 (с, 1Н Н в положенні 10), 5 00 (уш д, J = 10, 1Н Н в положенні 5), 5 30 (уш д, J = 10, 1Н Н в положенні 3і), 5 47 (д, J = 10,1Н CONH), 5 66(д, J = 7, 1Н Н в положенні 2), 6 24 (ушт, J = 9, Ш Н в положенні 13), 7 30-7 50 (м, 5Н ароматичні Н в положенні 3'), 7 52 (т, J = 7 5, 2Н ОСОС6Н5 - Н в мета-положенні), 7 63 (т, J = 7 5, 1Н ОСОС6Н5 -Н в пара-положенні), 812 (д, J = 7 5, 2Н ОСОСєНб - Н в орто-положенні) 4а-Ацетокси-2а-бензоілокси-5р, 20-епокси-1р, 13а-дипдрокси-7р, Юр-диметокси-9-оксо-такс-Иен (або 7(3, 10р-диметокси-10-дезатокси-баккатин (III)) може бути отриманий слідуючим чином До розчину 500мг 4а-ацетокси-2а-бензоілокси5р, 20-епокси-1 (3,7(3,1 За-трипдрокси-10р-метокси9-оксо-такс-11-ена в 5см 3 йодметану та 0 5см 3 диметилформаміду, що знаходиться в атмосфері аргону, при температурі біля 0°С порціями додають 86мг 50%-ного (за масою) гідриду натрію у вазелиновому маслі Після витримування на протязі 45 хвилин при температурі біля 0°С, реакційну суміш розбавляють за допомогою 50см3 етилацетату та 8см 3 дистильованої води Після декантації органічну фазу промивають два рази по 8см3 дистильованою водою, потім 8см3 водного насиченого розчину хлориду натрію, сушать над сульфатом магнію, фільтрують через фільтр з фритованого скла та концентрують досуха при зниженому тиску (0 27кПа) при температурі біля 40°С Таким чином отримують 570мг твердої речовини блідо-жовтого кольору, яку очищають шляхом хроматографії при атмосферному тиску при використанні 50г диоксиду кремнію (0 063-0 2мм), що знаходяться в колонці діаметром 2 5см, елюючи сумішшю метанолу з дихдфметаном (в об'ємному співвідношенні 2 98) та збираючи фракції по 10см3 Фракції, що містять тільки цільовий продукт, об'єднують та концентрують при зниженому тиску (0 27кПа) при 40°С на протязі двох годин Таким чином отримують 380мг 4а-ацетокси-2а-бензоілокси-5р,20-епокси-1 р, 13адипдрокси-7р, 10р-диметокси-9-оксо-такс-11-єна у вигляді твердої речовини блідо-жовтого кольору, 24 характеристики якої слідуючі 1 Н-ЯМР-спектр (400МГц, дейтерохлороформ з декількома краплинами дейтерованого метанолу, хімздвиг 5 в м д , константи зв'язування J в Гц) 1 03 (с, ЗН СНз), 111 (с, ЗН СНз), 1 65 (с, ЗН СНз), 1 72 та 2 67 (2м, 1Н кожний СН 2 в положенні 6), 2 05 (с, ЗН СНз), 2 21 (АВ обмежений, J = 14 та 9, 2Н СН 2 в положенні 14), 2 25 (с, ЗН СОСН3), 3 26 та 3 40 (2с, ЗН кожний ОСН3), 3 85 (д, J = 7,1Н Н в положенні 3), 3 89 (дд, J = 11 та 6 5, 1Н Н в положенні 7), 4 12 та 4 25 (2 д , J = 8 5, 1Н кожний СН 2 в положенні 20), 4 78 (уш т, J = 9, 1Н Н в положенні 13), 4 83 (с, 1Н Н в положенні 10), 4 98 (уш д, J = 10, 1Н Н в положенні 5), 5 53 (д, J = 7 1Н, Н в положенні 2), 7 43 (т, J = 7 5, 2Н ОСОС6Н5 -Н в мета-положенні), 7 56 (т, J = 7 5, 1Н ОСОСєНб- Н в пара-положенні), 8 05 (д, J = 7 5, 2Н ОСОСєНб - Н в орто-положенні) 4а-Ацетокси-2а-бензошокси-5р, 20-епокси1р,7р,1 За-трипдрокси-10р-метокси-9-оксо-такс-11ен (або 10р-метокси-10-дезацетокси-баккатин (III)) може бути отриманий слідуючим чином До розчину 3 62г 4а-ацетокси-2а-бензоілокси5р, 20-епокси-1 р-пдрокси-10р-метокси-9-оксо-7[3, 13а-бістриетилсилілокси-такс-11-ена в 30см3 дихлорметану, що знаходиться в атмосфері аргону при температурі біля 0°С, повільно додають 50см комплексу фторводню з триетиламіном (3HF EtsN) Після витримування на протязі 48 годин при температурі біля 20°С, реакційну суміш виливають в суспензію 100см3 водного пересиченого розчину гідрокарбонату натрію, що підримується при температурі біля 0°С Після декантації водну фазу повторно екстрагують три рази по 80см3 дихлорметаном, потім два рази по 80см3 етилацетатом Органічні фази об'єднують, сушать над сульфатом магнію, відфільтровують та концентрують досуха при зниженому тиску (0 27кПа) при температурі біля 40°С Таким чином отримують 3 45г жовтого кольору повітряної маси, яку очищають шляхом хроматографії при атмосферному тиску при використанні 150г диоксиду кремнію (0 063-0 2мм), що містяться в колонці діаметром 3 5см, елюючи сумішшю метанолу з дихлорметаном у об'ємному співвідношенні 5 95 та збираючи фракції по 35см Фракції, що містять тільки цільовий продукт, об'єднують та концентрують досуха при зниженому тиску (0 27кПа) при 40°С на протязі двох годин Таким чином отримують 1 97г 4а-ацетокси-2абензоілокси-5р, 20-епокси-ір,7р,13а-трипдрокси10р-метокси-9-оксо-такс-11-ена у вигляді твердої речовини білого кольору, характеристики якого слідуючі -1Н-ЯМР-спектр (400МГц, дейтерохлороформ, хімздвиги 5 в м д , константи зв'язування J в Гц) 1 10 (с, ЗН СНз), 1 19 (с, ЗН СНз), 1 48 (д, J = 8 5, 1Н ОН в положенні 13), 1 70 (с, ЗН СН3), 1 81 та 2 61 (2м, 1Н кожний СН 2 в положенні 6), 2 09 (д, J = 5,1Н ОН в положенні 7), 2 11 (с, ЗН СН3), 2 30 (с, ЗН СОСНз), 2 32 (д, J = 9, 2Н СН 2 в положенні 14), 3 48 (с, ЗН ОСНз), 3 97 (д, J = 7, 1Н Н в положенні 3), 4 18 та 4 33 (2 д, J = 8 5, 1Н кожний СН 2 в положенні 20), 4 31 (м, 1Н Н в положенні 7), 4 93 (м, 1Н Н в положенні 13), 4 99 (с, 1Н Н в положенні 10), 5 01 (уш д , J = 10, 1Н Н в положенні 5), 5 66 25 26 (д, J = 7 5, 2Н ОСОСєНб - Н в орто-положенні) 4а-Ацетокси-2а-бензоілокси-5р, 20-епокси-1р, 10р-дипдрокси-9-оксо-7р,13а-бістриетилсилілокситакс-11 -єн (або 10-дезацител-7,13бістриетилсиліл-баккатин (III)) може бути отриманий слідуючим чином До розчину 14г 4а-ацетокси-2а-бензоілокси5р, 20-епокси-ір,7р,10р,13а-тетрапдрокси-9-оксотакс-11-ена (10-дезацетил-баккатина (III)) в 50см3 безводного піридину, що підтримується в атмосфері аргону, при температурі біля 20°С додають 10 8см триетилсилілхлориду Після витримування на протязі 17 годин при температурі біля 20°С, реакційну суміш доводять до температури біля 115°С, потім додають 10 8см триетилсилілхлориду Після витримування на протязі трьох годин 15 хвилин при температурі 115°С, реакційну суміш доводять до температури біля 20°С, розбавляють за допомогою ЗО см 3 етилацетату та 100см3 дистильованої води Після декантації водну фазу екстрагують 2 рази по 50см3 етилацетатом Органічні фази об'єднують, промивають за допомогою 50см3 водного насиченого розчину хлориду натрію, сушать над сульфатом магнію, фільтрують через фільтр з фритованого скла, потім концентрують досуха при зниженому тиску (0 27кПа) при температурі біля 40°С Таким чином отримують 63 1г коричневого кольору масло, яке очищають шляхом хроматографії при атмосферному тиску при використанні 800г диоксиду кремнію (0 063-0 2мм), що містяться в колонці діаметром 7см (градієнт елюювання суміш етилацетата з дихлорметаном в об'ємному співвідношенні від 0 100 до 5 95), збираючи фракції по 60см3 Фракції, що містять тільки цільовий продукт, об'єднують та концентрують досуха при зниженому тиску (0 27кПа) при 40°С на протязі 2 годин Таким чином отримують 9 77г 4аацетокси-2а-бензоілокси-5р, 20-епокси-1 р, 10рдипдрокси-9-оксо-7р,13а-бістриетилсилілокситакс-11-ена у вигляді повітряної маси кремнієвого кольору, характеристики якого слідуючі 1 Н-ЯМР-спектр (400МГц, дейтерохлороформ, хімздвиги 5 в м д , константи зв'язування J в Гц) 0 55 та 0 68 (2 м, 6Н кожний СН 2 етила), 0 94 та 1 03 (2 т, J = 7 5, 9Н кожний СН 3 етила), 1 08 (с, ЗН СНз), 1 17 (с, ЗН СНз), 1 58 (с, 1Н ОН в положенні 1), 1 73 (с, ЗН СНз), 1 91 та 2 57 (2 м, 1Н кожний СН 2 в положенні 6), 2 04 (с, ЗН СН3), 2 12 та 2 23 (2 дд, J = 16 та 9, 1Н кожний СН 2 в положенні 14), 2 30 (с, ЗН СОСНз), 3 88 (д, J = 7, 1Н Н в положенні 3), 4 16 та 4 32 (2 д, J = 8 5, 1Н кожний СН 2 в положенні 20), 4 27 (д, J = 1, 1Н ОН в положенні 10), 4 40 (дд, J = 11 та 7, 1Н Н в положенні 7), 4 95 (уш д, J = 10, 1Н Н в положенні 5), 4 95 (м, 1Н Н в положенні 13), 5 16 (д, J = 1, 1Н Н в положенні 10), 5 60 (д, J = 7, 1Н Н в положенні 2), 7 46 (т, J = 7 5, 2Н ОСОС6Н5 - Н в метаположенні), 7 60 (т, J = 7 5,1Н ОСОС6Н5 - Н в пара-положенні), 8 09 (д, J = 7 5,2Н ОСОС6Н5 - Н в орто-положенні) Приклад 2 340мг 4а-ацетокси-2а-бензилокси-5р, 20епокси-ір-пдрокси-7р,10р-диметокси-9-оксо-такс11 -ен-13a-in-(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2(4-метоксифеніл)-4-феніл-1 З-оксазолідин-5 61883 (д, J = 7,1Н Н в положенні 2), 7 49 (т, J = 7 5,2Н ОСОСєНб - Н в мета-положенні), 7 63 (т, J = 7 5, 1Н ОСОС6Н5 - Н в пара-положенні), 8 12 (д, J = 7 5, 2Н ОСОСєНб - Н в орто-положенні) 4а-Ацетокси-2а-бензоілокси-5р, 20-епокси-1рпдрокси-Юр-метокси-Э-оксо^р^Забістроетилсилілокси-такс-11-ен (або 10р-метокси10-дезацетокси-7-13-бістриетилсиліл-баккатин (III) може бути отриманий слідуючим чином До розчину 5г 4а-ацетокси-2а-бензоілокси-5р, 20-епокси-1 р, 10р-дипдрокси-9-оксо-7р,1 Забістроетилсилілокси-такс-11-ена в 25см3 йодметану, що підтримується в атмосфері аргону, при температурі біля 0°С порціями додають 375мг 50%ного (по масі) гідриду натрію у вазелиновому маслі Розчин витримують при перемішуванні на протязі 45 хвилин при температурі біля 0°С, потім на протязі 5 годин ЗО хвилин при температурі біля 20°С Реакційну суміш знову охолоджують до температури біля 0°С та порціями додають 125 мг 5%-ного (по масі) пдрида натрію у вазелиновому маслі Після витримування на протязі 1 години при 20°С, потім 18 годин при 5°С, реакційну суміш розбавляють за допомогою 50см3 дихлорметану, виливають в 50см3 водного насиченого розчину хлориду аммонію та декантують Водну фазу екстрагують 2 рази по 30см3 дихдерметаном, потім органічні фази об'єднують, промивають за допомогою 10см3 дистильованої води, сушать над сульфатом магнію, фільтрують через фільтр з фритованого скла та концентрують досуха при зниженому тиску (0 27кПа) при температурі біля 40°С Таким чином отримують 515г повітряної маси жовтого кольору, яку очищають шляхом хроматографії при атмосферному тиску при використанні 300г диоксиду кремнію (0 063-0 2мм), що містяться в колонці діаметром 5см (градієнт елюювання суміш етилацетата з дихорметаном в об'ємному співвідношенні від 0 100 до 10 90), збираючи фракції по 30см3 Фракції, що містять тільки цільовий продукт, об'єднують та концентрують досуха при зниженому тиску (0 27кПа) при 40°С на протязі двох годин Таким чином отримують 3 62г 4а-ацетокси-2а-бензоілокси-5р, 20-епокси-1рпдрокси-10р-метокси-9-оксо-7р,13абістриетилсилілокси-такс-11-ена у вигляді повітряної маси блідо-жовтого кольору, характеристики якого слідуючі 1 Н-ЯМР-спектр (600МГц, дейтерохлороформ, хімздвиги 5 в м д , константи зв'язування в Гц) 0 58 та 0 69 (2 м, 6Н кожний СН 2 етила), 0 97 та 1 04 (2 т, J = 7 5,9Н кожний СН 3 етила), 1 15 (с, ЗН СНз), 1 18 (с, ЗН СНз), 1 58 (с, 1Н ОН в положенні 1), 1 68 (с, ЗН СНз), 1 89 та 2 48 (2 м, 1Н кожний СН 2 в положенні 6), 2 04 (с, ЗН СН3), 2 15 та 2 23 (2 дд, J = 16 та 9, 1Н кожний СН 2 в положенні 14), 2 29 (с, ЗН СОСН), 3 40 (С, ЗН ОСН3), З 83 (д, J = 7, 1Н Н в положенні 3), 4 15 та 4 ЗО (2 д, J = 8 5,1Н кожний СН 2 в положенні 20), 4 43 (дд, J = 11 та 1, 1НН в положенні 7), 4 91 (с, 1НН в положенні 10), 4 96 (уш д , J = 10, 1Н Н в положенні 5), 5 01 (уш т, J = 9,Ш Н в положенні 13), 5 62 (д, J = 7, 1Н Н в положенні 2), 7 46 (т, J = 7 5,2Н ОСОС6Н5 - Н в мета-положенні), 7 60 (т, J = 7 5, 37 1Н ОСОС6Н5 - Н в пара-положенні), 8 09 61883 28 27 карбоксилата розчиняють у 8см 3 0 1 н розчину хло(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(4рводню в етанолі з 1% води Таким чином, отриметоксифен]іл)-4-феніл-1,3-оксазолідин-5маний розчин перемішують на протязі 13 годин карбоксилата у 100см3 безводного етанолу, що при температурі біля 20°С, потім на протязі 80 підтримується в атмосфері аргону та при перемігодин при 4°С та додають 20см3 дихлорметану шуванні, при температурі біля 20°С додають Органічну фазу відокремлюють шляхом декантації 100см3 суспензії в етанолі активованого нікеля та промивають послідовно З рази по 5см 3 водним Ренея (отримують з 80см3 приблизно 50%-ноі воднасиченим розчином пдрокарбоната натрію, суної продажної суспензії шляхом послідовних прошать над сульфатом магнію, фільтрують та концемивань, до рН приблизно 7,15 разів по 100см3 динтрують, щоб висушити при зниженому тиску стильованої води та 5 разів по 100см3 етанолу) (2 7кПа) при 40°С Отримують ЗООмг повітряної Реакційне середовище витримують при перемішумаси білого кольору, яку очищують шляхом хрованні на протязі 24-х годин при температурі біля матографії насшікогелі, що нанесений на пластини 20°С, потім фільтрують через фільтр з фритовано(гель товщиною 1 мм, пластини 20х20см, елююго скла, який промивають 4 рази по 80см3 етановання суміш дихлорметану з метанолом в об'ємлом, фільтрати об'єднують та концентрують досуному співвідношенні 95 5) фракціями по 80мг (4 ха при зниженому тиску (2 7кПа) при 40°С пластини) Після локалізації за допомогою УФОтримують 710мг повітряної маси жовтого кольопроменей зони, що відповідає адсорбованому ціру, яку очищають шляхом хроматографії на 60г льовому продукту, цю зону зіскоблюють та зібрадиоксиду кремнію (0 063-0 2мм), що містяться у ний диоксид кремнію промивають на фільтрі із колонці діаметром 2 5см (елюючий засібхуміш фритованого скла 10 раз по 5см5 етилацетатом дихлорметану з етилацетатом в об'ємному співФільтрати об'єднують та концентрують досуха при відношенні 90 10), що збирає фракції по 6см 3 зниженьому тиску (2 7кПа) при 40°С Отримують Фракції, що містять тільки цільовий продукт, об'єдповітряну масу білого кольору, яку знову очищанують та концентрують досуха при зниженому тисють тим самим способом (3 пластини 20x20x1 мм, ку (2 7кПа) при 40°С Таким чином отримують елюювання суміш дихлорметану з етилацетатом 350мг 4а-ацетокси-2а-бензоілокси-5р, 20-епоксив об'ємному співвідношенні 90 10) Таким чином 1р-пдрокси-7р, Юр-диметокси-9-оксо-такс-і-енотримують 205мг 4а-ацетокси-2а-бензоілокси-5р, 13a-in-(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(420-епокси-ір-пдрокси-7р,10р-диметокси-9-оксометоксифешл)-4-феніл-1,3-оксазолідин-5такс-11 -єн-13a-in-(2R,3S)-3-TpeT карбоксилата у вигляді повітряної маси білого кобутоксикарбоніламіно-2-пдрокси-З-фенілльору пропюната у вигляді повітряної маси білого кольору, характеристики якого такі 4а-Ацетокси-2а-бензоілокси-5р, 20-епокси-1рпдрокси-7р, 10р-біс(метилтюметокси)-9-оксо-такс11 -ен-13a -in-(2R,4S,5R)-3-TpeT -бутоксикарбоніл- обертальна здатність [а]о =-33° (с=0 5, ме2-(4-метоксифеніл)-4-феніл-1,3-оксазолідин-5танол), карбоксилат може бути отриманий слідуючим чи-1Н-ЯМР-спектр (400МГц, дейтерохлороформ, ном ХІМЗДВИГИІВ м д , константи зв'язування J в Гц) 1 23 (с, ЗН -СНз), 1 25 (с, ЗН -СН3), 1 39 [с, 9Н До розчину 3 1г 4а-ацетокси-2а-бензоілоксиС(СН3)з], 1 70 (с 1Н-ОН у положенні 1), 1 75 (с, 5р, 20-епокси-1 р, 7р-1 ОЬ-трипдрокси-9-оксо-таксЗН -СНз), 1 82 и 2 72 (2 м, 1Н кожний -СН2 у по11-eH-13a-in(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2ложенні 6), 1 91 (с, ЗН -СНз), 2 31 (АВ обмеже(4-метоксифеніл)-4-феніл-1,3-оксазолідин-5ний, 2Н -СН2 у положенні 14), 2 39 (с, ЗН карбоксилата в 102см3 диметилсульфоксида, що СОСНз), 3 33 та 3 48 (2с, ЗН кожний -ОСН3), 3 48 підтримується у атмосфері аргону та при перемі(м,1Н ОН у положенні 2'), 3 85 (д, J = 7, 1Н -Ну шуванні, при температурі біля 20°С додають положенні 3), 3 88 (дд, J = 11 та 7,1Н у положенні 2 Зсм3 оцтової кислоти та 7 55см3 оцтового ангід7), 4 20 та 4 33 (2д, J = 8 5, 1Н кожний -СН у пориду Реакційну суміш витримують при перемішуложенні 20), 4 65 (м, 1Н - Н у положенні 2'), 483 ванні на протязі 7 днів при температурі біля 20°С , (с, 1Н -Н у положенні 10), 5 00 (уш д, J = 10, 1Н -Н потім виливають у суміш 500см3 дистильованої у положенні 5), 5 30 (уш д, J = 10, 1Н -Ну половоди з 250см3 дихлорметану Після цього додають женні 3'), 5 47 (д, J = 10, 1Н -CONH-), 5 66 (д, J = при інтенсивному помішуванні 30см водного на7, 1Н -Ну положенні 2), 6 24 (уш т , J = 9, 1Н -Н у сиченого розчину карбонату калію до рН біля 7 положенні 13), 7 30-7 50 (м, 5Н - СєНз у положенні Після перемішування на протязі 10 хвилин, органіЗ'), 7 52 [т, J = 7 5, 2Н -ОСОС6Н5 (-Н у положенні З чну фазу відокремлюють шляхом декантації та та -Н у положенні 5) ], 7 63 [т, J = 7 5, 1Н знову екстрагують водну фазу 2 рази по 250см3 ОСОС6Н5 (-Н у положенні 4)], 8 12 [д, J = 7 5, 2Н дихлорметаном Органічні фази об'єднують, проОСОСєНб (-Н у положенні 2 та -Н у положенні 6) ] мивають за допомогою 250см3 дистильованої води, сушать над сульфатом магнію, відфільтрову4(-Ацетокси-2а(-бензоілокси-5р, 20-епокси1рють та фільтрат концентрують досуха при пдрокси-7р, 10р-диметокси-9-оксо-такс-11 -ен-1 Зазниженому тиску (2 7кПа) при 40°С Отримують in-(2R, 4S,5R)-3-TpeT -бутоксикарбоніл-2-(45 2г масла блідо-жовтого кольору, яке очищають метоксифеніл)-4-феніл-1,3-оксазолідин-5шляхом хроматографії на 200 г диоксиду кремнію карбоксилат може бути отриманий слідуючим чи(0 063-0 4 мм), ЩО МІСТЯТЬСЯ у колонці діаметром ном Зсм (елюючий засіб суміш дихлорметану з метаДо розчину 1г 4а-ацетокси-2а-бензоілокси-5р, нолом в об'ємному співвідношенні 99 1), збираючи 20-епокси-1 р-пдрокси-7р, 10рфракції по 50см3 Фракції, що містять тільки цільобіс(метилтюметокси)-9-оксо-такс-11 -ен-1 За-ілвий продукт, об'єднують та концентрують досуха 29 61883 при зиженому тиску (2 7кПа) при 40°С Таким чином отримують 1 25г 4а-ацетокси-2а-бензоілокси5(3, 20-епокси-1р-пдрокси-7р, 10(3біс(метилтюметокси)-9-оксо-такс-11 -ен-1 Зонл(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(4метоксифеніл)-4-феніл-1,3-оксазолідин-5карбоксилата у вигляді повітряної маси білого кольору 4а-Ацетокси-2а-бензоілокси-5р, 20-епокси1 р,7р,10р-трипдрокси-9-оксо-такс-11 -ен-1 За-іл(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(4метоксифеніл)-4-феніл-1,3-оксазолідин-5карбоксилат може бути отриманий слідуючим чином Розчин 5 1г 4а-ацетокси-2а-бензоілокси-5р, 20-епокси-1р-пдрокси-9-оксо-7р,10р-біс(2,2,2трихлоретокси) карбонілокси-такс-11-ен-13а-іл(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(4метоксифеніл)-4-феніл-1,3-оксазолідин-5карбоксилата у суміші 100см3 метанолу з 100см3 оцтової кислоти, при перемішуванні та в атмосфері аргону, нагрівають до температури біля 60°С, потім додають 10г цинку у порошку Реакційну суміш після цього перемішують на протязі 15 хвилин при 60°С, потім охолоджують до температури біля 20°С та фільтрують через фільтр з фритованого скла, вкритого целітом Фритоване скло промивають 2 рази по 15см3 метанолу Фільтрат концентрують досуха при зниженому тиску (2 7кПа) при температурі біля 40°С До залишку додають 50см3 етилацетату та 25см3 водного насиченого розчину гідрокарбонату натрію Органічну фазу відокремлюють шляхом декантації та промивають послідовно за допомогою 25см водного насиченого розчину гідрокарбонату натрію та 25см3 дистильваною водою, потім сушать над сульфатом магнію, фільтрують через фільтр з фритованого скла та концентрують досуха при зниженому тиску (2 7кПа) при 40°С Таким чином отримують 3 1г 4а-ацетокси-2а-бензоілокси-5р, 20-епокси1 р,7р,10р-трипдрокси-9-оксо-такс-11 -ен-1 За-іл(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(4метоксифеніл)-4-феніл-1,3-оксазолідин-5карбоксилата у вигляді повітряної маси білого кольору 4а-Ацетокси2абензоідокси-5р 20-епокси-1рпдрокси-9-оксо-7р, 10р-біс(2,2,2-трихлоретокси) Kap6oHinoKCH-TaKC-11-eH-13a-in-(2R,4S,5R)-3-TpeT бутоксикарбоніл-2-(4-метоксифеніл)-4-феніл-1,3оксазолідин-5-карбоксилат може бути отриманий в умовах, що описані у міжнародній заявці 94/07878 Приклад З До суспензії, що містить 135мг 4а-ацетокси2а-бензоілокси-5р, 20-епокси-10р-етоксн-1 р, 13адипдрокси- 7-метокси-9-оксо-такс-11-ена, 120 мг (2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(4метоксифеніл)-4-феніл-1,3-оксазолідин-5карбонової кислоти та 50мг молекулярного сита 4 А у порошку в 1см3 безводного толуолу, послідовно додають, при температурі біля 20°С, 76мг дициклогексикарбодиіміду, потім 8 5мг 4-N.N'диметиламшопіридину Отриману суспензію перемішують при температурі біля 20°С та в атмосфері аргонуна протязі 1 години, потім очищають шляхом прямого внесення до хроматографічної колон 30 ки при атмосферному тиску, що заповнена 30г диоксиду кремнію (0 063-0 2мм) та має діаметр 2 5см (градієнт елюювання суміш етилацетату з дихлорметаном в об'ємному співвідношенні від 2 98 до 10 90), збираючи фракції по 10см3 Фракції, що містять тільки цільовий продукт, об'єднують та концентрують досуха при зниженому тиску (2 7кПа) при 40°С на протязі 2 годин Таким чином отримують 320 6г твердої речовини білого кольору, яку очищають шляхом препаративної тонокої хроматографії 10 препаративних пластин фірми Мерк, силікогель 60F254, товщина 0 5мм, нанесення у вигляді розчину у дихлорметані, елюювання сумішшю метанола з дихлорметаном в об'ємному співвідношенні 3 97 Після елюювання зон, що відповідають основним продуктам, сумішшю метанолу з дихлорметаном (в об'ємному співвідношенні 15 85), фільтрації через вату, потім випарювання розчинників при пониженому тиску (2 7кПа) при температурі біля 40°С, отримують 47 7мг 4а-Ацетокси-2а-бензоілокси-5р, 20-епокси10р-етокси-1р, 13а-дипдрокси-7р-метокси-9-оксотакс-11-ена у вигляді твердої речовини кремового кольору та 37мг 4а-ацетокси-2а-бензоілокси-5р, 20-епокси-10р-етокси-1 р-пдрокси-7р-метокси-9OKCO-TaKC-11-eH-13a-in-(2R,4S,5R)-3-TpeT бутоксикарбоніл-2-(4-метоксифеніл)-4-феніл-1,3оксазолідин-5-карбоксилата у вигляді повітряної маси білого кольору, характеристики якої слідуючі -1Н-ЯМР-спектр (600МГц, дейтерохлороформ, при температурі 60°С, хімздвиги в 5 м д , константи зв'язування J в Гц) 1 09 (с, 9Н С(СН3)з), 1 19 (с, ЗН СНз), 1 21 (с, ЗН СНз), 1 27 (т, J = 7, ЗН СН 2 етилу), 1 43 (с, 1Н ОН у положенні 1), 1 62 (с, ЗН СНз), 1 68 (с, ЗН СНз), 1 77 та 2 63 (2 м, 1Н кожний СН 2 у положенні 6), 1 86 (с, ЗН СОСН3), 2 13 та 2 22 (2 дд, J = 16 та 9,1Н кожний у положенні 14), 3 27 (с, ЗН ОСНз), 3 45 та 3 68 (2 м, 1Н кожний СН 2 етилу), 3 76 (д, J = 7, 1Н н у положенні 3), З 81 (с, ЗН АЮСНз), 3 85 (дд, J = 11 та 7, 1Н Н у пооженні 7), 4 13 та 4 23 (2д, J = 8 5, 1Н кожний СН 2 у положенні 20), 4 58 (д, J = 4 5,1Н Ну положенні 2), 4 83 (с, 1Н н у положенні 10), 4 90 (уш д , J = 10,1Н Н у положенні 5), 5 46 (д, J = 4 5, 1Н Н у положенні 3'), 5 60 (д, J = 7,1Н Н у положенны 2), 6 13 (ушт, J = 9, 1Н ну положенні 13), 6 38 (с, 1Н н у положенні 5'), 6 92 (д, J = 8 5,2Н ароматичні Н в орто-положенні до ОСНз), 7 30-7 50 (м, 9Н ароматичні Н у положенні 3' - ароматичні Н у метаположенні до ОСНз та Н у мета-положенні ОСОС6Н5), 7 59 (т, J = 7 5, 1Н ОСОС6Н5 - Н у пара-положенні), 8 03 (д, J = 7 5,2Н ОСОС6Н5 - Н в орто-положенні) Розчин 48мг 4а-ацетокси-2а-бензощокси-5р, 20-епокси-10р-етокси-1 р-пдрокси-7р-метокси-9OKCO-TaKC-11-eH-13a-in-(2R,4S,5R)-3-TpeT бутоксикарбоніл-2-(4-метоксифеніл)-4-феніл-1,3оксазолідин-5-карбоксилата у 0 5см 3 етилацетату та 0 04см3 концентрованої 37%-ноі соляної кислоти витримують при перемішуванні та при температурі біля 20°С на протязі 1 5 годин в атмосфері аргону Реакційну суміш потім очищають шляхом препаративної тонкошарової хроматографії нанесення сирої реакційної суміші на 5 препаративних пластинах фірми Мерк, силікогель 60F254, товщи 32 31 61883 на 0 5мм, елюювання сумішшю метанолу з дихлозниженому тиску (0 27кПа) при 40°С на протязі рметаном в об "ємному співвідношенні 4 96 Після двох годин Таким чином отримують 380мг 4аелюювання зони, що відповідає основному продуацетокси-2а-бензоілокси-5р, 20-епокси-1 Оркту, сумішшю метанолу з дихлорметаном в етокси-1 р,13а-д ипд рокси-7р-метокси-9-оксо-таксоб'ємному співвідношенні 15 85, фільтрації через 11-єна у вигляді білого порошку, характеристики 1 вату, потім випарювання розчинників при понижеякого слідуючі - Н-ЯМР-спектр (300МГц, дейтероному тиску (2 7кПа) при температурі біля 40°С, хлороформ з добавкою декількох краплин дейтеотримують 28,5мг 4а-ацетокси-2а-бензоілокси-5р, рованого метанолу, хімздвиги 5 в м д , константи 20-епокси-1 Ор-етокси-1 р-пдрокси-7р-метокси-9зв'язування J в Гц) 0 99 (с, ЗН СН3), 1 09 (с,ЗН оксо-такс-11-єн-13а-іл-(2Р,33)-3-трет СНз), 1 22 (т, J = 7, ЗН СНз, етила), 1 62 (с, ЗН бутоксикарбоніламіно-2-пдрокси-З-фенілСНз), 1 68 та 2 66 (2м, 1Н кожний СН 2 в положенні пропюната у вигляді повітряної маси кольору сло6), 2 03 (с, ЗН СНз), 2 13 та 2 22 (2 дд, J = 16 та 9, 1 нової кістки, характеристики якого слідуючі - Н1Н кожний СН 2 в положенні 14), 2 23 (с, ЗН ЯМР- спектр (400МГц, дейтерохлороформ, хімздСОСНз), 3 23 (с, ЗН ОСНз), 3 40-3 65 (м, 2Н СН 2 виги 5 в м д , константи зв'язування J в Гц) 1 22 (с, етила), 3 84 (д, J = 7 5, 1Н Н в положенні 3), 3 88 ЗН СНз), 1 25 (с, ЗН СНз) 1 32 (т, J - 7, ЗН СН 3 (дд, J = Юта 6 5,1Н Н В положенні 7), 4 10 та 4 23 етила), 1 38 (с, 9Н С(СН3)з), 1 64 (с, 1Н ОН в по(2 д, J = 8 5, 1Н кожний СН 2 в положенні 20), 4 75 ложенні 1), 1 73 (с, ЗН СНз), 1 80 та 2 70 (2 м, 1Н (ушт, J = 9,1Н Н в положенні 13), 4 90 (с, 1Н Н в кожний СН 2 в положенні 6), 1 88 (с, ЗН СН3), 2 ЗО положенні 10), 4 97 (уш д, J = 10, 1Н Н в положен(м, 2Н СН 2 в положенні 14), 2 38 (с, ЗН СОСН3), ні 5), 5 51 (д, J = 7 5, 1Н Н в положенні 2), 7 42 (т, З 31 (с, ЗН ОСНз), 3 44 (масив, 1Н ОН в положенJ = 7 5,2НОСОС6Н5 - Н в мета-положенні), 7 53 (т, ні 2'), 3 50 та 3 70 (2 м, 1Н кожний ОСН2 етила), J = 7 5, 1Н ОСОС6Н5 - Н в пара-положенні), 8 03 З 84 (д, J = 7 5, 1Н Н в положенні 3), 3 87 (дц, J = (д, J = 7 5, 2Н ОСОСєНб - Н в орто-положенні) 11 та 6 5, 1Н Н в положенні 7), 4 18 та 4 32 (2 д, J 4а-Ацетокси-2а-бензоілокси-5р, 20-епокси= 8 5,1Н кожний СН 2 в положенні 20) 464 (м, 1Н 1 р,7р,1 За-трипдрокси-10р-етокси-9-оксо-такс-11 в положенні 2'), 4 90 (с, 1Н Н в положенні 10), 4 98 (уш д, J = 10, 1Н Н в положенні 5), 5 28 (уш д, J = єн (або 10р-етокси-10-дезацетокси-баккатин (111)) 10, 1Н Н в положенні 3% 5 42 (д, J = 10, 1Н може бути отриманий слідуючим чином CONH), 5 64 (д, J = 7 5, 1Н Н в положенні 2), 6 22 До розчину 591 мг 4а-ацетокси-2а-бензоілокси(ушт, J = 9, 1Н Н в положенні 13), 7 25-7 45 (м, 5р, 20-епокси-1 р-пдрокси-1 Ор-етокси-9-оксо5Н ароматичні Н в положенні 3і), 7 50 (т, J = 7 5, 7р,13а-бістриетилсилілокси-такс-11-ена в 6см 3 2Н ОСОС6Н5 - Н в мета-положенні), 7 62 (т, J = дихлорметану в атмосфері аргону, при температу7 5,1Н ОСОС6Н5 - Н в пара-положенні), 8 12 (д, J рі біля 20°С додають 9 см 3 комплекса фторводню з = 7 5, 2Н ОСОСєНб - Н в орто-положенні) триетиламіном (3HF EtsN) Після витримування на протязі 21 години при температурі біля 20°С, реа4а-Ацетокси-2а-бензоілокси-5р, 20-епоксикційну суміш розбавляють за допомогою 40см3 10Ь-етокси-1р,13а-дипдрокси-7р-метокси-9-оксодихлорметану та виливають в суспензію 40см3 такс-11 -єн (або 10р-етокси-7р-метокси-10перенасиченого водного розчину гідрокарбонату дезадетокси-баккатин (III)) може бути отриманий натрію, що підтримується при температурі біля слідуючим чином 0°С Після розбавлення за допомогою 10см3 дисДо розчину 235мг 4а-ацетокси-2а-бензоілокситильованою водою та декантації, водну фазу по5р, 20-епокси-1р,7р,13а-трипдрокси-10р-етокси-9вторно екстрагують 2 рази по 20см диетиловим 3 3 оксо-такс-11-ена в 2 5см йодметану та 1см димеефіром Органічні фази об'єднують, промивають тилформаміду, що підтримується в атмосфері арза допомогою 20см3 дистильованої води, 20см3 гону, при температурі біля 0°С порціями додають водного насиченого розчину хлориду натрію, су43мг гідриду натрію у вигляді 50%-ноі (по масі) шать над сульфатом магнію, фільтрують та концедисперсії у вазелиновому маслі Після витримунтрують досуха при зниженому тиску (2 7кПа) при вання на протязі ЗО хвилин при температурі біля температурі біля 40°С Таким чином отримують 0°С, реакційну суміш розбавляють за допомогою 370мг повітряної маси блідо-жовтого кольору, яку 40см етилацетату, 6см 3 дистильованою водою та очищають шляхом хроматографії при атмосфер8см 3 водного насиченого розчину хлориду амонію ному тиску на 35г диоксиду кремнію (0 063-0 2мм), Після декантації, органічну фазу промивають З що містяться в колонці діаметром 2 5см, елюючи рази по 8см 3 дистильованою водою, потім 8см 3 сумішшю метанолу з дихлорметаном в об'ємному водного насиченого розчину хлориду натрію, суспіввідношенні 2 98 та збираючи фракції по 15см3 шать над сульфатом магнію, фільтрують через Фракції, що містять тільки цільовий продукт, фільтр з фритованог скла та концентрують досуха об'єднують та концентрують досуха при зниженопри зниженому тиску (2 7кПа) при температурі біля му тиску (2 7кПа) при 40°С на протязі двох годин 40°С Таким чином отримують 268мг твердої речоТаким чином отримують 236 2мг 4а-ацетокси-2авини жовтого кольору, яку очищають шляхом хробензошокси-5р, 20-епокси-1р,7р,13а~трипдроксиматографії при атмосферному тиску на 30г диок10р-етокси-9-оксо-такс-11-ена у вигляді твердої сиду кремнію (0 063-0 2мм), що містяться в речовини білого кольору, характеристики якої сліколонці діаметром 2 5см (градієнт елюювання дуючі суміш етилацетату з дихлорметаном в об'ємному - 1'Н-ЯМР-спектр (400МГц, дейтерохлороформ, співвідношенні від 0 10 до 15 85), збираючи фрак3 ції по 10см Фракції, що містять тільки цільовий хімздвиги 5 в м д , константи зв'язування J в Гц) продукт, об'єднують та концентрують досуха при 1 08 (с, ЗН СНз), 1 19 (с, ЗН СН3), 1 29 (т, J = 7 5, ЗН СНз етила), 1 38 (д, J = 9, 1Н ОН в положенні 33 61883 7), 1 59 (с, 1Н ОН в положенні 1), 1 69 (с, ЗН СН3), 1 82 та 2 62 (2 м, 1Н кожний СН 2 в положенні 6), 2 02 (д, J = 5, 1Н ОН в положенні 13), 2 08 (с, ЗН СНз), 2 30 (с, ЗН СОСНз), 2 32 (д, J = 9, 2Н СН 2 в положенні 14), 3 56 та 3 67 (2 м, 1Н кожний ОСН2, етила), 3 98 (д, J = 7, 1Н Н в положенні З), 4 18 та 4 33 (2 д, J = 8 5, 1Н кожний СН 2 в положенні 20), 4 30 (м, 1Н Н в положенні 7), 4 90 (м, 1Н Н в положенні 13), 4 99 (дд, J - Ю т а 1 5, 1Н Н в положенні 5), 5 05 (с, 1Н Н в положенні 10), 5 66 (д, J = 7, 1Н Н в положенні 2), 7 49 (т, J = 7 5, 2Н ОСОСбНб - Н в пара-положенні), 7 63 (т, J = 7 5, 1Н ОСОС6Н5 - Н в пара-положенні), 8 12 (д, J = 7 5, 2Н ОСОСбНб - Н в орто-положенні) 4а-Ацетокси-2а-бензоілокси-5р, 20-епокси-1рпдрокси-10р-етокси-9-оксо-7р,13абістриетилсилілокси-такс-11 -єн (або 10р-етокси10-дезацетокси-7,13-бістриетилсиліл-баккатин (111)) може бути отриманий слідуючим чином До розчину 1г 4а-ацетокси-2а-бензоілокси-5р, 20-епокси-1р,10р-дипдрокси-9-оксо-7р,13абістриетилсилілокси-такс-11-ена в Зсм3 йодетана та 4см 3 диметилформаміду, що підтримується в атмосфері аргону, при температурі біля 20°С порціями додають 93мг гідриду натрію у вигляді 50%ноі (по масі) дисперцм у вазелиновому маслі Розчин перемішують на протязі 17 годин при температурі біля 20°С, потім порціями додають 93мг гідриду натрію у вигляді 50%-ноі (по масі) дисперсії у вазелиновому маслі Після витримування на протязі 50 хвилин при температурі біля 20°С реакційну суміш розбавляють за допомогою 100см3 етилацетату, 10см3 водного насиченого розчину хлориду амонію Декантовану органічну фазу промивають 6 раз по 10см3 дистильованою водою, потім 10см3 водного насиченого розчину хлориду натрію, сушать над сульфатом магнію, фільтрують через фільтр з фритованого скла та фільтрат концентрують досуха при зниженому тиску (2 7кПа) при температурі біля 40°С Таким чином отримують 1 2г повітряної маси жовтого кольору, яку очищають шляхом хроматографії при атмосферному тиску на 150г диоксиду кремнію (0 063-0 2 мм), що містяться в колонці діаметром 3 5см, елюючи сумішшю етилацетату з дихлометаном в об'ємному співвідношенні 2 98, потім 5 95, та збираючи фракції по 15см3 Фракції, що містять тільки ЦІЛЬОВІ продукти, об'єднують та концентрують досуха при зниженому тиску (0 27кПа) при 40°С на протязі двох годин Таким чином отримують 379 2мг 4а-ацетокси-2а-бензоілокси-5р, 20-епокси1р,10р-дипдрокси-9-оксо-7р,13абістриетилсилілокси-такс-11-ена у вигляді повітряної маси блідо-жовтого кольору та 430мг 4аацетокси-2а-бензоілокси-5р, 20-епокси-1рпдрокси-10р-етокси-9-оксо-7р,13абістриетилсилілокси-такс-11-ена у вигляді повітряної маси білого кольору, характеристики якого слідуючі - 1Н-ЯМР-спектр (400МГц, дейтерохлороформ, хімздвиги 5 в м д , константи зв'язування J в Гц) 0 57 та 0 70 (2 м, 6Н кожний СН 2 етила), 0 97 та 1 03 (2 т, J = 7 5,9Н кожний СН 3 етила), 1 13 (с, ЗН СН2), 1 20 (с, ЗН СНз), 1 29 (т, J = 7 5, ЗН СН 3 етокси-групи в положенні 10), 1 58 (с, 1Н ОН в 34 положенні 1), 1 66 (с, ЗН СНз), 1 89 та 2 58 (2 м, 1Н кожний СН 2 в положенні 6), 2 03 (с, ЗН СН3), 2 13 та 2 23 (2 дд, J = 16 та 9, 1Н кожний СН 2 в положенні 14), 2 30 (с, ЗН СОСН3), 3 53 (м, 2Н СН 2 етокси-групи в положенні 10), 3 84 (д, J = 7, 1Н Н в положенні 3), 4 15 та 4 ЗО (2 д, J = 8 5,1Н кожний СН 2 в положенні 20), 4 43 (дд, J = 11 та 6 5, 1Н Н в положенні 7), 4 90-5 00 (м, 2Н Н в положенні 13 та Н в положенні 5), 5 01 (с, 1Н Н в положенні 10), 5 61 (д, J = 7, 1Н Н в положенні 2), 7 48 (т, J = 7 5, 2Н ОСОС6Н5 - Н в метаположенні), 7 61 (т, J = 7 5, 1Н ОСОС6Н5 - Н в пара-положенні), 8 10 (д, J = 7 5, 2Н ОСОС6Н5 - Н в орто-положенні) ПРИКЛАД 4 До суспензії, що містить 115мг 4а-ацетокси2а-бензоілокси-5р, 20-епокси-10р-(1 -пропіл)окси1 р,13-дипдрокси-7-метокси-9-оксо-такс-11 -єна, ЮОмг (2R,4S,5R)-3-TpeT6yroKCHKap6oHin-2-(4метоксифеніл)-4-феніл-1,3-оксазолідин-5карбонової кислоти в 1см3 безводного толуола, послідовно додають, при температурі біля 20°С, 65мг дициклогексилкарбодиіміду, потім 7мг 4-N.N'диметиламшо-піридину Отриману суспензію перемішують при температурі біля 20°С та в атмосфері аргону на протязі 1 години, потім очищають шляхом нанесення прямо в хроматографічну колонку при атмосферному тиску на 30г диоксиду кремнію (0 063-0 2мм), що міститься в колонці діаметром 2 5см (градієнт елювання суміш етилацетату з дихлорметаном у співвідношенні по об'єму від 2 98 до 10 90), збираючи фракції по 10см Фракції, що містять тільки цільовий продукт, об'єднують та концентрують досуха при зниженому тиску (2 7кПа) при 40°С на протязі двох годин Таким чином отримують 276 2мг твердої речовини білого кольору, яку очищають шляхом препаративної тонкошарової хроматографії 10 препаративних пласитн фірми Мерк, силікагель 60F254, товщина 0 5мм, нанесення у вигляді розчину в дихлорметані в об'ємному співвідношенні 3 97 Після елюювання зон, що відповідають основним продуктам, сумішшю метанолу з дихлорметаном в об'ємному співвідношенні 15 85, фільтрації через вату, потім випарювання розчинників при зниженому тиску (2,7кПа) при температурі біля 40°С, отримують 84 8мг 4а-ацетокси-2абензоілокси-5р, 20-епокси-10р-(1 -пропіл)окси-1 рпдрокси-7р-метокси-9-оксо-такс-11-ен-13а-іл(2R,4S,5R)-3-TpeT -бутоксикарбоніл-2-(4метоксифеніл)-4-феніл-1,3-оксазолідин-5 карбоксилата у вигляді повітряної маси білого кольору, характеристики якого слідуючі, - 1Н-ЯМР-спектр (ЗООМНц, дейтерохлороформ, хімздвиги 5 в м д , константи зв'язування J в Гц) 0 97 (т, J = 7, ЗН СНз пропіла), 1 07 (с, 9Н С(СНз)з), 1 19 (с, 6Н СНз), 1 50-1 80 (м, ЗН ОН в положенні 1 та центральна група СН 2 пропіла), 1 60 (с, ЗН СНз), 1 70 (с, ЗН СН), 1 78 та 2 63 (2м, 1Н кожний СН 2 в положенні 6), 1 82 (масив, ЗН СОСНз), 2 07 та 2 19 (2 дд, J = 16 та 9, 1Н кожний СН 2 в положенні 14), 3 26 (с, ЗН ОСН3), 3 30 та 3 58 (2м, 1Н кожний ОСН2 пропіла), 3 73 (д, J = 7 5, 1Н Н в положенні 3),3 81 (с, ЗН АгОСНз), З 81 (м, 1Н Н в положенні 7), 4 09 та 4 23 (2 д, J = 8 5, 1Н кожний СН 2 в положенні 20), 4 57 (д, J = 35 4 5, 1H Н в положенні 2% 4 79 (с, 1Н Н в положенні 10),4 90(ушд, 3= 10, 1Н Н в положенні 5), 5 40 (масив, 1Н Н в положенні 3'), 5 58 (д, J = 7 5, 1Н, Н в положенні 2), 6 13 (уш т, J = 9, 1Н Н в положенні 13), 6 40 (масив розтягнутий, 1Н Н в положенні 5'), 6 92 (д, J = 8 5, 2Н ароматичні Н в орто-положенні до ОСНз), 7 30-7 60 (м, 9Н ароматичні Н в положенні 3 і - ароматичні Н в метаположенні од ОСНз та ОСОСєНб - Н в метаположенны), 7 63 (т, J = 7 5, 1Н ОСОС 6 Н 5 - Н в пара-положенны), 8 03 (д, J - 7 5,2Н ОСОС 6 Н 5 - Н в орто-положенні) 4а-Ацетокси-2а-бензоілокси-5В, 20-епокси10В-(1 -протл)окси-1 В-пдрокси-7В-метокси-9-оксотакс-11 -ен-13a-in-(2R,3S)-3-TpeT бутоксикарбоніламіно-2-пдрокси-З-фенілпропюнат може бути отриманий слідуючим чином Розчин 84мг 4а-ацетокси-2а-бензоілокси-5В, 20-епокси-10В-(1 -пропіл)окси-1 В-пдрокси-7Вметокси-9-оксо-такс-11-єн-13а-іл-(2Р,43,5Р)-3трет -бутоксикарбоніл-2-(4-метоксифеніл)-4-феніл1,3-оксазолідин-5-карбоксилату в 0 84см 3 етилацетату та 0 0071см 3 концентрованої 37%-ноі соляної кислоти перемішують на протязі 1 години при температурі біля 20°С і в атмосфері аргону Реакційну суміш потім очищають шляхом препаративної тонкошарової хроматографії нанесення сирої реакційної суміші на 6 препаративних пластин фірми Мерк, силікагеь 60F254, товщина 0 5мм, елюювання сумішшю метанолу з ацетонітрилом та дихлорметаном в об'ємному співвідношенні 3 7 90 Після елюювання зони, що відповідає основному продукту, сумішшю метанолу з дихорметаном в об'ємному співвідношенні 15 85, фільтрації через вату, потім випарювання розчинників при зниженому тиску (2 7кПа) при температурі біля 40°С, отримують 27мг 4а-ацетокси-2а-бензоілокси-5В, 20-епокси-10В-(1 -пропіл)окси-1 В-пдрокси-7Вметокси-9-оксо-такс-11-єн-13а-іл- (2R,3S)-3-TpeT бутоксикарбоніламіно-2-пдрокси-З-фенілпротоната у вигляді повітряної маси білого кольору, характеристики якого слідуючі - Н-ЯМР-спектр (400МГц, дейтерохлороформ, хімздвиги 5 в м д , константи зв'язування J в Гц) 0 99 (т, J = 7, ЗН СНз пропіла), 1 22 (с, ЗН СН 3 ), 1 25 (с, ЗН СНз), 1 38 (с, 9Н С(СН 3 )з), 1 64 (с, 1Н ОН в положенні 1), 1 69 (м, 2Н центральна СН 2 група пропіла), 1 73 (с, ЗН СН 3 ), 1 80 та 2 70 (2 м, 1Н кожний С Н 2 в положенні 6), 1 88 (с, ЗН СН 3 ), 2 30 (м, 2Н С Н 2 в пооженні 14), 2 38 (с, ЗН СОСНз), 3 31 (с, ЗН ОСНз), 3 36 та 3 64 (2 м, 1Н кожний ОСН2 пропілу), 3 44 (масив, 1Н ОН в пооженні 2% 3 84 (д, J = 7 5, 1Н Н в положенні 3), 3 87 (дд, J = 11 та 6 5,1Н Н в положенні 7), 4 18 та 4 ЗО (2 д, J = 8 5, 1Н кожний С Н 2 в положенні 20), 4 64 (м, 1Н Н в положенні 2'), 4 89 (с, 1Н Н в положенні 10), 4 98 (уш д, J = 10,1Н Н в положенні 5), 5 28 (уш д, J = 10,1Н Н в положенні 3'), 5 42 (д, J = 10, 1Н CONH), 5 64 (д, J = 7 5, 1Н Н в положенні 2), 6 22 (ушт, J = 9, 1Н Н в положенні 13), 7 25-7 45 (м, 5Н ароматичні Н в положенні 3'), 7 50 (т, J = 7 5, 2Н ОСОС 6 Н 5 - Н в мета-положенні), 7 6 1 (т, J = 7 5, 1Н ОСОС 6 Н 5 - Н в пара-положенні), 8 12 (д, J = 7 5, 2Н ОСОС 6 Н 5 - Н в ортоположенні) 61883 36 4а-Ацетокси-2а-бензоілокси-5В, 20-епокси10В-(1 -пропіл)окси-1 В,1 За-дипдрокси-7В-метокси9-оксо-такс-11 -єн (або 10В-(1 -пропіл)окси-9метокси-10-дезацетокси-баккатин (III)) може бути отриманий слідуючим чином До розчину 165мг 4а-ацетокси-2а-бензошокси5В, 20-епокси-1 (3,7(3,1 За-трипдрокси-10В-(1 пропіл)окси-9-оксо-такс-11-енав 1 7см 3 йодметанута 1см 3 диметилформаміду, що підтримується в атмосфері аргону, при температурі біля 0°С порціями додають ЗОмг гідриду натрію у вигляді 50%ноі (по масі) суспензії в вазелиновому маслі Після витримування на протязі ЗО хвилин при температурі біля 0°С, реакційну суміш розбавляють за допомогою 40см 3 етилацетату, 5см 3 дистильованої води та 7см 3 водного насиченого розчину хлориду амонію Після декантації, органічну фазу промивають три рази по 7см 3 дистльованої води, потім 7см 3 водного насиченого розчину хлориду натрію, сушать над сульфатом магнію, фільтрують через фільтр з фритованого скла та концентрують досуха при зниженому тиску (2 7кПа) при температурі біля 40°С Таким чином отримують 224мг твердої речовини жовтого кольору, яку очищають шляхом хроматографії при атмосферному тиску на 20г диоксиду кремнію (0 063-0 2мм), що містяться в колонці діаметром 2 5см (градієнт елюювання суміш етилацетату з дихлорметаном в об'ємному співвідношенні від 0 100 до 15 85), збираючи фракції по 10см 3 Фракції, що містять тільки цільовий продукт, об'єднують та концентрують досуха при зниженому тиску (0 27кПа) при 40°С на протязі двох годин Таким чином отримують 117 5мг 4aацетокси-2а-бензоілокси-5В, 20-епокси-10В-(1 пропіл)окси-1В,13а-дипдрокси-7В-метокси-9-оксотакс-11-ена у вигляді повітряної маси білого кольору, характеристики якого слідуючі - 1 Н-ЯМР-спектр (300МГц, дейтерохлороформ, хімздвиги 5 в м д , константи зв'язування J в Гц) 0 98 (т, J = 7, ЗН СНз пропіла), 1 05 (с, ЗН СН 3 ), 1 19 (с, ЗН СНз), 1 60-1 80 (м, 2Н центральна СН 2 -група пропіла), 1 65-1 85 та 2 66 (2м, 1Н кожний С Н 2 в положенні 6), 1 72 (с, ЗН СН 3 ), 2 10 (с, ЗН СНз), 2 05-2 35 (м, 2Н С Н 2 в положенні 14), 2 28 (с, ЗН СОСНз), 3 32 (с, ЗН ОСН 3 3 45 та 3 65 (2 м, 1Н кожний О С Н 2 пропіла), 3 92 (д, J = 7 5, 1Н Н в положенні 3), 3 93 (дд, J = 11 та 6, ІН Н в положенні 7), 4 16 та 4 32 (2 д, J = 8 5, 1Н кожний С Н 2 в положенні 20), 4 90 (м, 1Н Н в положенні 13), 4 94 (с, 1Н Н в положенні 10), 5 03 (уш д, J = 10, 1Н Н в положенні 5), 5 60 (д, J = 7 5, 1Н Н в положенні 2), 7 48 (т, J = 7 5, 2Н О С О С 6 Н 5 - Н в мета-положенні), 7 62 (т, J = 7 5, 1Н ОСОС 6 Н 5 - Н в пара-положенні), 8 11 (д, J - 7 5, 2Н ОСОС 6 Н 5 Н в орто-положенні) 4а-Ацетокси-2а-бензоілокси-5В, 20-епокси1 [3,7(3,1 За-трипдрокси-10В-(1 -пропіл)окси-9-оксотакс-11 -єн (або 10В-(і-пропіфкси-10-дезацетоксибаккатин (III)) може бути отриманий слідуючим чином До розчину 585мг 4а-ацетокси-2а-бензоілокси5В, 20-епокси-1 В-тідрокеи-10В-(1 -пропіл)окси-9оксо-7В,13а-бістриетилсилілокси-такс-11-ена в 6см 3 дихлорметану, що підтримується в атмосфері аргону, при температурі біля 20°С додають 61883 38 37 8 75см3 комплексу фтороводню з триетиламіном вання на протязі трьох годин при температурі біля (3HF EtsN) Після витримування на протязі трьох 20°С реакційну суміш розбавляють за допомогою годин при температурі біля 20°С реакційну суміш 100см3 етилацетату, 10см3 водного насиченого розбавляють за допомогою 30см дихлорметану розчину хлориду амонію Декантовану органічну та виливають в суспензію 30см3 водного перенафазу промивають 6 раз по 10см3 дистильованою сиченого розчину гідрокарбонату натрію, що підводою, потім 10см3 водного насиченого розчину тримується при температурі біля 0°С Після розхлориду натрію, сушать над сульфатом магнію, бавлення за допомогою 10см3 дистильованої води фільтрують через фільтр з фритованого скла та та декантації, вожну фазу повторно екстрагують концентрують фільтрат досуха при зниженому два рази по 20см3 диетиловим ефіром Органічні тиску (2 7кПа) при температурі біля 40°С Таким 3 фази об'єднують, помивають за допомогою 20см чином отримують 1 32г повітряної маси блідодистильованої води, 20см3 водного насиченого жовтого кольору, яку очищають шляхом хроматогрозчину хлориду натрію, сушать над сульфатом рафії при атмосферному тиску на 150г диоксиду магнію, відфільтровують та концентрують досуха кремнію (0 063-0 2мм), що містяться в колонці діапри зниженому тиску (2 7кПа) при температурі біля метром 3 5см, елюючи сумішшю етилацетату з 40°С Таким чином отримують 500мг повітряної дихлорметаном (в об'ємному співвідношенні 2 98, маси блідо-жовтого кольору, яку очищають шляпотім 5 95) та збираючи фракції по 15см3 Фракції, хом хроматографії при атмосферному тиску на 40г що містять тільки ЦІЛЬОВІ продукти, об'єднують та диоксиду кремнію (0 063-0 2мм), що містяться в концентрують досуха при зниженому тиску колонці діаметром 2 5см, елюючи сумішшю мета(0 27кПа) при 40°С на протязі двох годин Таким нолу з дихлорметаном (у співвідношенні 2 98 по чином отримують 376 Змг 4а-ацетокси-2аоб'єму) та збираючи фракції по 15см3 Фракції, що беюоілокси-5В, 20-епокси-1В,10В-дипдрокси-9містять тільки цільовий продукт, об'єднують та оксо-7В,13а-бістриетилсилілокси-такс-11-ена у концентрують досуха при зниженому тиску вигляді повітряної маси блідо-жовтого кольору та (2 7кПа) при 40°С на протязі двох годин Таким 395 Змг 4а-адетокси-2а-бензоілокси-5В, 20-епоксичином отримують 373 8мг 4а-ацетокси-2а1 В-пдрокси-10В-(1 -пропіл)окси-9-оксо-7В,1 Забензоілокси-5В, 20-епокси-1В,7В,13а-трипдроксибістриетилсилілокси-такс-11-ена у вигляді повітря10В-(1 -пропіл)окси-9-оксо-такс-11 -єна у вигляді ної маси блідо-жовтого кольору, характеристики твердої речовини білого кольору, характеристики якого слідуючі якої слідуючі - 1Н-ЯМР-спектр (400МГц, дейтерохлороформ, - 1Н-ЯМР-спектр (300МГц, дейтерохлороформ, хімздвиги 5 в м д , константи зв'язування J в ГГЦ) хімздвиги 5 в м д , константи зв'язування J в Гц) 0 57 та 0 70 (2 м, 6Н кожний СН 2 етила), 0 94 та 0 95 (т, J = 7, ЗН СНз пропіла), 1 06 (с, ЗН СН3), 1 03 (2 т, J = 7 5, 9Н кожний СН 3 етила), 0 94 (т, J 1 22 (с, ЗН СНз), 1 45 (д, J = 7 5,1Н ОН в поло= 7 5, ЗН, СН 3 пропіла), 1 14 (с, ЗН СН3), 1 21 (с, женні 7), 1 60-1 80 (м, 2Н центральна СН2-група ЗН СНз), 1 67 (С, ЗН СНз), 1 69 (м, 2Н центральпропіла), 1 67 (с, ЗН СН3), 1 83 та 2 62 (2 М, 1Н на СН2-група пропіла), 1 88 та 2 48 (2 м, 1Н кожкожний СН 2 в положенні 6), 2 05 (с, ЗН СН3), 2 05 ний СН 2 в положенні 6), 2 03 (с, ЗН СН3), 2 13 та (м, 1Н ОН в положенні 13), 2 27 (АВ обмежений, 2 33 (2 дд, J = 16 та 9, 1Н кожний СН 2 в положенні 2Н СН 2 в положенні 14), 2 28 (с, ЗН СОСН3), 3 40 14), 2 30 (с, ЗН СОСНз), 3 40 (м, 2Н та 3 57 (2 м, 1Н кожний ОСН2 пропіла), 3 97 (д, J = ОСН2пропіла), 3 84 (д, J = 7 5, 1Н Н в положенні 7 5, 1Н Н в положенні 3), 4 15 та 4 ЗО (2 д, J = 8 5, 3), 4 16 та 4 30 (2 д, J = 8 5, 1Н кожний СН 2 в поЩ кожний СН 2 в положенні 20), 4 28 (м, 1Н Н в ложенні 20), 4 44 (дд, J = 11 та 6 5, 1Н Н в полоположенні 7), 4 90 (м, 1Н Н в положенні 13), 4 98 женні 7), 4 96 (уш д , J = 10, 1Н Н в поолженні 5), ( y m f l , J = 10,1Н Н в положенні 5), 5 03 (с, 1Н Нв 4 97 (с, 1Н Н в положенні 10), 4 99 (уш т, J = 9, 1Н положенні 10), 5 65 (д, J = 7 5, 1Н Н в положенні Н в положенні 13), 5 62 (д, J - 7 5, 1Н Н в поло2), 7 50 (т, J = 7 5, 2Н ОСОС6Н5 - Н в метаженні 2), 7 48 (т, J = 7 5, 2Н ОСОС6Н5 - Н в метаположенні), 7 60 (т, J = 7 5, 1Н ОСОС6Н5 - Н в паположенні), 7 60 (т, J = 7 5, 1Н ОСОС6Н5 - Н в пара-положенні), 8 00 (д, J = 7 5,2Н ОСОС6Н5 - Н в ра-положенні), 8 10 (д, J = 7 5, 2Н ОСОС6Н5 - Н в орто-положенні) орто-положенні) 4а-Ацетокси-2В-бензоілокси-5В, 20-епокси-1ВНові продукти загальної формули (І), в якій Z пдрокси-10В-(1 -пропіл)окси-7В,1 Заозначає радикал загальної формули (м), проявлябістриетилсилілокси-такс-11-єн (або 10В-(1-пропіл) ють значну інгібуючу активність у відношенні аноокси-10-дезацетокси-7,13-бістриетилсилілрмальної проліферації клітин та володіють терабаккатин(ІІІ)) може бути отриманий слідуючим чипевтичними властивостями, що дозволяють ном лікувати хвороби з паталопчними станами, що пов'язані з порушеннями проліферації клітин До До розчину 1г 4а-ацетокси-2а-бензоілокси-5В, паталопчних станів відносяться анормальна про20-епокси-1В,10В-дипдрокси-9-оксо-7В,13аліферація злоякісних або незлоякісних клітин різбістриетилсилілокси-такс-11-ена в Зсм3 йодетану них тканин та/або органів, що включають, але тих, та 4см 3 диметилформаміду, що підтримується в що не обмежуються ними, м'язові, КІСТКОВІ або атмосфері аргону, при температурі біля 20°С порсполучні тканини, шкіру, головний мозок, легкі, ціями додають 93мг гідриду натрію у вигляді 50%статеві органи, лімфатичні та ниркові системи, ноі (по масі) суспензії у вазелиновому маслі Розклітини грудних залоз або клітини крові, печінку, чин перемішують на протязі дев'ятнадцяти годин травний апарат, підшлункову залозу та щитовидні при температурі біля 20°С, потім порціями додазалози До цих паталопчних станів також відноють 93мг гідриду натрію у вигляді 50%-ноі (по масі) сяться псоріаз, тверді пухлини, ракові захворюсуспензії у вазелиновому маслі Після витриму 39 вання яєчників, жіночих грудей, простати, ободковоі кишки, шлунку, нирок або тестикул, саркому Калоші, холанпокарциному, хорюкарциному, нейробластому, пухлину Вілмса, хворобу Ходжкіна, меланоми, множинні меланоми, хронічні лімфоцитарні лейкемії, гострі аб хронічні гранулоцитарні лімфоми Нові сполуки ВІДПОВІДНО винаходу особливо придатні для дікування раку яєчників Сполуки ВІДПОВІДНО винаходу також можна використовувати для попередження або уповільнення появи або повторної появи патологічних станів або для лікування цих патологічних станів Сполуки ВІДПОВІДНО винаходу можна вводити пацієнту у різних формах, які придатні для вибраного шляху введення, яким переважно є парентеральний шлях введення Введення парентеральним шляхом включає внутрішньовенне, штраперитоніальне, внутрішньом'язове або підшкірне введення Найбільш переважним є штраперитоніальне або внутрішньовенне введення Даний винахід також відноситься до фармацевтичних композицій, які містять принаймні один продукт загальної формули (І) у ефективній КІЛЬКОСТІ, що придатна для використання в терапії людини або тварини Композиції можна отримувати звичайними способами, використовуючи одну або декілька фармацевтично прийнятних домішок, основ або ексціпієнтів Придатними основами є розчинники, стерильні водні середовища та різні нетоксичні розчинники Переважно, композиції знаходяться у формі водних суспензій або розчинів, розчинів для ІН'ЄКЦІЙ, ЯКІ можуть містити емульгатори, барвники, консерванти або стабілізатори Однак, композиції також можуть знаходитися у формі таблеток, пілюль, порошків або гранул, що вводяться перорально Вибір домішок або ексціпієнтів можна визначити в залежності від розчинності та ХІМІЧНИХ властивостей продукту, конкретного способу введення та від практики, що склалась у фармацевтиці Для парентерального введення використовують стерильні водні або неводні розчини або суспензії Для отримання неводних розчинів або суспензій можна використовувати природні рослинні масла, такі, як оливкове масло, кунжутне масло або парафінове масло, або складні органічні ефіри для ІН'ЄКЦІЙ, такі, як етилолеат Стерильні водні розчини можуть бути утворені водним розчином фармацевтично прийнятної солі Водні розчини придатні для внутрішньовенного введення, якщо в них встановлено необхідне рН-значення та забезпечена ІЗОТОНІЧНІСТЬ, наприклад, за рахунок достатньої КІЛЬКОСТІ хлорида натрію або глюкози Стерилізацію можна здійснювати шляхом нагрівання або будь-яким іншим шляхом, який не погіршує властивостей композиції Само собою розуміється, що всі продукти, що входять в композицію ВІДПОВІДНО винаходу, мають бути чистими та нетоксичними у кількостях, що використовуються Композиції можуть містити принаймні 0 01% терапевтично активного продукту КІЛЬКІСТЬ активного продукта в композиції є такою, щоб можна було прописувати необхідну дозу Переважно, композиції отримують таким чином, щоб разова доза містила біля 0,01-ЮООмг активного продукта 61883 40 для введення 68 парентеральним шляхом Терапевтичне лікування модна здійснювати одночасно з іншим терапевтичним лікуванням, що включає лікування за допомогою противопухлинних лікарських засобів, моноклональних антитіл, імунологічну терапію або рентгенотерапію або лікування за допомогою модифікаторів біологічних відповідей Модифікатори відповідей включають, не вичерпним чином, лімфокши та цитокши, такі, як інтерлейкіни, інтерферони (або) та фактор некрозу пухлин Інші хіміотерапевтичні агенти, придатні для лікування порушень, що пов'язані з ненормальною проліферацією клітин, включають, не вичерпним чином, алкілюючи агенти, такі, як горчичні гази, наприклад, мехлоретамш, циклофосфамід, мелфалан та хлорамбуцил, алкілсульфонати, наприклад, бісульфан, нітрозосечовини, наприкад, кармустин, ломустин, семустин та стрептозоцин, триазіни, наприклад, дакарбазин, антиметаболіти, такі ж аналоги фолієвої кислоти, наприклад, метотрексат, аналоги піримідину, такі як флуороурацил та цитарабін, аналоги пуринів, такі як меркаптопурин та тюгуанш, природні продукти, такі, як алкалоїди vmca, наприкад, вінбластин, вінкристін та віндезін, епіподофілотоксини, такі як етопосид та тенипосид, антибіотики, такі як дактиноміцин, даунорубицин, доксорубіцин, блеоміцин, плікаміцин та МІТОМІЦИН, ферменти, як Lаспарапноза, різні агенти, такі як координаційні комплекси платини, такі як цисплатин, заміщені сечовини, такі як пдроксисечовина, ПОХІДНІ метилпдразину, такі як прокарбазин, адренокортикоідні супресори, такі, як мітотан та аміноглютетимід, гормони та антагоністи, такі, як адренокортикостероїди, наприклад, преднізолон, прогестини, такі як пдроксипрогестеронкапроат, метоксипрогестеронацетатта мєгестолацетат, естрогени, такі як диетилстильбестрол та етинілестрадюл, антиестрогени, такі як тамоксифен, андрогени, такі як тестостеронпропюнатта флуоксиместерон Дози, що використовуються для введення активного початку ВІДПОВІДНО винаходу, є такими, які дозволяють проводити профілактичне лікування або отримувати максимум терапевтичної ВІДПОВІДІ Дози змінюються в залежності від форми введення препарату, від конкретної вибраної сполуки та від особливостей, що належні хворому, що виліковується Звичайно дози є такими, які терапевтично ефективні для лікування порушень, що викликані ненормальною проліферацією клітин Продукти ВІДПОВІДНО винаходу можна також вводити настільки часто, наскільки це необхідно для досягнення бажаного терапевтичного ефекту У деяких хворих ВІДПОВІДЬ на відносно сильні або слабкі дози виникають швидко, тоді потім достатньо вводити назькі підтримуючі дози або взагалі ВІДМІНИТИ ЛІКИ Звичайно низькі дози використовують на початку 70 лікування та, якщо необхідно, вводять все більш та більш сильні дози до досягнення оптимального ефекту Іншим хворим може бути необхідним введення підтримуючих доз 1-8 раз в день, переважно 1-4 раза, в залежності від фізіологічних особливостей даного хворого Для деяких хворих може бути достатнім тільки 1-2 разове в день Для людини дози звичайно складають 0 01 61883 42 41 200мг/кг При штраперитоніальному введенні дози Слідуючий приклад ілюструє композицію ВІДзвичайно складають 0 1-100мг/кг, переважно, 0 5ПОВІДНО винаходу 50мг/кг та більш переважно 1-10мг/кг При внутріПРИКЛАД шньовенному введенні дози звичайно складають 40мг отриманої в прикладі 1 сполуки розчиня3 3 0 1-50мг/кг, переважно 0 1-5 мг/кгта більш конкреють в 1см Emulphor EL 620 та 1см етанолу, потім 3 тно 1-2мг/кг Розуміється, коли вибирають найрозчин розбавляють шляхом додавання 18см більш придатну дозу, то враховують шлях введенфізіологічної сироватки Композицію вводять меня, масу хворого, загаяний стан його здоров'я, тодом перфузії на протязі 1 голини з фізіологічним його вік та всі фактори, які можуть впливати на розчином ефективність лікування Комп'ютерна верстка О Кураєв Підписне Тираж39 прим Міністерство освіти і науки України Державний департамент інтелектуальної власності, Львівська площа, 8, м Київ, МСП, 04655, Україна ДП "Український інститут промислової власності", вул Сім'ї Хохлових, 15, м Київ, 04119
ДивитисяДодаткова інформація
Назва патенту англійськоюTaxoids, methods for preparation thereof and a pharmaceutical composition based thereon
Автори англійськоюCommercon Alain
Назва патенту російськоюТаксоиды, cпособ их получения и фармацевтическая композиция на их основе
Автори російськоюКоммерсон Ален
МПК / Мітки
МПК: A61K 31/335, C07D 305/00, A61K 31/337, A61K 31/00, A61P 35/00
Мітки: cпосіб, одержання, таксоїди, фармацевтична, композиція, основі
Код посилання
<a href="https://ua.patents.su/21-61883-taksodi-cposib-kh-oderzhannya-ta-farmacevtichna-kompoziciya-na-kh-osnovi.html" target="_blank" rel="follow" title="База патентів України">Таксоїди, cпосіб їх одержання та фармацевтична композиція на їх основі</a>
Попередній патент: Харчожирова композиція масла м’якого “кримське”
Наступний патент: Курильний матеріал на основі рослинних компонентів
Випадковий патент: Пристрій для тиснення щонайменше двошарових плоских виробів, таких як туалетний папір, паперові серветки або подібні вироби