Імуномодулюючі гетероциклічні сполуки
Формула / Реферат
1. Сполука, що описується формулою (І)
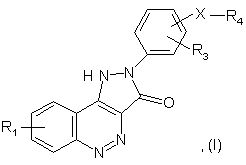
де
R1 і R3 незалежно один від одного є Н, F, Сl, Br, -NO2, -CN, С1-С6 алкіл, у разі потреби заміщений на F або Сl, або С1-С6 алкокси, у разі потреби заміщений на F;
R4 є карбокислотна група (-СООН) або її естер, або -C(=O)NR6R7, -NR7C(=O)R6, -NR7C(-O)OR6, -NHC(-O)NR7R6 чи -NHC(=S)NR7R6, де
R6 є Н або радикал за формулою -(Alk)m-Q, де
m є 0 або 1,
Alk означає в разі потреби заміщений двовалентний прямолінійний або розгалужений С1-С12 алкіленовий, С2-С12 алкеніленовий чи С2-С12 алкініленовий радикал або двовалентний С3-С12 карбоциклічний радикал, причому будь-який із цих радикалів може містити один або більше -О-, -S- або -N(R8)- зв'язків, де R8 означає Н або С1-С4 алкіл, С3-С4 алкеніл, С3-С4 алкініл або С3-С6 циклоалкіл, а
Q є: Н; -NR9R10, де R9 і R10 незалежно один від одного є Н; С1-С4 алкіл; С3-С4 алкеніл; С3-С4 алкініл; С3-С6 циклоалкіл; естерна група; в разі потреби заміщена карбоциклічна або гетероциклічна група; або R9 і R10 разом з атомом азоту, з яким вони зв'язані, утворюють цикл, який у разі потреби є заміщеним; і
R7 є Н або С1-С6 алкіл, або R6 і R7 разом з атомом або атомами, з якими вони зв'язані, утворюють у разі потреби заміщений моноциклічний гетероцикл, який містить 5, 6 або 7 атомів у кільці;
X означає зв'язок або двовалентний радикал, що описується формулою -(Z)n-(Alk)- або -(Alk)-(Z)n-, де Z означає -О-, -S- або -NH-, Alk визначений так, як це визначено для R6, a n є 0 або 1; або прийнятні у фармацевтиці чи ветеринарії її сіль, гідрат і сольват.
2. Сполука за п. 1, яка відрізняється тим, що радикал R4X- є в
положенні 4 фенільного кільця.
3. Сполука за п. 1, яка відрізняється тим, що X є зв'язок.
4. Сполука за п. 1, яка відрізняється тим, що R4 є водень.
5. Сполука за п. 1, яка відрізняється тим, що R1 є водень або фтор.
6. Сполука за п. 1, яка відрізняється тим, що R4 означає -C(=O)NR6R7, де R6 і R7 є такими, як визначено в п. 1.
7. Сполука за п. 1, яка відрізняється тим, що R4 означає -NHC(=O)NR7R6, де R6 і R7 є такими, як визначено в п. 1.
8. Сполука за п. 7, яка відрізняється тим, що R6 є радикал хінуклідил.
9. Сполука за п. 1, яка відрізняється тим, що R6 є радикал, що описується формулою -(Alk)m-Q, де m є 1, двовалентний радикал Alk містить 3 або 4 вуглецевих атоми і є незаміщеним, a Q означає -NR9R10, де R9 і R10 незалежно один від одного є Н; С1-С4 алкіл; С3-С4 алкеніл; С3-С4 алкініл; С3-С6 циклоалкіл; естерна група; у разі потреби заміщена карбоциклічна або гетероциклічна група; або R9 і R10 разом з атомом азоту, з яким вони зв'язані, утворюють кільце, яке в разі потреби є заміщеним.
10. Сполука за будь-яким з пп. 6-8, яка відрізняється тим, що R7 є водень.
11. Сполука за п. 1, яка відрізняється тим, що Q означає Н; CF3; -OH; -SH; -NR8R8, де кожний R8 незалежно один від одного означає Н; С1-С4 алкіл; С3-С4 алкеніл; С3-С4алкініл; С3-С6 циклоалкіл; естерну групу; у разі потреби заміщену арильну, арилокси, циклоалкільну, циклоалкенільну або гетероциклічну групу; або разом з атомом азоту, з яким вони зв'язані, утворюють кільце; а
R7 є Н або С1-С6 алкіл; або R6 і R7 разом з атомом або атомами, з якими вони зв'язані, утворюють моноциклічне гетероциклічне кільце, яке має 5, 6 або 7 атомів кільця.
12. Сполука за п. 11, яка відрізняється тим, що R4 є карбокислотна група (-СООН) або естерна група -COOR, де R означає метил, етил, н- або ізопропіл, н-, вторинний або третинний бутил або бензил.
13. Сполука за п. 11 або п. 12, яка відрізняється тим, що R6 є радикал, що описується формулою -(Alk)m-Q, де m є 1, Alk є: -СН2-, -СН2СН2-, -СН2СН2СН2- або -СН2СН(СН3)СН2-, або двовалентний циклопропіленовий, циклопентиленовий чи циклогексиленовий радикал, у разі потреби заміщений групою ОН, оксо, CF3, метокси або етокси, a Q є водень; -NR8R8, де R8 можуть бути однаковими або різними і бути вибраними з водню, метилу, етилу, н- або ізопропілу або трет-бутилу; метиловий, етиловий або бензиловий естер; або в разі потреби заміщена фенільна, фенокси, циклопентильна, циклогексильна, фурильна, тієнільна, піперидильна або піперазинільна група.
14. Сполука за будь-яким з пп. 11-13, яка відрізняється тим, що R7 є метил, етил, н- або ізопропіл, н-, вторинний або третинний бутил, або R6 і R7 разом з атомом або атомами, з котрими вони зв'язані, утворюють моноциклічне гетероциклічне кільце, яке має 5, 6 або 7 атомів кільця.
15. Сполука за будь-яким з пп. 11-14, яка відрізняється тим, що R1 є Н, F, Сl, метил, метокси або метилендіокси.
16. Сполука за будь-яким з пп. 11-14, яка відрізняється тим, що R1 є F у 6-му положенні 3-оксо-1,3-дигідро-2Н-піразол[4,3-с]цинолін-2-ільної циклічної системи.
17. Сполука за будь-яким з пп. 11-16, яка відрізняється тим, що R3 є Н, F, Сl, метил, метокси або метилендіокси.
18. Сполука за будь-яким з пп. 11-17, яка відрізняється тим, що X є зв'язок або радикал -СН2- чи -СН2-СН2-.
19. Сполука, яка описується формулою (IС)
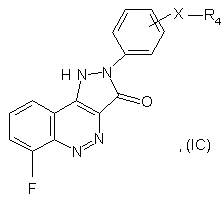
де Х і R4 є такими, як визначено в будь-якому з пп. 3, 7-10 або 11-18, або прийнятні у фармацевтиці чи ветеринарії її сіль, гідрат і сольват.
20. Сполука за п. 18, яка відрізняється тим, що радикал R4X- є в положенні 4 фенільного кільця.
21. Сполука за п. 19 або 20, яка відрізняється тим, що X є зв'язок, a R4 є -C(=C)NR6R7, де R6i R7 є такими, як визначено відповідно в пп. 11, 13 або 14.
22. Сполука, 4-(6-фтор-3-оксо-1,3-дигідропіразол[4,3-с]цинолін-2-іл)-N-(2,2-дифторетил)бензамід, що описується формулою (А)
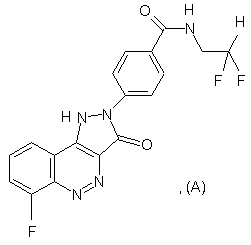
або прийнятні у фармацевтиці чи ветеринарії її сіль, гідрат і сольват.
23. Сполука, N-[3-(трет-бутилметиламіно)бутил]-4-(6-фтор-3-оксо-1,3-дигідропіразол[4,3-с]цинолін-2-іл)бензамід, що описується формулою (В):
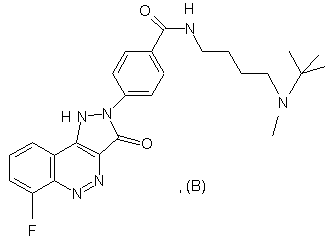
або прийнятні у фармацевтиці чи ветеринарії її сіль, гідрат і сольват.
24. Фармацевтичний або ветеринарний склад, який містить сполуку за будь-яким з пп. 1-23 разом із прийнятним у фармацевтиці або ветеринарії ексципієнтом чи носієм.
25. Сполука за будь-яким з пп. 1-23, яка відрізняється тим, що вона призначена для застосування при лікуванні медичних станів, на які благодійно впливає імуномодуляція.
26. Сполука за будь-яким з пп. 1-23, яка відрізняється тим, що вона призначена для виготовлення лікарського препарату для застосування при лікуванні медичних станів, на які благодійно впливає імуномодуляція.
27. Процес імуномодуляції у ссавця і, в тому числі, людини, який полягає в уведенні ссавцю, що потребує такого лікування, ефективної імуномодуляторної дози сполуки за будь-яким з пп. 1-23.
28. Сполука за п. 25 або п. 26, яка відрізняється тим, що імуномодуляцією є імуноінгібування.
29. Сполука за п. 25 або п. 26, яка відрізняється тим, що згаданим медичним станом є аутоімунне захворювання, ревматоїдний артрит, розсіяний склероз, діабет, астма, трансплантація, системний червоний вовчак і псоріаз.
30. Процес за п. 27, який відрізняється тим, що імуномодуляцією є
імуноінгібування.
31. Процес за п. 27, який відрізняється тим, що згаданим медичним станом є аутоімунне захворювання, ревматоїдний артрит, розсіяний склероз, діабет, астма, трансплантація, системний червоний вовчак і псоріаз.
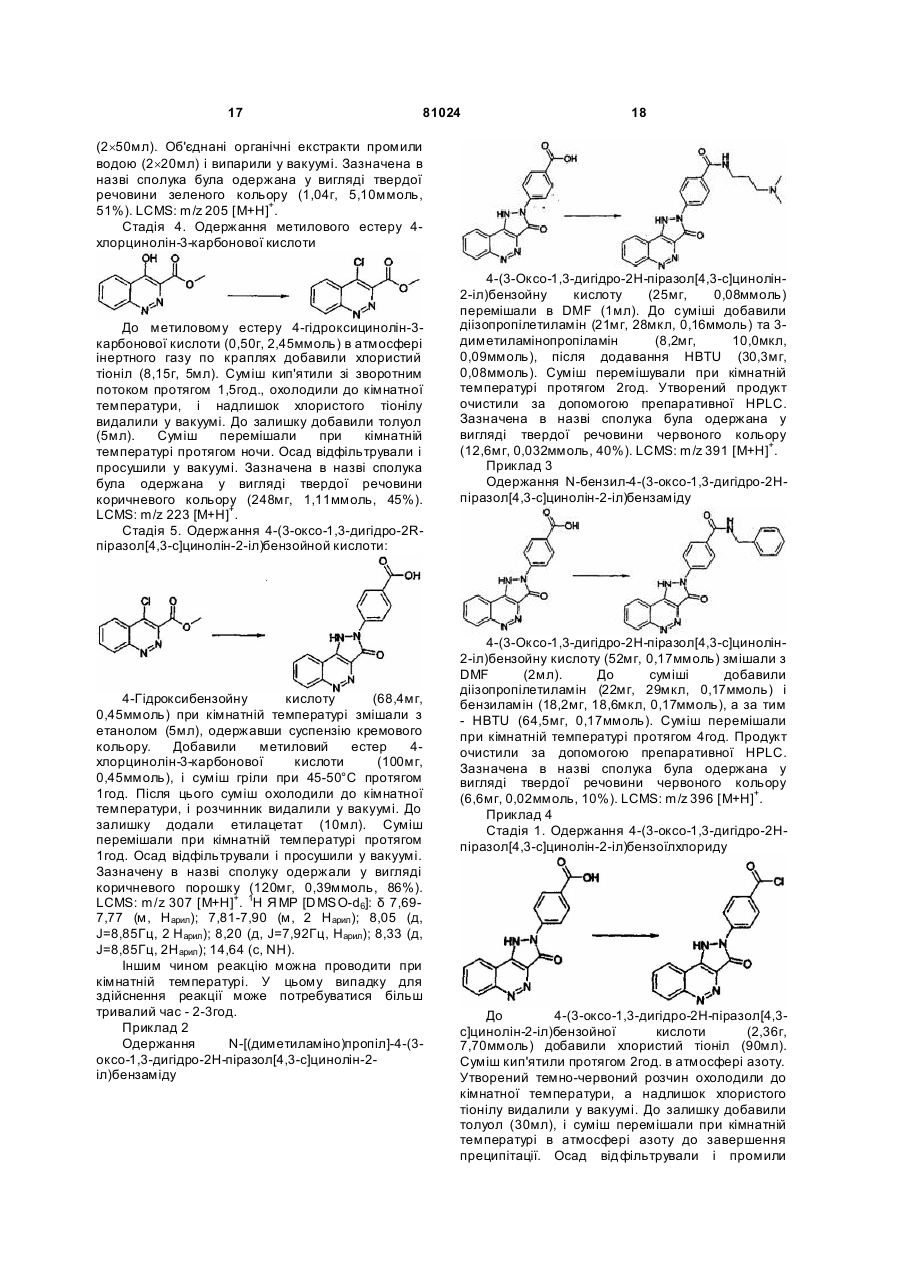
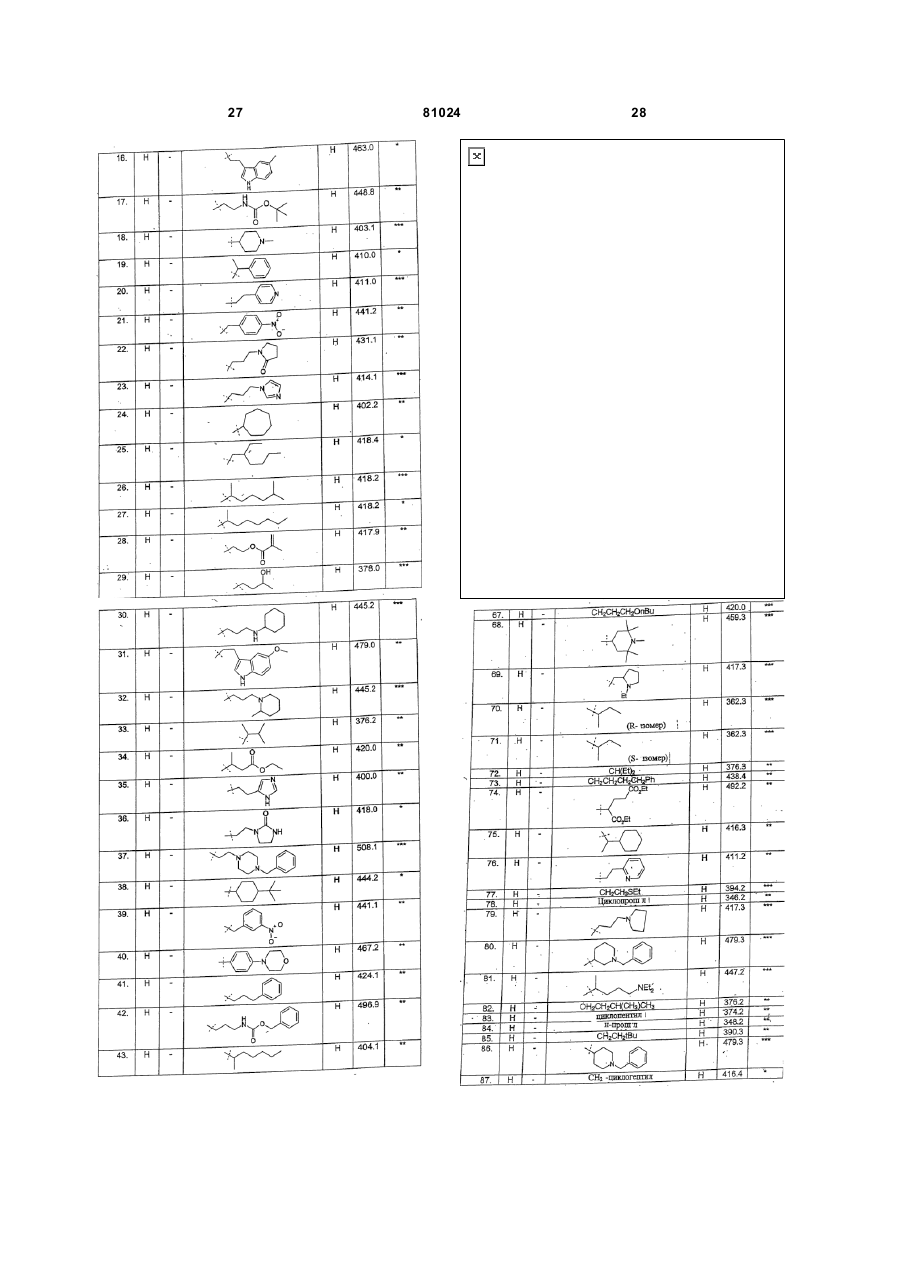
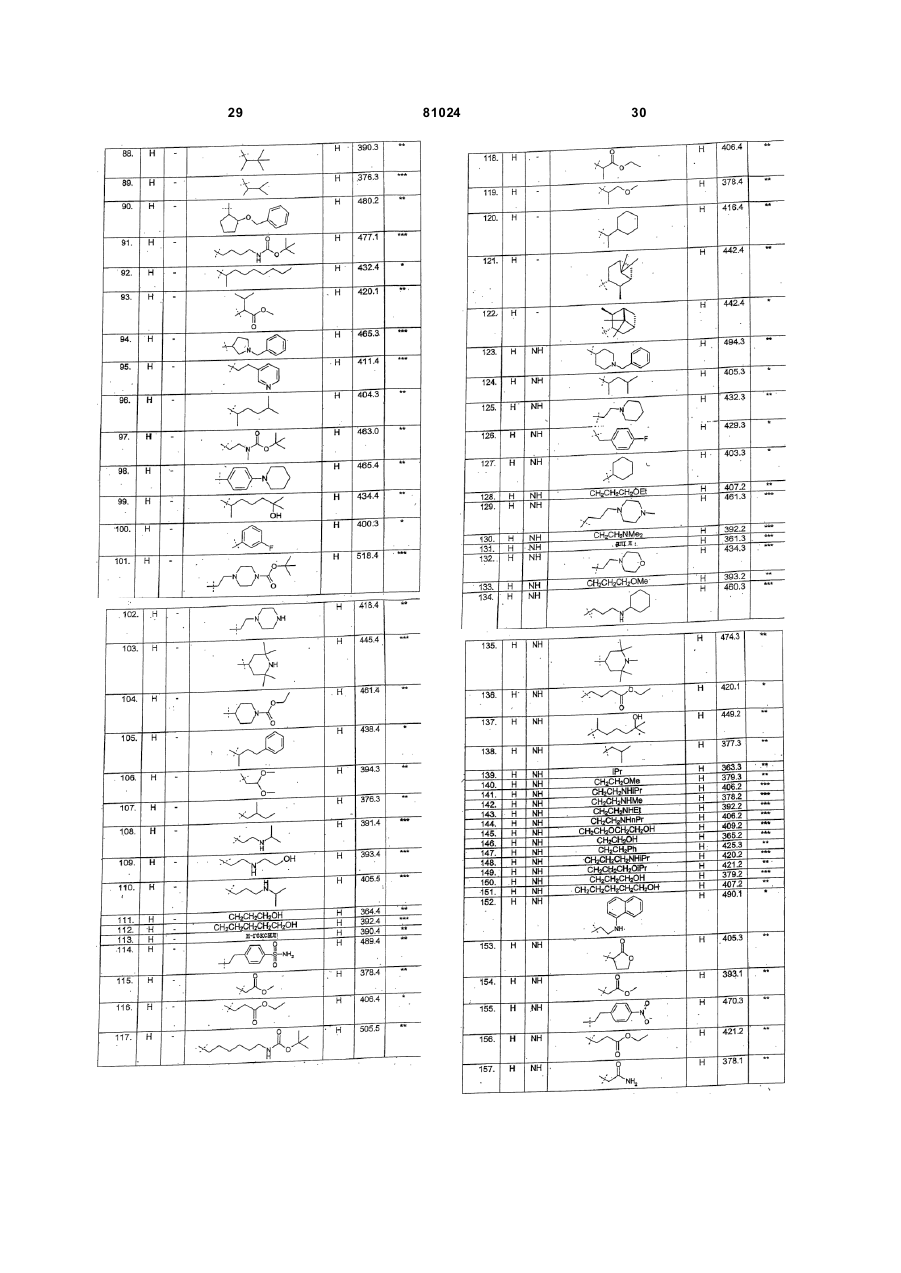
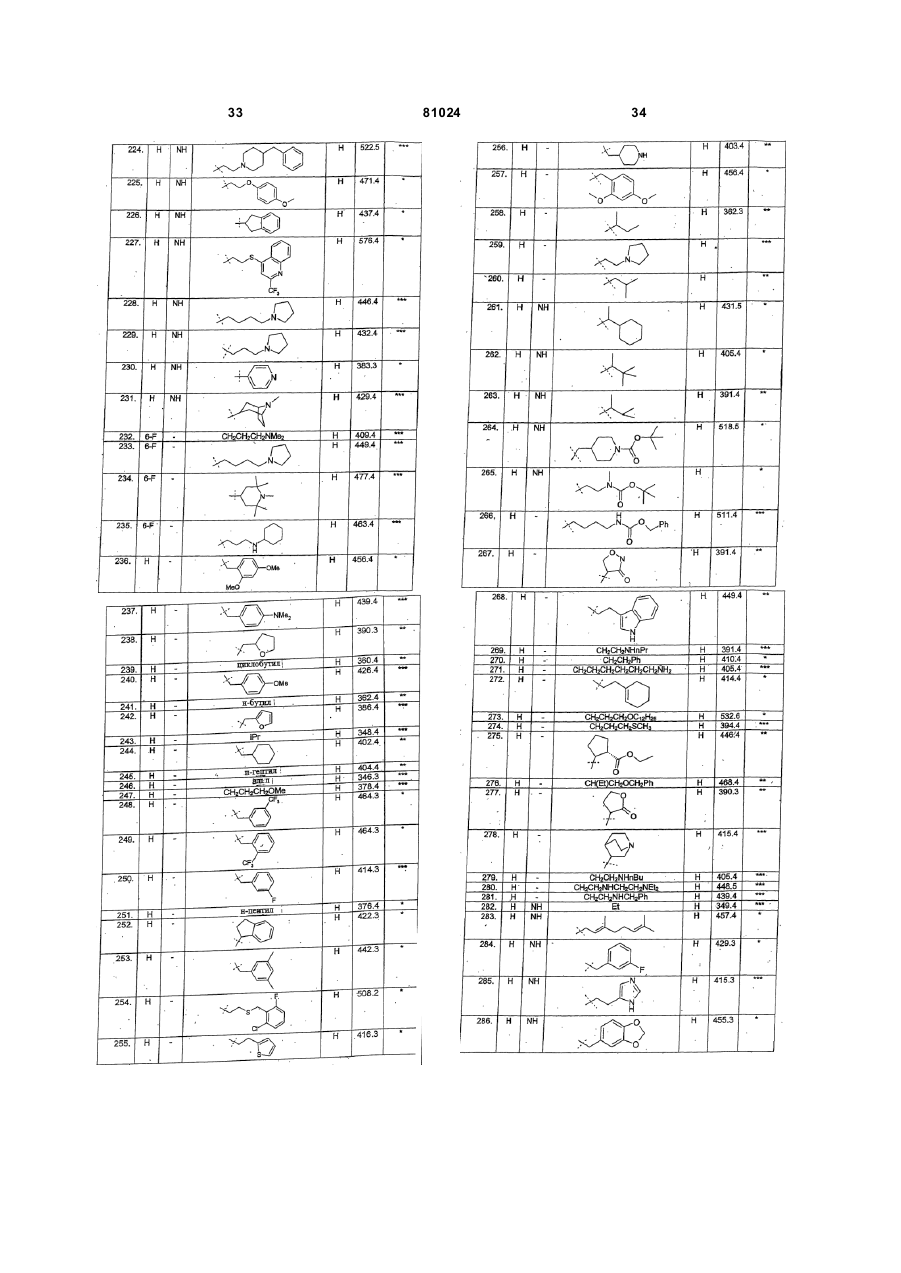
Текст
1. Сполука, що описується формулою (І) C2 2 (19) 1 3 81024 циклоалкіл; естерна група; у разі потреби заміщена карбоциклічна або гетероциклічна група; або R9 і R10 разом з атомом азоту, з яким вони зв'язані, утворюють кільце, яке в разі потреби є заміщеним. 10. Сполука за будь-яким з пп. 6-8, яка відрізняє ться тим, що R7 є водень. 11. Сполука за п. 1, яка відрізняється тим, що Q означає Н; CF3; -OH; -SH; -NR8R8, де кожний R8 незалежно один від одного означає Н; С1-С4 алкіл; С3-С4 алкеніл; С3-С4алкініл; С3-С6 циклоалкіл; естерну груп у; у разі потреби заміщену арильну, арилокси, циклоалкільну, циклоалкенільну або гетероциклічну груп у; або разом з атомом азоту, з яким вони зв'язані, утворюють кільце; а R7 є Н або С1-С6 алкіл; або R6 і R7 разом з атомом або атомами, з якими вони зв'язані, утворюють моноциклічне гетероциклічне кільце, яке має 5, 6 або 7 атомів кільця. 12. Сполука за п. 11, яка відрізняється тим, що R4 є карбокислотна група (-СООН) або естерна група -COOR, де R означає метил, етил, н- або ізопропіл, н-, вторинний або третинний бутил або бензил. 13. Сполука за п. 11 або п. 12, яка відрізняється тим, що R6 є радикал, що описується формулою (Alk)m-Q, де m є 1, Alk є: -СН2-, -СН2СН2-, СН2СН2СН2або -СН2СН(СН3)СН2-, або двовалентний циклопропіленовий, циклопентиленовий чи циклогексиленовий радикал, у разі потреби заміщений групою ОН, оксо, CF3, метокси або етокси, a Q є водень; NR8R8, де R8 можуть бути однаковими або різними і бути вибраними з водню, метилу, етилу, н- або ізопропілу або трет-бутилу; метиловий, етиловий або бензиловий естер; або в разі потреби заміщена фенільна, фенокси, циклопентильна, циклогексильна, фурильна, тієнільна, піперидильна або піперазинільна група. 14. Сполука за будь-яким з пп. 11-13, яка відрізняє ться тим, що R7 є метил, етил, н- або ізопропіл, н-, вторинний або третинний бутил, або R6 і R7 разом з атомом або атомами, з котрими вони зв'язані, утворюють моноциклічне гетероциклічне кільце, яке має 5, 6 або 7 атомів кільця. 15. Сполука за будь-яким з пп. 11-14, яка відрізняє ться тим, що R1 є Н, F, Сl, метил, метокси або метилендіокси. 16. Сполука за будь-яким з пп. 11-14, яка відрізняє ться тим, що R1 є F у 6-му положенні 3оксо-1,3-дигідро-2Н-піразол[4,3-с]цинолін-2-ільної циклічної системи. 17. Сполука за будь-яким з пп. 11-16, яка відрізняє ться тим, що R3 є Н, F, Сl, метил, метокси або метилендіокси. 18. Сполука за будь-яким з пп. 11-17, яка відрізняє ться тим, що X є зв'язок або радикал СН2- чи -СН2-СН2-. 19. Сполука, яка описується формулою (IС) 4 X HN R4 N O N N , (IC) F де Х і R4 є такими, як визначено в будь-якому з пп. 3, 7-10 або 11-18, або прийнятні у фармацевтиці чи ветеринарії її сіль, гідрат і сольват. 20. Сполука за п. 18, яка відрізняється тим, що радикал R4X- є в положенні 4 фенільного кільця. 21. Сполука за п. 19 або 20, яка відрізняється тим, що X є зв'язок, a R4 є -C(=C)NR6R7, де R6i R7 є такими, як визначено відповідно в пп. 11, 13 або 14. 22. Сполука, 4-(6-фтор-3-оксо-1,3дигідропіразол[4,3-с]цинолін-2-іл)-N-(2,2дифторетил)бензамід, що описується формулою (А) H O H N F F HN N O N N , (A) F або прийнятні у фармацевтиці чи ветеринарії її сіль, гідрат і сольват. 23. Сполука, N-[3-(трет-бутилметиламіно)бутил]-4(6-фтор-3-оксо-1,3-дигідропіразол[4,3-с]цинолін-2іл)бензамід, що описується формулою (В): H O N HN N N O N N , (B) F або прийнятні у фармацевтиці чи ветеринарії її сіль, гідрат і сольват. 24. Фармацевтичний або ветеринарний склад, який містить сполуку за будь-яким з пп. 1-23 разом із прийнятним у фармацевтиці або ветеринарії ексципієнтом чи носієм. 5 81024 25. Сполука за будь-яким з пп. 1-23, яка відрізняє ться тим, що вона призначена для застосування при лікуванні медичних станів, на які благодійно впливає імуномодуляція. 26. Сполука за будь-яким з пп. 1-23, яка відрізняє ться тим, що вона призначена для виготовлення лікарського препарату для застосування при лікуванні медичних станів, на які благодійно впливає імуномодуляція. 27. Процес імуномодуляції у ссавця і, в тому числі, людини, який полягає в уведенні ссавцю, що потребує такого лікування, ефективної імуномодуляторної дози сполуки за будь-яким з пп. 1-23. Даний винахід стосується нових гетероциклічних сполук, процесів їх одержання, композицій, що їх містять, а також їх застосування в клінічному лікуванні та процесів клінічного лікування за їх допомогою медичних станів, на які може благодійно впливати імуномодуляція, тобто таких станів, як автоімунне захворювання, ревматоїдний артрит, розсіяний склероз, діабет, астма, трансплантація, системний червоний вовчак, псоріаз тощо. Більш конкретно, даний винахід стосується нових гетероциклічних сполук, що є антагоністами CD80, здатними інгібувати взаємодію між CD80 і CD28, і є придатними до імуноінгібування. Імунна системамає здатність контролювати гомеостаз шляхом активації й інактивації лімфоцитів за допомогою різноманітних регуляторних механізмів під час імунної відповіді і після неї. Серед цих механізмів є такі, що специфічно інгібують і/або вимикають імунну відповідь. Так, коли антиген представлениймолекулами головного комплексу гістосумісності (МНС) до Т-клітинного рецептора, Т-клітини стають відповідним чином активованими тільки за наявності додаткових співстимуляторних сигналів. За відсутності цих додаткових сигналів активація лімфоцитів не відбувається, і викликається стан функціональної інактивації, що зветься анергією чи толерантністю, або Т-клітини специфічно видаляються шляхом апоптозу. Один із таких співстимуляторних сигналів викликає взаємодію CD80 на спеціалізованих клітинах, що презентують антигени, з CD28 на Тклітинах. Було показано, що цей сигнал є важливим для повної активації Т-клітин [Lenschow et al., (1996) Аппи. Rev. Immunol., 14, 233-258]. Отже існує потреба в сполуках, здатних інгібува ти взаємодію між CD80 і CD28. У зв'язку з вищевикладеним, даним винаходом пропонується сполука, що описується формулою (І) 6 28. Сполука за п. 25 або п. 26, яка відрізняється тим, що імуномодуляцією є імуноінгібування. 29. Сполука за п. 25 або п. 26, яка відрізняється тим, що згаданим медичним станом є аутоімунне захворювання, ревматоїдний артрит, розсіяний склероз, діабет, астма, трансплантація, системний червоний вовчак і псоріаз. 30. Процес за п. 27, який відрізняється тим, що імуномодуляцією є імуноінгібування. 31. Процес за п. 27, який відрізняється тим, що згаданим медичним станом є аутоімунне захворювання, ревматоїдний артрит, розсіяний склероз, діабет, астма, трансплантація, системний червоний вовчак і псоріаз. де R1 і R3 незалежно один від одного є Н, F, СІ, Br, -NO2, -CN, C1-C6алкіл, у разі потреби заміщений на F або СІ, або C1-C6алкокси, у разі потреби заміщений на F; R4 є карбокислотна група (-СООН) або її естер, або -C(=O)NR 6R7, -NR7C(=O)R6, NR7C(=O)OR6, -NHC(=O)NR7R6 чи -NHC(=S)NR7R6) де R6 є Н або радикал за формулою -(Alk)m-Q, де m є 0 або 1, Alk означає в разі потреби заміщений двовалентний прямолінійний або розгалужений С1-С12алкіленовий, С2-С12алкеніленовий чи С 2С12алкініленовий радикал, або двовалентний С3С12карбоциклічний радикал, причому будь-який із цих радикалів може містити один або більше -О-, S-або -N(R8)- зв'язків, де R8 означає Η або С 1С4алкіл, С3-С4алкеніл, С3-С4алкініл або С3С6циклоалкіл, і Q є: Н; -NR9R10, де R9 і R10 незалежно один від одного є Н; C1-C4алкіл; С3-С4алкеніл; С3-С4алкініл; С3-С6циклоалкіл; естерна група; в разі потреби заміщена карбоциклічна або гетероциклічна група; або R9 і R10 разом з атомом азоту, з яким вони зв'язані, утворюють цикл, який у разі потреби є заміщеним; і R7 є Η або C1-C6алкіл, або R6 і R7 разом з атомом або атомами, з якими вони зв'язані, утворюють у разі потреби заміщений моноциклічний гетероцикл, який містить 5, 6 або 7 атомів у кільці; X означає зв'язок або двовалентний радикал, що описується формулою -(Z)n-(Alk)-або -(Alk)-(Z)n, де Ζ означає -О-, -S- або -ΝΗ-, Alk визначений так, як це визначено для R6, а п є 0 або 1. Сполуки (І) можуть існувати у формі таутомерів на зразок (І1) і (І 2): 7 81024 У подальшому сполуки згідно з даним винаходом можуть подаватися і позначатися в тій чи іншій таутомерній формі (І), яка разом з усіма іншими таутомерними формами, що мають структур у (І) і, зокрема, структури (І1) і (І2), охоплюються об'ємом даного винаходу. Сполуки, що описуються загальною формулою (І), є антагоністами CD80. Вони інгібують взаємодію між CD80 і CD28 і, отже, активацію Тклітин, модулючи тим імунну відповідь. У відповідності з цим, даним винаходом також передбачені: (і) застосування сполуки, що описується формулою (І), або її прийнятної у фармацевтиці чи ветеринарії солі в лікуванні медичних станів, на які може благодійно впливати імуномодуляція, і зокрема в імуноінгібуванні; (іі) застосування сполуки, що описується формулою (І), або її прийнятної у фармацевтиці чи ветеринарії солі у виготовленні лікарського препарату для лікування медичних станів, на які може благодійно впливати імуномодуляція, і зокрема, для імуноінгібування; (ііі) процес імуномодуляції і, зокрема, імуноінгібування у ссавців, включаючи людей, який полягає в уведенні ссавцю, котрий потребує такого лікування, ефективної імуномодуляторної дози сполуки, що описується формулою (І), або її прийнятної у фармацевтиці чи ветеринарії солі; (iv) фармацевтичний або ветеринарний склад, який містить сполуку, що описується формулою (І), або її прийнятну у фармацевтиці чи ветеринарії сіль разом з прийнятним у фармацевтиці чи в ветеринарії ексципієнтом чи носієм. До числа станів, на які благодійно впливає імуномодуляція, належать Гострий розсіяний енцефаломієліт Недостатність ниркової залози Алергічний васкуліт і гранульоматоз Амілоїдоз Анкілозивний спондилоартрит Астма Автоімунна хвороба Адісона Автоімунна алопеція Автоімунний хронічний активний гепатит Автоімунна гемолітична анемія Автоімунний Neutrogena Автоімунна тромбоцитопенічна пурпура Хвороба Бехчета Церебелярна дегенерація 8 Хронічний активний гепатит Хронічна запальна демієлінізивна полірадикулоневропатія Хронічна нейропатія з моноклональною гамопатією Класичний вузликовий поліартеріїт Уроджена гіперплазія надниркових залоз Кріопатія Герпетиформний дерматит Діабет Міастенічний синдром Ітона-Ламберта (EatonLambert) Енцефаломієліт Набутий бульозний епідермоліз Вузликова еритема Глютенова ентеропатія Синдром Гудпасчера (Goodpasture) Синдром Пйєна- Баре Тиреоїдит Хашімото Гіпертиреоз Ідіопатичний гемохроматоз Ідіопатичний мембранозний гломерулонефрит Ізольований васкуліт центральної нервової системи Хвороба Кавасакі Хвороба нирок з мінімальними змінами Багатобічні васкуліти Хвороба змішаних сполучни х тканин Мультифокальна моторна невропатія з провідниковою анестезією Розсіяний склероз Тяжка псевдопаралітична міастенія Очний опсоклонус-міоклонус Пемфігоїд Пухирчатка Злоякісна анемія Поліміозит і дерматоміозит Постінфекційні ураження шкіри Первинний біліарний склероз Псоріаз Реактивні ураження шкіри Хвороба Рейтера Ретинопатія Ревматоїдний артрит Склерозивний холангід Синдром Сьогрена Синдром ригідності людини Підгострий тиреоїдит Системний червоний вовчак Системні некротизивні васкуліти Системний склероз (склеродермія) Артеріїт Такаясу Скроневий артеріїт Облітеруючий тромбоангіїт Автоімунний полігландулярний синдром І типу і II типу Виразковий коліт Увеїт Гранульоматоз Вегенера Терміном "естер" у даному описі позначаються групи виду -COOR, де R є радикал, який умовно походить від спирту ROH. До числа естерних гр уп належать, наприклад, естери, що піддаються фізіологічному гідролізу, такі як метилові, етилові, 9 81024 н- та ізопропілові, н-, вторинні і третинні бутилові і бензилові естери. Використовуваним у даному описі терміном "алкілен" позначається прямолінійний або розгалужений алкільний ланцюг, який має дві вільні валентності, наприклад, -СН2-, -СН2СН2-, СН2СН2СН2-, -СН2(СН3)СН2-, СН(СН2СН3)СН2СН2СН2- і -С(СН3)3. Використовуваним у даному описі терміном "алкенілен" позначається прямолінійний або розгалужений алкенільний ланцюг, який має дві вільні валентності, наприклад, -СН Н -, = С СН2СН СН-, = -С(СН3)=СНі СН(СН2СН3)СН СНСН2-. = Використовуваним у даному описі терміном "алкінілен" позначається прямолінійний або розгалужений алкінільний ланцюг, який має дві вільні валентності, наприклад, -СºСН-, -СН2СºС- і -СН(СН2СН3)СºССН2-. Якщо в контексті терміну "заміщений" не зазначено іншого, то застосовуваний до будь-якої хімічної субстанції, він означає, що вона є заміщеною, принаймні, одним замісником, вибраним, наприклад, серед (С1-C6)алкілу, (С1C6)алкенілу, (С2-С6)алкінілу, фторзаміщеного (С1C6)алкілу, фторзаміщеного (С1-C6)алкенілу, фторзаміщеного (С2-С6)алкінілу, (С1-C6)алкокси і фторзаміщеного (С1-C6)алкокси (включаючи особливий випадок, коли цикл є заміщеним на сусідніх С-атомах кільця групою алкілендіокси, наприклад, метилендіокси або етилендіокси), (С1C6)алкілтіо, фенілу, бензилу, фенокси, бензилокси, гідрокси, меркапто, аміно, фтор у, хлор у, брому, ціано, нітро, оксо, -СООН, -SO2OH, -CONH2, SO2NH2, -COR A, -COOR A , -SO2 ORA, -NHCORA, NHSO2RA, -CONHRA, -SO 2NHRA, -NHRA, -NRARB, CONRARB або -SO2NRARB, де RA і RB незалежно один від одного є (С1-C6)алкільною або (С2С6)алкоксильною групою або моноциклічною карбоциклічною чи гетероциклічною 5-7- членною групою, або ж RA і RB разом з атомом вуглецю, з яким вони зв'язані, утворюють цикл. У тому випадку, коли термін "заміщений" означає заміщеність фенільною, бензильною, феноксиабо бензилоксигрупою, фенільне кільце в цих групах само може бути заміщеним будь-яким із вищезазначених замісників, за винятком фенілу, бензилу, фенокси та бензилокси. Використовуваний у даному описі термін "арил" означає моно-, бі- або трициклічний ароматичний радикал, а також два такі радикали, ковалентно зв'язані один з одним, наприклад, феніл, біфеніл, нафтил і т.п. Використовуваний у даному описі узагальнений термін "карбоцикліл" або "карбоциклічний" охоплює своїм значенням арил, циклоапкіл і циклоалкеніл і стосується циклічної системи (моноциклічної, біциклічної, трициклічної або зшитої), в котрій всіма атомами кільця є атоми вуглецю. Використовуваний у даному описі узагальнений термін "цикпоалкіл" означає карбоциклічну систему, котра містить тільки прості зв'язки між атомами вуглецю в кільці. 10 Використовуваний у даному описі узагальнений термін "циклоалкеніл" означає карбоциклічну систему, котра містить, принаймні, один подвійний зв'язок між двома атомами вуглецю в кільці. Використовуваний у даному описі термін "гетероарил" означає моно, бі- або трициклічний ароматичний радикал, який містить один або більше гетероатомів, вибраних серед S, N і О. Як приклади таких радикалів можна назвати тієніл, бензотієніл, фурил, бензофурил, піроліл, імідазоліл, бензимідазоліл, тіазоліл, бензотіазоліл, ізотіазоліл, бензизотіазоліл, піразоліл, оксазоліл, бензоксазоліл, ізоксазоліл, бензизоксазоліл, триазоліл, бензтриазоліл, тіадіазоліл, оксадіазоліл, піридиніл, піридазиніл, піримідиніл, піразиніл, триазиніл, індоліл і індазоліл. Використовуваний у даному описі узагальнений термін "гетероцикліл" або "гетероциклічний" охоплює своїм значенням "гетероарил" згідно з визначеним вище і, зокрема, означає моно, бі- і трициклічний або зшитий неароматичний радикал, який містить один або більше гетероатомів, вибраних серед S, N і О, а також означає групи, які по суті являють собою моноциклічний неароматичний радикал, що містить один або більше гетероатомів і є ковалентно зв'язаний з іншим таким же радикалом або з моноциклічним карбоциклічним радикалом. Як приклади таких радикалів можна назвати піроліл, фураніл, тетрагідрофураніл, тієніл, піперидиніл, імідазоліл, оксазоліл, ізоксазоліл, тіазоліл, тіадіазоліл, піразоліл. піридиніл, піролідиніл, піримідиніл, морфолініл, піперазиніл, індоліл, морфолініл, бензофураніл, піраніл, тетрагідропіраніл, хінуклідиніл, ізоксазоліл, бензимідазоліл, метилендіоксифеніл, етилендіоксифеніл, малеїнімідоі сукцинимідогрупи. Деякі сполуки згідно з даним винаходом внаслідок наявності в них асиметричних вуглецевих атомів містять один і більше хіральних центрів. Наявність асиметричних вуглецевих атомів є причиною виникнення стереоізомерів або діастереоізомерів з R і S стереохімією на кожному хіральному центрі. Даним винаходом охоплюються всі такі стереоізомери і діастереоізомери та їх суміші. До числа солей солетворних сполук згідно з даним винаходом належать фізіологічно прийнятні солі приєднання кислот та основні солі. Підходящі солі приєднання кислот одержують із кислот, що утворюють нетоксичні солі. Ними можуть бути, наприклад: ацетати, аспартати, бензоати, безилати, бікарбонати і карбонати, бісульфати і сульфати, борати, камзилати, цитрати, едизилати, езилати, форміати, фумарати, глюцептати, глюконати, глюкуронати, гексафторфосфати, гібензати, гідрохлориди і хлориди, гідроброміди і броміди, гідройодиди і йодиди, ізетіонати, лактати, малати, малеати, малонати, мезилати, метилсульфати, нафтилати, 2напсилати, нікотинати, нітрати, оротати, оксалати, пальмітати, памоати, фосфати, гідрофосфати і дигідрофосфати, сахарати, стеарати, сукцинати, 11 81024 тартрати, тозилати і трифторацетати. Відповідні основні солі одержують із основ, що утворюють нетоксичні солі. До їх числа належать, наприклад, солі алюмінію, аргінину, бензатину. кальцію, холіну, діетиламіну, діоламіну, гліцину, лізину, магнію, меглуміну, оламіну, калію, натрію, трометаміну і цинку. Процеси одержання Сполуки згідно з даним винаходом, у котрих R4 являє собою амідну гр упу -C(=O)NR 6R7, можна отримувати за допомогою реакції відповідного аміну HNR6R7 зі сполукою, що описується формулою (II) внаслідок чого відбувається амідування кислотної карбоксильної групи. У формулі (II) символи R1, R3, X, R6 i R7 відповідають визначенням, даним до формули (І). Сполуки (II) (тобто сполуки (І) згідно з даним винаходом, в яких R4 є кислотною карбоксильною групою) можна отримувати шляхом реакції сполуки, що описується формулою (III), з гідразином, що описується формулою (IV): У результаті цієї реакції може утворюватися суміш ізомерів положення (IIА) і (ІІВ): Сполуки (І), в яких R4 означає естерну або амідну груп у, можна також отримувати із проміжного продукту (III) шляхом реакції з відповідним гідразином (IVA) де R4 означає естерну або амідну групу. Тут також у результаті реакції може утворитися суміш естерних або амідних аналогів карбонових кислот (НА) і (ІІВ), із котрої можна виділити потрібний ізомер естеру або аміду. Інакше карбонову кислоту (II) можна просто естерифікувати або амідувати. Сполуки (І), в котрих R4 є "оберненою амідною" групою -NR7C(=O)R6, можна отримувати шляхом перегрупування Куртіса (Curtius) [Ninomiya, К.; Shiori, Т.; Yamada, S. Tetrahedron 12 (1974), 30(14), 2151-7] карбонової кислоти (II) на ізоціанат (V) з наступним гідролізом ізоціанатної групи до аміногрупи й ацилюванням аміногрупи, наприклад, хлорангідридом кислоти CI-C(=O)R 6. У тих випадках, коли R7 не є воднем, замісник R7 може бути введений після стадії відновлення ізоціанату або після стадії ацилювання. В альтернативному процесі одержання "обернених амідів" (R4=-NR7C(=O)R6) згідно з даним винаходом сполуку зі стр уктурою (V), у котрій ізоціанатна частина заміщується нітрогрупою, можна відновити до відповідного аміну, котрий після цього можна піддати ацилюванню з утворенням потрібного оберненого аміду. Сполуки (І), в котрих R4 є карбамідною групою -NHC(=O)HNR6 або тіокарбамідною групою NHC(=S)HNR6, можна отримувати також із ізоціанату (V) або відповідного ізотіоціанату шляхом реакції з відповідним аміном H2NR5. Сполуки (І), в котрих R4 є карбаматною групою -NR7C(=O)OR6, можна отримувати за допомогою реакції ізоціанату з відповідним спиртом R6OH. Подальші деталі щодо процесів синтезу сполук (І) згідно з даним винаходом і проміжних продуктів (III) можна знайти в наведених нижче прикладах. У сполуках згідно з даним винаходом: радикал R4X- переважно займає положення 4 фенільного кільця; X може бути, наприклад, зв'язком або радикалом -СН2- чи - СН2СН2-, причому кращим є зв'язок; R3 може бути, наприклад, Н, F, СІ, метил, метокси або метилендіокси, причому в кращому варіанті R3 є Η; R1 може бути, наприклад, Н, F, СІ, метил, метокси або метилендіокси, причому в кращому варіанті R1 є водень або фтор і особливо в положенні 6 3-оксо-1,3-дигідро-2Н-піразол[4,3с]цинолін-2-ільної циклічної системи; R4 є карбокислотною групою (-СООН) або її естером, або -C(=O)NR 6R7, -NR7C(=O)R6, NR7C(=O)OR6 чи -NHC(=O)NHR6, що є такими, як визначено вище. У тих випадках, коли R4 є естерною групою, вона визначається формулою -COOR, де R є, наприклад, метиловий, етиловий, набо ізопропіловий, н-, вторинний або третинний бутиловий, або бензиловий естер. R6 у разі його наявності є Η або радикалом, що описується формулою -(Alk) m-Q, де m, Alk і Q є такими, як визначено вище. Коли m є 1, Alk може бути, наприклад, прямолінійним або розгалуженим С1-С6 алкіленом, наприклад, -СН2-, -СН2СН2-, СН2СН2СН2- і -СН2СН(СН3)СН2-. Alk може бути 13 81024 також двовалентним циклопропіленовим, циклопентиленовим або циклогексиленовим радикалом. Радикал Alk, у разі потреби, може бути заміщеним, наприклад, групою ОН, оксо, CF3, метокси або етокси. Радикал Alk, у разі потреби, може містити гетеро атом, наприклад, у формі етерного, тіоетерного або амінового зв'язку. Компонентом Q може бути, наприклад, водень; -NR9R10, де R9 і R10 можуть бути однаковими або різними і вибиратися серед водню, метилу, етилу, н- або ізопропілу або третбутилу; естерна група, наприклад, метиловий, етиловий або бензиловий естер; або, в разі потреби, заміщена арильна, арилокси, цикпоалкільна, циклоалкенільна або гетероциклічна група, така як фенільна, фенокси, циклопентильна, циклогексильна, фурильна, тієнільна, хінуклідильна, піперидильна або піперазинільна група. R7 у разі його наявності є Η або С 1-C6алкіл, наприклад, метил, етил, н- або ізопропіл, н-, вторинний або третинний бутил; або R6 і R7 разом з атомом або атомами, з котрими вони зв'язані, утворюють моноциклічний гетероцикл, який має 5, 6 або 7 кільцевих атомів. Особливо прийнятними є варіанти, в котрих R 4 є C(=O)NR6R7 або -NHC(=O)NR 7R6, де R7 означає водень, a R6 - радикал, що описується формулою (Alk)m-Q, де m є 1, а двовалентний Alk-радикал містить 3 або 4 вуглецевих атоми і є незаміщеним, Q є –NR 9R10 , де R9 і R10 незалежно один від одного є Н; С1-C4алкіл; С3-С4алкеніл; С3-С4алкініл; С3С6циклоалкіл; естерна група; у разі потреби заміщена карбоциклічна або гетероциклічна група; або R9 і R10 разом з атомом азоту, з яким вони зв'язані, утворюють кільце, яке в разі потреби є заміщеним. До особливо кращої підмножини сполук згідно з даним винаходом належать такі, що мають формулу (IС): де X і R4 є такими, як визначено вище. У цих сполуках радикал R4X- може займати положення 4 фенільного кільця. До числа сполук цієї підмножини входять, зокрема, такі, в котрих X є зв'язок, a R 4 є -C(=O)NR 6R7, де R6 і R7 є такими, як визначено вище. У таких сполуках R6 може бути, наприклад, хінуклідинілом, a R7 - воднем. У розглянути х нижче Прикладах наведені конкретні варіанти сполук згідно з даним винаходом. Кращою серед запропонованих сполук є 4-(6фтор-3-оксо-1,3-дигідропіразол[4,3-с]цинолін-2-іл)N-(2,2-дифторетил)бензамід за формулою (А): 14 її прийнятні у фармацевтиці чи ветеринарії сіль, гідрат чи сольват. Іншою кращою сполукою згідно з даним винаходом є Ν-[3-(трет-бутилметиламіно)бутил]-4(6-фтор-3-оксо-1,3-дигідропіразол[4,3-с]цинолін-2іл)бензамід за формулою (В): або її прийнятні у фармацевтиці чи ветеринарії сіль, гідрат чи сольват. Як зазначалося вище, винаходом передбачена фармацевтична або ветеринарна композиція, до якої входить сполука за формулою (І) або її прийнятна у фармацевтиці чи ветеринарії сіль разом з прийнятним у фармацевтиці чи ветеринарії ексципієнтом або носієм. Цілком зрозуміло, що рівень дози такої композиції для кожного пацієнта залежить від ряду чинників, включаючи активність конкретної використовуваної сполуки, вік, масу тіла, загальний стан здоров'я, стать, харчування, час уведення ι спосіб уведення ліків, швидкість екскреції, комбінування ліків і причину, а також тяжкість захворювання, що лікується. Оптимальні дози і частота прийому ліків визначаються шляхом клінічних тестів. Сполуки, яких стосується даний винахід, можна готува ти для введення будь-яким способом, що відповідає їхнім фармакокінетичним властивостям. Композиції для перорального застосування можуть мати форму таблеток, капсул, порошку, гранул, коржів, рідких і желеподібних препаратів, таких як розчини та суспензії для перорального або місцевого введення або стерильні розчини та суспензії для парентерального введення. Таблетки і капсули для перорального введення можуть мати порційну лікарську форму і містити звичайні ексципієнти, а саме: сполучні, такі як сироп, аравійську камедь, желатин, сорбіт, трагакантову камедь або полівінілпіролідон; наповнювачі, наприклад, лактозу, цукор, маїсовий крохмаль, фосфат кальцію, сорбіт або гліцин; мастило для таблетування, наприклад, стеарат магнію, тальк, 15 81024 поліетиленгліколь або оксид кремнію; речовини, що сприяють здрібненню, наприклад, картопляний крохмаль, а також підходящі поверхнево-активні речовини на зразок лаурилсульфату натрію. Таблетки можуть бути покриті оболонкою за допомогою процесів, добре відомих у звичайній фармацевтичній практиці. Пероральні рідкі препарати можуть мати форму, наприклад, водних або масляних суспензій, розчинів, емульсій, сиропів або еліксирів, або ж сухого продукту, який перед застосуванням приводять у рідку форму за допомогою води чи іншого підходящого носію. Такі рідкі препарати можуть містити звичайні добавки, такі як суспендувальні агенти, наприклад, сорбіт, сироп, метилцелюлозу, сироп глюкози, желатин, гідровані харчові жири; емульгатори, наприклад, лецитин, сорбітанмоноолеат або аравійська камедь; неводні носії (у тому числі харчові олії), наприклад, мигдальна олія, фракціонована кокосова олія, маслоподібні естери, такі, як гліцерин, пропіленгліколь, або етиловий спирт; консерванти, наприклад, метиловий або пропіловий естер п-гідроксибензойної кислоти, або сорбінова кислота, а в разі потреби також звичайні смакові коригенти, ароматизатори і барвники. Для місцевого застосування на шкірі лікарський препарат може бути приготований у формі крему, лосьйону або мазі. Склади цих лікарських форм є звичайними і описані, наприклад, в таких загальних посібниках з фармацевтики, як British Pharmacopoeia. Для місцевого застосування в офтальмології лікарському препарату можна надавати форму розчину або суспензії в підхожому стерильному водному чи іншому носію. До нього можуть входити також добавки, наприклад, буфери, такі як метабісульфіт натрію або двонатровий едеат; консерванти, включаючи бактерицидні і фунгіцидні агенти, такі, як фенілртутьацетат або фенілртутьнітрат, бензалконійхлорид або хлоргексидин, а також згущувачі, такі як гіпромелоза. Активний інгредієнт можна вводити також парентерально в стерильному середовищі. Залежно від використовуваного носія і концентрації, лікарський препарат може бути в носії в суспендованому або розчиненому стані. У носії можуть бути розчинені також такі ад'юванти, як місцеві анестетики, консерванти і буферизуючі агенти. У наведених нижче прикладах описані деякі варіанти здійснення даного винаходу, що не мають обмежувального характеру. При цьому в описах експериментів використовуються такі скорочення: DMF Диметилформамід DMA Диметилацетамід DMSO Диметилсульфоксид HBTU Гексафторфосфа т О-бензотриазол- 1іл-N,N,N',N'-тетраметилуронію HPLC Рідинна хроматографія високої розрізнювальної спроможності LCMS Рідинна хроматографія + масспектроскопія 16 ЯМР Спектроскопія ядерного магнітного резонансу Приклад 1 Стадія 1. Одержання (фенілгідразон)малонової кислоти Моногідрат мезоксалату натрію (5,00г, 27,8ммоля) розчинили в 1молі соляної кислоти (50мл), одержавши безколірний каламутний розчин. До цієї суміші в умовах перемішування при кімнатній температурі по краплях добавили фенілгідразин (3,00г, 2,72мл, 27,8ммоль). У результаті утворився жовтий осад. Через 90хв. осад відфільтрували і промили водою (50мл). Далі осад розтерли з сумішшю етилацетат/гексан [1:1], відфільтрували і просушили у вакуумі. Зазначена в назві сполука була одержана у вигляді жовтого порошку (4,74г, 22,7ммоль, 82%). LCMS: m/z 207 [М-Н]+. Іншим чином утворений продукт можна екстрагувати із водної фази етилацетатом (2´250мл), органічну фазу просушити над сульфатом магнію, відфільтрувати, а розчинник видалити у вакуумі. Стадія 2. Одержання (фенілгідразон)малоноїлдихлориду (Фенілгідразон)малонову кислоту (1,00г, 4,80ммоль) в атмосфері інертного газу змішали з сухим хлороформом (15мл), одержавши жовту суспензію. Суспензію перемішали при кімнатній температурі, і до неї порціями додали п'ятихлористий фосфор (2,19г, 10,5ммоль). Реакційну суміш кип'ятили зі зворотним потоком протягом 1,5год., одержавши розчин зеленого кольору. Суміш охолодили до кімнатної температури, і до неї добавили гексан (15мл). У результаті утворився зелений осад, який відфільтрували і просушили у вакуумі. Зазначена в назві сполука була одержана у вигляді порошку зеленого кольору (645мг, 2,63ммоль, вихід 53%). Стадія 3. Одержання метилового естеру 4гідроксицинолін-3-карбонової кислоти Дихлорангідрид (фенілгідразон)малонової кислоти (2,45г, 0,01ммоль) в інертній атмосфері змішали з 1,2- дихлоретаном (15мл), одержавши жовту суспензію. По краплях добавили чотирихлористий титан (1,89г, 1,09мл). В результаті утворився коричневий розчин. Суміш кип'ятили протягом ночі, після чого до неї добавили метанол (15мл). Далі перемішування продовжували ще протягом 30хв., і леткі продукти видалили у вакуумі. Добавили воду (100мл), й отриману суспензію екстрагували н-бутанолом 17 81024 18 (2´50мл). Об'єднані органічні екстракти промили водою (2´20мл) і випарили у вакуумі. Зазначена в назві сполука була одержана у вигляді твердої речовини зеленого кольору (1,04г, 5,10ммоль, 51%). LCMS: m/z 205 [М+Н]+. Стадія 4. Одержання метилового естеру 4хлорцинолін-3-карбонової кислоти До метиловому естеру 4-гідроксицинолін-3карбонової кислоти (0,50г, 2,45ммоль) в атмосфері інертного газу по краплях добавили хлористий тіоніл (8,15г, 5мл). Суміш кип'ятили зі зворотним потоком протягом 1,5год., охолодили до кімнатної температури, і надлишок хлористого тіонілу видалили у вакуумі. До залишку добавили толуол (5мл). Суміш перемішали при кімнатній температурі протягом ночи. Осад відфільтрували і просушили у вакуумі. Зазначена в назві сполука була одержана у вигляді твердої речовини коричневого кольору (248мг, 1,11ммоль, 45%). LCMS: m/z 223 [М+Н]+. Стадія 5. Одержання 4-(3-оксо-1,3-дигідро-2Rпіразол[4,3-с]цинолін-2-іл)бензойной кислоти: 4-Гідроксибензойну кислоту (68,4мг, 0,45ммоль) при кімнатній температурі змішали з етанолом (5мл), одержавши суспензію кремового кольору. Добавили метиловий естер 4хлорцинолін-3-карбонової кислоти (100мг, 0,45ммоль), і суміш гріли при 45-50°С протягом 1год. Після цього суміш охолодили до кімнатної температури, і розчинник видалили у вакуумі. До залишку додали етилацетат (10мл). Суміш перемішали при кімнатній температурі протягом 1год. Осад відфільтрували і просушили у вакуумі. Зазначену в назві сполуку одержали у вигляді коричневого порошку (120мг, 0,39ммоль, 86%). LCMS: m/z 307 [М+Н]+. 1Н Я МР [D MSO-d 6]: δ 7,697,77 (м, Нарил); 7,81-7,90 (м, 2 Нарил); 8,05 (д, J=8,85Гц, 2 Нарил); 8,20 (д, J=7,92Гц, Нарил); 8,33 (д, J=8,85Гц, 2Нарил); 14,64 (с, ΝΗ). Іншим чином реакцію можна проводити при кімнатній температурі. У цьому випадку для здійснення реакції може потребуватися більш тривалий час - 2-3год. Приклад 2 Одержання N-[(диметиламіно)пропіл]-4-(3оксо-1,3-дигідро-2Н-піразол[4,3-с]цинолін-2іл)бензаміду 4-(3-Оксо-1,3-дигідро-2Н-піразол[4,3-с]цинолін2-іл)бензойну кислоту (25мг, 0,08ммоль) перемішали в DMF (1мл). До суміші добавили діізопропілетиламін (21мг, 28мкл, 0,16ммоль) та 3диметиламінопропіламін (8,2мг, 10,0мкл, 0,09ммоль), після додавання HBTU (30,3мг, 0,08ммоль). Суміш перемішували при кімнатній температурі протягом 2год. Утворений продукт очистили за допомогою препаративної HPLC. Зазначена в назві сполука була одержана у вигляді твердої речовини червоного кольору (12,6мг, 0,032ммоль, 40%). LCMS: m/z 391 [М+Н]+. Приклад 3 Одержання N-бензил-4-(3-оксо-1,3-дигідро-2Hпіразол[4,3-с]цинолін-2-іл)бензаміду 4-(3-Оксо-1,3-дигідро-2Н-піразол[4,3-с]цинолін2-іл)бензойну кислоту (52мг, 0,17ммоль) змішали з DMF (2мл). До суміші добавили діізопропілетиламін (22мг, 29мкл, 0,17ммоль) і бензиламін (18,2мг, 18,6мкл, 0,17ммоль), а за тим - HBTU (64,5мг, 0,17ммоль). Суміш перемішали при кімнатній температурі протягом 4год. Продукт очистили за допомогою препаративної HPLC. Зазначена в назві сполука була одержана у вигляді твердої речовини червоного кольору (6,6мг, 0,02ммоль, 10%). LCMS: m/z 396 [М+Н]+. Приклад 4 Стадія 1. Одержання 4-(3-оксо-1,3-дигідро-2Нпіразол[4,3-с]цинолін-2-іл)бензоїлхлориду До 4-(3-оксо-1,3-дигідро-2Н-піразол[4,3с]цинолін-2-іл)бензойної кислоти (2,36г, 7,70ммоль) добавили хлористий тіоніл (90мл). Суміш кип'ятили протягом 2год. в атмосфері азоту. Утворений темно-червоний розчин охолодили до кімнатної температури, а надлишок хлористого тіонілу видалили у вакуумі. До залишку добавили толуол (30мл), і суміш перемішали при кімнатній температурі в атмосфері азоту до завершення преципітації. Осад відфільтрували і промили 19 81024 толуолом (2 χ 30мл). Зазначена в назві сполука була одержана у вигляді твердої речовини червоного кольору (2,20г, 6,77ммоль, 88%). LCMS: m/z 321 [М+Н]+ (метиловий естер, утворений зі складу зразка в метанолі). Стадія 2. Одержання N[(циклогексиламіно)пропіл]-4-(3-оксо-1,3-дигідро2Н-піразол[4,3-с]цинолін-2-іл)бензаміду 4-(3-Оксо-1,3-дигідро-2Н-піразол[4,3-с]цинолін2-іл)бензоїлхлорид (97мг, 0,30ммоль) розчинили в сухому DMA (2мл). Добавили діізопропілетиламін (39мг, 53мкл, 0,60ммоль), а за тим N-циклогексил1,3-пропандіамін (52мг, 0,60ммоль). Суміш перемішали протягом 30хв., після чого до неї добавили воду, одержавши в результаті темночервону суспензію. Суспензію піддали екстрагуванню н-бутанолом (2´20мл). Об'єднані органічні екстракти промили водою і випарювали у вакуумі доти, аж поки не розпочалася преципітація. Добавили гексан (20мл) і етилацетат (10мл), осад відфільтрували і просушили у вакуумі. Виділений продукт мав форму темночервоного порошку (82мг, 0,18ммоль, 62%). LCMS: m/z 445 [М+Н]+. Приклад 5 Стадія 1. Одержання [(2фтор феніл)гідразон]малонової кислоти Моногідрат мезоксалату натрію (2,21г, 12,3ммоль) розчинили в 1молі соляної кислоти (50мл), одержавши безколірний каламутний розчин. До цієї суміші в умовах перемішування при кімнатній температурі порціями добавили 2фтор фенілгідразингідрохлорид (2,00г, 12,3ммоль). У результаті утворився жовтий осад. Суміш розбавили водою (50мл) і продовжували перемішування протягом ночі. Після цього добавили етилацетат (150мл), і суміш інтенсивно перемішували до розчинення осаду. Фази розділили, і водний шар промили етилацетатом (50мл). Об'єднані органічні екстракти просушили сульфатом магнію, профільтрували, і розчинник видалили у вакуумі. Зазначена в назві сполука була одержана у вигляді жовтого порошку (2,55г, 11,7ммоль, 92%). LCMS: m/z 227 [М+Н]+. Стадія 2. Одержання [(2фтор феніл)гідразон]малоноїлдихлориду 20 (2-Фторфенілгідразон)малонову кислоту (1,33г, 5,88ммоль) змішали в атмосфері інертного газу з сухим хлороформом (20мл). У результаті утворилася жовта суспензія, яку перемішали при кімнатній температурі, і до неї порціями добавили п'ятихлористий фосфор (2,69г, 12,9ммоль). Реакційну суміш кип'ятили протягом 2год., одержавши темно-жовтий розчин. Суміш охолодили до кімнатної температури і випарювали у вакуумі, аж поки не випав осад. Осад відфільтрували, промили гексаном (30мл) і просушили у вакуумі. Зазначена в назві сполука була одержана у вигляді порошку жовтого кольору (760мг, 2,89ммоль, 49%). Стадія 3. Одержання метилового естеру 8фтор-4-гідроксицинолін-3-карбонової кислоти Дихлорангідрид (2фтор фенілгідразон)малонової кислоти (19,4г, 74ммоль) в інертній атмосфері змішали з 1,2дихлоретаном (100мл), одержавши жовту суспензію. До суспензії по краплях добавили чотирихлористий титан (13,9г, 8,08мл, 74ммоль), У результаті утворився коричневий розчин. Суміш кип'ятили протягом ночі, добавили додаткову кількість чотирихлористого титану (13,9г, 8,08мл, 74ммоль) і продовжували гріти ще протягом 24год. Після цього реакційну суміш охолодили до 0-5°С, і до неї по краплях добавили метанол (50мл). Далі перемішування продовжували при кімнатній температурі ще протягом 1год., і леткі продукти видалили у вакуумі. Добавили воду (300мл), і отриману суспензію екстрагували етилацетатом (3´100мл). Об'єднані органічні екстракти просушили сульфатом магнію, профільтрували і випарили у вакуумі. У результаті одержали тверду речовину жовтого кольору (12г, сирий продукт). LCMS: m/z 223 [М+Н]\ Стадія 4. Одержання 4-(6-фтор-3-оксо-1,3дигідро-2Н-піразол[4,3-с]цинолін-2-іл)бензойної кислоти Сирий естер 8-фтор-4-гідроксицинолін-3карбонової кислоти із попередньої стадії (1,00г, 4,95ммоль) розчинили в хлористому тіонілі (50мл). Розчин кип'ятили протягом 2-3 годин до припинення виділення газу. Реакційну суміш охолодили до кімнатної температури, і надлишковий хлористий тіоніл видалили у вакуумі. Сирий проміжний продукт просушили азеотропною перегонкою з толуолом (3´25мл). До утвореної в результаті темно-коричневої твердої речовини добавили етанол (25мл). Після цього добавили 4гідразинбензойну кислоту (640мг, 4,21ммоль), і 21 81024 суміш перемішали при кімнатній температурі протягом ночі. Осад відфільтрували, суспендували в 1молі НСІ (100мл), профільтрували, промили гексаном (50мл) і просушили у вакуумі. Виділений продукт мав форму твердої речовини коричневого кольору (890 мг сирого продукту). LCMS: m/z 325 [М+Н]+. Приклад 6 Стадія 1. Одержання хлорангідриду 4-(6-фтор3-оксо-1,3-дигідро-2Н-піразол[4,3-с]цинолін-2іл)бензойної кислоти Сиру 4-(6-фтор-3-оксо-1,3-дигідро-2Нпіразол[4,3-с]цинолін-2-іл)бензойну кислоту (1,45г) із попередньої стадії розчинили в хлористому тіонілі (50мл). Розчин гріли при 70°С протягом 2-3 годин до припинення виділення газу. Реакційну суміш охолодили до кімнатної температури, і надлишковий хлористий тіоніл видалили у вакуумі. Залишок просушили азеотропною перегонкою з толуолом (2´20мл), одержавши тверду речовину. Осад відфільтрували, промили толуолом і просушили у вакуумі. Виділений продукт мав форму порошку жовтого кольору (670мг, 1,95ммоль). LCMS: m/z 339 [М+Н]+ (метиловий естер, утворений зі складу зразка в метанолі). Стадія 2. Одержання 4-(6-фтор-3-оксо-1,3дигідро-2Н-піразол[4,3-с]цинолін-2-іл)-N(піролідин-1-ілбутил)бензаміду 4-(6-Фтор-3-оксо-1,3-дигідро-2Н-піразол[4,3с]цинолін-2-іл)бензоїлхлорид (100мг, 0,29ммоль) розчинили в безводному DMA (2мл). Добавили діізопропілетиламін (75мг, 101мкл, 0,58ммоль), а потім 1-(4-амінобутил)піролідин (41мг). Суміш перемішали при кімнатній температурі протягом ночі. Добавили воду (5мл) і н-бутанол (5мл). Фази розділили. Органічну фазу промили водою (2x5мл). Леткі продукти видалили у вакуумі. Виділений продукт мав форму порошку коричневого кольору (50мг, 0,11ммоль, 37%). LCMS: m/z 463 [М+Н]+. Приклад 7 Одержання 4-(6-фтор-3-оксо-1,3-дигідро-2Нпіразол[4,3-с]цинолін-2-іл)-N-(1,2,2,6,6пентаметилпіперидин-4-іл)бензаміду 22 4-(6-Фтор-3-оксо-1,3-дигідро-2Н-піразол[4,3с]цинолін-2-іл)бензоїлхлорид (100мг, 0,29ммоль) розчинили в сухому DMA (2мл). Додали діізопропілетиламін (75мг, 101мкл, 0,58ммоль), а потім 4-аміно-1,2,2,6,6-пентаметилпіперидин (49мг, 0,29ммоль). Суміш перемішали при кімнатній температурі протягом ночі. Добавили воду (5мл) і н-бутанол (5мл). Фази розділили. Органічну фаз у промили водою (2´5мл), і розчин випарили у вакуумі. Зазначена в назві сполука була одержана у вигляді твердої речовини темночервоного кольору (50мг, 0,105ммоль, 36%). LCMS: m/z [M+H]+ 477. Приклад 8 Стадія 1. Одержання 2-(4-нітрофеніл)-1,2дигідро-ЗН-піразол[4,3-с]цинолін-3-ону До метилового естеру 4-гідроксицинолін-3карбонової кислоти (10,0г, 49ммоль) в атмосфері інертного газу по краплях добавили хлористий тіоніл (326г, 200мл). Суміш кип'ятили протягом 2,5год., о холодили до кімнатної температури, і надлишок хлористого тіонілу видалили у вакуумі. До залишку добавили толуол (100мл) і видалили у вакуумі. Цю процедуру повторили, додавши ще 100мл толуолу і видаливши в вакуумі. У результаті одержали коричневий напіврідкий залишок, котрий розчинили в етанолі (200мл). 4-нітрофенілгідразин (5.99г, 39.2ммоль) додали порціями. Суміш перемішали при кімнатній температурі протягом ночі, потім гріли при 40-45°С протягом 1 години і охолодили до кімнатної температури. Осад відфільтрували, розтерли з етанолом (100мл) і просушили у вакуумі. Зазначена в назві сполука була одержана у вигляді твердої речовини коричневого кольору (8,42г, 27,4ммоль, 70%). LCMS: m/z 308 [М+Н]+. Стадія 2. Одержання 2-(4-амінофеніл)-1,2дигідро-3R-ліразол[4,3-с]цинолін-3-ону 2-(4-Нітрофеніл)-1,2-дигідро-3Н-ліразол[4,3с]цинолін-3-он (11,4г, 37,2ммоль) суспендували в суміші етанолу (100мл) і води (100мл). Добавили 23 81024 порошок заліза (11,1г, 200ммоль) і хлористий амоній (5,34г, 100ммоль). Суміш гріли при 80°С протягом ночі, охолодили до кімнатної температури ι підлужили до рН9-10 додаванням карбонату калію. Осад видалили фільтруванням через шар целіту (Celite®). Фільтрат екстрагували н-бутанолом (2´200мл). Об'єднані органічні екстракти випарили у вакуумі, одержавши твердий залишок червоного кольору. Залишок розтерли с метанолом (100мл), відфільтрували і просушили у вакуумі. Зазначену в назві сполуку одержали у вигляді темно-червоного порошку (5,58г, 20,1ммоль, 57%). LCMS: m/z 278 [М+Н]+. Стадія 3. Одержання N-[3(диметиламіно)пропіл]-N'-[4-(3-оксо)-1,3-дигідро2Н-піразол[4,3-с]цинолін-2-іл)феніл]сечовини 2-(4-амінофеніл)-1,2-дигідро-3H-піразол[4,3с]цинолін-3-он (44мг, 6ммоль) суспендували в толуолі (0,5мл) в атмосфері азоту при температурі 0-5°С. Добавили DMA (0,5мл), після додавання Ν,Ν'-карбонілдіімідазолу (26мг, 0,16ммоль). Суміш перемішали протягом 1 години при 0-5°С, а потім змішали з розчином 3-диметиламінопропіламіну (18мг, 0,18ммоль) в толуолі (0,5мл). Перемішування продовжували протягом 1 години, і утворений продукт очистили за допомогою препаративної HPLC. Зазначена в назві сполука була одержана у вигляді порошку темно-червоного кольору (2,6мг, 6мкмоль, 4%). LCMS: m/z 406 [М+Н]+. Приклад 9 Одержання етилового естеру 4-(3-оксо-1,3дигідро-2H-піразол[4,3-с]цинолін-2-іл)бензойної кислоти Зазначена в назві сполука була одержана у відповідності з процесом, описаним у Прикладі 1, Стадія 5, де замість 4-гідразинбензойної кислоти використовували її етиловий естер. MS: MH+=335,2. Результати Аналіз ВІАсоrе біомолекулярних взаємодій Біотинільована людськамолекула CD80 (hCDSO-BT) являє собою рекомбінантну розчинну форму мембраннозв'язаної рецепторноймолекули (CD80), яка, зв'язуючись з CD28, ініціює активацію Т-клітин. Взаємодія між CD80 і CD28 була широко досліджена [Collins et al., 2002]. Біотинильована 24 людськамолекула HLA-A2-ta x являє собою рекомбінантну розчинну форму мембраннозв'язаної рецепторноїмолекули, яку використовували в даному аналізі в ролі контрольного білка, що за припущенням не реагує з даними сполуками. Система BIAcore S51™ використовувалася для скринінгу сполук із описаних вище Прикладів 1-4. У BIAcore S51™ був поміщений сенсорний чіп СМ5 серії S. Шляхом звичайного амінного зв'язування до карбоксиметильної поверхні був приєднаний стрептавідин. Поверхню чіпа активували за допомогою 0,2Μ EDC/0,05M NHS з наступним зв'язуванням стрептавідину (0,25мг/мл в 10ммоль ацетату натрію з рН5,0) і насиченням незайнятих сайтів 1молем етилендіаміну. Сенсорний чіп BIAcore S51 має дві окремі сенсорні ділянки для імобілізації білків.молекулу hCDSO-BT імобілізували на покритій стрептавідином поверхні однієї із цих сенсорних ділянок доти, аж поки не починала спостерігатися відповідь порядку 3000 RU (щуриних одиниць). На іншій сенсорній ділянці закріплювали білок для контролю неспецифічного зв'язування даної сполуки. Для цього використовувалася біотинільована розчинна форма білка HLA людини. У проточному буфері (10нмоль, рН7,4, 150ммоль NaCI, 0,005 Р20; 5% DMSO) го тували серії розбавлених (1000нмоль-0,05нмоль) сполук. Система BIAcore S51™ працювала в режимі витрати 30мкл/хв. при використанні проточного буферу. У систему вводили розчини сполук і DMSO-еталону для корекції даних на вплив розчинника. Дані експерименту автоматично записувалися й аналізувалися за допомогою програми BIAcore S51 Evaluation. Взаємодія між CD80 і ендогенним білковим лігандом (CD28) є високоспецифічною, але порівняно слабкою і характеризується величинами KD 4750нМ і швидкості виключення більше 0,2с-1. Сполуки Прикладів 2, 3, 4, 6 і 7 виказували більш високу афінність до CD80 і більш тривалий час перебування на ній, ніж CD28, демонструючи величини KD менше 100нМ, а швидкості виключення 2´10-2 і засвідчуючи цим, що циноліни є здатними ефективно конкурува ти з ендогенним лігандом. Циноліни не показали достатнього для виявлення рівня їх взаємодії з контрольним білком. Першоджерела [Collins A.V. et al., (2002) Immunity 17, 201-210 "The interaction properties of costimulatory molecules revisited"]. Інгібування продукування інтерлейкіну-2 (IL-2) людськими Т-клітинами Jurkat Методика експерименту Людські клітини Raji розподіляли з концентрацією 2´105 клітин на лунку в середовищі RPMI-1640, доповненому 10% фетальної телячої сироватки, 1% пеніциліну зі стрептоміцином, 1% глутаміну (середовище RPMI) на 96-луночному круглодонному мікротитрувальному планшеті. Досліджувані сполуки (розчинені у 100% DMSO) розбавляли до восьмикратної від бажаної кінцевої 25 81024 концентрації в середовищі RPMI і додавали до потрібної кінцевої концентрації при загальному об'ємі 200мкл на лунку. Після інкубування протягом 20хв. при 37°С додавали Т-клітини Jurkat у концентрації 2´105 клітин на лунку. До культур додавали моноклональне антитіло до CD3 (UCHT1, R&D Systems) з кінцевою концентрацією 1мкг/мл, а в ти х випадках, де в тексті зазначено, додавали також моноклональне антитіло до CD28 (CD28.2, BD-Pharmingen) в концентрації 2,5мкл/мл. Клітини культивували при 37°С протягом 5год., після чого планшети центрифугували, і супернатанти збирали для твердофазного імуноферментного аналізу IL-2 ELISA з парним комплектом IL-2 Eli (DIACLONE Research, Besancon, France) у відповідності з інструкціями виробника. Як приклад, проведений аналіз показав інгібування сполукою із Прикладу 2 (AV1142005) на рівні 65% при 30мкМ. Аналіз методом гомогенної флуоресценції з розрізненням у часі Продукти, отримані в описаних вище прикладах, були піддані випробуванням методом гомогенної флуоресценції з розрізненням у часі (HTRF: Homogeneous Time Resolved Fluorescence Assay) у безклітинному середовищі з метою визначення їхньої активності як інгібіторів взаємодії CD80-CD28. У цих випробуваннях європій і алофікоціанін (АРС: allophycocyanin) непрямим чином (через сполучні антитіла) зв'язуються з CD28 і СВ80, утворюючи комплекс, який приводить європій і АРС у тісн у близькість один з одним, внаслідок чого генерується сигнал. Комплекс містить шість таких білків: флуоресцентну мітку 1, сполучне антитіло 1, злитий білок CD28, злитий білок CD80, сполучне антитіло 2 і флуоресцентну мітку 2. У наведеній нижче таблиці ці реагенти охарактеризовані більш детально. Флуоресцентна мітка 1 Сполучне антитіло 1 Злитий білок CD28 Злитий білок CD80 Сполучне антитіло 2 IgG прот и кроля, мічений єв ропієм (1мкг/мл) Кролячий IgG, специфічний до мишачого Fc-фрагменту (3мкг/мл) Злитий білок CD28 - мишачий фрагмент Fc (0,48мкг/мл) Злитий білок CD80 - мишачий фрагмент Fab (C215) (1,9мкг/мл) GaMK-біотин: біотинільов аний IgG кози, специфічний до капа-ланцюга мишачого імуноглобуліну (2мкг/мл) Флуоресцентна SA-APC: алофікоціанін, мічений мітка 2 стрептав ідином (8мкг/мл) При утворенні даного комплексу європій і АРС зближуються і генерується сигнал. Неспецифічну взаємодію виміряли шляхом заміщення мишачого Fab-фрагменту (С215) на злитий білок CD80 - мишачий Fab-фрагмент (1,9мкг/мл). Випробування проводили на чорних 384-лункових планшетах у кінцевому об'ємі 30мкл. Використовували такий буфер: 50мМ Tris-HCI, 150мМ NaCI pH7,8, до якого безпосередньо перед випробуваннями добавляли 0,1%(мас./об.) альбуміну бичачої сироватки. 26 Сполуки добавляли до зазначених реагентів низкою концентрацій від 100мкМ до 1,7нМ. Реакційну суміш інкубували протягом 4год. при кімнатній температурі. За допомогою багаторівневого лічильника Wallac Victor 1420 Multilabel Counter проводили два вимірювання. Перше вимірювання: збудження 340нм, випромінювання 665нм, затримка 50мкс, тривалість вікна 200мкс. Друге вимірювання: збудження 340нм, випромінювання 615нм, затримка 50мкс, тривалість вікна 200мкс. Підрахунок проводили з поправками на флуоресцентний перехід, гасіння і флуоресцентний фон. У записі активності ЕС50 випробуваних сполук використовували такі позначення: ЕС50: *=>10мкМ, **=1-10мкМ, ***=
ДивитисяДодаткова інформація
Назва патенту англійськоюImmunomodulating heterocyclic compounds
Автори англійськоюMathews Ian Richard
Назва патенту російськоюИммуномодулирующие гетероциклические соединения
Автори російськоюМетьюз Иан Ричард
МПК / Мітки
МПК: A61P 19/02, C07D 487/04, C07D 519/00, A61P 17/06, A61P 37/00, A61P 3/10
Мітки: гетероциклічні, сполуки, імуномодулюючі
Код посилання
<a href="https://ua.patents.su/21-81024-imunomodulyuyuchi-geterociklichni-spoluki.html" target="_blank" rel="follow" title="База патентів України">Імуномодулюючі гетероциклічні сполуки</a>
Наступний патент: Водогрійний котел
Випадковий патент: Спосіб зняття перегріву пари