Спосіб індукції диференціювання клітин
Номер патенту: 85039
Опубліковано: 25.12.2008
Автори: Райхлін Натан Танфєлєвіч, Гарін Август Міхайловіч, Желтухіна Галіна Алєксандровна, Трєщалін Іван Дмітрієвіч, Бичков Марк Борісовіч, Горбунова Вєра Андрєєвна, Трєщаліна Єлєна Міхайловна, Нєбольсін Владімір Євгєньєвіч
Формула / Реферат
1. Спосіб індукції диференціювання нормальних і пухлинних клітин і пухлинних клітин меланоми у ссавців, у тому числі людини, при якому вводять похідне пептиду загальної формули:
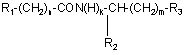 , (I)
, (I)
де R1 являє собою С1-С3 вуглеводневий радикал, заміщений функціональною групою, вибраною з аміно-, С1-C5 амідо- або карбоксильної груп, причому карбоксильна група може бути етерифікована; або
R1 являє собою С1-С3 вуглеводневий радикал, одночасно заміщений (а) аміногрупою, яка необов’язково заміщена ацильним замісником, і (b) карбоксильною групою, де карбоксильна група може бути приєднана до атома азоту у фрагменті -CON(H)k- загальної формули з отриманням C5-С6 членного циклічного іміду; або
R1 являє собою С1-С3 вуглеводневий радикал, заміщений 5-6-членною ненасиченою гетероциклічною групою, причому вуглеводневий радикал може містити одночасно аміногрупу, вільну або заміщену ацильним замісником; або
R1 може являє собою насичену гетероциклічну групу;
R2 являє собою атом водню або функціональну групу, вибрану з карбоксилу, який може бути етерифікований;
R3 являє собою 5-6-членну насичену або ненасичену циклічну або гетероциклічну групу, або аміно-, або карбоксильну групу, причому карбоксильна група може бути етерифікована;
n=0-4,
m=1-4,
k=0-1;
або його фармацевтично прийнятні солі в ефективній кількості.
2. Спосіб за п. 1, в якому похідне пептиду загальної формули (І), визначене в п. 1, вводять щодня перорально у дозі 0,5-5,0 мг/кг.
3. Спосіб за будь-яким з пп. 1 або 2, в якому похідне пептиду загальної формули (І), визначене в п. 1, вводять у поєднанні з курсом хіміотерапії.
4. Спосіб за будь-яким з пп. 1-3, в якому для стабілізації росту злоякісних пухлин похідне пептиду загальної формули (І), визначене в п. 1, вводять не менше 15 днів.
5. Спосіб за будь-яким з пп. 1-4, в якому для підвищення ефективності імунотерапії злоякісних пухлин похідне пептиду загальної формули (І), визначене в п. 1, вводять разом з інтерфероном.
6. Спосіб за будь-яким з пп. 4 або 5, в якому злоякісна пухлина є меланомою або гемобластозом.
7. Спосіб за будь-яким з пп. 1-3, в якому для зниження гематологічної токсичності похідне пептиду загальної формули (І), визначене в п. 1, вводять за 5 днів до початку курсу хіміотерапії і до його закінчення.
8. Спосіб за будь-яким з пп. 1-7, де R1=NH2-CH2-, НООС-СН2-, СН3СОNН-СН2-, СН3ОСО-СН2-,
![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
,
![]() ;
;
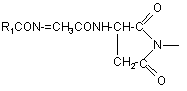 ,
, 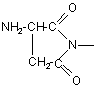 ;
;
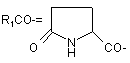 ,
, 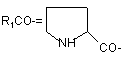 ,
,
n=0-4; k=0-1
R2=H, COOH, COOCH3;
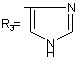 ,
, 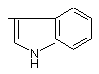 ,
, 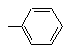 ,
, 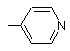 ,
, 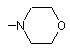 , NH2, COOH, COOCH3, m=1-4.
, NH2, COOH, COOCH3, m=1-4.
9. Спосіб за будь-яким з пп. 1-8, де похідне пептиду являє собою сполуку формули
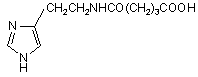 .
.
10. Застосування похідного пептиду загальної формули:
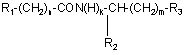 , (I)
, (I)
де R1 являє собою С1-С3 вуглеводневий радикал, заміщений функціональною групою, вибраною з аміно-, С1-C5 амідо- або карбоксильної груп, причому карбоксильна група може бути етерифікована; або
R1 являє собою С1-С3 вуглеводневий радикал, одночасно заміщений (а) аміногрупою, яка необов’язково заміщена ацильним замісником, і (b) карбоксильною групою, де карбоксильна група може бути приєднана до атома азоту у фрагменті -CON(H)k- загальної формули з отриманням C5-С6 членного циклічного іміду; або
R1 являє собою С1-С3 вуглеводневий радикал, заміщений 5-6-членною ненасиченою гетероциклічною групою, причому вуглеводневий радикал може містити одночасно аміногрупу, вільну або заміщену ацильним замісником; або
R1 може являє собою насичену гетероциклічну групу;
R2 являє собою атом водню або функціональну групу, вибрану з карбоксилу, який може бути етерифікований;
R3 являє собою 5-6-членну насичену або ненасичену циклічну або гетероциклічну групу, або аміно-, або карбоксильну групу, причому карбоксильна група може бути етерифікована;
n=0-4,
m=1-4,
k=0-1;
або його фармацевтично прийнятних солей для виробництва лікарського засобу для індукції диференціювання нормальних і пухлинних клітин у ссавців.
11. Застосування похідного пептиду загальної формули (І), визначеного у п. 10, у поєднанні з курсом хіміотерапії для захисту від гематотоксичності.
12. Застосування похідного пептиду загальної формули (І), визначеного у п. 10, для стабілізації росту злоякісних пухлин.
13. Застосування похідного пептиду загальної формули (І), визначеного у п. 10, у поєднанні з інтерфероном для підвищення ефективності імунотерапії.
14. Застосування за будь-яким з пп. 10-13, де R1=NH2-CH2, НООС-СН2-, СН2СОNН-СН2-, СН3ОСО-СН2-,
![]() ,
, ![]() ,
, ![]() ,
, ![]() ,
,
![]() ;
;
 ,
,  ;
;
 ,
,  ,
,
n=0-4; k=0-1
R2=H, COOH, COOCH3;
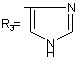 ,
,  ,
,  ,
,  ,
,  , NH2, COOH, COOCH3, m=1-4.
, NH2, COOH, COOCH3, m=1-4.
15. Застосування за будь-яким з пп. 10-14, де пептид загальної формули (І) являє собою сполуку формули
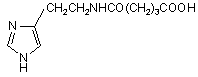 .
.
Текст
1. Спосіб індукції диференціювання нормальних і пухлинних клітин і пухлинних клітин меланоми у ссавців, у тому числі людини, при якому вводять похідне пептиду загальної формули: 2 (19) 1 3 85039 O O R1 CON-=CH3 CONH-CH-C NH 2-CH-C N N CH 2-C CH2 -C O R1CO-= O , ; R1CO-= N H O CO NH , n=0-4; k=0-1 R2=H, COOH, COOCH 3; C O , N R3 = N H N , N N H , , , O , NH2, COOH, COOCH 3, m=1-4. 9. Спосіб за будь-яким з пп.1-8, де похідне пептиду являє собою сполуку формули CH2CH2NHCO(CH2) 3COOH N 4 m=1-4, k=0-1; або його фармацевтично прийнятних солей для виробництва лікарського засобу для індукції диференціювання нормальних і пухлинних клітин у ссавців. 11. Застосування похідного пептиду загальної формули (І), визначеного у п.10, у поєднанні з курсом хіміотерапії для захисту від гематотоксичності. 12. Застосування похідного пептиду загальної формули (І), визначеного у п.10, для стабілізації росту злоякісних пухлин. 13. Застосування похідного пептиду загальної формули (І), визначеного у п.10, у поєднанні з інтерфероном для підвищення ефективності імунотерапії. 14. Застосування за будь-яким з пп.10-13, де R1=NH2-CH2, НООС-СН2-, СН2СОNН-СН2-, СН3ОСО-СН2-, NH 2-CHNH -CH2 , CH3 -CONH-CH N H . 10. Застосування похідного пептиду загальної формули: R1 -(CH2 )n -CON(H)k-CH-(CH 2)m-R3 R2 , (I) де R1 являє собою С1-С3 вуглеводневий радикал, заміщений функціональною групою, вибраною з аміно-, С1-C5 амідо- або карбоксильної груп, причому карбоксильна група може бути етерифікована; або R1 являє собою С1-С3 вуглеводневий радикал, одночасно заміщений (а) аміногрупою, яка необов’язково заміщена ацильним замісником, і (b) карбоксильною групою, де карбоксильна група може бути приєднана до атома азоту у фрагменті CON(H)k- загальної формули з отриманням C5-С6 членного циклічного іміду; або R1 являє собою С1-С3 вуглеводневий радикал, заміщений 5-6-членною ненасиченою гетероциклічною групою, причому вуглеводневий радикал може містити одночасно аміногрупу, вільну або заміщену ацильним замісником; або R1 може являє собою насичену гетероциклічну груп у; R2 являє собою атом водню або функціональну груп у, вибрану з карбоксилу, який може бути етерифікований; R3 являє собою 5-6-членну насичену або ненасичену циклічну або гетероциклічну групу, або аміно, або карбоксильну груп у, причому карбоксильна група може бути етерифікована; n=0-4, Винахід відноситься до медицини і, зокрема до лікування онкологічних захворювань, і може CH2-CH2 -COOH COOH , CH3 CO-NH-CH CH2 -COOH COOH , , NH2 -CHCH2 -4Im ; O O R1CON-=CH3 CONH-CH-C NH 2-CH-C N N CH2 -C CH 2-C O R1 CO- = ; R1CO-= N H O O , CO , NH C O , n=0-4; k=0-1 R2=H, COOH, COOCH 3; N R3= N H N , N H N , , , O , NH2, COOH, COOCH 3, m=1-4. 15. Застосування за будь-яким з пп.10-14, де пептид загальної формули (І) являє собою сполуку формули CH2CH2NHCO(CH2) 3COOH N N H . бути використаний при лікуванні пухлин різного генезу. 5 85039 Винахід відноситься до способу індукції диференціювання клітин із застосуванням похідних пептидів як агента, що індукує диференціювання клітин, і, зокрема до їх використання у протипухлинній нецитотоксичній терапії. Відомо, що відсутність здатності до диференціювання у більшої частини пухлинних клітин приводить до нестримного росту п ухлини. Тому одним з нових підходів до протипухлинної нецитотоксичної терапії є пошук засобів як специфічної, так і неспецифічної індукції диференціювання клітин. Під індукцією диференціювання клітин розуміють здатність різних речовин відновлювати (або запускати) втрачені або знижені внаслідок різних причин функції: проходження клітиною нормального клітинного циклу, синтез біологічно активних життєво важливих речовин у ній і т.п. Речовини або сполуки, механізм дії яких не пов'язаний з однією конкретною функцією клітини і які можуть викликати її диференціювання за декількома параметрами, можна віднести до неспецифічних індукторів диференціювання. Відомі способи індукції диференціювання пухлинних клітин шляхом введення ретиноїдів або α2-інтерферону [Cancer Res., 40, 3345-3350, 1980]. Як засіб продовження ремісії після індукційної або постремісійної терапії гострого промієлоцитарного лейкозу використовується індуктор диференціювання клітин - політрансретиноєва кислота (ПТРК). Диференціювання клітин під впливом похідних ретиноєвої кислоти веде до стабілізації росту пухлинних клітин [Абелєв Г.І. // Диференціювання і пухлинний фенотип у клітинах лейкозів і лімфом.-В кн.: Клінічна онкогематологія (під ред. М.А.Волкової).-Москва.-Медицина. -2001 -гл.11. стор.116-123]. Використання препаратів α-інтерферону при лікуванні меланоми як засобу імунотерапії також пов'язане з індукцією диференціювання пухлинних клітин, в яких підвищується здатність до адгезії та змінюється антигенний профіль. Проведення інтерферонотерапії викликає зниження прогресії пухлинного росту, а також запобігає розвитку і швидкості метастазування [Atzpodien J., Kirchner H. // Cancer, cytokines, and cytotoxic cells: interleukin-2 in the immunotherapy of human neoplasms. - KHn. Wochenschr. -1990. -v.68.-p.1-7]. В останні роки увійшли в клінічну практику препарати, що викликають диференціювання кровотворних клітин, пошкоджених у результаті цитотоксичної хіміотерапії. Дані препарати являють собою різні цитокіни, одержані з кісткового мозку, такі як гематогормони: гранулоцитарний колонієстимулюючий фактор, гранулоцитарномакрофагальний колонієстимулюючий фактор та ін. їх застосування при лікуванні різних пухлин людини приводить до прискорення дозрівання клітин кісткового мозку і запобігає гематологічному цитотоксичному ефекту хіміопрепаратів [Crawford J., Ozer H., Stoller R. et al. // Phase II of clinical investigation of GM-CSF by the patients of SCLC with the dose-intensive chemotherapy.-The New England Journal of Medicine.-1991-v. 325. -№3. -p.164-170]. 6 Таким чином, індукція диференціювання пухлинних клітин є одним з провідних механізмів стабілізації росту новоутворень, підвищення ефекту імунотерапії та корекції гематологічної токсичності хіміопрепаратів. Авторами даного винаходу було виявлено, що похідні пептидів загальної формули (І): (I) є потужними індукторами диференціювання клітин і можуть бути використані як агенти для нецитотоксичної терапії онкологічних захворювань, зокрема меланоми і гемобластозів, а також як гематокоригувальні агенти. Дані сполуки описані [у міжнародній заявці PCT/RU98/00215], (I) як такі, що володіють антиоксидантною, антиастматичною, антигіпоксичною, протизапальною, противірусною, антибактеріальною, ліпідрегулюючою, антиметастатичною, а також іншими видами терапевтичної дії. Сполуки циклічної структури аспартил-гістаміну і ацетил-аспартил-гістаміну описані у роботі [Kvamme, E.; Reichelt, K.L.; Edminson, P.D.; et al. N-substituted peptides in brain. // Fed. Eurr Biochem. Society Meet., [Proc]. 1975, 41, 127-136]. Даний винахід відноситься до способу індукції диференціювання клітин, що включає введення як активного агента ефективної кількості сполуки загальної формули: (I) або її фармацевтично прийнятних солей, де R1 являє собою C1-C3вуглеводневий радикал, заміщений функціональною групою, вибраною з аміно, С1-С5амідо- або карбоксильної груп, причому карбоксильна група може бути етерифікована, а аміногрупа може бути заміщена ацильним замісником; або C1-C3 вуглеводневий радикал, одночасно заміщений аміногрупою, причому аміногрупа може бути заміщена ацильним замісником і карбоксильною групою, причому карбоксильна група може входити до складу C5-C6 членного циклічного іміду з участю N-кінцевої аміногрупи або -NH-, що входить до складу -CONH- групи; або С1-С3 вуглеводневий радикал, заміщений 5-6-членною ненасиченою гетероциклічною групою, причому вуглеводневий радикал може містити одночасно аміногрупу, вільну або заміщену ацильним замісником; або R1 може являти собою насичену гетероциклічну груп у; R2 являє собою атом водню або функціональну групу, вибрану з карбоксилу, який може бути етерифікований; R3 являє собою 5-6членну насичену або ненасичену циклічну або гетероциклічну групу, або аміно-, або карбоксильну груп у, причому карбоксильна група може бути етерифікована; n=0-4, m=1-4, k=0-1. У переважному варіанті даний винахід відноситься до способу індукції диференціювання клі 7 тин, що включає введення як активного агента ефективної кількості 4-[N-(2-(імідазол-4іл)етил)карбамоїл] масляної кислоти (Дикарбамін®). 85039 8 Переважними сполуками загальної формули (І), такими, що використовуються у даному винаході, є сполуки загальної формули (І), наведені у наступній таблиці: 9 Більш переважними сполуками загальної формули (І), що використовуються у даному винахо 85039 10 ді, є сполуки загальної формули (І), в яких R 1=NH2CH2-, HOOC-CH 2, CH3CONH-CH2-, CH 3OCO-CH2-, 11 85039 Найбільш переважною сполукою, що використовується у даному винаході, є сполука формули: У переважному варіанті винаходу похідні пептидів загальної формули (І) вводять тривало у разовій дозі 0,5-5,0мг/кг ваги тіла. В іншому переважному варіанті винаходу похідні пептидів загальної формули (І) вводять у поєднанні з хіміотерапією. Переважним варіантом винаходу також є спосіб індукції диференціювання клітин, в якому для стабілізації росту злоякісних пухлин, зокрема меланоми або гемобластозу, похідні пептидів загальної формули (І) вводять у дозі 0,5-5,0мг/кг ваги тіла протягом не менш ніж 15 днів при вичерпаних можливостях хіміотерапії. Введення похідних пептидів загальної формули (І) разом із засобом імунотерапії - інтерфероном приводить до підвищення його ефективності відносно клітин злоякісних пухлин, зокрема меланоми. Ще одним переважним варіантом здійснення даного винаходу є спосіб індукції диференціювання клітин, в якому для підвищення ефективності імунотерапії меланоми, похідні пептидів загальної формули (І) вводять у дозі 0,5-5,0мг/кг ваги тіла протягом не менш ніж 15 днів разом з введенням інтерферону. Переважним варіантом даного винаходу також є спосіб індукції диференціювання клітин, в якому для зниження гематологічної токсичності похідні пептидів загальної формули (І) вводять у разовій дозі щодня 0,5-5,0мг/кг ваги тіла за 5 днів до початку курсу хіміотерапії, під час проведення хіміотерапії та у період між курсами аж до наступного курсу цито токсичної терапії. Далі наведені приклади, що ілюструють переважні варіанти втілення винаходу. Приклад 1. Активність похідних пептидів загальної формули (І) відносно диференціювання клітин меланоми М-6 12 Дослідження проводили на безтимусних (nude) мишах-самках лінії Balb/C 10-12 тижневого віку, вагою 20-22 грами (розведення РОНЦ ім. Н.Н. Блохіна PAMH). Для трансплантації безтимусним мишам "nude" з банку пухлинних штамів ГУ РОНЦ ім. Н.Н. Блохіна PAMH був взятий штам меланоми людини, раніше одержаний з первинного клінічного матеріалу. Пухлину дезінтегрували розчином Версена з прижиттєвим забарвлюванням трипановим синім і перевивали мишам під шкіру по 1,6млн клітин на мишу. Дикарбамін вводили мишам щодня у дозі 1,0мг/кг у шлунок за допомогою металевого зонда, починаючи за 4 дні до перевивання пухлини, і потім протягом 10-11 днів (курс введення - до 15 днів). Через 12, 24 і 48 годин після останнього введення препарату мишей вбивали ефірним наркозом. У досліді використовували 4 групи мишей: - 1 група - контрольна, без впливу Дикарбаміну. Мишей вбивали у строки, паралельно групам, що одержували Дикарбамін. - 2 група - вводили Дикарбамін і вбивали мишей через 12 годин після закінчення його введення. - З група - вводили Дикарбамін і вбивали мишей через 24 години після закінчення його введення. - 4 група - вводили Дикарбамін і вбивали мишей через 48 годин після закінчення його введення. Для контролю за ступенем диференціювання і проліферації меланоми М-6 у гр упах контрольних тварин і у групах з Дикарбаміном визначали 4 морфологічних показники, такі як число клітин з пігментом і число клітин з ознаками апоптозу (здатність до диференціювання), число мітозів (проліферативна активність) і площа некрозу. Дані показники визначали у динаміці та співвідносили із загальною морфологічною картиною пухлинного росту, як інтегральною ознакою. З цією метою у мишей забирали пухлину, поміщали у формалін і проводили гістологічну обробку для світлової мікроскопії. Одержані дані наведені у Таблиці 1. Таблиця 1 Морфологічні показники меланоми М-6 (світлова мікроскопія) Показники (у %) Контроль Після введення Дикарбаміну Контроль Мітози Після введення Дикарбаміну Контроль Апоптоз Після введення Дикарбаміну Клітини з пігментом Контроль Після введення Дикарбаміну Площа некрозу Час, що минув з моменту скасування Дикарбаміну 12 годин 24 години 48 годин 1-2 2-3 3-5 6-7 7-9 8-10 3-5 3-5 3-5 3-5 3-5 3-5 0,1-0,2 0,1-0,2 0,1-0,2 0,1-0,2 0,2-0,3 0,2-0,3 1-2 1-2 2-3 2-3 2-4 3-5 13 85039 Проведене дослідження дозволило встановити, що меланома людини, яка перевивається безтимусним мишам, на 9 добу утворює пухлин у, що складається з поліморфних клітин, які ростуть суцільними полями з незначним розвитком строми. У пухлині зустрічаються невеликі ділянки некрозу, які дещо збільшуються до 48 годин (до 3-5% площі зрізу) у порівнянні зі строками забою 12, 24 години (відповідно, 1-2% і 2-3%). У всі періоди росту у пухлині спостерігається (3-5%) мітозів. Апоптоз виражений слабо. Клітини, що містять пігмент, зустрічаються рідко, їх число протягом першої доби не перевищує 1-2% і тільки через 48 годин росту збільшується до 2-3%. Таким чином, інтенсивність меланіногенезу у цей період незначна. Одержана характеристика дозволяє зробити висновок про те, що меланома є швидко зростаючою пухлиною, яка практично втратила здатність до диференціювання як за ступенем апоптозу, так і, 14 передусім, за основною функціональною здатністю - меланіногенезом. Оцінку впливу Дикарбаміну на диференціювання клітин меланоми за інтенсивністю меланіногенезу проводили шляхом підрахунку числа клітин з меланіном у зрізах пухлини. З цією метою у мишей забирали пухлину, поміщали у глутаральдегід і проводили гістологічну обробку для електронної мікроскопії. В одержаних зрізах розраховували Індекс інтенсивності меланіногенезу (ІІM), який відображає ступінь диференціювання клітин: ІІМ=ПК´П М, де: ПК- кількість клітин, що містять меланосоми; ПМ – середня кількість меланосом на клітину. Аналіз інтенсивності меланіногенезу, проведений по даному показнику, наведений у Таблиці 2. Таблиця 2 Порівняльна інтенсивність меланіногенезу у клітинах меланоми після введення Дикарбаміну (електронна мікроскопія) Показники (абсолютні величини) Число клітин з меланосомами (на 500 клітин) Середнє число меланосом на клітину ПМ Контроль Після введення Дикарбаміну Контроль Після-введення Дикарбаміну Контроль Після введення Дикарбаміну Час, що минув з моменту скасування Дикарбаміну 12 годин 24 години 48 годин 135,0 144,0 159,0 175,0 210,0 227,0 19,0 21,0 26,0 28,0 35,0 42,0 5,1 6,0 8,2 9,8 14,7 19,0 * починаючи з 9 доби після перевивання пухлини Внаслідок електронномікроскопічного дослідження показано, що у порівнянні з контролем під впливом Дикарбаміну збільшується число пухлинних клітин, які містять меланосоми, і число меланосом на одну клітину. Індекс ІІМ збільшується за строками спостереження: через 12 годин - у 1,9 рази, через 24 години - у 2,4 рази і через 48 годин - у 2,3 рази. Таким чином, після 15-денного курсу введення Дикарбаміну збільшується ступінь диференціювання пухлинних клітин меланоми М-6, в середньому, у 2,2 рази, що підтверджується інтенсивністю меланіногенезу (індекс ІІМ), збільшенням числа клітин, що містять меланосоми (в 1,3 рази), і збільшенням у них числа меланосом (у 1,3 рази). Приклад 2. Дія Дикарбаміну на меланінсинтезуючу функцію клітин меланоми, що перевивається, людини Мишам з перевитою підшкірно меланомою людини, як описано у прикладі 1, вводили Дикарбамін щодня перорально у більш високій разовій дозі 4,5мг/кг протягом 3 тижнів від моменту трансплантації пухлини. Забій тварин проводили через 3 тижні від моменту трансплантації пухлини. Об'єм пухлин до моменту забою складав в середньому 150мм 3. Після забою у мишей забирали пухлину, яку дезінтегрували розчином Версена і виділяли клітинну фракцію, в якій при світловій мікроскопії у камері Горяєва підраховували число клітин з пігментом. Внаслідок проведених досліджень показано, що у контролі середнє число клітин з меланіном становило 39,14±8,72, а у досліді - 108,42±11,91, тобто число меланінсинтезуючих клітин достовірно (р
ДивитисяДодаткова інформація
Назва патенту англійськоюInduction method for cell differentiation
Автори англійськоюNiebolsin Vladimir Yevhenievich, Horbunova Vera Andrieevna, Treshchalin Ivan Dmitrievich, Raikhlin Natan Tanfelevich, Harin Avhust Mikhailovich, Bychkov Mark Borisovich, Treshchalina Yelena Mikhailovna, Zheltukhina Galina Aleksandrovna
Назва патенту російськоюСпособ индуцирования дифференцирования клеток
Автори російськоюНебольсин Владимир Евгеньевич, Горбунова Вера Андреевна, Трещалин Иван Дмитриевич, Райхлин Натан Танфелевич, Гарин Август Михайлович, Бычков Марк Борисович, Трещалина Елена Михайловна, Желтухина Галина Александровна
МПК / Мітки
МПК: A61K 38/00, A61P 35/00
Мітки: індукції, спосіб, клітин, диференціювання
Код посилання
<a href="https://ua.patents.su/22-85039-sposib-indukci-diferenciyuvannya-klitin.html" target="_blank" rel="follow" title="База патентів України">Спосіб індукції диференціювання клітин</a>
Попередній патент: Пристрій для нагрівання рідини
Наступний патент: Спосіб диференційної діагностики впливу ксенобіотиків на стійкість рослин
Випадковий патент: Креш-модуль для рейкового транспортного засобу












