Композиція, що містить триазинони і залізо, для подолання кокцидіозних інфекцій та дефіциту заліза
Номер патенту: 97985
Опубліковано: 10.04.2012
Автори: Торрес Іслас Хуан Агустін, Мундт Ханс-Крістіан, Хофманн Штефан, Хееп Іріс
Формула / Реферат
1. Композиція, що містить триазинони формул (І) або (II)
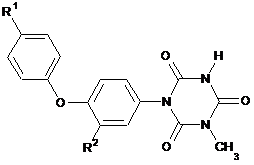 (I)
(I)
або
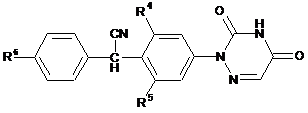 , (II)
, (II)
де
R1 означає R3-SO2- або R3-S-,
R2 означає алкіл, алкокси, галоген або SO2N(CH3)2, a
R3 означає галогеналкіл,
R4 і R5 незалежно один від іншого означають водень або хлор, а
R6 означає фтор або хлор,
або їх фізіологічно прийнятні солі
і
сполуки Fe(2+) або Fe(3+), вибрані із групи, що включає:
(a) солі Fe(II) карбонових кислот, комплексні сполуки Fе(ІІ)-карбонових кислот і хелатні комплекси Fe(II) з амінокислотами,
(b) солі Fe(III) карбонових кислот, комплексні сполуки Fе(III)-карбонових кислот і хелатні комплекси Fe(III) з амінокислотами і
(c) комплексні сполуки багатоатомних полісахаридів з Fe(III).
2. Композиція за п. 1, містить від 1 до 30 % м/о, переважно 3-7 % м/о триазинону.
3. Композиція за будь-яким із попередніх пунктів, в якій диспергований триазинон має розміри частинок d(v,90)≤30 мкм, переважно d(v,90)≤20 мкм, особливо переважно d(v,90)≤10 мкм.
4. Композиція за будь-яким із попередніх пунктів, у якій концентрація сполуки заліза становить від 10 % м/о до 30 % м/о активного заліза, переважно 11,4 % м/о - 25 % м/о, одначе особливо переважно 20 % м/о - 25 % м/о.
5. Композиція за будь-яким із попередніх пунктів, що має в'язкість, визначену шляхом утворення середнього із значень, виміряних при швидкостях зсуву 128 с-1 і 256 с-1 за допомогою побудованого за принципом конус/пластина реометра, у діапазоні від 10 до 2500 мПа.с, переважно у діапазоні 20-1500 мПа.с.
6. Композиція за пунктом 1 на основі води.
7. Композиція за пунктом 1, що містить щонайменше один багатоатомний аліфатичний спирт.
8. Композиція за будь-яким із попередніх пунктів, що містить багатоядерну Fe(III)-полісахаридну комплексну сполуку групи (с), багатоядерна основа якої складається із b-FеО(ОН)-одиниць і яка містить полісахаридну молекулу у іншій координаційній сфері.
9. Композиція за пунктом 8, що містить багатоядерну Fе(III)-полісахаридну комплексну сполуку, вибрану із групи: Fе(ІІІ)-декстран, Fе(ІІІ)-гідрокси-полімальтоза / Fе(ІІІ)-декстрин і не стехіометрична сполука із багатоядерної одиниці b-FeO(OH) і сахарози та олігосахаридів.
10. Композиція за будь-яким із попередніх пунктів, що як триазон містить триазинтріон.
11. Композиція за будь-яким із попередніх пунктів, що як триазинон містить толтразурил, а як багатоядерну Fе(ІІІ)-полісахаридну комплексну сполуку містить Fе(ІІІ)-декстран.
12. Композиція за будь-яким із пунктів 1-11, що містить одну або кілька структурних складових.
13. Застосування композиції за будь-яким із попередніх пунктів для виготовлення лікарських засобів.
14. Застосування за пунктом 13 для виготовлення лікарських засобів для одночасного подолання кокцидіозних інфекцій і станів дефіциту заліза.
15. Застосування за пунктом 13 або 14 для виготовлення лікарських засобів для орального введення.
16. Застосування за пунктом 15 для виготовлення лікарських засобів для орального введення молочним поросятам.
17. Застосування за пунктом 15 для виготовлення лікарських засобів для орального введення молочним поросятам у проміжку часу від народження до 10 днів після народження, переважно у проміжку часу від народження до 3 днів після народження.
Текст
Реферат: Винахід стосується одночасного застосування триазинів, таких як толтразурил, поназурил або диклазурил, і сполук заліза у композиції для подолання кокцидіозних інфекцій і станів дефіциту заліза у тварин і людей. UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 60 Винахід стосується композицій, що містять триазинони і сполуки заліза (солі і комплексні сполуки заліза), і придатні для одночасного подолання кокцидіозів і станів дефіциту заліза у тварин. Сучасні економічно успішні підприємства з виробництва м'яса відрізняються високоінтенсивним веденням господарства, тобто утриманням великої кількості тварин, спеціально відібраних для оптимізації розведення. Відмітними ознаками є, наприклад, високий рівень застосування машин, введення кормових домішок і якомога менше залучення персоналу. У разі підприємства з розведення поросят це означає, що велику кількість свиноматок, які дають велику кількість поросят за опорос, утримують у відповідно просторих приміщеннях. Оптимізація корму і відповідний відбір уможливлюють швидкий ріст поросят. Такий вид утримання тварин часто зумовлює почастішання звичайних типових захворювань і патологічних станів. Поряд зі стресом, до яких зокрема схильні свині при інтенсивному утриманні, у разі молодих свиней це можуть бути крім іншого найпростіші інфекції (кокцидіози) і стани браку заліза, які часто мають бути усунуті шляхом профілактичного застосування медикаментів. У разі тварин кокцидіози є часто виникаючими, паразитичними інфекційними захворюваннями. Так, наприклад, найпростіші з родів Eimeria, Isospora, Neospora, Sarkosporidien і Toxoplasma спричинюють поширені у всьому світі кокцидіози. Суттєвими з господарської точки зору є, наприклад, зараження свиней кокцидами роду Isospora або корів кокцидами роду Eimeria. Зараження кокцидами Isospora suis були виявлені і інтенсивно досліджені лише в останні роки як причина поносу поросят. Зараження передається, як правило, від довкілля до поросят або від поросят до поросят через ооцисти, які мають два спороцисти, у кожному з яких є два спорозоїти. Розмноження стадій паразитів здійснюється у епітеліальних клітинах ворсинок тонких кишок. До клінічних проявів захворювання належить некротичне, запальне руйнування клітин епітелію кишок з атрофією ворсинок і викликані цим порушення травлення і всмоктування. Відмітними ознаками гострого захворювання є водянистий, від білого до жовтого кольору пронос, що проявляється частіш за все на 2-3 тижні життя. Інфіковані поросята мають зменшений приріст ваги. Профілактика і лікування захворювання досі розроблені недостатньо. Антибіотики неефективні, сульфонаміди хоча і допускаються для боротьби з кокцидіозом, одначе їх дія сумнівна і часто повторюване введення у кожному разі є не придатним для практики. Інші можливості лікування є суперечливими. Шляхом введення, наприклад, монензину, ампролію чи фуразолідону експериментально інфікованим поросятам захворювання усунути не вдавалося. Нові дослідження показали, що в окремих підприємствах незважаючи на добру гігієну до 92 % усіх опоросів можуть бути заражені Isospora suis. Цей вид захворювання не обмежується лише свинями, а може проявлятися також у багатьох інших тварин, наприклад, птахів, телят, ягнят чи дрібних домашніх тварин (кроликів). Прикладом стану дефіциту є стан дефіциту заліза у новонароджених поросят. Внаслідок швидкого росту у перші дні після народження відбувається швидке вичерпання наявних у організмі запасів заліза, які мають бути компенсовані зовнішніми джерелами. Внаслідок великої кількості молочних поросят ця компенсація не може бути здійснена в достатній мірі шляхом всмоктування молока свиноматки. До того ж, у разі утримування свиней на бетонних чи синтетичних підлогах поросята не можуть здобути сполуки заліза шляхом риття в землі. Поросята стають анемічними. Клінічно суттєвий анемічний стан настає тоді, коли вміст гемоглобіну в крові стає нижчим, ніж 80 г/л. Згідно з рекомендаціями NRC (National Research Council, Nutrient Requirements of Domestic Animals, No.2, Nutrient Requirements of Swine, National Academy of Sciences, Washington DC, 1973) 90 г/л вказується як мінімальне значення вмісту гемоглобіну, при якому поросята ростуть здоровими і не мають ознак анемії. Одначе явні симптоми, такі як втрата ваги чи уповільнення росту, проявляються лише тоді, коли вміст гемоглобіну в крові знижується до значень, менших, ніж 80 г/л. Іншими індикаторами для підживлення залізом є значення гематокриту і кількість червоних кров'яних тілець на одиницю об'єму. Важка залізодефіцитна анемія веде також до смерті поросят. Для подолання вказаних хвороб і дефіцитних станів уже є в розпорядженні препарати. Кокцидіоз може бути успішно подоланий шляхом введення активних речовин із групи триазинонів. Тут розрізняють триазиндіони - представниками яких є, наприклад, активні речовини клазурил, диклазурил, летразурил - і триазинтриони, активними речовинами яких є толтразурил, толтразурил-сульфоксид і поназурил. Триазини, зокрема толтразурил, понзазурил або диклазурил, а також їх дія проти кокцидів описані, наприклад, у публікаціях DE-OS2718799 і DE-OS2413722. Із публікації WO 99/62519 відомі напівтверді водні препарати толтазурилсульфону (поназурил). Відомо також, що зокрема толтразурил придатний для лікування кокцидіозу (наприклад Isospora suis) у свиней. Див. також, наприклад, такі публікації: Don't forget 1 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 60 coccidiosis, update on Isosporosis in piglets. Part I, Pig Progress volume17, No2, 12-14; Mundt, H.C., A. Daugschies, V. Letkova (2001): be aware of piglet coccidiosis diagnostits. Part II, Pig Progress volume17, No 4, 18-20; Mundt, H.-C., G.-PI Martineau, K. Larsen (2001): control of coccidiosis Part III, Pig Progress volume17, No 6, 18-19. Кокцидіози у великої рогатої худоби, викликані різними патогенними Eimeria spp. (наприклад Ε. bovis і Ε. zürnii) виражаються проносами різного ступеню тяжкості аж до кров'яних проносів зі смертністю. У публікаціях WO 96/38140, DE 10049468, DE 19958388, WO 00/19964, WO 99/62519 або WO 00/37063, а також в DE 102006038292.7 описані засоби проти кокцидіозу у тварин. Поряд з іншими видами введення там згадують у загальній формі оральне введення. У публікації DE 19603984 описані грануляти для орального введення. У публікації DE 19824483 описані напівтверді, водні препарати (пасти) для лікування тварин. У публікації ЕР 0116175 описані розчини для орального введення. У галузі птахівництва часто застосовують розчинні у питній воді препарати чи розчини для пиття, тоді як активні речовини на підприємствах з розведення великих тварин скоріше додають до корму або у вигляді суспензій вводять орально за допомогою аплікатора. При цьому значення для ринку мають, наприклад: диклазурил (2,6-дихлоро-α-(4-хлорофеніл)-4-(4,5дигідро-3,5-діоксо-1,2,4-триазин-2(3Н)-іл)бензенацетонітрил; CAS Nr 101831-37-2) (CLINACOX™ 0,5 %, Janssen Animal Health; VECOXAN™, Biokema SA) для домішування до кормів і толтразурил (1-метил-3-[3-метил-4-[4-[(трифторометил)тіо]-фенокси-]феніл]-1,3,5-триазин2,4,6(1Н,3Н,5Н)-трион; CAS Nr 69004-03-1). Толтразурил є наявним на ринку прикладом препарату у вигляді питної води для птахів і у вигляді суспензії для лікування молочних поросят. Рекомендується введення поросятам дози 20 мг на кілограм ваги на третій-п'ятий день після народження. Недоліком є порівняно високі трудові витрати при оральному введенні указаних антикокцидіантів (інколи їх не зовсім коректно називають кокцидіостатиками): Для цього поросят треба ловити і за допомогою аплікатора або впорскувального пістолета ввести продукт у горло. До того ж, такий спосіб спричинює суттєвий стрес для поросят. Для запобігання залізодефіцитній анемії є у розпорядженні ряд різних препаратів заліза, які відрізняються як типом сполук, так і способом введення і біологічною переносністю. Розрізняють (І) прості неорганічні солі Fe(2+), (llа) комплексні сполуки Fe(2+) з органічними лігандами, наприклад, з молочною кислотою, або (llb) комплексні сполуки Fe(3+), наприклад, з лимонною кислотою, і (III) полімероподібні комплексні сполуки Fе(3+)-оксо-гідроксо-комплекс FeO(OH) типу акаганеїту з вуглеводами/полісахаридами, зокрема з олігомерними чи полімерними вуглеводними сполуками, такими як декстран чи декстрин/полімальтоза. В подальшому під полімерними вуглеводами/вуглеводними сполуками і полісахаридами маються на увазі як олігомерні, так і полімерні сполуки. Звичайними і здавна відомими є оральні препарати типу (І), наприклад, солі заліза як кормові добавки. У цих сполуках залізо перебуває у формі іонів Fe(2+), наприклад, у вигляді сульфату заліза FeSO4. Ці продукти можуть бути як додані до корму свиноматки, так і введені поросятам орально. У більшості випадків поросятам вводять кілька окремих доз у перші дні життя з метою компенсації порівняно низької біопридатності. Альтернативою багаторазовому введенню є пізніше введення залізовмісної кормової домішки. Тоді як у неорганічних солях Fe(2+) іони заліза швидко вивільняються шляхом дисоціації, вивільнення у комплексних сполуках Fe(2+) відбувається із затримкою. Ресорбція вільних іонів Fe(2+) із солей заліза відбувається у верхній частині тонкої кишки. Розчинність Fe(2+) за фізіологічних умов верхньої частини тонкої кишки на кілька порядків вища, ніж Fe(3+) (Forth, W., in: Dünndarm, Handbuch der inneren Medizin, Bd.3 Verd.Org.Teil 3(A); W.F. Caspary, Hrsg.; Springer 1983). До того ж, вільні іони Fe(3+) всередині кишки відновлюються цистеїном, глутатіоном, аскорбіновою кислотою та іншими речовинами до Fe(2+) і як такі сприймаються клітинами епітелію слизової оболонки кишки. Одначе питання про те, чи є це відновлення необхідною передумовою для сприймання клітинами слизової оболонки - спірне. Ймовірно, градієнт концентрації внаслідок вищої розчинності Fe(2+) є підставою для вищої біоприйнятності. Згідно з сучасними уявленнями відбувається спочатку зв'язування іонів Fe(2+) на білку мобілферин, у якому вони знову оксидуються до Fe(3+) і зв'язуються на слизовому накопичувальному білку феритин. У разі потреби організму у іонах Fe(3+) вони передаються плазмі крові, де фериоксидазою знову відновлюються до Fe(2+) і зв'язуються з білком апо-трансферин - залізов'язуючим транспортним білком організму. Спірним є питання, чи трансферний уже перебувають у клітинах слизової і там принаймні частково приймають залізо. Стала комплексоутворення трансферину зі значенням log K близько 30-31 настільки велика, що ніде в організмі вільне 2 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 60 залізо не може існувати, доки не буде перевищена залізозв'язувальна ємність трансферину. У цьому полягає причина токсичних ефектів, що можуть виникати при раптовому передозуванні солей заліза, що є недоліком при їх застосуванні. Потім через кров і лімфатичні судини залізо потрапляє до місця синтезу гемоглобіну у кістковому мозку (див. E. Kolb, U.Hofmann "Anwendungen von Eisenverbindungen beim Schwein" Tierärtzl. Umschau 60, (2005) 365-371 і Forth, W. "Eisen і Eisenversorgung des Warmblüterorganismus", Naturwissenschaften74, (1987) 175-180, а також John, A.; "Neue Möglichkeiten der Eisenversorgung neugeborener Ferkel unter Beachtung biochemischer Aspekte" in: Trächtigkeit und Geburt beim Schwein, 8.Bernburger BiotechnikWorkshop 2002, 89-94). He потрібне залізо залишається у клітинах слизової, але після їх відмирання більше не може бути використане. Таким чином зрозуміло, що біоприйнятність оральних сполук заліза значною мірою залежить від інших факторів, таких як дійсна потреба організму у залізі, стан годування (молозиво) і стан здоров'я (діарея: завчасна втрата верхніх клітин слизової). Розуміння механізму важливе для розуміння і оцінки переваг і недоліків певних препаратів заліза. Крім того, використовуються сполуки із другої групи (II) желеподібних комплексних сполук Fe(2+) і Fe(3+). Вони утворюють порівняно стабільні комплекси заліза, які лише частково розбиваються на іони кислотою шлункового соку. Біоприйнятність у ході подальшого руху визначається тим, що залізо частково замінюється лігандами на або в клітинах слизової, що залежить від констант утворення комплексних сполук. Комплекси внаслідок вищої ліпофілії можуть проникати крізь мембранну систему епітелію і мають метаболізуватися. Це пояснює, чому органічні низькомолекулярні комплекси є повільно біосприйнятними, але завдяки цьому мають більш тривалу дію (Н. Dietzfelbinger; "Bioavailability of Ві- and Trivalent Oral Iron Preparations"; Arzneim.-Forsch. / Drug. Res 37(1), Nr.1a, (1987) 107-112 i E.B.Kegley et al, "Iron Memionin as a Source of Iron for the Neonatal Pig", Nutrition Research 22 (2002) 1209-1217). Третя група сполук, які вводяться парентерально і лише у меншій мірі орально, складається із дуже стабільних сполук типу полі-β-FеО(ОН) з комплекснозв'язаними полімерними вуглеводами. Тут комерційного успіху досягли в основному, але не виключно Fе(ІІІ)-декстран (CAS Nr 9004-66-4), Fe(lll)-гідроксид-полімальтоза (Fе(ІІІ)-гідроксид-декстрин; CAS Nr. 53858-869) Fe(lll)-сахароза (Fе(ІІІ)-сукроза, Fе(ІІІ) "цукор" CAS Nr. 8047-67-4) і комплекс натрій Fe(lll)глуконат у розчині сахарози (CAS Nr. 34089-81-1). У літературі є різні назви цих сполук. Під сполуками Fе(ІІІ)-декстран, -полімальтоза, -декстрин, -сахароза, -глуконат, -цукор тут маються на увазі комплекси іонів Fe(3+) з іонами гідроксиду (ОН ), води (Н2О) і кисню (О), що перебувають у оліго- або полімерній формі, і комплексно асоціюються з однією чи кількома названими олігомерними і полімерними вуглеводними сполуками у їх координаційній сфері. На цій підставі сполуки називаються також як Fе(ІІІ)-гідроксид-полісахарид або Fe(lll)-окси-гідроксиполісахарид, причому полісахарид означає наведені вище оліго- і полімерні вуглеводні сполуки чи їх похідні або загалом сполуки із групи олігомерних чи полімерних вуглеводів. Багатоядерні Fе(lІІ)-комплекси цього виду описані, наприклад, у (D.S.Kudasheva et al. "Structure of Carbohydrate-bound Polynuclear Oxyhydroxide Nanoparticles in Parenteral Formulation", J. Inorg. Biochem. 98 (2004) 1757-1769; I.Erni et al "Chemical Characterization of Iron(lll)-Hydroxide-Dextrin Complexes" Arzneim.-Forsch. / Drug Res.34 (II) (1984) 1555-1559; F.Funk et al. "Physical and Chemical Characterization of Therapeutic Iron Containing Materials", Hyperfine Interactions 136 (2001) 73-95; E.London "The Molecular Formula and Proposed Structure of the Iron-Dextran Complex, IMFERON", J. Pharm. Sci. 93 (2004) 1838-1846; A.John "Neue Moglichkeiten der Eisenversorgung neugeborener Ferkel unter Beachtung biochemischer Aspekte", Trächtigkeit und Geburt beim Schwein: 8. Bernburger Biotechnik-Workshop, Bernburg (2002) 89-94.). Оскільки склад цих сполук у багатьох випадках якісно не описаний і всередині сполук також може варіюватися в залежності від виду виготовлення, під цими багатоядерними полісахаридними Fе(ІІІ)-сполуками слід розуміти усі відомі фахівцеві комплекси описаного класу сполук. Ці сполуки заліза знаходять застосування майже винятково при виготовленні ін'єкційних препаратів для медицини і ветеринарії. Однак у ветеринарії використовують також деякі препарати для орального введення. Ці комплексні сполуки характеризуються загалом високою стабільністю і відрізняються в основному молекулярною масою, що може варіюватися від 30 кДа до 400 кДа, а також силою комплексного зв'язку. У водному розчині вони перебувають у формі колоїдної дисперсії з розмірами частинок 7-35 нм. Вирішальним для біоприйнятності у разі орального введення є, по-перше, міра утворення осаду і гідролізу залізного ядра під дією кислоти шлункового соку, а по-друге - стабільність комплексної сполуки за кислих відновних умов. Механізми приймання організмом і перетворення у біологічні сполуки заліза ще не повністю з'ясовані і у літературі ще частково дискутуються. Але деякі основні положення щодо механізму дії можуть бути сформульовані. Чим стабільніший комплекс, тим вища частка 3 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 60 сполуки, що незмінною витримує умови шлунку і тим меншою є частка вільних іонів заліза. Стабільність комплексу у свою чергу залежить від методу синтезу. Високомолекулярні Fе(ІІІ)полімальтоза і Fе(ІІІ)-декстран виявилися досить стабільними. На противагу цьому є необхідність передачі заліза білкові транспортного каналу. Ця передача природно тим нижча, чим стабільнішими є комплекси. Ці взаємозв'язки були підтверджені різними дослідами з кислотами, відновлювальними засобами і комплексоутворювачами (R.Lawrence "Development and Comparison of Iron Dextran Products"; PDA J Pharm. Sci. Techn. 52(5) (1998) 190-197; F.Funk et al "Physical and Chemical Characterization of Therapeutic Iron Containing Materials"; Hyperfine Interactions 136 (2001) 73-95; I.Erni et al "Chemical Characterization of Iron(lll)-Hydroxide-Dextrin Complexes" Arzneim.-Forsch. / Drug Res.34(11) 11 (1984) 1555-1559). Із цих міркувань випливає висновок, що Fе(3+)-сполуки загалом і зокрема багатоядерні сполуки, такі як Fе(ІІІ)-декстран, не придатні для орального введення (H.Dietzfelbinger "Bioavailability of Ві- and Trivalent Oral Iron Preparations" Arzneim.-Forsch. / Drug Res.37(1), Nr 1(a) (1987) 107-112.). Іншою підставою для скепсису проти орального введення багатоядерних Fe(3+)-комплексів, зокрема Fе(ІІІ)-декстрану, є специфічний шлях поглинання β-FeO(OH)-комплексів у кишковому тракті. Ці сполуки вбираються шляхом піноцитозу у клітини епітелію слизової оболонки кишок і потім мають бути віддані організмові через лімфові русла, накопичені у лімфатичних вузлах і зрештою транспортовані у кров'яні русла (див. уже вказану статтю авторів Kolb, Hofmann; Forth; John). Оскільки вони - як було сказано - досить стабільні, біоприйнятність залежить від метаболізму і ферментного розкладу комплексів лізосомальними ферментами. Із дослідів з полівілінпіролідоном, декстраном і міченим фарбниками Fe(lll)-декстраном з різною молекулярною масою відомо, що у молочних поросят вбирання цих полімерних комплексів шляхом піноцитозу може бути здійснене через епітеліальні клітини дванадцятиперсної кишки і верхньої частини тонкої кишки на перших днях життя (R.M.Clarke, R.N.Hardy "Histological Changes in the Small Intestine of the Young Pig and Their Relation to Macromolecular Uptake"; J. Anat. 108(1), (1971) 63-7; K.Thoren-Tolling, L.Jönsson "Cellular Distribution of Orally and Intramuscularly Administered Iron Dextran in Newborn Piglets", Can. J. Соmр. Med. 41 (1977) 318325; K. Martinsson, L.Jönsson "On the Mechanism of Intestinal Absorption of Macromolecules in Piglets Studied with Dextran Blue", Zbl. Vet. Med. A22 (1975) 276-282). Одначе відомо також, що цей перехід високомолекулярних сполук від клітин слизової у лімфатичні і кров'яні русла поросят безперешкодно можливий лише безпосередньо після народження. Цей механізм гарантує, що живлення поросят імуноглобулінами і антитілами шляхом вживання молозива свиноматки може відбуватися відразу після народження. Як тільки це живлення припиняється, транспортний механізм занепадає. Ця блокада слизової оболонки ("Intestinal Closure") у ході подальшого росту тварини є біологічно раціональною для уникнення зараження мікроорганізмами і токсинами (K. Martinsson, L.Jönsson "The Uptake of Macromolecules in the lleum of Piglets after Intestinal Closure", Zbl. Vet. Med. A 23 (1976) 277-282). Тому інтервал часу між народженням і блокадою слизової оболонки значною мірою залежить від стану годування поросят. У голодаючих поросят ця передача ще може здійснюватися до чотирьох днів після народження (J.G. Lecce, D.O. Morgan "Effect of Dietary Regimen on Cessation of Intestinal Absorption of Large Molecules (Closure) in the Neonatal Pig and Lamb", J. Nutrition 78 (1962) 263268). Одначе оскільки загальні умови утримання у розплідних підприємствах природно уможливлюють ссання, на сьогоднішній день загальний рівень медичних знань визнає, що достатнє введення поросятам високомолекулярних комплексних сполук заліза оральним шляхом можливе лише у перші години після народження, якщо уникати багаторазового введення. Деякі автори, які систематично досліджують ефективність Fе(ІІІ)-декстран в залежності від моменту часу орального введення, повідомляють про значно зменшену ефективність у разі введення Fе(ІІІ)-декстрану через 24-72 години після народження (L.BIomgren, N.Lanneck "Prevention of Anaemia in Piglets by a Single Oral Dose of Iron Dextran", Nord. Vet.-Med. 23 (1971) 529-536). Правда, в залежності від умов утримання і годування введенням на другому дні життя ще може бути досягнутий досить добрий результат (S.Kadis, "Relationship of Iron Administration to Susceptibility of Newborn Pigs to Enterotoxic Colibacillosis"; Am. J. Vet. Res. 45(2), (1984) 255-259). На противагу цьому при введенні Fе(ІІІ)-декстрану через 72-96 годин після народження ефективність значно зменшується (Ueda Η. "Prevention of Piglet Anemia by Oral Administration of Iron Dextran", Nicchiku Kaiho56(11), 1985, 872-877). Тому на ринку закріпилися лише деякі оральні препарати заліза з багатоядерними комплексами (Ursoferran150 р.о.; Fa Serumwerke Bernburg - Fe(lll)-Dextran; Ferrum Hausmann Syrup® Hausmann Laboratories Inc., St.Gallen; - Fe(lll)-Hydroxid-polymaltose). У сучасних препаратах для орального застосування Fe-декстран для покращення біоприйнятності зв'язують із 4 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 60 емульгаторами з розмірами краплинок мікроемульсії 1-2 мкм (Bioveyxin FeVit™, Fa. VeyxPharma GmbH, Schwarzenborn; SintaFer™, Fa. Sinta GmbH, Schwarzenborn). Цей тонкодисперсний стан і приєднання до ліпофільного носія має стимулювати поглинання епітеліальними клітинами і передачу в організм. Але навіть для цих препаратів для досягнення оптимальної ефективності виробником рекомендується введення до максимум 8-10 годин після народження. Це у свою чергу обумовлює безперервний контроль свиноматок, що значно збільшує витрати на персонал. Загалом для досягнення достатньої ефективності орального препарату заліза рекомендується доза 100-200 мг активного заліза на порося і одиничну дозу. Одначе на практиці лише для вищої дози достатньо одноразового введення. Для оминання описаних складнощів з дозуванням при оральному застосуванні у галузі вирощування свиней звичайним є введення багатоядерних Fe(lll)-комплексів внутрішньом'язовими ін'єкціями. Це здійснюють, як правило, шляхом ін'єкції 100-200 мг активного заліза на третій день після народження. Транспортування від місця ін'єкції здійснюється через лімфатичну систему і клітини ретикулогістіоцитарної системи. Накопичення комплексу здійснюється у печінці і селезінці, звідки залізо у разі потреби вивільняється і ферментативно метаболізується. Зрештою вільні іони Fe(3+) знову зв'язуються з трансферином і доставляються до місця використання у кістковому мозку. Але навіть ця парентеральна форма застосування має ряд недоліків. Явним недоліком внутрішньом'язового введення поросятам є часті прояви шкідливих ефектів. У місці ін'єкції часто виникають кровотечі із м'язів, зміни м'язових волокон і набряки. Це - локальні пошкодження. Одначе спостерігалися також пошкодження серцевого м'яза, зокрема при одночасному бракові вітаміну Е. У таких випадках може бути зафіксоване значне зростання вмісту калію у плазмі крові, що може призвести до значного пошкодження серцевого м'яза і до смерті поросяти. Сучасна наукова думка вважає, що найменші кількості вільних іонів Fe(2+) спричинює утворення радикальних сполук з органічними молекулами, наприклад, ліпідпероксидних сполук, що пов'язано з високим вмістом калію у крові. Вітамін Ε діє як уловлювач радикалів і може певною мірою буферувати ці шкідливі реакції, але при цьому значною мірою перевищуються власні можливості організму. (Тому до уже згаданих оральних препаратів, в яких Fe(ІІІ)-декстран зв'язаний з краплинками мікроемульсії, також додають вітамін Е). Одначе внутрішньом'язове застосування має недолік з іншої точки зору: після введення Fе(ІІІ)декстрану слід рахуватися із певним обмеженням ефективності імунної системи, оскільки макрофаги у крові навантажуються багатоядерними комплексами заліза. Захисна здатність проти бактеріальних інфекцій зменшується. Огляд описаних недоліків внутрішньом'язового введення наведений у літературі: (E.Kolb, U.Hofmann "Zur Frage der zweckmäβigen Form der Anwendung von Fe-Dextran, seiner Verwertung, sowie des Mechanismus einer moglichen Schadigung der Ferkel"; Mh.Vet.-Med. 44 (1989) 497-501). Підсумовуючи, можна констатувати, що використовувані досі методи профілактики анемії у поросят мають ряд недоліків: 1. При оральному введенні сполук Fe(II) типів (І) і (II) згідно з публікаціями у більшості випадків спостерігається значно менша біоприйнятність. Рекомендується вводити ці препарати кілька разів, що при інтенсивному утриманні тварин збільшує витрати на персонал і є економічним недоліком. 2. Оральне введення багатоядерних сполук Fe(lll) типу (III), зокрема Fe(lll)-декстрану хоча і веде до кращих результатів, і одноразове введення дози близько 200 мг активного заліза, як правило є достатнім для забезпечення в організмі поросяти потрібної кількості заліза, вирішальним недоліком є те, що згідно з сучасним рівнем знань достатня ефективність може бути досягнута лише тоді, коли поросятам вводять Fе(ІІІ)-декстран протягом перших 8-10 годин життя. Це можна було б забезпечити лише при суцільному контролі народження у розплідниках, що часто здійснити неможливо через значну потребу у персоналі. Пропускання цього моменту часу часто веде до значних втрат поросят. 3. Препарати заліза для внутрішньом'язового введення є найбільш застосовуваними, оскільки введення в інтервалі часу від 1 до 3 днів після народження дає дуже добрі результати. Недоліком такого введення є потенційне ушкодження поросят токсичними побічними ефектами і короткочасне ослаблення імунної системи. Препарати для орального введення не мають цього недоліку. 4. Крім того, спостереження за часто необхідною профілактикою кокцидіозу з використанням толтразурилу або подібних сполук показало, що для успішного вирощування поросят дуже часто необхідно здійснювати дві робочі операції: (1) уловлювання поросят у перший день після народження і введення, наприклад, Fе(ІІІ)-декстран, наступне уловлювання поросят на третій 5 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 день і оральне введення наявного на ринку суспензійного препарату толтразурилу або (2) уловлювання поросят на третій день і окреме введення наявного на ринку суспензійного препарату толтразурилу для орального застосування, а також ін'єкційного препарату Fе(ІІІ)декстрану (з описаними вище недоліками). Таким чином, значні переваги мали б препарати, які без описаних вище недоліків, тобто без шкідливих побічних ефектів при більш надійній і високій ефективності, уможливили б об'єднання обох робочих операцій. Придатним препаратом могла б бути, наприклад, композиція активної речовини толтразурил і Fе(ІІІ)-декстрану для орального введення поросятам в інтервалі часу першого-третього дня після народження. Одначе препарати, що об'єднують обидві робочі операції, мають задовольняти ряду умов: ▪ Достатня кількість активних речовин: Одинична доза має містити достатню для фармакологічної ефективності кількість антикокцидіального засобу, зазвичай 20-70 мг, наприклад, 30 мг, 44 мг або 50 мг толтразурилу, і щонайменше 100 мг, одначе краще щонайменше 150 мг, переважно 200-250 мг активного заліза (відповідно, наприклад, 400-600 мг багатоядерного Fе(ІІІ)-комплексу) для профілактики анемії - відповідно рекомендовані дозування 20 мг толтразурилу на кілограм ваги тіла і 200 мг активного заліза на порося. Це відповідає концентрації 2-7 % м/о антикокцидіального засобу і 10-25 % м/о активного заліза у композиції (при цьому під % м/о слід розуміти масу відповідного компонента у грамах на 100 мл об'єму). ▪ Незначний об'єм дози для орального введення: Наприклад, для молочних поросят оптимальним об'ємом дози є 1 мл, оскільки при значно більшому об'ємі часто не забезпечується повне поглинання поросятами. Значна кількість рідини часто витікає із рота або відригується. ▪ Придатна консистенція: В'язкість має перебувати у діапазоні, який уможливлює введення впорскувальними пістолетами або шприцами, наприклад, від 10 до 2500 мПас. У разі надто рідкої консистенції препарат після введення може витікати із рота тварини, а у разі надто густої масове введення за допомогою шприців чи впорскувальних пістолетів є втомливим для оператора, а тварини, зокрема поросята, мають проблеми із ковтанням. ▪ Якість композиції: Мають бути забезпечені фізична і хімічна стабільність, а також фармакологічна ефективність. Так, наприклад, має бути забезпечено, щоб іони заліза не погіршували хімічної стабільності антикокцидіальної речовини. Крім того, має бути забезпечено, щоб у разі суспензійної композиції залишалося дрібнодисперсне розподілення активної речовини; коагулювання чи навіть грудкування диспергованих частинок активної речовини є неприпустимим. Цим може бути погіршена фармакологічна ефективність, оскільки швидкість розчинення і таким чином вивільнення активної речовини із частинок у кишці зменшується внаслідок меншої площі поверхні. ▪ Ефективність введення у більшому інтервалі часу після народження: Бажаною є достатня ефективність проти кокцидіозу і анемії при введенні у проміжку часу від одного до трьох днів після народження, особливо при одноразовому застосуванні. ▪ Достатня профілактика анемії при одноразовому застосуванні: Кількість заліза, наявна у згаданих незначних дозах препарату, має бути достатньою для покриття потреби організму поросяти у залізі після одноразового введення за нормальних умов утримування. Комбінація триазинонів і препаратів заліза у одній придатній композиції досі ще не була описана. Винахід стосується: 1. Засобу, що містить триазинони формул (І) або (II) або Де 1 3 3 R означає R -SO2- або R -S-, 2 R означає алкіл, алкокси, галоген або SO2N(CH3)2 і 3 R означає галогеналкіл 4 5 R і R незалежно один від іншого означають водень або СІ, а 6 R означає фтор або хлор. або їх фізіологічно переносні солі 6 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 60 і сполуки Fe(2+) або Fe(3+), вибрані із групи, що включає: (а) солі Fe(ll) карбонових кислот, комплексні сполуки Fe(ll)карбонових кислот і хелатні комплекси Fe(ll) з амінокислотами (b) солі Fe(lll) карбонових кислот, комплексні сполуки Fe(lll)-карбонових кислот і хелатні комплекси Fe(lll) з амінокислотами і (c) комплексні сполуки багатоядерних полісахаридів і Fe(lll). У формулах (І) і (II) окремі замісники мають переважно і особливо переважно такі значення: 2 R означає переважно алкіл або алкокси кожен з 1-4 атомами вуглецю або фтор, хлор, бром 2 або SO2N(CH3)2;R означає особливо переважно С1-4-алкіл. 3 R означає переважно фторалкіл з 1-4 атомами вуглецю, особливо переважно трифторметил. Триазинони самі по собі як активні речовини проти кокцидіозних інфекцій добре відомі; можна назвати такі триазинтриони, як толтразурил і поназурил, а також триазиндіони клазурил, диклазурил і летразурил. Триазиндіони відображаються формулою (II): 4 5 6 Клазурил R = СІ, R = Н, R = СІ у формулі (II) 4 5 6 Летразурил R = СІ, R = СІ, R =F у формулі (II) і 4 5 6 Диклазурил R = СІ, R = СІ, R = СІ у формулі (II) Із цих 1,2,4-триазиндіонів найбільш переважним є диклазурил. Згідно з винаходом як активні речовини особливо переважними є триазинтріони формули (І), 2 3 де R і R мають такі переважні і особливо переважні значення: 2 R означає переважно алкіл або алкокси, кожен з яких містить до 4 атомів вуглецю, особливо переважно метил, етил, н-пропіл, і-пропіл. 3 R означає переважно перфторалкіл з 1-3 атомами вуглецю, особливо переважно трифторметил або пентафторетил. Переважні триазинтріони відображаються формулою (І): 1 3 2 3 Толтразурил (R =R -S-, R = СН3,R =CF3) 1 3 2 3 Поназурил (R =R -SO2-, R = СН3,R =CF3) Дозування триазинону може - як було пояснено вище - варіюватися в залежності від особливостей тварин. Звичайні дозування становлять від 1 до 60 мг активної речовини на кілограм тіла (мг/кг) оброблюваної тварини на день, 5-40 мг/кг і особливо переважно 10-30 мг/кг. Толтразурил при оральному застосуванні дозують зазвичай у таких кількостях: Свиня: 20 мг/кг ваги тіла Корова: 15 мг/кг ваги тіла Вівця: 20 мг/кг ваги тіла Птиця: 15 мг/кг ваги тіла Лише у разі птиці толтразурил вводять лише один раз, а для свині, корови і вівці вказані дозування дійсні як на день, так і на лікування. Придатними Fe(2+)- або Fе(3+)-сполуками є: (a) солі Fe(2+) карбонових кислот, комплексні сполуки Fе(2+)-карбонових кислот і хелатні комплекси Fe(2+) з амінокислотами (b) солі Fe(3+) карбонових кислот, комплексні сполуки Fе(3+)-карбонових кислот і хелатні комплекси Fe(3+) з амінокислотами (c) комплексні сполуки багатоатомних полісахаридів і Fe(3+) Як приклади сполук заліза типу (а) можуть бути названі: Fе(ІІ)-лактат (FеС6Н10О6), Fe(ll)-глуконат (FeC12H22O14), Fе(ll)-фумарат (FeC4H2O4) і хелатні комплекси заліза з амінокислотами, наприклад, Fе(ІІ)-біс-гліцинат (Fe(C2H4NO2)2),Fe(ll)-Meтіонат (Fe(C5H10NO2S)2) та їх гідратні сполуки. Як приклади сполук заліза типу (а) можуть бути названі: Fе(ІІІ)-цитрат (FeC6H5O7), амонійFе(ІІІ)-цитрат та у разі потреби їх гідратні сполуки. Під сполуками заліза групи с) тут маються на увазі комплекси іона Fe(3+) з іонами гідроксиду (ОН ), води (Н2О) і кисню (О), які перебувають в оліго- чи полімерній формі і комплексно асоціюються з однією чи кількома із вказаних олігомерних і полімерних вуглеводних сполук у їх координаційній сфері. На цій підставі сполуки називаються також як Fе(ІІІ)-гідроксидполісахарид або Fе(ІІІ)-окси-гідрокси-полісахарид, причому полісахарид означає відповідні оліго- і полімерні вуглеводи або їх похідні. Багатоядерні Fе(ІІІ)-комплекси цього типу описані, наприклад, у публікаціях (D.S.Kudasheva et al. "Structure of Carbohydrate-bound Polynuclear Oxy 7 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 60 Hydroxide Nanoparticles in Parenterai Formulation", J. Inorg. Biochem. 98 (2004) 1757-1769; I.Erni et al. "Chemical Characterization of Iron(lll)-Hydroxide-Dexthn Complexes" Arzneim.-Forsch. / Drug Res.34 (II) (1984) 1555-1559; F.Funk et al. "Physical and Chemical Characterization of Therapeutic Iron Containing Materials", Hyperfine Interactions 136 (2001) 73-95; E.London "The Molecular Formula and Proposed Structure of the Iron-Dextran Complex, IMFERON", J. Pharm. Sci. 93 (2004) 1838-1846; A.John "Neue Möglichkeiten der Eisenversorgung neugeborener Ferkel unter Beachtung biochemischer Aspekte", Trächtigkeit und Geburt beim Schwein: 8. Bernburger Biotechnik-Workshop, Bernburg (2002) 89-94.). Оскільки точний склад цих сполук у багатьох випадках кількісно не описаний і в межах сполук також може варіюватися в залежності від методу виготовлення, під багатоатомними Fe(lll)-полісахаридними сполуками слід розуміти усі сполуки, які фахівець відносить до цього класу сполук. Як приклади сполук заліза типу (а) можуть бути названі: багатоядерні Fe(lll)-полісахаридні комплексні сполуки, в яких багатоядерний β-FеО(ОН)-комплекс у вільних координаційних місцях містить асоційовані полімерні вуглеводні сполуки, наприклад, Fе(ІІІ)-декстран, Fе(ІІІ)-гідроксиполімальтоза (Fе(ІІІ)-декстрин), нестехіометричні сполуки β-FeΟ(ΟΗ) з сахаридами і олігосахаридами "Fe(lll)-сахароза/цукроза" "Fе(ІІІ)-'цукор'". Із названих вище сполук заліза переважно використовуваними є сполуки типів (b) і (с), причому останні є особлива переважними. Як особливо переважний приклад слід назвати Fе(ІІІ)-декстран. Переважними придатними для тварин відповідними винаходові композиціями є розчини, суспензії або пасти, желе. Перевагу мають суспензії або пасти. Розчини виготовляють шляхом розчинення активної речовини чи активних речовин у придатних розчинниках або сумішах розчинників. У разі потреби додають інші допоміжні складові, такі як агенти розчинення, актиоксиданти, консерванти, згущувачі, адгезійні засоби, речовини, що регулюють значення рН, світлозахисні засоби або барвники. Як розчинники можуть бути названі: фізіологічно переносні розчинники, такі як вода, спирти, такі як одноатомні алканоли (наприклад етанол або н-бутанол), багатоатомні спирти, такі як гліколі (наприклад етиленгліколь, пропіленгліколь, тетрагліколь/глікофурол), поліетиленгліколі, поліпропіленгліколі, гліцерин; ароматично заміщені спирти, такі як бензиловий спирт, фенілетанол, феноксиетанол; естери, такі як естер оцтової кислоти, бутилацетат, бензилбензоат, етилолеат; етери, такі як алкіленглікольалкіловий етер (наприклад дипропіленглікольмонометиловий етер, діетиленглікольмонобутиловий етер); кетони, такі як ацетон, метилетилкетон; ароматичні і/або аліфатичні вуглеводи, рослинні або синтетичні масла; гліцеринформал, золькетал (2,2-диметил-4-гідроксиметил-1,3-діоксолан), Nметилпіролідон, 2-піролідон, Ν,Ν-диметилацетамід, глікофурол, диметилізосорбіт, лаурогліколь, пропіленкарбонат, октилдодеканол, диметилформамід, а також суміші названих розчинників. Як агенти розчинення можуть бути названі: розчинники, які стимулюють розчинення активної речовини у основному розчиннику або перешкоджають його осадженню. Прикладами є полівінілпіролідон, поліоксиетильована рицинова олія, поліоксиетильований сорбітановий естер. Антиоксидантами є сульфіти або метабісульфіти, такі як метабісульфіти калію чи натрію або дисульфіт калію аскорбіновакислота, ізо-аскорбінова кислота, пальмітат аскорбінової кислоти, естери галової кислоти, бутилгідрокситолуол, бутилгідроксианізол або токофероли. Синергістами цих антиоксидантів можуть бути: амінокислоти(наприклад аланін, аргінін, метіонін, цистеїн), лимонна кислота, винна кислота, едетинова кислота або їх солі, похідні фосфорної кислоти або багатоатомні спирти (поліетиленгліколь). Консервантами є: бензиловий спирт, хлорид бензалконію, трихлорбутанол, естери пгідроксибензойної кислоти, н-бутанол, хлорокрезол, крезол, фенол, бензойна кислота, лимонна кислота, винна кислота або сорбінова кислота. Згущувачами є: неорганічні згущувачі, такі як бентоніти, колоїдна кремнева кислота, стеарати алюмінію, органічні згущувачі, такі як похідні целюлози, наприклад, гідроксипропілметилцелюлоза 4000, полівінілові спирти та їх співполімери, ксантан, акрилати і метакрилати, карбоксиметилцелюлоза та її солі. Адгезійними засобами є, наприклад, похідні целюлози, похідні крохмалю, поліакрилати, натуральні полімери, такі як альгінати, желатини. Адгезійні засоби, що мають згущувальні властивості, можуть бути використані також як згущувачі. Речовини, що регулюють рН, є фармацевтично звичними кислотами чи основами. До основ належать гідроксиди лужних чи лужноземельних металів (наприклад NaOH, KOH), основні солі, такі як хлорид амонію, основні амінокислоти, такі як аргінін, холін, меглумін, етаноламіни, або 8 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 60 також буфер, такий як трис(гідроксиметил)амінометан, буфер на базі лимонної кислоти чи фосфатний буфер. До кислот належать, наприклад, соляна кислота, оцтова, винна, лимонна, молочна, бурштинова, адипінова, метансульфонова, актанова, ліноленова кислоти, глуконолактон, а також кислі амінокислоти, такі як аспарагінова кислота. Світлозахисними засобами є, наприклад, речовини із класу бензофенонів або новантізолова кислота. Придатними фарбниками є усі допущені для застосування для тварин чи людей фарбники, які можуть бути розчинені чи суспендовані. Суспензії виготовляють шляхом суспендування активної речовини чи активних речовин у несучій рідині, у разі потреби з додаванням інших допоміжних речовин, таких як змочувальні засоби, фарбники, стимулятори ресорбції, згущувачі, адгезійні засоби, консерванти, антиоксиданти, світлозахисні засоби або протиспінювачі. Як несучі рідини можуть бути використані усі гомогенні розчинники і суміші розчинників. Як змочувальні засоби (диспергатори) можуть бути використані: Поверхнево-активні речовини (включно з емульгаторами і змочувальними засобами), такі як 1. аніонактивні, такі як Na-лаурилсульфат, сульфати етерів жирних спиртів, моноетаноламінова сіль естеру моно/діалкілполіглікольетерортофосфорної кислоти, лігнінсульфонати або діоктилсульфосукцинат, 2. катіонантивні, такі як хлорид цетитриметиламонію, 3. амфолітичні, такі як ди-Nа-N-лаурил-β-імінодипропіонат або лецитин, 4. неіоногенні, наприклад, поліоксиетильована рицинова олія, поліоксиетильований сорбітан-моноолеат, сорбітан-моностеарат, етиловий спирт, гліцеринмоностеарат, поліоксиетиленстеарат, алкілфенолполігліколевий етер, Pluronic®. Як протиспінювачі використовують переважно сполуки на основі силікону, наприклад, диметікон або симетікон. Як інші допоміжні засоби можуть бути названі наведені вище сполуки. Переважними є суспензії і пасти, причому останні - з низькою в'язкістю. Під пастами маються на увазі зазвичай суспензії з відповідно вищою в'язкістю. Суспензії і пасти вводяться переважно орально. Відповідні винаходові композиції містять активну речовину триазинон у концентрації від 0,1 до 30 % (м/о), відповідно від 1 до 300 мг/мл, переважно 2-25 % (м/о), відповідно 20-250 мг/мл, особливо переважно 3-15 % (м/о), відповідно 30-150 мг/мл, зокрема 3-7 % (м/о), відповідно 30 70 мг триазинону в 1 мл. Внаслідок поганої розчинності триазинонів вони часто перебувають у відповідних винаходові композиціях у вигляді тонкодисперсного порошку. При цьому диспергований триазинон має розміри частинок (виміряні методом лазерної дифракції за допомогою Malvern Mastersizer® 2000) d(v,90) ≤ 30 мкм, переважно d(v,90) ≤ 20 мкм, особливо переважно d(v,90) ≤ 10 мкм, і цілком особливо переважно d(v,90) ≤ 7 мкм. У смислі цього винаходу позначення d(v,90) означає об'ємний розподіл розмірів частинок, при якому 90 % усіх частинок мають розмір (діаметр), менший або рівний вказаному значенню. Зазвичай цей параметр позначають як d(90), одначе для чіткішого підкреслення того факту, що йдеться про об'ємний розподіл розмірів частинок, може бути вибране більш точне позначення d(v,90). Наведені тут розміри частинок вимірювали методом лазерної дифракції за допомогою приладу Mastersizer 2000 (Dispergiereinheit Hydro 2000G) фірми Malvern і визначали оціночний модуль фраунгоферовської дифракції, оскільки показники заломлення частинок активної речовини не відомі. При цьому потрібну кількість пробного розчину попередньо з перемішування диспергували з 2-3 мл диспергувального середовища (0,1 % водний розчин сульфосукцинату діоктилнатрію). Потім дисперсію з перемішуванням (300 об/хв) і циркуляцією (900 об/хв) подавали до диспергувального блоку приладу і здійснювали вимірювання. Обробне програмне забезпечення видавало розміри частинок у вигляді значень d(0.5), d(0.9) і т.д. Ці сполуки заліза містяться у оральних композиціях для профілактики станів дефіциту заліза у великих підприємствах з розведення тварин зазвичай у концентраціях від 100 мг до 200 мг активного заліза у одиничній дозі для одноразового чи багаторазового введення. У розчинах для пиття для постачання заліза у великих підприємствах з птахівництва кількість може бути також меншою, ніж 100 мг активного заліза у одиничній дозі. У відповідних винаходові композиціях сполуки заліза містяться зазвичай у концентраціях від 10 %(м/о) до 30 % (м/о) активного заліза, відповідно 100-300 мг активного заліза у 1 мл, переважно 11,4 % (м/о) - 25 % м/о, відповідно 114 мг - 250 мг активного заліза у 1 мл, одначе особливо переважно 20 % м/о - 25 % м/о, відповідно 200 мг - 250 мг активного заліза у 1 мл композиції. Активним залізом називають процентний вміст заліза, що міститься у формі 9 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 комплексних сполук заліза у композиції. Сполуки заліза, як правило, перебувають у композиціях розчиненими або колоїдально розчиненими. Тонкодисперсні сполуки заліза у відповідних винаходові композиціях є менш переважними. Перевагу мають відповідні винаходові композиції "на основі води". Це означає, що вони містять, як правило, 10-90 мас. %, переважно 20-80 мас. %, особливо переважно 30 - 50 мас. % води. Композиції можуть містити також інші вказані вище змішувані з водою розчинники. Ними можуть бути, наприклад, переважно багатоатомні аліфатичні спирти, такі як етиленгліколь, діетиленгліколь, триетиленгліколь, пропіленгліколь і гліцерин, з яких особливо переважним є пропіленгліколь. Такі змішувані з водою розчинники присутні у концентраціях від 1 до 45 мас. %, переважно 1-20 мас. %, особливо переважно 5-10 мас. %. Перевагою додавання таких багатоатомних аліфатичних спиртів є також те, що знижується точка замерзання композиції. Вводжувана за один раз кількість композиції залежить від того, скільки триазинону і заліза має бути введено. При цьому намагаються варіювати порівняно невеликі, придатні для легкого перорального введення об'єми в залежності від виду тварин, наприклад, для молочних поросят ця кількість становить від 0,3 до 2 мл, переважно 0,5-1 мл. Відповідні винаходові композиції мають бути придатними для легкого введення, наприклад, звичайними допоміжними засобами, такими як шприци, аплікатори чи впорскувальні пістолети, і для цього повинні мати рідку, злегка згущену або злегка пастоподібну консистенцію, яка характеризується в'язкістю - визначеною шляхом обчислення середнього із значень в'язкості, -1 -1 виміряних при температурі 20 °C при швидкостях зсуву 128 с і 256 с за допомогою побудованого за принципом конус/пластина реометра (Thermo Scientific RheoStress 600; Kegeldurchmesser 35°; Kegelwinkel 4°; Constant Rate Modus) - у діапазоні від 10 до 2500 мПас, переважно 10-2500 мПас, переважно у діапазоні 20-1500 мПас, особливо переважно у діапазоні 50-500 мПас і цілком особливо переважно між 20 і 250 мПас. Для встановлення бажаного діапазону в'язкості відповідні винаходові композиції містять у разі потреби відповідні вказані вище речовини (згущувачі). Зазвичай відповідні винаходові композиції мають значення рН від 3 до 8, переважно 4-7, особливо переважно 4-6. Приклади підходящих речовин для регулювання значення рН уже були наведені вище. Для встановлення значення рН використовують переважно органічні кислоти, такі як лимонна кислота чи винна кислота, мінеральні кислоти, такі як соляна кислота, переважно розведена соляна кислота, наприклад, 0,1n НСІ або основи, такі як розчин їдкого натру (наприклад 1N-NaOH). Крім того, відповідні винаходові композиції можуть містити вказані вище консерванти у разі потреби у комбінації із так званими синергістами. Концентрація консервантів становить зазвичай від 0,01 до 5 мас. % і зокрема 0,05 - 1 мас. %. Як оксиданти у вказаних композиціях у разі потреби можуть бути використані переважно ВНА або ВНТ. Консерванти можуть бути використані для достатнього консервування окремо або у комбінації з так званими синергістами. Синергісти, такі як лимонна кислота, винна кислота, аскорбінова кислота або натрієва сіль едитинової кислоти, використовують зазвичай у концентраціях 0,01 - 1 мас. %, зокрема 0,05 - 0,15 мас. %. Відповідні винаходові композиції у разі потреби можуть містити звичайні протиспінювачі у концентрації від 0,01 до 1 мас. %. Відповідні винаходові композиції виготовляють переважно таким чином: у розчиннику, переважно у воді, попередньо розчиняють або диспергують у разі потреби допоміжні і додаткові засоби, такі як агенти розчинення, консерванти, антиоксиданти і регулятори в'язкості. У переважній формі виконання способу у другій стадії до цього попереднього розчину вносять триазинон у формі попередньо приготовленого дисперсійного концентрату і за допомогою потужного гомогенізувального пристрою гомогенізують до отримання тонкої суспензії. Після цього до дисперсії вносять сполуку заліза, переважно у формі порошку, і знову гомогенізують. У останній стадії шляхом додавання придатного регулятора встановлюють бажане значення рН. У разі потреби окремі або усі допоміжні і/або додаткові засоби можуть бути додані після останньої стадії гомогенізації; це може бути рекомендовано у разі певних згущувачів, структура яких руйнується під час гомогенізації. Відповідні винаходові композиції придатні для комбінованого подолання кокцидіозу і станів дефіциту заліза, зокрема у тварин. За допомогою композицій тваринам можуть бути просто одночасно введені ефективні проти кокцидій триазинони і залізо. Композиції можуть бути використані при утриманні і розведенні корисних, племінних, лабораторних, дослідних і любительських тварин. Спектр дії триазинонів в принципі добре відомий. Як кокцидії можуть бути зокрема названі: 10 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 55 Mastigophora (Flagellata), такі як, наприклад, Trypanosomatidae, наприклад, Trypanosoma brucei, Т. gambiense, T. rhodesiense, Т. congolense, Т. cruzi, Т. evansi, Т. equinum, Т. lewisi, Т. percae, Т. simiae, Т. vivax, Leishmania brasiliensis, L. donovani, L. tropica, такі як, наприклад, Trichomonadidae, наприклад, Giardia lamblia, G. canis. Sarcomastigophora (Rhizopoda), такі як Entamoebidae, наприклад, Entamoeba histolytica, Hartmanellidae, наприклад, Acanthamoeba sp., Hartmanella sp. Apicomplexa (Sporozoa), такі як Eimeridae, наприклад, Eimeria acervulina, E. adenoides, E. alabahmensis, E. anatis, E. anseris, E. arloingi, E. ashata, E. auburnensis, E. bovis, E. brunetti, E. canis, E. chinchillae, E. clupearum, E. columbae, E. contorta, E. crandalis, E. debliecki, E. dispersa, E. ellipsoidales, E. falciformis, E. faurei, E. flavescens, E. gallopavonis, E. hagani, E. intestinalis, E. iroquoina, E. irresidua, E. labbeana, E. leucarti, E. magna, E. maxima, E. media, E. meleagridis, E. meleagrimitis, E. mitis, E. necatrix, E. ninakohlyakimovae, E. ovis, E. parva, E. pavonis, E. perforans, E. phasani, E. piriformis, E. praecox, E. residua, E. scabra, E. spec, E. stiedai, E. suis, E. tenella, E. truncata, E. truttae, E. zuernii, Globidium spec, Isospora belli, I. canis, I. felis, I. ohioensis, I. rivolta, I. spec, I. suis, Neospora caninum, N. hugesi, Cystisospora spec, Cryptosporidium spec. Таки як Toxoplasmadidae, наприклад, Toxoplasma gondii, такі як Sarcocystidae, наприклад, Sarcocystis bovicanis, S. bovihominis, S. neurona, S. ovicanis, S. ovifelis, S spec, S. suihominis такі як Leucozoidae, наприклад, Leucozytozoon simondi, такі як Plasmodiidae, наприклад, Plasmodium berghei, P. falciparum, P. malariae, P. ovale, P. vivax, P. spec, такі як Piroplasmea, наприклад, Babesia argentina, B. bovis, B. canis, B. spec, Theileria parva, Theileria spec, такі як Adeleina, наприклад, Hepatozoon canis, H. spec. Крім того Myxospora і Microspora, наприклад, Glugea spec.Nosema spec. Крім того Pneumocystis carinii, а також Ciliophora (Ciliata) такі як, наприклад, Balantidium coli, Ichtiophthirius spec, Trichodina spec, Epistylis spec. Цілком особливо слід виділити такі роди і види найпростіших, які у разі свиней ведуть до субклінічних або клінічних інфекцій, зокрема: Eimeria debliecki, Ε. suis, E. scabra, Ε. perminuta, Ε. spinosa, Ε. polita, Ε. роrсі, Ε. neodebliecki, Isospora suis, Cryptosporidium, Toxoplasma gondii, Sarcocystis miescheriana, S. suihominis, Babesia trautmanni, B. perroncitoi, Balantidium coli. До корисних і племінних тварин належать ссавці, такі як, наприклад, корови, коні, вівці, свині, кози, верблюди, водяні буйволи, віслюки, кролики, лані, олені, хутрові тварини, такі як, наприклад, норки, шиншили, єноти, птахи, такі як, наприклад, кури, гуси, індики, качки, голуби, страуси, птахи для домашнього і зоопаркового утримання. Крім того, сюди належать також корисні і декоративні риби. Особливо виділити слід свиней, корів, овець і собак усіх видів, підвидів і порiд. До лабораторних і дослідних тварин належать миші, пацюки, морські свинки, хом'яки, собаки і коти. До любительських тварин належать собаки і коти. Особливо доцільним є застосування для свиней. Відповідні винаходові композиції застосовують переважно для молодих тварин, зокрема невдовзі після народження, переважно для молочних поросят. Відповідні винаходові композиції (комбінований препарат залізо/триазинон) застосовують зазвичай лише один раз. Особливо переважні відповідні винаходові композиції уможливлюють оральне введення поросятам таким чином, що може бути забезпечене достатнє постачання поросят залізом у перші чотири тижні життя шляхом одноразового введення 0,7 - 1,3 мл, переважно 0,7 - 1,0 мл композиції навіть на третій день після народження, причому показником достатнього постачання може вважатися значення гемоглобіну щонайменше 8 г/100 мл крові, переважно понад 9 г/100 мл крові. Додатково завдяки триазиноновій складовій забезпечується ефективне подолання кокцидій. Відповідні винаходові композиції можуть містити інші активні речовини чи компоненти окремо або у комбінації, наприклад, структурні складові, до яких належать, наприклад, вітаміни, мінеральні речовини і фосфорні сполуки, що стимулюють обмін речовин і імунітет: Вітаміни, такі як вітамін Е, вітаміни серії В, такі як вітамін В12, вітамін С. Мінеральні речовини, переважно солі кальцію або магнію, зокрема наприклад глюконат кальцію, глюкогептаноат кальцію, сахарат кальцію. Фосфорні сполуки, зокрема фармакологічно переносні органічні похідні фосфорної кислоти, придатні як стимулятори обміну речовин і тонізуючі засоби. Як переважні приклади можуть бути названі уже здавна відомі сполуки толдімфос i зокрема бутафосфан. Предмет і переважні форми винаходу: 1. Композиція, що містить триазинони формул (І) або (II) 11 UA 97985 C2 5 10 15 20 25 30 35 40 45 50 або де 1 3 3 R означає R -SO2- або R -S-, 2 R означає алкіл, алкокси, галоген або SO2N(CH3)2,a 3 R означає галогеналкіл 4 5 R і R незалежно один від іншого означають водень або хлор, а 6 R означає фтор або хлор, або їх фізіологічно переносні солі і сполуки Fe(2+) або Fe(3+), вибрані із групи, що включає: (a) солі Fe(ll) карбонових кислот, комплексні сполуки Fe(ll)-карбонових кислот і хелатні комплекси Fe(ll) з амінокислотами (b) солі Fe(lll) карбонових кислот, комплексні сполуки Fe(lll)-карбонових кислот і хелатні комплекси Fe(lll) з амінокислотами і (c) комплексні сполуки багатоатомних полісахаридів з Fe(lll). 3. Композиція згідно з пунктом 1, що містить від 1 до 30 % (м/о), переважно 3 - 7 % (м/о) триазинону. 4. Композиція згідно з одним із попередніх пунктів, причому диспергований триазинон має розміри частинок d(v,90) ≤ ЗО мкм, переважно d(v,90) ≤ 20 мкм, особливо переважно d(v,90) ≤ 10 мкм. 5. Композиція згідно з одним із попередніх пунктів, у якій концентрація сполуки заліза становить від 10 %(м/о) до 30 % (м/о) активного заліза, переважно 11,4 % (м/о) - 25 % м/о, одначе особливо переважно 20 % м/о - 25 % м/о. 6. Композиція згідно з одним із попередніх пунктів, що має в'язкість, визначену шляхом -1 -1 утворення середнього із значень, виміряних при швидкостях зсуву 128 с і 256 с за допомогою побудованого за принципом конус/пластина реометра, у діапазоні від 10 до 2500 мПас, переважно у діапазоні 20-1500 мПас. 7. Композиція згідно з пунктом 1 на основі води. 8. Композиція згідно з пунктом 1, що містить щонайменше один багатоатомний аліфатичний спирт. 9. Композиція згідно з одним із попередніх пунктів, що містить багатоядерну Fе(ІІІ)полісахаридну комплексну сполуку групи (с), багатоядерна основа якої складається із βFеО(ОН)-одиниць і яка містить полісахаридну молекулу в іншій координаційній сфері. 10. Композиція згідно з пунктом 8, що містить багатоядерну Fе(ІІІ)-полісахаридну комплексну сполуку, вибрану із групи: Fе(ІІІ)-декстран, Fе(ІІІ)-гідрокси-полімальтоза / Fе(ІІІ)-декстрин і не стехіометрична сполука із багатоядерної одиниці β-FeO(OH) і сахарози та олігосахаридів. 11. Композиція згідно з одним із пунктів 1-7, яка як сполуку заліза групи (b) містить цитрат заліза, переважно амоній-Fе(ІІІ)-цитрат. 12. Композиція згідно з одним із попередніх пунктів, що як триазон містить триазинтріон. 13. Композиція згідно з пунктом 11, що як триазинтріон містить толтразурил, поназурил або толтразурил-сульфоксид. 14. Композиція згідно з одним із пунктів 1-8 і 11-12, що як триазинон містить толтразурил, а як багатоядерну Fе(ІІІ)-полісахаридну комплексну сполуку містить Fe(lІІ)-декстран. 15. Композиція згідно з одним із пунктів 1-10, що як триазинон містить триазиндіон, зокрема клазурил, диклазурил або летразурил. 16. Застосування композиції згідно з одним із попередніх пунктів для виготовлення лікарських засобів. 17. Застосування згідно з пунктом 15 для виготовлення лікарських засобів для одночасного подолання кокцидіозних інфекцій і станів дефіциту заліза. 18. Застосування згідно з пунктом 15 або 16 для виготовлення лікарських засобів для орального введення. 19. Застосування згідно з пунктом 17 для виготовлення лікарських засобів для орального введення молочним поросятам. 12 UA 97985 C2 5 10 20. Застосування згідно з одним із пунктів 17 або 18 для виготовлення лікарських засобів для орального лікування поросят у проміжку часу від народження до 10 днів після народження, переважно у проміжку часу від народження до 3 днів після народження. 21. Композиції згідно з одним із пунктів 1-14, що додатково містять одну чи кілька структурних складових. 22. Композиція згідно з пунктом 20, що додатково містить сіль кальцію чи магнію. 23. Композиція згідно з пунктом 20 або 21, що містить бутафосфан. Наведені нижче приклади мають пояснити винахід, не обмежуючи його. Приклади виготовлення Приклад 1 Застосування Fе(ІІІ)-декстрану у формі порошку 38,4 % м/м Набір для виготовлення 10 л дисперсії Fe-декстран / толтразурил (22,8 % м/о активного заліза + 5 % м/о толтразурилу) для орального введення молочним поросятам Використовувана речовина Толтразурил, суспензійний концентрат (30 %) Пропіонат натрію (консервант) Бензоат натрію (консервант) Пропіленгліколь Безводна лимонна кислота Fе(Іll)-декстран, порошок 38,4 % м/м Вода до 10 л Регулятор(и) в'язкості Загальна маса 15 20 25 30 35 40 45 Маса/г 1666,67 17,00 17,00 1000,00 87,10 5937,50 5138,00 13863,27 По 17,00 г консервантів пропіонату натрію і бензоату натрію зважували у окремій посудині з 1000,00 г розчинника пропіленгліколю і розчиняли з перемішуванням. Усю кількість води заливали у посудину із нержавіючої сталі (Koruma Disho; Maschinen-Type: DH V100/45). В залежності від потреби і бажаної в'язкості кінцевого продукту до цієї кількості води може бути доданий регулятор в'язкості (так званий згущувач). У цьому прикладі 1 від нього відмовилися. Пропіленглікольну маточну суміш виливали у посудину із нержавіючої сталі і гомогенізували з перемішуванням (20-40 хв). У наступній стадії попередньо відважену кількість 1666,67 г дисперсійного концентрату 30 % толтразурилу додавали до суміші, перемішували протягом 3040 хв і одночасно гомогенізували циркуляційним гомогенізатором (система ротор-статор) при швидкості 2500 об/хв протягом 20 хв. Вказані значення часу перемішування і гомогенізації можуть бути збільшені або зменшені, в залежності від зовнішнього вигляду суспензії. Бажано підтримувати температуру суміші 20-30 °C за допомогою підходящої охолоджувальної системи. У наступній стадії 6015,83 г порошку Fе(ІІІ)-декстрану кількома порціями додавали до дисперсії. Під час додавання суміш слід постійно перемішувати і гомогенізувати за допомогою циркуляційного гомогенізатора зі швидкістю 2500 об/хв. При цьому температуру підтримували на рівні 20-30 °C шляхом активування системи охолодження. Після повного додавання порошку Fе(ІІІ)-декстрану до суміші додавали лимонну кислоту (85,90 г) і розчиняли. Значення рН встановлювалося на рівні 4,1-4,4. Після введення усіх складових перемішували ще протягом 20 хвилин і одночасно гомогенізували при швидкості 2500 об/хв. Під час цієї стадії перемішування шляхом охолодження температуру дисперсії підтримували на рівні кімнатної. Готову дисперсію крізь сито з розміром вічок 0,1 мм переводили із посудини із нержавіючої сталі у підходящий збірник. Значення рН після деякого часу зберігання зростало до рівня 4,8-5,2. Для визначення якості дисперсії залучали значення рН, розподіл розмірів частинок (виміряний методом лазерної дифракції за допомогою приладу Malvern Mastersizer 2000) і в'язкість. В'язкість вимірювали за допомогою побудованого за принципом конус/пластина -1 -1 приладу при швидкостях зсуву 128 с і 256 с (RheoStress 600; Thermo Haake). Середнє значення виміряних значень в'язкості використовували як опорне значення. Ці значення в'язкості виявилися придатними для характеризування опору текучості таких суспензій при проходженні крізь впорскувальний пістолет. При цьому принципово слід намагатися отримати якомога тонше розподілену дисперсію для досягнення високої біопридатності активних речовин. Виготовлена описаним вище чином суспензія мала такі дані: 13 UA 97985 C2 Процентний Процентний Розмір Розмір В’язкість рН після рН після вміст вміст Сполука заліза частинок частинок частинок частинок / мПас виготовлення зберігання d(v,50)/мкм d(v,90)/мкм
ДивитисяДодаткова інформація
Назва патенту англійськоюFormulations containing triazinones and iron for controlling coccidia infections and iron deficiencies
Автори англійськоюHofmann, Stefan, Heep, Iris, Mundt, Hans-Christian, Torres Islas, Juan, Agustin
Назва патенту російськоюКомпозиция, содержащая триазиноны и железо, для преодоления кокцидиозных инфекций и дефицита железа
Автори російськоюХофманн Штефан, Хээп Ирис, Мундт Ханс-Кристиан, Торрес Ислас Хуан Агустин
МПК / Мітки
МПК: A61P 33/02, A61P 7/06, A61K 33/26, A61K 31/53, A61K 31/295
Мітки: триазинони, заліза, подолання, залізо, композиція, кокцидіозних, інфекцій, містить, дефіциту
Код посилання
<a href="https://ua.patents.su/23-97985-kompoziciya-shho-mistit-triazinoni-i-zalizo-dlya-podolannya-kokcidioznikh-infekcijj-ta-deficitu-zaliza.html" target="_blank" rel="follow" title="База патентів України">Композиція, що містить триазинони і залізо, для подолання кокцидіозних інфекцій та дефіциту заліза</a>
Попередній патент: Пристрій і спосіб відновної обробки для одержання металевого заліза
Наступний патент: Курильний виріб з контрольованим ароматовивільненням
Випадковий патент: Спосіб виготовлення матів із очерету












