Аміди карбонових кислот
Номер патенту: 77684
Опубліковано: 15.01.2007
Автори: Хорват Чілла, Ваго Іштван, Колок Шандор, Кешеру Дьйордь, Домані Дьйордь, Біелік Аттіла, Борза Іштван, Фаркаш Шандор, Ігнацне Сендреі Дьйордь, Ковачне Бозо Ева, Бартане Салаі Гішелла, Надь Йожеф
Формула / Реферат
1. Амідні похідні карбонових кислот формули (І)
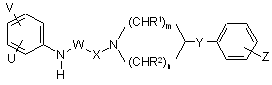 (I),
(I),
де: обидві -(CHR1)m- і -(CHR2)n- є -CH2-CH2-групами,
суміжні V і U групи утворюють разом одна з одною і з одним або більше ідентичними або різними додатковими гетероатомоми і -CH= і/або -CH2-групами необов'язково заміщене 4-7-членне гомо- або гетероциклічне кільце, переважно морфолін, пірол, піролідин, оксо- або тіоксопіролідин, піразол, піразолідин, імідазол, імідазолідин, оксо- або тіоксоімідазол або імідазолідин, 1,4-оксазин, оксазол, оксазолідин, оксо- або тіоксооксазолідин або 3-оксо-1,4-оксазинове кільце,
Х є -CO-групою,
W є -CO-, -CH2- або -СН(-алкільною) групою, де алкіл є C1-C4 алкільною групою,
Y є атомом кисню, так само як C1-C4 алкіленом, C2-C4 алкініленом, циклоалкіленом, амінокарбонілом, -NH-, -N(алкіл)-, -CH2O-, -СН(ОН)-, -ОСН2-групою, де алкіл є C1-C4 алкільною групою,
Z є воднем або атомом галогену, нітро, аміно, C1-C4 алкілом, C1-C4 алкокси, ціано, трифторметилом, гідроксильною або карбоксильною групою і оптичні антиподи або рацемати та/або їхні фармацевтично прийнятні солі, утворені з кислотами й основами.
2. Сполуки за п. 1, які відрізняються тим, що обидві -(CHR1)m- i -(CHR2)n- є -CH2-CH2-групами, Х означає -CO-групу і W означає -CH2-групу, і V, U, Y і Z мають значення, подані для сполуки формули (І).
3. Сполуки за п. 1, які відрізняються тим, що обидві -(CHR1)m- і -(CHR2)n- є -CH2-CH2-групами, обидва Х і W означають -CO-групи, і V, U, Y і Z мають значення, подані для сполук формули (І).
4. Сполука за п. 1, яка відрізняється тим, що вибрана з наступної групи амідних похідних карбонової кислоти:
2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідро-1Н-індол-5-іл)-ацетамід,
2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідро-1Н-бензимідазол-5-іл)-ацетамід,
2-(4-бензилпіперидин-1-іл)-2-оксо-N-(2-оксо-2,3-дигідро-1Н-індол-5-іл)-ацетамід,
2-(4-бензилпіперидин-1-іл)-2-оксо-N-(2-оксо-2,3-дигідро-1Н-бензимідазол-5-іл)-ацетамід,
2-(4-бензилпіперидин-1-іл)-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
5-{2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксоетиламіно}-1,3-дигідробензо-імідазол-2-он,
6-{2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксоетиламіно}-3Н-бензоксазол-2-он,
2-[4-(4-метилбензил)-піперидин-1-іл]-2-оксо-N-(3-оксо-3,4-дигідро-2Н-бензо[1,4]оксазин-7-іл)-ацетамід,
2-[4-[4-метилбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідро-1Н-індол-5-іл)-ацетамід,
2-[4-(4-хлорфенокси)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідро-1Н-бензимідазол-5-іл)-ацетамід,
2-[4-(4-хлорфенокси)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
2-[4-(4-хлорбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
2-[4-(4-хлорбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідро-1Н-бензимідазол-5-іл)-ацетамід,
2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-2-(4-п-толілоксипіперидин-1-іл)-ацетамід,
2-оксо-N-(2-оксо-2,3-дигідро-1Н-бензимідазол-6-іл)-2-(4-п-толілоксипіперидин-1-іл)-ацетамід,
2-[4-(4-хлорбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідро-1Н-індол-5-іл)-ацетамід,
6-[2-(4-бензилпіперидин-1-іл)-2-оксоетиламіно]-3Н-бензоксазол-2-он,
2-(4-бензилпіперидин-1-іл)-N-(2-меркапто-3Н-бензимідазол-5-іл)-2-оксоацетамід,
2-(4-бензилпіперидин-1-іл)-2-оксо-N-(2-оксо-2,3-дигідробензотіазол-6-іл)-ацетамід,
2-[4-(4-фторбензил)-піперидин-1-іл]-N-(2-меркапто-3Н-бензимідазол-5-іл)-2-оксоацетамід,
2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензотіазол-6-іл)-ацетамід,
2-оксо-N-(2-оксо-2,3-дигідробензотіазол-6-іл)-2-(4-п-толілоксипіперидин-1-іл)-ацетамід,
N-(2-меркапто-3Н-бензимідазол-5-іл)-2-(4-п-толілоксипіперидин-1-іл)-2-оксоацетамід,
2-[4-(4-метилбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл]-ацетамід,
2-[4-(4-метоксибензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
2-[4-(3-метоксибензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
2-[4-(3-метилбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
2-[4-(4-ціанобензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
2-[4-(3-фторбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
2-[4-(2,4-дифторбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідро-бензоксазол-6-іл)-ацетамід,
6-{2-[4-(4-метилбензил)-піперидин-1-іл]-2-оксоетиламіно}-3Н-бензоксазол-2-он,
2-[4-(3,4-дифторбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід,
2-[4-(4-метилбензил)-піперидин-1-іл)-2-оксо-N-(2-оксо-1,2,3,4-тетрагідрохінолін-6-іл)-ацетамід,
2-[4-(4-метилбензил)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензотіазол-6-іл)-ацетамід,
2-[4-(4-хлорфенокси)-піперидин-1-іл]-2-оксо-N-(2-оксо-2,3-дигідробензотіазол-6-іл)-ацетамід,
2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-2-(4-п-толілоксипіперидин-1-іл)-ацетамід,
і/або їхніх рацематів, оптичних антиподів і/або фармацевтично прийнятних солей, утворених з кислотами або основами.
5. Фармацевтична композиція, що має ефект специфічного антагоніста NMDA NR2B підтипу, яка відрізняється тим, що містить біологічно ефективну дозу похідної аміду карбонової кислоти формули (І), де значення R1, R2, V, U, W, X, Y, Z, m i n є такими, як подано в пункті 1, і/або її рацематів, оптичних антиподів і/або фармацевтично прийнятних солей, утворених з кислотами або основами, як активний інгредієнт, і носії, наповнювачі та подібні до них добавки, звичайно застосовувані у фармацевтиці.
6. Спосіб одержання похідних амідів карбонових кислот формули (І),
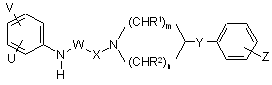 , (I)
, (I)
де значення R1, R2, V, U, W, X, Y, Z, m i n є такими, як подано в пункті 1, і/або їхніх рацематів, оптичних антиподів і/або фармацевтично прийнятних солей, утворених з кислотами або основами, як активного інгредієнта, який відрізняється тим, що
а) карбонову кислоту формули (II)
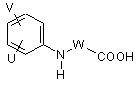 , (II)
, (II)
де значення U, V і W є такими, як подано для формули (І), або її реакційноздатну похідну піддають взаємодії з аміном формули (III)
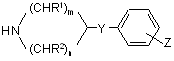 , (III)
, (III)
де значення R1, R2, Y, Z, n i m є такими, як подано раніше для сполук формули (І), або
b) для одержання сполук формули (І), що мають -CO-групу в положенні W, де значення R1, R2, Y, Z, U, V, X, n i m є такими, як подано раніше для сполук формули (І), карбонову кислоту формули (IV)
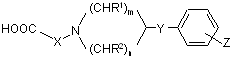 , (IV)
, (IV)
де значення X, R1, R2, Y, Z, n i m є такими, як подано раніше для сполук формули (І), або її реакційноздатну похідну піддають взаємодії з аміном формули (V)
 , (V)
, (V)
де значення U і V є такими, як подано раніше для сполук формули (І),
або
c) для одержання сполук формули (I), що мають -CH2- або -CH(-алкільну)групу в положенні W, де алкіл є С1-C4 алкільною групою і значення R1, R2, Y, Z, U, V, X, n i m є такими, як подано раніше для сполук формули (І), галоїдну похідну сполуки формули (VII)
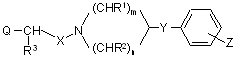 , (VII)
, (VII)
де Q є атомом галогену, R3 є атомом водню або С1-C4 алкільною групою і X, R1, R2, Y, Z, n i m є такими, як подано вище для сполук формули (І), піддають взаємодії з аміном формули (V):
 ,(V)
,(V)
де значення U і V є такими, як визначено раніше для сполук формули (І), або
d) вторинний амін формули (III)
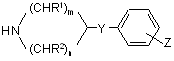 , (III)
, (III)
де R1, R2, m, n, Y і Z мають ті самі значення, як подано для сполук
формули (І), піддають взаємодії з етилоксалілхлоридом у присутності основи на твердій підкладці в дихлорметані,
отриманий ефір формули (VIII)
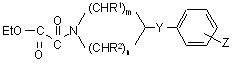 , (VIII)
, (VIII)
де R1, R2, m, n, Y і Z мають ті самі значення, як подано для сполук формули (І), підлуговують сильноосновною іонообмінною смолою в етанолі й отриманий оксаламід кислоти формули (IX):
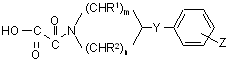 , (IX)
, (IX)
де R1, R2, m, n, Y і Z мають ті самі значення, як подано для сполук формули (І), піддають взаємодії з амідом формули (V).
 , (V)
, (V)
де значення U і V є такими, як подано раніше для сполук формули (І), у суміші розчинників дихлорметан/диметилформамід у присутності 1-[3-(диметиламіно)-пропіл]-3-етилкарбодііміду,
і перетворюють отримані сполуки формули (І), де R1, R2, Y, Z, U, V, X, W, n i m є такими, як описано вище, в даному випадку на іншу сполуку формули (І) шляхом уведення додаткових замісників і/або модифікування, і/або видалення наявних замісників, і/або шляхом утворення солей з кислотами, і/або вивільнення похідної аміду карбонової кислоти формули (І) з отриманої кислотно-адитивної солі шляхом обробки основою, і/або вільна похідна аміду карбонової кислоти формули (І) може бути перетворена на сіль шляхом обробки основою і/або розділена на її оптичні антиподи.
7. Спосіб за п. 6, який відрізняється тим, що утворення реакційноздатної похідної карбонових кислот формули (II) і (IV), де U, V, W, або X, R1, R2, Y, Z, n i m є такими, як визначено для сполук формули (І), відповідно, здійснюють при використанні гексафторфосфату O-бензотриазол-1-іл-N,N,N',N'-тетра-метилуронію.
8. Спосіб одержання фармацевтичної композиції, що має ефект специфічного антагоніста NMDA NR2B підтипу, який відрізняється тим, що змішують похідну аміду карбонової кислоти формули (І), де значення R1, R2, V, U, W, X, Y, Z, m i n є такими, як визначено в п. 1, і/або її рацемати, оптичні антиподи і/або фармацевтично прийнятні солі, утворені з кислотами або основами, з носіями, наповнювачами та подібними до них добавками, звичайно застосовуваними у фармацевтиці.
9. Спосіб лікування і полегшення симптомів таких захворювань ссавців, включаючи людину: травматичне пошкодження мозку або спинного мозку, вірус людського імунодефіциту (ВІЛ), пов'язаний з пошкодженням нейрона, аміотрофічний бічний склероз, стійкість до і/або залежність від опіоїдного лікування болю, синдром залежності, наприклад, від алкоголю, опіоїдів або кокаїну, ішемічне порушення ЦНС, хронічне нейродегенеративне захворювання, таке як хвороба Альцгеймера, хвороба Паркінсона, хвороба Хантингтона, біль і хронічний хворобливий стан, такий як невропатичний біль або біль, пов'язаний з раком, епілепсія, занепокоєння, депресія, мігрень, психоз, м'язова судома, деменція різноманітного походження, гіпоглікемія, дегенеративна хвороба сітківки, глаукома, астма, шум у вухах, аміноглікозидна, пов'язана із застосуванням антибіотика, втрата слуху, який відрізняється тим, що включає введення ефективної кількості/кількостей похідної аміду карбонової кислоти формули (І), де значення R1, R2, V, U, W, X, Y, Z, m i n є такими, як визначено в пункті 1, і/або її рацематів, оптичних антиподів і/або фармацевтично прийнятних солей, утворених з кислотами або основами, як таких або у поєднанні з носіями, наповнювачами і подібними до них добавками, звичайно застосовуваними у фармацевтиці для лікування ссавців.
Текст
1. Амідні похідні карбонових кислот формули (І) (19) (21) 2004021342 (22) 23.07.2002 (24) 15.01.2007 (86) PCT/HU02/00071, 23.07.2002 (31) P 0103055 (32) 24.07.2001 (33) HU (31) P 0202213 (32) 10.07.2002 (33) HU (46) 15.01.2007, Бюл. № 1, 2007 р. (72) Домані Дьйордь , HU, Хорват Чілла , HU, Фаркаш Шандор , HU, Бартане Салаі Гішелла, HU, Надь Йожеф , HU, Колок Шандор , HU, Ковачне Бозо Ева, HU, Борза Іштван , HU, Ваго Іштван , HU, Біелік Аттіла , HU, Ігнацне Сендреі Дьйордь, HU, Кешеру Дьйордь , HU (73) РІХТЕР ГЕДЕОН ВЕДЬЄСЕТІ ДЬЯР РТ., HU (56) EP 0 824 098 A 18.02.1998 US 6 048 900 A 11.04.2000 FR 2 672 286 A 07.08.1992 EP 0 648 744 A 19.04.1995 WO 97 23216 A 03.07.1997 B. L. CHENARD ET AL.: "Separation of 'alpha'1 adrenergic and N-methyl-D-aspartate antagonist activity in a series of ifenprodil compounds" J. MED. CHEM., vol. 34, no. 10, 1991 C. DOMINGUEZ ET AL.: "Designand syntesis of potent and selective 5,6-fused heterocyclic thrombin inhibitors" BIOORG. MED. CHEM. LETT., vol. 9, 1999 2 3 77684 4 2. Сполуки за п.1, які відрізняються тим, що оби2-[4-(3-метоксибензил)-піперидин-1-іл]-2-оксо-N-(2дві -(CHR1)m- i -(CHR2)n- є -CH2-CH2-групами, Х оксо-2,3-дигідробензоксазол-6-іл)-ацетамід, означає -CO-групу і W означає -CH2-групу, і V, U, Y 2-[4-(3-метилбензил)-піперидин-1-іл]-2-оксо-N-(2і Z мають значення, подані для сполуки формули оксо-2,3-дигідробензоксазол-6-іл)-ацетамід, (І). 2-[4-(4-ціанобензил)-піперидин-1-іл]-2-оксо-N-(23. Сполуки за п.1, які відрізняються тим, що обиоксо-2,3-дигідробензоксазол-6-іл)-ацетамід, дві -(CHR1)m- і -(CHR2)n- є -CH2-CH2-групами, обид2-[4-(3-фторбензил)-піперидин-1-іл]-2-оксо-N-(2ва Х і W означають -CO-групи, і V, U, Y і Z мають оксо-2,3-дигідробензоксазол-6-іл)-ацетамід, значення, подані для сполук формули (І). 2-[4-(2,4-дифторбензил)-піперидин-1-іл]-2-оксо-N4. Сполука за п.1, яка відрізняється тим, що виб(2-оксо-2,3-дигідро-бензоксазол-6-іл)-ацетамід, рана з наступної групи амідних похідних карбоно6-{2-[4-(4-метилбензил)-піперидин-1-іл]-2вої кислоти: оксоетиламіно}-3Н-бензоксазол-2-он, 2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксо-N-(22-[4-(3,4-дифторбензил)-піперидин-1-іл]-2-оксо-Nоксо-2,3-дигідро-1Н-індол-5-іл)-ацетамід, (2-оксо-2,3-дигідробензоксазол-6-іл)-ацетамід, 2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксо-N-(22-[4-(4-метилбензил)-піперидин-1-іл)-2-оксо-N-(2оксо-2,3-дигідробензоксазол-6-іл)-ацетамід, оксо-1,2,3,4-тетрагідрохінолін-6-іл)-ацетамід, 2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксо-N-(22-[4-(4-метилбензил)-піперидин-1-іл]-2-оксо-N-(2оксо-2,3-дигідро-1Н-бензимідазол-5-іл)-ацетамід, оксо-2,3-дигідробензотіазол-6-іл)-ацетамід, 2-(4-бензилпіперидин-1-іл)-2-оксо-N-(2-оксо-2,32-[4-(4-хлорфенокси)-піперидин-1-іл]-2-оксо-N-(2дигідро-1Н-індол-5-іл)-ацетамід, оксо-2,3-дигідробензотіазол-6-іл)-ацетамід, 2-(4-бензилпіперидин-1-іл)-2-оксо-N-(2-оксо-2,32-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-2-(4дигідро-1Н-бензимідазол-5-іл)-ацетамід, п-толілоксипіперидин-1-іл)-ацетамід, 2-(4-бензилпіперидин-1-іл)-2-оксо-N-(2-оксо-2,3і/або їхніх рацематів, оптичних антиподів і/або фадигідробензоксазол-6-іл)-ацетамід, рмацевтично прийнятних солей, утворених з кис5-{2-[4-(4-фторбензил)-піперидин-1-іл]-2лотами або основами. оксоетиламіно}-1,3-дигідробензо-імідазол-2-он, 5. Фармацевтична композиція, що має ефект спе6-{2-[4-(4-фторбензил)-піперидин-1-іл]-2цифічного антагоніста NMDA NR2B підтипу, яка оксоетиламіно}-3Н-бензоксазол-2-он, відрізняє ться тим, що містить біологічно ефекти2-[4-(4-метилбензил)-піперидин-1-іл]-2-оксо-N-(3вну дозу похідної аміду карбонової кислоти фороксо-3,4-дигідро-2Н-бензо[1,4]оксазин-7-іл)мули (І), де значення R1, R2, V, U, W, X, Y, Z, m i n ацетамід, є такими, як подано в пункті 1, і/або її рацематів, 2-[4-[4-метилбензил)-піперидин-1-іл]-2-оксо-N-(2оптичних антиподів і/або фармацевтично прийнятоксо-2,3-дигідро-1Н-індол-5-іл)-ацетамід, них солей, утворених з кислотами або основами, 2-[4-(4-хлорфенокси)-піперидин-1-іл]-2-оксо-N-(2як активний інгредієнт, і носії, наповнювачі та пооксо-2,3-дигідро-1Н-бензимідазол-5-іл)-ацетамід, дібні до них добавки, звичайно застосовувані у 2-[4-(4-хлорфенокси)-піперидин-1-іл]-2-оксо-N-(2фармацевтиці. оксо-2,3-дигідробензоксазол-6-іл)-ацетамід, 6. Спосіб одержання похідних амідів карбонових 2-[4-(4-хлорбензил)-піперидин-1-іл]-2-оксо-N-(2кислот формули (І), V оксо-2,3-дигідробензоксазол-6-іл)-ацетамід, (CHR1 ) m 2-[4-(4-хлорбензил)-піперидин-1-іл]-2-оксо-N-(2Y W N N X Z оксо-2,3-дигідро-1Н-бензимідазол-5-іл)-ацетамід, U (CHR2 ) n H 2-оксо-N-(2-оксо-2,3-дигідробензоксазол-6-іл)-2-(4, (I) п-толілоксипіперидин-1-іл)-ацетамід, де значення R1, R2, V, U, W, X, Y, Z, m i n є такими, 2-оксо-N-(2-оксо-2,3-дигідро-1Н-бензимідазол-6як подано в пункті 1, і/або їхніх рацематів, оптичіл)-2-(4-п-толілоксипіперидин-1-іл)-ацетамід, них антиподів і/або фармацевтично прийнятних 2-[4-(4-хлорбензил)-піперидин-1-іл]-2-оксо-N-(2солей, утворених з кислотами або основами, як оксо-2,3-дигідро-1Н-індол-5-іл)-ацетамід, активного інгредієнта, який відрізняється тим, що 6-[2-(4-бензилпіперидин-1-іл)-2-оксоетиламіно]-3На) карбонову кислоту формули (II) V бензоксазол-2-он, 2-(4-бензилпіперидин-1-іл)-N-(2-меркапто-3НW N бензимідазол-5-іл)-2-оксоацетамід, COOH U H 2-(4-бензилпіперидин-1-іл)-2-оксо-N-(2-оксо-2,3, (II) дигідробензотіазол-6-іл)-ацетамід, де значення U, V і W є такими, як подано для фо2-[4-(4-фторбензил)-піперидин-1-іл]-N-(2-меркаптормули (І), або її реакційноздатну похідну піддають 3Н-бензимідазол-5-іл)-2-оксоацетамід, взаємодії з аміном формули (III) (CHR 1)m 2-[4-(4-фторбензил)-піперидин-1-іл]-2-оксо-N-(2Y оксо-2,3-дигідробензотіазол-6-іл)-ацетамід, HN Z (CHR 2)n 2-оксо-N-(2-оксо-2,3-дигідробензотіазол-6-іл)-2-(4, (III) 1 2 п-толілоксипіперидин-1-іл)-ацетамід, де значення R , R , Y, Z, n i m є такими, як подано N-(2-меркапто-3Н-бензимідазол-5-іл)-2-(4-праніше для сполук формули (І), або толілоксипіперидин-1-іл)-2-оксоацетамід, b) для одержання сполук формули (І), що мають 2-[4-(4-метилбензил)-піперидин-1-іл]-2-оксо-N-(2CO-груп у в положенні W, де значення R1, R2, Y, Z, оксо-2,3-дигідробензоксазол-6-іл]-ацетамід, U, V, X, n i m є такими, як подано раніше для спо2-[4-(4-метоксибензил)-піперидин-1-іл]-2-оксо-N-(2лук формули (І), карбонову кислоту формули (IV) оксо-2,3-дигідробензоксазол-6-іл)-ацетамід, 5 77684 6 метан/диметилформамід у присутності 1-[3Y HOOC N (диметиламіно)-пропіл]-3-етилкарбодііміду, X Z (CHR 2)n , (IV) і перетворюють отримані сполуки формули (І), де де значення X, R1, R2, Y, Z, n i m є такими, як поR1, R2, Y, Z, U, V, X, W, n i m є такими, як описано дано раніше для сполук формули (І), або її реаквище, в даному випадку на іншу сполуку формули ційноздатну похідну піддають взаємодії з аміном (І) шляхом уведення додаткових замісників і/або формули (V) модифікування, і/або видалення наявних замісниV ків, і/або шляхом утворення солей з кислотами, і/або вивільнення похідної аміду карбонової кислоNH U , (V) ти формули (І) з отриманої кислотно-адитивної де значення U і V є такими, як подано раніше для солі шляхом обробки основою, і/або вільна похідсполук формули (І), на аміду карбонової кислоти формули (І) може або бути перетворена на сіль шляхом обробки осноc) для одержання сполук формули (I), що мають вою і/або розділена на її оптичні антиподи. CH2- або -CH(-алкільну)групу в положенні W, де 7. Спосіб за п.6, який відрізняється тим, що утвоалкіл є С1-C4 алкільною групою і значення R1, R2, рення реакційноздатної похідної карбонових кисY, Z, U, V, X, n i m є такими, як подано раніше для лот формули (II) і (IV), де U, V, W, або X, R1, R2, Y, сполук формули (І), галоїдну похідн у сполуки фоZ, n i m є такими, як визначено для сполук формурмули (VII) ли (І), відповідно, здійснюють при використанні (CHR 1) m гексафторфосфату O-бензотриазол-1-іл-N,N,N',N'Y Q CH N тетра-метилуронію. X Z (CHR 2) n R3 , (VII) 8. Спосіб одержання фармацевтичної композиції, де Q є атомом галогену, R3 є атомом водню або що має ефект специфічного антагоніста NMDA 1 2 С1-C4 алкільною групою і X, R , R , Y, Z, n i m є NR2B підтипу, який відрізняє ться тим, що змішутакими, як подано вище для сполук формули (І), ють похідну аміду карбонової кислоти формули (І), піддають взаємодії з аміном формули (V): де значення R1, R2, V, U, W, X, Y, Z, m i n є такими, V як визначено в п.1, і/або її рацемати, оптичні антиподи і/або фармацевтично прийнятні солі, утворені з кислотами або основами, з носіями, наповнюваNH 2 U ,(V) чами та подібними до них добавками, звичайно де значення U і V є такими, як визначено раніше застосовуваними у фармацевтиці. для сполук формули (І), або 9. Спосіб лікування і полегшення симптомів таких d) вторинний амін формули (III) захворювань ссавців, включаючи людину: травма(CHR1)m тичне пошкодження мозку або спинного мозку, Y HN Z вірус людського імунодефіциту (ВІЛ), пов'язаний з (CHR2)n , (III) пошкодженням нейрона, аміотрофічний бічний 1 2 де R , R , m, n, Y і Z мають ті самі значення, як склероз, стійкість до і/або залежність від опіоїдноподано для сполук го лікування болю, синдром залежності, наприформули (І), піддають взаємодії з етилоксалілхлоклад, від алкоголю, опіоїдів або кокаїну, ішемічне ридом у присутності основи на твердій підкладці в порушення ЦНС, хронічне нейродегенеративне дихлорметані, захворювання, таке як хвороба Альцгеймера, хвоотриманий ефір формули (VIII) роба Паркінсона, хвороба Хантингтона, біль і хро(CHR1) m O нічний хворобливий стан, такий як невропатичний Y EtO C N біль або біль, пов'язаний з раком, епілепсія, занеZ C (CHR2) n O , (VIII) покоєння, депресія, мігрень, психоз, м'язова судоде R1, R2, m, n, Y і Z мають ті самі значення, як ма, деменція різноманітного походження, гіпогліподано для сполук формули (І), підлуговують сикемія, дегенеративна хвороба сітківки, глаукома, льноосновною іонообмінною смолою в етанолі й астма, шум у вухах, аміноглікозидна, пов'язана із отриманий оксаламід кислоти формули (IX): застосуванням антибіотика, втрата слуху, який (CHR1) m відрізняє ться тим, що включає введення ефектиO Y HO C N вної кількості/кількостей похідної аміду карбонової Z C (CHR2) n O кислоти формули (І), де значення R1, R2, V, U, W, , (IX) 1 2 X, Y, Z, m i n є такими, як визначено в пункті 1, де R , R , m, n, Y і Z мають ті самі значення, як і/або її рацематів, оптичних антиподів і/або фарподано для сполук формули (І), піддають взаємодії мацевтично прийнятних солей, утворених з кислоз амідом формули (V). V тами або основами, як таких або у поєднанні з носіями, наповнювачами і подібними до них добаN H2 вками, звичайно застосовуваними у фармацевтиці U , (V) для лікування ссавців. де значення U і V є такими, як подано раніше для (CHR 1) m 2 сполук формули (І), у суміші розчинників дихлор Винахід стосується нових похідних амідів карбонових кислот, що є антагоністами NMDA рецеп тора або є проміжними сполуками для їхнього одержання. 7 77684 8 N-Метил-О-аспартат (NMDA) рецептори є ліпіперидиніл]ацетил]аміно]бензойної кислоти. ганд-залежними катіонними каналами, вставлениОксоетиламінові похідні характеризуються як ми в клітинні мембрани нейронів. Надактивація проміжні сполуки для інгібіторів тромбіну [Bioorg. NMDA рецепторів за допомогою глутамату, його Med. Chem. Letters, 9, 925, (1999)]. Публікація не природного ліганду, може призвести до надлишку описує ефект NMD A антагоніста рецептора. кальцію в клітинах. Це запускає каскад внутрішN-(4-бензоїлфеніл)-4-(фенілметил)-1ньоклітинних процесів, що змінює функцію клітини піперидинацетамід наведений [у патенті US й у кінцевому рахунку може призвести до загибелі 6048900] як селективний антагоніст нейропептиднейронів [TINS, 10, 299-302 (1987)]. Антагоністи ного Υ рецептора. NMDA рецепторів можуть бути використані для N-(2-форміл-6-метилфеніл)-4-(фенілметил-1лікування багатьох хвороб, що супроводжуються піперидинацетамід описаний [у патенті AU 639529] надлишковим виділенням глутамату, основного як проміжна сполука для карбостирольної похіднервового трансмітера в центральній нервовій ної, що є корисною як антиаритмік. системі. Аміноацетариліди є також відомими [Rev. Знання структури NMD A рецептора, функції і Chim. (Bucharest), 33(7), 601 (1982); СА 97: фармакології досягнуто внаслідок нещодавніх до174467а] як локальні анестезуючі й антифібрилясягнень молекулярної біології. NMDA рецептори є ційні агенти. гетеромерними комплексами, утворюваними з Похідні піперидину й аналоги, заміщені фенопринаймні однієї NR1 субодиниці й принаймні одлами або еквівалентами фенолу, що мають спенієї з чотирьох різноманітних NR2 субодиниць цифічно антагоністичну активність NMDA NR2B, (NR2A-D). Обидва просторових розподіли в CNS і [описані в міжнародних патентних заявках фармакологічна чутливість NMD A рецепторів, WO90/14087, WO90/14088, WO97/23202, створених з різних NR2 субодиниць, є різними. WO97/23214, WO97/23215, WO97/23216, Особливо цікавою з них є NR2B субодиниця, внаWO97/23458, WO99/21539, WO2000/25109, слідок її обмеженого розподілу (найвища питома ЕР648744 і в US 5436255]. Сполуки, що містять вага в передній частці кори головного мозку і жепідструктур у 2-бензоксазолінону з подібною біололатиноподібна субстанція спинного мозку). Сполугічною активністю, [описані в міжнародних патентки, вибрані для такого підтипу, є доступними [Curr. них заявках WO98/18793 і WO2000/00197]. Інші Pharm. Des., 5, 381-404 (1999)] і, як було доведено, селективні антагоністи NMDA NR2B, що мають є ефективними на моделях інсульту у тварин конденсовані гетероциклічні структури, [описані у [Stroke, 28, 2244-2251 (1997)], травматичного поWO2001/30330, WO2001/32171, WO2001/32174, шкодження мозку [Brain Res., 792, 291-298 (1998)], WO2001/32177, WO2001/32179, WO2001/32615, хвороби Паркінсона [Exp. Neurol., 163, 239-243 WO2001/32634]. (2000)], невропатичного й запального болю [NeuВтім, як і раніше, залишається необхідність у ropharmacology, 38, 611-623 (1999)]. Крім того, сенових антагоністах N MD A, що впливають на таку лективні антагоністи рецепторів NMDA підтипу мішень, як NR2B рецептор. NR2B, як припускають, мають невеличкі або не Несподівано було виявлено, що нові амідні мають взагалі несприятливих побічних ефектів, які похідні карбонових кислот формули (І) за даним звичайно спричиняються невибірними антагонісвинаходом є функціональними антагоністами тами NMDA рецепторів, такими, як психодислепNMDA рецепторів, які вражають (блокують) NMDA тичні ефекти, такими, як запаморочення, головний рецептори, переважно шляхом зв'язування із сайбіль, галюцинації, дисфорія і порушення пізнаватом зв'язування іфенпродилу. Тому вважається, льної і рухової функції. що вони є специфічними антагоністами підтипу Селективний антагонізм NMDA підтипу NR2B NR2B. може досягатися сполуками, які спеціально зв'яТаким чином, даний винахід стосується назуються і діють на алостеричний модулюючий сайт самперед нових амідних - лохідних карбонових NR2B субодиниці рецептора. Цей зв'язуючий сайт кислот формули (І) може бути описаний за допомогою досліджень зв'язування зі специфічними радіолігандами, та(I) кими, як [125І]-іфенпродил [J.Nerochem., 61, 1203 126 (1993)] або [ H]-Ro 25,6981 [J.Neurochem., 70, де: 2147-2155 (1998)]. Звідтоді, як іфенпродил став обидві -(CHR1)m- і -(CHR2)n- є –СН2-СН2першим, хоча не достатньо специфічним, відомим групами, лігандом зазначеного рецептора, він був також суміжні V і U групи утворюють разом одна з названий як іфенпродил зв'язуючий сайт. одною і з одним або більше ідентичними або різАналоги похідних аміду карбонової кислоти ними додатковими гетероатомами і -СН= і/або формули (І) закритої структури відомі з літератури. СН2-групами, необов'язково заміщене 4-7-членне Флоридський Центр гетероциклічних сполук гомо- або гетероциклічне кільце, переважно мор[Department of Chemistry, University of Florida, Ρ Ο фолін, пірол, піролідин, оксо- або тіоксопіролідин, Box 117200, Gainesville, FL, 32611-7200, USA] одепіразол, піразолідин, імідазол, імідазолідин, оксоржав міліграмові кількості трьох сполук формули або тіоксоімідазол або імідазолідин, 1,4-оксазин, (І) для біологічного тестування: N-(4-бромфеніл)-4оксазол, оксазолідин, оксо- або тіоксооксазолідин (фенілметил)-1-піперидинацетамід, 4-[[оксо[4або 3-оксо-1,4-оксазинове кільце, (фенілметил)-1X є -СО-гр упою, піперидиніл]ацетил]аміно]бензойної кислоти й W є -CO-, -СН2- або -СН(-алкільною)-групою, етилового ефіру 4-[[оксо[4-(фенілметил)-1де алкіл є С -С алкільною групою, 1 4 9 77684 10 Υ є атомом кисню, так само як С 1-С4алкіленом, сполуки формули (VII) С2-С4алкініленом, циклоалкіленом, амінокарбонілом, -ΝΗ-, -N(алкіл)-, -СН2О-, -СН(ОН)-, -ОСН2(VII) групою, де алкіл є С 1-С4алкільною групою, Ζ є воднем або атомом галогену, нітро, аміно, де значення Q є атомом галогену, R3 є атомом С1-С4алкілом, С1-С4алкокси, ціано, трифторметиводню або С1-С4алкільною групою і X, R1, R2, Υ, Ζ, лом, гідроксильною або карбоксильною групою й n і m є такими, як подано вище для сполук формуоптичних антиподів або рацематів та/або їхніх фали (І), взаємодіє з аміном формули (V): рмацевтично прийнятних солей, утворених з кислотами й основами. (V) Крім того, об'єктами даного винаходу є фармацевтичні композиції, що містять амідні сполуки де значення U і V є такими, як подано раніше карбонових кислот формули (І) або оптичні антидля сполук формули (І), або поди або рацемати або їхні солі як активні інгредіd) вторинний амін формули (lll): єнти. Наступними об'єктами винаходу є способи (III) одержання амідних сполук карбонових кислот формули (І) і фармацевтичне виробництво лікарських де R1, R2, m, n, Υ і Ζ мають такі самі значення, препаратів, що містять ці сполуки, а також спосіб як подано для сполук формули (І), взаємодіє з лікування з використанням зазначених сполук, етилоксалілхлоридом у присутності основи на твеякий включає введення ссавцеві, що потребує рдій підкладці в дихлорметані, лікування, включаючи людину, - ефективної кільодержаний ефір формули (VIII): кості/кількостей сполук формули (І) даного винаходу як таких або як лікарського засобу. (VIII) Нові амідні похідні карбонової кислоти формуде R1, R2, m, n, Υ і Ζ мають такі самі значення, ли (І) даного винаходу є високоефективними й як подано для сполук формули (І), підлуговують селективними антагоністами NMDA рецептора, і, сильноосновною іонною смолою в етанолі, й одебільш того, більшість цих сполук є селективними антагоністами підтипу NR2B NMDA рецептора. ржаний оксаламід кислоти формули (IX): Відповідно до даного винаходу амідні похідні (IX) карбонових кислот формули (І) можуть бути одержані за допомогою наступних процесів де R1, R2, m, n, Υ і Ζ мають такі самі значення, a) карбонова кислота формули (II): як подано для сполук формули (І), взаємодіє з амідом формули (V): (II) (V) де значення U, V і W є такими, що подані для формули (І), або її реакційноздатна похідна взаємодіє з аміном формули (III): (III) де значення R1, R2, Υ, Ζ, n і m є такими, як подано раніше для сполук формули (І), або b) для одержання сполук формули (І), що мають -CO- групу в положенні W, де значення R1, R2, Y, Z, U, V, Χ, n і m є такими, як подано раніше для сполук формули (І), карбонова кислота формули (IV): (IV) де значення X, R1, R2, Υ, Ζ, n і m є такими, як подано раніше для сполук формули (І), або її реакційноздатна похідна, взаємодіє з аміном формули (V): (V) де значення U і V є такими, як подано раніше для сполук формули (І); або c) для одержання сполук формули (І), що мають -СН2- або -СН(-алкільну)-груп у в положенні W, де алкіл є С1-С4алкільною групою і значення R1, R2, Υ, Ζ, U, V, Χ, n і m є такими, як подано раніше для сполук формули (І), галогеновмісна похідна де значення U і V є такими, як подано раніше для сполук формули (І), у суміші дихлорметан/диметилформамід у присутності 1-[3(диметиламіно)-пропіл]-3-етилкарбодиіміду й одержану сполуку формули (І), де R1, R2, Υ, Ζ, U, V, X, W, n і m є такими, як згадано вище, - в даному випадку перетворюють на іншу сполуку формули (І) шляхом уведення додаткових замісників і/або модифікування і/або видалення наявних замісників і/або шляхом утворення солей з кислотами і/або вивільнення амідної похідної карбонової кислоти формули (І) з отриманої кислотноадитивної солі шляхом обробки основою, і/або вільна амідна похідна карбонової кислоти формули (І) може бути перетворена на сіль шляхом обробки основою і/або розділена на її оптичні антиподи. Утворення амідного зв'язку переважно здійснюють шляхом одержання активної похідної з карбонової кислоти формули (II) або (IV), яка реагує з аміном формули (III) або (V), переважно в присутності основи. Перетворення карбонової кислоти на активну похідну може бути здійснене in situ під час утворення амідного зв'язку в придатному розчиннику (наприклад, диметилформаміді, ацетонітрилі, хлорованих вуглеводнях або вуглеводнях). Активними похідними можуть бути хлорангідриди кислот (на 11 77684 12 приклад, отримані з карбонової кислоти з тіонілхформули (І) може бути переведена в сіль шляхом лоридом), змішані ангідриди (наприклад, отримані обробки основою. з карбонової кислоти з ізобутилхлорформіатом у Наприклад, відщеплення метальної і бензильприсутності основи, наприклад, триетиламіну), ної групи від метокси і бензилоксигруп, що знахоактивні ефіри (наприклад, отримані з карбонової дяться в Ζ положенні, приводить до похідних фекислоти з гідроксибензтриазолом і дициклогексилнолу. Видалення бензильної групи може бути карбодиімідом або О-бензотриазол-1-іл-N,N,N',N'здійснено, наприклад, каталітичною гідрогенізацітетраметилуроній гексафторфосфат (HBTU) в єю або за допомогою броміду водню в розчині присутності основи, наприклад, триетиламіну), оцтової кислоти, відщеплення метальної групи кислотні азиди (наприклад, отримані з гідразиду може бути здійснене за допомогою триброміду карбонової кислоти). Активні похідні можуть бути бору в розчині дихлорметану. Сполуки формули одержані при температурі в інтервалі від кімнатної (І), що містять вільну фенольну гідроксильну гр упу, до 0°С. При цьому додають придатний амін форможуть бути перетворені на ацилокси або сульфомули (III) або (V) як основу або як сіль, утворену з ксипохідні за допомогою різноманітних ацилюючих неорганічною кислотою, до отриманого таким чиабо сульфонуючи х агентів. Реакції виконують при ном розчину або суспензії в присутності основи, кімнатній температурі в хлорованих вуглеводнях, наприклад триетиламіну, необхідної для вивільвикористовуючи хлорангідрид кислоти або ангіднення аміну. Після реакцій конденсації здійснюють рид кислоти як ацилюючий агент у присутності тонкошарову хроматографію. Необхідний час реаоснови (наприклад, триетиламіну або карбонату кції складає 6-20 годин. Обробка реакційної маси натрію). Похідні аміду карбонової кислоти формуможе бути виконана за допомогою різноманітних ли (І), що містять нітрогрупу (І), можуть бути переспособів. ведені в аміни за допомогою каталітичної гідрогеУтворення амідного зв'язку переважно виконізації, й аміни можуть потім реагувати таким нують шля хом нагрівання при кипінні в придатному чином, що утворюються кислотні аміди як описано розчиннику аміну формули (V) з галогеновмісною для процесу ацилювання фенольних гідроксильсполукою формули (IV) або (VII) у присутності орних груп.Вільні гідроксильні групи можуть бути ганічної основи (наприклад, триетиламіну, піридиетерифіковані за допомогою ангідридів кислот або ну, піперидину) або неорганічної основи (наприхлорангідридів кислот у присутності основи. клад, карбонату натрію або карбонату калію) і Карбонові кислоти формули (II) або (IV), перйодиду натрію. Придатний розчинник може бути винні або вторинні аміни формули (III) або (V) і апротонним розчинником (наприклад, толуолом, галогеновмісні сполуки формули (VII) є або комерхлорованими вуглеводнями) або диполярним апційно доступними, або вони можуть бути синтезоротонним розчинником (наприклад, кетоном, ацевані за допомогою різноманітних відомих способів. тонітрилом або диметилформамідом). Після проСинтез деяких комерційно недоступних карбоноведення реакції виконують тонкошарову вих кислот формули (II) або (IV) або галогеновмісхроматографію. Необхідний час реакції складає них сполук (VII) наведені в прикладах. Згідно з 20-50 годин. Обробку реакційної маси також можцими методиками також можуть бути отримані інші на здійснити за допомогою різноманітних способів. комерційно недоступні карбонові кислоти формули Коли реакційна суміш є суспензією, осад від(II) або (IV) або галогеновмісні сполуки формули фільтровують, промивають водою і/або органічним (VII). розчинником і перекристалізують з придатного Експериментальні методики розчинника, що дає чистий продукт. Якщо кристаОцінка функціонального NMDAлізація не приводить до чистого продукту, тоді антагоністичного потенціалу сполук у первинних використовують хроматографію на колонці для культурах коркових нейронів пацюка, заснована на його очищення. Хроматографію на колонці виковимірюванні внутрішньоклітинної концентрації нують у нормальній фазі, використовуючи Кизелькальцію за допомогою флуориметричного лічильгель (Kieselgel) 60 як адсорбент і різноманітні сисника теми розчинників, наприклад толуол/метанол, Відомо, що в процесі постнатального розвитку хлороформ/метанол або толуол/ацетон, як елюенсубодиничний склад нейронних NMD A рецепторів ти. Якщо реакційна суміш наприкінці реакції ацизмінюється. Подібна зміна була виявлена в нейлювання або алкілування являє собою розчин, ронних клітинних культурах [Eur. J. Neurosci., 10, тоді його концентрують і залишок кристалізують 1704-1715 (1998)]. Відповідно до даних рівня техніабо очищують за допомогою хроматографії на ки і наших власних імуноцитохімічних досліджень, колонці, як описано вище. Структур у продуктів нейронні клітини, культивовані протягом 4-7 днів in визначають за допомогою ІЧ, ЯМР і масvitro, переважно експресують NR2B субодиницю спектрометрії. разом із NR1 субодиницею. Тому функціональний Отримані амідні похідні карбонової кислоти тест на NMD A-антагонізм у цих клітинах відобраформули (І), попри залежність від способу одержує головним чином дію на рецептори, що містять жання, в кожному випадку можуть бути переведені NR2B субодиницю. Оскільки NMDA рецептори, як в інші сполуки формули (І) шляхом уведення довідомо, є проникними для іонів кальцію при збудаткових замісників і/або модифікування і/або видженні, ступінь активації NMDA рецептора і його далення наявних замісників, і/або шляхом утвоінгібування функціональними антагоністами може рення солей кислот, і/або вивільнення похідної характеризуватися шля хом вимірювання підвиаміду карбонової кислоти формули (І) з одержаних щення внутрішньоклітинної концентрації кальцію кислотно-адитивних солей шляхом обробки оснопісля введення в клітини агоністу (NMD A). Позаяк вою, і/або вільна похідна аміду карбонової кислоти між NMDA рецепторами пацюка і людини спостері 13 77684 14 гається дуже висока гомологія послідовності (99, ценції на розміри концентрації кальцію. 95, 97% для NR1, NR2A і NR2B субодиниць, відпоІнгібуючий потенціал сполуки в окремій точці відно), припускається, що існує невелике, якщо концентрації виражають у вигляді процентного взагалі є, розходження в їхній фармакологічній інгібування контрольної NMDA відповіді. Сигмоїчутливості. Отже, результати, отримані з (клонодальні криві концентрація-інгібування будують за ваними або природними) NMDA рецепторами паданими і визначають значення ІС 50 як концентрацюка, можуть добре екстраполюватися на NMDA цію, що забезпечує половину максимального інгірецептори людини. бування, що досягається за допомогою сполуки. Вимірювання внутрішньоклітинного кальцію Середні значення ІС 50 одержують принаймні з виконувалися на первинних неокортикальних клітрьох незалежних експериментів. тинних культурах, отриманих від 17-денних ембріВизначення зв'язування сполук з NR2B субонів пацюків Charles River [для докладного одеродиницею [3H]-Ro 25,6981 дослідом на зв'язування жання неокортикальної клітинної культури див. Метод по суті подібний до методу, описаного Johnson, Μ. І; Bunge, R.P. (1992): Primary cell culMutel та ін. [J. Neurochem., 70, 2147-2155 (1998)], tures of peripheral and central neurons and glia. In: за винятком температури інкубації й концентрації Protocols for Neural Cell Culture, eds: Fedoroff, S.; радіоліганду. Коротко кажучи, мембрани виділяють Richardson Α., The Humana Press Inc., 13-38]. Після з передньої частки мозку самців пацюків Wistar. Їх виділення клітини вміщають у стандартні 96інкубують у присутності й відсутності тестованої коміркові мікропланшети і культури підтримують в сполуки протягом 2 годин при кімнатній темпераатмосфері 95% повітря - 5% СО2 при 37°С до дотурі. Неспецифічне зв'язування визначають за слідження. допомогою 10мкМ Ro-25,6981, й воно звичайно Культури використовують для внутрішньоклістановить менше за 7% від повного зв'язування. тинних вимірювань кальцію через 4-7 днів in vitro. Концентрація застосовуваного радіоліганду (3H2+ Клітини фарбують флуоресцентним Са -чутливим Ro-25,6981) становить 4нМ. Значення ІС50 (концебарвником Fluo-4/ΑΜ (2-2,5мкМ) до дослідження. нтрації 50% інгібування) визначають за сигмоїдаФарбування зупиняють, промиваючидвічі розчильними кривими, побудованими за кривими конценом, що використовується також у процесі вимірюнтрація - заміщення. вання (140мМ NaCl, 5мМ KСl, 2мМ СаСl2, 5мМ Біологічна активність сполук HEPES [4-(2-гідроксіетил)-1Значення ІС50 для вибраних прикладів сполук піперазинетансульфонова кислота], 5мМ HEPESцього винаходу у функціональному NMDA антагоNa, 20мМ глюкози, 10мкМ гліцину, рН=7,4). Потім нізмі й у тестах на зв'язування подані в Таблиці 1 і додають тестовану сполук у, розчинену у вищезгапорівнюються зі значеннями, вказаними для найданому розчині (90мкл/комірка). Вимірювання внусильніших відомих з рівня техніки сполук. трішньоклітинного кальцію проводять за допомоСполуки даного винаходу виявляють значення гою флюорометричного лічильника. Зміни ІС50 менше, ніж 50мкМ у функціональному NMDA викликають уведенням 40мкМ NMDA у флуо-4антагонізмі й у теста х на зв'язування. Таким чифлуоресценцію, що відбиває внутрішньоклітинну ном, сполуки і фармацевтичні композиції даного концентрацію кальцію. Інгібуючу активність тестовинаходу є специфічними NMDA антагоністами ваної сполуки оцінюють вимірюванням зниження NR2B-підтипу. Деякі зі сполук мають переважаючу росту кальцію при різноманітних концентраціях активність порівняно до відомих з рівня техніки сполуки. Після вимірювання застосовують стандасполук (див. Таблицю 1). ртну процедуру калібрування [Meth. Cell. Biol., 40, 155-181 (1994)] для перетворення даних флуоресТаблиця 1 NMDA антагоніст/зв 'язу юча актив ність сполу к на природних нейронах/нейронн их мембр анах пацюків Код сполу ки NMDA ІС 50[мкМ] Ro- зв 'язув ання ІС 50[мкМ] 7000162 3 7000182 4 7000186 1 7000162 0 7000186 3 7000184 4 7000184 3 7000175 9 0.0007 0.0014 0.0024 0.0032 0.048 0.113 0.533 4.71 0.0047 0.0044 0.0055 0.018 0.091 0.214 0.972 >30 Код сполу ки з рів ня техніки СІ-1041 Со-101244 EMD 95885 СР 101606 Со-111 103 Ro 25.6981 і фенпр оди л NMDA ІС 50[мкМ] 0.0066 0.023 0.035 0.041 0.060 0.159 0.483 Ro- зв 'язув ання ІС 50[мкМ] 0.004 0.0033 0.0072 0.0084 0.0084 0.0059 0.096 2+ NMDA IC 50: ІС 50, в изначено дослі дом із в ну трішньоклі тинною кон цент рацією Са на корков их нейронах 3 Ro-зв 'язув ання ІС 50: ІС 50, в изначено дослідом на зв 'язув ання з [ H]-Ro 25,6981 на церебральних ме мбра нах пацюка Сполуками з рівня техніки є такі сполуки: СІ-1041: 6-{2-[4-(4-фторбензил)-піперидин-1іл]-етансульфінил}-3Н-бензо-оксазол-2-он; Со-101244: 1-[2-(4-гідроксифенокси)етил]-4гідрокси-4-(4-метилбензил)піперидин; EMD 95885: 6-[3-(4-фторбензил)піперидин-1іл]пропіоніл]-2,3-дигідробензоксазол-2-он; CP-101,606: (1S,2S)-1-(4-гідроксифеніл)-2-(4гідрокси-4-фенілпіперидин-1-іл)-1-пропанол; Со-111103: 1-[2-(4-гідроксифенокси)етил]-4-(4 15 77684 16 CP-101,606 >20мг/кг* фторбензил)піперидин; Co-111103 >20мг/кг* Ro 256981: R-(R*,S*)-1-(4-гідроксифеніл)-2Ro-256981 >20мг/кг* метил-3-[4-(фенілметил)піперидин-1-іл]-1пропанол. *: Значення ED 50 не бу ли в изначені, якщо інгібу в ання складало ме н ше за 50 % при дозі 20 мг/кг. Іфенпродил: еритро-2-(4-бензилпіперидино)-1(4-гідроксифеніл)-1-пропанол. Формаліновий тест на миші для вимірювання Захворювання, що їх можна успішно лікувати ефективності in vivo Ін'єкція розчиненого формаліNMDA антагоністами, включають травматичне ну в задню лапу пацюків або мишей, як відомо, пошкодження головного мозку [Neurol. Res., 21, викликає двофазну, пов'язану з болем поведінку, 330-338 (1999)] або спинного мозку [Eur. J. вимірювану як час, витрачений на облизуванPharmacol., 175, 165-74 (1990)], нейронні пошконя/покусування пошкодженої лапи. Друга фаза дження, пов'язані з вірусом імунодефіциту людини звичайно визначається як події, пов'язані з болем, (ВІЛ) [Annu. Rev. Pharmacol. Toxicol., 1998; 38159що відбуваються з 15-60хв. часовими інтервалами 77], аміотрофічний бічний склероз [Neurol. Res., після ін'єкції формаліну. Відомо, що NMDA рецеп21, 309-12 (1999)], толерантність і/або залежність тори залучені в другій фазі відповіді на ін'єкцію від опіоїдного лікування болю [Brain. Res., 731, формаліну, і ця поведінкова відповідь чутлива до 171-181 (1996)], синдроми залежності, наприклад, блокади NMDA рецепторів [Dickenson, А. і Besson від алкоголю, опіатів або кокаїну [Drug and Alcohol J.-M. (Editors): Chapter 1, стор.6-7: Animal models of Depend., 59, 1-15 (2000)], м'язові судоми [Neurosci. Analgesia; і Глава 8, стор.180-183: Mechanism of Lett., 73, 143-148 (1987)], слабоумство різноманітCentral Hypersensitivity: Excitatory Amino Acid ного походження [Expert Opin. Investig. Drags, 9, Mechanisms and Their Control - In Pharmacology of 1397-406 (2000)]. NMDA антагоніст може також Pain. Springer-Verlag (Berlin) 1997]. Тому друга фабути корисний для лікування церебральної ішемії за формалінових дослідів використовується для будь-якого походження (наприклад, інсульт, хірурхарактеристики ефективності сполук in vivo. Ввагія серця), хронічних нейродегенеративних поружається, що інгібування другої фази відповіді вкашень, таких як хвороба Альцгеймера, хвороба зує на болезаспокійливу дію проти хімічноПаркінсона, хвороба Хантингтона, біль (наприіндукованого постійного болю [Hunskaar, S., та ін.: клад, посттравматичний або післяопераційний) і Formalin Test in Mice, a Useful Technique for Evaluхронічних болючих станів, таких як невропатичний ating Mild Analgesics, Journal of Neuroscience Methбіль або біль, пов'язаний з раком, епілепсії, занеods, 14 (1985) 69-76]. покоєння, депресії, мігрені, психозу, гіпоглікемії, Використовують самців альбіносів мишей дегенеративних порушень сітківки (наприклад, NMRI Charles River (20-25г). До експерименту не CMV ретиніт), глаукоми, астми, шуму у вуха х, давали жодної твердої їжі протягом 16 годин, але утрати слуху, викликаної аміноглікозидним антибітварини мали вільний доступ до 20% розчину глюотиком [Drag News Perspect 11, 523-569 (1998) і кози. Тварин залишали на 1 годину акліматизуваWO 00/00197]. тися у скляному циліндрі (15см у діаметрі), потім Відповідно, ефективні кількості сполук за випереміщували в ідентичний циліндр із дзеркалом, находом можуть успішно використовуватися для уміщеним позаду, для полегшення спостереження. лікування травматичних пошкоджень головного Тестовані речовини суспендували в 5% Твін-80 мозку або спинного мозку, нейронних пошкоджень, (10мл на кг ваги тіла) і вводили орально за 15 хвипов'язаних із вірусом імунодефіциту людини (ВІЛ), лин до ін'єкції формаліну (20мкл 1%-го формаліну аміотрофічного бічного склерозу, толерантності в 0,9% сольовому розчині, що вводиться підшкірно і/або залежності від опіоїдного лікування болю, в дорзальну поверхню правої задньої лапки). Висиндромів залежності, наприклад, від алкоголю, мірювали час, витрачений на облизування й покуопіатів або кокаїну, ішемічних захворювань ЦНС, сування ін'єктованої лапи від 20 до 25хв. після хронічних нейродегенеративних порушень, таких ін'єкції формаліну. Для виявлення значень ED50 як хвороба Альцгеймера, хвороба Паркінсона, групам з 5 мишей уводили різноманітні дози (прихвороба Хантингтона, болю і хронічних болючих наймні п'ять) тестованих речовин і в той самий станів, таких як невропатичний біль або біль, подень спостерігали результати, виражені як % часу в'язаний із раком, епілепсії, занепокоєння, депреінгібування, витраченого на облизування порівнясії, мігрені, психозу, м'язових спазмів, слабоумства но до контрольної групи. Значення ED50 (тобто різноманітного походження, гіпоглікемії, дегенерадоза, що приводить до 50% інгібування) були розтивних порушень сітківки, глаукоми, астми, шуму у раховані вирівнюванням сигмоїдальної кривої Бовуха х, утрати слуху, викликаної аміноглікозидним льтцмана. антибіотиком. Сполуки за винаходом, а також їхні фармацевТаблиця 2 тично прийнятні солі, можуть використовуватися Значення ED 5 0 в ибраних сполу к окремо або відповідно у формі фармацевтичних композицій. Ці композиції (лікарські засоби) моID код сполу к ED 50 (мг/кг) жуть бути у твердій, рідкій або напіврідкій формі, і 45-70001 598 0.46 45-70002 346 0.48 можуть додаватися фармацевтичні ад'юванти й 45-70002 407 4.4 допоміжні матеріали, які звичайно використову45-70001 620 6.9 ються на практиці, такі як носії, наповнювачі, розСІ-1041 5.3мг/кг ріджувачі, стабілізатори, зволожуючі або емульгуCo-101244 >20мг/кг* ючі агенти, регулятори рН і осмотичного тиску, EMD 95885 5.9мг/кг 17 77684 18 віддушки або ароматизатори, а також добавки, що му випадку таблетки зроблені з поглибленням, що полегшують просування або забезпечують одеррозділяє навпіл, щоб спростити введення. жання складу. Таблетки можуть бути виготовлені безпосереДозування, потрібне для прояву терапевтичнодньо з суміші активного інгредієнта і придатних го ефекту, може змінюватися в широких межах і допоміжних засобів за допомогою пресування. В залежатиме від індивідуальних вимог у кожному з даному випадку таблетки можуть бути покриті за конкретних випадків, залежно від стадії хвороби, допомогою добавок, що звичайно використовустану і ваги тіла пацієнта, що лікується, а також від ються у фармацевтичній практиці, наприклад, стачутливості пацієнта до активного компонента, спобілізаторами, віддушками, барвниками, такими, як собу введення й кількості щоденних прийомів. Фацукор, похідними целюлози (метил- або етилцектична доза використовуваного активного комполюлоза, натрію карбоксиметилцелюлоза тощо), нента може бути успішно визначена лікарем, полівініл піролідоном, фосфатом кальцію, карбофа хівцем в області хвороби пацієнта. натом кальцію, харчовими барвниками, харчовими Фармацевтичні композиції, що містять активлікерами, ароматичними агентами, пігментами ний інгредієнт відповідно до даного винаходу, звиоксиду заліза тощо. Щодо капсул, то вони заповчайно включають від 0,01 до 100мг активного інгнюються сумішшю активного інгредієнта і допоміредієнта в окремому одиничному дозуванні. жних засобів. Звичайно, можливо, що кількість активного інгреРідкі оральні композиції, наприклад суспензії, дієнта в деяких композиціях перевищує вер хню сиропи, еліксири, можуть бути отримані, викорисабо нижню межу, визначені вище. товуючи воду, гліколі, олії, спирти, барвники й відТвердими формами фармацевтичних комподушки. зицій можуть бути, наприклад, таблетки, драже, Для ректального введення композицію готують капсули, пілюлі або ампули з ліофілізованим поу вигляді свіч або клізм. Свічі можуть містити, крім рошком, корисні для одержання ін'єкцій. Рідкими активного інгредієнта, носій, так званий свинячий композиціями є ін'єктовані й вливані композиції, жир для свіч. Носіями можуть бути рослинні олії, рідкі лікарські засоби, упаковані рідини і краплі. такі, як гідрогенізовані рослинні олії, тригліцериди Напіврідкими складами можуть бути мазі, бальзаС12-С18 жирних кислот (переважно носії з торговою ми, креми, струшуючі суміші і свічі. назвою Witepsol). Активний інгредієнт гомогенно Для простого введення підходить, якщо фарзмішується з розплавленим загусником для свіч, і мацевтичні композиції включають одиниці дозуформуються свічі. вання, що містять кількість активного інгредієнта, Для парентерального введення композицію що вводиться однократно або в декілька прийомів, одержують у ви гляді розчину для ін'єкції. Для одеабо половину, третину або четверту частину від ржання розчину для ін'єкції активні інгредієнти цієї кількості. Такими одиницями дозування є, нарозчиняють у дистильованій воді і/або в різноманіприклад, таблетки, що можуть бути виконані з потних органічних розчинниках, таких, як гліколеві глибленнями, які забезпечують розподіл таблетки ефіри, в даному випадку в присутності солюбілізана дві або чотири частини, щоб точно ввести поторів, наприклад поліоксіетиленсорбітантрібну кількість активного інгредієнта. монолаурат, моноолеат або моностеарат (Tween Таблетки можуть бути покриті кислоторозчин20, Tween 60, Tween 80). Розчин для ін'єкції може ним прошарком, щоб полегшити вивільнення вмістакож містити різноманітні допоміжні засоби, такі, ту активного інгредієнта після проходження шлуняк консерванти, наприклад етилендіамін тетраацека. Такі таблетки є покритими для кишечнику. тат, а також агенти для регулювання рН і буфери, Подібний ефект може досягатися також при ввей у даному випадку місцевий знеболюючий засіб, денні в капсулу активного інгредієнта. наприклад лідокаїн. Розчин для ін'єкції, що містить Фармацевтичні композиції для орального ввеактивний інгредієнт за винаходом, відфільтровудення можуть містити, наприклад, лактозу або ють до заповнення в ампули і стерилізують після крохмаль як ексципієнти, натрію карбоксиметилзаповнення. целюлозу, метилцелюлозу, полівініл піролідин або Якщо активний інгредієнт є гігроскопічним, він крохмальну пасту як зв'язуючі агенти або гранупотім може бути стабілізований ліофілізацією. люючі агенти. Картопляний крохмаль або мікроТакі приклади ілюструють винахід без наміру кристалічну целюлозу додають як розпушувальні так чи інакше обмежити його обсяг. агенти, може також використовуватися ультраміПриклад 1 лопектин або формальдегідний казеїн. Тальк, ко2-[4-(4-Фторбензил)-піперидин-1-іл1-2-оксi-Nлоїдна кремнієва кислота, стеарин, стеарат каль(2-оксо-2
ДивитисяДодаткова інформація
Назва патенту англійськоюCarboxylic acid amide derivatives
Автори англійськоюHorvath Csilla, Farkash Shandor, Nagy Jozsef, Kolok Sandor, Borza Istvan, Vago Istvan, Vago, Istvan
Назва патенту російськоюАмиды карбоновых кислот
Автори російськоюХорват Чилла, Фаркаш Шандор, Надь Йожеф, Колок Шандор, Борза Иштван, Ваго Иштван
МПК / Мітки
МПК: A61K 31/4709, C07D 417/12, A61P 25/06, C07D 211/14, A61P 25/36, C07D 413/12, A61P 29/00, A61P 31/12, A61P 9/00, A61K 31/454, A61K 31/445, C07D 211/18, A61P 25/22, C07D 401/12, A61P 27/16, A61P 25/16, A61P 25/28, A61K 31/46, A61P 3/10, C07D 211/16, A61P 27/02, A61P 25/32, A61P 25/18, A61P 11/06, A61P 21/04, A61P 21/00, A61P 43/00, A61P 25/24, A61P 25/14, A61P 31/18, A61P 25/08, A61P 27/06, A61K 31/4545
Мітки: карбонових, аміди, кислот
Код посилання
<a href="https://ua.patents.su/25-77684-amidi-karbonovikh-kislot.html" target="_blank" rel="follow" title="База патентів України">Аміди карбонових кислот</a>
Попередній патент: Спосіб ушивання очеревини при видаленні матки
Наступний патент: 2-(3,5-біс-трифторметилфеніл)-n-[6-(1,1-діоксо-1l6-тіоморфолін-4-іл)-4-(2-метил або 4-фтор-2-метилзаміщений)фенілпіридин-3-іл]-n-метил-ізобутирамід
Випадковий патент: Спосіб лікування гайморитів, обумовлених кістами верхньої щелепи












