Терапевтичний засіб проти мігрені
Номер патенту: 102106
Опубліковано: 10.06.2013
Автори: Ікеда Юнічі, Ічікава Шунджі, Канда Томоюкі, Курокава Масако
Формула / Реферат
1. Терапевтичний та/або профілактичний засіб проти мігрені, що містить як активний інгредієнт, сполуку, що має селективну антагоністичну активність щодо аденозинових рецепторів А2А та афінність щодо аденозинових рецепторів А2A, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів А1, або її фармацевтично прийнятну сіль, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А2А, є сполукою, представленою наступною формулою (II)
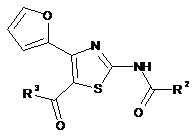 (II),
(II),
де R2 означає феніл, піридил, піримідиніл, 5,6-дигідро-2Н-піридилметил або тетрагідропіранілокси, або будь-яку із цих груп, заміщену 1-3 замісниками, вибраними з атома фтору, атома хлору, атома брому, метилу, етилу, метокси та етокси; і R3 означає піридил або тетрагідропіраніл.
2. Засіб за пунктом 1, де R3 означає піридил.
3. Засіб за пунктом 1, де R3 означає тетрагідропіраніл.
4. Засіб за пунктом 1, де сполука є сполукою, представленою наступною формулою (ІІС)
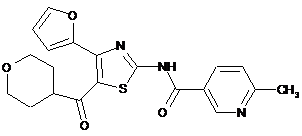 (ІІС).
(ІІС).
5. Спосіб лікування та/або профілактики мігрені, що включає введення ефективної кількості сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів А2А та має афінність щодо аденозинових рецепторів А2А, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів А1, або її фармацевтично прийнятної солі, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А2А, є сполукою, представленою наступною формулою (II)
 (II),
(II),
де R2 і R3 мають ті ж самі значення, як описано вище, відповідно.
6. Спосіб за пунктом 5, де R3 означає піридил.
7. Спосіб за пунктом 5, де R3 означає тетрагідропіраніл.
8. Спосіб за пунктом 5, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А2A, є сполукою, представленою наступною формулою (ІІС)
 (ІІС).
(ІІС).
9. Застосування сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів А2А та має афінність щодо аденозинових рецепторів А2А, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторівА1, або її фармацевтично прийнятної солі для виробництва терапевтичного та/або профілактичного засобу проти мігрені, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А2А, є сполукою, представленою наступною формулою (II)
 (II),
(II),
де R2 й R3 мають ті ж самі значення, як описано вище, відповідно.
10. Застосування за пунктом 9, де R3 означає піридил.
11. Застосування за пунктом 9, де R3 означає тетрагідропіраніл.
12. Застосування за пунктом 9, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А2A, є сполукою, представленою наступною формулою (ІІС)
 (ІІС).
(ІІС).
Текст
Реферат: Винахід стосується терапевтичного та/або профілактичного засобу проти мігрені, що містить, як активний інгредієнт, сполуку, що має селективну антагоністичну активність щодо аденозинових рецепторів А2А та афінність щодо аденозинових рецепторів А 2A, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів А1, або її фармацевтично прийнятну сіль, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А 2А, є сполукою, представленою наступною формулою (II) O N NH R S 3 R 2 O O (II), 2 де R означає феніл, піридил, піримідиніл, 5,6-дигідро-2Н-піридилметил або тетрагідропіранілокси, або будь-яку із цих груп, заміщену 1-3 замісниками, вибраними з атома 3 фтору, атома хлору, атома брому, метилу, етилу, метокси та етокси; і R означає піридил або тетрагідропіраніл. UA 102106 C2 (12) UA 102106 C2 UA 102106 C2 5 10 15 20 25 30 35 40 45 50 55 Галузь винаходу Даний винахід відноситься до терапевтичних та/або профілактичних засобів проти мігрені. Попередній рівень техніки Мігрень - пароксизмальний головний біль, що триває 4-72 години, супроводжуваний нудотою, блювотою, чутливістю до світла, чутливістю до звуків, або подібного [The Merck Manual, Seventeenth Edition, Chapter 168; Therapeutic Guideline of The Japanese Society of Neurology; International Classification of Headache Disorders-II: ICHD-II, 2004]. Вазодилатація екстра-та/або інтракраніальних судин, включаючи поверхневу темпоральну артерію, була запропонована як одна з причин патофізіології мігрені і її патогенезу [Arch. Neurol. Psychiatr., том 39, стор. 737-763(1938); Cephalagia, том 1, стор. 143-147 (1981); Internal medicine, том 81, стор. 601-609 (1998); Internal Medicine, том 81, стор. 639 (1998)]. Також було відомо, що ерготаміновий алкалоїд і суматриптан, гідрофільні агоністи 5-HT1 серотонінових рецепторів (5гідрокситриптамін 1), які не перетинають гематоенцефалічний бар'єр, ефективні для лікування мігрені, тому що ці агоністи діють на серотонінові рецептори 5-HT1 у гладких м'язах церебральних судин, щоб звузити розширені кровоносні судини [Ann. N.Y. Acad. Sci., том 600, стор. 587-600 (1990); Neurology, том 43, стор. S43-S47 (1993)]. Таким чином, вважається, що мігрень можна лікувати, пригнічуючи вазодилатацію екстрата/або інтракраніальних судин. Щодо причин початку мігрені, також були повідомлення, що представляють теорії, засновані на нейрогенному запаленні навколо трійчастого нерва й церебральних кровоносних судин, або навколо кровоносних судин твердої мозкової оболонки, або засновані на активації центрального нерва, так як при кортикальній поширюваній депресії [Lancet, том 363, стор. 381-391 (2004)]. Є додаткові повідомлення щодо мігрені (див. Непатентні документи 1-3). Деякі із прикладів терапевтичних засобів проти мігрені, що використовуються в клініці, включають нестероїдні протизапальні анальгетики, такі як триптани (наприклад, суматриптан) та ібупрофен. Що стосується профілактичних засобів, то на даний час в клінічній практиці використовуються, наприклад, антиепілептичні засоби, такі як топірамат, та антагоністи кальцію, такі як флунаризин. Відомо, що концентрація аденозину в плазмі крові у пацієнтів з мігренню через годину після мігренозної атаки збільшується в середньому на 68 % від його концентрації під час нормального періоду, і що активація аденозинових рецепторів A2 аденозином пригнічує поглинання серотоніну тромбоцитами залежно від концентрації аденозину, і викликає вазодилатацію в результаті швидкого вивільнення серотоніну [Can. J, Neurol. Sci., том 2, стор. 55-58 (1998)]. Крім того, внутрішньовенне введення підсилювача аденозину пацієнту з мігренню, як відомо, викликає напад мігрені [Med. J. Aust., том 162, стор. 389-390 (1995)]. Також відомо, що аденозин має сильну вазодилатаційну активність, і що аденозиновий рецептор A2A й аденозиновий рецептор A2B залучені у вазодилатацію під час мігрені та у аденозин-індуковану вазодилятацію [Am. J. Physiol. Heart Circ. Physiol., том 280, стор. 2329-2335 (2001)]. Таким чином, вважаються, що мігрень можна лікувати, пригнічуючи аденозин-індуковану вазодилятацію. Кофеїн, який має неселективну аденозинову антагоністичну активність, як відомо, зменшує мігрень; однак, кофеїн має побічні ефекти, а саме, психіатричну залежність, та викликає головний біль при відміні кофеїну [див. Pain, 1991, том 44, стор. 151-155; Drugs, 1998, том 49, стор. 37-50]. Крім того, відомо, що похідні ксантину є корисними як терапевтичні препарати проти мігрені (див. Непатентний документ 1). Відомо, що аденозин розподілється в значній кількості в організмі і проявляє безліч фізіологічних дій на центральну нервову систему, серцевий м'яз, нирки, гладкі м'язи, і т.п. через його рецептори (див. Непатентний документ 4). Наприклад, антагоністи аденозину A1, як відомо, полегшують дефекацію (Jpn. J. Pharmacol., 1995, том 68, стор. 119). Крім того, відомо про залученість аденозинових рецепторів A2A, особливо в центральній нервовій системі. Антагоністи аденозинових рецепторів A2A, як відомо, корисні як, наприклад, терапевтичні препарати при хворобі Паркінсона (див. Непатентний документ 5), або терапевтичні препарати при порушенні сну (див. Nature Neuroscience, 2005, стор. 1; патентний документ 2). Є деякі повідомлення щодо взаємозв'язку між рецепторами аденозину й мігренню (див. Непатентні документи 6-13). Наприклад, сполуки, представлені наступними формулами (I), (II), (III), (IV), (V), (VI), і (VII), відомі як сполуки, що мають селективну антагоністичну активність щодо аденозинових рецепторів A2A (див. Патентні Документи 3-9, і Непатентні документи 14 й 15). 1 UA 102106 C2 [Хімічна Формула 1] NH2 N O N N N R1 O N N R3 N NH2 N N N CH3 6 R ( IV ) 30 35 40 N N N CH3 25 N N ( III ) H3C N 20 O N N N N ( II ) N S 15 N O O S 10 N R2 S (I) 5 R5 NH NH2 R4 O N O N N S NH N N CH3 H3C N N O (V) ( VI ) 1 N N N H2N NH2 ( VII ) де R означає метил, етил, пропіл, бутил або 3-метилбутил, або будь-яку із цих груп, 2 заміщену гідрокси; R означає феніл, піридил, піримідиніл, 5,6-дигідро-2H-піридилметил або тетрагідропіранілокси, або будь-яку із цих груп, заміщену 1-3 замісниками, вибраними з атома 3 фтору, атома хлору, атома брому, метилу, етилу, метокси, і етокси; R означає піридил або 4 5 тетрагідропіраніл; R і R можуть бути однаковими або різними, і кожний означає атом водню, 6 атом фтору або 2-метоксиетокси; і R означає метил, етил, пропіл або бутил. Документи попереднього рівня техніки. Патентні документи: Патентний документ 1: WO2005/072739 Патентний документ 2: WO2007/015528 Патентний документ 3: WO98/42711 Патентний документ 4: WO00/17201 Патентний документ 5: WO2005/063743 Патентний документ 6: WO2002/055524 Патентний документ 7: WO2003/011864 Патентний документ 8: WO2006/032273 Патентний документ 9: WO2002/055083 Непатентні документи: Непатентний документ 1: Proceedings of the National Academy of Sciences of the United States of America, 2001, том 98, стор. 4687. Непатентний документ 2: Nature Neuroscience, 2007, том 10, стор. 754. Непатентний документ 3: Neurological Research, 2005, том 27, стор. 175. Непатентний документ 4: Nature Reviews Drug Discovery, 2006, том 5, стор. 247. Непатентний документ 5: Progress in Neurobiology, 2007, том 83, стор. 332. Непатентний документ 6: Can. J. Neurol. Sci., 1998, том 253, стор. 55. Непатентний документ 7: Cephalalgia, 2006, том 26, стор. 925. Непатентний документ 8: Cephalalgia, 2007, том 27, стор. 177. Непатентний документ 9: Brain, 2002, том 125, стор. 1392. Непатентний документ 10: Am. J. Physiol., 2001, том 281, H2018-H2027. Непатентний документ 11: J. Pharmacol. Sci., 2004, том 94, стор. 100. Непатентний документ 12: Pharmacological Reviews, 1999, том 51, стор. 83. Непатентний документ 13: Pharmacology & Therapeutics, 2006, том 112, стор. 199. Непатентний документ 14: European Journal of Pharmacology, 1994, том 267, стор. 335. Непатентний документ 15: Bioorganic & Medicinal Chemistry Letters, 2007, том 17, стор. 1376. Короткий зміст винаходу. Проблеми, які повинен вирішити винахід. Об'єктом даного винаходу є одержання терапевтичних та/або профілактичних засобів проти мігрені, які включають, як активний інгредієнт сполуку, що має антагоністичну активність щодо аденозинових рецепторів A2A, або її фармацевтично прийнятну сіль і т.п. Засоби вирішення проблем. 2 UA 102106 C2 5 10 Даний винахід охоплює наступні об'єкти: (1) - (47). (1) Терапевтичний та/або профілактичний засіб проти мігрені, що включає, як активний інгредієнт, сполуку, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, або її фармацевтично прийнятну сіль. (2) Засіб за пунктом 1, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, має афінність щодо аденозинових рецепторів A2A, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів A1, (3) Засіб згідно (1), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, вибраною із групи, що складається із сполук, представлених наступними формулами (I) - (VII). [Хімічна Формула 2] NH2 O N N N N N N R1 O R3 N N N N N ( II ) O N N N O O ( III ) H3C S N S NH2 N N N CH3 N 6 R N ( IV ) N N CH3 O N O N N CH3 20 N R2 S NH2 R4 R NH (I) 15 5 N S NH N H3C N N O (V) ( VI ) N N N H2N NH2 ( VII ) 1 (де R означає метил, етил, пропіл, бутил або 3-метилбутил, або будь-яку із цих груп, заміщену гідрокси; 2 R означає феніл, піридил, піримідиніл, 5,6-дигідро-2H-піридилметил або тетрагідропіранілокси, або будь-яку із цих груп, заміщену 1-3 замісниками, вибраними з атома 3 фтору, атома хлору, атома брому, метилу, етилу, метокси та етокси; R означає піридил або 4 5 тетрагідропіраніл; R і R можуть бути однаковими або різними, і кожний означає атом водню, 6 атом фтору або 2-метоксиетокси; і R означає метил, етил, пропіл або бутил); (4) Засіб згідно (1), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, представленою наступною формулою (I) або (II). [Хімічна Формула 3] 25 NH2 N N O N NH R3 1 2 R2 S O O (I) 30 N N N N R1 O ( II ) 3 (де R , R і R мають ті ж самі визначення, як описано вище, відповідно). (5) Засіб згідно (1), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, представленою наступною формулою (I). 3 UA 102106 C2 [Хімічна Формула 4] NH2 N N N N N R1 O N (I) 5 10 1 (де R має те ж саме визначення, як описано вище). 1 (6) Засіб згідно (5), де R означає етил, який може бути заміщений гідрокси, або 3метилбутил, який може бути заміщений гідрокси. (7) Засіб згідно (1), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, представленою наступною формулою (II). [Хімічна Формула 5] O N NH R3 R2 S O O ( II ) 2 15 20 25 3 (де R й R мають ті ж самі визначення, як описано вище, відповідно). 3 (8) Засіб згідно (7), де R означає піридил. 3 (9) Засіб згідно (7), де R означає тетрагідропіраніл. (10) Спосіб лікування та/або профілактики мігрені, що включає застосування ефективної кількості сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, або її фармацевтично прийнятної солі. (11) Спосіб згідно (10), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, має афінність щодо аденозинових рецепторів A2A, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів A1, (12) Спосіб згідно (10), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, вибраною із групи, що складається із сполук, представлених наступними формулами (I) - (VII). [Хімічна Формула 6] NH2 N R O N N N 1 O N N R3 N N N R2 S N N N ( II ) O N N N O O (I) ( III ) H3C S N S NH2 N N N 6 CH3 N R 1 N 3 4 5 N S NH H3C O ( VI ) 6 N H2N ( VII ) (де R , R , R , R , R , і R мають ті ж самі визначення, як описано вище, відповідно). 4 N N N N (V) 2 O N O N N CH3 N ( IV ) N N CH3 30 R5 NH NH2 R4 NH2 UA 102106 C2 (13) Спосіб згідно (10), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, представленою наступною формулою (I) або (II). [Хімічна Формула 7] NH2 N N NH R3 N (I) 1 2 R2 S O O 5 10 O N N R1 O N N ( II ) 3 (де R , R , і R мають ті ж самі визначення, як описано вище, відповідно). (14) Спосіб згідно (10), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, представленою наступною формулою (I). [Хімічна Формула 8] NH2 N N N N N R1 O N (I) 1 15 (де R має те ж саме визначення, як описано вище). 1 (15) Спосіб згідно (14), де R означає етил, який може бути заміщений гідрокси, або 3метилбутил, який може бути заміщений гідрокси. (16) Спосіб згідно (10), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, представленою наступною формулою (II). [Хімічна Формула 9] 20 O N NH R3 R2 S O O ( II ) 2 25 30 3 (де R й R мають ті ж самі визначення, як описано вище, відповідно). 3 (17) Спосіб згідно (16), де R означає піридил. 3 (18) Спосіб згідно (16), де R означає тетрагідропіраніл. (19) Застосування сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, або її фармацевтично прийнятної солі для виробництва терапевтичного та/або профілактичного засобу проти мігрені. (20) Застосування згідно (19), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, має афінність щодо аденозинових рецепторів A2A, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів A1, (21) Застосування згідно (19), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, вибраною із групи, що складається із сполук, представлених наступними формулами (I) - (VII). 35 5 UA 102106 C2 [Хімічна Формула 10] NH2 O N N N R N N N 1 O R3 N N N R2 S N N N ( II ) O N N N O O (I) ( III ) H3C S N S NH2 N N N R6 CH3 N 1 N NH 3 4 5 H3C O ( VI ) N N N N (V) 2 N S N N CH3 N ( IV ) N O N O N CH3 5 R5 NH NH2 R4 N H2N NH2 ( VII ) 6 (де R , R , R , R , R , і R мають ті ж самі визначення, як описано вище, відповідно). (22) Застосування згідно (19), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, представленою наступною формулою (I) або (II). [Хімічна Формула 11] 10 NH2 N N N O N N R1 O NH R3 N 1 2 R2 S O O (I) 15 N ( II ) 3 (де R , R , і R мають ті ж самі визначення, як описано вище, відповідно). (23) Застосування згідно (19), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, представленою наступною формулою (I). [Хімічна Формула 12] NH2 N O N N R1 N N N (I) 20 1 (де R має те ж саме визначення, як описано вище). 1 (24) Застосування згідно (23), де R означає етил, який може бути заміщений гідрокси, або 3метилбутил, який може бути заміщений гідрокси. (25) Застосування згідно (19), де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, є сполукою, представленою наступною формулою (II). 25 6 UA 102106 C2 [Хімічна Формула 13] O N NH R3 R2 S O O ( II ) 5 10 15 2 3 (де R й R мають ті ж самі визначення, як описано вище, відповідно). 3 (26) Застосування згідно (25), де R означає піридил. 3 (27) Застосування згідно (25), де R означає тетрагідропіраніл. (28) Сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, або її фармацевтично прийнятна сіль для застосування для лікування та/або профілактики мігрені. (29) Сполука або її фармацевтично прийнятна сіль для застосування для лікування та/або профілактики мігрені, де сполука має афінність щодо аденозинових рецепторів A 2A 10 кратну або вищу, ніж щодо аденозинових рецепторів A1, (30) Сполука або її фармацевтично прийнятна сіль для застосування для лікування та/або профілактики мігрені, де сполука вибрана із групи, що складається із сполук, представлених наступними формулами (I) - (VII). [Хімічна Формула 14] NH2 O N N N N N N R1 O R3 N R5 NH N N N ( II ) O N N N O O (I) N N R2 S NH2 R4 ( III ) H3C S N S NH2 N N N 6 CH3 N R 1 NH 3 4 5 H3C O ( VI ) N N N N (V) 2 N S N N CH3 CH3 20 N N N ( IV ) N O N O N H2N NH2 ( VII ) 6 (де R , R , R , R , R , і R мають ті ж самі визначення, як описано вище, відповідно). (31) Сполука або її фармацевтично прийнятна сіль для застосування для лікування та/або профілактики мігрені, де сполука представлена наступною формулою (I) або (II). [Хімічна Формула 15] 25 NH2 N N N R1 N O N NH R3 1 2 R2 S O O (I) 30 O N N ( II ) 3 (де R , R , і R мають ті ж самі визначення, як описано вище, відповідно). (32) Сполука або її фармацевтично прийнятна сіль для застосування для лікування та/або профілактики мігрені, де сполука представлена наступною формулою (I). 7 UA 102106 C2 [Хімічна Формула 16] NH2 N N N N N R1 O N (I) 5 10 1 (де R має те ж саме визначення, як описано вище). 1 (33) Сполука або її фармацевтично прийнятна сіль згідно (32), де R означає етил, який може бути заміщений гідрокси або 3-метилбутил, який може бути заміщений гідрокси. (34) Сполука або її фармацевтично прийнятна сіль для застосування для лікування та/або профілактики мігрені, де сполука представлена наступною формулою (II). [Хімічна Формула 17] O N NH R3 R2 S O O ( II ) 2 15 20 25 30 35 40 45 3 (де R й R мають ті ж самі визначення, як описано вище, відповідно). 3 (35) Сполука або її фармацевтично прийнятна сіль згідно (34), де R означає піридил. 3 (36) Сполука або її фармацевтично прийнятна сіль згідно (34), де R означає тетрагідропіраніл. (37) Засіб за будь-яким з (1) - (9), де мігренню є мігрень із аурою. (38) Засіб за будь-яким з (1) - (9), де мігренню є мігрень без аури. (39) Терапевтичний та/або профілактичний засіб від головного болю, що містить сполуку або її фармацевтично прийнятну сіль за будь-яким з (1) - (9). (40) Спосіб за будь-яким з (10) - (18), де мігренню є мігрень із аурою. (41) Спосіб за будь-яким з (10) - (18), де мігренню є мігрень без аури. (42) Застосування за будь-яким з (19) - (27), де мігренню є мігрень із аурою. (43) Застосування за будь-яким з (19) - (27), де мігренню є мігрень без аури. (44) Сполука або її фармацевтично прийнятна сіль за будь-яким з (28) - (36), де мігренню є мігрень із аурою. (45) Сполука або її фармацевтично прийнятна сіль за будь-яким з (28) - (36), де мігренню є мігрень без аури. (46) Спосіб лікування та/або профілактики головного болю, що включає застосування сполуки або її фармацевтично прийнятної солі за будь-яким з (1) - (9). (47) Застосування сполуки або її фармацевтично прийнятної солі за будь-яким з (1) - (9) для виробництва терапевтичного та/або профілактичного засобу від головного болю. Ефекти винаходу Даний винахід може забезпечити терапевтичні та/або профілактичні засоби проти мігрені, які містять, як активний інгредієнт, сполуку, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, або їх фармацевтично прийнятні солі і т.п. Спосіб здійснення винаходу В подальшому сполука, представлена загальною формулою (I), буде також згадуватися як Сполука (I). Сполуки, що мають інші номери формул, також згадуються таким же чином. Сполука, що має антагоністичну активність щодо аденозинових рецепторів A 2A, даного винаходу переважно є сполукою, яка має сильну антагоністичну активність щодо аденозинових рецепторів A2A серед різних субтипів (наприклад, рецептори аденозину A1, A2A, A2B і A3) рецепторів аденозину. Відповідно, сполука, що має сильну афінність щодо аденозинових рецепторів A 2A, є переважною сполукою, що має селективну антагоністичну активність щодо аденозинових 8 UA 102106 C2 5 10 15 20 25 30 рецепторів A2A даного винаходу. Наприклад, переважною є сполука, яка має 50 % або більше -8 інгібуючого ефекту при тестовій концентрації сполуки 3×10 моль/л, більш переважною є -8 сполука, що має 50 % або більше інгібуючого ефекту при тестовій концентрації сполуки 1×10 моль/л, подальшою переважною сполукою є сполука, що має 50 % або більше інгібуючого -9 ефекту при тестовій концентрації сполуки 3×10 моль/л, ще більш переважною є сполука, що -9 має 50 % або більше інгібуючого ефекту при тестовій концентрації сполуки 1×10 моль/л, як виміряно тестом зв'язування аденозинових рецепторів A2A, описаним в Тестовому Прикладі 1 нижче. Крім того, переважною сполукою є сполука, що має інгібуючий ефект із константою інгібування (значення Ki, отримане в тому ж самому тесті) 30 нмоль/л або менше, більш переважною є сполука, що має інгібуючий ефект із константою інгібування 10 нмоль/л або менше, більш переважною є сполука, що має інгібуючий ефект із константою інгібування 3 нмоль/л або менше, ще більш переважною є сполука, що має інгібуючий ефект із константою інгібування 1 нмоль/л або менше. Крім того, сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, використовувана в даному винаході, є переважно сполукою, що має селективну афінність щодо аденозинових рецепторів A2A серед різних субтипів аденозинових рецепторів. Наприклад, переважною є сполука, що має більш високу афінність щодо аденозинових рецепторів A2A, ніж до аденозинових рецепторів A. Зокрема, наприклад, переважною сполукою є сполука, що має 5 кратну або більшу афінність, більш переважно 10 кратну або більшу афінність, додатково переважно 50 кратну або більшу афінність, ще більш переважно 100 кратну або більшу афінність, найбільш переважно 500 кратну або більшу афінність щодо аденозинових рецепторів A2A ніж щодо аденозинових рецепторів A1, Афінність може бути визначена звичайним способом, наприклад, відповідно до способу Тестового Прикладу 1, описаного нижче, або способів, описаних, наприклад, в Naunyn Schmiedebergs Arch Pharmacol. 1987, 355(1), стор. 59-63; Naunyn Schmiedebergs Arch Pharmacol. 1987, 355(2), стор. 204-210; або Br. J. Pharmacol. 1996, 117(8), стор. 1645-1652. Сполуки, представлені наступними формулами (I) - (VII) або їх фармацевтично прийнятні солі, є більш конкретними прикладами сполук, що мають селективну антагоністичну активність щодо аденозинових рецепторів A2A даного винаходу. [Хімічна Формула 18] NH2 N O N N N R1 O N N R3 N N N R2 S N N N ( II ) O N N N O O (I) ( III ) H3C S N S NH2 6 CH3 R N CH3 1 N 3 4 5 N S NH H3C O ( VI ) 6 N N N N (V) 2 O N O N N CH3 N ( IV ) N N N N N 35 R5 NH NH2 R4 N H2N NH2 ( VII ) (де R , R , R , R , R , і R мають ті ж самі визначення, як описано вище, відповідно). Сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A 2A даного винаходу, є більш переважною сполукою, представленою наступною формулою (I) або (II), або її фармацевтично прийнятними солями. 9 UA 102106 C2 [Хімічна Формула 19] NH2 N N N O N N N R1 O NH R3 N 10 O O (I) 5 R2 S 1 2 ( II ) 3 (де R , R , і R мають ті ж самі визначення, як описано вище, відповідно). Більш конкретно, наприклад, сполука, представлена наступними формулами (IA), (IB), (IIA), (IIB), (IIC), (IID), (IIIA), (IIIB), (IV), (VA), (VI), або (VII), або її фармацевтично прийнятна сіль є переважними, і сполука, представлена наступними формулами (IA), (IB), (IIA), (IIB), (IIC), або (IID) є ще більш переважною. [Хімічна Формула 20] NH2 NH2 N N N O HO N HO H3C N O CH3 ( IIA ) O N O NH O N NH N ( IIB ) O S N N ( IID ) NH2 N O N F N NH2 F N N N N N N N ( IIIA ) O N N N N N N O O O ( IIC ) CH3 O O NH CH3 O O N S CH3 O O O N S ( IIIB ) H3C S NH2 N S N CH3 H3C(H2C)3 N N N N N N N O N O N S NH N N CH3 H3C O ( VA ) ( VI ) N N N N CH3 ( IV ) N O O ( IB ) O 20 NH S N ( IA ) 15 O O N N N N N N N N H2N NH2 ( VII ) Фармацевтично прийнятні солі сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, використовувані в даному винаході, включають, наприклад, фармацевтично прийнятні кислотно-адитивні солі, солі металів, солі амонію, солі приєднання органічного аміну, амінокислотно-адитивні солі, і подібні. Фармацевтично прийнятні кислотно-адитивні солі сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, використовувані в даному винаході, включають, наприклад, солі неорганічних кислот, такі як гідрохлорид, гідробромат, 10 UA 102106 C2 5 10 15 20 25 30 35 40 45 50 55 60 нітрат, сульфат і фосфат; солі органічних кислот, такі як ацетат, оксалат, малеат, фумарат, цитрат, бензоат і метансульфонат, і подібні. Приклади фармацевтично прийнятних солей металів включають солі лужних металів, такі як сіль натрію і калію; солі лужноземельних металів, такі як сіль магнію і сіль кальцію; сіль алюмінію; сіль цинку, і подібні. Приклади фармацевтично прийнятних солей амонію включають солі амонію, тетраметиламонію і подібні. Приклади фармацевтично прийнятних органічних солей приєднання аміну включають адитивні солі морфоліну, піперидину або подібні. Приклади фармацевтично прийнятних амінокислотноадитивних солей включають адитивні солі лізину, гліцину, фенілаланіну, аспарагінової кислоти, глутамінової кислоти або подібні. Сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A 2A, або її фармацевтично прийнятна сіль, використовувана в даному винаході, може бути одержана загальноприйнятними способами, відповідно. Наприклад, сполука (I) може бути одержана способами, описаними, наприклад, в WO98/42711, WO00/17201, або подібними. Сполука (II) може бути одержана способами, описаними, наприклад, в WO2005/063743, або подібними. Сполука (III) може бути одержана способами, описаними, наприклад, в WO2001/092264, або подібними. Сполука (IV) може бути одержана способами, описаними, наприклад, в WO2002/055524, або подібними. Сполука (V) може бути одержана способами, описаними, наприклад, в WO2003011864, або подібними. Сполука (VI) може бути одержана способами, описаними, наприклад, в WO2006/032273, або подібними. Сполука (VII) може бути одержана способами, описаними, наприклад, в WO2002/055083, або подібними. Сполуки, що мають селективну антагоністичну активність щодо аденозинових рецепторів A2A, використовувані в даному винаході, можуть існувати як стереоізомери, такі як геометричні ізомери або оптичні ізомери, або таутомери. Вони й всі інші можливі ізомери та їх суміші можуть також застосовуватися як, наприклад, терапевтичні та/або профілактичні засоби проти мігрені. Щоб одержати сіль сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, використовувану в даному винаході, коли сполуку одержують у формі солі, її необхідно очистити. Крім того, коли сполуку одержують у вільній формі, сполуку можна розчинити або суспендувати у прийнятному розчиннику з наступним додаванням кислоти або основи, щоб утворити сіль. Потім одержану сіль можеа виділити й очистити. Сполуки, що мають селективну антагоністичну активність щодо аденозинових рецепторів A2A, або їх фармацевтично прийнятні солі, використовувані в даному винаході, можуть існувати у формі аддукта з водою або різними розчинниками. Такі аддукти можуть також застосовуватися як, наприклад, терапевтичні та/або профілактичні засоби проти мігрені, і в способах лікування та/або профілактики мігрені згідно з даним винаходом. Приклади розладів, які можуть підлягати лікуванню та/або профілактиці, наприклад, терапевтичними та/або профілактичними засобами проти мігрені, і способами лікування та/або профілактики мігрені даного винаходу, включають різні типи мігрені, представлені, наприклад, в The International Classification of Headache Disorders, 2-е вид. (ICHD-II) (The International Headache Society (IHS) 2003). Конкретні приклади включають: мігрень без аури, мігрень із аурою, ювенільні періодичні синдроми (із частим переходом у мігрень), ретинальну мігрень, ускладнення мігрені, ймовірну мігрень, і т.п. Вони включають мігрень у жінок під час менструації, таку як менструальна мігрень, мігрень у молодому віці, таку як ювенільна мігрень, і т.п. Далі конкретно описується біологічна активність представлених сполук, що мають селективну антагоністичну активність щодо аденозинових рецепторів A2A, базуючись на Тестових Прикладах. Тестовий Приклад 1: Зв'язувальна активність аденозинових рецепторів (1) Тест на зв'язування аденозинових рецепторів A2A Тест виконували відповідно до способу Bruns та ін. (Молекулярна Фармакологія, том 29, стор.331, 1986). Полосате тіло пацюка (пацюк SD, Japan SLC, Inc) суспендували в 50 мл охолодженого льодом трис(гідроксиметил)амінометангідрохлоридного (Трис HCl) буфера (50 ммоль/л, 7,7), використовуючи гомогенізатор Polytron (Kinematica, Inc). Суспензію центрифугували (48 000 об./хвил., 20 хвилин), і одержаний осад ресуспендували, додаючи до нього ту ж саму кількість буфера Трис HCl (50 ммоль/л), з наступним центрифугуванням в тих же самих умовах. Одержаний кінцевий осад суспендували у буфері Трис HCl (50 ммоль/л) [що містив хлорид магнію (10 ммоль/л), і аденозиндеаміназу (0,02 одиниць/мг тканини) (Sigma)], щоб одержати суспензію при концентрації тканини 5 мг (волога вага)/ мл. 3 До 100 мкл очищеної суспензії клітин додавали 80 мкл міченого тритієм CGS-21680 { H-2-[п(2-карбоксиетил)фенетиламіно]-5’-(N-етилкарбоксамідо)аденозину: 40 Кюрі/ммоль; New England Nuclear [The Journal of Pharmacology and Experimental Therapeutics, том 251, стор. 888, 1989]} 11 UA 102106 C2 5 10 (заключна концентрація 6,0 ммоль/л) і 20 мкл розчину тестової сполуки (розчин тестової сполуки у диметилсульфоксиді, розведений Трис HCl буфером). Суміші дозволяли відстоятися при 25 °C протягом 120 хвилин, потім піддавали швидкій аспіраційній фільтрації, використовуючи скловолокнистий фільтрувальний папір (GF/C; Whatman), і потім негайно промивали три рази з 200 мкл охолодженого льодом буфера Трис HCl (50 ммоль/л). Скловолокнистий фільтрувальний папір потім поміщали у флакон і додавали рідину MicroScinti (PKI). Потім вимірювали радіоактивність з TopCount (PerkinElmer). Відсоток інгібування зв'язування аденозинового рецептораA2A (3H-CGS21680 зв'язування) тестовою сполукою може бути обчислений за наступним рівнянням. [Рівняння 1] Величина зв язування в присутності медикамент а - величина неспецифіч ного зв язування Відсоток інгібування (%) 1 100 язування - величина неспецифіч ного Загальна величина зв зв язування 3 15 20 25 30 35 40 45 У рівнянні загальна величина зв'язування відноситься до зв'язування радіоактивного HCGS21680 за відсутності тестової сполуки. Величина неспецифічного зв'язування відноситься 3 до зв'язування радіоактивного H-CGS21680 у присутності 100 мкмоль/л циклопентиладенозину (CPA; Sigma). Величина зв'язування в присутності медикаменту відноситься до зв'язування 3 радіоактивного H-CGS21680 у присутності тестової сполуки. У вищезгаданому тесті відсоток інгібування для аденозинових рецепторів A 2A при різних концентраціях тестової сполуки або її фармацевтично прийнятної солі, і концентрація тестової сполуки, при якій тестова сполука інгібує зв'язування на 50 % (IC50), можуть бути обчислені відповідним регулюванням концентрації тестової сполуки. Константа інгібування (значення Ki) тестової сполуки для зв'язування аденозинового рецептора A2A може бути обчислена відповідно до наступного рівняння. [Рівняння 2] Ki=IC50 / (1+L/Kd) 3 У рівнянні L означає концентрацію H-CGS21680, використовуваного в тесті, і Kd - константа 3 дисоціації H-CGS21680, використовуваного в тесті. 3 3 3 Замість H-CGS21680 може використовуватися, наприклад, H-SCH58261 [ H-5-аміно-7-(2фенілетил)-2-(2-фурил)піразол[4,3-e]-1,2,4-триазол[1,5-c]піримідин (синтезований GE healthcare bio-sciences)]. Афінність тестової сполуки щодо аденозинових рецепторів A2A може бути підтверджена попереднім тестом. (2) Тест на зв'язування аденозинового рецептора А1 Константа інгібування (значення Ki) тестової сполуки для аденозинових рецепторів A 1 може бути обчислена тим же самим способом як в (1), використовуючи матеріали, наведені нижче. Зокрема, наприклад, використовується клітинна мембрана пацюка, що експресує рецептор A1 (PerkinElmer) і, наприклад, мічений тритієм CHA [N6-циклоаденозин (PerkinElmer)] використовуються як мічена сполука. Для вимірювання величини неспецифічного зв'язування, 3 зв'язування радіоактивного H-CHA вимірювали в присутності, наприклад, 10 мкмоль/л DPCPX [1,3-дипропіл-8-циклопентилксантину (Sigma)]. Афінність тестової сполуки щодо аденозинових рецепторів A1 може бути підтверджена попереднім тестом. Попередніми тестами (1) і (2) можуть бути підтверджені селективні афінності сполук (I) - (VII) і т.п. щодо аденозинових рецепторів A2A. Деякі із прикладів афінностей щодо аденозинових рецепторів A 2A, як визначено попереднім тестом із сполуками, що мають селективну антагоністичну активність щодо аденозинових рецепторів A2A, або їх фармацевтично прийнятними солями, використовуваними в даному винаході, представлені нижче. 50 12 UA 102106 C2 Таблиця 1 3 № Сполуки (IA) (IB) Відсоток інгібування зв'язування аденозинового рецептора A2A ( H-CGS21680 зв'язування) 75 %* 81 % ** *: Відсоток інгібування при 100 нмоль/л сполуки (IA) **: Відсоток інгібування при 1 000 нмоль/л сполуки (IB) 5 10 15 Тестовий Приклад 2: Зв'язувальна активність аденозинових рецепторів (2) (1) Тест на зв'язування людських аденозинових рецепторів A2A Тест виконують відповідно до способу, наприклад, Varani та ін. [[British Journal of Pharmacology, том 117, стор.1693 (1996)]. Зокрема, наприклад, людські рекомбінантні аденозинові рецептори A2A експресували в клітинах HEK-293. Клітинні мембрани рецептор-експресуючих клітин збирали і одержували суспензію клітинних мембран. Після розбавлення з буфером Трис HCl, до суспензії клітинних мембран додавали мічений тритієм CGS-21680 (50 ммоль/л) і розчин тестової сполуки (розчин тестової сполуки у диметилсульфоксиді) для зв'язування з рецепторами. Після реакції суміш піддавали швидкій аспіраційній фільтрації, використовуючи скловолоконний фільтрувальний папір, і вимірювали радіоактивність скловолоконного фільтрувального паперу. Таким чином, може бути визначений відсоток інгібування тестової сполуки для зв'язування аденозинового 3 рецептора A2A ( H-CGS21680 зв'язування). Відсоток інгібування може бути обчислений відповідно до наступного рівняння. [Рівняння 3] Величина зв язування в присутності медикамент а - величина неспецифіч ного зв язування Відсоток інгібування (%) 1 100 язування - величина неспецифіч ного Загальна величина зв зв язування 20 25 30 35 3 У рівнянні загальна величина зв'язування відноситься до зв'язування радіоактивного HCGS21680 за відсутності тестової сполуки. Величина неспецифічного зв'язування відноситься 3 до зв'язування радіоактивного H-CGS21680 у присутності 50 мкмоль/л 5’-Nетилкарбоксамідаденозину (NECA) або 100 мкмоль/л CPA. Величина зв'язування в присутності 3 медикаменту відноситься до зв'язування радіоактивного H-CGS21680 у присутності тестової сполуки. У вищезгаданому тесті відсоток інгібування людських аденозинових рецепторів A 2A при різних концентраціях тестової сполуки або її фармацевтично прийнятної солі, і концентрація тестової сполуки, при якій тестова сполука інгібує зв'язування на 50 % (IC50) можуть бути обчислені, відповідно регулюючи концентрацію тестової сполуки. Константа інгібування (значення Ki) тестової сполуки зв'язування людських аденозинових рецепторів A2A може бути обчислена відповідно до наступного рівняння. [Рівняння 4] Ki=IC50 / (1+L/Kd) 3 40 45 У рівнянні L означає концентрацію H-CGS21680, використовуваного в тесті, і Kd - константа 3 дисоціації H-CGS21680, використовуваного в тесті. 3 3 Замість H-CGS21680, наприклад, може використовуватися H-SCH58261. (2) Тест на зв'язування людських аденозинових рецепторів А1 Константа інгібування (значення Ki) тестової сполуки для людських аденозинових рецепторів A1 може бути обчислена тим же самим способом як в (1), використовуючи матеріали, наведені нижче. Зокрема використовуються, наприклад, клітинні мембрани CHO, що експресують людські рецептори А1, і використовується, наприклад, мічений тритієм DPCPX як мічена сполука. Величина неспецифічного зв'язування може бути визначена, вимірюючи радіоактивність 3 6 зв'язування H-DPCPX у присутності, наприклад, 100 мкмоль/л R(-)-PIA((-)-N -2 13 UA 102106 C2 5 10 фенілізопропіладенозину). Афінність тестової сполуки щодо людських аденозинових рецепторів A1 може бути підтверджена аналогічним способом. Попередніми тестами (1) і (2) можуть бути підтверджені селективні афінності сполук (I) - (VII) та подібних шодо людських аденозинових рецепторів A2A. (3) Афінність сполуки або її фармацевтично прийнятної солі використана в даному винаході щодо людських аденозинових рецепторів. Деякі із прикладів афінностей сполук (IIA)-(IID) для людських аденозинових рецепторів A1 і людських аденозинових рецепторів A2A представлені нижче. Слід зазначити, що результати тесту, наведеного нижче, є результатами вимірів, виконаних MDS Pharma Services Inc відповідно до попередніх способів. Таблиця 2 Афінність щодо аденозинових рецепторів Відсоток інгібування зв'язування людських Відсоток інгібування зв'язування 3 № Сполуки аденозинових рецепторів A2A ( H- людських аденозинових рецепторів A1 3 CGS21680 зв'язування) * ( H-DPCPX зв'язування) * (IIA) 92 % 14 % (IIB) 98 % 4% (IIC) 88 % 29 % (IID) 100 % 28 % *Відсоток інгібування при100 нмоль/л сполуки 15 20 25 30 35 40 45 Селективні афінності сполук (IIA) - (IID) для людських аденозинових рецепторів A 2A були підтверджені попередніми тестами. Тестовий Приклад 3: Ефект церебральної вазоконстрикції Собаки були анестезовані внутрішньовенним призначенням фенобарбіталу натрію, знекровлені декапітацією і піддані краніотомії. Базилярні артерії вилучали і одержували кільцеві зразки церебральних судинних гладких м'язів, шириною приблизно 2 мм, . Кожен кільцевий зразок був фіксований до ін'єкційної голки (зріз фрагменту 2 мм) шовковою ниткою. Ін'єкційна голка була зафіксована у штативі, установленому в Easy Magnus Device (Модель: UC-2; Kishimoto Medical Instruments), і зразок залишали стабілізуватися протягом 60 хвилин або більше при напрузі спокою 0,2 г (1,96 мN) при 37C в живильному розчині. Мозковий судинний гладкий м'яз розслабляли з 2 мкл водного розчину аденозину (10 ммоль/л), доданого до ванни (2 мл) Easy Magnus Device, і тестову сполуку додавали кумулятивно як 1 мкл розчин диметилсульфоксиду 0,2 ммоль/л, 1 мкл розчин диметилсульфоксиду 0,4 ммоль/л, і 0,7 мкл розчин диметилсульфоксиду 2 ммоль/л у цьому порядку (група додавання тестової сполуки). Окремо, тим же самим способом, як у групі призначення тестових сполук, кумулятивно додавали лише один диметилсульфоксид замість тестової сполуки (група додавання розчинника). Скорочення церебральних судинних гладких м'язів потім реєстрували на записному пристрої (Yokogawa Electric Corporation) від датчика (Nihon Kohden Corporation), з'єднаного із штативом, на якому зразок був зафіксований, через підсилювач тиску напруги (Nihon Kohden Corporation) (n=6). Було підтверджено розслаблення вилучених церебральних судинних гладких м'язів додаванням аденозину. Ефект церебральної вазоконстрикції буввизначений як відсоток інгібування (%) індукованого аденозином розслаблення гладких м'язів церебральних судин, і порівняння було зроблено між групою додавання тестової сполуки і групою додавання розчинника. Тест демонструє, що сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A або її фармацевтично прийнятна сіль даного винаходу, може пригнічувати індуковану аденозином цереброваскулярну релаксацію. Результат попереднього тесту підтвердив, що група додавання сполук (IIC; 10 нмоль/л), мала значний ефект пригнічення (відсоток інгібування: 97,4±1,8 %) щодо групи додавання розчинника (відсоток інгібування: 0,6±7,6 %). Ефект був також підтверджений наприклад, сполукою (IB). Таким чином, результат припускає, що сполуки, які мають селективну антагоністичну активність щодо аденозинових рецепторів A2A, такі як сполуки (I) - (VII) та ін. або їх фармацевтично прийнятні солі, є корисними як терапевтичні та/або профілактичні засоби проти 14 UA 102106 C2 5 10 15 20 25 30 35 40 45 50 55 60 мігрені. Тестовий Приклад 4: Ефект збільшення церебрального кровотоку елекростимуляцією трійчастого нерва у анестезованих пацюків Тест здійснювали відповідно до способу Tsukahara та ін. [Cerebral Blood Flow and Metabolism, том 14, стор. 8 (2002)]. Пацюків SD (самці, Charles River) анестезували інтраперитонеальним введенням фенобарбіталу натрію (60 мг/кг; Tokyo Chemical Industry Co., Ltd). Цервікальна область кожного пацюка відкривали розсіченням, і вставляли трахеальний зонд. Зонд вимірювання кров'яного тиску вставляли у праву стегнову артерію. Пацюка фіксували до стереотаксичного інструмента (стереотаксичний інструмент для пацюків; Summit Medical), і температуру тіла підтримували при 37 електрогрілкою (Модель: CMA/150; Carnegie Medicine). Электротрепан (Модель: C-201; C Urawa Kogyo), використовували, щоб утворити краніальне вікно з діаметром 5 мм (центральні координати черепного вікна AP:-1,5, L:-1, Н:-1,5), і вимірювали мозковий кровоток. Для вимірювання церебрального кровотоку використовували лазерний доплеровський витратомір (Модель: ALF-2100; Advance). Кожне значення кров'яного тиску реєстрували на записному пристрої (Модель: PE3066; Yokogawa Electric Corporation) через вимірювання від датчика тиску (Модель: DX-312, Nihon Kohden Corporation) через підсилювач тиску напруги (Модель: AP612GA; Nihon Kohden Corporation), використовуючи поліграфічну систему (Модель: RM6000; Nihon Kohden Corporation). Артеріальний парціальний тиск газу крові (рН, PaО 2, PaCO2) вимірювали, використовуючи комп'ютерну систему дослідження крові (Модель: AVL-OPTI-CCA; Sysmex). Дистальну частина трійчастого нерва відділяли і фіксували до стимуляційного біполярного електрода (вольфрамовий дріт, 5 мм шириною). Для електростимуляції встановлювали прямокутну хвилю (30 Гц, 2-8 V), що показала максимальне збільшення кровотоку, накладену через трійчастий нерв, використовуючи біоелектростимулятор (Модель: SEN-3301; Nihon Kohden Corporation) і ізолятор (Модель: SS-201J; Nihon Kohden Corporation). Електростимуляцію трійчастого нерва проводили протягом 30 секунд в 5-хвилинних інтервалах, і тестову сполуку або розчинник давали після того, як стимульоване збільшення кровотока стало стабільним. Вимірювали зміни в мозковому кровотоці при електростимуляції через 10, 20 і 30 хвилин від призначення, і порівнювали ефекти тестової сполуки і розчинника. Коли сполука, що має антагоністичну активність щодо аденозинових рецепторів A 2A даного винаходу використовувалася як тестова сполука, збільшення інтракраніального церебрального кровотоку, шляхом активації трійчастого нерва, пригнічувалося у групі призначення тестових сполук. Вважається, виходячи з цих результатів, що сполуки, які мають селективну антагоністичну активність щодо аденозинових рецепторів A2A, такі як сполуки (I) - (VII) і подібні, або їх фармацевтично прийнятні солі, ефективні як терапевтичні та/або профілактичні засоби проти мігрені. Тестовий Приклад 5: Ефект на транссудацію у тверду мозкову оболонку, індуковану елекростимуляцією трійчастого нерва у анестезованих пацюків. Пацюки SD (самці, Charles River) були анестезовані інтраперитонеальним введенням фенобарбіталу натрію (60 мг/кг; Tokyo Chemical Industry Co., Ltd). Дистальна частина трійчастого нерва була відділена, і зафіксована до стимуляційного біполярного електрода (вольфрамовий дріт, 5 мм шириною). Через 5 хвилин після внутрішньовенного введення Evans Blue (10 ваг/об %, 30 мл/кг; Sigma), трійчастий нерв піддавали еклектростимуляції протягом 30 секунд тим же самим способом, як в Тестовому Прикладі 3. Після безпосередньої транскардіальної перфузії з фізіологічним сольовим розчином протягом 5 хвилин тверду мозкову оболонку вилучали і зважували, щоб визначити вологу вагу. Evans Blue у твердій мозковій оболонці екстрагували з формамідом (Wako Pure Chemical Industries, Ltd) при 60C протягом 24 годин, і оптичну щільність при 625 нм вимірювали, використовуючи абсорбційний спектрометр (Модель: Power Wave X; Bio-Tec-Instrument). Концентрацію Evans Blue в екстракті обчислювали від стандартної кривої, створеної від стандартного зразка Evans Blue, і врівноваженої вагою твердої мозкової оболонки. Тестову сполуку або розчинник вводили за 30 хвилин до електростимуляції. Витік Evans Blue у тверду мозкову оболонку порівнювали між групою призначення тестових сполук і групою призначення розчинника. Було продемонстровано, що транссудація у тверду мозкову оболонку, заснована на активації трійчастого нерва, може бути пригнічена в групі призначення тестових сполук, коли сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A 2A даного винаходу, використовуються як тестова сполука. Вважається, виходячи з цих результатів, що сполуки, які мають селективну антагоністичну 15 UA 102106 C2 5 10 15 20 25 30 35 40 45 50 55 60 активність щодо аденозинових рецепторів A2A, такі як сполуки (I) - (VII) і т.п. їх або фармацевтично прийнятні солі, ефективні як терапевтичні та/або профілактичні засоби проти мігрені. Тестовий Приклад 6: Ефект на кортикальну поширювану депресію у анестезованих пацюків. Тест був виконаний, використовуючи як покажчик повторне збільшення вторинного мозкового кровотоку кортикальною поширюваною депресією [NeuroReport, том 17, стор. 1709 (2006)]. Є повідомлення, що профілактичні препарати проти мігрені мають ефекти пригнічення для кортикальної поширюваної депресієї [Annals of Neurology, том 59, стор. 652 (2006)]. SD пацюків (самці, Charles River) анестезували інтраперитонеальним введенням фенобарбіталу натрію (60 мг/кг; Tokyo Chemical Industry Co., Ltd). Цервікальну область відкривали розсіченням і вставляли трахеальний зонд. Зонд вимірювання кров'яного тиску вставляли у праву стегнову артерію. Пацюка фіксували до стереотаксичного інструмента (стереотаксичний інструмент для пацюків; Summit Medical) і температуру тіла підтримували при 37 електрогрілкою (Модель: CMA/150; Carnegie Medicine). Два краніальних вікна, кожний з C діаметром приблизно 5 мм, формували по корі головного мозку (краніальне вікно для вимірювання мозкового кровотоку; AP:-1,5, L:-1, Н:-1,5, і краніальне вікно використовували для додавання розчину хлориду калію; AP:-4,5, L:-1, Н:-4,5). Для вимірювання церебрального кровотоку використовували лазерний доплеровський витратомір (Модель: ALF-2100; Advance). Значення кров'яного тиску реєстрували на записному пристрої типу ручки (Модель: Тип 3066; Yokogawa Електрична Корпорація) через вимірювання від датчика тиску (Модель: DX-312; Nihon Kohden Corporation) через підсилювач тиску напруги (Модель: AP-612GA; Nihon Kohden Corporation), використовуючи поліграфічну систему (Модель: RM6000; Nihon Kohden Corporation). Артеріальний парціальний тиск газу крові (pH, PaO 2, PaCO2) вимірювали, використовуючи комп'ютерну систему дослідження крові (Модель: AVL-OPTI-CCA; Sysmex). Після додавання розчину хлориду калію (2 моль/л, 0,01 мл) через краніальне вікно, вимірювали зміни в мозковому кровотоці за період понад 30 хвилин, щоб оцінити кортикальну поширювану депресію. Тестову сполука або розчинник застосовували за 30 хвилин до додавання хлориду калію. Вплив на повторне збільшення церебрального кровотоку порівнювали між групою призначення тестових сполук й групою розчинника. Було продемонстровано, що повторне збільшення церебрального кровотоку може бути пригнічено в групі призначення тестових сполук, коли сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A або її фармацевтично прийнятна сіль даного винаходу, використовуються як тестова сполука. Вважається, виходячи з результату тесту, що сполуки, які мають селективну антагоністичну активність щодо аденозинових рецепторів A2A, такі як сполуки (I) - (VII) або подібні, або їх фармацевтично прийнятні солі, є ефективними як профілактичні засоби проти мігрені. Також вважається, виходячи з результату тесту, що медикаментозна резистентність не розвивається повторним призначенням сполук, що мають селективну антагоністичну активність щодо аденозинових рецепторів A2A, таких як сполуки (I) - (VII) або подібні, або їх фармацевтично прийнятні солі. Сполука даного винаходу, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A або її фармацевтично прийнятна сіль, може призначатися самостійно. Однак, звичайно, сполука даного винаходу, що має антагоністичну активність щодо аденозинових рецепторів A2A або її фармацевтично прийнятна сіль переважно вводяться в різних фармацевтичних препаратах. Такі фармацевтичні препарати можуть використовуватися для тварин і людей. Фармацевтичний препарат відповідно до даного винаходу може містити як активний інгредієнт сполуку, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A або її фармацевтично прийнятну сіль, самостійно або як суміш із будь-яким іншим терапевтичним активним інгредієнтом. Крім того, ці фармацевтичні препарати одержують, змішуючи активний інгредієнт із одним або кількома фармацевтично прийнятними носіями (наприклад, розріджувачами, розчинниками, наповнювачами або подібними), і потім піддаючи суміш будь-якому способу формування, відомому в галузі технології лікарських форм. Що стосується шляхів введення, переважно, вибрати найбільш ефективний шлях введення для лікування. Приклади шляхів введення включають пероральний прийом і парентеральне введення, наприклад, таке як внутрішньовенне, назальне і інгаляційне введення. Приклади дозованих форм включають таблетки, ін'єкції, назальні препарати, інгаляції, і т.п. Прийнятні дозовані форми для перорального прийому, наприклад, таблетки, можуть бути одержані при використанні наповнювачів, таких як лактоза, дезінтегрантів, таких як крохмаль, лубрикантів, таких як стеарат магнію, або зв'язуючих, таких як гідроксипропілцелюлоза, або 16 UA 102106 C2 5 10 15 20 25 30 35 40 45 50 55 60 подібні. Прийнятні дозовані форми для парентерального введення, наприклад, ін'єкції, можуть бути одержані при використанні розріджувачів або розчинників, таких як фізіологічний розчин, розчин глюкози, або суміші сольового розчину і глюкози, або подібних. Назальний препарат може бути одержаний як розчин, наприклад, додаванням активного інгредієнта до стерильної очищеної води з додатковим(и) інгредієнтом(ами), включаючи, наприклад, агенти ізотонічності, такі як хлорид натрію, антисептики, такі як естер пгідроксибензойної кислоти, буферні засоби, такі як фосфатний буфер, або подібні. Альтернативно, назальний препарат може бути одержаний як суспензія, змішуючи активний інгредієнт із диспергатором(ами), таким(и) як поліетиленгліколь 400, або подібні, або як порошок, змішуючи активний інгредієнт із носієм(ями), таким(и) як гідроксипропілцелюлоза з додатковим(и) інгредієнтом(ами), включаючи, наприклад, мукозо-адгезувальну основу, таку як Carbopol, або подібні. Інгаляційні форми можуть бути одержані, змішуючи активний інгредієнт або в порошковій, або в рідкій формі в інгаляційний аерозоль або носій, і наповнюючи суміш в інгалятор(и), наприклад, такий(і) як дозований(і) інгалятор(и), небулайзер(и) або сухий(і) порошковий(і) інгалятор(и). Широкий діапазон традиційно відомих інгаляційних аерозолів може використовуватися, включаючи, наприклад, хлорфторвуглецевий газ, такий як CFC-11; альтернативний газ CFC, такий як HFA-227; вуглеводневий газ, такий як пропан, ізобутан, і нбутан; діетиловий етер; газоподібний азот; вуглекислий газ, і т.п. Широкий діапазон традиційно відомих носіїв може використовуватися, включаючи, наприклад, цукри, цукрови спирти, амінокислоти, і т.п. Переважні приклади включають лактозу, D-манітол і т.п. Дози і частота введення сполуки даного винаходу, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, або її фармацевтично прийнятної солі, можуть змінюватися залежно від дозованої форми, віку й маси тіла пацієнта, природи або серйозності симптому, що буде підлягати лікуванню, або подібних. При пероральному призначенні, загалом, доза 0,001-1000 мг, переважно, 0,05-100 мг, застосовується дорослому пацієнтові один раз або кілька разів на день. При парентеральному призначенні, такому як внутрішньовенне введення, назальне введення, і інгаляція, загалом, доза 0,001-1000 мг, переважно, 0,01-100 мг, застосовується дорослому пацієнтові один раз або кілька разів на день. Однак, ці дози й частота введення змінюються залежно від різних станів, описаних вище. Даний винахід, включаючи терапевтичні та/або профілактичні засоби проти мігрені, і способи лікування та/або профілактики мігрені, має переважний терапевтичний та/або профілактичний ефект щодо головного болю, такого як мігрень. Додатково, як описано вище, сполуки, що мають антагоністичну активність щодо аденозинових рецепторів A 2A, включаючи, наприклад, сполуки (I) - (VII) і т.п., або їх фармацевтично прийнятні солі можуть використовуватися в комбінації з одним або кількома іншими фармацевтичними інгредієнтами. Приклади інших фармацевтичних інгредієнтів, використовуваних у комбінації, включають відомі медикаменти, корисні як, наприклад, терапевтичні та/або профілактичні засоби від головного болю, наприклад, такого як мігрень (Pharmacology & Therapeutics, 2006, 112, стор. 199-212). Конкретні приклади включають 5-HT1 агоністи [наприклад, триптани, такі як алмотриптан, елетриптан, фроватриптан, наратриптан, ризатриптан, суматриптан, і золмітриптан; 5-HT1D агоністи, такі як PNU-109291, і PNU-142633; 5-HT1F агоністи, такі як LY334370; і т.п.], агоністи γ-аміномасляної кислоти [наприклад, такі як вальпроат, і дивальпроекс], антагоністи допаміну [наприклад, такі як дроперидол, і локсапін], модулятори глутамату [наприклад, неселективні антагоністи -аміно-3-гідрокси-5-метил-4ізоксазолпропіонової (AMPA)/каїнової кислоти (KA) антагоністи (неселективні антагоністи AMPA/KA), такі як LY293558, і E2007; метаботропні модулятори глутаматних рецепторів, такі як ADX-10059; антагоністи NR2B, такі як CP-101, 606; антагоністи гліцинових сайтів, такі як ZD9379; і т.п.], агоністи аденозинових рецептрів A1 [наприклад, такі як GR79236], антагоністи кальцитонінового пептиду, пов'язаного з геном (CGRP) [наприклад, такі як BIBN4096BS, і MKG0974], інгібітори синтази оксиду азоту (NO) [наприклад, такі як гідрохлорид N метил-L-аргінін (546C88), і GW-274150], модулятори ванілоїдних рецепторів [наприклад, такі як капсаїцин, цивамід, і зукапсаїцин], агоністи рецепторів соматостатину, модулятори ангіотензину [наприклад, інгібітори рецепторів ангіотензину II (AT)-1, такі як кандесартан; інгібітори ангіотензин-конвертуючого ензиму (АКЕ), такі як лізиноприл; і т.п.], антидепресанти [наприклад, такі як амітриптилін, венлафаксин, мітразапін, мільнаципран, і дулоксетин], антиепілептичні препарати [наприклад, габапентиноїди, такі як габапентин, і прегабалін; топірамат; Srx-502; зонізамід; лонозамід; і т. п.], блокатори кальцієвих каналів [наприклад, такі як верапаміл, флунаризин, ломеризин, і німодипін], ацетоамінофени, ізометептани, ерготамінові 17 UA 102106 C2 5 10 15 20 25 30 35 40 45 50 55 60 алкалоїди[наприклад, такі як ерготамін, і дигідроерготамін], нестероїдні протизапальні засоби (НПЗЗ) [наприклад, такі як аспірин, диклофенак, флурбіпрофен, ібупрофен, кетопрофен, мефенамінова кислота, напроксен, рофекоксиб, толфенамінова кислота, і німесулід], модулятори адренергічних рецепторів [наприклад, 2-адренергічні агоністи, такі як клонідин, і тізанідин; - -адренергічні блокатори, такі як атенолол, метопролол, надолол, пропранолол, тімолол; і т.п.], 5-HT2 антагоністи [наприклад, такі як метисергід, і пізотифен], агоністи сігми рецепторів (R1) [наприклад, такі як декстрометорфан, карбетапентан, і 4-IBP], модулятори Kпотоку, підсилювачі каналів іонів хлору [наприклад, такі як BTS72664], модулятори конексинових геміканалів [наприклад, такі як фенамат НПЗЗ], магній, рибофлавін, кофермент Q10, ботуліничний токсин, тонабераст, стероїдні протизапальні препарати [наприклад, такі як дексаметазон], модулятори ацетилхолінових рецепторів [наприклад, такі як донепезил], і т.п. Дозована форма сполуки, що має антагоністичну активність щодо аденозинових рецепторів A2A, такої як сполуки (I) - (VII) або подібні, або її фармацевтично прийнятної солі, коли використовуються в комбінації з іншим(и) фармацевтичним(и) інгредієнтом(ами) особливо не обмежена, поки (a) сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, така як сполуки (I) - (VII) або подібні, або їх фармацевтично прийнятна сіль, і (b) інший фармацевтичний(і) інгредієнт(и) скомбіновані під час призначення. Наприклад, інгредієнти (a) і (b) можуть використовуватися або призначатися як єдиний засіб (комбінований засіб) або як комбінація більше, ніж одного препарату, за умови, що ці засоби одержані і містять ці інгредієнти. Коли призначаються як комбінація більше, ніж одного препарату, препарати можуть призначатися одночасно або послідовно. Переважно, ці препарати використовуються у формі, наприклад, таблетки, ін'єкції, назальних форм, інгаляційних форм або подібних. Крім того, ці препарати одержують, використовуючи будь-який спосіб, відомий у галузі технології лікарських форм, як описано вище. Коли призначається комбінація більше, ніж одного препарату, наприклад, (a) перший інгредієнт, що містить сполуку, яка має селективну антагоністичну активність щодо аденозинових рецепторів A2A, таку як сполуки (I) - (VII) або подібні, або їх фармацевтично прийнятну сіль, і (b) другий інгредієнт, що містить інший фармацевтичний(і) інгредієнт(и), можуть бути окремо одержані у комплекті, і можуть вводитися тому ж самому суб'єктові тим же самим шляхом або різними шляхами одночасно або послідовно, використовуючи комплект. Комплект забезпечується у формі двох або більше контейнерів (наприклад, флакони, пакети, або подібні, так, щоб перший й другий інгредієнти могли застосовуватися різними шляхами (наприклад, тюбик, або подібні) або тим же самим шляхом. Матеріал, форма або інші варіації контейнерів особливо не обмежені, поки, наприклад, інгредієнти контейнерів не змінюються у відповідь на зовнішню температуру або світло, або хімічні інгредієнти не розкладаються в контейнерах під час зберігання. Зокрема, комплект може бути для таблеток, ін'єкцій, назальних форм, інгаляцій, або подібних. Коли сполука, що має антагоністичну активність щодо аденозинових рецепторів A 2A, така як сполуки (I) - (VII) або подібні, або їх фармацевтично прийнятна сіль, використовуються в комбінації з іншим фармацевтичним(и) інгредієнтом(ами), (a) сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, така як сполуки (I) - (VII) або подібні, або їх фармацевтично прийнятна сіль, і (b) інший фармацевтичний(і) інгредієнт(и) можуть застосовуватися одночасно або послідовно. Дози змінюються залежно від комбінацій різних факторів, таких як суб'єкт призначення, шлях введення, розлад і фармацевтичний інгредієнт, і т.п., і повинні бути визначені відповідно до доз, використовуваних у клінічній практиці. Наприклад, при пероральному введенні у формі, наприклад, таблетки, загалом, (a) сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, такі як сполуки (I) - (VII) або подібні, або їх фармацевтично прийнятна сіль, і (b) інший(і) фармацевтичний(і) інгредієнт(и) дають в дозах 0,001-1 000 мг і 0,01-3 000 мг, переважно 0,05-1 000 мг і 0,1-3 000 мг, додатково переважно 0,05-100 мг і 0,1-3 000 мг, ще більш переважно 0,5100 мг і 0,1-3 000 мг, відповідно, дорослому пацієнтові один раз або кілька разів на день або одночасно, або послідовно. Крім того, наприклад, при парентеральному введенні у формі, наприклад, ін'єкції, загалом, (a) сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів A 2A, така як сполуки (I) - (VII) або подібні, або їх фармацевтично прийнятна сіль, і (b) інший(і) фармацевтичний(і) інгредієнт(и) дають в дозах 0,001-1 000 мг і 0,001-3 000 мг, переважно 0,001500 мг і 0,01-3 000 мг, додатково переважно 0,01-300 мг і 0,01-3 000 мг, ще більш переважно 0,01-100 мг і 0,01-3 000 мг, відповідно, дорослому пацієнтові один раз або кілька разів у день, або одночасно або послідовно. 18 UA 102106 C2 5 10 15 Дози і частота призначення (a) сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, такої як сполуки (I) - (VII) або подібних, або їх фармацевтично прийнятних солей, і (b) іншого(их) фармацевтичного(их) інгредієнта(ів) не обмежені попередніми прикладами, тому що дози й частота призначення відповідно встановлюються залежно від ефективності активних інгредієнтів, дозованої форми, віку й маси тіла пацієнта, симптому, і т.п. Наступне більш конкретно описує даний винахід за допомогою Прикладів. Потрібно відзначити, однак, що обсяг даного винаходу не обмежується наступними Прикладами. Приклад 1 Таблетка (Сполука IB) Таблетки, що мають наступні інгредієнти, одержували звичайним способом. Сполуку IB (40 г), лактозу (286,8 г), і картопляний крохмаль (60 г) змішували і потім до цього додавали 10 % водний розчин гідроксипропілцелюлози (120 г). Одержану суміш змішували звичайним способом, гранулювали і висушували, щоб утворити гранули для таблетування. Після додавання до них 1,2 г стеарату магнію суміш змішували, пресували на таблетувальній машині, що мав пуансон 8 мм у діаметрі (Модель RT-15; Kikusui), щоб одержати таблетки (що містять 20 мг активного інгредієнта на таблетку). Таблиця 3 Композиція Сполука ІB Лактоза Картопляний крохмаль Гідроксипропілцелюлоза Стеарат магнію 20 мг 143,4 мг 30 мг 6 мг 0,6 мг 200 мг Приклад 2 Таблетка (Сполука IIC) Таблетки, що мають наступні інгредієнти, одержували тим же самим способом як у Прикладі 20 1. Таблиця 4 Композиція Сполука ІIC Лактоза Картопляний крохмаль Гідроксипропілцелюлоза Стеарат магнію 20 мг 143,4 мг 30 мг 6 мг 0,6 мг 200 мг Приклад 3 Таблетка (Сполука IIIA) Таблетки, що мають наступні інгредієнти, одержували тим же самим способом як у Прикладі 25 1. Таблиця 5 Композиція Сполука ІIIA Лактоза Картопляний крохмаль Гідроксипропілцелюлоза Стеарат магнію 20 мг 143,4 мг 30 мг 6 мг 0,6 мг 200 мг 30 19 UA 102106 C2 Приклад 4 Таблетка (Сполука VA) Таблетки, що мають наступні інгредієнти, одержували тим же самим способом як у Прикладі 1. 5 Таблиця 6 Композиція Сполука VA Лактоза Картопляний крохмаль Гідроксипропілцелюлоза Стеарат магнію 10 20 мг 143,4 мг 30 мг 6 мг 0,6 мг 200 мг Приклад 5 Ін'єкція (Сполука IA) Ін'єкції, що мають наступні інгредієнти, одержували звичайним способом. Сполуку IA (1 г) додали до дистильованої води для ін'єкції, потім змішували. Після коригування рН суміші до 7, додаючи соляну кислоту і водний розчин гідроксиду натрію до неї, загальний об'єм доводили до 1000 мл дистильованою водою для ін'єкцій. Одержану суміш асептично розливали в скляні флакони 2 мл порціями, щоб одержати ін'єкції (що містять 2 мг активного інгредієнта на флакон). 15 Таблиця 7 Композиція Сполука ІA 2 мг Відповідна Соляна кислота кількість Водний розчин Відповідна гідроксиду натрію кількість Дистильована Відповідна вода для ін'єкцій кількість 2,00 мл Приклад 6 Ін'єкція (Сполука IIA) Ін'єкції, що мають наступні інгредієнти, одержували тим же самим способом як у Прикладі 5. 20 Таблиця 8 Композиція Сполука ІIA 2 мг Відповідна Соляна кислота кількість Водний розчин Відповідна гідроксиду натрію кількість Дистильована Відповідна вода для ін'єкцій кількість 2,00 мл Приклад 7 Ін'єкція (Сполука IV) Ін'єкції, що мають наступні інгредієнти, одержували тим же самим способом як у Прикладі 5. 25 20 UA 102106 C2 Таблиця 9 Композиція Сполука IV 2 мг Відповідна Соляна кислота кількість Водний розчин Відповідна гідроксиду натрію кількість Дистильована Відповідна вода для ін'єкцій кількість 2,00 мл 5 Приклад 8 Ін'єкція (Сполука VI), Ін'єкції, що мають наступні інгредієнти, одержували тим же самим способом як у Прикладі 5. Таблиця 10 Композиція Сполука VI 2 мг Відповідна Соляна кислота кількість Водний розчин Відповідна гідроксиду натрію кількість Дистильована Відповідна вода для ін'єкцій кількість 2,00 мл 10 15 Приклад 9 Назальний препарат (Сполука IB). Назальні препарати, що мають наступні інгредієнти, одержували звичайним способом. Сполуку IB (10 мг) і хлорид натрію (0,9 г) додавали до приблизно 80 мл стерильної очищеної води, і розчиняли перемішуванням. Потім, додавали стерильну очищену воду, щоб одержати загальний об'єм 100 мл й одержати назальні препарати. Одержану суміш розливали в назальні контейнери порціями по 1 мл, щоб одержати назальні препарати (що містять 0,1 мг активного інгредієнта на контейнер). Таблиця 11 Композиція Сполука ІB 0,1 мг Хлорид натрію 9,0 мг Стерильна Відповідна очищена вода кількість 1,0 мл 20 Приклад 10 Назальний препарат (Сполука IIC). Назальні препарати, що мають наступні інгредієнти, одержували тим же самим способом як у Прикладі 9. Таблиця 12 Композиція Сполука ІIC Хлорид натрію Стерильна очищена вода 25 0,1 мг 9,0 мг Відповідна кількість 1,0 мл Приклад 11 Назальний препарат (Сполука VII). Назальні препарати, що мають наступні інгредієнти, одержували звичайним способом. 21 UA 102106 C2 Гідроксипропілцелюлозу (49 г) і карбоксиметилцелюлозу (49 г) додавали до сполуки VII (2 г), і суміш ретельно перемішували. Одержану порошкову суміш поміщали в назальні контейнери порціями по 1 г, щоб одержати назальні препарати (що містять 0,1 г активного інгредієнта на контейнер). 5 Таблиця 13 Композиція Сполука VII Гідроксипропілцелюлоза Карбоксиметилцелюлоза 0,02 г 0,49 г 0,49 г 1,00 г 10 Приклад 12 Суха порошкова інгаляція (Сполука IB) 2 Сполуку IB (10 г) розпилювали під тиском повітря 5 кг/см при швидкості подачі 1,5 г/хвилин, використовуючи струменевий млин (A-OJET; Seishin Enterprise Co., Ltd). Розпилену сполуку (I) і лактозу (Pharmatose 325M; DMV) змішували у ваговому співвідношенні 1:5, щоб одержати сухі порошкові препарати. Таблиця 14 Композиція 15 20 Сполука (IB) Лактоза 16,7 мг 83,3 мг 100 мг Промислова придатність Даний винахід може забезпечити терапевтичні та/або профілактичні засоби проти мігрені, які містять, як активний інгредієнт, сполуку, що має селективну антагоністичну активність щодо аденозинових рецепторів A2A, або її фармацевтично прийнятну сіль; терапевтичні та/або профілактичні засоби проти мігрені, які містять, як активний інгредієнт, сполуку, що має селективну антагоністичну активність щодо аденозинових рецепторів A 2A, і яка має афінність щодо аденозинових рецепторів A2A, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів A1, або її фармацевтично прийнятну сіль, і т.п. ФОРМУЛА ВИНАХОДУ 25 30 1. Терапевтичний та/або профілактичний засіб проти мігрені, що містить як активний інгредієнт, сполуку, що має селективну антагоністичну активність щодо аденозинових рецепторів А 2А та афінність щодо аденозинових рецепторів А2A, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів А1, або її фармацевтично прийнятну сіль, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А 2А, є сполукою, представленою наступною формулою (II) O N NH R S 3 R 2 O O 35 (II), 2 де R означає феніл, піридил, піримідиніл, 5,6-дигідро-2Н-піридилметил або тетрагідропіранілокси, або будь-яку із цих груп, заміщену 1-3 замісниками, вибраними з атома 3 фтору, атома хлору, атома брому, метилу, етилу, метокси та етокси; і R означає піридил або тетрагідропіраніл. 3 2. Засіб за пунктом 1, де R означає піридил. 3 3. Засіб за пунктом 1, де R означає тетрагідропіраніл. 4. Засіб за пунктом 1, де сполука є сполукою, представленою наступною формулою (ІІС) 22 UA 102106 C2 O N NH O S CH3 N O O 5 (ІІС). 5. Спосіб лікування та/або профілактики мігрені, що включає введення ефективної кількості сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів А 2А та має афінність щодо аденозинових рецепторів А2А, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів А1, або її фармацевтично прийнятної солі, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А 2А, є сполукою, представленою наступною формулою (II) O N NH R S 3 R 2 O O 10 (II), 2 3 де R і R мають ті ж самі значення, як описано вище, відповідно. 3 6. Спосіб за пунктом 5, де R означає піридил. 3 7. Спосіб за пунктом 5, де R означає тетрагідропіраніл. 8. Спосіб за пунктом 5, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А2A, є сполукою, представленою наступною формулою (ІІС) O N NH O S CH3 N O O 15 20 (ІІС). 9. Застосування сполуки, що має селективну антагоністичну активність щодо аденозинових рецепторів А2А та має афінність щодо аденозинових рецепторів А2А, яка в 10 разів або більше перевищує афінність щодо аденозинових рецепторів А 1, або її фармацевтично прийнятної солі для виробництва терапевтичного та/або профілактичного засобу проти мігрені, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А 2А, є сполукою, представленою наступною формулою (II) O N NH R S 3 R 2 O O 25 (II), 2 3 де R й R мають ті ж самі значення, як описано вище, відповідно. 3 10. Застосування за пунктом 9, де R означає піридил. 3 11. Застосування за пунктом 9, де R означає тетрагідропіраніл. 12. Застосування за пунктом 9, де сполука, що має селективну антагоністичну активність щодо аденозинових рецепторів А2A, є сполукою, представленою наступною формулою (ІІС) 23 UA 102106 C2 O N NH O S CH3 O O N (ІІС). Комп’ютерна верстка А. Крижанівський Державна служба інтелектуальної власності України, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601 24
ДивитисяДодаткова інформація
Назва патенту англійськоюTherapeutic agent for migraine
Автори англійськоюIkeda, Junichi, Ichikawa, Shunji, Kurokawa, Masako, Kanda, Tomoyuki
Назва патенту російськоюТерапевтическое средство от мигрени
Автори російськоюИкеда Юничи, Ичикава Шунджи, Курокава Масако, Канда Томоюки
МПК / Мітки
МПК: A61K 31/427, A61P 25/06
Мітки: терапевтичний, мігрені, засіб
Код посилання
<a href="https://ua.patents.su/26-102106-terapevtichnijj-zasib-proti-migreni.html" target="_blank" rel="follow" title="База патентів України">Терапевтичний засіб проти мігрені</a>
Попередній патент: Випускне горлечко для гнучких упаковок
Наступний патент: Вузол приводу і натягнення для скребкового ланцюгового конвеєра
Випадковий патент: Імітаційна модель дизеля