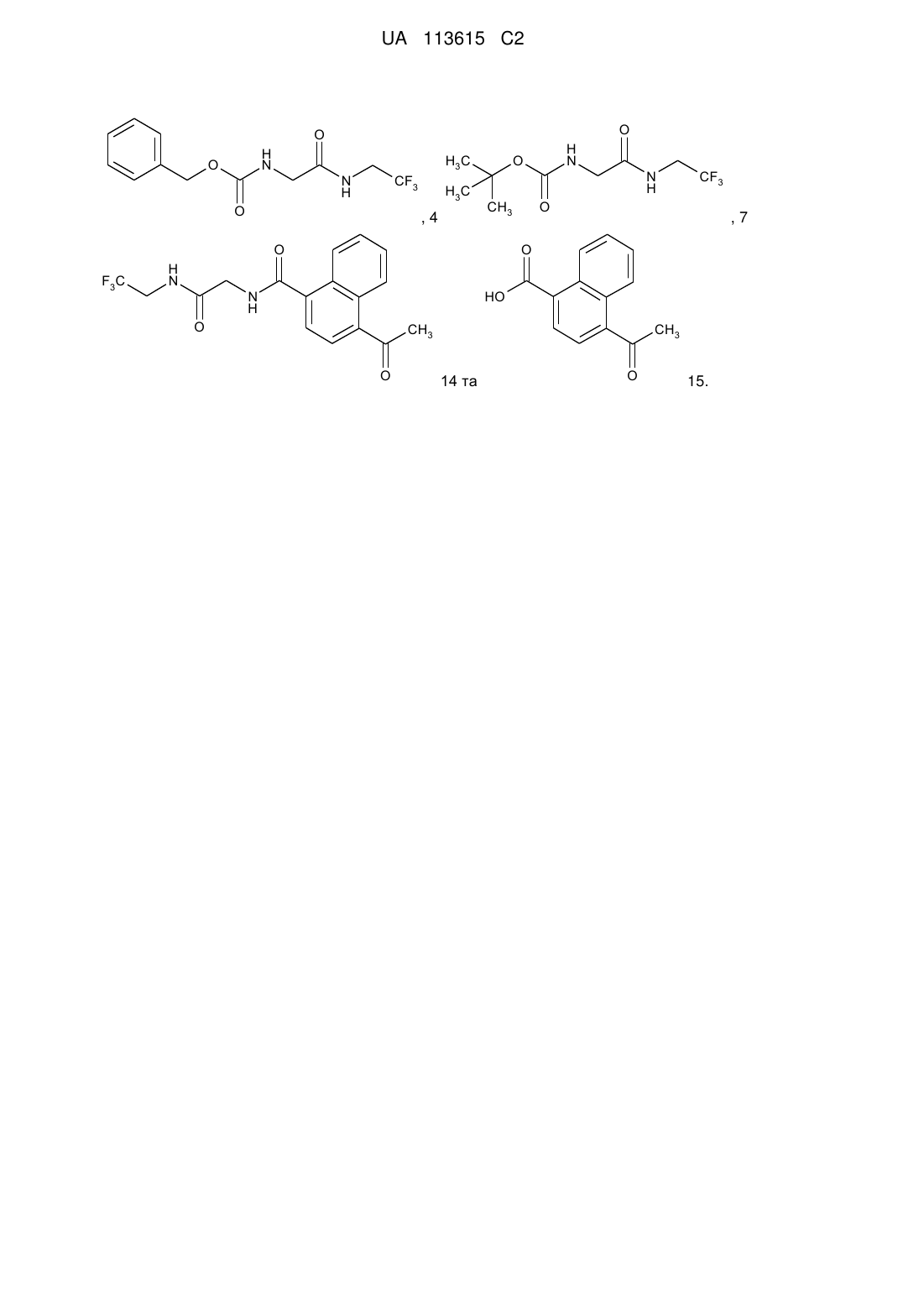
Спосіб отримання 2-аміно-n-(2,2,2-трифторетил)ацетаміду
Формула / Реферат
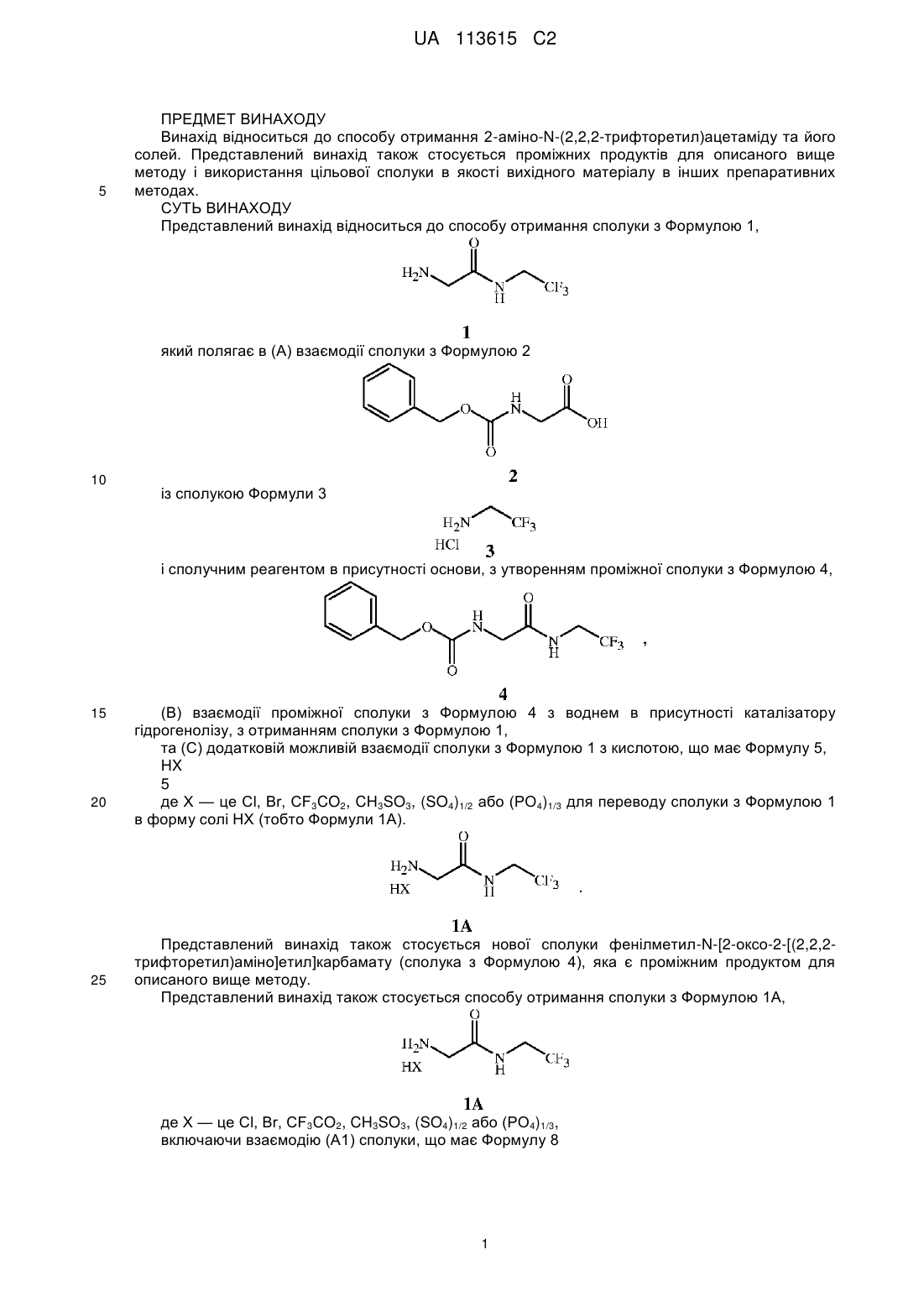
1. Спосіб отримання сполуки Формули 1
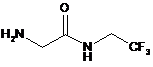 , 1
, 1
який включає стадії, на яких:
(А) приводять у контакт у полярному апротонному розчиннику, що не змішується з водою, сполуку з Формул 2
 2
2
зі сполучним реагентом, при тому, що сполучним реагентом є N,N'-карбонілдіімідазол, та потім у присутності основи, отриманої зі вказаного сполучного реагенту, додають сіль Формули 3
![]() 3
3
для отримання проміжної сполуки Формули 4
 , 4
, 4
(В) приводять у контакт проміжну сполуку Формули 4 з воднем у присутності каталізатора гідрогенолізу, з отриманням сполуки Формули 1,
та (С) необов’язково приводять у контакт сполуку з Формули 1 з кислотою Формули 5
![]() , 5
, 5
де X - це Сl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (РО4)1/3,
з отриманням сполуки Формули 1 у вигляді солі НХ.
2. Спосіб за п. 1, який відрізняється тим, що на стадії (А) сіль Формули 3 додають у присутності додаткової основи.
3. Спосіб за п. 2, який відрізняється тим, що додаткова основа являє собою триетиламін.
4. Спосіб за п. 1, який відрізняється тим, що на стадії (В) сполуку Формули 4 та водень приводять у контакт у присутності каталізатора гідрогенолізу та розчинника, що не змішується з водою.
5. Спосіб за п. 4, який відрізняється тим, що каталізатор гідрогенолізу являє собою паладій на вугіллі.
6. Спосіб за п. 1, який відрізняється тим, що на стадії (С) сполуку Формули 1 приводять у контакт з кислотою Формули 5 у присутності розчинника, що не змішується з водою.
7. Спосіб за п. 1, який відрізняється тим, що кислота Формул 5 містить хлорид водню.
8. Спосіб будь-яким із пп. 4 або 6, який відрізняється тим, що розчинник, який не змішується з водою, містить етилацетат або ізопропілацетат.
9. Спосіб отримання солі Формули 1А
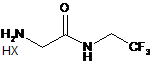 , 1A
, 1A
де X - це Сl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (РО4)1/3,
який включає стадії, на яких
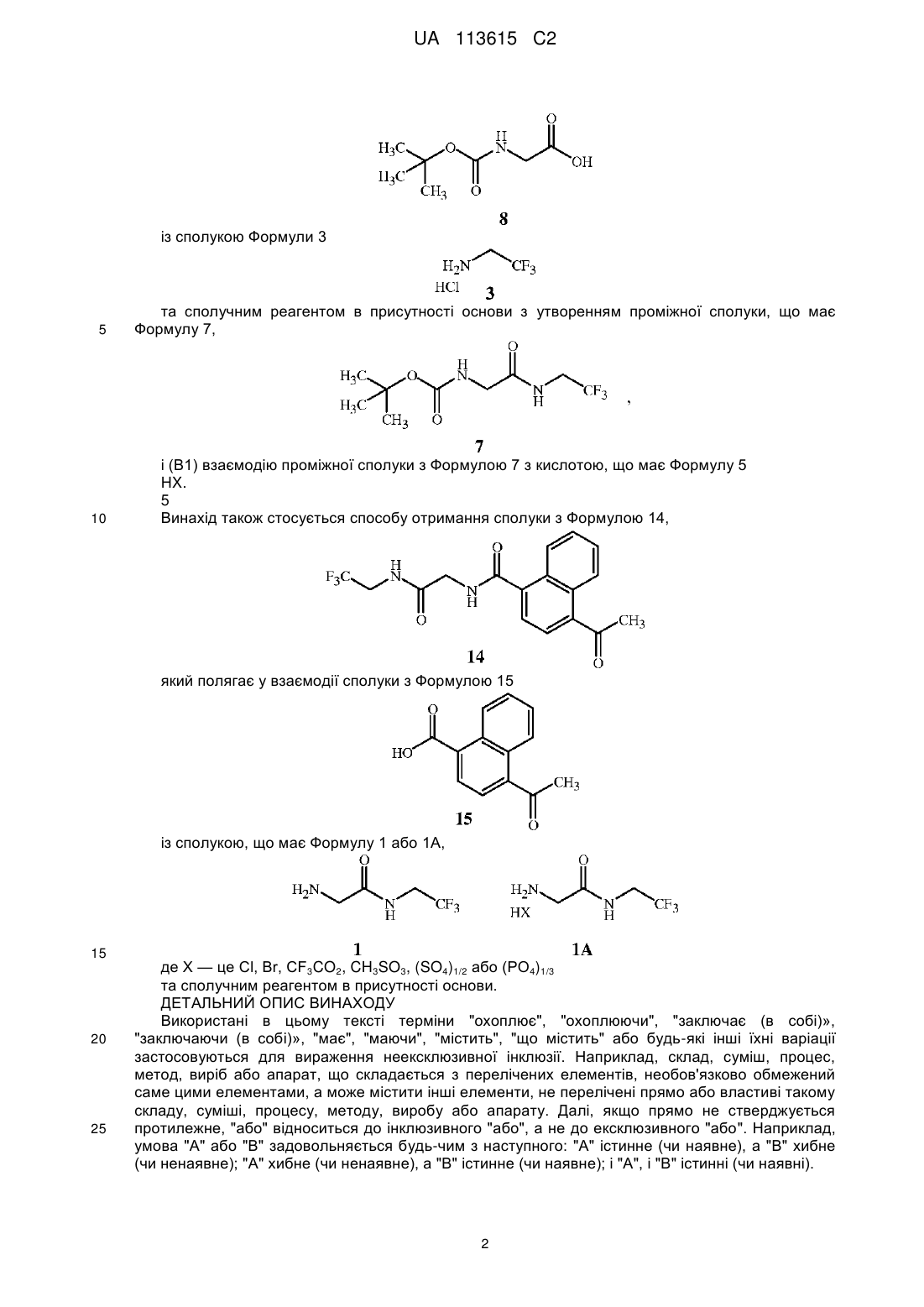
(А1) приводять у контакт сполуку Формули 8
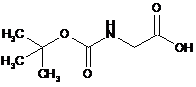 8
8
із сіллю Формули 3
![]() 3
3
та сполучним реагентом, при тому, що сполучним реагентом є N,N'-карбонілдіімідазол, у присутності основи, отриманої зі вказаного сполучного реагенту, з утворенням проміжної сполуки Формулу 7
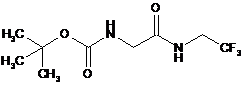 , 7
, 7
та (В1) приводять у контакт проміжну сполуку Формули 7 з кислотою Формули 5
![]() 5.
5.
10. Спосіб за п. 9, який відрізняється тим, що на стадії (А1) сполуку Формули 8 та сіль Формули 3, а також сполучний реагент приводять у контакт у присутності додаткової основи.
11. Спосіб за п. 10, який відрізняється тим, що додаткова основа являє собою триетиламін.
12. Спосіб за п. 9, який відрізняється тим, що на стадії (В1) сполуки Формул 7 та 5 приводять у контакт у присутності розчинника, який не змішується з водою.
13. Спосіб за п. 12, який відрізняється тим, що кислота Формул 5 містить хлорид водню.
14. Спосіб будь-яким із пп. 10 або 12, який відрізняється тим, що розчинник, який не змішується з водою, містить етилацетат або ізопропілацетат.
15. Спосіб отримання сполуки Формули 14
 , 14
, 14
який включає стадію, на якій приводять у контакт сполуку Формули 15
 15
15
із сполукою Формули 1 або 1А
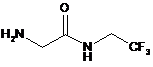 , 1
, 1
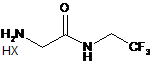 , 1A
, 1A
де X - це Сl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (РО4)1/3,
та сполучним реагентом, при тому, що сполучним реагентом є N,N'-карбонілдіімідазол, у присутності основи, отриманої з вказаного сполучного реагенту.
16. Спосіб за п. 15, який відрізняється тим, що сполуки Формул 1 або 1А та Формули 15, а також сполучний реагент приводять у контакт у присутності основи та полярного апротонного розчинника, який змішується з водою.
17. Спосіб за п. 16, який відрізняється тим, що полярний апротонний розчинник, який змішується з водою, містить ацетонітрил, тетрагідрофуран або діоксан.
18. Спосіб за п. 16 або п. 17, який відрізняється тим, що основу отримують із сполучного реагенту, при тому, що сполучним реагентом є N,N'-карбонілдіімідазол.
19. Спосіб за п. 18, який відрізняється тим, що сполуку Формули 15 спочатку приводять у контакт із сполучним реагентом з утворенням суміші, а потім до цієї суміші у присутності основи додають сполуку з Формули 1 або 1А.
20. Спосіб за п. 19, який відрізняється тим, що сполуку Формулою 1 або 1А додають до суміші у вигляді твердої речовини або у вигляді розчину в полярному апротонному розчиннику, що змішується з водою.
21. Спосіб за п. 19, який відрізняється тим, що сполуку Формули 1 або 1А додають до суміші у вигляді розчину або суспензії у воді.
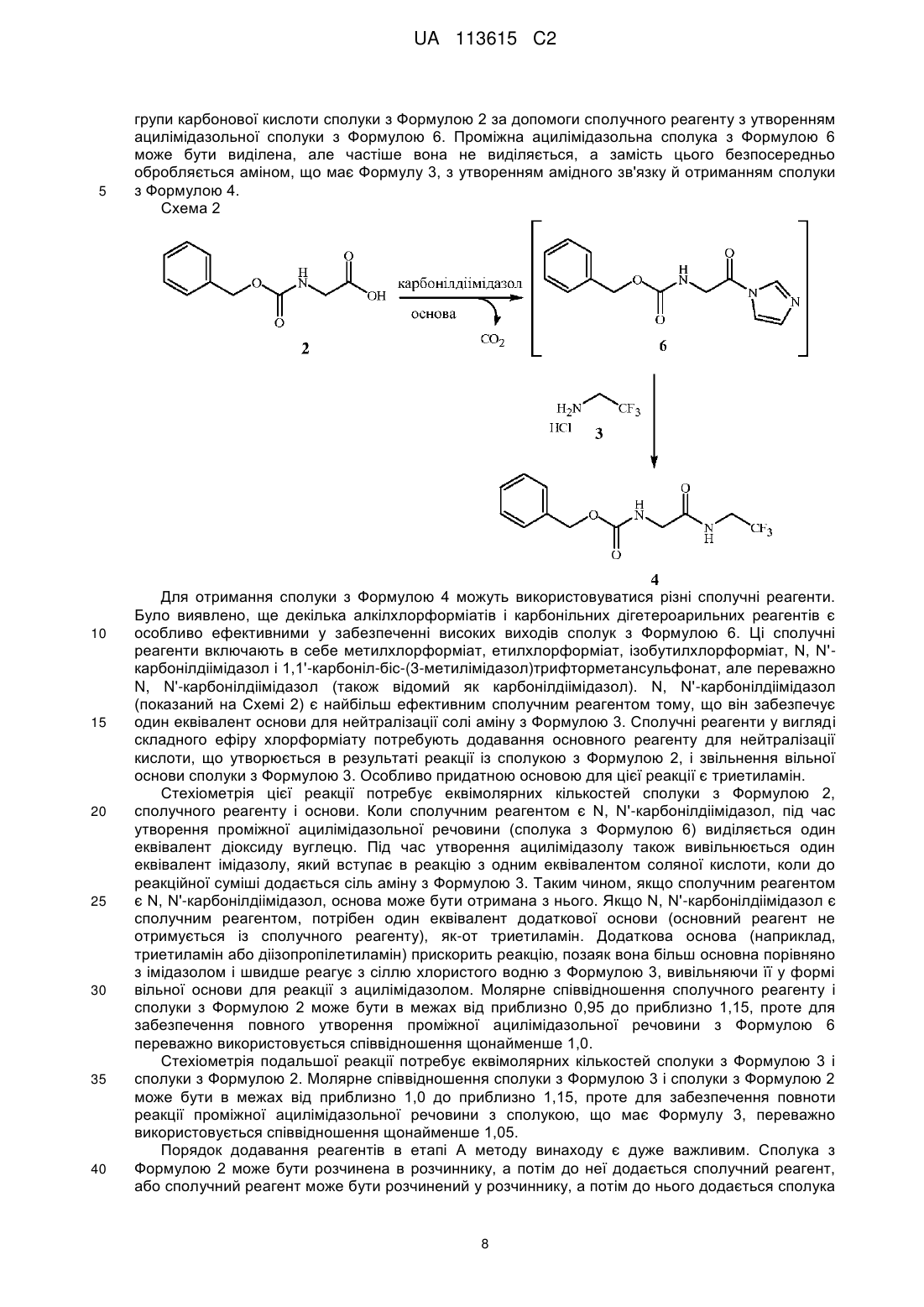
Текст
Реферат: Розкриваються способи отримання сполуки Формули 1 та 1А. У першому способі використовується бензилкарбамат для захисту аміногрупи та проміжна сполука Формули 4. У другому способі використовується трет-бутилкарбамат для захисту аміногрупи та проміжна сполука Формули 7. У третьому способі як захисна група використовується дибензиламін. Також розкривається сполука фенілметил-N-[2-оксо-2-[(2,2,2-трифторетил)аміно]етил]карбамат (сполука Формули 4). Далі розкриваються способи отримання сполуки Формули 14 із сполуки Формули 15 та сполуки Формули 1 або 1А. O H2 N O N H H2 N HX CF3 ,1 N H CF3 , 1A UA 113615 C2 (12) UA 113615 C2 O O H N O H3 C N H CF3 O H3 C ,4 O N H CF3 O CH3 O F3C H N ,7 O H N N H HO O CH3 O CH3 14 та O 15. UA 113615 C2 5 ПРЕДМЕТ ВИНАХОДУ Винахід відноситься до способу отримання 2-аміно-N-(2,2,2-трифторетил)ацетаміду та його солей. Представлений винахід також стосується проміжних продуктів для описаного вище методу і використання цільової сполуки в якості вихідного матеріалу в інших препаративних методах. СУТЬ ВИНАХОДУ Представлений винахід відноситься до способу отримання сполуки з Формулою 1, який полягає в (A) взаємодії сполуки з Формулою 2 10 із сполукою Формули 3 і сполучним реагентом в присутності основи, з утворенням проміжної сполуки з Формулою 4, 15 20 25 (B) взаємодії проміжної сполуки з Формулою 4 з воднем в присутності каталізатору гідрогенолізу, з отриманням сполуки з Формулою 1, та (С) додатковій можливій взаємодії сполуки з Формулою 1 з кислотою, що має Формулу 5, HX 5 де X — це Cl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (PO4)1/3 для переводу сполуки з Формулою 1 в форму солі HX (тобто Формули 1A). Представлений винахід також стосується нової сполуки фенілметил-N-[2-оксо-2-[(2,2,2трифторетил)аміно]етил]карбамату (сполука з Формулою 4), яка є проміжним продуктом для описаного вище методу. Представлений винахід також стосується способу отримання сполуки з Формулою 1А, де X — це Cl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (PO4)1/3, включаючи взаємодію (A1) сполуки, що має Формулу 8 1 UA 113615 C2 із сполукою Формули 3 5 10 та сполучним реагентом в присутності основи з утворенням проміжної сполуки, що має Формулу 7, і (B1) взаємодію проміжної сполуки з Формулою 7 з кислотою, що має Формулу 5 HX. 5 Винахід також стосується способу отримання сполуки з Формулою 14, який полягає у взаємодії сполуки з Формулою 15 із сполукою, що має Формулу 1 або 1А, 15 20 25 де X — це Cl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (PO4)1/3 та сполучним реагентом в присутності основи. ДЕТАЛЬНИЙ ОПИС ВИНАХОДУ Використані в цьому тексті терміни "охоплює", "охоплюючи", "заключає (в собі)», "заключаючи (в собі)», "має", "маючи", "містить", "що містить" або будь-які інші їхні варіації застосовуються для вираження неексклюзивної інклюзії. Наприклад, склад, суміш, процес, метод, виріб або апарат, що складається з перелічених елементів, необов'язково обмежений саме цими елементами, а може містити інші елементи, не перелічені прямо або властиві такому складу, суміші, процесу, методу, виробу або апарату. Далі, якщо прямо не стверджується протилежне, "або" відноситься до інклюзивного "або", а не до ексклюзивного "або". Наприклад, умова "А" або "В" задовольняється будь-чим з наступного: "А" істинне (чи наявне), а "В" хибне (чи ненаявне); "А" хибне (чи ненаявне), а "В" істинне (чи наявне); і "А", і "В" істинні (чи наявні). 2 UA 113615 C2 5 10 Крім того, вживання прихованої невизначеності при описі елементу або компоненту цього винаходу вважається таким, що не обмежує кількість варіантів (тобто випадків) елементу або компоненту. Тому таку невизначеність треба сприймати як "один" або "принаймні один", і опис елементу або компоненту в єдиностi має на увазі також і множину, за винятком випадків, коли число явно вказує на єдинiсть. Термін "сполучний реагент" відноситься до реагенту, що використовується для активації функціональної групи карбонової кислоти для полегшення її конденсації з аміногрупою з утворенням амідного зв'язку. Сполука Формули 1 у формі солі HX є сполукою з Формулою 1А. де X — це Cl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (PO4)1/3. Мається на увазі, що сполука з Формулою 1А являє собою сіль сполуки з Формулою 1 і альтернативно може бути зображена Формулою 1AA, як показано нижче: 15 де Х — це Cl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (PO4)1/3. Коли вказується, що Х буде (SO4)1/2 це означає, що сірчана кислота утворює сульфат сполуки з Формулою 1, як показано нижче, де дві структури стосуються, відповідно, до Формулі 1AA і Формулі 1А. 20 Сполукою з Формулою 1 є 2-аміно-N-(2,2,2-трифторетил)ацетамід. Сполукою Формули 1A є 2-аміно-N-(2,2,2-трифторетил)ацетаміду гідрохлорид. Сполукою Формули 4 є фенілметил-N-[2оксо-2-[(2,2,2-трифторетил)аміно]етил]карбамат. Сполукою Формули 14 є 4-ацетил-N-[2-оксо-2[(2,2,2-трифторетил)аміно]етил]-1-нафталінкарбоксамід. Варіанти здійснення цього винаходу включають: Варіант здійснення 1.0. Метод, описаний в етапі (A) Суті винаходу, в якому сполуки з формулами 2 та 3 i сполучний реагент контактують у присутності основи та розчинника, що не змішується з водою. Варіант здійснення 1.1. Метод Варіанта здійснення 1.0, де розчинник, що не змішується з водою, містить етилацетат або ізопропілацетат. Варіант здійснення 1.2. Метод Варіанта здійснення 1.1, де розчинник, що не змішується з водою, містить етилацетат. Варіант здійснення 1.3. Метод, описаний в етапі (А) Суті винаходу або в будь-якому з Варіантів здійснення від 1.0 до 1.3, де сполучний реагент містить ізобутилхлорформіат або N, N'-карбонілдіімідазол. Варіант здійснення 1.4. Метод Варіанта здійснення 1.3, де сполучний реагент містить N, N'карбонілдіімідазол. Варіант здійснення 1.5. Метод, описаний в етапі (А) Суті винаходу або в будь-якому з Варіантів здійснення від 1.0 до 1.4, де основа, крім сполуки, отриманої з сполучного реагенту, містить основний реагент. Варіант здійснення 1.6. Метод Варіанту здійснення 1.5, де основний реагент містить триетиламін або N, N-діізопропілетиламін. Варіант здійснення 1.7. Методі Варіанту здійснення 1.6, де основний реагент містить триетиламін. 25 30 35 40 3 UA 113615 C2 5 10 15 20 25 30 35 40 45 50 55 60 Варіант здійснення 1.8. Метод, описаний в етапі (А) Суті винаходу або в будь-якому з Варіантів здійснення від 1.0 до 1.7, де основа отримується із сполучного реагенту, а сполучним реагентом є N, N'-карбонілдіімідазол. Варіант здійснення 1.9. Метод, описаний в етапі (А) Суті винаходу або в будь-якому з Варіантів здійснення від 1.0 до 1.8, де спочатку сполука, що має Формулу 2, взаємодіє з сполучним реагентом з утворенням суміші (тобто містить ацилімідазол Формули 6), а потім сполука з Формулою 3 додається до суміші в присутності основи. Варіант здійснення 1.10. Метод, описаний у пункті (А) Суті винаходу або в будь-якому з Варіантів здійснення від 1.0 до 1.9, де суміш має температуру щонайменше близько 15 °C. Варіант здійснення 1.11. Метод, описаний в етапі (А) Суті винаходу або в будь-якому з Варіантів здійснення від 1.0 до 1.10, де суміш має температуру не більшу за приблизно 40 °C. Варіант здійснення 1.12. Метод, описаний в етапі (А) Суті винаходу або в будь-якому з Варіантів здійснення від 1.0 до 1.11, де молярне співвідношення сполучного реагенту до сполуки з Формулою 2 становить від приблизно 1,0 до приблизно 1,1. Варіант здійснення 1.13. Метод, описаний в етапі (А) Суті винаходу або в будь-якому з Варіантів здійснення від 1.0 до 1.12, де молярне співвідношення сполуки з Формулою 3 до сполуки з Формулою 2 становить приблизно 1,0. Варіант здійснення 1.14. Метод, описаний в етапі (В) Суті винаходу, де відбувається взаємодія сполуки з Формулою 4 з воднем в присутності каталізатору гідрогенолізу та розчинника, що не змішується з водою. Варіант здійснення 1.15. Метод Варіанта здійснення 1.14, де розчинник, що не змішується з водою, містить етилацетат або ізопропілацетат. Варіант здійснення 1.16. Метод Варіанта здійснення 1.15, де розчинник, що не змішується з водою, містить етилацетат. Варіант здійснення 1.17. Метод, описаний в етапі (В) Суті винаходу або в будь-якому з Варіантів здійснення від 1.14 до 1.16, де каталізатором гідрогенолізу є каталізатор з благородного металу або каталізатор на носії з благородного металу. Варіант здійснення 1.18. Метод Варіанта здійснення 1.17, де каталізатором гідрогенолізу є паладій, нанесений на вуглець. Варіант здійснення 1.19. Метод Варіанта здійснення 1.18, де каталізатором гідрогенолізу є паладій, нанесений на вуглець у кількості 5 % або 10 %. Варіант здійснення 1.20. Метод, описаний в етапі (В) Суті винаходу або в будь-якому з Варіантів здійснення від 1.14 до 1.19, де гідрогеноліз проводиться при кімнатній температурі. Варіант здійснення 1.21. Метод, описаний в етапі (В) Суті винаходу або в будь-якому з Варіантів здійснення від 1.14 до 1.20, де гідрогеноліз проводиться при тиску від атмосферного до приблизно 0,34 MПa (50 фунтів на квадратний дюйм). Варіант здійснення 1.22. Метод Варіанта здійснення 1.21, де гідрогеноліз проводиться під атмосферним тиском. Варіант здійснення 1.23. Метод, описаний в етапі (С) Суті винаходу, де сполука з Формулою 1 взаємодіє з кислотою з Формулою 5 в присутності розчинника, що не змішується з водою. Варіант здійснення 1.24. Метод Варіанта здійснення 1.23, де розчинник, що не змішується з водою, містить етилацетат або ізопропілацетат. Варіант здійснення 1.25. Метод Варіанта здійснення 1.24, де розчинник, що не змішується з водою, містить етилацетат. Варіант здійснення 1.26. Метод, описаний в етапі (С) Суті винаходу або в будь-якому з Варіантів здійснення від 1.23 до 1.25, де кислота з Формулою 5 містить хлорид водню, бромід водню, трифтороцтову кислоту, сірчану кислоту, метансульфокислоту або ортофосфорну кислоту. Варіант здійснення 1.27. Метод Варіанта здійснення 1.26, де кислота з Формулою 5 містить хлорид водню, бромід водню та сірчану кислоту. Варіант здійснення 1.28. Метод Варіанта здійснення 1.27, де кислота з Формулою 5 містить хлорид водню. Варіант здійснення 1.29. Метод Варіанта здійснення 1.28, де хлорид водню являє собою водний розчин (тобто соляну кислоту). Варіант здійснення 1.30. Метод Варіанта здійснення 1.28, де хлорид водню — безводний (тобто газоподібний хлорид водню). Варіант здійснення 1.31. Метод, описаний в етапі (С) Суті винаходу або в будь-якому з Варіантів здійснення від 1.23 до 1.30, де суміш має температуру щонайменше близько 20 °C. Варіант здійснення 1.32. Метод, описаний в етапі (С) Суті винаходу або в будь-якому з Варіантів здійснення від 1.23 до 1.31, де суміш має температуру не більшу за приблизно 45 °C. 4 UA 113615 C2 5 10 15 20 25 30 35 40 45 50 55 60 Варіант здійснення 1.33. Метод, описаний в етапі (С) Суті винаходу або в будь-якому з Варіантів здійснення від 1.23 до 1.32, де молярне співвідношення сполуки з Формулою 1 до кислоти з Формулою 5 становить щонайменше приблизно 1,0. Варіант здійснення 1.34. Метод, описаний в етапі (С) Суті винаходу або в будь-якому з Варіантів здійснення від 1.23 до 1.33, де молярне співвідношення сполуки з Формулою 1 до кислоти з Формулою 5 є не більше ніж приблизно 5,0. Варіант здійснення 2.0. Метод, описаний в етапі (A1) Суті винаходу, де сполуки з Формулами 8 та 3 і сполучний реагент взаємодіють в присутності основи і розчинника, що не змішується з водою. Варіант здійснення 2.1. Метод Варіанта здійснення 2.0, де розчинник, що не змішується з водою, містить етилацетат або ізопропілацетат. Варіант здійснення 2.2. Метод Варіанта здійснення 2.1, де розчинник, що не змішується з водою, містить етилацетат. Варіант здійснення 2.3. Метод, описаний в етапі (A1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.0 до 2.2, де сполука, що має Формулу 8, спочатку взаємодіє з сполучним реагентом з утворенням суміші (тобто містить ацилімідазол з Формулою 9), а потім до суміші додають сполуку з Формулою 3. Варіант здійснення 2.4. Метод, описаний в етапі (A1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.0 до 2.3, де сполучний реагент містить ізобутилхлорформіат або N, N'-карбонілдіімідазол. Варіант здійснення 2.5. Метод Варіанта здійснення 2.4, де сполучний реагент містить N, N'карбонілдіімідазол. Варіант здійснення 2.6. Методі, описаний у пункті (А1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.0 до 2.5, де основа, крім сполуки, отриманої з сполучного реагенту, містить основний реагент. Варіант здійснення 2.7. Метод Варіанта здійснення 2.6, де основний реагент містить триетиламін або N, N-діізопропілетиламін. Варіант здійснення 2.8. Метод Варіанта здійснення 2.7, де основний реагент містить триетиламін. Варіант здійснення 2.9. Метод, описаний в етапі (A1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.0 до 2.8, де основа отримується із сполучного реагенту, а сполучним реагентом є N, N'-карбонілдіімідазол. Варіант здійснення 2.10. Метод, описаний в етапі (A1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.0 до 2.9, де сполука з Формулою 8 спочатку взаємодіє з сполучним реагентом з утворенням суміші, а потім до суміші додається сполука з Формулою 3 в присутності основи. Варіант здійснення 2.11. Метод, описаний в етапі (A1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.0 до 2.10, де суміш має температуру щонайменше близько 15 °C. Варіант здійснення 2.12. Метод, описаний в етапі (A1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.0 до 2.11, де суміш має температуру не більшу за приблизно 40 °C. Варіант здійснення 2.13. Метод, описаний у пункті (A1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.0 до 2.12, де молярне співвідношення сполучного реагенту до сполуки з Формулою 8 становить приблизно 1,0. Варіант здійснення 2.14. Метод, описаний в етапі (A1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.0 до 2.13, де молярне співвідношення сполуки з Формулою 3 до сполуки з Формулою 8 становить приблизно 1,0. Варіант здійснення 2.15. Метод, описаний в етапі (B1) Суті винаходу, де сполуки з Формулами 7 та 5 взаємодіють в присутності розчинника, що не змішується з водою. Варіант здійснення 2.16. Метод Варіанта здійснення 2.15, де розчинник, що не змішується з водою, містить етилацетат або ізопропілацетат. Варіант здійснення 2.17. Метод Варіанта здійснення 2.16, де розчинник, що не змішується з водою, містить етилацетат. Варіант здійснення 2.18. Метод, описаний в етапі (B1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.15 до 2.17, де кислота з Формулою 5 містить хлорид водню, бромід водню, трифтороцтову кислоту, сірчану кислоту, метансульфокислоту або ортофосфорну кислоту. Варіант здійснення 2.19. Метод Варіанта здійснення 2.18, де кислота, що має Формулу 5, містить хлорид водню, бромід водню та сірчану кислоту. Варіант здійснення 2.20. Метод Варіанта здійснення 2.19, де кислота, що має Формулу 5, містить хлорид водню. 5 UA 113615 C2 5 10 15 20 25 30 35 40 45 50 55 Варіант здійснення 2.21. Метод Варіанта здійснення 2.20, де хлорид водню являє собою водний розчин (тобто соляну кислоту). Варіант здійснення 2.22. Метод Варіанта здійснення 2.20, де хлорид водню — безводний (тобто газоподібний хлорид водню). Варіант здійснення 2.23. Метод, описаний в етапі (B1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.15 до 2.22, де суміш має температуру щонайменше близько 20 °C. Варіант здійснення 2.24. Метод, описаний в етапі (B1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.15 до 2.23, де суміш має температуру не більшу за приблизно 45 °C. Варіант здійснення 2.25. Метод, описаний в етапі (B1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.15 до 2.24, де молярне співвідношення сполуки з Формулою 7 до кислоти з Формулою 5 становить принаймні приблизно 1,0. Варіант здійснення 2.26. Метод, описаний в етапі (B1) Суті винаходу або в будь-якому з Варіантів здійснення від 2.15 до 2.25, де молярне співвідношення сполуки з Формулою 7 до кислоти з Формулою 5 становить не більше ніж приблизно 5,0. Варіант здійснення 3.0. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу, де сполуки з Формулами 1 або 1А і Формулою 15 та сполучний реагент взаємодіють в присутності основи і полярного апротонного розчинника, що змішується з водою. Варіант здійснення 3.1. Метод Варіанта здійснення 3.0, де полярний апротонний розчинник, що змішується з водою, містить ацетонітрил, тетрагідрофуран або діоксан. Варіант здійснення 3.2. Метод Варіанта здійснення 3.1, де полярним апротонним розчинником, що змішується з водою, є ацетонітрил. Варіант здійснення 3.3. Метод приготування сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.2, де сполучний реагент містить ізобутилхлорформіат або N, N'-карбонілдіімідазол. Варіант здійснення 3.4. Метод Варіанта здійснення 3.3, де сполучний реагент містить N, N'карбонілдіімідазол. Варіант здійснення 3.5. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.4, де основа, крім сполуки, отриманої із сполучного реагенту, містить основний реагент. Варіант здійснення 3.6. Метод Варіанта здійснення 3.5, де основний реагент містить триетиламін або N, N-діізопропілетиламін. Варіант здійснення 3.7. Метод Варіанта здійснення 3.6, де основний реагент містить триетиламін. Варіант здійснення 3.8. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.7, де основа отримується із сполучного реагенту, а сполучним реагентом є N, N'-карбонілдіімідазол. Варіант здійснення 3.9. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.8, де сполука, що має Формулу 15, спочатку взаємодіє з сполучним реагентом з утворенням суміші (тобто містить ацилімідазол Формули 16), а потім в присутності основи до суміші додають сполуку з Формулою 1 або 1А. Варіант здійснення 3.10. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.9, де сполука з Формулою 1 або 1А додається до суміші в твердому стані або у вигляді розчину в полярному апротонному розчиннику, що змішується з водою. Варіант здійснення 3.11. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.10, де сполука з Формулою 1 або 1А додається до суміші у вигляді розчину або суспензії у воді. Варіант здійснення 3.12. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.12, де суміш має температуру щонайменше приблизно 20 °C. Варіант здійснення 3.13. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.12, де суміш має температуру не більше ніж приблизно 45 °C. Варіант здійснення 3.14. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.13, де молярне співвідношення сполучного реагенту до сполуки з Формулою 15 становить від приблизно 1,0 до приблизно 1,1. Варіант здійснення 3.15. Метод отримання сполуки з Формулою 14, описаний в Суті винаходу або в будь-якому з Варіантів здійснення від 3.0 до 3.14, де молярне співвідношення сполуки з Формулою 1 або 1А до сполуки з Формулою 15 становить приблизно 1,0. 6 UA 113615 C2 5 10 15 20 25 30 35 40 45 50 Варіанти здійснення цього винаходу, включаючи Варіанти здійснення 1.0–3.15, що приведені вище, так само як і будь-який з інших варіантів здійснення, описаних тут, можуть бути об'єднані будь-яким способом, а описи змінних параметрів у варіантах здiйснення стосуються не тільки описаних вище способів отримання сполук з Формулами 1, 1А і 14, але також вихідних і проміжних сполук, стосованих для отримання сполук з Формулами 1, 1А і 14 за допомогою цих методів. У наступних схемах 1–9 у сполуках Формул від 1 до 16 визначення Х таке саме, як зазначено вище у Суті винаходу й описі варіантів, якщо не вказано інше. У методі винаходу група бензилкарбамату (CBZ), що захищає аміногрупу, використовується для отримання сполуки з Формулою 1, як показано в Схемах 1 і 2. В подальшому, для утворення солі з Формулою 1А, сполука з Формулою 1 може вступати в реакцію з кислотою, як показано в Схемі 3 (див. приклади Синтезу 1 і 2). Етап B методу даного винаходу включає в себе видалення за допомогою гідрогенолізу захисної групи бензилкарбамату з проміжної сполуки з Формулою 4, щоб утворити сполуку з Формулою 1, яка має вільну аміногрупу, як показано на схемі 1. Схема 1 Видалення захисних груп бензилкарбамату може бути виконане при різних умовах реакції. Див., наприклад, Greene, T. W.; Wuts, P. G. M. Protective Groups in Organic Synthesis, 2nd ed.; Wiley: New York, 1991. Один особливо зручний метод видалення бензильной захисної групи полягає в гідрогенолізі з воднем, як правило, під атмосферним тиском. Зазвичай використовуються каталізатори з благородного металу або каталізатори з благородного металу на носії. Також гідрогеноліз може проводитися шляхом переносу водню за допомогою каталізатора з благородного металу на носії та донору водню (наприклад, форміата амонію або циклогексадієну). Ці методи описані в: Rylander, P. N.; Hydrogenation Methods, Academic Press: San Diego, 1985. Одним особливо зручним каталізатором гідрогенолізу є паладій на вуглецю (звичайно 5–10 %). Цей метод описано в: Harada et al., Bioorganic and Medicinal Chemistry2001, 9, 2709–2726 та Janda et al., Synthetic Communications1990, 20, 1073–1082. Також захисна група бензилкарбамату може бути видалена за допомогою кислоти, як описано в: Lesk et al., Synthetic Communications1999, 28, 1405–1408. Метод за Схемою 1 може бути проведений в діапазоні температур. Як правило, реакцію проводять при температурі щонайменше приблизно 20 °C або кімнатній температурі. Гідрування може бути проведене в діапазоні тисків. Звичайно гідрування проводиться при атмосферному тиску з використанням водневого балону. Час, необхідний для реакціі, звичайно лежить у межах від 2 до 24 годин в залежності від масштабу реакції. В представленому методі реакційна суміш містить розчинник, що не змішується з водою. Було встановлено, що особливо зручними розчинниками є етилацетат та ізопропілацетат. Полярні апротонні розчинники, які не змішуються з водою, завдяки їх здатності розчиняти вихідну речовину з Формулою 4 є особливо зручними. Кількість використаного розчинника, тобто об'єм, необхідний для розчинення вихідної речовини, звичайно знаходиться в межах від 0,5 до 1,0 молярної концентрації. Для розчинення сполуки з Формулою 4 і для того, щоб концентрація реакційної суміші перевищувала 0,5 моль, суміш вихідної речовини і розчинника може бути нагріта до приблизно 30 °C. За протіканням реакції можна спостерігати за допомогою стандартних методів, як-от 1 тонкошарова хроматографія, ГХ, ВРХ і H ЯМР-аналіз аліквот. Після закінчення реакції продукт відділяється від каталізатору фільтруванням. Отриманий розчин містить сполуку з вільною аміногрупою, що має Формулу 1. Для виділення сполуки з Формулою 1 цей розчин може бути випарений. Або, для отримання сполуки з Формулою 1А, можна далі провести реакцію цього розчину з кислотою так, як показано на Схемі 3. Іншим варіантом може бути додавання води у відфільтрований розчин, де сполука з Формулою 1 розподілиться у воді і утворить водний розчин, який може бути виділений і використаний у наступних реакціях. Етапом А методу цього винаходу є реакція вихідної речовини з Формулою 2, захищеної бензилкарбаматом, з сполукою, що має Формулу 3, з утворенням проміжної сполуки, що має Формулу 4, як показано в Схемі 2. Етап А включає в себе попередню активацію функціональної 7 UA 113615 C2 5 10 15 20 25 30 35 40 групи карбонової кислоти сполуки з Формулою 2 за допомоги сполучного реагенту з утворенням ацилімідазольної сполуки з Формулою 6. Проміжна ацилімідазольна сполука з Формулою 6 може бути виділена, але частіше вона не виділяється, а замість цього безпосередньо обробляється аміном, що має Формулу 3, з утворенням амідного зв'язку й отриманням сполуки з Формулою 4. Схема 2 Для отримання сполуки з Формулою 4 можуть використовуватися різні сполучні реагенти. Було виявлено, ще декілька алкілхлорформіатів і карбонільних дiгетероарильних реагентів є особливо ефективними у забезпеченні високих виходів сполук з Формулою 6. Ці сполучні реагенти включають в себе метилхлорформіат, етилхлорформіат, ізобутилхлорформіат, N, N'карбонілдіімідазол і 1,1'-карбоніл-біс-(3-метилімідазол)трифторметансульфонат, але переважно N, N'-карбонілдіімідазол (також відомий як карбонілдіімідазол). N, N'-карбонілдіімідазол (показаний на Схемі 2) є найбільш ефективним сполучним реагентом тому, що він забезпечує один еквівалент основи для нейтралізації солі аміну з Формулою 3. Сполучні реагенти у вигляді складного ефіру хлорформіату потребують додавання основного реагенту для нейтралізації кислоти, що утворюється в результаті реакції із сполукою з Формулою 2, і звільнення вільної основи сполуки з Формулою 3. Особливо придатною основою для цієї реакції є триетиламін. Стехіометрія цієї реакції потребує еквімолярних кількостей сполуки з Формулою 2, сполучного реагенту і основи. Коли сполучним реагентом є N, N'-карбонілдіімідазол, під час утворення проміжної ацилімідазольної речовини (сполука з Формулою 6) виділяється один еквівалент діоксиду вуглецю. Під час утворення ацилімідазолу також вивільнюється один еквівалент імідазолу, який вступає в реакцію з одним еквівалентом соляної кислоти, коли до реакційної суміші додається сіль аміну з Формулою 3. Таким чином, якщо сполучним реагентом є N, N'-карбонілдіімідазол, основа може бути отримана з нього. Якщо N, N'-карбонілдіімідазол є сполучним реагентом, потрібен один еквівалент додаткової основи (основний реагент не отримується із сполучного реагенту), як-от триетиламін. Додаткова основа (наприклад, триетиламін або діізопропілетиламін) прискорить реакцію, позаяк вона більш основна порівняно з імідазолом і швидше реагує з сіллю хлористого водню з Формулою 3, вивільняючи її у формі вільної основи для реакції з ацилімідазолом. Молярне співвідношення сполучного реагенту і сполуки з Формулою 2 може бути в межах від приблизно 0,95 до приблизно 1,15, проте для забезпечення повного утворення проміжної ацилімідазольної речовини з Формулою 6 переважно використовується співвідношення щонайменше 1,0. Стехіометрія подальшої реакції потребує еквімолярних кількостей сполуки з Формулою 3 і сполуки з Формулою 2. Молярне співвідношення сполуки з Формулою 3 і сполуки з Формулою 2 може бути в межах від приблизно 1,0 до приблизно 1,15, проте для забезпечення повноти реакції проміжної ацилімідазольної речовини з сполукою, що має Формулу 3, переважно використовується співвідношення щонайменше 1,05. Порядок додавання реагентів в етапі А методу винаходу є дуже важливим. Сполука з Формулою 2 може бути розчинена в розчиннику, а потім до неї додається сполучний реагент, або сполучний реагент може бути розчинений у розчиннику, а потім до нього додається сполука 8 UA 113615 C2 5 10 15 20 25 30 35 40 45 50 55 з Формулою 2. Проте важливо перед додаванням сполуки з Формулою 3 дати достатньо часу для утворення ацилімідазолу. Зазвичай утворення ацилімідазолу можна спостерігати за виділенням газоподібного діоксиду вуглецю протягом 1–2 годин, в залежності від масштабу реакції. Сполуки з Формулою 2 і Формулою 3 є комерційно доступними. Сполуці з Формулою 3 віддається особлива перевага, тому що з нею легше працювати. Може бути використаний трифторетиламін в нейтральному стані, але він є летючим (температура кипіння 36–37 °C) і менш зручним. В представленому методі реакційна суміш містить розчинник, що не змішується з водою. Було встановлено, що особливо зручними розчинниками є етилацетат та ізопропілацетат. Завдяки можливості розчиняти вихідну речовину, що має Формулу 2, і можливості виділення з води після обробки водою, полярні апротонні розчинники, що не змішуються з водою, є особливо зручними. Кількість використаного розчинника, тобто об'єм, необхідний для розчинення вихідної речовини, звичайно лежить у межах від 0,75 до 1,5 молярної концентрації, але особливо зручною є молярна концентрація 1,0. Реакцію методуза Схемою 2 можна проводити в широкому діапазоні температур. Як правило, температура реакції становить щонайменше приблизно 15 °C, а найчастіше — щонайменше приблизно 20 °C. Як правило, температура реакції не перевищує приблизно 40 °C, а найчастіше — не перевищує приблизно 35 °C. За протіканням реакції можна спостерігати за допомогою стандартних методів, як-от 1 тонкошарова хроматографія, ГХ, ВРХ і H ЯМР-аналіз аліквот. Після закінчення реакції суміш звичайно обробляється шляхом додавання водного розчину мінеральної кислоти, як-от соляна кислота. Відділення органічної фази з подальшою промивкою соляною кислотою (1.0 N) для видалення імідазолу (а також будь-якого триетиламіну, якщо він був доданий), сушка над осушувачем, як-от сульфат магнію або молекулярні сита, або азеотропна сушка, а потім випарювання розчинника дає продукт з Формулою 4 у вигляді безбарвної твердої речовини. Випаровування розчинника є необов'язковим; коли використовується азеотропна сушка, розчинник не видаляється і розчин сполуки з Формулою 4 переноситься далі. Етап C методу винаходу не є обов'язковим і включає в себе реакцію вільного аміну Формули 1 з кислотою Формули 5 з отриманням кислої солі, що має Формулу 1А, як показано в Схемі 3. Схема 3 де Х — це Cl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (PO4)1/3. Вільний амін Формули 1 є чутливим до повітря. Отриманий (в етапі В) розчин сполуки з Формулою 1 може оброблятися кислотою для отримання більш стабільної кислої солі з Формулою 1А. Потім сполуку з Формулою 1А виділяють фільтруванням і сушать у вакуумній печі (50–60 °C) або повітрям. Сіль з Формулою 1А можна зберігати в умовах навколишнього середовища без негативних ефектів збільшення ваги від вологи і впливу повітря, та проблем з обробкою, визваних гігроскопічною липкою текстурою. Для порівняння сполук з Формулами 1 і 1А та інших солей див. Приклад 12. Було встановлено, що безводні кислоти з Формулою 5 є особливо ефективними у забезпеченні високих виходів сполук з Формулою 1A. Ці кислоти включають в себе соляну кислоту, бромистий водень, трифтороцтову кислоту, метансульфокислоту, сірчану або ортофосфорну кислоту, хоча завдяки низькій вартості перевага надається соляній кислоті. Як правило, кислота барботується через реакційну суміш, звільнену від каталізатора, або, у випадку з рідкими кислотами, додається по краплях. Для утворення твердої солі з Формулою 1А, яку можна легко виділити фільтруванням, безводні кислоти з Формулою 5 додаються до розчину в розчиннику, що не змішується з водою, з етапу В. В іншому випадку для отримання водної фази, що містить сполуку з Формулою 1А, водні розчини кислот з Формулою 5 (наприклад, концентрована соляна кислота) можуть по краплях додаватися в розчин з Формулою 1 з етапу В. Ця водна фаза може бути відділена від розчинника, що не змішується з водою, та використана в наступних реакціях. Альтернативою використаній для захисту аміногрупі в методі винаходу в Схемах 1 і 2 групі бензилкарбамату, є трет-бутилкарбамат (BOC), що захищає аміногрупу, як це показано в Схемах 4 і 5 (див. Приклади синтезу 3 і 4). 9 UA 113615 C2 5 10 15 20 25 30 35 40 45 50 В етапі В методу винаходу, зображеному в Схемі 4, сполука з Формулою 1А отримується шляхом безпосередньої взаємодії сполуки з Формулою 7 з кислотою, що має Формулу 5. Реакція включає в себе як видалення захисної групи трет-бутилкарбамату, так і одночасне утворення солі функціональної аміногрупи. Схема 4 де Х — це Cl, Br, CF3CO2, CH3SO3, (SO4)1/2 або (PO4)1/3. Стехіометрія цієї реакції потребує еквімолярної кількості кислоти з Формулою 5 по відношенню до сполуки з Формулою 7. Проте для забезпечення повного видалення захисної групи трет-бутилкарбамату із сполуки з Формулою 7 і повного утворення кислої солі з Формулою 1А бажано, щоб молярний надлишок кислоти з Формулою 5 був від приблизно 2,0 до приблизно 5,0. Було встановлено, що безводні кислоти з Формулою 5 є особливо ефективними у забезпеченні високих виходів сполук з Формулою 1А. Ці кислоти включають в себе соляну кислоту, бромистий водень, трифтороцтову кислоту, метансульфокислоту, сірчану або ортофосфорну кислоту, хоча завдяки низькій вартості перевага надається соляній кислоті. Безводні кислоти у формі газу, як-от соляна кислота (див. Приклад синтезу 4, етап В), зазвичай барботуються через реакційну суміш. У випадку з рідкими кислотами, як-от трифтороцтова кислота (див. Приклад синтезу 7) рідина додається по краплях. Безводні кислоти з Формулою 5 використовуються в розчиннику, що не змішується з водою, для отримання твердої солі з Формулою 1А, яку можна легко виділити фільтрацією реакційної суміші. Утворення і виділення солі продукту з використанням описаної вище процедури дозволяє уникнути етапу обробки водою. Виділена тверда сіль з Формулою 1А може бути використана в наступних реакціях. Було визначено, що водні кислоти з Формулою 5 є особливо ефективними у забезпеченні високих виходів сполук з Формулою 1A. Ці кислоти включають в себе соляну й бромистоводневу кислоти, хоча завдяки низькій вартості перевага надається соляній кислоті (див. Приклад синтезу 4, Етап B1). Як правило, водні кислоти додаються у реакційну суміш по краплях. Коли водні кислоти з Формулою 5 використовуються в розчиннику, що не змішується з водою, утворюється сіль з Формулою 1А, яка потім розчиняється у водній фазі, а тоді відділяється від органічної фази. Концентрований водний розчин сполуки з Формулою 1А може бути легко виділений шляхом виведення водної фази з більшою густиною з нижньої частини реакційної посудини. Концентрований водний розчин сполуки з Формулою 1А може бути використаний у наступних реакціях. В представленому методі реакційна суміш містить розчинник, що не змішується з водою. Було встановлено, що особливо зручними розчинниками є етилацетат та ізопропілацетат. Завдяки можливості розчиняти вихідну речовину, що має Формулу 7, і осаджувати продукт, що має Формулу 1А, полярні апротонні розчинники, які не змішуються з водою, є особливо зручними. Кількість використаного розчинника, тобто об'єм, необхідний для розчинення вихідної речовини, звичайно знаходиться в межах від 0,5 до 1,0 молярної концентрації. Для розчинення сполуки з Формулою 7 і для того, щоб концентрація реакційної суміші перевищувала 0,5 моль, суміш вихідної речовини і розчинника може бути нагріта до приблизно 30 °C. Як тільки вихідна речовина розчиниться, джерело тепла видаляється і до реакційної суміші при кімнатній температурі додається кислота. Метод, показаний в Схемі 4, може бути проведений в широкому діапазоні температур. Як правило, реакцію проводять при температурі щонайменше приблизно 20 °C або кімнатній температурі. Зазвичай в ході реакції реакційна суміш нагрівається, але, як правило, екзотермічність реакції не потребує зовнішнього охолодження, і температура реакції звичайно залишається нижче температури кипіння розчинника. Звичайно температура реакції становить не більше ніж приблизно 45 °C, а частіше — не більше ніж приблизно 40 °C. За протіканням реакції можна спостерігати за допомогою стандартних методів, як-от 1 тонкошарова хроматографія, ГХ, ВРХ і H ЯМР-аналіз аліквот. Після завершення реакції суміш звичайно охолоджується до кімнатної температури, а продукт виділяється за допомогою стандартних методів, як-от фільтрування. Твердий продукт, виділений фільтруванням, може бути висушений у вакуумній печі (50–60 °C) або на повітрю. 10 UA 113615 C2 5 10 15 20 25 30 35 40 У пункті А методу винаходу, зображеному у Схемі 5, сполука з Формулою 7 отримана шляхом взаємодії сполуки з Формулою 8 із сполукою, що має Формулу 3, і сполучним реагентом. Метод отримання сполуки з Формулою 7 включає в себе попередню активацію функціональної групи карбонової кислоти сполуки з Формулою 8 сполучним реагентом для отримання ацилімідазольної сполуки з Формулою 9. Ацилімідазольна сполука з Формулою 9 може бути виділена, але, як правило, її не виділяють. Вона утворює амідний зв'язок з функціональною аміногрупою сполуки з Формулою 3 з утворенням сполуки з Формулою 7. Схема 5 Стехіометрія цієї реакції потребує еквімолярних кількостей сполуки з Формулою 8, сполучного реагенту і основи. Якщо сполучним реагентом є N, N'-карбонілдіімідазол, під час утворення проміжної ацилімідазольної сполуки (сполука з Формулою 9) виділяється один еквівалент діоксиду вуглецю. Під час утворення ацилімідазолу також вивільнюється один еквівалент імідазолу, який вступає в реакцію з одним еквівалентом соляної кислоти, коли до реакційної суміші додається сіль аміну з Формулою 3. Таким чином, якщо сполучним реагентом є N, N'-карбонілдіімідазол, основа може бути отримана з нього. Якщо N, N'-карбонілдіімідазол є сполучним реагентом, потрібен один еквівалент додаткової основи (основний реагент не отримується із сполучного реагенту), як-от триетиламін. Додаткова основа (наприклад, триетиламін або діізопропілетиламін) прискорить реакцію, позаяк вона більш основна порівняно з імідазолом і швидше реагує з сіллю хлористого водню з Формулою 3, вивільняючи її у формі вільної основи для реакції з ацилімідазолом. Молярне співвідношення сполучного реагенту й сполуки з Формулою 2 може бути в межах від приблизно 0,95 до приблизно 1,15, проте для забезпечення повного утворення проміжної ацилімідазольної речовини з Формулою 9 переважно використовується співвідношення щонайменше 1,0. Стехіометрія реакції потребує еквімолярних кількостей сполуки з Формулою 3 і сполуки з Формулою 8. Молярне співвідношення сполуки з Формулою 3 до сполуки з Формулою 8 може бути в межах від приблизно 1,0 до приблизно 1,15, проте для забезпечення повноти реакції проміжної ацилімідазольної речовини з сполукою з Формулою 3 переважно використовується співвідношення щонайменше 1,05. В етапі А можуть бути використані різні сполучні реагенти. Було виявлено, ще декілька алкілхлорформіатів і карбонільних дiгетероарильних реагентів є особливо ефективними у забезпеченні високих виходів сполук з Формулою 7. Ці сполучні реагенти включають в себе метилхлорформіат, етилхлорформіат, ізобутилхлорформіат, N, N'-карбонілдіімідазол й 1,1'карбоніл-біс-(3-метилімідазол)трифторметансульфонату, але переважно N, N'карбонілдіімідазол (також відомий як карбонілдіімідазол). N, N'-карбонілдіімідазол є найбільш ефективним сполучним реагентом, тому що він забезпечує один еквівалент основи для нейтралізації солі аміну з Формулою 3. Сполучні реагенти у вигляді ефіру хлорформіату потребують додавання основного реагенту для нейтралізації кислоти, що утворюється в результаті реакції із сполукою з Формулою 8, і звільнення вільної основи сполуки з Формулою 3 (див. Приклад синтезу 6). Особливо придатною основою для цієї реакції є триетиламін. 11 UA 113615 C2 5 10 15 20 25 30 35 40 45 Порядок додавання реагентів в етапі А методу винаходу є дуже важливим. Сполука з Формулою 8 може бути розчинена в розчиннику, а потім до неї додається сполучний реагент, або сполучний реагент може бути розчинений у розчиннику, а потім до нього додається сполука з Формулою 8. Проте важливо перед додаванням сполуки з Формулою 3 дати достатньо часу для утворення проміжної ацилімідазольної сполуки. Зазвичай утворення проміжної ацилімідазольної сполуки можна спостерігати за виділенням газоподібного діоксиду вуглецю протягом 1–2 годин, в залежності від масштабу реакції. Сполуки з Формулою 8 і Формулою 3 є комерційно доступними. Сполуці з Формулою 3 віддається особлива перевага, тому що з нею легше працювати. Може бути використаний трифторетиламін в нейтральному стані, але він є летючим (температура кипіння 36–37 °C) і менш зручним. Сполука з Формулою 7 також може бути отримана з комерційно доступного NBOC-гліцин-N-карбоксіангідриду (див. Приклад синтезу 5). В представленому методі реакційна суміш містить розчинник, що не змішується з водою. Було встановлено, що особливо зручними розчинниками є етилацетат та ізопропілацетат. Завдяки можливості розчиняти вихідну речовину, що має Формулу 8, і можливості виділення з води після обробки водою полярні апротонні розчинники є особливо зручними. Кількість використаного розчинника, тобто об'єм, необхідний для розчинення вихідної речовини, звичайно лежить у межах від 0,75 до 1,5 молярної концентрації, але особливо зручною є молярна концентрація 1,0. Метод реакції в Схемі 5 може бути проведений в широкому діапазоні температур. Як правило, температура реакції становить щонайменше приблизно 15 °C, а найчастіше — щонайменше приблизно 20 °C. Зазвичай в ході реакції реакційна суміш нагрівається, але, як правило, екзотермічність реакції не потребує зовнішнього охолодження, і температура реакції звичайно залишається нижче температури кипіння розчинника. Як правило, температура реакції не перевищує приблизно 40 °C, а найчастіше — не перевищує приблизно 35 °C. За протіканням реакції можна спостерігати за допомогою стандартних методів, як-от 1 тонкошарова хроматографія, ГХ, ВРХ і H ЯМР-аналізи аліквот. Після завершення реакції суміш, як правило, обробляють додаванням розбавленого водного розчину мінеральної кислоти, як-от соляна кислота. Відділення органічної фази з подальшою промивкою соляною кислотою (1,0 N) для видалення імідазолу або іншої доданої основи, сушка над осушувачем, якот сульфат магнію або молекулярні сита, або азеотропна сушка, а потім випарювання розчинника залишає продукт з Формулою 7 у вигляді безбарвної твердої речовини. Випаровування розчинника є необов'язковим; коли використовується азеотропна сушка, розчинник не видаляється і розчин сполуки з Формулою 7 переноситься далі. Іншою альтернативою бензилкарбамату, захисній групі, що використовується в цьому методі винаходу в Схемах 1 і 2 для захисту аміногрупи, є захисна група дибензиламін, показана на Схемах 6, 7 і 8 (див. Приклад синтезу 8). Альтернативний процес з групою дибензиламіну включає в себе видалення шляхом гідрогенолізу дибензильної захисної групи в проміжній сполуці з Формулою 10 з утворенням сполуки вільного аміну з Формулою 1 так, як показано в Схемі 6. Схема 6 Видалення бензильних захисних груп може бути виконане при різних умовах реакції. Див., наприклад, Greene, T. W.; Wuts, P. G. M. Protective Groups in OrganicSynthesis, 2nd ed.; Wiley: New York, 1991. Один з особливо зручних методів видалення бензильной захисної групи є гідрогеноліз з воднем з використанням каталізаторів з благородних металів, як правило під тиском. Цей метод описан в: Rylander, P. N.; Hydrogenation Methods, Academic Press: San Diego, 1985. Одним особливо зручним каталізатором гідрогенолізу являється паладій на вуглецю (звичайно 5–10 %). 12 UA 113615 C2 5 10 15 20 25 30 35 40 45 Видалення бензильної захисної групи від азоту вимагає більш жорстких умов, ніж видалення бензильної захисної групи від кисню (як в процедурі з трет-бутилоксікарбаматом). Реакцію гідрогенолізу, як правило, проводять під тиском і при підвищеній температурі. Звичайно тиск водню становить 0,34–0,69 MПa (50–100 фунтів на квадратний дюйм). Звичайно температура реакції становить від 50 до 80 °C. Краще, якщо температура буде в межах приблизно 70 °C. Реакція не екзотермічна і для підтримання необхідної температури потребує зовнішнього нагрівання. В методі у Схемі 6 реакційна суміш містить органічний розчинник. Було виявлено, що особливо зручними розчинниками є метанол і етанол, також можуть бути використані інші розчинники, що звичайно використовуються для гідрогенізації. Кількість використаного органічного розчинника, тобто об'єм, необхідний для розчинення вихідної речовини, звичайно лежить у межах від 0,3 до 1,0 молярної концентрації. Суміш вихідної речовини з Формулою 10 в розчиннику під тиском водню нагрівається до необхідної температури. Реакція нагрівається, поки реакція не закінчиться, про що буде свідчити припинення поглинання водню. За протіканням реакції можна спостерігати за допомогою стандартних методів, як-от 1 тонкошарова хроматографія, ГХ, ВРХ і H ЯМР-аналізи аліквот, або по швидкості поглинання водню. Після завершення реакції суміш звичайно охолоджують до кімнатної температури і відфільтровують для видалення нанесеного каталізатора. Продукт реакції, сполука з Формулою 1, виділяється випарюванням і отримується у вигляді олії. Сполука з Формулою 10 може бути отримана взаємодією сполуки з Формулою 11 із сполукою, що має Формулу 12, в присутності основи. Алкілування аміну з Формулою 12 хлоралкілом, що має Формулу 11, показано в Схемі 7. Схема 7 Стехіометрія цієї реакції потребує еквімолярної кількості аміду хлороцтової кислоти з Формулою 11 відносно аміну з Формулою 12. Проте, щоб забезпечити повне протікання реакції аміду хлороцтової кислоти з Формулою 11 і повного утворення дибензиламіну з Формулою 10, бажано мати молярний надлишок аміну з Формулою 12 від близько 1,1 до близько 1,2. Реакція також потребує еквімолярної кількості основи. Залежно від використаної основи, може знадобитися молярний надлишок до 2,0 еквівалентів. Кращою основою є третинний амін, як-от триетиламін або основа Хуніга (діізопропілетиламін), але можуть використовуватись i карбонати лужних металів. В методі, показаному у Схемі 7, реакційна суміш містить органічний розчинник. Було визначено, що особливо зручним розчинником є метанол, але також можна використовувати ароматичні розчинники, як-от толуол, або полярні апротонні розчинники, як-от ацетонітрил. Кількість використаного органічного розчинника, тобто об'єм, необхідний для розчинення вихідної речовини, звичайно лежить у межах від 0,5 до 1,0 молярної концентрації, при цьому особливо зручною є молярна концентрація 0,7. Суміш вихідних аміду хлороцтової кислоти, дибензиламіну і основи в розчиннику нагрівають до кипіння зі зворотним холодильником або до більш високих температур при роботі під тиском. Кращими є температури в діапазоні від 80 до 100 °C. Реакційну суміш нагрівають до завершення реакції, як правило, від 12 до 24 годин. За протіканням реакції можна спостерігати за допомогою стандартних методів, як-от 1 тонкошарова хроматографія, ГХ, ВРХ і H ЯМР-аналіз аліквот. Після завершення реакції реакційна суміш звичайно охолоджується до кімнатної температури і випаровується для видалення розчинника. Залишок масла розчиняють в метиленхлориді або подібному розчиннику і промивають водою принаймні два рази. Продукт виділяється стандартними методами, як-от випаровування. Маслянистий продукт, виділений шляхом випаровування, кристалізується при охолодженні. Вихідна речовина дибензиламін (сполука з Формулою 12) є комерційно доступною. 13 UA 113615 C2 Сполука з Формулою 11 може бути синтезована в результаті взаємодії сполуки з Формулою 13 із сполукою, що має Формулу 3А, в присутності основи. Реакцію аміну з Формулою 3А з хлорангідридом, що має Формулу 13, показано у Схемі 8. Схема 8 5 10 15 20 25 30 35 40 Стехіометрія цієї реакції потребує еквімолярної кількості хлорангідриду з Формулою 13 по відношенню до аміну з Формулою 3А. Проте, для забезпечення повноти реакції аміну з Формулою 3А і повноти утворення продукту з Формулою 11 бажано, щоб молярний надлишок хлорангідриду з Формулою 13 складав від приблизно 1,05 до приблизно 1,1. Також реакція потребує еквімолярної кількості основи. Перевага надається молярному надлишку, подібному до молярного надлишку хлорангідрида. Кращою основою є карбонат калію, але можуть використовуватись різні карбонати або бікарбонати лужних металів. В методі за Схемою 8 реакційна суміш містить двофазну систему з води і розчинника, що не змішується з водою. Було визначено, що особливо зручними розчинниками є етилацетат і диетиловий ефір. Кількість використаного органічного розчинника, тобто об'єм, необхідний для розчинення вихідних речовин, звичайно знаходиться в межах від 1,0 до 1,5 молярної концентрації для аміну і від 4,0 до 5,0 моль для хлорангідриду. Кількість використаної води, тобто об'єм, необхідний для розчинення основи карбонату лужного металу, різниться в залежності від розчинності використаної основи. Стандартною молярною концентрацією для карбонату калію є концентрація в межах від 1,0 до 3,0. Суміш вихідного трифторетиламіну (сполука з Формулою 3А) в розчиннику і водного розчину карбонату перемішується і охолоджується до температури приблизно від –5 до 0 °C. Розчин хлорангідриду хлороцтової кислоти (сполука з Формулою 13) в розчиннику додається протягом 0,5–2 годин до охолодженої реакційної суміші, при цьому температура суміші підтримується в межах від –5 до 0 °C, потім реакційну суміш протягом 1 години перемішують при цій температурі. Реакція за методом, зображеним у Схемі 8, може проводитись у вузькому діапазоні температур. Стандартно реакцію проводять при температурі нижче 10 °C, а найчастіше при температурі нижче 0 °C. Реакція є екзотермічною, тому підтримання бажаної температури потребує зовнішнього охолодження. За протіканням реакції можна спостерігати за допомогою стандартних методів, як-от 1 тонкошарова хроматографія, ГХ і H ЯМР-аналізи аліквот. Після завершення реакції, як правило, суміш розділяється на фази, i фаза, що містить розчинник, промивається водою, а продукт виділяється з розчинника шляхом випаровування розчинника. Маслянистий продукт, виділений при випаровуванні, кристалізується при стоянні. Вихідні речовини хлорангідрид хлороцтової кислоти (сполука з Формулою 13) і трифторетиламін (сполука з Формулою 3А) є комерційно доступними. В іншому варіанті представленого винаходу сполуки з Формулою 14 отримуються із сполук з Формулами 1 або 1А. В методі, показаному в Схемі 9, сполука з Формулою 15 реагує з сполучним реагентом з утворенням проміжної сполуки, що має Формулу 16. Проміжна ацилімідазольна сполука з Формулою 16 може бути виділена (див. Приклад синтезу 9). Частіше ацилімідазол не виділяється, а замість цього безпосередньо обробляється сполукою, що має Формулу 1 або 1А, з утворенням сполуки з Формулою 14. 14 UA 113615 C2 Схема 9 5 10 15 20 25 30 35 Якщо сполучним реагентом є N, N'-карбонілдіімідазол, під час утворення проміжної ацилімідазольної сполуки (сполука з Формулою 16) виділяється один еквівалент діоксиду вуглецю. Під час утворення ацилімідазолу також вивільнюється один еквівалент імідазолу, який вступає в реакцію з одним еквівалентом кислоти (тобто соляною кислотою, бромистим воднем, трифтороцтовою кислотою, метансульфокислотою, сірчаною або ортофосфорною кислотою), коли до реакційної суміші додається сіль аміну з Формулою 1А. Таким чином, якщо сполучним реагентом є N, N'-карбонілдіімідазол, основа може бути отримана з нього. Якщо N, N'карбонілдіімідазол є сполучним реагентом, потрібен один еквівалент додаткової основи (основний реагент не отримується із сполучного реагенту), як-от триетиламін. Додаткова основа (наприклад, триетиламін або діізопропілетиламін) прискорить реакцію, позаяк вона більш основна порівняно з імідазолом і швидше реагує з сіллю хлорида водню з Формулою 1A, вивільняючи її у формі вільної основи для реакції з ацилімідазолом. Як варіант ацилімідазол з Формулою 16 може вступати в реакцію з вільним аміном, що має Формулу 1, замість йогокислої солі з Формулою 1А. Якщо для отримання сполуки з Формулою 14 використовується вільний амін, що має Формулу 1, додаткова основа не потрібна. Див. Приклад синтезу 10 для реакції з використанням сполуки з Формулою 1 і Приклад синтезу 11 для реакції з використанням сполуки, що має Формулу 1А. Стехіометрія реакції в Схемі 9 потребує еквімолярних кількостей сполуки з Формулою 15, сполучного реагенту і основи Молярне співвідношення сполучного реагенту до сполуки з Формулою 15 може бути в межах від приблизно 0,95 до приблизно 1,15, проте для максимального утворення проміжної ацилімідазольної сполуки з Формулою 16 без будь-якого залишку N, N'-карбонілдіімідазолу переважно застосовується співвідношення приблизно 0,97. Стехіометрія реакції потребує еквімолярної кількості сполуки з Формулою 1 або 1А і сполуки, що має Формулу 15. Молярне співвідношення сполуки з Формулою 1 або 1А до сполуки з Формулою 15 може бути в межах від приблизно 1,0 до приблизно 1,15, проте для забезпечення повного протікання реакції проміжної ацилімідазольної сполуки (сполука з Формулою 16) із сполукою, що має Формулу 1 або 1А, переважно застосовується співвідношення приблизно 1,05. В схемі 9 можуть застосовуватись різні сполучні реагенти. Було виявлено, що кілька алкілхлорформіатів і карбонільних дигетероарильних реагентів є особливо ефективними у забезпеченні високих виходів сполук з Формулою 14. Ці сполучні реагенти включають в себе метилхлорформіат, етилхлорформіат, ізобутилхлорформіат, N, N'-карбонілдіімідазол і 1,1'карбоніл-біс-(3-метилімідазол)трифторметансульфонат, але переважно N, N'-карбонілдіімідазол 15 UA 113615 C2 5 10 15 20 25 30 35 40 45 50 55 60 (також відомий як карбонілдіімідазол). N, N'-карбонілдіімідазол є найбільш ефективним сполучним реагентом тому, що він забезпечує один еквівалент основи для нейтралізації солі аміну з Формулою 1А. Сполучні реагенти у вигляді ефіру хлорформіату потребують додавання основного реагенту для нейтралізації кислоти, що утворюється в результаті реакції із сполукою з Формулою 15, і звільнення вільної основи сполуки з Формулою 3. Особливо придатною основою для цієї реакції є триетиламін. Порядок додавання реагентів важливий. Як правило, сполучний реагент розчиняється в розчиннику, і сполука з Формулою 15 додається до нього. Важливо перед додаванням сполуки з Формулою 1 або 1А дати достатньо часу для утворення ацилімідазолу. Зазвичай, утворення проміжної ацилімідазольної сполуки (сполука з Формулою 16) можна спостерігати по виділенню газоподібного діоксиду вуглецю протягом 0,5–2 годин, в залежності від масштабу реакції. Сполука з Формулою 1 або 1А є комерційно доступною або отримується за методом винаходу, описаному в попередніх схемах. Сполука з Формулою 1 або 1А може додаватися в суміш у твердому стані або у вигляді суспензії в полярному апротонному розчиннику, що змішується з водою. Сполука з Формулою 15 була отримана відповідно до процедури F. Feist в Justus Liebigs Annalen der Chemie1932, 496, 99–122. Сполука з Формулою 1А є особливо зручною тому, що її легко обробляти, позаяк вона не є гігроскопічною (див. Приклад 16). Використання нейтральної сполуки вільного аміну з Формулою 1 є менш зручним, позаяк вона є гігроскопічною і тому необхідно мінімізувати вплив повітря. В представленому методі реакційна суміш містить полярний апротонний розчинник, що змішується з водою. Було визначено, що зручними розчинниками є ацетонітрил, тетрагідрофуран і діоксан. Було встановлено, що ацентонітрил є особливо зручним. Кількість використаного розчинника, тобто об'єм, необхідний для розчинення вихідної речовини, звичайно лежить у межах від 0,75 до 1,5 молярної концентрації, але особливо зручною є молярна концентрація 1,0. Метод за Схемою 9 може бути виконаний в широкому діапазоні температур. Як правило, температура реакції становить щонайменше приблизно 20 °C, а частіше — щонайменше приблизно 30 °C. Зазвичай в ході реакції реакційна суміш нагрівається, але, як правило, екзотермічність реакції не потребує зовнішнього охолодження, і температура реакції звичайно залишається нижче температури кипіння розчинника. Як правило, температура реакції становить не більше ніж приблизно 45 °C, а частіше не більше ніж приблизно 35 °C. За протіканням реакції можна спостерігати за допомогою стандартних методів, як-от 1 тонкошарова хроматографія, ГХ, ВРХ і H ЯМР-аналіз аліквот. Після завершення реакції суміш, як правило, обробляють додаванням водного розчину мінеральних кислот, як-от соляна кислота (1,1 моль або 1N). Для проведення гідролізу будь-якого іміну, що може утворитися в результаті взаємодії ацетильної групи продукту (сполука з Формулою 14) і надлишку аміну з сполуки, що має Формулу 1, проводиться нетривала обробка кислотою. Потім, з допомогою основи (гідроксиду або карбонату натрію) рН доводять до 9–10, що призводить до виникнення суспензії. Суспензія охолоджується до 20 °C і фільтрується. Отриманий твердий продукт промивають водою і сушать у вакуумній печі (50–60 °C). В альтернативній процедурі отримання сполуки з Формулою 14 використовують водний розчин сполуки з Формулою 1 або 1А. Варто зазначити, що в реакційній суміші з проміжною ацилімідазольною сполукою, що має Формулу 16, припустима наявність води. Проміжна ацилімідазольна сполука з Формулою 16 швидше реагує з більш нуклеофільним аміном, що має Формулу 1 (доданим безпосередньо або утвореним нейтралізацією солі соляної кислоти з Формулою 1А), чим з менш нуклеофільною водою, що вноситься з водним розчином сполуки з Формулою 1 або 1А. Ця реакція отримання сполуки з Формулою 14 з використанням водного розчину сполуки з Формулою 1 або 1А виконується аналогічно процедурі з використанням сполуки з Формулою 1 або 1А у твердій формі. Порядок додавання реагентів подібний тому, що обговорювався раніше. Після завершення утворення проміжної ацилімідазольної сполуки, для гідролізу надлишку N, N'-карбонілдіімідазолу і для запобігання протіканню побічних реакцій додається невелика кількість води (еквівалентна 0,26 моль). Після гасіння водою надлишку N, N'карбонілдіімідазолу у воді при 20 °C протягом 1 години, по краплях додається концентрований водний розчин сполуки з Формулою 1 або 1А (приблизно 50 М) або суспензія сполуки з Формулою 1 або 1А у воді. Повне протікання реакції між сполукою з Формулою 1 або 1А і проміжною сполукою з Формулою 16 у водному розчині ацетонітрилу, як правило, займає від 12 до 24 годин. Див. Приклади синтезу 12, 13, 14 та 15. Водний розчин сполуки з Формулою 1 або 1А отримується шляхом додавання води до сухої твердої речовини або отримується безпосередньо під час процедури, що була обговорена після 16 UA 113615 C2 5 10 15 20 25 30 35 40 45 50 55 60 Схеми 1. Сполука з Формулою 15 була отримана відповідно до процедури F. Feist в Justus Liebigs Annalen der Chemie1932, 496, 99–122. Інший альтернативний метод отримання сполуки з Формулою 14 з використанням хлорангідриду сполуки з Формулою 15 і сполуки з Формулою 1 описано в Прикладі 7 публікації WO 2009/025983. Без подальшого уточнення вважається, що фахівці в даній області можуть, користуючись попереднім описом, використати цей винахід найповніше. Таким чином, наступні приклади належить тлумачити як просто ілюстративні й не обмежені в розкритті будь-чого будь-яким чином. Етапи в наступних Прикладах ілюструють процедуру для кожного етапу в загальному синтетичному перетворенні, і вихідна речовина для кожного етапу не обов'язково може бути отримана шляхом особливої препаративної дії, процедура якої описана в інших Прикладах або Етапах. Відсотки є ваговими, крім сумішей хроматографічного розчинника або якщо зазначено інше. Долі та відсотки для сумішей хроматографічного розчинника є об'ємними, якщо не вказано 1 інше. Н ЯМР спектри представлені в мільйонних частинах в слабкому полi від тетраметилсилану, "s" означає синглет, "d" означає дублет, "t" означає триплет, "q" означає квартет, "m" означає мультиплет, "dd" означає дублет дублетів, "dt »означає дублет триплетів, і "br" означає широкий. ПРИКЛАД 1 Отримання 2-аміно-N-(2,2,2-трифторетил)ацетамід гідрохлориду N, N-Карбонілдіімідазол (8,2 г, 50,5 ммоль) протягом 14 хв. додавався до суспензії N[(фенілметоксі)карбоніл]гліцину (10 г, 47,8 ммоль) в ізопропілацетаті (100 мл). Отриманий розчин перемішували протягом приблизно 1 години, а потім додали триетиламін (4,84 г, 47,8 ммоль) з наступним порційним додаванням протягом 25 хвилин гідрохлориду трифторетиламіну (6,8 г, 50,2 ммоль), підтримуючи температуру нижче 30 °C. Суспензію було оброблено водою (50 мл) і ізопропілацетатом (25 мл). Отриману двофазну суміш залишили відстоятися, після чого фази були розділені. Водний шар екстрагували ізопропілацетатом (2 × 25 мл). Об'єднані органічні фази промили 1 N соляною кислотою (50 мл), водою (50 мл), насиченим водним розчином бікарбонату натрію (50 мл), розсолом (50 мл), а потім протягом ночі сушили над сульфатом натрію (25 г). Суспензію відфільтрували, а осад промили ізопропілацетатом (30 мл). До об'єднаного промивного розчину й фільтрату додали 10 % паладію на вугіллі (1,00 г) і суміш помістили в атмосферу водню (балон). Приблизно через 2 години реакційну суспензію нагріли до 50 °C і гідрували протягом приблизно 4 годин. Реакційну суміш помістили в атмосферу азоту, охолодили до кімнатної температури, а потім відфільтрували через фільтруючу прокладку Celite® (15 г), змочену ізопропілацетатом. Залишок промили ізопропілацетатом (30 мл). Об'єднані фільтрат і промивний розчин обробили газоподібним хлористим воднем до досягнення рН суміші 1–2 за індикаторним папером, потім через суспензію при температурі 30–35 °C барботували азот до рН 4–6, що визначали за допомогою індикаторного паперу. Суспензію було охолоджено до
ДивитисяДодаткова інформація
Автори англійськоюBruening, Joerg
Автори російськоюБрюнинг Йорг
МПК / Мітки
МПК: C07C 237/22, C07C 231/12, C07C 237/06, C07C 231/14
Мітки: отримання, спосіб, 2-аміно-n-(2,2,2-трифторетил)ацетаміду
Код посилання
<a href="https://ua.patents.su/26-113615-sposib-otrimannya-2-amino-n-222-triftoretilacetamidu.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання 2-аміно-n-(2,2,2-трифторетил)ацетаміду</a>