Сполука 3-децилоксикарбонілметил-4-метил-5-(2-гідроксіетил)тіазолій хлорид, яка має блокуючий ефект на іонну провідність каналів, утворених ністатином
Номер патенту: 27417
Опубліковано: 25.10.2007
Автори: Вовк Андрій Іванович, Романенко Олександр Вікторович, Гіммельрейх Ніна Германівна, Шатурський Олег Ярославович
Формула / Реферат
Сполука 3-децилоксикарбонілметил-4-метил-5-(2-гідроксіетил)тіазолій хлорид, яка має блокуючий ефект на іонну провідність каналів, утворених ністатином, загальної формули:
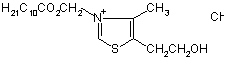 .
.
Текст
Сполука 3-децилоксикарбонілметил-4-метил5-(2-гідроксіетил)тіазолій хлорид, яка має блокуючий ефект на іонну провідність каналів, утворених ністатином, загальної формули: H 21C 10CO 2CH 2 CH 3 + ClN Корисна модель відноситься до медицини, а саме до фармакології. Завданням корисної моделі є дослідження дії сполуки 3-децилоксикарбонілметил-4-метил-5-(2гідроксиетил)тіазолій хлориду (ДМГТ) на іонні канали, утворені ністатином в штучній пласкій бішаровій мембрані. Вивчення дії ДМГТ на іонні канали, сформовані ністатином в штучній пласкій фосфоліпідній мембрані, проводилось у відділі нейрохімії Інституту біохімії імені О.В. Палладіна НАН України і на кафедрі біології Національного медичного університету імені О.О. Богомольця. ДМГТ синтезовано у відділі механізмів біоорганічних реакцій Інституту біоорганічної хімії та нафтохімії НАН України. Тіаміну (вітаміну В1) належить значна роль в організмі людини і тварини у забезпеченні функціонування нервової і м'язової систем. Внаслідок дефіциту вітаміну В1 в організмі можуть порушуватися координація рухів, рефлекторна діяльність, моторика шлунково-кишкового тракту, розвиватися параліч та атрофія м'язів кінцівок. Такі реакції організму можуть обумовлюватися послабленням впливу вітаміну В1 та його похідних на залежні від них ферментативні реакції та квантову секрецію медіатора з нервових закінчень в синапсах різних типів [1-4]. Також виявлено здатність тіаміну та його фосфорильованих форм впливати на проникність іонних каналів збудливих мембран нервових клітин [5], та на іонні струми, обумовлені активацією ацетилхоліном нікотинових та мускаринових холінорецепторів [6]. Серед сполук, які знаходяться в організмах, тіазолієвий цикл виявляється тільки в молекулі тіаміну та продуктах його метаболізму. Було синтезовано нове похідне вітаміну В1 з непорушеним тіазолієвим циклом - сполуку ДМГТ, як потенційний лікарський засіб, та встановлено ряд її властивостей [7-9]. Наявність в складі молекули ДМГТ тіазолієвого циклу визначає можливість її впливу на один із шляхів реалізації біологічної активності вітаміну В1, а довголанцюгового вуглецевоводневого радикалу можливість взаємодії з мембранними структурами. Синтетичне похідне вітаміну В1, що вміщує у своїй структурі тіазолієвий цикл - (ДМГТ), має ряд властивостей, характерних для потенційних лікарських засобів [7-9]. Зокрема, ДМГТ чинить на лабораторних тварин седативну, центральну міорелаксантну, протисудомну та снотворну дію, підвищує поріг їх больової чутливості, послаблює їх агресивність, орієнтувальні реакції та пошукову діяльність, зменшує нейротоксичний вплив на лабораторних тварин a-латротоксину (a-LT) білкового токсину з отрути павука каракурта (Latrodectus mactans tradecimguttatus). ДМГТ блокує спонтанну, викликану подразненням нервових волокон, а також обумовлену дією aлатротоксину квантову секрецію ацетилхоліну із нервових закінчень. a-LT може також підсилювати іонну проникність нервових закінчень, формуючи в (11) 27417 (13) U . UA CH 2CH 2OH (19) S 3 27417 4 мембрані проникні для катіонів білкові пори. потенціал тефлонового стаканчика (цис-сторона) Наведені вище дані обумовили дослідження було задано відносно потенціалу внутрішнього впливу ДМГТ на іонні струми, що виникають після об'єму (транс-сторона), прийнятого рівним віртуальному нулю напруги. Поляризація між облаштування a-LT в штучн у фосфоліпідну електродами не перевищувала 1,5мВ. Потенціал мембрану [10]. прикладався до мембрани від джерела напруги в В основу корисної моделі поставлено те, що діапазоні від -100мВ до +100мВ, що дозволяло блокуюча дія ДМГТ реалізується завдяки його проникненню в порожнину локалізованого в отримувати постійну або лінійно змінювану з швидкістю 100мВ/хв. напругу того ж діапазону бішаровій ліпідній мембрані (БЛМ) амплітуд. Трансмембранні струми записували на каналоформеру, а ступінь блокуючого ефекту двокоординатному самописці Н307/1 зростає при збільшенні співпадіння (Краснодарський завод вимірювальних приладів, гідродинамічного радіусу ДМГТ та радіусу о твору пори, утвореної каналоформером в БЛМ. Російська Федерація). Для перемішування розчину, який оточуючував мембрану, Встановлена здатність ДМГТ в концентрації використовували магнітну мішалку. Всі досліди 0,1мМ послаблювати трансмембранний струм проводили при температурі 22-24°С. через іонні канали, утворені a-LT в бішарових Через 1-2хв після введення ністатину з цисліпідних мембранах (БЛМ) на 31,6±3% на отворі боку БЛМ в симетричному розчині 100мМ КСl пори з ефективним радіусом 0,9нм, та на 50-52% відбувалось збільшення трансмембранного на отворах утворених a-латроінсектотоксином (aструму. Це вказувало на формування іонLIT) із отрути павука каракурта Latrodectus провідних каналів у ліпідному бішарі. mactans tradecimguttatus і токсином морської Беручи до уваги незначні провідності актинії Radianthus macrodactilus (RTX) з схожими поодиноких каналів, сформованих ністатином в ефективними радіусами пор 0,55нм і 0,53нм, БЛМ [12], для дослідження дії ДМГТ на їх іонвідповідно [10, 11]. Ці дані дозволяють припустити, провідну властивість ми використовували БЛМ з що інгібуючий вплив ДМГТ на іонну провідність великою кількістю сформованих ністатином каналів в БЛМ залежить від розмірів отвору пори і каналів. Стаціонарну провідність БЛМ, індуковану збільшується у випадку прикладання цієї сполуки ністатином, використовували як контроль для на отворах каналів меншого розміру. Наведене подальшого вивчення впливу ДМГТ на вище дало підстави очікувати підсилення трансмембранний іонний струм через утворені блокуючого впливу ДМГТ на трансмембранний ністатином канали в БЛМ. В якості еталону іонний струм у випадку прикладання ДМГТ до приймали блокуючу дію тетраметиламонію на ці іонних каналів, утворених ністатином, тому що він канали. Він є найефективнішим із застосованих здатний формувати в БЛМ іонні канали з раніше сполук метонієвого ряду, які блокують приблизним радіусом пори 0,35нм [12]. іонний струм через утворені ністатином в БЛМ Методика формування БЛМ та вивчення іонканали з приблизним ефективним радіусом отвору провідних властивостей каналів, утворених 0,35нм [12]. ністатином. Блокуючий ефект 0,1мМ ДМГТ на вхідний Приготування розчину ністатину. струм через іонні канали, сформовані ністатином в Ністатин ("Fluka", Румунія) спочатку розчиняли БЛМ представлено на Фіг.1. Стаціонарний струм в диметилсульфоксиді (ДМСО), а потім, після через БЛМ у симетричному розчині 100мМ КСl доведення водним розчином 100мМ КСl (рН 7,4) обумовлювався сформованими ністатином до концентрації 100мкг/мл при кінцевій іонними каналами. Потенціал на мембрані концентрації ДМСО 1-4 %, озвучували становив 50мВ. Уведення ДМГТ в комірку з БЛМ ультразвуковим диспергатором УЗДН-2Т (Сумське позначено стрілкою. Ністатин вводили з цисВиробниче Об'єднання "Електрон", Україна) 1хв. сторони мембрани в кінцевій концентрації при частоті 22кГц. 0,09мкг/мл. Нульовий струм позначено Формування БЛМта вимірювання їх іонприривчастою лінією. Після введення 0,1мМ ДМГТ провідних властивостей в симетричному розчині 100мМ КСl Бішарові ліпідні мембрани формували в трансмембранний струм через утворені розчині н-гептану із фосфатидилхоліну (ФХ) (ЗАТ ністатином іонні канали послаблювався порівняно „Біолек", Україна) та холестерину („Sigma", США) з контролем на 67±3% за 4-7хв при постійному при співвідношенні ФХ:холестерин =2:1 у перемішуванні оточуючого мембрану воднорозчиннику. Загальна концентрація ліпідів сольового розчину (Фіг.1). становила 20мг/мл. Мембрану наносили на отвір у Ступінь блокування іонного струму через тефлоновому стаканчику з діаметром 0,6мм. утворені ністатином в БЛМ канали залежить від Тефлоновий стаканчик розміщували в скляній концентрації ДМГТ і може описуватись кривою комірці, через яку у відображеному світлі візуально насичення Ленгмюра. Зменшення спостерігали формування ліпідного бішару за трансмембранного струму через утворені допомогою бінокулярного мікроскопа. Оточуючий ністатином в БЛМ канали можна описати за мембрану водно-сольовий розчин вміщував 10мМ допомогою експоненціального наближення трис-НСІ ("Sigma", США) та необхідну кількість залежності трансмембранного струму від хлориду калію кваліфікації „особлива ступінь концентрації ДМГТ. При цьому початок насичення чистоти" (о.с.ч.). Провідності мембрани досягається при концентрації ДМГТ 0,02мМ. вимірювали за допомогою хлор-срібних Швидкість блокування провідності утворених електродів, занурених у розчин 2М КСl через ністатином іонних каналів визначали після агарові містки з обох боків БЛМ. Зовнішній 5 27417 6 введення кожної концентрації ДМГТ. Блокування 8. Романенко А.В., Вовк А.И., Шатурский О.Я. іонного струму через утворені ністатином в БЛМ Действие тиазолевых аналогов витамина В1 на канали на 50% досягалося при концентрації ДМГТ нервно-мышечную передачу и вызванную a17мкМ. латротоксином секрецию медиатора в скелетной Інгібуюча дія ДМГТ не залежала від знаку мышце // Нейрофизиология. - 1995. - 27, №5/6. потенціалу, прикладеного до БЛМ в діапазоні С.368-374. напруг від -40мВ до +80, і була зворотною. При 9. Романенко А.И., Гнатенко В.М., цьому за 25-30хв перфузії комірки з БЛМ розчином Владимирова И.А., Вовк А.И. Преи 100мМ КСl (80мл) повністю відновлювалась постсинаптическая модуляция нервно-мышечной вихідна провідність іонних каналів, утворених передачи в гладких мышцах тиазолевыми ністатином в БЛМ. аналогами витамина В1 // Нейрофизиология. Звернемо увагу на те, що інгібуюча дія ДМГТ 1995. - 27, №5/6. - С.375-386. 10. Шатурский О.Я., Романенко А.В, на іонну провідність, утворених a-LT, a-LIT та RTX каналів в БЛМ також має зворотний характер [10, Производное тиазолия уменьшает 11]. Імовірно, ДМГТ не утворює стійких зв'язків з трансмембранный ток через ионные каналы, селективними центрами в порожнині вказаних образованные a-латротоксином и токсином вище іонних каналів. морской актинии в бислойных липидных Можна припустити, що е фективний радіус мембранах // Укр. биохим. журн. - 2005. - 74, №4. пори іонного каналу близький до мінімального С.48-55. гідродинамічного розміру непроникаючої в нього 11. Шатурський О.Я., Волкова Т.М., Романенко молекули або ассоціату молекул блокатора. Тоді є О.В., Гіммельрейх Н.Г., Грішин Є.В. Інгибуюча дія підстави вважати, що посилення блокуючого тіазолевого аналога вітаміну В1 на іонні канали, ефекту ДМГТ має місце при наближенні що утворені a-латроінсектотоксином з отрути гідродинамічного розміру блокатора, який каракурта в бішарових фосфоліпідних мембранах проникає в порожнину каналу, до пори // Доп. Н АН України. - 2006. - №5, С.158-162. відповідного розміру. Таким чином, слід 12. Борисова М.П., Ермишкин Л.Н., підкреслити наступне: Зильберштейн А.Я. Блока-горы ионных каналов, 1. ДМГТ на відміну від еталону образуемых в липидном бислое полиеновыми (тетраметиламонію) має гетероциклічну природу. антибиотиками // Биофизика - 1978. - 23, №7. 2. ДМГТ в концентрації 17мкМ зменшує С.1093-1094. трансмембранний струм через сформовані ністатином в БЛМ іонні канали на 50%, а еталон (тетраметиламоній), за даними літератури [12], зменшує трансмембранний струм через сформовані ністатином в БЛМ іонні канали на 50% при концентрації 4,3мМ. Література: 1. Романенко А.В. Действие тиамина на нервно-мышечную передачу у лягушки // Нейрофизиология. - 1985. - 17, №6. - С.794-800. 2. Романенко А.В. Действие тиамина на различные типы синаптических соединений // Нейрофизиология. - 1986. - 18, №5. - С.621-629. 3. Романенко А.В., Гнатенко В.М., Владимирова И.А.. Действие тиамина на нервномышечную передачу в гладких мышцах // Нейрофизиология. - 1994. - 26, №6. - С.449-457. 4. Романенко А.В., Феник В.Б., Арсан О.М. Действие тиамина в скелетной мышце крысы // Физиол. журн. - 1991. - 37, №1. - С.35-41. 5. Bettendorff L. Thiamine in excitable tissues: reflections on a non-cofactor role // Me tab. Brain Dis. - 1994. - 9, №3. - P.183-209. 6. Дятлов В.А., Романенко А.В. Модуляторная роль тиамина в синаптической передаче у пресноводного моллюска // Гидробиол. Журн. 1995. - 31, №6. - С.66-70. 7. Вовк А.И., Романенко А.В., Муравьева И.В., Зайцев Л.М. 3-децоксикарбонилметил-4-метил-5β-гидроксиэтилтиазолий хлорид или децоксикарбонилметил-4-метилтиазолий хлорид, угнетающие нервно-мышечную передачу и обладающие транквилизирующей активностью // Авторское свидетельство 1547267 СССР, МКИ 4 С07D277/24, А61К31/425. Заявлено 18.07.88. Зарегистрировано 01.11.89.
ДивитисяДодаткова інформація
Назва патенту англійською3-decyloxycarbonylmethyl-4-methyl-5-(2-hydroxyethyl)thiazolium chloride compound having blocking action on ion conductance of channels formed by nystatin
Автори англійськоюShaturskyi Oleg Yaroslavovych, Romanenko Oleksandr Viktorovych, Vovk Andrii Ivanovych, Gimmelreikh Nina Germanivna
Назва патенту російськоюСоединение 3-децилоксикарбонилметил-4-метил-5-(2-гидроксиэтил)тиазолий хлорид, которая имеет блокирующий эффект на ионную проводимость каналов, образованных нистатином
Автори російськоюШатурский Олег Ярославович, Романенко Александр Викторович, Вовк Андрей Иванович, Гиммельрейх Нина Германовна
МПК / Мітки
МПК: C07D 277/00
Мітки: провідність, ністатином, має, хлорид, яка, утворених, каналів, 3-децилоксикарбонілметил-4-метил-5-(2-гідроксіетил)тіазолій, сполука, ефект, іонну, блокуючий
Код посилання
<a href="https://ua.patents.su/3-27417-spoluka-3-deciloksikarbonilmetil-4-metil-5-2-gidroksietiltiazolijj-khlorid-yaka-maeh-blokuyuchijj-efekt-na-ionnu-providnist-kanaliv-utvorenikh-nistatinom.html" target="_blank" rel="follow" title="База патентів України">Сполука 3-децилоксикарбонілметил-4-метил-5-(2-гідроксіетил)тіазолій хлорид, яка має блокуючий ефект на іонну провідність каналів, утворених ністатином</a>
Попередній патент: Спосіб виготовлення тимчасових незнімних конструкцій при м’язово-суглобових розладах зубощелепно-лицевої ділянки
Наступний патент: Спосіб визначення та фіксації центрального співвідношення щелеп
Випадковий патент: Похідні 5-арилізоксазолу, спосіб їх одержання (варіанти) і гербіцидна композиція на їх основі та спосіб пригнічення бур'янів в локусі







