Подрібнена форма (s)-2-етокси-3-[4-(2-{4-метансульфонілоксифеніл}етокси]феніл)пропанової кислоти, спосіб її приготування та фармацевтична композиція
Формула / Реферат
1. Подрібнена форма (S)-2-етокси-3-[4-(2-{4-метансульфонілоксифеніл}етокси]феніл)пропанової кислоти, представленої формулою І
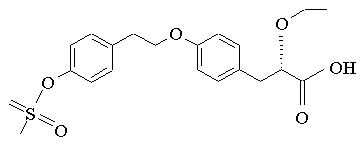 , (І)
, (І)
або її фармацевтично прийнятна сіль чи їх сольват, яка є помірно тонкою, всі частинки якої проходять крізь сито з номінальним розміром комірки 355 мкм і не більше ніж 40,0 % масової частки проходить крізь сито з номінальним розміром комірки 250 мкм.
2. Форма тонкого порошку (S)-2-етокси-3-[4-(2-{4-метансульфонілоксифеніл}етокси]феніл)пропанової кислоти формули І або її фармацевтично прийнятна сіль чи їх сольват, всі частинки якого проходять крізь сито з номінальним розміром комірки 180 мкм і не більше ніж 40,0 % масової частки проходить крізь сито з номінальним розміром комірки 125 мкм.
3. Форма дуже тонкого порошку (S)-2-етокси-3-[4-(2-{4-метансульфонілоксифеніл}етокси]феніл)пропанової кислоти формули І або її фармацевтично прийнятна сіль чи їх сольват, всі частинки якого проходять крізь сито з номінальним розміром комірки 125 мкм і не більше ніж 40,0 % масової частки проходить крізь сито з номінальним розміром комірки 45 мкм.
4. Форма мікротонкого порошку (S)-2-етокси-3-[4-(2-{4-метансульфонілоксифеніл}етокси]феніл)пропанової кислоти формули І або її фармацевтично прийнятна сіль чи їх сольват, не менше ніж 90 % масової частки частинок якого проходять крізь сито з номінальним розміром комірки 45 мкм.
5. Форма супертонкого порошку (S)-2-етокси-3-[4-(2-{4-метансульфонілоксифеніл}етокси]феніл)пропанової кислоти формули І або її фармацевтично прийнятна сіль чи їх сольват, не менше ніж 90 % масової частки частинок якого проходять крізь сито з номінальним розміром комірки 10 мкм.
6. Форма за будь-яким з пп. 1-5 для використання у медичній терапії.
7. Форма за будь-яким з пп. 1-5 для використання в лікуванні або профілактиці станів, що пов’язані зі зниженою чутливістю до інсуліну.
8. Форма за будь-яким з пп. 1-5 для використання в лікуванні або профілактиці дисліпідемії, цукрового діабету 2-го типу, гіперглікемії, гіперінсулінемії, артеріальної гіпертензії та/або абдомінального ожиріння.
9. Застосування форми за будь-яким з пп. 1-5 у виготовленні медикаменту для використання при лікуванні метаболічних розладів.
10. Фармацевтична композиція, що містить форму за будь-яким з пп. 1-5 у поєднанні з фармацевтично прийнятним розріджувачем, ад’ювантом або носієм.
11. Фармацевтична композиція за п. 10, у якій фармацевтично прийнятним розріджувачем, ад’ювантом чи носієм є гідроксипропілцелюлоза.
12. Спосіб приготування форми сполуки формули І із зменшеним розміром частинок або її фармацевтично прийнятної солі чи їх сольвату за будь-яким з пп. 1-5, що включає перетворення на порошок твердої форми сполуки формули І або її фармацевтично прийнятної солі чи їх сольвату за період часу, достатній для одержання бажаного розміру частинки сполуки формули І або її фармацевтично прийнятної солі чи їх сольвату.
Текст
Винахід стосується форми сполуки (S)-2-етокси-3-[4-(2-{4метансульфонілоксифеніл}етокси)феніл]пропанової кислоти, представленої формулою І або її фармацевтично прийнятної солі чи сольвату зі зменшеним розміром частинок. Винахід також стосується способів лікування одного чи більше станів, пов'язаних з синдромом інсулінорезистентності, застосовуючи форму сполуки або її фармацевтично прийнятної солі зі зменшеним розміром частинок у виробництві медикаментів призначених для застосування при одному чи більше розладах. Винахід також стосується фармацевтичних композицій, що містять форму сполуки або її фармацевтично прийнятної солі чи сольвату зі зменшеним розміром частинок, як активний інгредієнт, а також способів виготовлення форми сполуки, або її фармацевтично прийнятної солі зі зменшеним розміром частинок. При утворенні лікарських композицій важливо, щоб лікарська речовина мала таку форму, яка б дозволяла легке користування та оброблення. Це важливо з огляду на виготовлення фармацевтичних композицій, які містять активну сполуку. Сполуку згідно з винаходом застосовують при лікуванні такого порушення обміну речовин, як синдром інсулінорезистентності - зменшеної чутливості до дії інсуліну в усьому тілі чи окремих його тканинах, таких як скелетний м'яз, міокард, жир та печінка, що превалює у багатьох осіб з цукровим діабетом чи без нього. Синдром інсулінорезистентності, пов'язаний із сукупністю проявів, включно з резистентністю до інсуліну, що супроводжуються гіперінсулінемією, можливим цукровим діабетом 2-го типу, артеріальною гіпертензію, центральним (вісцеральним) ожирінням, дисліпідемію у вигляді порушених рівнів ліпопротеїну, які типово характеризуються підвищеною ЛДНГ (ліпопротеїни з дуже низькою густиною) та зменшеною ЛВГ (ліпопротеїни з високою густиною), а також зниженим фібринолізом. Як показали нещодавні епідеміологічні дослідження, особи з резистентністю до інсуліну зазнають підвищеного ризику серцево-судинних захворювань та смертності, особливо ті, хто переніс інфаркт міокарда чи інсульт. Атеросклероз, пов'язаний з цукровим діабетом 2-го типу, виявляється причиною майже 80% смертей. Щодо клінічної медицини, тут також усвідомлюють необхідність підвищити сприйнятливість інсуліну серед хворих на синдром інсулінорезистентності та, відповідно, ліквідувати дисліпідемію, яку вважають причиною прискореного розвитку атеросклерозу. Проте сьогодні таке захворювання не є чітко визначеним. Винайдено форму описаної вище сполуки зі зменшеним розміром частинок, яка складає основу винаходу. Значні переваги можуть виникнути тоді, коли сполука формули І має вигляд форми зі зменшеним розміром частинок, наприклад, при її отриманні для утворення однорідних композицій з однаковою кількістю активного інгредієнту для кожної партії. Крім того, зменшення розміру частинок звичайно пов'язане з підвищеною швидкістю розчинення при пероральному уведенні та покращеною пероральною біодоступностю, якщо останню обмежено швидкістю розчинення активного інгредієнта. Отже, даний винахід стосується форми (S)-2-етокси-3-[4-(2-{4-метансульфонілоксифеніл}етокси)феніл]пропанової кислоти, представленої формулою І або її фармацевтично прийнятної солі чи сольвату зі зменшеним розміром частинок. Термін "зменшений розмір частинок" стосується твердої Сполуки І або її фармацевтично прийнятної солі чи сольвату, подрібненої відповідними способами обробки, до твердої речовини з меншим розміром частинок і, відповідно, більшою площею поверхні. Для зменшення розміру частинок твердої речовини можна використовувати будь-які способи обробки, відомі в галузі фармацевтики, наприклад, подрібнення, розмелювання, тонке подрібнення, для більш вичерпного огляду слід зробити посилання на Ремінгтон (Remington): The Science and Practise of Pharmacy, 19 th Ed., стор. 1598-1602. Термін "сольватований" також розуміють як гідратований. Винахід стосується способу виготовлення форми сполуки формули І або її фармацевтично прийнятної солі чи сольвату зі зменшеним розміром частинок, який включає подрібнення твердої речовини сполуки формули І або її фармацевтично прийнятної солі чи сольвату протягом часу, необхідного для одержання бажаного розміру частинки сполуки формули І або її фармацевтично прийнятної солі чи сольвату. У цьому винаході діапазон переважного розміру частинок представлено згідно зі збільшенням переваги, починаючи з порошку середньої дисперсності, дисперсного, дуже дисперсного, мікродисперсного та супердисперсного порошку. Переваги щодо розміру частинок порошку запозичені з фармакопеї Британії 1993, Том II, Додаток XVII В, А193 та наведені нижче як посилання. Порошок середньої дисперсності Порошок, усі частинки якого проходять крізь сито, номінальний отвір якого становить 355мкм та не більше ніж 40,0% масової частки проходить крізь сито, номінальний отвір якого становить 250мкм. Дисперсний порошок Порошок, усі частинки якого проходять крізь сито, номінальний отвір якого становить 180мкм та не більше ніж 40,0% масової частки проходить крізь сито, номінальний отвір якого становить 125мкм. Дуже дисперсний порошок Порошок, усі частинки якого проходять крізь сито, номінальний отвір якого становить 125мкм та не більше ніж 40,0% масової частки проходить крізь сито, номінальний отвір якого становить 45мкм. Мікродисперсний порошок Порошок, не менше ніж 90% масової частки частинок якого проходять крізь сито, номінальний отвір якого становить 45мкм. Супердисперсний порошок Порошок, не менше ніж 90% масової частки частинок якого проходять крізь сито, номінальний отвір якого становить 10мкм. Окремі сита, які використовують для визначення розміру частинок, описані у фармакопеї Британії 1993, Том II, Додаток XVII В, А193-А194 та включені тут як посилання. Винахід також стосується форми сполуки формули І, яку описано вище, зі зменшеним розміром частинок для застосування у медичній терапії. Об'єктом винаходу є також фармацевтична композиція, яка містить форму сполуки формули І, яку описано вище, зі зменшеним розміром частинок у поєднанні з фармацевтично прийнятним розріджувачем, ад'ювантом чи носієм. Композиція може мати форму, для перорального уведення, наприклад, таблетки, капсули, розчину у воді чи в олії, суспензії чи емульсії; місцевого призначення, наприклад, крем, мазь, гель, водний, олійний розчин чи суспензія; назального введення, наприклад, лікарський порошок для вдихання через ніс, назальний спрей або краплі; вагінального чи ректального введення, наприклад, супозиторій; для інгаляційного введення, наприклад, у вигляді високодисперсного порошку, такого як сухий порошок чи рідкий аерозоль; сублінгвального чи букального введення, наприклад, таблетка чи капсула; або парентерального введення (включно з внутрішньовенним, підшкірним, внутрішньом'язовим, внутрішньосудинним чи інфузією), наприклад, стерильний водний або масляний розчин, або суспензія. Взагалі, композиція може бути одержана традиційним способом, застосовуючи традиційні ексципієнти. Кількість форми сполуки формули І, яку описано вище, зі зменшеним розміром частинок, поєднаної з одним чи кількома ексципієнтами (для виготовлення одноразової дозованої форми), обов'язково буде змінюватися залежно від хворого та способу введення. Наприклад, композиція призначена для перорального введення людині, як правило, буде містити від 0,01мг до 50мг активного засобу у поєднанні з відповідною і стандартною кількістю ексципієнтів, масова частка яких може змінюватися від 20% до 99,99% від загальної маси композиції. Одинична дозована форма, як правило, буде містити приблизно від 0,0001мг до 1мг активного інгредієнту. Винахід також пов'язаний із застосуванням Сполуки згідно з винаходом, яку описано вище, для виготовлення медикаменту, призначеного для: (і) лікування дисліпідемії; (іі) лікування цукрового діабету 2го типу; (ііі) лікування гіперглікемії; (iv) лікування гіперліпідемії; (ν) лікування гіперінсулінемії; (vi) лікування артеріальної гіпертензії; та/або (vii) лікування абдомінального ожиріння. Винахід також стосується способу одержання ефекту, який описано вище, або лікування хвороби чи розладу, який включає введення теплокровній тварині, яка потребує такого лікування, ефективної кількості форми Сполуки формули І, яку описано вище, зі зменшеним розміром частинок. Величина дози форми Сполуки зі зменшеним розміром частинок згідно винаходу, для терапевтичних чи профілактичних цілей безумовно буде змінюватися залежно від типу та складності медичного стану, віку та статі тварини чи пацієнта, які потребують лікування, а також способу введення згідно з відомими правилами медицини. Відповідні щоденні дози сполук, згідно з винаходом, при терапевтичному лікуванні людей становлять приблизно від 0,001-10мг/кг маси тіла, найкраще 0,01-1мг/кг маси тіла. Подрібнена форма сполуки формули І може бути призначена як єдиний засіб лікування або спільно з іншими фармакологічно активними агентами, такими як протидіабетичний, протигіпертензивний, діуретик чи протигіперліпідемічний. Далі винахід буде підтверджений Прикладами, які не обмежують його. Приклад 1 Синтез (S)-2-етокси-3-[4-[[4-(метилсульфонілокси)фенетил]окси]феніл]пропанової кислоти 1-(метилсульфонілокси)-2-[4-(метилсульфонілокси)феніл]етан 2-(4-гідроксифеніл)етанол (356г, 2,58 моль, 1,0екв.) розчинили у метиленхлориді (3500мл) та триетиламіні (653г, 6,44 моль, 2,5екв.). Суміш охолодили до -20°С. Додали метансульфонілхлорид (657г, 5,74 моль, 2,2екв.) підтримуючи температуру між -25°С та -15°С. Коли конверсія досягала більше 95%, утворену під час реакції сіль відфільтрували та промили метиленхлоридом (600мл). Спочатку органічний шар промили насиченим розчином гідрокарбонату натрію (700мл) при температурі 20°С, а після цього водою (700мл). Метиленхлорид випарили досуха, а залишок використовували на наступному етапі. Етилу (S)-2-етокси-3-[4-[[4-(метилсульфонілокси)фенетил]окси]феніл]пропаноат Етилу (S)-2-етокси-3-(4-гідроксифеніл)пропаноат (325г, 1,36 моль, 1,0екв.) розчинили у ацетонітрилі (2600мл). Коли утворився гомогенний розчин, додали карбонат калію (560г, 4,05 моль, 3,0екв.) та сульфат магнію (100г, (0,2г/г К2СО3)). До ацетонітрильного розчину влили 1-(метилсульфонілокси)-2-[4(метилсульфонілокси)феніл]етан (приблизно 2050мл (0,3г/мл, 2,21 моль, 1,65екв.)) і реакцію суміші вели із зворотним холодильником при температурі 82°С протягом 24 годин, інтенсивно перемішуючи. Коли конверсія перевищила 98%, реакційну суміш охолодили до кімнатної температури. Солі, що залишились, відфільтрували та промили ацетонітрилом (800мл). Фільтрат випарили досуха. Масляний залишок використовували на наступному етапі. Етил (S)-2-етокси-3-[4-[[4-(метилсульфонілокси)фенетил]окси]феніл]пропанова кислота До масла етил (S)-2-етокси-3-[4-[[4-(метилсульфонілокси) фенетил] окси]феніл] пропаноату (723г, (71,2% дослід), 1,18 моль, 1,0екв.) додали тетрагідрофуран (3900мл). Коли утворився гомогенний розчин, додали воду (900мл). Суміш охолодили до +10°С. Через одну годину додали розчин гідроксиду літію (390мл, 4М, 1,32екв.). Далі температуру підвищували до +30°С, реакцію вели при такій температурі протягом 2-3 годин. Коли конверсія досягла перевищила 99%, реакцію припинили. Додали етилацетат (500мл), а суміш охолодили до кімнатної температури. Розчин перемішували протягом приблизно 30 хвилин та випаровували тетрагідрофуран. Коли приблизно 80%-90% тетрагідрофурану випарилось, додали воду (1900мл). Випарювання продовжували, доки у суміші зовсім не залишалось тетрагідрофурану. Далі лужний водяний розчин промили етилацетатом (1000мл, 2x1250мл та 950мл). рН водного розчину (S)-2 етокси-3-[4-[[4-(метилсульфонілокси)фенетил]окси]феніл] пропанової кислоти довели до 2,0-2,5 за допомоги НСІ (водний) (550мл, 3,0М). Додали етилацетат (2500мл) та розділили фази. Етилацетатний розчин (S)-2-етокси-3-[4-[[4-(метилсульфонілокси)фенетил]окси]феніл]пропанової кислоти промили водою (700 мл), а після розділення випарили досуха. Масло, що залишилась, використовували у подальшій кристалізації. Кристалізація (S)-2-етокси-3-[4-[[4-(метилсульфонілокси)фенетил]окси]феніл]пропанова кислота Масло з трьох порцій (S)-2-етокси-3-[4-[[4-(метилсульфонілокси)фенетил]окси]феніл]пропанової кислоти (1262г, 3,09 моль, 1,0екв.) розчинили у толуолі (2500мл) при температурі 50°С. Після того, як одержали прозорий розчин, його випарювали, щоб зменшити кількість присутнього етилацетату. Об'єм до випарювання становив 6750мл. Додали ще одну порцію толуолу (2500), після додавання об'єм становив 7750 мл випарювання продовжили. Далі до розчину додали третю порцію толуолу (2500 мл), об'єму до випарювання становив 6300 мл, після додавання об'єм становив 8800 мл Випарювання продовжували, доки не утворився непрозорий розчин об'ємом 8200мл Ізооктан (1000 мл) додали до розчину, який був підігрітий до 40°С. Кристалізацік розпочинали введенням затравки при 40°С. Суміш інтенсивно перемішували, доки ж утворилась суспензія. Інтенсивність змішування підвищували. Суспензію залишали на ніч для кристалізації. Далі, суспензію фільтрували та промивали толуолом:ізооктаном 5:1 (1800мл). Після чого, кристали висушували під зниженим тиском при температурі 40°С. Приклад 2 Одержання форми сполуки І зі зменшеним розміром частинок Приклад 2:1: Сполука І 0,8г Гідроксипропілцелюлоза LF 24г Вода 1000г Сполуку І диспергували у 600г води перемішуючи за допомоги змішувача з великими зсувними зусиллями. Додали гідроксипропілцелюлозу LF та продовжували перемішування, доки суспензія не стала однорідною. Суспензію перекачали до кулькового млину, обладнаного скляними кульками приблизно 500мл 1,0-1,5мм, із застосуванням перистальтичного насосу приблизно 70г/хвил. Розмелювання виконували при 2000 обертах на хвилину. Перші 200г подрібненої суспензії знову вливали. Змішувач, посудину, шланги та млин ополоскували 400г води. Розмір частинки аналізували на суспензії перед та після розмелювання, із застосуванням Coulter LS. Середній розмір частинки становив 24,93мкм та 7,086мкм відповідно. Приклад 2:2: Сполука І 8г Гідроксипропілцелюлоза LF 24г Вода 1000г Сполуку І диспергували у 400г води перемішуючи за допомоги змішувача з великими зсувними зусиллями. Додали гідроксипропілцелюлозу LF та продовжували перемішування, доки суспензія не стала однорідною. Суспензію перекачали до кулькового млину, обладнаного скляними кульками приблизно 500 мл 1,0-1,5мм, застосовуючи перистальтичний насос приблизно 80г/хвил. Розмелювання виконували при 2000 обертах на хвилину. Перші 200г подрібненої суспензії знову вливали. Змішувач, посудину, шланги та млин ополоскували 600г води. Розмір частинки аналізували на суспензії перед та після розмелювання, застосовуючи Coulter LS. Середній розмір частинки становив 14,79мкм та 7,614мкм відповідно. Приклад 2:3: Сполука І 5г Гідроксипропілцелюлоза LF 600г Вода 8000г Сполуку І диспергували у 4000г води перемішуючи за допомоги змішувача з великими зсувними зусиллями. Додали гідроксипропілцелюлозу LF та продовжували перемішування, доки суспензія не стала однорідною. Суспензію перекачали до кулькового млину, обладнаного скляними кульками приблизно 500 мл 1,0-1,5мм, застосовуючи перистальтичний насос приблизно 75г/хвил. Розмелювання виконували при 2000 обертах на хвилину. Перші 200г подрібненої суспензії знову вливали. Змішувач, посудину, шланги та млин ополоскували 4000г води. Розмір частинки аналізували на суспензії перед та після розмелювання, застосовуючи Coulter LS. Середній розмір частинки становив 48,35мкм та 6,822мкм відповідно.
ДивитисяДодаткова інформація
Назва патенту англійськоюGrinded form of (s)-2-ethoxy-3-[4-(2-{4-methanesulfonyloxyphenyl}ethoxy]phenyl)]propane acid, a method for the preparation thereof and a pharmaceutical composition
Назва патенту російськоюИзмельченная форма (s)-2-этокси-3-[4-(2-{4-метансульфонилоксифенил}этокси]фенил)пропановой кислоты, способ ее приготовления и фармацевтическая композиция
МПК / Мітки
МПК: C07C 303/00, A61K 31/255, C07C 309/00, A61P 3/04, A61P 3/10, A61P 5/48, A61K 9/14, A61P 3/06, A61P 3/00, A61P 9/12
Мітки: подрібнена, композиція, приготування, s)-2-етокси-3-[4-(2-{4-метансульфонілоксифеніл}етокси]феніл)пропанової, спосіб, кислоти, фармацевтична, форма
Код посилання
<a href="https://ua.patents.su/3-73959-podribnena-forma-s-2-etoksi-3-4-2-4-metansulfoniloksifeniletoksifenilpropanovo-kisloti-sposib-prigotuvannya-ta-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Подрібнена форма (s)-2-етокси-3-[4-(2-{4-метансульфонілоксифеніл}етокси]феніл)пропанової кислоти, спосіб її приготування та фармацевтична композиція</a>
Попередній патент: Нові фторалкілзаміщені циклотрисилоксани (варіанти), їх використання для одержання нових полімерів та нові полімери
Наступний патент: Гербіцидний засіб, що містить гербіцид з групи інгібіторів гідроксифенілпіруватдіоксигенази
Випадковий патент: Перемикаючий пристрій







