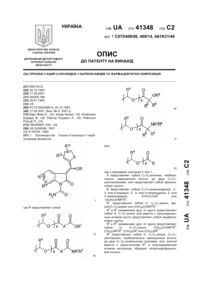
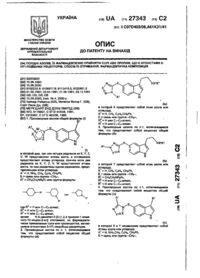
Проліки 3-ацил-2-оксіндол-1-карбоксамідів та фармацевтична композиція
Номер патенту: 41348
Опубліковано: 17.09.2001
Автори: Робінсон Ральф П., Клейнман Едвард Ф., Барт Вейн Е., Рейтер Лоуренс А., Купер Келвін
Формула / Реферат
1. Пролекарства З-ацил-2-оксиндол-1-карбоксамида формулы:
где R представляет собой
где х принимает значение 0 или 1,
А представляет собой С1-С5-алкилен, необязательно замещенный вплоть до двух Сз-С7-циклоалкилами, или представляет собой фениленовую группу,
В представляет собой С2-С6-алкенилфенил, 2-, 3- или 4-пиридил, 2-, 3- или 4-пиперидинил, 2- или 3-пирролидинил, -OCH2CO2R1 или –OCH2CONR2R3,
R1 представляет собой Н, С1-С7-алкил, фенил(С1-С4)алкил или (CH2)pCONR2RЗ,
R2 и R3 независимо друг от друга представляют собой Н, С1-С7-алкил или вместе с присоединенным атомом азота представляют собой морфолиновую группу,
R4 и R5 независимо друг от друга представляют собой Н, С1-С7-алкил, (CH2)pCONR2R3, (CH2)pNR7R8, (CH2)pOR6 или (CH2)pSR6,
R6 представляет собой Н, C1-С6-алкил, Сз-С7-циклоалкил, необязательно замещенный вплоть до двух С1-С6-алкильными группами, или, взятый вместе с заместителем R4 и присоединенным атомом кислорода, образует тетрагидрофурановое кольцо,
R7 и R8 независимо друг от друга представляют собой Н, C1-С6-алкил,
R9 представляет собой Н или метил,
R10 и R11 представляют галоген,
R12 и R13 независимо представляют водород, галоген,
р равно 1-3,
при условии, что, когда заместитель R представляет собой формулу II, а х принимает значение 0, А должен представлять собой группу, отличную от С2-С6-алкиленовой группы.
2. Соединение по пункту 1, где один из заместителей R10 и R11 представляет собой 5-фтор, а другой - 6-хлор.
3. Соединение по пункту 2, где R представляет собой группу формулы:
где значения R1, R9, А и х указаны выше.
4. Соединение по пункту 3, где х принимает значение 0.
5. Соединение по пункту 3, где х принимает значение 1.
6. Соединение по пункту 5, где А представляет собой С1-С5-алкилен.
7. Соединение по пункту 6, где R1 представляет собой бензил.
8. Соединение по пункту 2, где R представляет собой группу формулы:
где R4, R5, R6 и R9 имеют значения, указанные выше, и х принимает значение 1.
9. Соединение по пункту 1, где R4, R9, R12 и R13 представляют собой атом водорода, R5 представляет собой атом водорода, метил или этил, а R6 представляет собой атом водорода, метил.
10. Соединение по пункту 2, где R представляет собой группу формулы:
где R4, R5, R7, R8 и R9 имеют значения, указанные выше, и х принимает значение 1.
11. Соединение по пункту 10, где R4, R7, R8, R9, R12 и R13 представляют собой атом водорода, а R5 представляет собой (CH2)pNR7R8 или метил.
12. Соединение по пункту 2, где R представляет собой группу формулы:
где R9 и В имеют значения, указанные выше, и х принимает значение 1.
13. Соединение по пункту 12, где В представляет собой 2- или 3-пирролидинил.
14. Соединение по пункту 2, где R представляет собой группу формулы:
где R2, R3, R9, А и х имеют значения, указанные выше.
15. Фармацевтическая композиция, проявляющая обезболивающую и противовоспалительную активность, отличающаяся тем, что содержит эффективное количество соединения формулы I по пункту 1 и фармацевтически приемлемый носитель.
Текст
1. Пролекарства 3-ацил-2-оксиндол-1-карбоксамида формулы: , IV , V , III (13) 41348 II (11) , где R представляет собой UA I (19) , , VI где х принимает значение 0 или 1, А представляет собой С1-С5-алкилен, необязательно замещенный вплоть до двух С3-С7циклоалкилами, или представляет собой фениленовую группу. В представляет собой С2-С6-алкенилфенил, 2-, 3- или 4-пиридил, 2-, 3- или 4-пиперидинил, 2- или 3-пирролидинил, -OCH2CO2R1 или 2 3 -OCH2CONR R , R1 представляет собой Н, С1-С7-алкил, фенил(С1-С4)алкил или (CH2)pCONR2R3, R2 и R3 независимо друг от друга представляют собой Н, С1-С7-алкил или вместе с присоединенным атомом азота представляют собой морфолиновую группу, R4 и R5 независимо друг от друга представляют собой Н, С1-С7-алкил, (CH2)pCONR2R3, 7 8 6 (CH2)pNR R , (CH2)pOR или (CH2)pSR6, R6 представляет собой Н, C1-С6-алкил, С3-С7циклоалкил, необязательно замещенный вплоть до двух С1-С6-алкильными группами, или, взятый вместе с заместителем R4 и присоединенным атомом кислорода, образует тетрагидрофурановое кольцо, C2 или 41348 R7 и R8 независимо друг от друга представляют собой Н, C1-С6-алкил, R9 представляет собой Н или метил, R10 и R11 представляют галоген, R12 и R13 независимо представляют водород, галоген, р равно 1-3, при условии, что, когда заместитель R представляет собой формулу II, а х принимает значение 0, А должен представлять собой группу, отличную от С2-С6-алкиленовой группы. 2. Соединение по пункту 1, где один из заместителей R10 и R11 представляет собой 5-фтор, а другой - 6-хлор. 3. Соединение по пункту 2, где R представляет собой группу формулы: ляет собой атом водорода, метил или этил, а R6 представляет собой атом водорода, метил. 10. Соединение по пункту 2, где R представляет собой группу формулы: , V где R4, R5, R7, R8 и R9 имеют значения, указанные выше, и х принимает значение 1. 11. Соединение по пункту 10, где R4, R7, R8, R9, R12 и R13 представляют собой атом водорода, а R5 представляет собой (CH2)pNR7R8 или метил. 12. Соединение по пункту 2, где R представляет собой группу формулы: , II где значения R1, R9, А и х указаны выше. 4. Соединение по пункту 3, где х принимает значение 0. 5. Соединение по пункту 3, где х принимает значение 1. 6. Соединение по пункту 5, где А представляет собой С1-С5-алкилен. 7. Соединение по пункту 6, где R1 представляет собой бензил. 8. Соединение по пункту 2, где R представляет собой группу формулы: , VI где R9 и В имеют значения, указанные выше, и х принимает значение 1. 13. Соединение по пункту 12, где В представляет собой 2- или 3-пирролидинил. 14. Соединение по пункту 2, где R представляет собой группу формулы: , III где R2, R3, R9, А и х имеют значения, указанные выше. 15. Фармацевтическая композиция, проявляющая обезболивающую и противовоспалительную активность, отличающаяся тем, что содержит эффективное количество соединения формулы I по пункту 1 и фармацевтически приемлемый носитель. , IV где R4, R5, R6 и R9 имеют значения, указанные выше, и х принимает значение 1. 9. Соединение по пункту 1, где R4, R9, R12 и R13 представляют собой атом водорода, R5 представ карбоксамидов, которые имеют следующую формулу: Настоящее изобретение относится к противовоспалительным и обезболивающим агентам и, в частности, к енольным сложноэфирным и эфирным пролекарствам 3-ацил-2-оксиндол-1карбоксамидов, составляющих новый класс известных нестероидных противовоспалительных агентов. Использование оксиндолов в качестве противовоспалительных агентов сообщалось в патенте США 3634453, в котором описываются 1-замещенные 2-оксиндол-3-карбоксамиды. Недавно в патенте США 4556672 был описан ряд 3-ацил-2-оксиндол-1-карбоксамидов, которые являются ингибиторами ферментов циклооксигеназы (ЦО) и липоксигеназы (ЛО) и которые могут быть использованы в качестве обезболивающих и противовоспалительных агентов для млекопитающих. В патенте США 5118703 описаны некоторые пролекарства на основе 3-ацил-2-оксиндол-1 (A) где каждый из заместителей X и Y представляет собой атом водорода, фтора или хлора; заместитель R1 представляет собой 2-тиенил или бензил; а заместитель R представляет собой алканоил, содержащий от двух до десяти атомов углерода, 2 41348 циклоалкилкарбонил, содержащий пять-семь атомов углерода, фенилалканоил, содержащий семьдесять атомов углерода, хлор-бензоил, метоксибензоил, теноил, ω-алкоксикарбонилалканоил, где вышеуказанная алкокси-группа содержит от одного до трех атомов углерода и вышеуказанная алканоильная группа содержит от трех до пяти атомов углерода; алкоксикарбонил, содержащий от двух до десяти атомов углерода; феноксикарбонил; 1-(ацилокси)алкил, где вышеуказанная ацильная группа содержит от одного до четырех атомов углерода, а вышеуказанная алкильная группа - от двух до четырех атомов углерода; 1-(алкоксикарбонилокси)алкил, где вышеуказанная алкокси-группа содержит от двух до 5 атомов углерода, а вышеуказанная алкильная группа - от одного до четырех атомов углерода; алкильная группа - от одного до трех атомов углерода; алкилсульфонильную группу, содержащую от одного до трех атомов углерода; метилфенилсульфонильную или диалкилфосфонатную группу, где каждый из вышеуказанных алкилов содержит от одного до трех атомов углерода. Патенты США 5118703 и 4556672 включены в качестве справочного материала. Настоящее изобретение предлагает противовоспалительные эфирные или сложноэфирные пролекарства формулы: , , ,I II , V , VI где х принимает значения 0 или 1; А представляет собой С1-С5-алкилен, необязательно замещенный вплоть до двух С3-С7циклоалкилами или представляет собой фениленовую группу; В - представляет собой С2-С6-алкенилфенил, 2-, 3- или 4-пиридил, 2-, 3- или 4-пиперидинил, 2- или 3-пирролидинил, -OCH2CO2R1 или 2 3 -OCH2CONR R ; заместитель R1 представляет собой Н, С1-С7алкил, фенил(С1-С4)алкил или (CH2)pCONR2R3; заместители R2 и R3 независимо друг от друга представляют собой Н, С1-С7-алкил или вместе с присоединенным атомом азота представляют собой морфолиновую группу; R4 и R5 независимо друг от друга представляют собой Н, С1-С7-алкил, (CH2)pCONR2R3, 7 8 6 (CH2)pNR R , (CH2)pOR или (CH2)pSR6; R6 представляет собой Н, С1-С6-алкил, С3-С7циклоалкил, необязательно замещенный вплоть до двух C1-C6-алкильными группами, или взятый вместе с заместителем R4 и присоединенным атомом кислорода образует тетрагидрофурановое кольцо; R7 и R8 независимо друг от друга представляют собой Н, C1-C6-алкил; R9 представляет собой Н или метил; R10 и R11 представляют галоген; R12 и R13 независимо представляют водород, галоген; р принимает значения 1-3; при условии, что когда заместитель R представляет собой формулу II, а х равен 0, А должен представлять собой группу, отличную от С2-С6алкиленовой группы. Предпочтительными являются соединения, где один из заместителей R10 и R11 представляет собой 5-фтор, а другой - 6-хлор. где R представляют собой , IV III 3 41348 Другими предпочтительными соединениями являются соединения, где R представляет собой группу формулы: или смесь изомеров, которую представляют в виде формулы где значения R1, R9, А указаны выше и х принимает значение 0. Третью предпочтительную группу соединений формулы I составляют соединения, где R4, R9, R12 и R13 представляют собой атом водорода, R5 представляет собой атом водорода, метил или этил, a R6 представляет собой атом водорода, метил. Енольные сложные и простые эфиры настоящего изобретения не являются енольными кислотами, которыми являются исходные соединения, и обладают способностью в меньшей степени раздражать желудок в сравнении .с вышеуказанными исходными соединениями. Понятие "пролекарство" относится к соединениям, которые являются предшественниками лекарства, которые в свою очередь после применения и абсорбции высвобождают лекарство in vivo в результате метаболизма. Хотя все обычные способы введения могут быть использованы для соединений настоящего изобретения, предпочтительным способом является оральный. После абсорбции в желудочнокишечном тракте соединения настоящего изобретения гидролизуются in vivo до соответствующих соединений формулы I, где заместитель R представляет собой атом водорода, или до их солей. Так как пролекарства настоящего изобретения не являются енольными кислотами, то воздействие на желудочно-кишечный тракт кислых исходных соединений сводится до минимума. Кроме того, поскольку желудочно-кишечные осложнения считаются основной отрицательной реакцией на кислотные нестероидные противовоспалительные лекарства /см, например, Del Favero в книге "Side Effects of Drugs Annual 7", Dukes and Elus, Eds. Excerpta Medica, Amsterdam, 1983, p. 104-115/, заявляемые соединения формулы I, вероятно, обладают отчетливым преимуществом по сравнению с исходными енольными соединениями. 3-Ацил-2-оксиндол-1-карбоксамиды, превращаемые в соединения формулы I, могут иметь расположение заместителей при экзоциклической двойной связи в положении 3, соответствующее син-, анти-конфигурации, или могут представлять собой смесь изомеров. Следовательно, они представляют собой соединения формул Все формы этих изомеров рассматриваются, как часть настоящего изобретения. 3-Ацил-2-оксиндол-1-карбоксамиды, которые используются в качестве исходного продукта, могут быть получены по методикам, известным в данной области, описанным, например, в пат. США 3634453 и 4556672. Другие исходные реагенты, указанные выше, являются коммерчески доступными или могут быть получены по известным методикам или по методикам, описанным в экспериментальной части данной работы. Соединения настоящего изобретения могут быть легко получены. Соль соответствующего 3-ацил-2-оксиндол-1-карбоксамида получают в среде инертного растворителя и используют без выделения или после выделения в следующей реакции с хлорангидридом кислоты или α-галогеналкиловым сложным эфиром. Условия этих реакций не являются критическими; температура может изменяться приблизительно от 0 до 50°С, причем предпочтительным температурным интервалом является интервал приблизительно от 0 до 20°С. Время реакции будет изменяться в зависимости от выбранных реагентов и температуры реакции, но предпочтительное время составляет приблизительно от 8 до 90 часов, причем более предпочтительное время составляет приблизительно 20 часов. Соль 3-ацил-2-оксиндол-1-карбоксамида может представлять собой соль щелочного металла, третичного амина или четвертичную аммонийную соль. Примерами щелочных металлов являются литий, натрий и калий. Третичные амины обычно представляют собой низкомолекулярные алифатические амины, такие как триметиламин, триэтиламин, трибутиламин, и смешанные амины, такие как диизопропилэтиламин, диэтиламинопиридин; а также гетероциклические амины, такие как пиридин-N-метилморфолин. Четвертичные аммонийные соединения могут быть симметричными или смешанными алкиламинами с линейными или разветвленными цепочками. Предпочтительными солями являются натриевые, диизопропилэтиламинные, триэтиламинные и тетрабутиламмониевые соли. Галогенангидриды кислот могут представлять собой хлорангидриды или бромангидриды; предпочтительными являются хлорангидриды. В качестве α-галогензамещенных сложных эфиров могут использоваться хлор-, бром- или иод-замещенные эфиры, причем предпочтительными являются хлор- и иод-замещенные. Хлорзамещенный сложный эфир предпочтительно используется с иодидом натрия для образования in situ иодзамещенного сложного эфира. 4 41348 Биологическая активность пролекарств настоящего изобретения измеряется его конверсией в исходное соединение in vivo или его биодоступностью, и определяется в сравнении с исходным соединением. Например, 3-[гидрокси-2 (тиенил)метилен]-6хлор-5-фтор-2,3-дигидро-2-оксо-1Н-индол-1-карбоксамид и выбранные пролекарства вводят орально некормленным самцам крыс Sprague-Dawley в дозах 3 мг-экв. 3-[гидрокси-2 (тиенил)метилен]-6хлор-5-фтор-2,3-дигидро-2-оксо-1Н-индол-1-карбоксамид/кг в виде раствора, или суспензии в 0,1%-ной метилцеллюлозе. Дозируемые объемы каждой лекарственной рецептуры сохраняются на уровне 1 мл на 1 кг веса тела. После орального применения отбирают образцы крови путем кровопускания через ретроглазничную пазуху в гепаринизированные пробирки через 1, 3 и 6 часов после введения дозы и сразу же охлаждают. До проведения анализа плазму хранят при -20°С. Концентрацию 3-[гидрокси-2 (тиенил)метилен]6-хлор-5-фтор-2,3-дигидро-2-оксо-1Н-индол-1карбоксамида в плазме после введения 3[гидрокси-2 (тиенил)метилен]-6-хлор-5-фтор-2,3дигидро-2-оксо-1Н-индол-1-карбоксамида и пролекарства определяют с помощью высокоэффективной жидкостной хроматографии с ультрафиолетовым детектором при 360 нм. Нижний предел количественного определения 3-[гидрокси-2 (тиенил)метилен]-6-хлор-5-фтор-2,3-дигидро-2-оксо1Н-индол-1-карбоксамида составляет 0,2 мкг/мл. Площадь под кривой концентрация-время [AUC(0-6 ч)] определяют линейным трапецоидным методом для 3-[гидрокси-2 (тиенил)метилен]-6хлор-5-фтор-2,3-дигидро-2-оксо-1Н-индол-1-карбоксамида после введения 3-[гидрокси-2 (тиенил)метилен]-6-хлор-5-фтор-2,3-дигидро-2-оксо1Н-индол-1-карбоксамида и каждого пролекарства. Относительная биоактивность 3-[гидрокси-2 (тиенил)метилен]-6-хлор-5-фтор-2,3-дигидро-2оксо-1Н-индол-1-карбоксамида после введения каждого пролекарства оценивается путем определения отношения значения площади [AUC(0-6 ч)] 3-[гидрокси-2(тиенил)метилен]-6-хлор-5-фтор-2,3дигидро-2-оксо-1Н-индол-1-карбоксамида после введения пролекарства к значению площади [АUC(0-6 ч)] 3-[гидрокси-2-(тиенил)метилен-6хлор-5-фтор-2,3-дигидро-2-оксо-1Н-индол-1карбоксамида после введения 3-[гидрокси2(тиенил)метилен-6-хлор-5-фтор-2,3-дигидро-2оксо-1Н-индол-1-карбоксамида. Данные по "биодоступности" для предложенных соединений приведены ниже. Соединение примера 12 24 30 31 35 36 39 43 44 Пролекарства формулы (I) оценивались на противовоспалительную и обезболивающую активность по известным методикам, таким как тест на пищевой отек у крыс, тест на вызываемый адъювантами артрит у крыс или тест на вызванные фенилбензохиноном болевые симптомы у мышей, которые ранее использовались для оценки исходных соединений и которые описаны в приведенных выше справочных работах и в других литературных источниках; см., например, С.A. Winter, "Progress in Drug Research", ed. E. Jucker, Birkhauser Verlag, Basel, Vol. 10, стр. 139-192 (1966). Ниже описываются испытания по трем исходным оксиндол карбоксамидам и одному пролекарству, в отношении данных по противовоспалительной активности in vivo. O OH O O S F Cl N H2N O O CP-144,477 S F OH Cl N H2N O O СР-72,133 S Cl OH Биодоступность % 95 53 90 143 58 86 62 80 100 N H2N O O Тенидап CP-144.477 представляет собой Е-1карбоксамидо-3-[3-карбокси-Е-пропеноилокси-(2тиенил)метилен]-6-хлор-2,3-дигидро-5-фтор-2 5 41348 оксо-1Н-индол в виде твердого желтого кристаллического вещества при комнатной температуре, имеющего молекулярный вес 436,8. Тенидап является прототипом структурно нового класса противовоспалительных средств - оксиндолов, имеющих биологические характеристики, отличные от характеристик классических нестероидных противовоспалительных лекарственных средств. Так же как и нестероидные противовоспалительные лекарственные средства, тенидап обладает способностью ингибировать доступ СО при метаболизме арахидоновой кислоты и, следовательно, in vivo противовоспалительными/обезболивающими свойствами. Однако тенидап обладает несколькими дополнительными видами активности, которыми не обладает класс нестероидных противовоспалительных лекарственных средств. Тенидап подтвердил свою клиническую активность при лечении как ревматоидного артрита (RA), так и остеоартрита (ОА). Промежуточный анализ данных сравнительных испытаний с напроксеном позволяет предположить, что эффективность тенидапа может превысить активность напроксена после длительного приема (в течение месяцев), особенно в случаях с ревматоидным артритом. Кроме того, тенидап (а не напроксен) заметно снижает уровень сыворотки острой фазы белков CRP (С-реактивных) и SAA у пациентов с ревматоидным артритом после нескольких недель терапии. В настоящее время принято считать, что уровень сыворотки CRP связан с тяжестью ревматоидного артрита и длительностью этого заболевания. Такое свойство не присуще нестероидным противовоспалительным лекарственным средствам, в то время как было установлено, что стероиды и золото снижают уровень CRP в такой же степени, как и тенидап. Результаты лабораторных исследований, которые бы конкретно подтверждали свойство тенидапа снижать CRP у пациентов с ревматоидным артритом, пока отсутствуют. Фармакокинетика СР-144.477 на крысах, собаках и обезьянах Сравнительная биодоступность СР-72.133 после перорального введения СР-144.477 по сравнению с биодоступностью после перорального введения самого СР-72.133, составила 111%, 62% и 80% у крыс, собак и обезьян, соответственно. Концентрация СР-144.477 в крови после перорального введения не подлежала определению у всех видов. Отсутствие систематического воздействия СР-144.477 было неудивительным, поскольку это соединение быстро гидролизовалось in vitro до СР-72.133 в кишечных гомогенатах обезьян и в крысиной, собачьей, обезьяньей и человеческой плазме. Испытания in vitro также показали, что СР-144.477 сохранял стабильность в желудочном соке крыс и обезьян. Все эти данные позволяют предположить, что СР-144.477 сохраняет стабильность в верхней части желудочно-кишечного тракта, но быстро гидролизуется во время и сразу же после пероральной абсорбции. А. Фармакокинетика СР-72.133 после перорального введения СР-144.477 Фармакокинетика СР-72.133 сравнивалась после перорального введения пролекарства СР-144.477 или СР-72.133 крысам, собакам и обе зьянам. Концентрация в плазме СР-144.477 и СР-72.133 определялась с использованием жидкостной хроматографии высокого разрешения с ультрафиолетовым определением. Очевидное время полужизни СР-72.133 было таким же после перорального введения СР-144.477 или СР-72.133 крысам и обезьянам; время полужизни СР-72.133 у собак после перорального введения СР-144.477 по существу больше, чем после введения СР-72.133, вероятно, благодаря пролонгированной абсорбции пролекарства. Эти испытания также позволили определить относительную биодоступность СР-72.133 после введения СР-144.477 посредством определения отношения AUC СР-72.133 после введения пролекарства или исходного лекарства. После перорального введения СР-144.477 в дозах, равных 3 мг/кг СР-72.133, относительная биодоступность СР-72.133 у крыс, собак и обезьян составила 111%, 62% и 80%, соответственно. Важно отметить, что содержание в крови общего количества СР-144.477 было ниже порога количественного определения (
ДивитисяДодаткова інформація
Назва патенту англійськоюProdrugs of 3-acyl-2-oxindol-1-carboxamides and a pharmaceutical composition
Автори англійськоюBARTH WAYNE E, COOPER KELVIN, KLEINMAN EDWARD F, REITER LAWRENCE A, ROBINSON RALPH P
Назва патенту російськоюПролекарства 3-ацил-2-оксиндол-1-карбоксамидов и фармацевтическая композиция
Автори російськоюБарт Вейн Э., Купер Келвин, Клейнман Эдвард Ф., Рейтер Лоуренс А., Робинсон Ральф П.
МПК / Мітки
МПК: A61K 31/40, A61K 31/55, C07F 7/18, C07D 409/14, A61K 31/445, A61K 31/465, A61P 29/00, C07D 409/06, A61K 31/4433, A61P 25/04, A61P 43/00, A61K 31/535
Мітки: 3-ацил-2-оксіндол-1-карбоксамідів, фармацевтична, проліки, композиція
Код посилання
<a href="https://ua.patents.su/30-41348-proliki-3-acil-2-oksindol-1-karboksamidiv-ta-farmacevtichna-kompoziciya.html" target="_blank" rel="follow" title="База патентів України">Проліки 3-ацил-2-оксіндол-1-карбоксамідів та фармацевтична композиція</a>
Попередній патент: Спектрометр випромінювань людини
Наступний патент: Спосіб одержання карбаміду
Випадковий патент: Штамп для штампування виробів з площинних заготівок