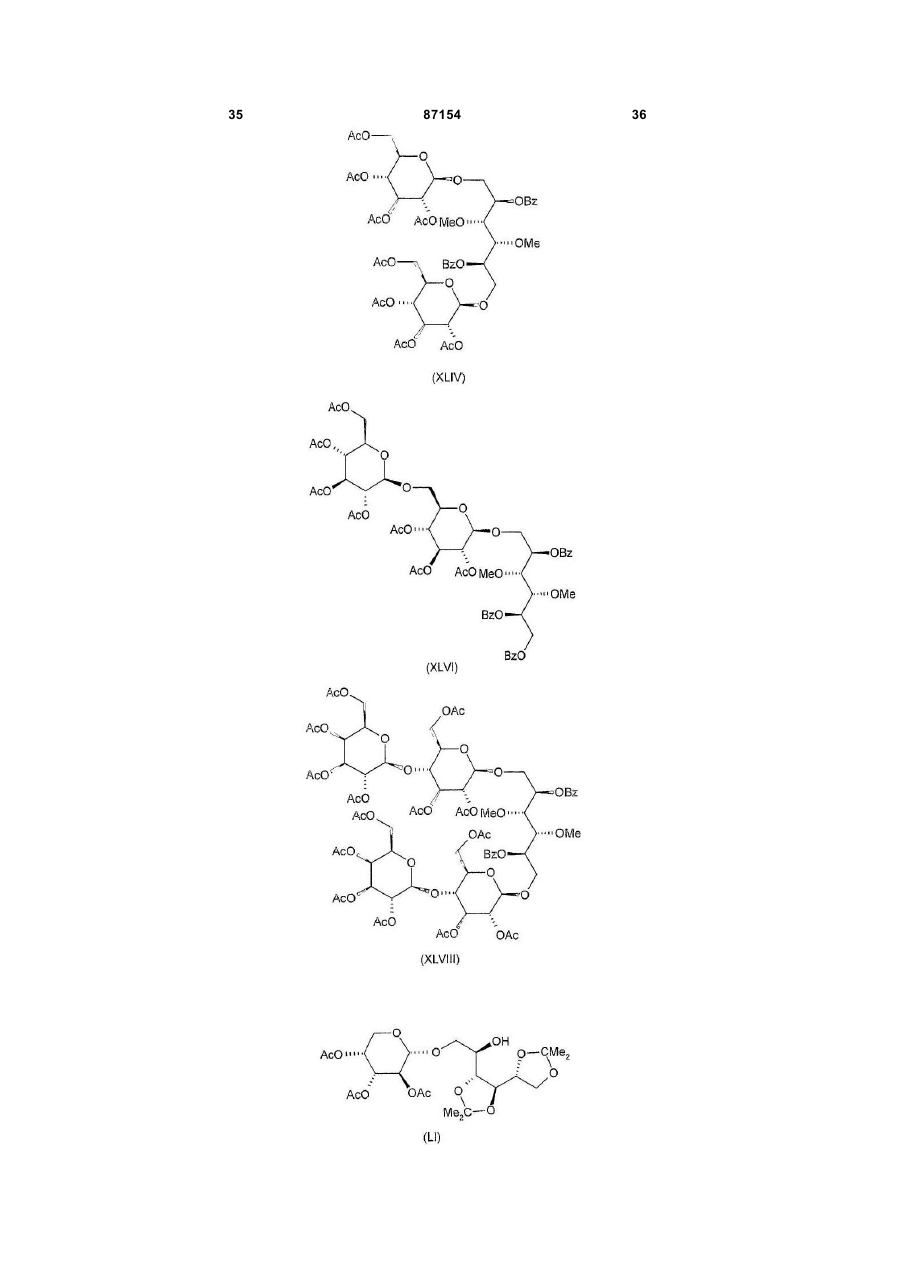
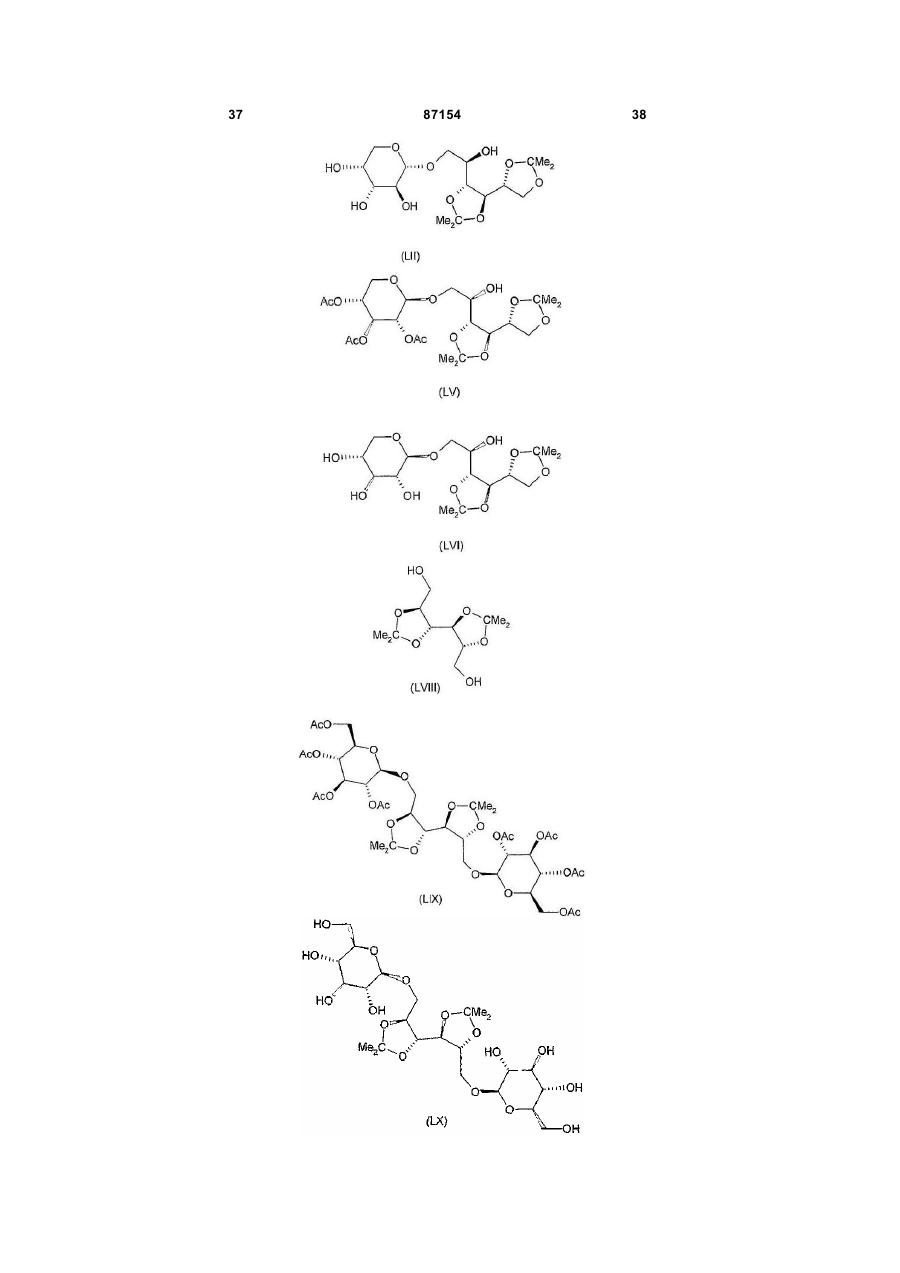
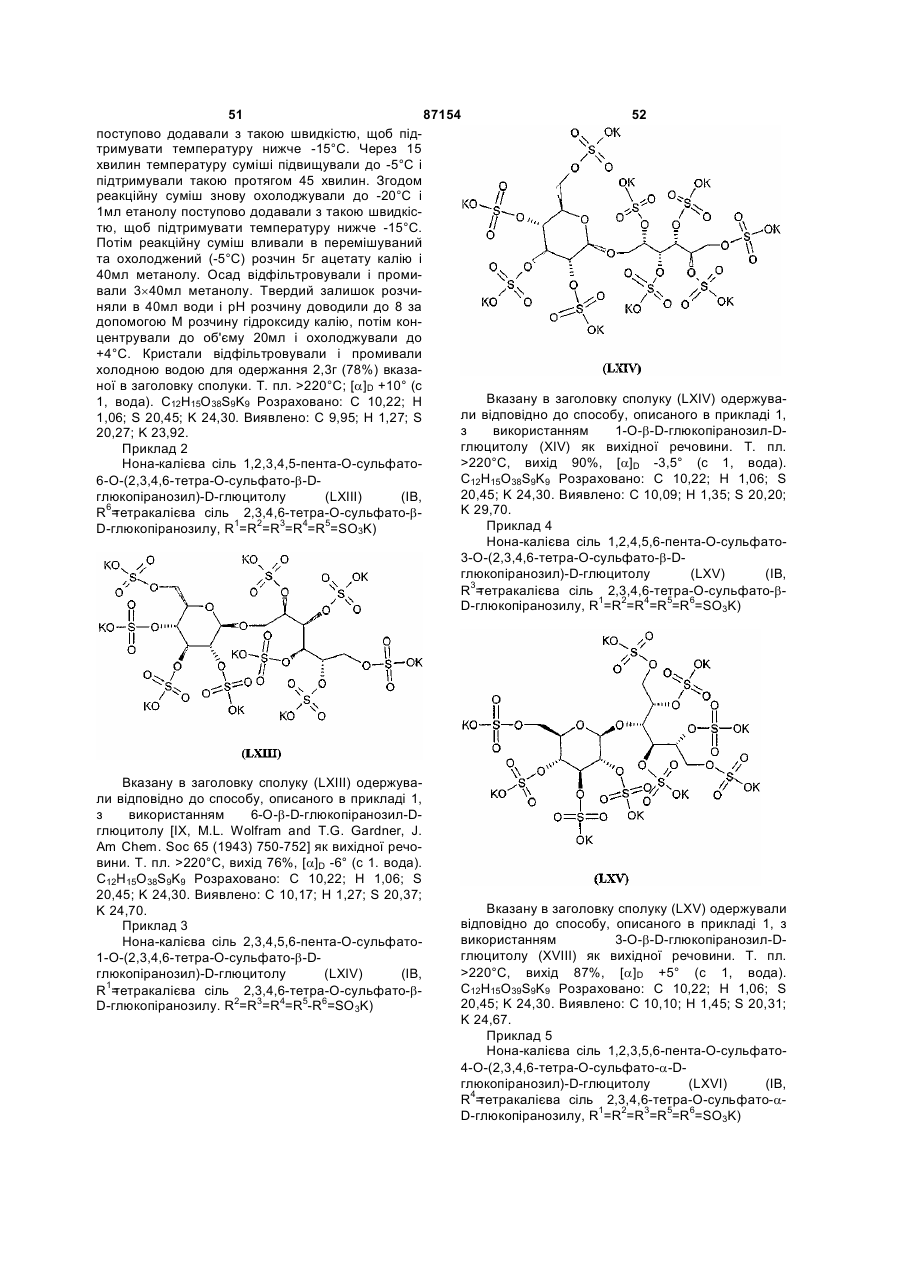
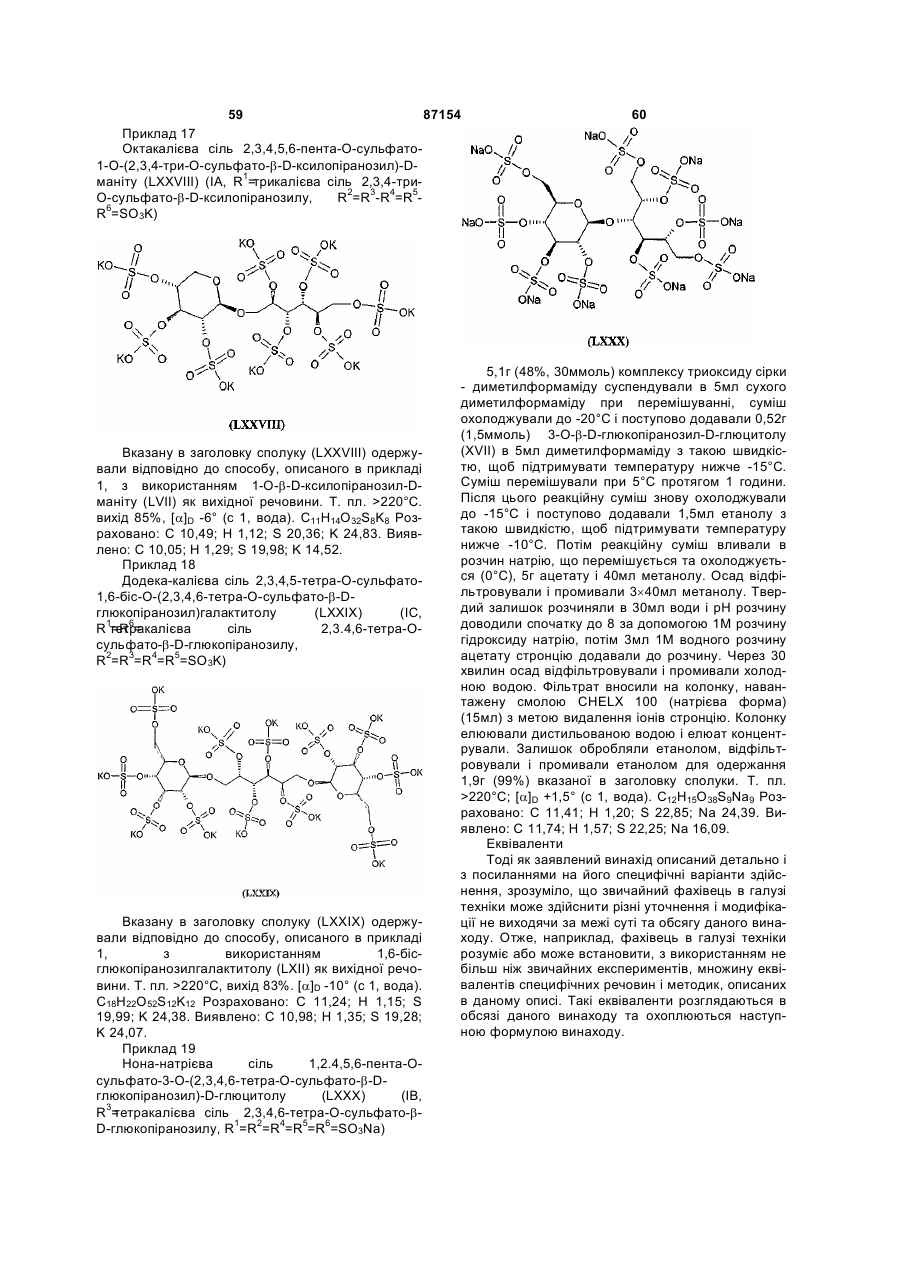
Полісульфатовані глікозиди та їх солі
Номер патенту: 87154
Опубліковано: 25.06.2009
Автори: Меддьєш Габор, Бодор Ніколас, Кусманн Янош, Куруц Іштван
Формула / Реферат
1. Сполука формули (І)
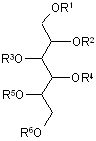 , (I)
, (I)
де R1, R2, R3, R4, R5 та R6 незалежно один від одного означають С1-4алкіл, -SO3H, полісульфатовану β-глікозильну або полісульфатовану диглікозильну групу, за умови, що щонайменше один з R1-R6 являє собою полісульфатовану β-глікозильну або полісульфатовану диглікозильну групу, або її фармацевтично прийнятна сіль.
2. Сполука або сіль за п. 1, де R1 означає полісульфатовану β-глікозильну або полісульфатовану диглікозильну групу, a R2-R6 являють собою -SO3H групи.
3. Сполука або сіль за п. 1, де R1, R2, R4, R5 та R6 означають -SO3H групи, a R3 являє собою полісульфатовану β-глікозильну або поліфосфатовану диглікозильну групу.
4. Сполука або сіль за п. 1 де R1 та R3 означають полісульфатовані β-глікозильні або полісульфатовані диглікозильні групи, a R2, R4, R5 та R6 являють собою -SO3H групи.
5. Сполука або сіль за п. 1 де R1 та R6 означають полісульфатовані β-глікозильні або полісульфатовані диглікозильні групи, a R2, R3, R4 та R5 являють собою -SO3H групи.
6. Сполука або сіль за п. 1, де R1 означає полісульфатовану β-глікозильну або полісульфатовану диглікозильну групу, R3 та R4 являють собою С1-4алкільні групи, a R2, R5 та R6 є -SO3H групами.
7. Сполука або сіль за п. 1, де R1 та R6 означають полісульфатовані β-глікозильні або полісульфатовані диглікозильні групи, R3 та R4 являють собою С1-4алкільні групи, a R2 та R5 є -SO3H групами.
8. Сполука за п. 1, вибрана з групи, яка складається з:
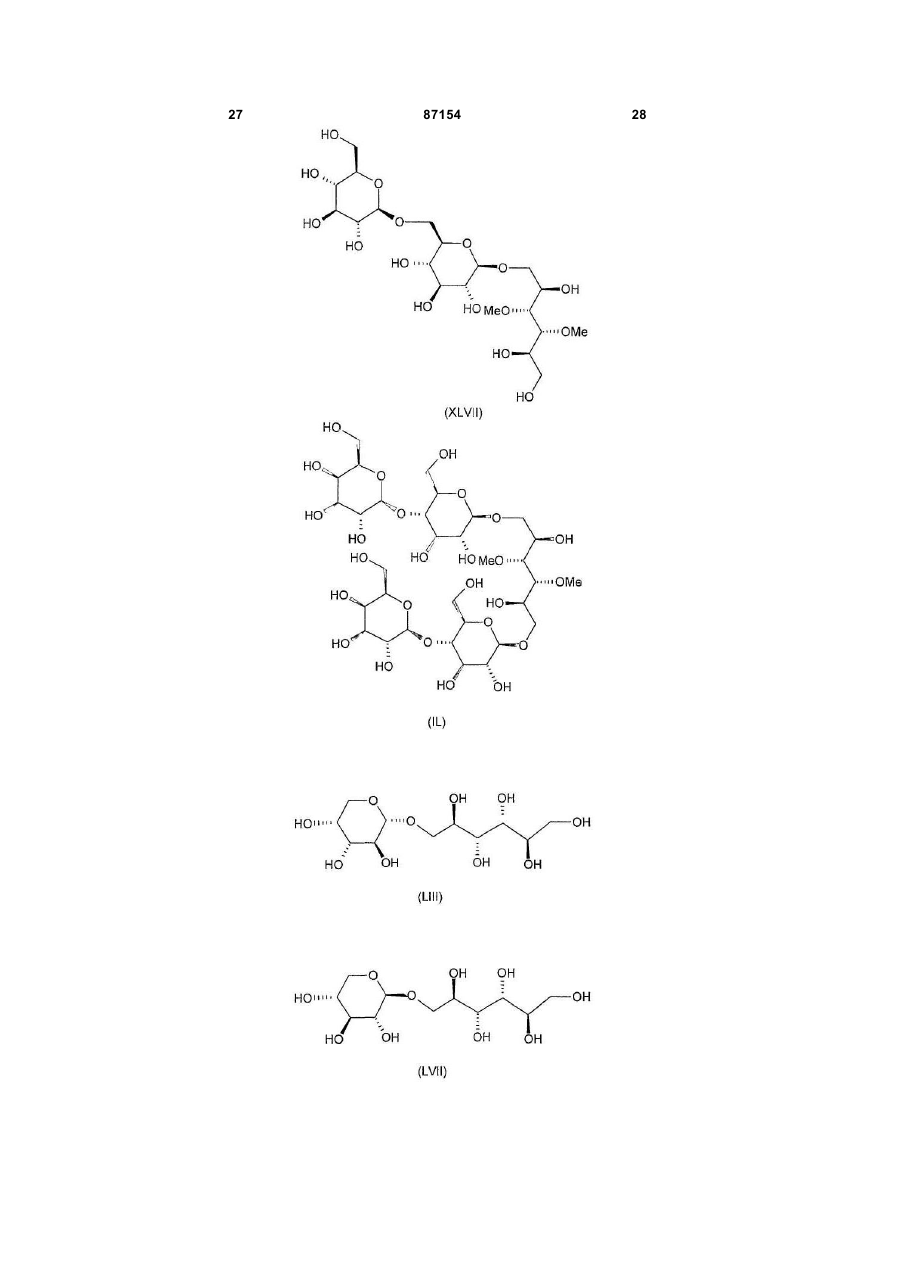
2,3,4,5,6-пента-О-сульфато-1-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-D-маніту,
1,2,3,4,5-пента-О-сульфато-6-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-D-глюцитолу,
2,3,4,5,6-пента-О-сульфато-1-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-D-глюцитолу,
1,2,4,5,6-пента-О-сульфато-3-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-D-глюцитолу,
1,2,3,5,6-пента-О-сульфато-4-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-D-глюцитолу,
1,2,3,5,6-пента-О-сульфато-4-О-(2,3,4,6-тетра-О-сульфато-β-D-галактопіранозил)-D-глюцитолу,
2,4,5,6-тетра-О-сульфато-1,3-біс-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-D-глюцитолу,
2,3,4,5-тетра-О-сульфато-1,6-біс-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-D-маніту,
2,3,4,5-тетра-О-сульфато-1,6-біс-О-(2,3,4,2',3',4',6'-гепта-О-сульфато-β-гентіобіопіранозил)-D-маніту,
2,3,4,5,6-пента-О-сульфато-1-О-(2,3,4,2',3',4',6'-гепта-О-сульфато-β-гентіобіопіранозил)-D-маніту,
3,4-ди-О-метил-2,5,6-три-О-сульфато-1-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-D-маніту,
3,4-ди-О-метил-2,5-ди-О-сульфато-1,6-біс-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-D-маніту,
3,4-ди-О-метил-2,5,6-три-О-сульфато-1-О-(2,3,4,2',3',4',6'-гепта-О-сульфато-β-гентіобіопіранозил)-D-маніту,
3,4-ди-О-метил-2,5-ди-О-сульфато-1,6-біс-О-(2,3,6,2',3',4',6'-гепта-О-сульфато-β-лактозил)-D-маніту,
2,3,4,5,6-пента-O-сульфато-1-О-(2,3,4-три-O-сульфато-β-D-ксилопіранозил)-D-маніту,
2,4,5,6-тетра-О-сульфато-1,6-біс-О-(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)галактитолу
або фармацевтично прийнятної солі будь-якої з цих сполук.
9. Фармацевтична композиція, яка містить сполуку за п. 1 і фармацевтично прийнятний носій.
10. Застосування сполуки за п. 1 при одержанні лікарського засобу для лікування гострого або хронічного запального захворювання дихальних шляхів у ссавця.
11. Застосування за п. 10, де запальне захворювання дихальних шляхів являє собою алергічне запальне захворювання дихальних шляхів.
12. Застосування за п. 10, де запальне захворювання дихальних шляхів вибирають з групи, яка складається з астми, алергічного риніту, вродженої або набутої бронхіальної астми, гострого або хронічного бронхіту, хронічних обструктивних захворювань легенів і пневмосклерозу.
13. Застосування за п. 10, де вказаний лікарський засіб вводиться у вигляді однієї або декількох доз.
14. Застосування за п. 11, де алергічне запальне захворювання вибране з групи, що складається з ідіопатичного пневмосклерозу і аутоімунних захворювань легень.
15. Сполука або сіль за п. 1, в якій полісульфатована β-глікозильна або полісульфатована диглікозильна група являють собою полісульфатовану β-D-глікозильну або полісульфатовану β-D-диглікозильну групу.
16. Сполука або сіль за п. 15, де полісульфатована β-D-глікозильна або полісульфатована β-D-диглікозильна групи являють собою полісульфатовану β-D-глікопентапіранозильну групу, полісульфатовану β-D-глікогексапіранозильну групу, полісульфатовану β-D-диглікопентапіранозильну групу або полісульфатовану β-D-диглікогексапіранозильну групу.
17. Сполука або сіль за п. 3, де R3 означає полісульфатовану β-глікозильну групу, тa R1, R2, R4, R5 і R6 є -SO3H групами.
18. Сполука за п. 17, де полісульфатована β-глікозильна група являє собою полісульфатовану β-D-глікозильну групу.
19. Сполука за п. 18, де полісульфатована β-D-глікозильна група являє собою полісульфатовану β-D-глікопентапіранозильну групу або полісульфатовану β-D-глікогексапіранозильну групу.
20. Сполука за п. 1 у формі калієвої солі.
21. Сполука за п. 8 у формі калієвої солі.
22. Сполука за п. 17 у формі калієвої солі.
23. Сполука за п. 22, де полісульфатована β-глікозильна група являє собою полісульфатовану β-D-глікозильну групу.
24. Сполука за п. 23, де полісульфатована β-D-глікозильна група являє собою полісульфатовану β-D-глікопентапіранозильну групу або полісульфатовану β-D-глікогексапіранозильну групу.
25. Сполука за п. 24, яка являє собою нонакалієву сіль 1,2,3,5,6-пента-О-сульфато-4-О-(2,3,4,6-тетра-О-сульфато-β-D-глікопіранозил)-D-глюцитолу.
26. Сполука за п. 25 у кристалічній формі.
27. Сполука за п. 24, яка являє собою нонакалієву сіль 1,2,3,5,6-пента-О-сульфато-4-О-(2,3,4,6-тетра-O-сульфато-β-D-галактопіранозил)-D-глюцитолу.
28. Сполука за п. 27 у кристалічній формі.
29. Застосування сполуки формули (І)
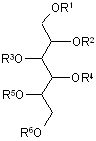 , (I)
, (I)
де R1, R2, R3, R4, R5 і R6 незалежно один від одного означають С1-4алкіл, -SO3H, полісульфатовану β-глікозильну або полісульфатовану диглікозильну групу, за умови, що щонайменше один з R1-R6 являє собою полісульфатовану β-глікозильну або полісульфатовану диглікозильну групу, або її фармацевтично прийнятної солі, при одержанні лікарського засобу для лікування гострих або хронічних запальних захворювань дихальних шляхів у ссавців.
30. Застосування за п. 29, де фармацевтично прийнятна сіль сполуки формули (І) являє собою натрієву сіль.
31. Застосування за п. 29, де запальне захворювання дихальних шляхів вибирають із групи, що складається з астми, алергічного риніту, вродженої або набутої бронхіальної астми, гострого або хронічного бронхіту, хронічних обструктивних захворювань легень і пневмосклерозу.
32. Застосування за п. 29, де запальне захворювання дихальних шляхів являє собою алергічне запальне захворювання дихальних шляхів.
33. Застосування за п. 32, де алергічне запальне захворювання дихальних шляхів вибране з групи, що складається з ідіопатичного пневмосклерозу і аутоімунного захворювання легень.
34. Застосування за п. 29, де вказаний лікарський засіб вводиться у вигляді однієї або декількох доз.
35. Фармацевтична композиція, яка містить сполуку за п. 8 і фармацевтично прийнятний носій.
36. Фармацевтична композиція, яка містить сполуку за п. 26 і фармацевтично прийнятний носій.
37. Фармацевтична композиція, яка містить сполуку за п. 28 і фармацевтично прийнятний носій.
Текст
1. Сполука формули (І) 2 3 87154 4 2,3,4,5,6-пента-О-сульфато-1-О-(2,3,4,6-тетра-Огрупу або полісульфатовану β-Dсульфато-β-D-глюкопіранозил)-D-глюцитолу, диглікогексапіранозильну групу. 1,2,4,5,6-пента-О-сульфато-3-О-(2,3,4,6-тетра-О17. Сполука або сіль за п. 3, де R3 означає полісусульфато-β-D-глюкопіранозил)-D-глюцитолу, льфатовану β-глікозильну групу, тa R1, R2, R4, R5 і 1,2,3,5,6-пента-О-сульфато-4-О-(2,3,4,6-тетра-ОR6 є -SO3H групами. сульфато-β-D-глюкопіранозил)-D-глюцитолу, 18. Сполука за п. 17, де полісульфатована β1,2,3,5,6-пента-О-сульфато-4-О-(2,3,4,6-тетра-Оглікозильна група являє собою полісульфатовану сульфато-β-D-галактопіранозил)-D-глюцитолу, β-D-глікозильну групу. 2,4,5,6-тетра-О-сульфато-1,3-біс-О-(2,3,4,6-тетра19. Сполука за п. 18, де полісульфатована β-DО-сульфато-β-D-глюкопіранозил)-D-глюцитолу, глікозильна група являє собою полісульфатовану 2,3,4,5-тетра-О-сульфато-1,6-біс-О-(2,3,4,6-тетраβ-D-глікопентапіранозильну групу або полісульфаО-сульфато-β-D-глюкопіранозил)-D-маніту, товану β-D-глікогексапіранозильну групу. 2,3,4,5-тетра-О-сульфато-1,6-біс-О-(2,3,4,2',3',4',6'20. Сполука за п. 1 у формі калієвої солі. гепта-О-сульфато-β-гентіобіопіранозил)-D-маніту, 21. Сполука за п. 8 у формі калієвої солі. 2,3,4,5,6-пента-О-сульфато-1-О-(2,3,4,2',3',4',6'22. Сполука за п. 17 у формі калієвої солі. гепта-О-сульфато-β-гентіобіопіранозил)-D-маніту, 23. Сполука за п. 22, де полісульфатована β3,4-ди-О-метил-2,5,6-три-О-сульфато-1-О-(2,3,4,6глікозильна група являє собою полісульфатовану тетра-О-сульфато-β-D-глюкопіранозил)-D-маніту, β-D-глікозильну групу. 3,4-ди-О-метил-2,5-ди-О-сульфато-1,6-біс-О24. Сполука за п. 23, де полісульфатована β-D(2,3,4,6-тетра-О-сульфато-β-D-глюкопіранозил)-Dглікозильна група являє собою полісульфатовану маніту, β-D-глікопентапіранозильну групу або полісульфа3,4-ди-О-метил-2,5,6-три-О-сульфато-1-Отовану β-D-глікогексапіранозильну групу. (2,3,4,2',3',4',6'-гепта-О-сульфато-β25. Сполука за п. 24, яка являє собою нонакалієву гентіобіопіранозил)-D-маніту, сіль 1,2,3,5,6-пента-О-сульфато-4-О-(2,3,4,6-тетра3,4-ди-О-метил-2,5-ди-О-сульфато-1,6-біс-ОО-сульфато-β-D-глікопіранозил)-D-глюцитолу. (2,3,6,2',3',4',6'-гепта-О-сульфато-β-лактозил)-D26. Сполука за п. 25 у кристалічній формі. маніту, 27. Сполука за п. 24, яка являє собою нонакалієву 2,3,4,5,6-пента-O-сульфато-1-О-(2,3,4-три-Oсіль 1,2,3,5,6-пента-О-сульфато-4-О-(2,3,4,6-тетрасульфато-β-D-ксилопіранозил)-D-маніту, O-сульфато-β-D-галактопіранозил)-D-глюцитолу. 2,4,5,6-тетра-О-сульфато-1,6-біс-О-(2,3,4,6-тетра28. Сполука за п. 27 у кристалічній формі. О-сульфато-β-D-глюкопіранозил)галактитолу 29. Застосування сполуки формули (І) OR1 або фармацевтично прийнятної солі будь-якої з цих сполук. 9. Фармацевтична композиція, яка містить сполуку OR2 за п. 1 і фармацевтично прийнятний носій. R3O 10. Застосування сполуки за п. 1 при одержанні (I) лікарського засобу для лікування гострого або OR4 хронічного запального захворювання дихальних 5O R шляхів у ссавця. 11. Застосування за п. 10, де запальне захворювання дихальних шляхів являє собою алергічне R6O , запальне захворювання дихальних шляхів. де R1, R2, R3, R4, R5 і R6 незалежно один від одного 12. Застосування за п. 10, де запальне захворюозначають С1-4алкіл, -SO3H, полісульфатовану βвання дихальних шляхів вибирають з групи, яка глікозильну або полісульфатовану диглікозильну складається з астми, алергічного риніту, вроджегрупу, за умови, що щонайменше один з R1-R6 явної або набутої бронхіальної астми, гострого або ляє собою полісульфатовану β-глікозильну або хронічного бронхіту, хронічних обструктивних заполісульфатовану диглікозильну групу, або її фахворювань легенів і пневмосклерозу. рмацевтично прийнятної солі, при одержанні лі13. Застосування за п. 10, де вказаний лікарський карського засобу для лікування гострих або хронізасіб вводиться у вигляді однієї або декількох доз. чних запальних захворювань дихальних шляхів у 14. Застосування за п. 11, де алергічне запальне ссавців. захворювання вибране з групи, що складається з 30. Застосування за п. 29, де фармацевтично приідіопатичного пневмосклерозу і аутоімунних зайнятна сіль сполуки формули (І) являє собою нахворювань легень. трієву сіль. 15. Сполука або сіль за п. 1, в якій полісульфато31. Застосування за п. 29, де запальне захворювана β-глікозильна або полісульфатована дигліковання дихальних шляхів вибирають із групи, що зильна група являють собою полісульфатовану βскладається з астми, алергічного риніту, вроджеD-глікозильну або полісульфатовану β-Dної або набутої бронхіальної астми, гострого або диглікозильну групу. хронічного бронхіту, хронічних обструктивних за16. Сполука або сіль за п. 15, де полісульфатовахворювань легень і пневмосклерозу. на β-D-глікозильна або полісульфатована β-D32. Застосування за п. 29, де запальне захворюдиглікозильна групи являють собою полісульфавання дихальних шляхів являє собою алергічне товану β-D-глікопентапіранозильну групу, полісузапальне захворювання дихальних шляхів. льфатовану β-D-глікогексапіранозильну групу, по33. Застосування за п. 32, де алергічне запальне лісульфатовану β-D-диглікопентапіранозильну захворювання дихальних шляхів вибране з групи, 5 87154 6 що складається з ідіопатичного пневмосклерозу і 36. Фармацевтична композиція, яка містить сполуаутоімунного захворювання легень. ку за п. 26 і фармацевтично прийнятний носій. 34. Застосування за п. 29, де вказаний лікарський 37. Фармацевтична композиція, яка містить сполузасіб вводиться у вигляді однієї або декількох доз. ку за п. 28 і фармацевтично прийнятний носій. 35. Фармацевтична композиція, яка містить сполуку за п. 8 і фармацевтично прийнятний носій. Даний винахід стосується глікозидів, їх солей та фармацевтичних композицій, які містять такі глікозиди як активні інгредієнти. Більше того, винахід забезпечує спосіб профілактики, лікування або полегшення симптомів гострих або хронічних запальних розладів дихальних шляхів у ссавців включаючи астму та патології, пов'язані з астмою. Запалення являє собою багатоступінчастий каскадний процес, який може бути предметом потенційного терапевтичного втручання. Коротко, запалення викликає інфільтрацію імунологічно компетентних клітин (наприклад, еозинофілів, тучних клітин, активованих Т-лімфоцитів) в місці пошкодження, де вони, разом з резидентними клітинами, вивільняють біологічно активні медіаторні речовини (наприклад, гістамін, протеази, множину цитокінів та хемокінів), які збільшують проникність близьких кровоносних судин, залучають і стимулюють сусідні клітини. Змінена проникність судин призводить до утворення рідкого ексудату в місці пошкодження з подальшим припливом реактивних лейкоцитів та їх потенційним відтоком в пошкоджену ділянку. [Для опису дивіться, Trowbridge and Emling, Inflammation: A Review of the Process Quintessence Pub. Co., 1997]. Секреція колагену та слизу і проліферація резидентних клітин (гладком'язові та епітеліальні клітини або фібробласти, стимульовані вивільненими медіаторами) встановлюють ступінь того, наскільки виражені патологічні зміни (наприклад, обструкції дихальних шляхів) і беруть участь в їх розвитку. Запалення пов'язане з множиною легеневих станів, включаючи, наприклад, ендогенну або екзогенну бронхіальну астму, будь-яке запальне захворювання легенів, гострий або хронічний бронхіт, легеневі запальні реакції, вторинні по відношенню до хронічного бронхіту, хронічні обструктивні захворювання легенів, пневмосклероз, а також будь-які захворювання легенів, при яких можуть відігравати роль лейкоцити, включаючи, але не обмежуючись, ідіопатичний пневмосклероз та будь-які інші аутоімунні захворювання легенів. Астма є однією з найбільш частих форм легеневого запалення, що вражає великі та дрібні дихальні шляхи легенів. На неї страждає від 5% до 10% населення, що призводить до передбачуваних 27 мільйонів візитів пацієнтів, 6 мільйонів втрачених робочих днів, і 90,5 мільйонів днів обмеженої активності на рік. Ступінь захворюваності та смертності від астми збільшується у всьому світі [Plaut and Zimmerman, «Allergy and Mechanisms of Hypersensitivity» in Fundamental Immunology. 3rd Ed,, Paul (ed.), Raven Press, New York, NY, at 1399 (1993)]. Звичайне лікування від астми основане на чіткому уникненні всіх ініціюючих алергенів, чого по суті важко досягнути, і на терапевтичних схемах, основаних на фармакологічних агентах, які мають несприятливі побічні ефекти та субоптимальні фармакокінетичні властивості. b2-адренергічні агоністи, що використовуються для лікування бронхоспазму, не впливають ефективно на запалення дихальних шляхів або гіперреактивність бронхів [Palmer et al., New Engl. J. Med. 331:1314 (1994)]. Також, систематичне або тривале застосування b2-адренергічних агоністів пов'язане з недостатнім контролем астми, збільшенням гіперреактивності дихальних шляхів у відповідь на алерген, і зниженим захистом від бронхоконстрикції [Bhagat et al., Chest 108:1235 (1995)]. Більше того, вважається, що хронічне використання b2-адренергічних агентів окремо за допомогою приглушення b 2адренерпчних рецепторів, буде погіршувати гіперреактивність бронхів. Теофілін (протиастматичний метилксантин) характеризується істотною варіабельністю всмоктування і виведення. Кортикостероїди, хоча є відносно безпечними у дорослих пацієнтів, є токсичними для дітей, призводячи до приглушення надниркової залози і зниження кісткової щільності і росту [Woolock et al., am. Respir. Crit. Care Med. 153:1481 (1996)]. Кромолін, що використовується для запобігання астматичним епізодам, ефективний для запобігання астматичній реакції тільки при введенні перед впливом [Volcheck et al., Postgrad Med. 104(3): 127 (1998)]. Антигістамінні засоби періодично запобігають або зупиняють алергічні астматичні епізоди, особливо у дітей, але часто є тільки частково ефективними, оскільки гістамін є тільки однією з множини медіаторів, пов'язаних із запаленням [Cuss, «The Pharmacology of Antiasthma Medications», in Asthma as an Inflammatory Disease. O'Byrne, Ed., Dekker, Inc., New York, at 199 (1990)) and O'Byrne, «Airway Inflammation and Asthma», in Asthma as an Inflammatory Disease. O'Byrne, Ed., Dekker, Inc., New York, NY, 143 (1990)]. Отже, існуючі можливості лікарських засобів мають ряд недоліків. Загалом, звичайні агенти мають відносно невелику тривалість дії і можуть бути частково або повністю неефективними при введенні після виникнення антигенної стимуляції. Більше того, через серйозні побічні ефекти, пов'язані із застосуванням агентів, таких як b 2адренергічні агоністи та кортикостероїди, терапевтичні межі діапазону безпеки таких агентів є відносно вузькими, і за пацієнтами, що використовують такі агенти, необхідно ретельно спостерігати [дивіться, наприклад, WO 94/06783, WO 99/06025, патенти США №№ 5690910 та 5980865]. В останньому клінічному дослідженні інгаляційних кортикостероїдів у дітей 5-11 років виникало тільки тимчасове поліпшення функції дихальних шляхів з астмою після першого року лікування, із помітним зменшенням при використанні плацебо протягом 7 87154 8 подальших 3 років [The Childliood Asthma «ізомер» в даному описі включає всі такі сполуки Management Program Research Group, N. Engl. J. та їх варіанти в сполуці формули (І). Med., 343:1054 (2000)]. Таке зниження найкращим Значенням сульфатованої глікозильної групи чином може бути пояснене перебудовувальними може бути молекула пентопіранози або гексопіразмінами (характерною властивістю астми), вининози з конфігурацією за вибором, одна або більше каючими в дихальних шляхах, які є стійкими до гідроксильних груп якої присутні у вигляді Окортикостероїдів [Davies, Curr. Opin. Allergy Clin. сульфатного складного ефіру, і компонент цукру Immunol, 1:67(2001)]. прикріплений до аглікону його аномерним атомом З відповідної літератури відомо, що визначені вуглецю за допомогою a- або b-зв'язку. Несульфасуміші полісульфатованих дисахаридів - що мають тована глікозильна група містить всі гідроксильні структуру, тісно зв'язану з такою згідно з даним групи або їх захищені варіанти. Несульфатовані винаходом і які були синтезовані обробкою азотисполуки є застосовними як проміжні сполуки для стою кислотою таких природних продуктів, як, наодержання сульфатованих сполук, вказаних в даприклад, гепарин або сульфат гепарину, з поданому описі. льшим відновленням боргідридом і подальшим Значенням полісульфатованої диглікозильної сульфатуванням частково очищених зразків [US групи може бути молекула пентопіранози або гек5690910; US 5980865 та WO 02/083700] - виявляли сопіранози з конфігурацією за вибором, одна з протизапальний ефект на різних моделях астми. гідроксильних груп якої є глікозилірованою додатДаний винахід стосується нових глікозидів та ковою молекулою пентопіранози або гексапіранози способів одержання таких сполук і фармацевтичз конфігурацією за вибором, і всі гідроксильні груних композицій, які містять такі сполуки, з чітко пи утвореного таким чином дигликозильного комвизначеною хімічною структурою, які мають більш понента присутні у вигляді О-сульфатних складних сприятливі фармакологічні властивості і менше ефірів, а цукровий компонент прикріплений до небажаних побічних ефектів, ніж відомі протиастаглікону своїм аномерним атомом вуглецю за доматичні засоби. Винахід, крім того, стосується спопомогою a- або b-зв'язку. собів лікування пацієнтів, які потребують лікуванВсі можливі стереоізомери (арабіно-, ліксо-, ня, що включає введення нових глікозидів і рібо- та ксило-) включені в структуру пентоз, а такомпозицій вказаних глікозидів вказаним пацієнкож їх D- та L-енантіомерів. Подібним чином всі там. можливі стереоізомери (ало-, альтро-, галакто-, Відповідно до згаданих вище фактів винахід глюко-, гуло-, ідо-, мано- і тало-) включені в струкстосується нових полісульфатованих глікозидів туру гексоз, а також їх D- та L-енантіомерів. Термін формули (І), «ізомер» включає всі такі сполуки та їх варіанти в сполуку формули (І). Значенням С1-4 алкільної групи є групи метил, етил, н-пропіл, ізопропіл, н-бутил, ізобутил, вторбутил, трет-бутил переважно метильна група. Солі лужних металів і сполук за винаходом означають солі Na, К або Li, тоді як солі лужноземельних металів переважно являють собою солі Mg та Са. Такі сполуки формули (І), а також їх солі лужних металів та лужноземельних металів, де значенням R1 є полісульфатована глікозильна або диглікозильна група, а значенням R2-R6 є -SO3H, являють собою переважну групу сполук за винаходом. де R1, R2, R3, R4, R5 та R6 незалежно один від Такі сполуки формули (І), а також їх солі лужодного означають -Н, С1-4 алкіл, -SO3H, сульфатоних металів та лужноземельних металів, де знавану або несульфатовану глікозильну або сульфаченням R1, R2, R4, R3 та R6 є -SO3H, а значенням товану або несульфатовану диглікозильну групу, R3 є полісульфатована глікозильна або диглікозиза умови, що щонайменше один з R1-R6 являє сольна група, являють собою додаткову переважну бою сульфатовану або несульфатовану глікозильгрупу сполук за винаходом. ну або сульфатовану або несульфатовану дигліТакі сполуки формули (І), а також їх солі лужкозильну групу - а також їх можливі ізомери і них металів і лужноземельних металів, де значенфармацевтично прийнятні солі. Термін «фармаценям R1, R2, R3, R5 та R6 є -SO3H, а значенням R4 є втично прийнятні солі» включає, наприклад, солі полісульфатована глікозильна або диглікозильна лужних металів і солі лужноземельних металів та група, являють собою додаткову переважну групу будь-які інші фармацевтично прийнятні протиіона сполук за винаходом. або протиіонів, зв'язаних з однією або більше суТакі сполуки формули (І), а також їх солі лужльфатними групами в молекулі. них металів та лужноземельних металів, де знаОскільки всі чотири вторинних атоми вуглецю ченням R1 та R3 є полісульфатована глікозильна цукрового спирту являють собою хіральні центри, група, а значенням R2, R4, R5 та R6 є -SO3H, являочевидно, всі можливі стереоізомери (аліт, галакють собою іншу переважну групу сполук за винатит, ідит. маніт, глюцит і таліт), а також їх D- та Lходом. енантіомери охоплюються формулою (І). Термін Такі сполуки формули (І), а також їх солі лужних металів та лужноземельних металів, де зна 9 87154 10 гексадека-калієва сіль 3,4-ди-O-метил-2,5-диченням R1 та R6 є полісульфатована глікозильна O-сульфато-1,6-біс-О-(2,3,6,2',3',4',6'-гепта-Оабо диглікозильна група, а значенням R2, R3, R4 та R5 є -SO3H, являють собою іншу переважну групу сульфато-b-лактозил)-D-маніту, сполук за винаходом. окта-калiєва сіль 2,3,4,5,6-пента-О-сульфатоТакі сполуки формули (І), а також їх солі луж1-О-(2,3,4-три-О-сульфато-a-D-арабінопіранозил)них металів та лужноземельних металів, де знаD-маніту, ченням R1 є полісульфатована глікозильна або окта-калієва сіль 2,3,4,5,6-пента-O-сульфато3 4 диглікозильна група, значенням R та R є С1-4 ал1-O-(2,3,4-три-O-сульфато-b-D-ксилопіранозил)-Dкільна група, тоді як значенням R2, R5 та R6 є маніту, SO3H, являють собою іншу переважну групу спододека-калієва сіль 2,4,5,6-тетра-О-сульфатолук за винаходом. 1,6-біс-О-(2,3,4,6-тетра-О-сульфато-b-DТакі сполуки формули (І), а також їх солі лужглюкопіранозил)галактитолу, них металів та лужноземельних металів, де знанона-натрієва сіль 1,2,4,5,6-пента-О-сульфаточенням R1 та R6 є полісульфатована глікозильна 3-О-(2,3,4,6-тетра-О-сульфато-b-D3 4 або диглікозильна група, значенням R та R є С1-4 глюкопіранозил)-D-глюцитолу. алкільна група, тоді як значенням R2 та R5 є Сполуки формули (І) за даним винаходом моSO3H, являють собою іншу переважну групу спожуть бути синтезовані із сполук формули (II) лук за винаходом. Особливо переважними представниками сполук формули (І) за даним винаходом є - без обмеження - такі: нона-калієва сіль 2,3,4,5,6-пента-O-сульфато1-O-(2,3,4,6-тетра-O-сульфато-b-Dглюкопіранозил)-D-маніту, нона-калієва сіль 1,2,3,4,5-пента-O-сульфато6-O-(2,3,4,6-тетра-O-сульфато-b-Dглюкопіранозил)-D-глюцитолу, нона-калієва сіль 2,3,4,5,6-пента-O-сульфато1-O-(2,3,4,6-тетра-O-сульфато-b-Dглкжопіранозил)-D-глюцитолу, нона-калієва сіль 1,2,4,5,6-пента-О-сульфатоде R7, R8, R9. R10, R11 та R12 незалежно один 3-О-(2,3,4,6-тетра-О-сульфато-b-Dвід одного означають атом водню, С1-4 алкільну, глюкопіранозил)-D-глюцитолу. глікозильну або диглікозильну групу і щонайменше нона-калієва сіль 1,2,3,5,6-пента-О-сульфатоодин з R7-R12 являє собою глікозильну або диглі4-О-(2,3,4,6-тетра-О-сульфато-a-Dкозильну групу; глюкопіранозил)-D-глюцитолу, перетворенням його вільних гідроксильних нона-калієва сіль 1,2,3,5,6-пента-О-сульфатогруп в сульфатні складні ефірі з використанням 4-О-(2,3,4,6-тетра-О-сульфато-b-Dвідомих способів. глюкопіранозил)-D-глюцитолу. Триоксид сірки або його аддукт, утворений з нона-калієва сіль 1,2,3,5,6-пента-O-сульфатоорганічною основою (наприклад, триетиламіном 4-O-(2,3,4,6-тетра-O-сульфато-b-Dабо піридин) або з диметилформамідом. може галактопіранозил)-D-глюцитолу, бути використаний для одержання О-сульфатних додека-калієва сіль 2,4,5,6-тетра-О-сульфатоскладних ефірів. 1,3-біс-О-(2,3,4,6-тетра-О-сульфато-b-DНеобов'язково монофункціональні кислі склаглюкопіранозил)-D-глюцитолу, дні ефіри, одержані вищезгаданими способами, додека-калієва сіль 2,4,5,6-тетра-О-сульфатоможуть бути перетворені в солі, наприклад, з аце1,6-біс-О-(2,3,4,6-тетра-О-сульфато-b-Dтатами лужних металів або лужноземельних меглюкопіранозил)-D-маніту, талів. Після очищення солі можуть бути одержані октадека-калієва сіль 2.4,5,6-тетра-Oліофілізацією, осадженням або кристалізацією. сульфато-1,6-біс-O-(2,3,4,2',3',4',6'-гепта-ОДеякі із сполук формули (II), що використовусульфато-b-гентіобіопіранозил)-D-маніту. ються у вигляді вихідних речовин у вищезгаданих додека-калієва сіль 2,3,4,5,6-пента-Опроцесах для синтезу сполук формули (І) за даним сульфато-1-О-(2,3,4,2',3',4',6'-гепта-О-сульфато-bвинаходом, можуть бути синтезовані, наприклад, гентіобіопіранозил)-D-маніту, наступними відомими способами. гепта-калієва сіль 3,4-ди-О-метил-2,5,6-три-ОТакі сполуки формули (II), де один з R7 та R8 сульфато-1-О-(2,3,4,6-тетра-О-сульфато-b-Dпредставляє глікозильну групу і інший являє соглюкопіранозил)-D-маніту. бою атом водню, а також значеннями R9-R12 є дека-калієва сіль 3,4-ди-О-метил-2,5-ди-Оатом водню, можуть бути синтезовані, наприклад, сульфато-1,6-біс-О-(2,3,4,6-тетра-О-сульфато-b-Dз використанням сполуки формули (III) або (IV) глюкопіранозил)-D-маніту, дека-калієва сіль 3,4-ди-О-метил-2,5,6-три-Осульфато-1-О-(2,3,4,2',3',4',6'-гепта-O-сульфато-bгентіобіопіранозил)-D-маніту, 11 87154 12 де X означає атом галогену, трихлорацетимідат або фенілтіогрупу і R13-R19 являють собою аліфатичний або ароматичний складний ефір або групу простого ефіру, як молекула-донор, і сполуки формули (V) де R20 та R21 означають атоми водню, R22-R25 являють собою захисні групи типу простого ефіру, як акцептор, і глікозилювання проводять в присутності відповідних активаторів. Потім захисні групи відщеплюють від одержаної таким чином сполуки формули (V), де R22-R25 означають захисну групу типу простого ефіру, тоді як один з R20 та R21 являє собою захищену глікозильну групу і інша є атомом водню. Відповідно до іншого способу сполуку формули (V) використовують у вищезгаданій реакції, в якій R20 та R22 означають атом водню, тоді як R21, R23, R24 та R23 являють собою захисні групи типу простого ефіру, потім захисні групи відщеплюють від одержаної таким чином сполуки формули (V), де R21, R23, R24 та R25 є захисними групами типу простого ефіру, R20 являє собою захищену глікозильну групу та R22 є атомом водню. Такі сполуки формули (II), де R7 та R9 означають глікозильну групу, тоді як R8, R10, R11 та R12 являють собою атом водню, можуть бути синтезовані, наприклад, проведенням глікозилювання відповідно до способу b), але з використанням молекули-донора в надлишку, і захисні групи відщеплюють від утвореної іаким чином сполуки загальної формули (V), де R20 та R22 являють собою захищені глікозильні групи і R21. R2j, R24 та R25 є захисними групами типу простого ефіру. Такі сполуки формули (II), де один з R7 та R8 являє собою диглікозильну групу, інший є атомом водню, a R9-R12 означають атоми водню, можуть бути синтезовані, наприклад, з використанням сполуки формули (VI) або (VII) де X означає атом галогену, трихлорацетимідат або фенілтіо групу і R26-R32 являють собою аліфатичний або ароматичний складний ефір або групу простого ефіру, як молекула-донор, і сполуки формули (V), де R20 та R21 означають атом водню, R22-R25 являють собою захисні групи типу простого ефіру, як акцептор, і глікозилювання проводять в присутності відповідних активаторів. Потім захисні групи відщеплюють від одержаної таким чином сполуки загальної формули (V) - де R22-R25 є захисними групами типу простого ефіру, тоді як один з R20 та R21 являє собою захищену глікозильну групу і інший є атомом водню. Такі сполуки формули (II), де R7 означає диглікозильну групу, можуть бути синтезовані, наприклад, з використанням сполуки формули (V), де R20 та R25 є атомами водню, R21 та R24 являють собою захисні групи типу складного ефіру, тоді як R22 та R23 є захисними групами типу простого ефіру, як акцептор у вищезгаданій реакції, потім захисні групи відщеплюють від одержаної таким чином сполуки формули (V), де R21 та R24 являють собою захисні групи типу складного ефіру, тоді як R22 та R23 являють собою захисні групи типу простого ефіру, R20 являє собою захищену диглікозильну групу і значенням R25 є атом водню. Такі сполуки формули (II), де R7 та R12 означають диглікозильну групу, і R8-R11 являють собою атом водню, можуть бути синтезовані, наприклад, з використанням сполуки формули (VI) або (VII), де X означає атом галогену, трихлорацетимідат або фенілтіогрупу і R26-R32 являють собою аліфатичний або ароматичний складний ефір або групу простого ефіру; як молекула-донор в надлишку, і сполуки формули (V), де R20 та R25 означають атом водню, R21 та R24 являють собою захисні групи типу складного ефіру, тоді як R22 та R23 являють собою захисні групи типу простого ефіру, як акцептор, і глікозилювання проводять в присутності відповідних активаторів. Потім захисні групи відщеплюють від одержаної таким чином сполуки формули (V) - де R21 та R24 являють собою захисні групи типу складного ефіру, R22 та R23 являють собою захисні групи типу простого ефіру, тоді як R20 та R25 є захищеними диглікозильними групами. 13 87154 14 У вищезгаданих реакціях глікозилювання, солі хронічного бронхіту, алергічний риніт, легеневі ртуті або срібла, діетиловий етерат трифтористого запальні і структурні реакції, вторинні по віднобору, N-йодсукцинімід і трифторметансульфонова шенню до хронічного бронхіту, хронічні обструктикислота або суміш двох останніх також можуть вні захворювання легенів, пневмосклероз. Винахід використовуватися як активатори. також застосовний для станів легенів, при яких Відщеплення захисних груп може проводитися можуть відігравати роль лейкоцити і перебудова кислим гідролізом або відновленням в присутності дихальних шляхів, включаючи, без обмеження каталізатора у випадку простих ефірів і ацеталій, переліченими, ідіопатичний пневмосклероз та тоді як у випадку складних ефірів може використобудь-яке інше аутоімунне захворювання легенів. вуватися метод Цемплена (транс-естерифікація. Під «астмою» мають на увазі стан алергічного що каталізується основою) або гідроліз в присутпоходження, симптоми якого включають безпереності основи. рвну або пароксизмальну задишку, що супровоСкорочення і вирази, що використовуються в джується хрипами, відчуттям стискання в грудній описі: клітці, і частими приступами кашлю або утруднеАс = ацетил ного дихання. Під «патологією, пов'язаною з астBz = бензоїл мою» мають на увазі стан, симптоми якого є переMe = метил важно запальними за природою із зв'язаним Ph = феніл бронхоспазмом. Отже, і астма, і патології, пов'язаNIS = N-йодсукцинімід ні з астмою, характеризуються симптомами, які TfOH = трифторметансульфонова кислота включають звуження дихальних шляхів, зумовлеЯк використовується в даному описі, форми не різними ступенями скорочення (спазму) гладких однини також охоплюють форми множини термім'язів, набряком слизової, включаючи таку верхніх нів, яких вони стосуються, якщо тільки із змісту дихальних шляхів і слизової оболонки в просвіті явно не виходить інше. Наприклад, посилання на бронхів і бронхіол. Необмежені характерні прикла«модулятор» включає суміш модуляторів. ди «патологій, пов'язаних з астмою» включають Як використовується в даному описі, або в неастматичні стани, що характеризуються гіперпроміжній фразі або в тексті формули винаходу, реактивністю дихальних шляхів (наприклад, хронітерміни «включає» і «що включає» повинні інтерчний бронхіт, емфізема, муковісцидоз та респірапретуватися як такі, що мають відкрите значення. торний дистрес-синдром). А саме, терміни повинні інтерпретуватися одноКомпозиції та способи, вказані в даному описі, значно з фразами «що має, щонайменше» або є зразковими для астми. Однак винахід не повинен «що включає, щонайменше». При використанні в розглядатися як обмежений таким визначеним контексті способу термін «що включає» означає, захворюванням легенів. Астма дає перевагу ретещо спосіб включає щонайменше вказані стадії, але льного дослідження і забезпечує декілька прийняможе включати додаткові стадії. При використанні тних моделей для оцінки винаходу. Відомо, що в контексті сполуки або композиції термін «що сенсибілізація і введення алергену призводить до включає» означає, що сполука або композиція гіперреактивності дихальних шляхів на різні агонівключає щонайменше вказані властивості або сти. Отже, ацетилхолін, відомий як спазмогенний компоненти, але також може включати додаткові агент, здатний спричинити більш сильні скороченвластивості або компоненти. ня м'язових клітин в тканинах, одержаних з трахеї Термін «близько» використовується в даному умертвлених тварин (які були сенсибілізовані для описі для позначення приблизно, в зоні, орієнтовпровокації гіперреактивності дихальних шляхів), но або приблизно. Коли термін «близько» викориніж від контрольних тварин після введення алерстовують в зв'язку із зоною числових значень, він гену [дивіться, наприклад, Tokuoka et at, Br. J. визначає, що вказується діапазон з розширеними Pharmacol. 134:1580 (2001); Nakata et al., Int. межами вище і нижче вказаної зони числових знаImmunol. 13:329 (2001); Emala та Hirshman. чень. Загалом, термін «близько» використовується Monogr. Allergy 33:35 (1996)]. в даному описі для модифікації зони числових Найбільш явною характеристикою астми є значень вище і нижче вказаного значення з відхибронхоспазм, або звуження дихальних шляхів. У ленням 20%. пацієнтів з астмою розвивається виражене скороЯк використовується в даному описі, якщо чення гладких м'язів великих та дрібних дихальних особливо не вказано інакше, слово «або» викорисшляхів, збільшена продукція слизу, і збільшене товується з «включеним» значенням «і/або» і не запалення [Plaut і Zimmerman, вище]. Запальна «виключним» значенням «або/або». відповідь при астмі є типовою для тканин, покриЯк використовується в даному описі, терміни тих слизовою оболонкою і характеризується роз«лікування» або «виліковування» використовують ширенням кровоносних судин, випотом плазми, для вказівки зниження, полегшення, профілактики, залученням запальних клітин, таких як нейтрофіінгібування розвитку і/або обернення симптомів ли, моноцити, макрофаги, лімфоцити та еозинофістану. Стани для лікування способами та комполи, до місця запалення, і вивільненням запальних зиціями за винаходом включають будь-який стан, медіаторів місцевими тканинними клітинами (нащо характеризується або включає гострі і хронічні приклад, тучними клітинами або епітеліальними запальні розлади дихальних шляхів. Отже, терміклітинами дихальних шляхів) або міграцією запани «запальний розлад» або «запальні розлади льних клітин [Hogg, «Pathology of Asthma», in дихальних шляхів» охоплюють будь-які запальні Asthma as an Inflammatory Disease. O'Byrne (ed.), захворювання легенів, включаючи астму, ендогенMarcel Dekker, Inc., New York, NY, at 1 (1990)]. Асну або екзогенну бронхіальну астму, загострення тму можуть запускати ряд причин, таких як алергі 15 87154 16 чні реакції, вторинна відповідь на інфекції, виробМодель 1 ничі або професійні впливи, споживання певних Вивчення ефекту полісульфатованих глікозихімічних речовин або лікарських речовин, фізичні дів, що вводяться місцево, на гіперреактивність навантаження [Hargreave et al., J. Allergy Clin. дихальних шляхів ex vivo Immunol. 83:1013 (1986)]. Запалення дихальних шляхів може призвести Сполуки формули (І) відповідно до винаходу до гіперреактивності бронхів, що є характерною також були виявлені як ефективні в зниженні проознакою астми. дукування слизу епітеліальними клітинами бронхів Коричневих Норвезьких (BN) щурів активно та інгібуванні проліферації гладком'язових клітин, сенсибілізували яєчним білком (ОА) за допомогою опосередкованої факторами росту. підшкірної ін'єкції 0,5мл гелевої суміші ОА/Аl(ОН)3 Збільшення гіперреактивності бронхів (AHR), (2мг ОА+10г Аl(ОН)3/100мл фізіологічного розчину) ознака більш важкої форми астми, може бути індув день 1 з подальшими підшкірними ін'єкціями коване і антигенними і неантигенними подразни(10мг ОА+10г Аl(ОН)3/100мл фізіологічного розчиками дихальних шляхів. Відповідь пізньої фази і ну), що вводяться в дні 14 та 21. У день 28 тварипостійна гіперреактивність при астмі, індукованій ни одержували сполуку, описану в прикладі 4, іналергеном, асоційовані із залученням лейкоцитів і тратрахеально (дозу 0,01, 0,1 або 1,0мг/кг) за 2 особливо еозинофілів в запалену тканину легенів години до впливу антигену. Подразнення антиге[Abraham et al., Am. Rev. Respir. Dis. 138:1565 ном проводили інгаляцією розпиленого яєчного (1988)]. Еозинофіли вивільняють декілька медіабілка (1% розчин антигену, що вводиться в системі торів запалення, включаючи 15-НЕТЕ, лейкотриен для інгаляцій TSE протягом 1 години). Тварин С4, PAF, катіонні білки, еозинофільну пероксидазу. умертвляли через 48 годин після впливу антигену, Терміни «антиген» та «алерген» використовупотім видаляли трахеї в кювету для органів. Посіють взаємозамінно для опису таких молекул, як ченим трахеям дозволяли урівноважитися протяпил або пилок, які можуть спричинити алергічні гом 30 хвилин до вимірювання кривих спазмогені/або індукувати астматичні симптоми у пацієнта, ної відповіді трахеї на ацетилхолін (Ach). що страждає від астми. Таким чином, пацієнт з Як показано в таблиці 1 подразнення яєчним астмою «при впливі» алергену або антигену забілком сенсибілізованих тварин в цій моделі спризнає впливу достатньої кількості алергену або анчинило істотну гіперреактивність трахеї на ацетилтигену, щоб викликати астматичну відповідь. Було холін, коли відповідь на спазмогенний агент вивиявлено, що сполуки формули (І) за винаходом значали через 48 годин після впливу антигену. ефективні для лікування AHR після сенсибілізації Сполука, описана в прикладі 4, в дозі 0,01мг/кг, яєчним білком і впливу антигену. повертала це підвищення зворотно майже до конБіологічна активність сполук формули (І) за трольного рівня. даним винаходом на різних тваринних моделях продемонстрована нижче: Таблиця 1 Ефект впливу антигену та інтратрахеального попереднього лікування сполукою прикладу 4 на скорочення трахеї у відповідь на ацетилхолін у ΒΝ щурів Параметри Контроль Плацебо ED50* ρ MAX** ρ 4,73±0,05 0,032 100±0 0.006 5,51±0,21 334±68 Сполука, що досліджується 0,01мг/кг 1,0мг/кг 4,40±0,30 4,60±0,55 220°С, вихід 73%, [a]D +40° (с 1, вода). С12Н15O39S9K9 Розраховано: С 10,22; Η 1,06; S 20,45; K 24,30. Виявлено: С 9,84; Η 1,40; S 19,98; K 23,99. Приклад 6 Нона-калієва сіль 1,2,3,5,6-пента-O-сульфато4-О-(2,3,4,6-тетра-О-сульфато-b-Dглюкопіранозил)-D-глюцитолу (LХVII) (IB, R4=тетракалієва сіль 2,3,4,6-тетра-О-сульфато-bD-глюкопіранозилу, R1=R2=R3=R5=R6=SO3K) Вказану в заголовку сполуку (LXVIII) одержували відповідно до способу, описаного в прикладі 1, з використанням 4-О-b-D-галактопіранозил-Dглюцитолу [XXI, W.J. Whelan і K. Morgan, Chem. і Ind. (1955) 1449-1450] як вихідної речовини. Т. пл. >220°С, вихід 40%, [a]D 0° (с 1, вода). С12Н15O39S9K9 Розраховано: С 10,22; Η 1,06; S 20,45; K 24,30. Виявлено: С 9,99; Η 1,29; S 19,88; K 23,87. Приклад 8 Додека-калієва сіль 2,4,5,6-тетра-О-сульфато1,3-біс-О-(2,3,4,6-тетра-О-сульфато-b-Dглюкопіранозил)-D-глюцитолу (LXIX) (IB, R1тетракалієва = =R3 сіль 2,3,4,6-тетра-Осульфато-b-D-глюкопіранозилу, R2=R4=R5=R6=SO3K) Вказану в заголовку сполуку (LXVII) одержували відповідно до способу, описаного в прикладі 1, з використанням 4-О-b-D-глюкопіранозил-Dглюцитолу [XX, MX. Wolfram et al., J. Am. Chem. Soc. 74 (1952) 1105] як вихідної речовини. Т. пл. >220°С, вихід 41%, [a]D +5° (с 1, вода). С12Н15O39S9K9 Розраховано: С 10,22; Η 1,06; S 20,45; K 24,30. Виявлено: С 9,89; Η 1,42; S 19,99; K 23,87. Приклад 7 Нона-калієва сіль 1,2,3,5,6-пента-О-сульфато4-О-(2,3,4,6-тетра-О-сульфато-b-Dгалактопіранозил)-D-глюцитолу (LXVIII) (IB, R4=тетракалієва сіль 2,3,4,6-тетра-О-сульфато-bD-галактопіранозилу, R1=R2=R3=R5=R6=SO3K) Вказану в заголовку сполуку (LXIX) одержували відповідно до способу, описаного в прикладі 1, з використанням 1,3-біс-О-b-D-глюкопіранозил-Dглюцитолу (XXIV) як вихідної речовини. Т. пл. >220°С, вихід 82%. [a]D -6,5° (с 1, вода). C18H22O52S12K12 Розраховано: С 11,24; Η 1,15; S 19,99; K 24,38. Виявлено: С 11,01; Η 1,32; S 19,07; K 23,99. Приклад 9 Додека-калієва сіль 2,3,4,5-тетра-О-сульфато1,6-біс-О-(2,3,4,6-тетра-О-сульфато-b-Dглюкопіранозил)-D-маніту (LXX) (ІА, R1тетракалієва = =R6 сіль 2,3,4,6-тетра-О 55 сульфато-b-D-глюкопіранозилу, O3K) R2=R3=R4=R5= Вказану в заголовку сполуку (LXX) одержували відповідно до способу, описаного в прикладі 1, з використанням 1,6-біс-О-b-D-глюкопіранозил-Dманіту (XXIX) як вихідної речовини. Т. пл. >220°С, вихід 83%, [a]D +1,5° (с 1, вода). С18H22O52S12K12 Розраховано: С 11,24; Η 1,14; S 19,98; K 24,35. Виявлено: С 10,93; Η 1,55; S 19,26; K 23,99. Приклад 10 Октадека-калієва сіль 2,3,4,5-тетра-Осульфато-1,6-біс-О-(2,3,4,2',3',4',6'-гепта-Осульфато-b-гентіобіопіранозил)-D-маніту (LXXI) (IA, R1=R6=гептакалієва сіль 2,3,4,2',3',4',6'-гептаО-b-гентіобіопіранозилу, R2=R3=R4=R5= SO3K) Вказану в заголовку сполуку (LXXI) одержували відповідно до способу, описаного в прикладі 1. з використанням 1,6-біс-О-b-гентіобіопіранозил-Dманіту (XXXIII) як вихідної речовини, з відмінністю, що додавали 20мл етанолу до дуже тиксотропного водного розчину, концентрованого до 20мл, потім суміш охолоджували до +4°С. Осаджений продукт відфільтровували і промивали етанолом. Т. пл. >220°С, вихід 99%, [a]D +0° (с 1, вода). С30Н36O80S18K18 Розраховано: С 12,18; Η 1,33; S 19,51; K 23,80. Виявлено: С 11,88; Η 1,65; S 19,92; K 24,16. Приклад 11 Додека-калієва сіль 2,3,4,5,6-пента-Oсульфато-1-О-(2,3,4,2',3',4',6'-гепта-О-сульфато-bгентіобіопіранозил)-D-маніту (LXXII) (ІА, гептакалієва = R1 сіль 2,3,4,2',3',4',6'-гепта-О 87154 56 сульфато-b-гентіобіопіранозилу, R4=R5=R6=SO3K) R2=R3 Вказану в заголовку сполуку (LXXII) одержували відповідно до способу, описаного в прикладі 1. з використанням 1-О- b-гентіобіопіранозил-Dманіту (XXXVII) як вихідної речовини. Т. пл. >220°С, вихід 79%, [a]D +6° (с 1, вода). C18H22O52S12K12 Розраховано: С 11,24; Η 1,14; S 19,98; K 24,38. Виявлено: С 10,98; Η 1,51; S 19,37; K 24,02. Приклад 12 Гептакалієва сіль 3,4-ди-O-метил-2,5,6-три-Oсульфато-1-O-(2,3,4,6-тетра-O-сульфато-b-Dглюкопіранозил)-D-маніту (LXXIII) (ІА, R1=тетракалієва сіль 2,3,4,6-тетра-О-сульфато-bD-глюкопіранозилу, R3=R4=Me, R2=R5=R6=SO3K) Вказану в заголовку сполуку (LXXIII) одержували відповідно до способу, описаного в прикладі 1, з використанням 1-Ο-b-D-глюкопіранозил-Dманіту (XLVI) як схожої речовини, з відмінністю, що сирий продукт, який осаджували метанолом і відфільтровували, розчиняли у воді і рН одержаного таким чином розчину доводили до 8 за допомогою 1н. розчину гідроксиду калію. Після цього 3мл 1н. водного розчину ацетату стронцію додавали до розчину, до закінчення утворення осаду (SrSO4). Осад відфільтровували і фільтрат вносили на ко 57 87154 58 лонку, навантажену смолою CHELX 100 (калієва Вказану в заголовку сполуку (LXXV) одержуформа) (10мл), з метою видалення іонів стронцію. вали відповідно до способу, описаного в прикладі Колонку елюювали дистильованою водою і елюат 1, з використанням 1-O-b-гентіобіопіранозил-3,4концентрували. Залишок обробляли етанолом, ди-O-метил-D-маніту (XLVII) як вихідної речовини. відфільтровували і промивали етанолом. Т. пл. Т. пл. >220°С, вихід 99%, [a]D -5° (с 1. вода). >220°С, вихід 94%, [a]D 0° (с 1, вода). C20H28O46S10K10 Розраховано: С 14,00; Η 1,64; S C14H21O32S7K7 Розраховано: С 14,02; Η 1,76; S 18,68; K 22,78. Виявлено: С 13,87; Η 1,99; S 19,24; 18,71; K 22,82. Виявлено: С 14,06; Η 2,02; S 18,31; K 22,43. K 22,67. Приклад 15 Приклад 13 Гексадека-калієва сіль 3,4-ди-О-метил-2,5-диДека-калієва сіль 3,4-ди-О-метил-2,5-ди-ОО-сульфато-1,6-біс-О-(2,3,6,2',3',4',6'-гепта-Осульфато-1,6-біс-О-(2,3,4,6-тетра-O-сульфато-b-Dсульфато-b-лактозил-D-маніту (LXXVI) (IΑ, глюкопіранозил)-D-маніту (LXXIV) (ІА, R1=R6 ептакалієва сіль г = 2,3,6,2',3',4',6'-гепта-ОR1тетракалієва = =R6 сіль 2,3,4,6-тетра-Осульфато-b-лактозилу, R3=R4=Me, R2=R5=SO3K) 3 4 сульфато-b-D-глюкопіранозилу, R =R =Me, R2=R5=SO3K) Вказану в заголовку сполуку (LXXIV), отриману відповідно до способу, описаного в прикладі 1, з використанням 1,6-біс-О-b-D-глюкопіранозил-3,4ди-О-метил-D-маніту (XLVIII) як вихідної речовини. Т. пл. >220°С, вихід 85%, [a]D -6,5° (с 1, вода). C20H28O46S10K10 Розраховано: С 14,00; Η 1,63; S 18,68; K 22,78. Виявлено: С 13,85; Η 1,99; S 18,06; K 21,97. Приклад 14 Дека-калієва сіль 3,4-ди-О-метил-2,5,6-три-Осульфато-1-О-(2,3,4,2',3',4',6'-гепта-О-сульфато-bгентіобіопіранозил)-D-маніту (LXXV) (IΑ, гептакалієва = R1 сіль 2,3,4,2',3',4',6'-гепта-Осульфато-b-гентіобіопіранозилу, R3=R4=Me, R2=R5=R6=SO3K) Вказану в заголовку сполуку (LXXVI) одержували відповідно до способу, описаного в прикладі 1 з використанням 1,6-біс-лактопіранозил-3,4диметил-D-маніту (LII) як вихідної речовини. Т. пл. >220°С, вихід 44%. [a]D +2° (с 1, вода). C32H42O74S16K16 Розраховано: С 13,98; Η 1,53; S 18,65; K 22,75. Виявлено: С 13,51; Η 1,73; S 17,98; K 21,15. Приклад 16 Октакалієва сіль 2,3,4,5,6-пента-О-сульфато1-О-(2,3,4-три-О-сульфато-a-D-арабінопіранозил)D-маніту (LXXVII) (ІА, R1=трикалієва сіль 2,3,4-триО-сульфато-b-D-арабінопіранозилу, R2=R3=R4=R5=R6=SO3K) Вказану в заголовку сполуку (LXXVII) одержували відповідно до способу, описаного в прикладі 1 з використанням 1-О-a-D-арабінопіранозил-Dманіту (LV) як вихідної речовини. Т. пл. >220°С, вихід 99%, [a]D +19° (с 1, вода). С11Н14O34S8K8 Розраховано: С 10,49; Η 1,12; S 20,36; K 24,83. Виявлено: С 10,06; Η 1,40; S 19,56; K 24,04. 59 87154 Приклад 17 Октакалієва сіль 2,3,4,5,6-пента-О-сульфато1-О-(2,3,4-три-О-сульфато-b-D-ксилопіранозил)-Dманіту (LXXVIII) (ΙΑ, R1=трикалієва сіль 2,3,4-триО-сульфато-b-D-ксилопіранозилу, R2=R3-R4=R56 R =SO3K) Вказану в заголовку сполуку (LXXVIII) одержували відповідно до способу, описаного в прикладі 1, з використанням 1-Ο-b-D-ксилопіранозил-Dманіту (LVII) як вихідної речовини. Т. пл. >220°С. вихід 85%, [a]D -6° (с 1, вода). С11Н14O32S8K8 Розраховано: С 10,49; Η 1,12; S 20,36; K 24,83. Виявлено: С 10,05; Η 1,29; S 19,98; K 14,52. Приклад 18 Додека-калієва сіль 2,3,4,5-тетра-О-сульфато1,6-біс-О-(2,3,4,6-тетра-О-сульфато-b-Dглюкопіранозил)галактитолу (LXXIX) (IС, R1тетракалієва = =R6 сіль 2,3.4,6-тетра-Осульфато-b-D-глюкопіранозилу, R2=R3=R4=R5=SO3K) Вказану в заголовку сполуку (LXXIX) одержували відповідно до способу, описаного в прикладі 1, з використанням 1,6-бісглюкопіранозилгалактитолу (LXII) як вихідної речовини. Т. пл. >220°С, вихід 83%. [a]D -10° (с 1, вода). C18H22O52S12K12 Розраховано: С 11,24; Η 1,15; S 19,99; K 24,38. Виявлено: С 10,98; Η 1,35; S 19,28; K 24,07. Приклад 19 Нона-натрієва сіль 1,2.4,5,6-пента-Осульфато-3-О-(2,3,4,6-тетра-О-сульфато-b-Dглюкопіранозил)-D-глюцитолу (LXXX) (IB, R3=тетракалієва сіль 2,3,4,6-тетра-О-сульфато-bD-глюкопіранозилу, R1=R2=R4=R5=R6=SO3Na) 60 5,1г (48%, 30ммоль) комплексу триоксиду сірки - диметилформаміду суспендували в 5мл сухого диметилформаміду при перемішуванні, суміш охолоджували до -20°С і поступово додавали 0,52г (1,5ммоль) 3-O-b-D-глюкопіранозил-D-глюцитолу (XVII) в 5мл диметилформаміду з такою швидкістю, щоб підтримувати температуру нижче -15°С. Суміш перемішували при 5°С протягом 1 години. Після цього реакційну суміш знову охолоджували до -15°С і поступово додавали 1,5мл етанолу з такою швидкістю, щоб підтримувати температуру нижче -10°С. Потім реакційну суміш вливали в розчин натрію, що перемішується та охолоджується (0°С), 5г ацетату і 40мл метанолу. Осад відфільтровували і промивали 3´40мл метанолу. Твердий залишок розчиняли в 30мл води і рН розчину доводили спочатку до 8 за допомогою 1Μ розчину гідроксиду натрію, потім 3мл 1Μ водного розчину ацетату стронцію додавали до розчину. Через 30 хвилин осад відфільтровували і промивали холодною водою. Фільтрат вносили на колонку, навантажену смолою CHELX 100 (натрієва форма) (15мл) з метою видалення іонів стронцію. Колонку елюювали дистильованою водою і елюат концентрували. Залишок обробляли етанолом, відфільтровували і промивали етанолом для одержання 1,9г (99%) вказаної в заголовку сполуки. Т. пл. >220°С; [a]D +1,5° (с 1, вода). C12H15O38S9Na9 Розраховано: С 11,41; Η 1,20; S 22,85; Na 24,39. Виявлено: С 11,74; Η 1,57; S 22,25; Na 16,09. Еквіваленти Тоді як заявлений винахід описаний детально і з посиланнями на його специфічні варіанти здійснення, зрозуміло, що звичайний фахівець в галузі техніки може здійснити різні уточнення і модифікації не виходячи за межі суті та обсягу даного винаходу. Отже, наприклад, фахівець в галузі техніки розуміє або може встановити, з використанням не більш ніж звичайних експериментів, множину еквівалентів специфічних речовин і методик, описаних в даному описі. Такі еквіваленти розглядаються в обсязі даного винаходу та охоплюються наступною формулою винаходу.
ДивитисяДодаткова інформація
Назва патенту англійськоюPolysulfated glycosides and salts thereof
Автори англійськоюKuszmann Janos, Kurucz Istvan, Medgyes Gabor, Bodor Nicholas
Назва патенту російськоюПолисульфатованые гликозиды и их соли
Автори російськоюКусманн Янош, Куруц Иштван, Меддьеш Габор, Бодор Николас
МПК / Мітки
МПК: C07H 15/00
Мітки: глікозиди, солі, полісульфатовані
Код посилання
<a href="https://ua.patents.su/31-87154-polisulfatovani-glikozidi-ta-kh-soli.html" target="_blank" rel="follow" title="База патентів України">Полісульфатовані глікозиди та їх солі</a>
Попередній патент: Енантіомерно чисті аміногетероарильні сполуки як інгібітори протеїнкінази
Наступний патент: Машина для обгортання профілів
Випадковий патент: Гомогенізатор