Гербіцидні сполуки піридазинону
Номер патенту: 112890
Опубліковано: 10.11.2016
Автори: Мет'юз Крістофер Джон, Бартон Пол, Морріс Джеймс Алан, Шенехен Стівен, Козакевіч Ентоні
Формула / Реферат
1. Сполука формули (І)
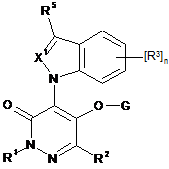
або її прийнятна з погляду сільського господарства сіль,
де
X1 являє собою N або CR4;
R1 вибраний з групи, що складається з С1-С4алкілу, С1-С2алкоксі-С1-С2алкілу, С2-С4алкенілу, С1-С4галогеналкілу, С2-С4галогеналкенілу, С2-С4алкінілу та С2-С4галогеналкінілу;
R2 вибраний з групи, що складається з водню, галогену, ціано, С1-С6алкілу, С1-С6галогеналкілу, С1-С6галогеналкокси, С1-С3галогеналкоксі-С1-С3алкілу-, С1-С6алкокси, С1-С3алкоксі-С1-С3алкілу, С1-С3алкоксі-С1-С3алкоксі-С1-С3алкілу-, С3-С6циклоалкілу, С2-С6алкенілу, С2-С6галогеналкенілу, С2-С6алкінілу, С1-С6гідроксіалкілу-, С1-С6алкілкарбонілу-, -S(О)рС1-С6алкілу, аміно, С1-С6алкіламіно, С1-С6діалкіламіно, -С(С1-С3алкіл)=N-О-С1-С3алкілу та С2-С6галогеналкінілу;
R3 незалежно вибраний з групи, що складається з водню, галогену, нітро, ціано, аміно, С1-С6алкілу, C1-С6галогеналкілу, С3-С6циклоалкілу, С1-С6алкокси, С1-С6алкоксикарбонілу та -S(О)рС1-С6алкілу;
R4 та R5 незалежно вибрані з групи, що складається з водню, гідроксилу, галогену, нітро, ціано, аміно, С1-С6алкілу, С1-С6галогеналкілу, С3-С6циклоалкілу, С1-С6алкокси, С1-С6алкоксикарбонілу та -S(O)pC1-С6алкілу;
G являє собою водень або -C(O)-R6;
R6 вибраний з групи, що складається з С1-С6алкілу, С1-С6алкенілу, С1-С6алкінілу, С1-С6алкіл-S-, С1-С6алкокси, -NR7R8 та фенілу, необов'язково заміщених одним або декількома R9;
R7 та R8 незалежно вибрані з групи, що складається з С1-С6алкілу, С1-С6алкокси-;
де R7 та R8 разом можуть утворювати морфолінільне кільце;
R9 вибраний з групи, що складається з галогену, ціано, нітро, C1-С3алкілу, С1-С3галогеналкілу, C1-С3алкокси та С1-С3галогеналкокси;
n = 0, 1, 2, 3 або 4; та
p = 0, 1 або 2.
2. Сполука за п. 1, де G являє собою водень.
3. Сполука за п. 1 або п. 2, де R2 вибраний з групи, що складається з водню, C1-С6алкілу, С1-С6галогеналкілу, С1-С6алкокси, С1-С3алкоксі-С1-С3алкілу, С3-С6циклоалкілу, С2-С6алкенілу, С2-С6галогеналкенілу, С1-С6алкінілу та С2-С6галогеналкінілу.
4. Сполука за п. 3, де R2 вибраний з групи, що складається з водню, метилу, етилу, циклопропілу та метоксиметилу.
5. Сполука за будь-яким з попередніх пунктів, де R2 являє собою метил.
6. Сполука за будь-яким з попередніх пунктів, де n = 0.
7. Сполука за будь-яким з попередніх пунктів, де R1 вибраний з групи, що складається з метилу, етилу та н-пропілу.
8. Сполука за будь-яким з попередніх пунктів, де X1 являє собою N.
9. Сполука за будь-яким з попередніх пунктів, де X1 являє собою CR4.
10. Сполука за п. 9, де R4 являє собою галоген та/або R5 являє собою галоген.
11. Гербіцидна композиція, яка містить гербіцидну сполуку за будь-яким з попередніх пунктів і прийнятний з погляду сільського господарства допоміжний засіб для складання.
12. Гербіцидна композиція за п. 11, яка додатково містить щонайменше один додатковий пестицид.
13. Гербіцидна композиція за п. 12, яка відрізняється тим, що додатковий пестицид являє собою гербіцид або антидот гербіциду.
14. Спосіб боротьби з бур'янами в місці зростання, який включає застосування до місця зростання достатньої для боротьби з бур'янами кількості композиції за будь-яким з пп. 11-13.
15. Застосування сполуки формули (І) за п. 1 як гербіциду.
Текст
Реферат: Даний винахід стосується сполук формули (I) (72) Винахідник(и): Бартон Пол (GB), Козакевіч Ентоні (GB), Морріс Джеймс Алан (GB), Метьюз Крістофер Джон (GB), Шенехен Стівен (GB) (73) Власник(и): СІНГЕНТА ЛІМІТЕД, European Regional Centre, Priestley Road, Surrey Research Park, Guildford Surrey GU2 7YH, United Kingdom (GB) (74) Представник: Петров Андрій Володимирович, реєстр. №139 (56) Перелік документів, взятих до уваги експертизою: WO 2009/086041 A1, 09.07.2009 WO 2011/045271 A1, 21.04.2011 UA 112890 C2 (12) ОПИС ДО ПАТЕНТУ НА ВИНАХІД UA 112890 C2 R X 5 1 [R3]n N O R O 1 N N R G 2 або прийнятної з погляду сільського господарства солі зазначених сполук, де визначення для 1 1 2 3 5 X , R , R , R , R , G та n наведені в даному документі. Даний винахід, крім того, стосується гербіцидних композицій, які містять сполуку формули (І), та їхнього застосування для боротьби з бур'янами, зокрема серед сільськогосподарських культур корисних рослин. UA 112890 C2 5 10 15 20 25 30 35 40 45 Даний винахід відноситься до нових гербіцидних сполук, способів їх одержання, гербіцидних композицій, які містять нові похідні, та до їхнього застосування для боротьби з бур'янами, зокрема, серед сільськогосподарських культур корисних рослин, або для пригнічення росту рослин. Гербіцидні піридазинони відомі з WO2009/086041. Крім того, гербіцидні 5/6-членні гетероцикліл-заміщені піридазинони відомі з WO 2011/045271. Даний винахід заснований на ідентифікації альтернативних гетероцикліл-заміщених піридазинонів, які характеризуються покращеними гербіцидними властивостями. Таким чином, відповідно до даного винаходу представлена сполука формули (I), (I) , або її прийнятна з погляду сільського господарства сіль, де 1 4 X являє собою N або CR ; 1 R обраний з групи, що складається з C1-C4алкілу, C1-C2алкокси-C1-C2алкілу, C2-C4алкенілу, C1-C4галогеналкілу, C2-C4галогеналкілу, C2-C4алкінілу та C2-C4галогеналкінілу; 2 R обраний з групи, що складається з водню, галогену, ціано, C 1-C6алкілу, C1C6галогеналкілу, C1-C6галогеналкоксі, C1-C3галогеналкокси-C1-C3алкілу-, C1-C6алкоксі, C1C3алкокси-C1-C3алкілу, C1-C3алкокси-C1-C3алкокси-C1-C3алкілу-, C3-C6циклоалкілу, C2C6алкенілу, C2-C6галогеналкенілу, C2-C6алкінілу, C1-C6гідроксіалкілу-, C1-C6алкілкарбонілу-, S(O)pC1-C6алкілу, аміно, C1-C6алкіламіно, C1-C6діалкіламіно, -C(C1-C3алкіл)=N-O-C1-C3алкілу та C2-C6галогеналкінілу; 3 R незалежно обраний з групи, що складається з водню, галогену, нітро, ціано, аміно, C 1C6алкілу, C1-C6галогеналкілу, C3-C6циклоалкілу, C1-C6алкоксі, C1-C6алкоксикарбонілу та S(O)pC1-C6алкілу; 4 5 R та R незалежно обрані з групи, що складається з водню, гідроксилу, галогену, нітро, ціано, аміно, C1-C6алкілу, C1-C6галогеналкілу, C3-C6циклоалкілу, C1-C6алкоксі, C1C6алкоксикарбонілу та -S(O)pC1-C6алкілу; 6 G являє собою водень або -C(O)-R ; 6 R обраний з групи, що складається з C1-C6алкілу, C1-C6алкенілу, C1-C6алкінілу, C1-C6алкіл7 8 9 S-, C1-C6алкоксі, -NR R та фенілу, необов'язково заміщених одним або декількома R ; 7 8 R та R незалежно обрані з групи, що складається з C1-C6алкілу, C1-C6алкоксі-; 7 8 де R та R разом можуть утворювати морфолінільне кільце; 9 R обраний з групи, що складається з галогену, ціано, нітро, C 1-C3алкілу, C1-C3галогеналкілу, C1-C3алкоксі або C1-C3галогеналкоксі; n=0,1,2,3 або 4; та p=0, 1 або 2. Галоген (або галогено) охоплює фтор, хлор, бром або йод. Те саме, відповідно, стосується галогену в контексті інших визначень, таких як галогеналкіл або галогенфеніл. Галогеналкільними групами з довжиною ланцюга від 1 до 6 атомів вуглецю є, наприклад, фторметил, дифторметил, трифторметил, хлорметил, дихлорметил, трихлорметил, 2,2,2трифторетил, 2-фторетил, 2-хлоретил, пентафторетил, 1,1-дифтор-2,2,2-трихлоретил, 2,2,3,3тетрафторетил і 2,2,2-трихлоретил, гептафтор-н-пропіл і перфтор-н-гексил. Алкоксигрупи переважно характеризуються довжиною ланцюга від 1 до 6 атомів вуглецю. Алкоксі являє собою, наприклад, метоксі, етоксі, пропоксі, ізопропоксі, н-бутоксі, ізобутоксі, втор-бутоксі, або трет-бутоксі, або ізомер пентилоксі або гексилоксі, переважно метоксі та етоксі. Також слід відзначити, що два замісники алкоксі присутні на одному і тому ж атомі вуглецю. 1 UA 112890 C2 5 10 Галогеналкоксі являє собою, наприклад, фторметоксі, дифторметоксі, трифторметоксі, 2,2,2-трифторетоксі, 1,1,2,2-тетрафторетоксі, 2-фторетоксі, 2-хлоретоксі, 2,2-дифторетоксі або 2,2,2-трихлоретоксі, переважно дифторметоксі, 2-хлоретоксі або трифторметоксі. C1-C6алкіл-S- (алкілтіо) являє собою, наприклад, метилтіо, етилтіо, пропілтіо, ізопропілтіо, нбутилтіо, ізобутилтіо, втор-бутилтіо або трет-бутилтіо, переважно метилтіо або етилтіо. C1-C6алкіл-S(O)- (алкілсульфініл) являє собою, наприклад, метилсульфініл, етилсульфініл, пропілсульфініл, ізопропілсульфініл, н-бутилсульфініл, ізобутилсульфініл, втор-бутилсульфініл або трет-бутилсульфініл, переважно метилсульфініл або етилсульфініл. C1-C6алкіл-S(O)2(алкілсульфоніл) являє собою, наприклад, метилсульфоніл, етилсульфоніл, пропілсульфоніл, ізопропілсульфоніл, н-бутилсульфоніл, ізобутилсульфоніл, втор-бутилсульфоніл або трет-бутилсульфоніл, переважно метилсульфоніл або етилсульфоніл. В переважному варіанті здійснення даного винаходу представлена сполука формули II (формула I, де G являє собою водень). (II) 15 20 25 30 35 40 45 2 В іншому переважному варіанті здійснення даного винаходу R обраний з групи, що складається з водню, C1-C6алкілу, C1-C6галогеналкілу, C1-C6алкоксі, C1-C3алкокси-C1-C3алкілу, C3-C6циклоалкілу, C2-C6алкенілу, C2-C6галогеналкенілу, C2-C6алкінілу та C2-C6галогеналкінілу. 2 Особливо переважно, якщо R обраний з групи, що складається з водню, метилу, етилу, циклопропілу та метоксиметилу, найбільш переважно метилу. 2 В іншому варіанті здійснення даного винаходу R являє собою водень. В іншому варіанті здійснення даного винаходу n=0. 1 В іншому варіанті здійснення даного винаходу R обраний з групи, що складається з метилу, етилу та н-пропілу. 1 В іншому варіанті здійснення даного винаходу X являє собою N. 1 4 В іншому варіанті здійснення даного винаходу X являє собою CR . Особливо переважно, 4 5 якщо R являє собою галоген (найбільш переважно хлор) та/або R являє собою галоген (найбільш переважно хлор). Сполуки формули I можуть містити асиметричні центри та можуть бути представлені у вигляді одного енантіомеру, пар енантіомерів у будь-якій пропорції або, за наявності більш одного асиметричного центру, містити діастереоізомери у всіх можливих співвідношеннях. Як правило, один з енантіомерів має підвищену біологічну активність у порівнянні з іншими варіантами. Аналогічно, у випадку дизаміщених алкенів, вони можуть бути представлені в E- або Zформі або у вигляді їх сумішей у будь-якій пропорції. Більш того, сполуки формули I можуть перебувати у стані рівноваги з альтернативними таутомерними формами. Слід розуміти, що всі таутомерні форми (окремий таутомер або їх суміші), рацемічні суміші та окремі ізомери охоплюються обсягом даного винаходу. Даний винахід також включає прийнятні з погляду сільського господарства солі, які можуть утворювати сполуки формули I з амінами (наприклад, аміаком, диметиламіном та триетиламіном), основами лужного металу та лужно-земельного металу або четвертинними амонієвими основами. Серед гідроксидів, оксидів, алкоксидів і гідрокарбонатів і карбонатів лужних металів і лужноземельних металів, застосовуваних у якості солеутворювачів, особливу увага слід приділити гідроксидам, алкоксидам, оксидам і карбонатам літію, натрію, калію, магнію та кальцію, але особливо гідроксидам, алкоксидам, оксидам і карбонатам натрію, магнію та кальцію. Також можна застосовувати відповідну триметилсульфонієву сіль. Сполуки формули (I) за даним винаходом можна самі по собі застосовувати в якості гербіцидів, але зазвичай їх складають у гербіцидні композиції із застосуванням допоміжних засобів для складання, таких як носії, розчинники та поверхнево-активні речовини (SFA). Таким чином, даний винахід додатково забезпечує гербіцидну композицію, яка містить гербіцидну 2 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 60 сполуку за будь-яким з попередніх пунктів і прийнятний з погляду сільського господарства допоміжний засіб для складання. Композиція може бути представлена у формі концентратів, які розводять перед застосуванням, хоча також можна одержати готові до застосування композиції. Кінцеве розведення зазвичай виконують за допомогою води, але замість води або на додаток до води можна використовувати, наприклад, рідке добриво, мікроелементи, біологічні організми, масло або розчинники. Гербіцидні композиції, як правило, містять від 0,1 до 99 ваг. %, зокрема від 0,1 до 95 ваг. % сполук формули I та від 1 до 99,9 ваг. % допоміжного засобу для складання, який переважно включає від 0 до 25 ваг. % поверхнево-активної речовини. Композиції можна вибрати з ряду типів складів, багато з яких відомі з Manual on Development and Use of FAO Specifications for Plant Protection Products, 5th Edition, 1999. Вони включають порошки, що розпорошуються (DP), розчинні порошки (SP), розчинні у воді гранули (SG), гранули, що диспергуються у воді (WG), порошки, що змочуються (WP), гранули (GR) (з повільним або швидким вивільненням), розчинні концентрати (SL), рідини, що змішуються з маслом (OL), рідини, застосовувані у наднизькому об'ємі (UL), здатні до емульгування концентрати (EC), здатні до диспергування концентрати (DC), емульсії (як "масло у воді" (EW), так і "вода в маслі" (EO)), мікроемульсії (ME), суспензійні концентрати (SC), аерозолі, капсульні суспензії (CS) ісклади для обробки насіння. Вибраний тип складу у будь-якому випадку буде залежати від конкретного передбачуваного призначення та фізичних, хімічних і біологічних властивостей сполуки формули (I). Порошки, що розпорошуються (DP), можна одержувати шляхом змішування сполуки формули (I) з одним або декількома твердими розріджувачами (наприклад, природними глинами, каоліном, пірофілітом, бентонітом, оксидом алюмінію, монтморилонітом, кізельгуром, крейдою, діатомовими землями, фосфатами кальцію, карбонатами кальцію та магнію, сіркою, вапном, мукою, тальком та іншими органічними і неорганічними твердими носіями) і механічного подрібнення суміші в тонкодисперсний порошок. Розчинні порошки (SP) можна одержувати змішуванням сполуки формули (I) з однією або декількома розчинними у воді неорганічними солями (такими як бікарбонат натрію, карбонат натрію або сульфат магнію) або з однією або декількома розчинними у воді органічними твердими речовинами (такими як полісахарид) і необов'язково з одним або декількома змочувальними засобами, одним або декількома диспергувальними засобами або сумішшю зазначених засобів для покращення диспергованості/розчинності у воді. Потім суміш подрібнюють у тонкодисперсний порошок. Подібні композиції також можна гранулювати з утворенням розчинних у воді гранул (SG). Порошки, що змочуються (WP), можна одержувати змішуванням сполуки формули (I) з одним або декількома твердими розріджувачами або носіями, одним або декількома змочувальними засобами та переважно одним або декількома диспергувальними засобами, а також необов'язково з одним або декількома суспендувальними засобами для полегшення дисперсії в рідинах. Потім суміш подрібнюють у тонкодисперсний порошок. Подібні композиції також можна гранулювати з утворенням гранул, що диспергуються у воді (WG). Гранули (GR) можуть бути утворені або гранулюванням суміші сполуки формули (I) та одного або декількох порошкових твердих розріджувачів або носіїв, або з попередньо утворених порожніх гранул за допомогою абсорбції сполуки формули (I) (або її розчину в придатному засобі) пористим матеріалом гранули (таким як пемза, атапульгітова глина, фулерова земля, кізельгур, діатомові землі або подрібнені кукурудзяні качани), або за допомогою адсорбції сполуки формули (I) (або її розчину в придатному засобі) на матеріалі твердого ядра (такому як пісок, силікати, мінеральні карбонати, сульфати або фосфати) і сушіння, за необхідності. Засоби, які зазвичай використовують для абсорбції або адсорбції, включають розчинники (такі як аліфатичні та ароматичні нафтові розчинники, спирти, прості ефіри, кетони та естери) та засоби, що сприяють прилипанню (такі як полівінілацетати, полівінілові спирти, декстрини, цукри та рослинні олії). В гранулах також можуть міститися одна або декілька інших добавок (наприклад, емульгувальний засіб, змочувальний засіб або диспергувальний засіб). Здатні до диспергування концентрати (DC) можна отримати розчиненням сполуки формули (I) у воді або в органічному розчиннику, такому як кетон, спирт або гліколевий ефір. Ці розчини можуть містити поверхнево-активний засіб (наприклад, для покращення розведення водою або запобігання кристалізації в резервуарі обприскувача). Здатні до емульгування концентрати (EC) або емульсії "масло-у-воді" (EW) можна отримувати розчиненням сполуки формули (I) в органічному розчиннику (що необов'язково містить один або декілька змочувальних засобів, один або декілька емульгувальних засобів або суміш зазначених засобів). Придатні органічні розчинники для застосування в EC включають 3 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 60 ароматичні вуглеводні (такі як алкілбензоли або алкілнафталіни, представлені для прикладу SOLVESSO 100, SOLVESSO 150 та SOLVESSO 200; SOLVESSO являє собою зареєстрований знак для товарів і послуг), кетони (такі як циклогексaнон або метилциклогексанон) та спирти (такі як бензиловий спирт, фурфуриловий спирт або бутанол), N-алкілпіролідони (такі як Nметилпіролідон або N-октилпіролідон), диметиламіди жирних кислот (такі як диметиламід C 8C10жирної кислоти) та хлоровані вуглеводні. Продукт EC може довільно емульгуватися при додаванні в воду з утворенням емульсії з достатньою стабільністю, що дозволяє використовувати її для нанесення розпиленням за допомогою відповідного обладнання. Отримання EW включає отримання сполуки формули (I) або у вигляді рідини (якщо вона не є рідиною за кімнатної температури, її можна розплавити за помірної температури, зазвичай нижче 70 °C), або у розчині (шляхом розчинення її у відповідному розчиннику), а потім емульгування отриманої рідини або розчину у воді, що містить один або декілька SFA, при високому зсувному зусиллі з отриманням емульсії. Придатні розчинники для застосування в EW включають рослинні олії, хлоровані вуглеводні (такі як хлорбензоли), ароматичні розчинники (такі як алкілбензоли або алкілнафталіни) та інші відповідні органічні розчинники, які характеризуються низькою розчинністю у воді. Мікроемульсії (ME) можна отримувати змішуванням води із сумішшю одного або декількох розчинників з одним або декількома SFA з довільним утворенням термодинамічно стабільного ізотропного рідкого складу. Сполука формули (I) присутня спочатку або у воді, або у суміші розчинника з SFA. Придатні розчинники для застосування в ME включають ті, що перелічені в даному документі вище для застосування в EC або в EW. ME може бути системою або "маслоу-воді", або "вода-в-маслі" (яка система присутня, можна визначити вимірюванням питомої електричної провідності) та може бути придатною для змішування розчинних у воді та розчинних у маслі пестицидів в цьому ж складі. ME є придатною для розведення водою, при цьому вона або залишається у вигляді мікроемульсії, або утворює звичайну емульсію масло-уводі. Суспензійні концентрати (SC) можуть містити водні або неводні суспензії тонко подрібнених нерозчинних твердих частинок сполуки формули (I). SC можна отримувати розмелюванням на кульовому або бісерному млині твердої сполуки формули (I) в придатному середовищі необов'язково з одним або декількома диспергувальними засобами з отриманням суспензії тонкодисперсних частинок сполуки. В композицію можна включити один або декілька змочувальних засобів, а для зниження швидкості, з якою осідають частинки, можна включити суспендувальний засіб. В якості альтернативи, сполуку формули (I) можна подрібнювати сухою та додавати у воду, що містить засоби, описані вище в даному документі, з отриманням бажаного кінцевого продукту. Аерозольні склади містять сполуку формули (I) і придатний газ-витискувач (наприклад, нбутан). Сполуку формули (I) також можна розчинити або диспергувати у придатному середовищі (наприклад, у воді або у рідині, що змішується з водою, такій як н-пропанол) з отриманням композицій для застосування в насосах, що не перебувають під тиском, для обприскування з ручним управлінням. Капсульні суспензії (CS) можна отримати подібно отриманню складів EW, але з додатковим етапом полімеризації з отриманням водної дисперсії крапель масла, в якій кожна крапля масла інкапсулюється полімерною оболонкою та містить сполуку формули (I) та необов'язково її носій або розріджувач. Полімерну оболонку можна отримати або за допомогою реакції міжфазної поліконденсації, або за допомогою методики коацервації. Композиції можуть забезпечувати контрольоване вивільнення сполуки формули (I), та їх можна застосовувати для обробки насіння. Для забезпечення повільного контрольованого вивільнення сполуки, сполуку формули (I) також можна складати у вигляді біорозкладної полімерної матриці. Композиція може включати одну або кілька добавок для поліпшення біологічної дії композиції, наприклад, шляхом поліпшення змочування, утримання на поверхнях або розподілу по поверхнях; стійкості до змивання дощем з оброблених поверхонь; або поглинання, або рухливості сполуки формули (I). Такі добавки включають поверхнево-активні речовини (SFA), добавки для обприскування на основі масел, наприклад, визначених мінеральних масел або природних рослинних олій (таких як соєва та рапсова олія), та їх суміші з іншими біопідсилювальними допоміжними засобами (інгредієнтами, які можуть сприяти дії або модифікувати дію сполуки формули (I)). Змочувальні засоби, диспергувальні засоби та емульгувальні засоби можуть являти собою SFA катіонного, аніонного, амфотерного або неіоногенного типу. Придатні SFA катіонного типу включають четвертинні амонійні сполуки (наприклад, цетилтриметиламонію бромід), імідазоліни та солі амінів. 4 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 60 Придатні аніонні SFA включають солі лужних металів жирних кислот, солі аліфатичних моноефірів сірчаної кислоти (наприклад, лаурилсульфат натрію), солі сульфонованих ароматичних сполук (наприклад, додецилбензолсульфонат натрію, додецилбензолсульфонат кальцію, бутилнафталін сульфонат та суміші діізопропіл- та триізопропілнафталінсульфонатів натрію), сульфати простих ефірів, сульфати ефірів спиртів (наприклад, лаурет-3-сульфат натрію), карбоксилати простих ефірів (наприклад, лаурет-3-карбоксилат натрію), естери фосфорної кислоти (продукти реакції між одним або декількома жирними спиртами та фосфорною кислотою (переважно моноестери) або пентаоксидом фосфору (переважно діестери), наприклад, при реакції між лауриловим спиртом та тетрафосфорною кислотою; додатково ці продукти можуть бути етоксильовані), сульфосукцинамати, парафін- або олефінсульфонати, таурати та лігносульфонати. Придатні SFA амфотерного типу включають бетаїни, пропіонати та гліцинати. Придатні SFA неіонного типу включають продукти конденсації алкіленоксидів, таких як етиленоксид, пропіленоксид, бутиленоксид або їх суміші, з жирними спиртами (такими як олеїловий спирт або цетиловий спирт) або з алкілфенолами (такими як октилфенол, нонілфенол або октилкрезол); неповні ефіри, отримані із довголанцюгових жирних кислот або ангідридів гекситолу; продукти конденсації зазначених неповних ефірів з етиленоксидом; блокполімери (що містять етиленоксид та пропіленоксид); алканоламіди; естери (наприклад, поліетиленгліколеві естери жирної кислоти); аміноксиди (наприклад, лаурилдиметиламіну оксид) та лецитини. Придатні суспендуючі засоби включають гідрофільні колоїди (такі як полісахариди, полівінілпіролідон або карбоксиметилцелюлоза натрію) та глини, що набухають (такі як бентоніт або атапульгіт). Композиція за даним винаходом може додатково містити щонайменше один додатковий пестицид. Наприклад, сполуки за даним винаходом також можна застосовувати в комбінації з іншими гербіцидами або регуляторами росту рослин. В переважному варіанті здійснення додатковим пестицидом є гербіцид та/або антидот гербіциду. Прикладами таких сумішей (в яких "I" представляє сполуку формули I) є: I + ацетохлор, I + ацифлуорфен, I + ацифлуорфен-натрій, I + аклоніфен, I + акролеїн, I + алахлор, I + алоксидим, I + аметрин, I + амікарбазон, I + амідосульфурон, I + амінопіралід, I + амітрол, I + анілофос, I + асулам, I + атразин, I + азафенідин, I + азимсульфурон, I+BCPC, I + бефлубутамід, I + беназолін, I + бенкарбазон, I + бенфлуралін, I + бенфуресат, I + бенсульфурон, I + бенсульфурон-метил, I + бенсулід, I + бентазон, I + бензфендизон, I + бензобіциклон, I + бензофенап, I + біциклопірон, I + біфенокс, I + біланафос, I + біспірибак, I + біспірибак-натрій, I + бура, I + бромацил, I + бромобутид, I + бромоксиніл, I + бутахлор, I + бутаміфос, I + бутралін, I + бутроксидим, I + бутилат, I + какодилова кислота, I + хлорат кальцію, I + кафенстрол, I + карбетамід, I + карфентразон, I + карфентразон-етил, I + хлорфлуренол, I + хлорфлуренол-метил, I + хлоридазон, I + хлоримурон, I + хлоримурон-етил, I + хлороцтова кислота, I + хлоротолурон, I + хлорпрофам, I + хлорсульфурон, I + хлортал, I + хлортал-диметил, I + цинідон-етил, I + цинметилін, I + циносульфурон, I + цисанілід, I + клетодим, I + клодинафоп, I + клодинафоп-пропаргіл, I + кломазон, I + кломепроп, I + клопіралід, I + клорансулам, I + клорансулам-метил, I + ціаназин, I + циклоат, I + циклосульфамурон, I + циклоксидим, I + цигалофоп, I + цигалофоп-бутил, I+2,4-D, I + даїмурон, I + далапон, I + дазомет, I+2,4-DB, I+I + десмедифам, I + дикамба, I + дихлобеніл, I + дихлорпроп, I + дихлорпроп-P, I + диклофоп, I + диклофоп-метил, I + диклосулам, I + дифензокват, I + дифензокват метилсульфат, I + дифлуфенікан, I + дифлуфензопір, I + димефурон, I + димепіперат, I + диметахлор, I + диметаметрин, I + диметенамід, I + диметенамід-P, I + диметипін, I + какодилова кислота, I + динітрамін, I + динотерб, I + дифенамід, I + дипропетрин, I + дикват, I + дикват дибромід, I + дитіопір, I + діурон, I + ендотал, I+EPTC, I + еспрокарб, I + еталфлуралін, I + етаметсульфурон, I + етаметсульфурон-метил, I + етефон, I + етофумезат, I + етоксифен, I + етоксисульфурон, I + етобензанід, I + феноксапроп-P, I + феноксапроп-P-етил, I + фентразамід, I + сульфат заліза, I + флампроп-M, I + флазасульфурон, I + флорасулам, I + флуазифоп, I + флуазифоп-бутил, I + флуазифоп-P, I + флуазифоп-P-бутил, I + флуазолат, I + флукарбазон, I + флукарбазон-натрій, I + флусетосульфурон, I + флухлоралін, I + флуфенацет, I + флуфенпір, I + флуфенпір-етил, I + флуметралін, I + флуметсулам, I + флуміклорак, I + флуміклорак-пентил, I + флуміоксазин, I + флуміпропін, I + флуометурон, I + флуороглікофен, I + флуороглікофен-етил, I + флуоксапроп, I + флупоксам, I + флупропацил, I + флупропанат, I + флупірсульфурон, I + флупірсульфуронметил-натрій, I + флуренол, I + флуридон, I + флурохлоридон, I + флуроксипір, I + флуртамон, I + флутіацет, I + флутіацет-метил, I + фомесафен, I + форамсульфурон, I + фосамін, I + глуфосинат, I + глуфосинат-амоній, I + гліфосат, I + галоксифен, I + галосульфурон, I + 5 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 галосульфурон-метил, I + галоксифоп, I + галоксифоп-P, I + гексазинон, I + імазаметабенз, I + імазаметабенз-метил, I + імазамокс, I + імазапік, I + імазапір, I + імазаквін, I + імазетапір, I + імазосульфурон, I + інданофан, I + індазифлам, I + йодметан, I + іодосульфурон, I + іодосульфурон-метил-натрій, I + іоксиніл, I + ізопротурон, I + ізоурон, I + ізоксабен, I + ізоксахлортол, I + ізоксафлутол, I + ізоксапірифоп, I + карбутилат, I + лактофен, I + ленацил, I + лінурон, I + мекопроп, I + мекопроп-P, I + мефенацет, I + мефлуїдид, I + мезосульфурон, I + мезосульфурон-метил, I + мезотрион, I + метам, I + метаміфоп, I + метамітрон, I + метазахлор, I + метабензтіазурон, I + метазол, I + метиларсонова кислота, I + метилдимрон, I + метилізотіоціанат, I + метолахлор, I+S-метолахлор, I + метосулам, I + метоксурон, I + метрибузин, I + метсульфурон, I + метсульфурон-метил, I + молінат, I + монолінурон, I + напроанілід, I + напропамід, I + напталам, I + небурон, I + нікосульфурон, I + н-метилгліфосат, I + нонанова кислота, I + норфлуразон, I + олеїнова кислота (жирні кислоти), I + орбенкарб, I + ортосульфамурон, I + оризалін, I + оксадіаргіл, I + оксадіазон, I + оксасульфурон, I + оксазикломефон, I + оксифлуорфен, I + паракват, I + паракват дихлорид, I + пебулат, I + пендиметалін, I + пеноксулам, I + пентахлорфенол, I + пентанохлор, I + пентоксазон, I + петоксамід, I + фенмедифам, I + піхлорам, I + піколінафен, I + піноксаден, I + піперофос, I + претилахлор, I + примісульфурон, I + примісульфурон-метил, I + продіамін, I + профоксидим, I + прогексадіон-кальцій, I + прометон, I + прометрин, I + пропахлор, I + пропаніл, I + пропаквізафоп, I + пропазин, I + профам, I + пропізохлор, I + пропоксикарбазон, I + пропоксикарбазон-натрій, I + пропізамід, I + просульфокарб, I + просульфурон, I + піраклоніл, I + пірафлуфен, I + пірафлуфен-етил, I + пірасульфотол, I + піразолінат, I + піразосульфурон, I + піразосульфурон-етил, I + піразоксифен, I + пірибензоксим, I + пірибутикарб, I + піридафол, I + піридат, I + пірифталід, I + піримінобак, I + піримінобак-метил, I + піримісульфан, I + піритіобак, I + піритіобак-натрій, I + піроксасульфон, I + піроксулам, I + квінклорак, I + квінмерак, I + квінокламін, I + квізалофоп, I + квізалофоп-P, I + римсульфурон, I + сафлуфенацил, I + сетоксидим, I + сидурон, I + симазин, I + симетрин, I + хлорат натрію, I + сулькотрион, I + сульфентразон, I + сульфометурон, I + сульфометурон-метил, I + сульфосат, I + сульфосульфурон, I + сірчана кислота, I + тебутіурон, I + тефурилтрион, I + темботрион, I + тепралоксидим, I + тербацил, I + тербуметон, I + тербутилазин, I + тербутрин, I + тенілхлор, I + тіазопір, I + тифенсульфурон, I + тієнкарбазон, I + тифенсульфурон-метил, I + тіобенкарб, I + топрамезон, I + тралкоксидим, I + триалат, I + триасульфурон, I + триазифлам, I + трибенурон, I + трибенурон-метил, I + трихлопір, I + триетазин, I + трифлоксисульфурон, I + трифлоксисульфурон-натрій, I + трифлуралін, I + трифлусульфурон, I + трифлусульфуронметил, I + триокситриазин, I + тринексапак-етил, I + тритосульфурон, I + складний етиловий ефір [3-[2-хлор-4-фтор-5-(1-метил-6-трифторметил-2,4-діоксо-1,2,3,4-тетрагідропіримідин-3іл)фенокси]-2-піридилоксі]оцтової кислоти (CAS RN 353292-31-6). Сполуки за даним винаходом можна також комбінувати з гербіцидними сполуками, розкритими у WO06/024820 та/або WO07/096576. Компоненти, змішувані зі сполукою формули I, можуть також перебувати у формі естерів або солей, які згадані, наприклад, в The Pesticide Manual, Fourteenth Edition, British Crop Protection Council, 2006. Сполуку формули I також можна застосовувати в сумішах з іншими агрохімічними засобами, такими як фунгіциди, нематоциди або інсектициди, приклади яких наведені в The Pesticide Manual. Співвідношення в суміші сполуки формули I та змішуваного компонента переважно складає від 1:100 до 1000:1. Суміші переважно можна застосовувати в згаданих вище складах (у цьому випадку вираз "активний інгредієнт" відноситься до відповідної суміші сполуки формули I зі змішуваним компонентом). Сполуки формули I відповідно до даного винаходу можна також застосовувати в комбінації з одним або декількома антидотами. Аналогічно, суміші сполуки формули I відповідно до даного винаходу з одним або декількома додатковими гербіцидами також можна застосовувати в комбінації з одним або декількома антидотами. Антидотами можуть бути AD 67 (MON 4660), беноксакор, клоквінтосет-мексил, ципросульфамід (CAS RN 221667-31-8), дихлормід, фенхлоразол-етил, фенклорим, флуксофенім, фурилазол і відповідний R-ізомер, ізоксадифенетил, мефенпір-діетил, оксабетриніл, N-ізопропіл-4-(2-метоксибензоїлсульфамоїл)бензамід (CAS RN 221668-34-4). Інші можливі варіанти включають сполуки-антидоти, розкриті, наприклад, в EP0365484, наприклад, N-(2-метоксибензоїл)-4[(метиламінокарбоніл)аміно]бензолсульфонамід. Особливо переважними є суміші сполуки 6 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 формули I з ципросульфамідом, ізоксадифен-етилом, клоквінтосет-мексилом та/або N-(2метоксибензоїл)-4-[(метил-амінокарбоніл)аміно]бензолсульфонамідом. Антидоти сполуки формули I також можуть перебувати у формі естерів або солей, як th згадується, наприклад, в The Pesticide Manual, 14 Edition (BCPC), 2006. Посилання на клоквінтосет-мексил також відноситься до його літієвої, натрієвої, калієвої, кальцієвої, магнієвої, алюмінієвої, залізної, амонієвої, четвертинної амонієвої, сульфонієвої або фосфонієвої солі, як розкрито у WO 02/34048, а посилання на фенхлоразол-етил також відноситься до фенхлоразолу тощо. Переважно співвідношення в суміші сполуки формули I та антидоту становить від 100:1 до 1:10, зокрема, від 20:1 до 1:1. Суміші можна переважно застосовувати у вищезгаданих складах (у цьому випадку вираз "активний інгредієнт" відноситься до відповідної суміші сполуки формули I з антидотом). Даний винахід, крім того, додатково забезпечує спосіб вибіркової боротьби з бур'янами у місці зростання культурних рослин та бур'янів, при цьому спосіб включає застосування відносно місця зростання достатньої для боротьби з бур'янами кількості композиції за даним винаходом. "Боротьба" означає знищення, зменшення або сповільнення росту, або попередження, або зниження проростання. Зазвичай рослинами, з якими необхідно боротися, є небажані рослини (бур'яни). "Місце зростання" означає територію, на якій рослини зростають або будуть зростати. Норми внесення сполук формули I можуть варіювати в широких межах та залежать від властивостей ґрунту, способу внесення (до або після появи сходів; протравляння насіння; внесення по відношенню до борозни для насіння; внесення безорною обробкою тощо), культурної рослини, бур'яну(бур'янів), з яким(и) необхідно боротися, переважних кліматичних умов та інших факторів, за якими регулюють спосіб внесення, час внесення та цільову культуру. Сполуки формули I за даним винаходом зазвичай вносять з нормою від 10 до 2000 г/га, зокрема, від 50 до 1000 г/га. Внесення зазвичай здійснюють шляхом розпилення композиції, як правило, за допомогою установленого на тракторі розпилювача для великих територій, але також можна застосовувати інші способи, такі як обпилювання (для порошків), краплинне поливання або зрошення. Придатні рослини, для яких можна застосовувати композицію за даним винаходом, включають сільськогосподарські культури, такі як зернові, наприклад, ячмінь і пшеницю, бавовник, олійний рапс, соняшник, маїс, рис, сою, цукровий буряк, цукрова тростина і дерновий покрив. Культурні рослини можуть також включати дерева, такі як плодові дерева, пальми, кокосові пальми або інші горіхи. Також включені кручені рослини, такі як виноград, плодові чагарники, фруктові рослини та овочі. Сільськогосподарські культури також слід розуміти як ті, що охоплюють такі сільськогосподарські культури, яким була надана толерантність до гербіцидів або класів гербіцидів (наприклад, ALS-, GS-, EPSPS-, PPO-, ACCаза- та HPPD-інгібітори) за допомогою традиційних способів селекції або за допомогою генної інженерії. Прикладом сільськогосподарської культури, якій була надана толерантність до імідазолінонів, наприклад, до імазамоксу, за допомогою загальноприйнятих способів селекції, є капуста польова Clearfield® (канола). Приклади сільськогосподарських культур, яким була надана толерантність до гербіцидів із застосуванням способів генної інженерії, включають, наприклад, стійкі до гліфосату та глюфосинату сорти маїсу, комерційно доступні під торговими назвами RoundupReady® та LibertyLink®. В особливо переважному аспекті сільськогосподарську культуру модифікували методиками генної інженерії для надекспресії гомогентизат соланезилтрансферази, як зазначено в, наприклад, WO2010/029311. Під сільськогосподарськими культурами також слід розуміти такі, яким була надана стійкість до шкідливих комах за допомогою способів генної інженерії, наприклад, маїс Bt (стійкий до метелика кукурудзяного), бавовник Bt (стійкий до довгоносика бавовняного), а також різновиди картоплі Bt (стійкі до колорадського жука). Прикладами маїсу Bt є гібриди маїсу Bt 176 NK® (Syngenta Seeds). Токсин Bt являє собою білок, який в природі продукується ґрунтовою бактерією Bacillus thuringiensis. Приклади токсинів або трансгенних рослин, здатних синтезувати такі токсини, описані в EP-A-451878, EP-A-374753, WO 93/07278, WO 95/34656, WO 03/052073 і EP-A-427529. Прикладами трансгенних рослин, що містять один або декілька генів, що кодують стійкість до інсектицидів та експресують один або декілька токсинів, є KnockOut (маїс), Yield Gard (маїс), NuCOTIN33B (бавовник), Bollgard (бавовник), NewLeaf (різновиди картоплі), NatureGard та Protexcta. Рослинні культури або їх насіннєвий матеріал можуть бути як стійкими до гербіцидів так і, в той же час, стійкими до поїдання комахами (трансгенні об'єкти з 7 UA 112890 C2 5 10 15 20 25 "пакетованими генами"). Наприклад, насінина може мати здатність експресувати інсектицидний білок Cry3, в той же час будучи толерантною до гліфосату. Сільськогосподарські культури також слід розуміти, як культури, які отримані традиційними способами селекції або генної інженерії та характеризуються так званими привнесеними ознаками (наприклад, покращеною стабільністю під час зберігання, більш високою поживною цінністю та покращеним смаком). Інші придатні рослини включають газонну траву, наприклад, на гольф-майданчиках, лужках, у парках і на узбіччях дороги або комерційно вирощувану для газону, і декоративні рослини, такі як квіти або чагарники. Композиції можна застосовувати для боротьби з небажаними рослинами (збірно, "бур'янами"). Бур'яни, з якими необхідно боротися, можуть являти собою як види однодольних рослин, наприклад, Agrostis, Alopecurus, Avena, Brachiaria, Bromus, Cenchrus, Cyperus, Digitaria, Echinochloa, Eleusine, Lolium, Monochoria, Rottboellia, Sagittaria, Scirpus, Setaria та Sorghum, так і види дводольних рослин, наприклад, Abutilon, Amaranthus, Ambrosia, Chenopodium, Chrysanthemum, Conyza, Galium, Ipomoea, Nasturtium, Sida, Sinapis, Solanum, Stellaria, Veronica, Viola та Xanthium. Бур'яни також можуть охоплювати рослини, які можна вважати культурними рослинами, але які виростають за межами посівної площі ("утікачі"), або які виростають із насіння, що залишилося від попереднього посіву іншої сільськогосподарської культури ("рослини-самосіви"). Такі рослини-самосіви або втікачі можуть бути толерантними до деяких інших гербіцидів. Сполуки за даним винаходом можна отримати за допомогою наведеної далі схеми(схем). Певні сполуки за даним винаходом можна отримати зі сполук формули (1a) шляхом нагрівання з морфоліном (Nagashima, Hiromu et al. Heterocycles, 26(1), 1-4; 1987), як показано на схемі реакції 1. Схема реакції 1 R3 R3 (1a) Сполуки формули (1а) можна отримати зі сполук формули (2), як показано на схемі реакції 2. Схема реакції 2 30 35 Сполуки формули (1a) можна отримати шляхом реакції піридазинонів (2) з відповідною біциклічною злитою гетероароматичною функціональною групою в присутності сильної основи, такої як NaH або NaHMDS. Придатними розчинниками є THF або DMF. 1 2 Сполуку (2), де R =Me та R =H, можна отримати шляхом реакції комерційно доступного 4,5дихлор-2-метил-3(2H)-піридазинону з NaOMe в 1,4-діоксані згідно з Tetrahedron 2001, 57, 13231330. 1 2 Сполуку (2), де R =Me та R =Me, можна отримати як показано на схемі реакції 3. Схема реакції 3 8 UA 112890 C2 В якості альтернативи, певні сполуки за даним винаходом можна отримати згідно зі схемою реакції 4. Схема реакції 4 5 Сполуки за даним винаходом можна отримати із сполук формули (3) шляхом нагрівання з концентрованим водним NaOH в придатному розчиннику. Сполуки формули (3) можна отримати як показано на схемі реакції 5. Схема реакції 5 9 UA 112890 C2 5 Сполуки формули (3) можна отримати шляхом реакції сполук (4) з 2 або більше еквівалентами відповідної біциклічної злитої гетероароматичної функціональної групи в присутності сильної основи та придатного розчинника. Прикладами придатних основ є NaH, NaHMDS та Cs2CO3. Прикладами придатних розчинників є THF та DMF. Прикладом сполук (4) є комерційно доступний 4,5-дихлор-2-метил-3(2H)-піридазинон. Варіант, що використовується для отримання певних сполук за даним винаходом, включає моно- або дихлорування сполук (1b), як показано на схемі реакції 6. Схема реакції 6 R3 R3 SO2Cl2 DCM (1b) 10 Певні сполуки формули (1а) можна отримати шляхом монобромування монохлорпохідних сполук, як показано на схемі реакції 7. Схема реакції 7 R3 R3 NBS DCM 15 Певні сполуки формули (1а) можна отримати шляхом трихлорування сполук (1b), як показано на схемі реакції 8. Схема реакції 8 10 UA 112890 C2 R3 R3 SO2Cl2 DCM (1b) Певні сполуки формули (1a) можна отримати шляхом монобромування сполук (1b), як показано на схемі реакції 9. Схема реакції 9 R3 R3 NBS DCM 5 (1b) Певні сполуки формули (1а) можна отримати шляхом монохлорування монобромпохідних сполук, як показано на схемі реакції 10. Схема реакції 10 R3 R3 SO2Cl2 DCM 10 Певні сполуки формули (1а) можна отримати шляхом ди- та трибромування сполук (1b), як показано на схемі реакції 11. Схема реакції 11 R3 R3 R3 NBS DCM (1b) 15 20 Певні сполуки формули (1a) можна отримати шляхом реакції сполуки, що містить бром, з придатним засобом, що бере участь в реакції поєднання, використовуючи придатний каталізатор/ліганд, основу та розчинник, як показано на схемі реакції 12. Прикладами придатних каталізаторів/лігандів є Pd2dba3/XantPhos, [Pd(аліл)Cl]2/RockPhos або предкаталізатор tBuXPhos. Прикладами придатних основ є DIPEA, LiHMDS або Cs2CO3. Прикладами придатних розчинників є 1,4-діоксан, THF, DMF або толуол. Схема реакції 12 11 UA 112890 C2 5 10 Певні сполуки формули (1a) можна отримати шляхом реакції сполуки, що містить бром, з придатним борорганічним засобом, що бере участь в реакції поєднання, використовуючи придатний каталізатор/ліганд, основу та розчинник, як показано на схемі реакції 13. Прикладами придатних борорганічних засобів, що беруть участь у реакції поєднання, є боронові кислоти, складні боронові ефіри та солі трифторборату калію. Прикладами придатного каталізатора/лігандів є Pd(OAc)2/RuPhos або Pd-dppf. Прикладом придатної основи є CsF. Прикладами придатних розчинників є 1,4-діоксан, вода або DME. Схема реакції 13 Придатні солі трифторборату калію є комерційно доступними або можуть бути отримані шляхом реакції трифторетанолу з (бромметил)трифторборатом калію, які є комерційно доступними, як показано на схемі реакції 14. Схема реакції 14 NaH THF 15 20 Певні сполуки метилсульфіду можна отримати шляхом перехресного поєднання NaSMe зі сполукою, що містить бром, як показано на схемі реакції 15. Схема реакції 15 Певні сполуки формули (1a) можна отримати шляхом окиснення сірки, як показано на схемі реакції 16, (n=1 або 2). 12 UA 112890 C2 Схема реакції 16 R3 R3 mCPBA DCM 5 Певні сполуки формули (1а) можна отримати шляхом відновлення сполуки, що містить ізопропеніл, як показано на схемі реакції 17. Схема реакції 17 10 Певні сполуки формули (1a) можна отримати шляхом утворення нітрилу, як показано на схемі реакції 18. (Необхідний вихідний матеріал, що містить альдегід, як правило, отримують згідно зі схемою реакції 21). Схема реакції 18 R3 R3 NH3/H2O I2 THF Певні сполуки за даним винаходом можна отримати згідно зі схемою реакції 19. Схема реакції 19 15 20 З посиланням на схему реакції 19, певні сполуки за даним винаходом можна отримати шляхом завершального етапу отримання похідного діону. Субстрат, що містить діон, вступає в реакцію з 1 або декількома еквівалентами відповідних електрофільних сполук R-X в присутності NEt3 та придатного розчинника при температурі від 0 °C до дефлегмування. Прикладами придатних розчинників є DCM та THF. Прикладами придатних комерційно доступних електрофільних сполук R-X є хлорангідриди, хлорформіати, сульфонілхлориди, амінокарбонілхлориди, алкілгалогеніди, S-алкілхлортіоформіати. Певні сполуки формули (1a) можна отримати шляхом монохлорування або монобромування проміжних сполук індолу, заміщених в 2-положенні індолу, як показано на схемі реакції 20. Схема реакції 20 13 UA 112890 C2 Певні сполуки формули (1a) можна отримати шляхом озонолізу алкенів, як показано на схемі реакції 21. Схема реакції 21 5 10 15 Певні сполуки формули (1a) можна отримати шляхом дифторування карбонільних сполук, як показано на схемі реакції 22. Карбонільна сполука вступає в реакцію з 2 або більше еквівалентами трифториду діетиламіносірки (DAST) в придатному розчиннику при від -78 °C до 25 °C. Прикладами придатних розчинників є дихлорметан та хлороформ. (Вихідний матеріал на основі карбонільної сполуки, як правило, отримують згідно зі схемою реакції 21). Схема реакції 22 Певні сполуки формули (1a) можна отримати шляхом відновлення карбонільних сполук, як показано на схемі реакції 23. Субстрат на основі карбонільної сполуки вступає в реакцію з 0,5 або декількома еквівалентами борогідриду натрію в придатному розчиннику при від -78 °C до 25 °C. Прикладами придатних розчинників є метанол та етанол. Схема реакції 23 14 UA 112890 C2 5 10 15 20 25 30 35 Певні сполуки формули (1a) можна отримати шляхом метилювання спиртів, як показано на схемі реакції 24. Вихідний матеріал на основі спирту вступає в реакцію з 1 або декількома еквівалентами йодметану в присутності придатної основи в придатному розчиннику при від 78 °C до 25 °C. Прикладом придатної основи є гідрид натрію. Прикладами придатних розчинників є N, N-диметилформамід та тетрагідрофуран. (Спиртовий субстрат, як правило, отримують згідно зі схемою реакції 23) Схема реакції 24 Певні сполуки формули (1a) можна отримати шляхом фторування спиртів, як показано на схемі реакції 25. Вихідний спиртовий матеріал вступає в реакцію з 1 або декількома еквівалентами трифториду діетиламіносірки (DAST) в придатному розчиннику при від -78 °C до 25 °C. Прикладами придатних розчинників є дихлорметан та хлороформ. Схема реакції 25 Приклади Приклад 1. 4-(3-Хлор-індол-1-іл)-2-метил-2H-піридазин-3,5-діон Суміш 4-(3-хлор-індол-1-іл)-5-метокси-2-метил-2H-піридазин-3-ону (1,70 г, 5,87 ммоля) і морфоліну (8 мл) нагрівали до 140 °C в умовах мікрохвильового випромінювання протягом10 хв. Суміші дозволяли охолонути, а потім випарювали при пониженому тиску для видалення більшої частини морфоліну. Залишок перемішували 1:1 об'єм/об'єм крижаною AcOH: DCM (100 мл) з отриманням напівтвердої речовини, що вільно тече. Легковипарні речовини видаляли invacuo, а отриману тверду речовину суспендували у воді. Тверду речовину добували шляхом фільтрації при пониженому тиску та висушували при 1 мбар та 60 °C з отриманням титульної 1 сполуки у вигляді бежевої твердої речовини, 1,54 г, вихід 95 %. H ЯМР (DMSO-d6) δ (ppm) 7,89 (1H, s), 7,57-7,50 (2H, m), 7,24-7,17 (2H, m), 7,12-7,06 (1H, m), 3,66 (3H, s) (Деякі інші сполуки за даним винаходом згідно зі схемою реакції 1 можуть окремо потребувати модифікованої процедури очищення, такої як використання колонкової хроматографії на силікагелі, препаративної HPLC або кристалізації). 4-(3-Хлор-індол-1-іл)-5-метокси-2-метил-2H-піридазин-3-он Гідрид натрію (60 % за вагою в мінеральному маслі, 874 мг, 21,9 ммоля) суспендували в сухому DMF (10 мл) в атмосфері N2. При перемішуванні протягом 20 хвилин додавали розчин 3хлоріндолу (3,01 г, 19,9 ммоля) в DMF (30 мл). Під час додавання застосовували охолодження шляхом водяної бані при температурі навколишнього середовища. Спостерігали газоутворення та суміш перемішували протягом 30 хв. Реакційну суміш додатково розбавляли DMF (20 мл). Протягом 5 хвилин додавали розчин 5хлор-4-метокси-2-метил-2H-піридазин-3-ону (3,47 г, 19,9 ммоля) в DMF (30 мл). Далі суміш перемішували протягом ще 3 годин при температурі навколишнього середовища перед охолодженням на крижаній бані та гасили насиченим водним KH 2PO4 (100 мл). Суміш екстрагували в EtOAc (3 × 150 мл) та об'єднані органічні екстракти сушили над MgSO4. 15 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 60 Випарювали in vacuo до отримання неочищеного осаду, який очищували за допомогою флешхроматографії (силікагель, елюент 0–100 % EtOAc в градієнті ізогексану). Титульну сполуку 1 отримували у вигляді пофарбованої в бежевий твердої речовини, 3,41 г, вихід 59 %. H ЯМР (CDCl3) δ (ppm) 7,92 (1H, s), 7,62-7,67 (1H, m), 7,20-7,28 (3H, m), 6,96-7,01 (1H, m), 3,86 (3H, s), 3,85 (3H, s). Приклад 2. 4-(3-Хлоріндазол-1-іл)-2-метил-піридазин-3,5-діон Суміш 32 % NaOH:вода 1:1, вага/вага (усього 8 г) додавали до 4,5-біс(3-хлоріндазол-1-іл)-2метил-піридазин-3-ону (768 мг, 1,87 ммоля) в метанолі (30 мл), а потім суміш нагрівали при 80 °C протягом 20 хвилин. Суміші дозволяли охолонути до кімнатної температури, а потім концентрували in vacuo. До залишку додавали дихлорметан (50 мл) та воду (50 мл) та видаляли органічний шар. Водний шар підкислювали до pH 1 конц. HCl, а потім екстрагували дихлорметаном (40 мл x 2). Об'єднані органічні екстракти пропускали через фільтр для розділення фаз та концентрували in vacuo з отриманням титульної сполуки у вигляді твердої 1 білої речовини (490 мг). H ЯМР (DMSO-d6) δ (ppm) 7,93 (1H, s), 7,71-7,79 (1H, m), 7,45-7,54 (1H, m), 7,26-7,38 (2H, m), 3,66 (3 H, s). Деякі інші аналогічно отримані продукти на основі діону подрібнювали з етилацетатом або ефіром. 4,5-Біс(3-хлоріндазол-1-іл)-2-метил-піридазин-3-он Суміш 4,5-дихлор-2-метил-піридазин-3-ону (551 мг, 3,08 ммоля), 3-хлор-1H-індазолу (1,17 г, 7,70 ммоля) та карбонату цезію (1,48 г, 7,70 ммоля) в DMF (15 мл) нагрівали до 110 °C протягом 1 год. Реакційну суміш охолоджували, а потім концентрували in vacuo. Реакційну суміш розбавляли етилацетатом (50 мл) та промивали водою (50 мл) та сольовим розчином (50 мл x 2). Органічний екстракт висушували над сульфатом магнію, фільтрували та концентрували in vacuo. Неочищений продукт очищали за допомогою хроматографії на силікагелі з елююванням 0-95 % етилацетатом в ізогексані з отриманням продукту у вигляді світло-оранжевого масла 1 (940 мг). H ЯМР (CDCl3) δ (ppm) 8,36 (1H, s), 7,45-7,62 (2H, m), 7,34 (1H, ddd), 7,08-7,20 (3H, m), 7,04 (1 H, ddd) 6,68 (1 H, d) 3,97 (3 H, s). Приклад процедури згідно зі схемою реакції 6 – дихлорування 4-(2,3-Дихлоріндол-1-іл)-5-метокси-2,6-диметил-піридазин-3-он До перемішуваного розчину 4-індол-1-іл-5-метокси-2,6-диметил-піридазин-3-ону (175 мг, 0,650 ммоля) в дихлорметані (4 мл) за RT додавали сульфурилхлорид (116 мкл, 1,43 ммоля). Реакційна суміш ставала світло-коричневою. Після перемішування протягом 1 години охолоджували реакційну суміш до 0 °C, а потім додавали по краплях насичений водний NaHCO3 (5 мл). Колір змінювався на світло-жовтий та перемішування продовжували протягом 10 хв. Потім суміш виливали в дихлорметан (20 мл) та воду (20 мл) і розділяли шари. Водний шар повторно екстрагували дихлорметаном (20 мл x 2) та об'єднані речовини висушували (MgSO4), та концентрували при пониженому тиску на силікагелі. За допомогою флеш-хроматографії (combiflash, 10 % EtOAc/ізогексан на колонці GOLD) отримували необхідний продукт 4-(2,3дихлоріндол-1-іл)-5-метокси-2,6-диметил-піридазин-3-он (150 мг, 0,444 ммоля, 68 %) у вигляді світло-жовтої твердої речовини. 1 H ЯМР (CDCl3) δ (ppm) 7,60 (1H, m), 7,27 – 7,24 (2H, m), 6,98 (1H, m), 3,74 (3H, s), 3,46 (3H, s), 2,35 (3H, s). Отримання 5-хлор-4-метокси-2,6-диметил-піридазин-3-ону згідно зі схемою реакції 3 5-Хлор-4-метокси-2,6-диметил-піридазин-3-он 4,5-дихлор-1H-піридазин-6-он (1,95 г, 11,8 ммоля) та бром (0,73 мл, 14,2 ммоля) суспендували у воді (10 мл) та нагрівали суміш в умовах мікрохвильового випромінювання до 180 °C протягом 30 хв. Отриману реакційну суміш фільтрували та отриману неочищену тверду речовину ретельно промивали водою, а потім DCM з отриманням 3-бром-4,5-дихлор-1Hпіридазин-6-ону, 2,06 г, у вигляді білої твердої речовини (вихід 71,5 %). 1 H ЯМР (DMSO-d6) δ ppm=13,88 (1H, br. s) До перемішуваного розчину 3-бром-4,5-дихлор-1H-піридазин-6-ону (12,5 г, 51,3 ммоля) в DMF (75,0 мл) додавали K2CO3 (10,7 г, 76,9 ммоля) та йодметан (10,9 г, 76,9 ммоля, 4,79 мл). Отриману суміш перемішували при температурі навколишнього середовища протягом 18 год. Потім реакційну суміш виливали в крижану воду (300 мл) та суміш перемішували протягом 2 год. Збирали отриманий осад шляхом фільтрації, а потім сушили з отриманням 6-бром-4,5дихлор-2-метил-піридазин-3-ону (10,7 г) у вигляді твердої бежевої речовини (вихід 77 %). 1 H ЯМР (CDCl3) δ ppm=3,83 (3H, s) 6-Бром-4,5-дихлор-2-метил-піридазин-3-он (1,5 г, 5,8 ммоля) розчиняли в 1,4-діоксані (150 мл). Метилат натрію (1,5 мл, 25 % за вагою метаноловий розчин, 6,4 ммоля) додавали по краплях та реакційну суміш перемішували протягом 2 год. Суміш концентрували до об'єму 50 мл, а потім розбавляли 50 мл EtOAc. Її промивали водним насиченим сольовим розчином 2 × 35 16 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 мл. Органічний шар ретельно висушували над сульфатом натрію, фільтрували та концентрували in vacuo. Отриманий таким чином неочищений залишок очищали за допомогою флеш-хроматографії (силікагель, елюент 0-10 % EtOAc в градієнті ізогексану) з отриманням 6бром-5-хлор-4-метокси-2-метил-піридазин-3-ону (960 мг) у вигляді твердої білої речовини (вихід 65 %). 1 H ЯМР (CDCl3) δ ppm=3,75 (3H, s) 4,32 (3 H, s) 6-Бром-5-хлор-4-метокси-2-метил-піридазин-3-он (500 мг, 1,68 ммоля, чистота 85 % за вагою), CsF (509 мг, 3,353 ммоля), триметилбороксин (242 мг, 1,93 ммоля) та аддукт дихлор[1,1'-біс(дифенілфосфіно)фероцен]паладію (II) та дихлорметану (140 мг, 0,168 ммоля) розчиняли в 1,2-диметоксіетані (5 мл) в атмосфері N2. Суміш нагрівали в умовах мікрохвильового випромінювання до 145 °C протягом 30 хв. Отриману суміш фільтрували через целіт, промиваючи за допомогою EtOAc. Розчин промивали водним насиченим сольовим розчином 2 × 25,0 мл. Органічний шар відділяли, висушували над Na2SO4, фільтрували та концентрували in vacuo. Неочищений залишок очищували за допомогою флеш-хроматографії (силікагель, елюент 0–20 % EtOAc в градієнті ізогексану). Титульну сполуку 5-хлор-4-метокси-2,6-диметил-піридазин-3-он отримували у вигляді світло-жовтої твердої речовини (212 мг, вихід 67 %). 1 H ЯМР (CDCl3) δ ppm=2,37 (3H, s) 3,72 (3H, s) 4,26 (3H, s). Приклад процедури згідно зі схемою реакції 7 – бромування сполуки, що містить хлор 5-Метокси-2,6-диметил-4-(2-бром-3-хлоріндол-1-іл)піридазин-3-oн Частину розчину брому (200 мг, 1,25 ммоля) в DCM (4 мл) додавали повільно по краплях до розчину 4-(3-хлоріндол-1-іл)-5-метокси-2,6-диметил-піридазин-3-ону (184 мг, 0,606 ммоля) в DCM (2 мл) при 0 °C. Бром знебарвлювався по мірі того, як його додавали, і додавання продовжували обережно до тих пір, доки зберігався тільки оранжевий колір. Обережно додавали NaHCO3 (0,5 г насиченого розчину у воді) з наступним додаванням достатньої кількості метабісульфіту натрію для знебарвлення надлишку брому. Отриману реакційну суміш екстрагували DCM (3 × 60 мл) і фільтрували об'єднані шари DCM за допомогою MgSO 4 і концентрували in vacuo. Отриману жовту смолу очищували за допомогою флеш-хроматографії (combiflash, 0-30 % DCM/EtOAc) з отриманням необхідного продукту 5-метокси-2,6-диметил-4(2-бром-3-хлоріндол-1-іл)піридазин-3-ону (115 мг, 0,301 ммоля, вихід 50 %) у вигляді білої твердої речовини. 1 H ЯМР (CDCl3) δ (ppm) = 7,64–7,58 (1H, m), 7,28-7,20 (2H, m), 7,02-6,96(1H, m), 3,74 (3H, s), 3,44 (3H, s), 2,35 (3H, s). Приклад процедури згідно зі схемою реакції 8 – трихлорування 5-Метокси-2,6-диметил-4-(2,3,6-трихлоріндол-1-іл)піридазин-3-он Розчин SO2Cl2 (185 мг, 1,365 ммоля) в DCM (2 мл + 0,5 мл відмивання) по краплях додавали до розчину 4-(індол-1-іл)-5-метокси-2,6-диметил-піридазин-3-ону (145 мг, чистота 85 %, 0,455 ммоля) в DCM (1,5 мл) при 0 °C. Розчин ставав жовтим, а потім оранжевим. Після перемішування протягом 30 хвилин розчин ставав жовтим та забезпечували нагрівання реакційної суміші протягом більше 1 години до температури навколишнього середовища та перемішували протягом додаткової 21 год. Реакційну суміш концентрували in vacuo та отриману смолу очищали за допомогою флеш-хроматографії (combiflash, 0-10 % DCM/EtOAc) з отриманням необхідного продукту 5-метокси-2,6-диметил-4-(2,3,6-трихлоріндол-1-іл)піридазин3-ону (128 мг, 0,344 ммоля, вихід 75 %) у вигляді білої твердої речовини. 1 H ЯМР (CDCl3) δ ppm=7,52 (1H, d), 7,22 (1H, dd), 6,99(1H, d), 3,74 (3H, s), 3,49 (3H, s), 2,35 (3H, s). Приклад процедури згідно зі схемою реакції 9 – монобромування 5-метокси-2,6-диметил-4-(3-броміндол-1-іл)піридазин-3-он Розчин NBS (110 мг, 0,619 ммоля) в DCM (3 мл) по краплях додавали до розчину 4-(індол-1іл)-5-метокси-2,6-диметил-піридазин-3-ону (197 мг, чистота 85 %, 0,619 ммоля) в DCM (2 мл) при 0 °C. Забезпечували нагрівання отриманої реакційної суміші до температури навколишнього середовища, перемішували протягом 2 год., а потім концентрували in vacuo. За допомогою флеш-хроматографії (combiflash, 0-10 % DCM/EtOAc) отримували перший необхідний продукт 4-(3-броміндол-1-іл)-5,6-диметокси-2-метил-піридазин-3-он (195 мг, 0,560 ммоля, вихід 90 %) у вигляді білої твердої речовини. 1 H ЯМР (CDCl3) δ ppm=7,63 – 7,59 (1H, m), 7,34 (1H, s), 7,32 – 7,23 (2H, m), 7,07 – 7,03 (1H, m), 3,76 (3H, s), 3,25 (3H, s), 2,34 (3H, s). Приклад процедури згідно зі схемою реакції 10 – хлорування сполуки, що містить бром 5-Метокси-2,6-диметил-4-(2-хлор-3-броміндол-1-іл)піридазин-3-он 17 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 60 Розчин SO2Cl2 (47 мкл, 0,583 ммоля) в DCM (2 мл) по краплях додавали до розчину 4-(3броміндол-1-іл)-5-метокси-2,6-диметил-піридазин-3-ону (203 мг, 0,583 ммоля) в DCM (6 мл) при 0 °C. Розчин ставав світло-жовтим. Після перемішування протягом 5 хвилин отриману реакційну суміш виймали з охолоджувальної бані та перемішували при температурі навколишнього середовища протягом 2 год. Реакційну суміш добре струшували з розчином NaHCO 3. Шари розділяли та водний шар екстрагували за допомогою DCM (3 × 20 мл). Об'єднані DCM шари фільтрували через MgSO 4 та концентрували in vacuo. Отриману тверду речовину очищали за допомогою флеш-хроматографії (combiflash, 0-10 % DCM/EtOAc) з отриманням бажаного продукту 5-метокси-2,6-диметил-4-(2-хлор-3-броміндол-1-іл)піридазин-3-ону (194 мг, 0,507 ммоля, вихід 87 %). 1 H ЯМР (CDCl3) δ (ppm) = 7,57–7,52 (1H, m), 7,30-7,22 (2H, m), 7,00-6,95 (1H, m), 3,74 (3H, s), 3,45 (3H, s), 2,35 (3H, s). Приклад процедури згідно зі схемою реакції 11 – ди- та трибромування 5-Метокси-2,6-диметил-4-(2,3-диброміндол-1-іл)піридазин-3-он та 5-метокси-2,6-диметил-4(2,3,6-триброміндол-1-іл)піридазин-3-он Розчин NBS (360 мг, 2,02 ммоля) в DCM (8 мл) по краплях додавали до розчину 4-(індол-1іл)-5-метокси-2,6-диметил-піридазин-3-ону (201 мг, чистота 85 %, 0,631 ммоля) в DCM (2 мл) при 0 °C. Забезпечували нагрівання отриманої реакційної суміші до температури навколишнього середовища, перемішували протягом 2 год., а потім концентрували in vacuo. З очищенням за допомогою флеш-хроматографії (combiflash, 0-10 % DCM/EtOAc) отримували перший необхідний продукт 4-(2,3-диброміндол-1-іл)-5,6-диметокси-2-метил-піридазин-3-он (40 мг, 0,094 ммоля, вихід 15 %) у вигляді жовтої твердої речовини. 1 H ЯМР (CDCl3) δ (ppm) = 7,58–7,53 (1H, m), 7,28-7,21 (2H, m), 7,01-6,95 (1H, m), 3,74 (3H, s), 3,43 (3H, s), 2,35 (3H, s). Шляхом повторного очищення виділеного неочищеного продукту за допомогою флешхроматографії (combiflash, 0-40 % EtOAc/ізогексан) отримували 4-(2,3,6-триброміндол-1-іл)-5,6диметокси-2-метил-піридазин-3-он (104 мг, 0,206 ммоля, вихід 33 %) у вигляді білої твердої речовини. 1 H ЯМР (CDCl3) δ ppm=7,42 (1H, d), 7,35 (1H, dd), 7,14 (1H, d), 3,75 (3H, s), 3,47 (3H, s), 2,36 (3H, s). Приклад процедури згідно зі схемою реакції 12 – перехресне поєднання зі сполукою, що містить бром 4-(2,3-Дихлоріндол-1-іл)-5,6-диметокси-2-метил-піридазин-3-он В толуолі (3 мл) та метанолі (60 мкл) суспендували 6-бром-4-(2,3-дихлоріндол-1-іл)-5метокси-2-метил-піридазин-3-он (0,200 г, 0,496 ммоля), Pd2Cl2(аліл)2 (2,7 мг, 0,00744 ммоля), дитрет-бутил-[6-метокси-3-метил-2-(2,4,6-триізопропілфеніл)феніл]фосфан (11,6 мг, 0,0248 ммоля) та карбонат дицезію (0,243 г, 0,744 ммоля). Отриману реакційну суміш нагрівали в умовах мікрохвильового випромінювання до 110 °C протягом 20 хв. Отриману реакційну суміш фільтрували, промивали з використанням EtOAc та концентрували при зниженому тиску на силікагелі. Шляхом очищення з використанням флеш-хроматографії (combiflash, 0-30 % EtOAc/ізогексан) отримували необхідний продукт 4-(2,3-дихлоріндол-1-іл)-5,6-диметокси-2метил-піридазин-3-он (0,116 г, 0,3275 ммоля, вихід 66 %) у вигляді коричневого масла. 1 H ЯМР (CDCl3) δ ppm=7,62-7,58 (1H, m), 7,28-7,22 (2H, m), 7,02-6,97 (1H, m), 3,98 (3H, s), 3,68 (3H, s), 3,60 (3H, s). Приклад процедури згідно зі схемами реакції 17 та 13 – відновлення ізо-пропенільної групи та перехресне поєднання сполуки, що містить бром, та борорганічної сполуки 4-Індол-1-іл-6-ізопропіл-5-метокси-2-метил-піридазин-3-он До перемішуваного розчину 4-(2,3-дихлоріндол-1-іл)-6-ізопропеніл-5-метокси-2-метилпіридазин-3-ону (355 мг, 0,975 ммоля) в етанолі (5,0 мл) додавали форміат амонію (1,24 г) та 20 % гідроксиду паладію на вугіллі (50 % води за вагою, 273 мг, 0,194 ммоля). Отриману реакційну суміш перемішували за температури навколишнього середовища протягом 1 год., а потім нагрівали до 60 °C протягом 30 хв. Отриманій реакційній суміші дозволяли охолонути, а потім фільтрували через целіт, промивали етанолом та концентрували in vacuo. Отримана неочищена тверда речовина являла собою 4-індол-1-іл-6-ізопропіл-5-метокси-2-метилпіридазин-3-он (253 мг, 0,851 ммоля, 87 %), який використовували без додаткового очищення. 1 H ЯМР (CDCl3) δ ppm=7,66-7,63 (1H, m), 7,30 (1H, d), 7,24-7,15 (2H, m), 7,05-7,02 (1H, m), 6,73 (1H, dd), 3,78 (3H, s), 3,24 (1H, m), 3,14 (3H, s), 1,28 (6H, m). 4-(2,3-Дихлоріндол-1-іл)-6-ізопропеніл-5-метокси-2-метил-піридазин-3-он 6-Бром-4-(2,3-дихлоріндол-1-іл)-5-метокси-2-метил-піридазин-3-он (0,600 г, 1,49 ммоля), комплекс дихлор[1,1'-біс(дифенілфосфіно)фероцен]паладію (II) та дихлорметану (0,0608 г, 18 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 0,0744 ммоля) та фторид цезію (0,476 г, 2,98 ммоля) суспендували в DME (3 мл) та додавали 2ізопропеніл-4,4,5,5-тетраметил-1,3,2-діоксаборолан (330 мкл, 1,79 ммоля). Отриману реакційну суміш нагрівали в умовах мікрохвильового випромінювання до 150 °C протягом 20 хв. Отриману реакційну суміш розбавляли EtOAc (50 мл), а потім промивали сольовим розчином (50 мл). Органічний шар висушували (MgSO4), а потім концентрували при зниженому тиску на силікагелі. Шляхом очищення з використанням флеш-хроматографії (combiflash, 0-20 % EtOAc/ізогексан) отримували необхідний продукт 4-(2,3-дихлоріндол-1-іл)-6-ізопропеніл-5-метокси-2-метилпіридазин-3-он (503 мг, 1,38 ммоля, 93 %) у вигляді світло-коричневого масла. 1 H ЯМР (CDCl3) δ (ppm) = 7,62–7,59 (1H, m), 7,28-7,25 (2H, m), 7,01-6,98 (1H, m), 5,62 (1H, m), 5,47 (1H, m), 3,81 (3H, s), 3,42 (3H, m), 2,15 (3H, m). Приклад процедури згідно зі схемою реакції 14 – утворення калієвої солі тетрафториду бору Калій трифтор(2,2,2-трифторетоксиметил)борат До суспензії гідриду натрію (0,5377 г, 60 % за вагою, 13,44 ммоля) в безводному THF (45 мл) при 0 °C по краплях додавали 2,2,2-трифторетанол (1,345 г, 13,44 ммоля). Отриману реакційну суміш повільно нагрівали до температури навколишнього середовища протягом більше 1 години, а потім повторно охолоджували до 0 °C. Додатково додавали за один раз калій бромметил(трифтор)борат (1,000 г, 4,481 ммоля) та отриману реакційну суміш перемішували при температурі навколишнього середовища протягом додаткових 22 год. Реакцію гасили гідрофторидом калію (2 мл, 4,5M, 9,1 ммоля) та перемішували протягом 30 хв. Суспензію концентрували in vacuo та до твердого залишку додавали діетиловий ефір. Отриману суспензію фільтрували, промивали великою кількістю діетилового ефіру та промиту тверду речовину повторно розчиняли в ацетонітрилі та фільтрували. Фільтрат концентрували in vacuo та подрібнювали з діетиловим ефіром з отриманням калій трифтор(2,2,2трифторетоксиметил)борату (0,950 г, 4,32 ммоля, вихід 96,4 %). 1 H ЯМР (DMSO-d6) δ ppm=3,72-3,65 (m, 2 H), 2,67-2,63 (m, 2 H). 19 F ЯМР (DMSO-d6) δ ppm = -72,7, -141,5. Приклад процедури згідно зі схемами реакції 16 та 15 – окиснення сірки та перехресне поєднання сполуки, що містить бром, з сіллю тіолової кислоти 4-(2,3-Дихлоріндол-1-іл)-5-метокси-2-метил-6-метилсульфініл-піридазин-3-он До перемішуваного розчину 4-(2,3-дихлоріндол-1-іл)-5-метокси-2-метил-6-метилсульфанілпіридазин-3-ону (60 мг, 0,16 ммоля) в DCM (2 мл) при -20 °C додавали mCPBA (36 мг, 0,17 ммоля). Після перемішування протягом 10 хв. за даної температури з'являвся жовтий осад. Реакційну суміш вливали в суміш з DCM (20 мл), насиченого розчину бікарбонату натрію (10 мл) та насиченого розчину тіосульфату натрію (10 мл), а потім перемішували протягом 10 хв. Отриману суміш пропускали через фазовий роздільник та шар, що містить DCM, концентрували при зниженому тиску з отриманням необхідного продукту 4-(2,3-дихлоріндол-1-іл)-5-метокси-2метил-6-метилсульфініл-піридазин-3-ону (59 мг, 0,12 ммоля, 95 %) у вигляді жовтої твердої речовини, яку використовували без додаткового очищення. 1 H ЯМР (CDCl3) δ (ppm) 7,59-7,66 (1H, m), 7,27-7,35 (2H, m), 6,98-7,05(0,6 H, m), 6,91-6,97 (0,4 H, m), 3,90 (3 H, m) 3,55 (3 H, m) 3,01 (3 H, m). 4-(2,3-Дихлоріндол-1-іл)-5-метокси-2-метил-6-метилсульфаніл-піридазин-3-он та 4-(2,3дихлоріндол-1-іл)-2-метил-6-метилсульфаніл-піридазин-3,5-діон 6-Бром-4-(2,3-дихлоріндол-1-іл)-5-метокси-2-метил-піридазин-3-он (600 мг, 1,49 ммоля), XantPhos (36 мг, 0,060 ммоля), Pd2dba3 (28 мг, 0,030 ммоля) та NaSMe (115 мг, 1,64 ммоля) суспендували в діоксані (8 мл) та додавали DIPEA (0,773 мл, 4,47 ммоля). Отриману реакційну суміш нагрівали до 60 °C та протягом 2 хвилин вона ставала чорною. Після перемішування при даній температурі протягом 1 год. реакційну суміш нагрівали до 80 °C та перемішували протягом ночі. Реакційній суміші дозволяли охолонути та виливали в DCM (100 мл) та 10 % розчин NaOH (100 мл). Розділяли шари та шар, що містить DCM, сушили (MgSO4) та концентрували при зниженому тиску на силікагелі, а потім очищали з використанням флешхроматографії (20 % EtOAc/ізогексан) з отриманням необхідного продукту 4-(2,3-дихлоріндол-1іл)-5-метокси-2-метил-6-метилсульфаніл-піридазин-3-ону (125 мг, 0,338 ммоля, 23 %) у вигляді жовтої кристалічної твердої речовини. 1 H ЯМР (CDCl3) δ ppm=7,62-7,58 (1H, m), 7,27-7,24 (2H, m), 7,01-6,97 (1H, m), 3,78 (3H, s), 3,49 (3H, s), 2,48 (3H, s). Водний шар, що містить NaOH, підкислювали конц. HCl, що викликало руйнування жовтого осаду. Даний осад потім екстрагували DCM (100 мл x 3), а шари, що містять DCM, висушували (MgSO4) та концентрували in vacuo. Отриманий неочищений залишок очищали за допомогою препаративної HPLC (звернено-фазове фракціонування lynx) з отриманням диметильованого 4 19 UA 112890 C2 5 10 15 20 25 30 35 40 45 50 55 (2,3-дихлоріндол-1-іл)-2-метил-6-метилсульфаніл-піридазин-3,5-діону (34 мг, 0,064 ммоля, 6 %) у вигляді світло-коричневої твердої речовини. 1 H ЯМР (CDCl3) δ ppm=7,61-7,57 (1H, m), 7,27-7,21 (2H, m), 6,95-6,91 (1H, m), 3,73 (3H, s), 2,53 (3H, s). Приклад процедури згідно зі схемами реакції 18 та 21 – утворення нітрилу та озоноліз 5-(2,3-Дихлоріндол-1-іл)-4-метокси-1-метил-6-оксо-піридазин-3-карбонітрил До перемішуваного розчину 5-(2,3-дихлоріндол-1-іл)-4-метокси-1-метил-6-оксо-піридазин-3карбальдегіду (98 мг, 0,278 ммоля) в THF (1,5 мл) додавали гідроксид амонію (30 % вод. розчин, 1,5 мл) з наступним додаванням сполуки, що містить йод (92 мг, 0,362 ммоля), що викликало появу темно-коричневого кольору. Отриману реакційну суміш перемішували протягом 1 год., а потім гасили розчином NaHCO3 (5 мл) та розчином Na2S2O3 (5 мл). Це викликало зміну кольору реакційної суміші від темно-коричневого до чистого світло-жовтого кольору. Після перемішування протягом 10 хв. реакційну суміш екстрагували з використанням DCM (20 мл x 2), сушили (MgSO4) та концентрували при зниженому тиску з отриманням необхідного продукту 5(2,3-дихлоріндол-1-іл)-4-метокси-1-метил-6-оксо-піридазин-3-карбонітрилу (82 мг, 0,235 ммоля, 85 %) у вигляді жовтої піни, подрібненої в жовту тверду речовину. 1 H ЯМР (CDCl3) δ ppm=7,65-7,61 (1H, m), 7,34-7,28 (2H, m), 7,00-6,95 (1H, m), 3,86 (3H, s), 3,61 (3H, s). 5-(2,3-Дихлоріндол-1-іл)-4-метокси-1-метил-6-оксо-піридазин-3-карбальдегід Колбу з 3 шийками наповнювали 4-(2,3-дихлоріндол-1-іл)-5-метокси-2-метил-6-вінілпіридазин-3-оном (418 мг, 1,19 ммоля) та дихлорметаном (10 мл). Колба була оснащена термометром, впускним патрубком та випускним патрубком, з'єднаними з двома склянками Дрекселя, при цьому кожна з останніх містила 10 % вод. розчину KI. Впускний патрубок з'єднували з генератором озону (виключеним). Включали обдування повітряним потоком для отримання стійкого барботування через реакційну колбу та виходу через розчин KI. Колбу охолоджували до -78 °C та при досягненні даної температури включали генератор озону та барботували протягом 10 хв. Розчин KI ставав темнішим в ході реакції. Виключали генератор озону та продували реакційну суміш повітрям протягом 2 хв. Потім від'єднували від впускного та випускного патрубків та додавали трифенілфосфін (939 мг, 3,58 ммоля). Реакційну суміш перемішували і поступово нагрівали до RT протягом більше 1 год., а потім перемішували при RT протягом додаткових 3 годин та залишали для відстоювання на ніч. Отриману реакційну суміш концентрували на силікагелі та очищали за допомогою хроматографії (combiflash, 0-50 % EtOAc/ізогексан) з отриманням необхідного продукту 5-(2,3-дихлоріндол-1-іл)-4-метокси-1метил-6-оксо-піридазин-3-карбальдегіду (262 мг, 0,744 ммоля, 63 %) у вигляді твердої жовтої речовини. 1 H ЯМР (CDCl3) δ ppm=9,92 (1H, s), 7,64-7,60 (1H, m), 7,31-7,26 (2H, m), 7,00-6,96 (1H, m), 3,93 (3H, s), 3,57 (3H, s). Приклад процедури згідно зі схемою реакції 19 – отримання похідного діону 5-(2,3-Дихлоріндол-1-іл)-1,3-диметил-6-оксо-піридазин-4-іл] ізопропілсульфанілформіат До перемішуваної суспензії 4-(2,3-дихлоріндол-1-іл)-2,6-диметил-піридазин-3,5-діону (120 мг, 0,370 ммоля) в дихлорметані (8 мл) при RT додавали триетиламін (129 мкл, 0,925 ммоля). Реакційна суміш ставала гомогенною. Додавали S-ізопропіл хлортіоформіат (69 мкл, 0,555 ммоля) та перемішували реакційну суміш протягом 15 хв. Потім суміш гасили водою (10 мл) та розділяли шари. Водний шар повторно екстрагували дихлорметаном (10 мл x 3) та об'єднані органічні шари висушували (фільтр для фазового роздільника) та концентрували при зниженому тиску на силікагелі. Шляхом флеш-хроматографії (combiflash, -20 % EtOAc/ізогексан) отримували необхідний продукт [5-(2,3-дихлоріндол-1-іл)-1,3-диметил-6-оксо-піридазин-4-іл] ізопропілсульфанілформіат (140 мг, 0,328 ммоля, 89 %) у вигляді жовтої твердої речовини. 1 H ЯМР (CDCl3) δ (ppm) 7,52-7,57 (1H, m), 7,21-7,27 (2H, m), 6,94-6,98 (1H, m), 3,86 (3H, s), 3,22 (1H, sept), 2,38 (3H, s), 1,11 (3H, d), 1,04 (3H, d). Приклад процедури згідно зі схемою реакції 20 – галогенування 2-заміщеного індолу 4-(3-Хлор-2-метил-індол-1-іл)-5-метокси-2,6-диметил-піридазин-3-он До перемішуваного розчину 5-метокси-2,6-диметил-4-(2-метиліндол-1-іл)піридазин-3-ону (147 мг, 0,52 ммоля) в DCM (3 мл) при 0 °C по краплях додавали розчин сульфурилхлориду (70 мг, 0,52 ммоля) в DCM (1 мл). Додатково додавали DCM (1 мл). Після реакції з тривалістю 1 година суміш гасили шляхом додавання нас. водного NaHCO 3 (2 мл). Отриману суміш фільтрували через твердий MgSO4, промивали використовуючи DCM. Фільтрати концентрували in vacuo з отриманням титульної сполуки у вигляді світло-коричневої твердої речовини (158 мг, 96 %). Даний матеріал використовували для наступних реакцій без додаткового очищення. 20 UA 112890 C2 1 5 10 15 20 25 30 35 40 45 50 55 H ЯМР (CDCl3) δ (ppm) 7,60-7,54 (1H, m), 7,22-7,16 (2H, m), 6,96-6,90 (1H, m), 3,75 (3H, s), 3,27 (3H, s), 2,34 (3H, s), 2,32 (3H, s). Приклад процедури згідно зі схемою реакції 22 – відновлення карбонільної сполуки 4-(2,3-Дихлоріндол-1-іл)-6-(дифторметил)-5-метокси-2-метил-піридазин-3-он До перемішуваного розчину 5-(2,3-дихлоріндол-1-іл)-4-метокси-1-метил-6-оксо-піридазин-3карбальдегіду (100 мг, 0,284 ммоля) в DCM (3 мл) при 0 °C додавали трифторид(діетиламіно)сірки (94 мкл, 0,710 ммоля). Забезпечували нагрівання реакційної суміші до RT протягом 1 год. Обережно гасили реакцію при 0 °C водою (5 мл), а потім додавали по краплях розчин NaHCO3 (5 мл). Після перемішування протягом 10 хв. здійснювали екстрагування з використанням DCM (20 мл), сушили (MgSO 4) та концентрували при зниженому тиску з отриманням 4-(2,3-дихлоріндол-1-іл)-6-(дифторметил)-5-метокси-2-метил-піридазин-3ону (102 мг, 0,273 ммоля, 96 %) у вигляді коричневої твердої речовини. 1H ЯМР (400 MГц, CDCl3): 7,64–7,59 (1H, m), 7,32–7,27 (2H, m), 7,01–6,97 (1H, m), 6,61 (1H, t), 3,82 (3H, s), 3,52 (3H, s). Приклад процедури згідно зі схемою реакції 23 – відновлення карбонільної сполуки 4-(2,3-Дихлоріндол-1-іл)-6-(1-гідроксіетил)-5-метокси-2-метил-піридазин-3-он До перемішуваного розчину 6-ацетил-4-(2,3-дихлоріндол-1-іл)-5-метокси-2-метил-піридазин3-ону (500 мг, 1,37 ммоля) в етанолі (1 мл) при 0 °C додавали борогідрид натрію (79 мг, 2,05 ммоля). Після перемішування протягом 20 хв. реакцію гасили водою (10 мл), а потім концентрували при зниженому тиску для видалення більшої частини етанолу. Потім водний розчин екстрагували з використанням Et2O (20 мл x 2), потім концентрували при зниженому тиску з отриманням необхідного продукту 4-(2,3-дихлоріндол-1-іл)-6-(1-гідроксіетил)-5-метокси2-метил-піридазин-3-ону (379 мг, 1,03 ммоля, 75 %) у вигляді білої твердої речовини. 1H ЯМР(400 МГц, CDCl3), 7,63 – 7,59 (1H, m), 7,31 – 7,22 (2H, m), 7,00 – 6,93 (1H, m), 5,05 – 4,97 (1H, m), 3,79 (3H, s), 3,47 (3H, s), 3,03 – 3,00 (1H, m), 1,56 – 1,53 (3H, m). Приклад процедури згідно зі схемою реакції 24 – метилювання спиртової сполуки 4-(2,3-Дихлоріндол-1-іл)-5-метокси-6-(1-метоксіетил)-2-метил-піридазин-3-он До перемішуваного розчину 4-(2,3-дихлоріндол-1-іл)-6-(1-гідроксіетил)-5-метокси-2-метилпіридазин-3-ону (98 мг, 0,27 ммоля) в DMF (1 мл) при 0 °C додавали гідрид натрію (60 % дисперсія в мінеральному маслі, 32 мг, 0,80 ммоля). Після перемішування протягом 5 хв. додавали MeI (50 мкл, 0,80 ммоля). Через 30 хв. обережно гасили реакцію розчином хлориду амонію (10 мл) та залишали на ніч. На наступний день реакційну суміш екстрагували з використанням DCM (10 мл x 3), а потім сушили (MgSO 4) та концентрували при зниженому тиску. Залишок повторно піддавали умовам реакції в тій же самій процедурі з тими кількостями реагенту/розчинника, як зазначено вище. Після перемішування протягом 30 хв. його нагрівали до RT та забезпечували його перемішування протягом додаткових 1,5 год. Потім його охолоджували до 0 °C, а потім обережно гасили розчином хлориду амонію (20 мл). Потім додавали Et2O та розділяли шари. Органічний шар повторно промивали водою (20 мл x 3), потім сушили (MgSO4) та концентрували при зниженому тиску на силікагелі. Шляхом хроматографії (0-30 % EtOAc/ізогексан) отримували необхідний продукт 4-(2,3-дихлоріндол-1іл)-5-метокси-6-(1-метоксіетил)-2-метил-піридазин-3-он (64 мг, 0,168 ммоля, 63 %) у вигляді безкольорового масла. 1H ЯМР (400 MГц, CDCl3): 7,63–7,58 (1H, m), 7,30–7,24 (2H, m), 7,01–6,94 (1H, m), 4,66–4,62 (1H, m), 3,80 (3H, s), 3,45-3,43 (6H, m), 1,56-1,54 (3H, m). Приклад процедури згідно зі схемою реакції 25 – фторування спиртової сполуки 4-(2,3-дихлоріндол-1-іл)-6-(1-фторетил)-5-метокси-2-метил-піридазин-3-он До перемішуваного розчину 4-(2,3-дихлоріндол-1-іл)-6-(1-гідроксіетил)-5-метокси-2-метилпіридазин-3-ону (185 мг, 0,502 ммоля) в DCM (4 мл) при 0 °C додавали трифторид(діетиламіно)сірки (86 мкл, 0,65 ммоля). Після перемішування протягом 30 хв. реакцію обережно гасили при 0 °C шляхом додавання по краплях розчину NaHCO 3 (10 мл). Після перемішування протягом 10 хв. екстрагували з використанням DCM (20 мл), сушили (MgSO4) та концентрували при зниженому тиску. За допомогою хроматографії (0-20 % EtOAc/ізогексан) отримували необхідний продукт 4-(2,3-дихлоріндол-1-іл)-6-(1-фторетил)-5метокси-2-метил-піридазин-3-он (194 мг, 0,524 ммоля, 104 %). 1H ЯМР аналіз продемонстрував ~10 % сторонніх домішок, які відділяли після наступного етапу 1H ЯМР (400 MГц, CDCl3): 7,63–7,59 (1H, m), 7,30–7,24 (2H, m), 7,01–6,94 (1H, m), 5,91–5,73 (1H, m), 3,81 (3H, s), 3,48 (3H, s), 1,75 (3H, dd). Таблиця 1. Приклади гербіцидних сполук за даним винаходом 21 UA 112890 C2 1 R -Cl 5 R -CH3 R H R H H -CH3 -CH3 4 Cl -Cl -CH3 -CH3 CR 4 H H -CH3 H 5-Br 1.005 CR 4 H H -CH3 H 4-Br 1.006 CR 4 H H -CH3 H 6-Br 1.007 CR 4 H -CH3 -CH3 H 1.008 CR 4 H H -CH3 H 7-Me 1.009 N H -CH3 H 1.010 CR 4 H -Cl -iPr H 1.011 CR 4 H -Cl -CH2OCH3 H 1.012 CR 4 H -Cl -CH3 H 1.013 CR 4 Cl -Cl -CH3 H 1.014 CR 4 H H -CH3 H 1.015 N H -CH3 H 4-Cl Сполука 1.001 X N 1.002 CR 4 1.003 CR 1.004 R 4 1 2 22 3 ЯМР (DMSO-d6) 7,93 (1H, s), 7,71-7,79 (1H, m), 7,45-7,54 (1H, m), 7,26-7,38 (2H, m), 3,66 (3H, s). (CDCl3) 7,69 (1H, d); 7,30-7,19 (3H, m); 7,02 (1H, d); 6,76 (1H, d); 3,75 (3H, s); 2,39 (3H, s). (CDCl3) 7,57-7,52 (1H, m); 7,24-7,15 (2H, m); 6,81-6,77 (1H, m), 3,47 (3H, s), 2,21 (3H, s). (d4MeOH) 7,86 (1H, s), 7,73 (1H, d), 7,26 (1H, d), 7,23 (1H, dd), 6,97 (1H, d), 6,62 (1H, dd), 3,76 (3H, s) (d4MeOH) 7,60 (1H, s), 7,24 (1H, d), 7,19 (1H, dd), 7,02 – 6,95 (2H, m), 6,59 (1H, dd), 3,68 (3H, s) (d4MeOH) 7,79 (1H, s), 7,48 (1H, dd), 7,20 (1H, d), 7,18-7,15 (2H, m), 6,62 (1H, d), 3,75 (3H, s) (d4MeOH) 7,87 (1H, s), 7,53 (1H, dd), 7,15-7,07 (2H, m); 6,99-6,96 (2H, m), 3,76 (3H, s), 2,34 (3H, s). (d4MeOH) 7,80 (1H, s), 7,36 (1H, d), 6,91-6,88 (2H, m); 6,80 (1H, d), 6,56 (1H, d), 3,69 (3H, s), 2,17 (3H, s). (d4MeOH) 8,26 (1H, d), 7,91 (1H, s), 7,83 (1H, dt), 7,43 (1H, td), 7,27-7,22 (2H, m), 3,78 (3H, s) (CDCl3) 7,74 (1H, s), 7,61 (1H, d), 7,207,12 (2H, m), 6,97 (1H, d), 6,65 (1H, d), 5,18-5,14 (1H, m), 1,35 (6H, d). (d4MeOH) 8,26 (1H, s), 7,58 (1H, dd), 7,24 (1H, d), 7,14-7,02 (2H, m), 6,63 (1H, dd), 3,92 (2H, s), 2,65 (3H, s) (DMSO-d6) 7,89 (1H, s), 7,57-7,50 (2H, m), 7,24-7,17 (2H, m), 7,12-7,06 (1H, m), 3,66 (3H, s) (CDCl3) 7,48 (1H, s), 7,48-7,43 (1H, m), 7,18-7,11 (2H, m), 6,76-6,70 (1H, m), 3,60 (3H, s) (DMSO-d6) 7,94 (1H, s), 7,59 (1H, dd), 7,31 (1H, d), 7,13-7,06 (2H, m), 7,05 (1H, dd), 6,62 (1H, d), 3,68 (3H, s) (CDCl3) 10,51 (1h, s), 8,40 (1H, d), 7,83 (1H, s), 7,67 (1H, d), 7,43 (1H, dd), 7,28 (1H, dd), 3,88 (3H, s) UA 112890 C2 Сполука 1.016 X 4 CR 1 R H 4 R Cl 5 R -CH3 1 R H 2 R 5-Cl 3 1.017 CR 4 H H -CH3 H 5-Cl 1.018 CR 4 H -Cl H 1.019 CR 4 H -Cl -третбутил -CH3 iPr 1.020 CR 4 Cl Cl -CH3 -CH3 6-Cl 1.021 CR 4 Cl Br -CH3 -CH3 1.022 CR 4 Br Br -CH3 -CH3 5-Br 1.023 CR 4 Br Br -CH3 -CH3 6-Br 1.024 CR 4 Br Br -CH3 -CH3 1.025 CR 4 H Br -CH3 -CH3 1.026 CR 4 Br Cl -CH3 -CH3 1.027 CR 4 H Cl -CH3 -CH3 ЯМР (DMSO-d6) 7,91 (1H, s), 7,64 (1H, s), 7,55-7,56 (1H, d), 7,24-7,26 (1H, dd), 7,14-7,16 (1H, d), 3,67 (3H, s) (DMSO-d6) 7,90 (1H, s), 7,64 (1H, s), 7,39-7,40 (1H, d), 7,03-7,13 (2H, m), 6,60-6,61 (1H, d), 3,67 (3H, s) (CDCl3) 7,49 (1H, s), 7,39 (1H, d), 7,297,20 (3H, m), 6,95 (1H, d), 1,51 (9H, s) (CDCl3) 7,71 (1H, m), 7,33-7,27 (2H, m), 7,23 (1H, s), 7,01-6,98 (1H, m), 3,75 (3H, s), 3,24 (1H, септет), 1,331,28 (6H, m) (CDCl3) 8,11 (1H, br s), 7,44 (1H, d), 7,18 (1H, dd), 6,79 (1H, d), 3,43 (3H, s), 2,18 (3H, s) (CDCl3) 7,54-7,48 (1H, m); 7,27-7,17 (2H, m), 6,87-6,80 (1H, m), 3,55 (3H, s), 2,27 (3H, s). (MeCN-d3) 7,72 (1H, d), 7,37 (1H, dd), 7,01 (1H, d), 3,63 (3H, s), 2,31 (3H, s) (DMSO-d6) 12,0 (1H, br s), 7,41 (1H, d), 7,39 (1H, s), 7,35 (1H, dd), 3,58 (3H, s), 2,26 (3H, s) (CDCl3) 7,46 (1H, dd), 7,14 (2H, m), 6,78 (1H, dd), 4,95 (1H, br s), 3,43 (3H, s), 2,13 (3H, s) (DMSO-d6) 11,4 (1H, bs), 7,47 (1H, s), 7,45-7,39 (1H, m), 7,19-7,11 (2H, m), 7,04-6,98 (1H, m), 3,54 (3H, s), 2,22 (3H, s) (CDCl3) 7,58-7,54 (1H, m), 7,22-7,14 (2H, m), 6,83-6,78 (1H, m), 3,49 (3H, s), 2,22 (3H, s) (DMSO-d6) 11,4 (1H, bs), 7,54-7,47 (1H, m), 7,45 (1H, s),7,20-7,10 (2H, m), 7,05-6,97 (1H, m), 3,54 (3H, s), 2,22 (3H, s) Таблиця 2. Приклади гербіцидних сполук за даним винаходом Сполука 2.001 -C≡N 2.002 -CHF2 2.003 -S-CH3 R 2 ЯМР (d4MeOH) 7,58-7,55 (1H, m), 7,28-7,22 (2H, m), 7,13-7,09 (1H, m), 3,80 (3H, s) (CDCl3) 7,62-7,58 (1H, m), 7,29-7,24 (2H, m), 6,93-6,90 (1H, m), 6,57 (1H, t), 3,74 (3H, s). (CDCl3) 7,61-7,57 (1H, m), 7,27-7,21 (2H, m), 6,95-6,91 (1H, m), 3,73 (3H, s), 2,53 (3H, s) 23 UA 112890 C2 2 Сполука 2.004 R -S(O)2CH3 2.005 -S(O)CH3 2.006 -S(O)C2H5 2.007 -S(O)2C2H5 2.008 -CH2OCH3 2.009 -CH2CH(CH3)2 2.010 -нбутил 2.011 -CH2OCH2-cгексил 2.012 -CH2OCH2CF3 2.013 iPr 2.014 -CH2OiPr 2.015 -CH2OC2H4OCH3 2.016 -C(=CH2)CH3 2.017 -S-C2H5 2.018 -O-nPr 2.019 -O-CH2-iPr 2.020 -O-CH2CHF2 2.021 -N(CH3)2 2.022 -OCH3 2.023 -OCH2CH3 2.024 -OCH2CF3 2.025 -CH2CH=CH2 2.026 -cPr 2.027 -C2H5 2.028 -Br 2.029 -C(CH3)OCH3 ЯМР (CDCl3) 7,62-7,59 (1H, m), 7,28-7,23 (2H, m), 6,97-6,93 (1H, m), 3,95 (3H, s), 3,42 (3H, s) (CDCl3) 7,55-7,63 (1H, m), 7,21-7,29 (2H, m), 6,96-7,02 (1H, m), 3,84 (3H, m), 3,21 (3H, m) (CDCl3) 7,54-7,63 (1H, m), 7,16-7,35 (2H, m), 6,92-7,03 (1H, m), 3,85 (3H, m), 3,24-3,43 (2H, m), 1,54 (3H, m) (CDCl3) 7,62-7,58 (1H, m), 7,27-7,23 (2H, m), 6,96-6,92 (1H, m), 3,95 (3H, s), 3,51 (2H, q), 1,51 (3H, t). (d4MeOH) 7,58–7,54 (1H, m), 7,27–7,22 (2H, m), 7,05–7,01 (1H, m), 4,54 (2H, s), 3,75 (3H, s), 3,47 (3H, s) (CDCl3) 7,55-7,61 (1H, m), 7,23 (2H, dd), 6,88-6,96 (1H, m), 3,73 (3H, s) 2,60 (2H, d), 2,08-2,20 (1H, m), 1,00 (6H, d) (CDCl3) 7,56 (1H, d), 7,22 (2H, d), 6,88-6,95 (1H, m), 3,69 (3H, s), 2,64-2,75 (2H, m), 1,68 (2H, dt), 1,36-1,51 (2H, m), 0,98 (3H, t) (CDCl3) 7,61-7,57 (1H, m), 7,24-7,20 (2H, m), 7,00-6,96 (1H, m), 4,78 (2H, dd) 3,79 (3H, s), 3,48 (2H, d), 1,75-1,64 (5H, m), 1,301,12 (4H, m), 1,01-0,88 (2H, m) (CDCl3) 7,58-7,54 (1H, m), 7,24-7,18 (2H, m), 6,85-6,80 (1H, m), 4,62 (2H, dd), 3,93 (2H, q), 3,58 (3H, s) (CDCl3) 7,61-7,58 (1H, m), 7,29-7,22 (2H, m), 6,92-6,88 (1H, m), 3,69 (3H, s), 3,18 (1H, cептет), 1,30-1,27 (6H, m) (CDCl3) 7,58-7,55 (1H, m), 7,23-7,19 (2H, m), 6,97-6,93 (1H, m), 4,76 (2H, s), 3,87 (1H, m), 3,74 (3H, s), 1,28 (6H, d) (CDCl3) 7,60-7,56 (1H, m), 7,23-7,19 (2H, m), 6,98-6,94 (1H, m), 4,74 (2H, dd), 3,83-3,81 (2H, m), 3,76 (3H, s), 3,61-3,58 (2H, m), 3,35 (3H, s) (d4MeOH) 7,62-7,53 (1H, m), 7,31-7,23 (2H, m), 7,04 (1H, s), 5,94–5,88 (1H, m), 5,56–5,47 (1H, m), 3,76 (3H, s), 2,23–2,17 (3H, m) (d4MeOH) 7,58-7,54 (1H, m), 7,27-7,21 (2H, m), 7,04-7,00 (1H, m), 3,74 (3H, s), 3,12 (2H, q), 1,42 (3H, t) (DMSO-d6) 7,55-7,51 (1H, m), 7,23-7,19 (2H, m), 7,11-7,07 (1H, m), 4,14 (2H, t), 3,50 (3H, s), 1,78 (2H, m), 1,00 (3H, t) (CDCl3) 7,60-7,57 (1H, m), 7,24-7,20 (2H, m), 6,98-6,96 (1H, m), 4,10 (2H, d), 3,67 (3H, s), 2,16 (1H, m), 1,05 (6H, d) (CDCl3) 7,58-7,56 (1H, m), 7,23-7,19 (2H, m), 6,95-6,92 (1H, m), 6,11 (1H, tt), 4,47 (2H, tq), 3,64 (3H, s) (CDCl3) 7,61-7,58 (1H, m), 7,25-7,22 (2H, m), 6,98-6,95 (1H, m), 3,71 (3H, s), 2,86 (6H, s) (d4MeOH) 7,55-7,51 (1H, m), 7,25-7,19 (2H, m), 7,04-7,00 (1H, m), 4,01 (3H, s), 3,66 (3H, s) (CDCl3) 7,60-7,57 (1H, m), 7,24-7,20 (2H, m), 6,99-6,96 (1H, m), 4,40 (2H, q), 3,68 (3H, s), 1,48 (3H, t) (d4MeOH) 7,57-7,53 (1H, m), 7,27-7,20 (2H, m), 7,07-7,03 (1H, m), 4,90-4,83 (2H, m), 3,66 (3H, s) (d4MeOH) 7,56 (1H, m), 7,26-7,21 (2H, m), 6,99 (1H, m), 6,08 (1H, m), 5,21-5,13 (2H, m), 3,72 (3H, s), 3,51 (2H, dt) (CDCl3) 7,62 (1H, m), 7,29-7,24 (2H, m), 6,96 (1H, m), 3,70 (3H, s), 2,17 (1H, m), 1,08-1,01 (4H, m) (CDCl3) 7,62 (1H, m), 7,26 (1H, dd), 7,24 (1H, dd), 6,94 (1H, dd), 3,73 (3H, m), 2,75 (2H, q), 1,29 (3H, t) (CDCl3) 7,61 (1H, m), 7,28-7,26 (2H, m), 6,94 (1H, m), 3,78 (3H, s) (d6-DMSO) 12,09 (1H, brs), 7,58–7,54 (1H, m), 7,29-7,23 (2H, m), 7,10–7,02 (1H, m), 4,67-4,62 (1H, m), 3,64 (3H, s), 3,30 (3H, d), 1,47-1,44 (3H, m). 24 UA 112890 C2 Сполука 2.030 R -CHFCH3 2 2.031 -CF2CH3 2.032 -CH(OH)CH3 2.033 -C(O)CH3 2.034 -CH2CHF2 ЯМР (d6-DMSO) 7,58–7,54 (1H, m), 7,28–7,24 (2H, m), 7,10–7,06 (1H, m), 5,88 (1H, dq), 3,66 (3H, s), 1,67 (3H, dd) (d6-DMSO) 7,58-7,54 (1H, m), 7,29-7,24 (2H, m), 7,15-7,11 (1H, m), 3,66 (3H, s), 2,04 (3H, t). (d6-DMSO) 7,60–7,56 (1H, m), 7,29–7,24 (2H, m), 7,08–7,02 (1H, m), 5,15–5,09 (1H, m), 3,78 (3H, s), 1,61–1,58 (3H, m). (d6-DMSO) 7,58–7,52 (1H, m), 7,27–7,23 (2H, m), 7,19–7,14 (1H, m), 3,80 (3H, s), 2,61 (3H, m). (d4-метанол) 7,61-7,57 (1H, m), 7,29-7,24 (2H, m), 7,06-7,02 (1H, m), 6,35 (1H, tt), 3,76 (3H, s), 3,36 (2H, td). Таблиця 3. Приклади гербіцидних сполук за даним винаходом 1 4 Сполука 3.001 X 4 CR R -Cl G -C(O)-S-iPr 3.002 CR 4 -Cl -C(O)-морфолініл 3.003 CR 4 -Cl -C(O)-iPr 3.004 CR 4 -Cl -C(O)ОCH3 3.005 N -C(O)ОCH3 3.006 N -C(O)CH3 3.007 CR 4 -Cl -C(O)-S-тбутил 3.008 CR 4 -Cl -C(O)-тбутил 3.009 CR 4 -Cl -C(O)-p-нітрофеніл 3.010 CR 4 -Cl -C(O)OCH2iPr 3.011 CR 4 -Cl -C(O)ОiPr ЯМР (CDCl3) 7,52-7,57 (1H, m), 7,21-7,27 (2H, m), 6,94-6,98 (1H, m), 3,86 (3H, s), 3,22 (1H, sept), 2,38 (3H, s), 1,11 (3H, d), 1,04 (3H, d). (CDCl3) 7,57-7,61 (1H, m), 7,21-7,23 (2H, m), 6,99-7,03 (1H, m), 3,87 (3H, s), 2,92-3,35 (8H, m), 2,38 (3H, s). (CDCl3) 7,55-7,58 (1H, m), 7,21-7,28 (2H, m), 6,96 – 7,02 (1H, m), 4,61 (1H, sept), 3,85 (3H, s), 2,40 (3H, s), 1,03 (3H, d), 0,98 (3H, d). (CDCl3) 7,55-7,59 (1H, m), 7,22-7,27 (2H, m), 6,95-7,01 (1H, m), 3,86 (3H, s), 3,64 (3H, s), 2,39 (3H, s). (CDCl3) 7,93 (1H, s), 7,71 (1H, d), 7,51 (1H, m), 7,39 (1H, d), 7,32 (1H, t), 3,92 (3H, s), 3,85 (3H, s) (CDCl3) 7,85 (1H, s), 7,71 (1H, d), 7,52 (1H, t), 7,38 (1H, d), 7,32 (1H, t), 3,92 (3H, s), 2,19 (3H, s) (CDCl3) 7,54-7,57 (1H, m), 7,22-7,25 (2H, m), 6,94-6,99 (1H, m), 3,85 (3H, s), 2,38 (3H, s), 1,19 (9H, s). (CDCl3) 7,54-7,58 (1H, m), 7,19-7,25 (2H, m), 6,95-6,99 (1H, m), 3,88 (3H, s), 2,30 (3H, s), 0,91 (9H, s). (CDCl3) 8,24 (2H, d), 8,16 (2H, d), 7,48-7,53 (1H, m), 7,13-7,19 (2H, m), 6,95–6,99 (1H, m), 3,68 (3H, s), 2,30 (3H, s). (CDCl3) 7,53-7,57 (1H, m), 7,21-7,26 (2H, m), 6,94 – 6,98 (1H, m), 3,84 (3H, s), 2,34 (3H, s), 1,97 – 2,30 (2H, m), 1,67-1,77 (1H, m), 0,64 (3H, d), 0,62 (3H, d). (CDCl3) 7,55-7,58 (1H, m), 7,21-7,28 (2H, m), 6,96 – 7,02 (1H, m), 4,61 (1H, sept), 3,85 (3H, s), 2,40 (3H, s), 1,03 (3H, d), 0,98 (3H, d). 5 25 UA 112890 C2 Таблиця 4. Приклади гербіцидних сполук за даним винаходом Сполука 4.001 4.002 4.003 4.004 4.005 4.006 4.007 4.008 4.009 4.010 4.011 4.012 4.013 4.014 4.015 4.016 4.017 4.018 4.019 4.020 4.021 4.022 4.023 4.024 4.025 4.026 2 3a 3b 3c 4 5 R -OCH3 H H H H F H H -CH3 H -OCH3 H H H H H F F H H -CH3 H H H H H R H H -Cl H F H H -CH3 H H H H H H Cl F H H H -CH3 H H H H H H R H H H H H H H H H H Cl Cl H Cl H Cl Cl H Cl Cl Cl Cl H Cl H CH3 R H H H H H H H H H H Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl Cl CH3 -C≡N H -CH3 H H H CH3 Cl 4.028 4.029 4.030 4.031 10 H H H H H H H H H H H H H H H H H H H H H H H H -CH3 -CH3 R H -CF3 H -Cl H H F H H -CH3 H -CF3 -CF3 -Br H H H H F H H -CH3 -CH3 H H H 4.027 5 R -CH3 -CH3 -CHF2 -CHF2 H H H H H H H H H H H H Cl Br Cl Br ЯМР H H H H (CDCl3) 7,53 (1H, m), 7,11 (2H, m), 6,85 (1H, m), 6,55 (1H, bs), 6,42 (1H, s), 3,66 (3H, s), 2,34 (3H, s), 2,19 (3H, d) (CDCl3) 7,56 (1H, d), 7,18 (2H, m), 6,85 (1H, d), 3,61 (3H, s), 2,28 (3H, s), 2,13 (3H, s). Біологічні приклади Насіння ряду тестованих видів висівали в стандартний ґрунт в горщиках: Solanum nigrum (SOLNI), Amaranthus retoflexus (AMARE), Setaria faberi (SETFA), Alopecurus myosuroides (ALOMY), Echinochloa crus-galli (ECHCG), Ipomoea hederacea (IPOHE). Після культивації протягом 8 днів (після появи сходів) за контрольованих умов в теплиці (при 24/16 °C, день/ніч; 14 годин світла; 65 % вологості) рослини обприскували водним розчином для обприскування, отриманим зі складу технічного активного інгредієнта в розчині ацетону/води (50:50), що містить 26 UA 112890 C2 5 0,5 % Tween 20 (поліоксіетиленсорбіту монолаурат, CAS RN 9005-64-5). Сполуки вносили у кількості 1000 г/га. Потім тестові рослини вирощували в теплиці за контрольованих умов в теплиці (при 24/16 °C, день/ніч; 14 годин світла; 65 % вологість) та поливали двічі на добу. Через 13 днів в тесті проводили оцінку відносного пошкодження, яке було завдане рослині. Значення біологічної активності показані в наведеній далі таблиці за п'ятибальною шкалою (5=80-100 %; 4=60-79 %; 3=40-59 %; 2=20-39 %; 1=0-19 %). Сполука 1.001 1.002 1.003 1.004 1.005 1.006 1.007 1.008 1.009 1.010 1.012 1.013 1.014 1.016 1.017 1.020 1.021 1.022 1.023 1.024 1.025 1.026 1.027 2.001 2.002 2.003 2.004 2.005 2.006 2.008 2.009 2.010 2.011 2.012 2.013 2.014 2.015 2.016 2.017 2.018 2.019 2.020 2.021 2.022 2.023 2.024 2.025 2.026 2.027 SOLNI 5 5 5 4 5 4 5 4 4 3 5 5 5 5 5 5 5 5 5 5 5 5 5 5 5 2 2 5 4 5 4 4 4 4 4 4 4 4 3 4 4 4 4 5 4 2 5 5 5 AMARE 5 4 5 1 2 1 2 1 4 1 5 5 3 2 3 5 5 3 5 5 4 5 4 3 5 2 2 2 1 3 1 3 2 1 3 2 2 4 4 3 4 4 3 4 2 2 2 4 4 Після внесення SETFA ALOMY 2 1 1 1 1 1 1 1 3 1 1 1 1 1 1 1 1 1 1 1 5 1 2 1 1 1 1 1 1 1 1 1 1 2 1 1 1 2 2 1 1 1 3 2 1 1 2 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 1 2 1 1 1 1 1 1 2 1 2 1 1 1 27 ECHCG 4 1 2 1 1 1 1 1 1 1 2 1 4 1 1 4 2 2 3 2 1 4 3 2 1 1 1 1 1 1 1 1 1 1 1 1 1 1 2 1 1 1 1 1 1 1 2 1 1 IPOHE 5 4 5 1 2 1 1 2 1 1 5 5 4 4 4 5 5 5 5 5 3 5 4 5 5 4 2 5 4 5 2 3 5 4 2 5 5 2 1 4 2 3 3 5 4 1 5 5 5 UA 112890 C2 Сполука 2.028 3.001 3.002 3.003 3.004 3.005 3.006 3.007 3.008 3.009 3.010 3.011 4.026 4.027 5 10 AMARE 5 5 2 5 5 4 4 5 5 5 5 5 4 5 Після внесення SETFA ALOMY 1 1 1 1 1 1 1 1 2 2 1 1 1 2 1 1 1 2 1 1 1 1 2 1 3 2 4 3 ECHCG 1 1 1 4 4 3 4 1 3 1 3 4 2 5 IPOHE 5 5 5 5 5 5 5 5 5 5 5 5 5 5 Порівняльний експеримент Порівняльний експеримент проводили для порівняння біологічної ефективності сполуки за даним винаходом з такими з WO 2011/045271. Тест виконували з використанням наступних сполук, як описано вище. Використовували три різні норми внесення (250 г/га, 500 г/га та 1000 г/га). Отримані результати наведені в таблиці нижче. Сполука Сполука А Сполука В 1.001 15 SOLNI 5 5 5 5 5 5 5 5 5 5 5 5 5 5 Норма внесення, г/га 1000 500 250 1000 500 250 1000 500 250 SOLNI 5 4 3 4 3 2 5 5 5 AMARE 4 4 3 4 3 2 4 4 4 Після внесення SETFA ALOMY 2 2 1 1 1 1 1 2 1 1 1 1 3 2 1 2 1 2 ECHCG 3 2 1 2 1 1 3 3 2 IPOHE 5 5 4 5 2 1 5 5 5 Дані результати демонструють, що сполуки за даним винаходом проявляють підвищену ефективність порівняно з тими, що розкриті в WO2011/045271, що особливо очевидно при більш низьких нормах внесення. 28
ДивитисяДодаткова інформація
Назва патенту англійськоюPyridazinone herbicidal compounds
Автори англійськоюBurton, Paul, Kozakiewicz, Anthony, Morris, James, Alan, Mathews, Christopher John, Shanahan, Stephan
Автори російськоюБартон Пол, Козакевич Энтони, Моррис Джэймс Алан, Метьюз Кристофер Джон, Шэнэхэн Стивен
МПК / Мітки
МПК: A01N 43/56, C07D 403/04
Мітки: гербіцидні, сполуки, піридазинону
Код посилання
<a href="https://ua.patents.su/32-112890-gerbicidni-spoluki-piridazinonu.html" target="_blank" rel="follow" title="База патентів України">Гербіцидні сполуки піридазинону</a>
Попередній патент: Способи для покращеної сівби насіння
Наступний патент: Суміш меркаптосилану із сажею
Випадковий патент: Привід круглов'язальної машини












