Композиції, синтез і способи застосування похідних фенілциклоалкілметиламіну
Номер патенту: 114807
Опубліковано: 10.08.2017
Автори: Адіей Коуакоу, Бхат Лаксмінараян, Бхат Сіма Рані
Формула / Реферат
1. Сполука структурної формули (І)
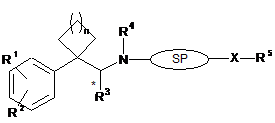 (I)
(I)
або її фармацевтично прийнятна сіль, де:
n дорівнює 1;
SP являє собою спейсер С4алкілену (бутилену);
X являє собою О, S або S(O)(O);
R1 і R2 незалежно являють собою Н, С1-6алкокси або галоген;
R3 являє собою С1-6алкіл;
R4 являє собою Н;
R5 являє собою С1-6алкіл;
R1, R2, R3, R4 і R5 необов'язково заміщені 2Н (дейтерієм); і
* означає атом вуглецю, який може бути оптично активним.
2. Сполука за п. 1, в якій R1 і R2 незалежно являють собою С1-6алкокси або галоген.
3. Сполука за п. 1 або п. 2, в якій Х являє собою О.
4. Сполука за п. 1 або п. 2, в якій R1 являє собою Н, a R2 являє собою галоген або алкокси.
5. Сполука за п. 1 або п. 2, в якій R3 є ізобутилом.
6. Сполука за п. 1, яка являє собою
 .
.
7. Сполука за п. 1 або п. 2, яка знаходиться щонайменше в 95 % надлишку в R-формі відносно S-форми або чистої R-форми.
8. Сполука за п. 1 або п. 2, яка знаходиться щонайменше в 95 % надлишку в S-формі відносно R-форми або чистої S-форми.
9. Фармацевтична композиція, яка містить сполуку за будь-яким із пп. 1-8 і фармацевтично прийнятний формотворний компонент.
10. Фармацевтична композиція для лікування або запобігання ожирінню у пацієнта, що являє собою ссавця, яка містить сполуку за будь-яким із пп. 1-8 і фармацевтично прийнятний формотворний компонент.
11. Фармацевтична композиція для лікування або запобігання депресії у пацієнта, що являє собою ссавця, яка містить сполуку за будь-яким із пп. 1-8 і фармацевтично прийнятний формотворний компонент.
Текст
Реферат: У даному винаході запропоновані нові похідні фенілциклоалкілметиламіну і способи одержання похідних фенілциклоалкілметиламіну. У даному винаході також запропоновані способи застосування похідних фенілциклоалкілметиламіну і композиції похідних фенілциклоалкілметиламіну. Зазначені фармацевтичні композиції сполук згідно з даним винаходом можуть бути застосовані для лікування та/або запобігання ожирінню та пов'язаним із ожирінням супутнім захворюванням, а також депресії та пов'язаним із депресією супутнім захворюванням. UA 114807 C2 (12) UA 114807 C2 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 Даний винахід відноситься до похідних фенілциклоалкілметиламіну, синтезу похідних фенілциклоалкілметиламіну і способів застосування похідних фенілциклоалкілметиламіну для фармакологічного лікування ожиріння, депресії й пов'язаних із ожирінням супутніх показань. РІВЕНЬ ТЕХНІКИ Ожиріння є хронічним захворюванням, яке торкається мільйонів людей по всьому світу, особливо в розвинених країнах. Воно визначається наявністю надлишкового жиру в організмі й, як правило, виміряється шляхом розрахунків ІМТ (індекс маси тіла) суб'єкта. Якщо ІМТ суб'єкта становить 30 або вище, він або вона вважається підданим ожирінню. Ожиріння може прямо або побічно викликати ряд проблем зі здоров'ям, таких як, наприклад, діабет 2 типу, ішемічну хворобу серця, високий рівень тригліцеридів у крові, високий кров'яний тиск й інсульт. Ожиріння також підвищує ризик деяких видів раку. Для чоловіків із ожирінням, у порівнянні з їхніми однолітками з нормальною вагою, існує підвищена ймовірність смерті від раку товстої кишки, прямої кишки і простати. Для жінок із ожирінням, у порівнянні з не страждаючими ожирінням жінками, існує підвищена ймовірність смерті від раку жовчного міхура, молочної залози, матки, шийки матки й яєчників. Смерть від деяких видів раку може бути більш імовірною, оскільки ожиріння утрудняє виявлення раку на ранніх стадіях (наприклад, маленька пухлина на початковій стадії, що відноситься до раку молочної залози, може не відчуватися в жінки з ожирінням). Недавні дослідження показують, що ожиріння підвищує ризик розвитку деменції альцгеймеровського типу. Інші захворювання й проблеми зі здоров'ям, пов'язані з ожирінням, включають: хворобу жовчного міхура, камені в жовчному міхурі, остеоартрит, подагру або біль у суглобах, апное в сні, психологічні й соціальні проблеми. Ожиріння пов'язане з декількома факторами, основним з яких є генетичний, що є одним із факторів, пов'язаних із ожирінням, над яким суб'єкти не мають контролю. Іншими важливими факторами, що впливають на ожиріння, є: механізми накопичення жиру; баланс між споживанням енергії та її витратою; стиль життя суб'єкта: звички у харчуванні й фізичні вправи; і психологічні, культурні й соціально-економічні впливи. Незважаючи на гадане невблаганним прогресування даного захворювання, в його фармакотерапії досягнуті обмежені успіхи. Лікарські засоби для лікування ожиріння можна розділити на три групи: ті, що зменшують споживання їжі або гнітять апетит; ті, що змінюють метаболізм або блокувальні поглинання жиру; ті, що й збільшують термогенез. У цей час є тільки два лікарські засоби, схвалені Федеральним управлінням з контролю якості харчових продуктів і лікарських засобів США (FDA) для довгострокового лікування ожиріння, і це блокатор поглинання жиру орлістат (КСЕНІКАЛ® (XENICAL®)) і засіб придушення апетиту, сібутрамін (МЕРІДІА® (MERIDIA®)). Єдиною протестованою термогенною комбінацією лікарських засобів є комбінація ефедрину і кофеїну, але таке лікування не було схвалено регулювальними органами. Блокатор поглинання жиру орлістат функціонує в шлунково-кишковому тракті шляхом блокування ферменту, який необхідний для переварювання жирів. Замість того, щоб всмоктуватися в кишечнику, до однієї третини жиру, який споживає суб'єкт, виводиться з організму з калом. Крім того, орлістат блокує поглинання необхідних жиророзчинних вітамінів A, D, Е і К, а також бета-каротину. Це одне з головних обмежень цього препарату для тривалого застосування при лікуванні ожиріння. Найбільше часто відмічуваними побічними ефектами орлістату є здуття живота, понос і маслянистий кал. У категорії засобів придушення апетиту, для лікування ожиріння в цей час на ринку доступні декілька норадренергічних і серотонінергічних лікарських засобів, що належать до сімейства 2арилетиламінів. Норадренергічні агенти, такі як фенілпропаноламін (АКЬЮТРІМ® (ACUTRIM®), ДЕКСАТРІМ® (DEXATRIM®)), діетилпропіон (ТЕНУАТ® (TENUATE®)), і фентермін (ФАСТІН® (FASTIN®), ІОНАМІН® (IONAMIN®)) схвалені для короткострокового лікування ожиріння. При цьому норадренергічний і серотонінергічний агент сібутрамін (МЕРІДІА® (MERIDIA®)) є єдиним препаратом, у цей час схваленим для тривалого лікування ожиріння в категорії засобів придушення апетиту. Сібутрамін має циклобутанметиламіновий кістяк, і саме цей кістяк в основному відповідає за його унікальні фармакологічні властивості сібутраміну. В останні 10 років був опублікований ряд доповідей про можливе застосування сібутраміну окремо або в комбінації з іншими терапевтичними агентами для лікування та/або запобігання різних захворювань і/або розладів, крім ожиріння (див. Montana, J. G., WO 2004/058237; Lulla, A. et al., WO 2004/096202; Jerussi, T. P. et al., WO 02/060424; Senanayake, С. H. et al., WO 01/51453; Heal, D. J., WO 01/00205; Birch, A. M. et al., WO 01/00187; Mueller, P., WO 00/32178; Bailey, C., WO 98/11884; Kelly, P., WO 98/13034). Приклади: лікування нудоти, блювоти і супутніх станів; когнітивних дисфункцій; розладів харчування; збільшення ваги; синдрому подразненого кишечнику; обсесивно-компульсивних розладів; адгезії тромбоцитів; апное, афективних розладів, таких як синдром дефіциту уваги, депресія й тривожність; розладів полової функції в 1 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 чоловіків і жінок; синдрому неспокійних ніг; остеоартриту; зловживання різними речовинами, включаючи нікотинову й кокаїнову залежність; нарколепсії; болю, такого як невропатичний біль, діабетична невропатія й хронічний біль; мігрені; розладів функції головного мозку; хронічних розладів, таких як предменструальний синдром; і нетримання сечі. У цілому, сібутрамін має ряд терапевтичних переваг через його унікальні фармакологічні властивості. Однак терапевтичне застосування сібутраміну для лікування ожиріння й інших захворювань і розладів у цей час не повною мірою використовується через певні обмеження й побічні ефекти, пов'язані з даним лікарським засобом. Основні небажані явища, про які повідомляється, у деяких випадках небезпечні для життя, включають підвищення артеріального тиску й побічні ефекти, що виникають з лікарських взаємодій, наприклад, серотонінового синдрому. Більшість цих побічних ефектів до деякої міри мають у своїй основі метаболізм. Сібутрамін виявляє свою фармакологічну дію переважно через його вторинні (M 1) і первинні (М2) амінові метаболіти. Сібутрамін метаболізується в печінці, головним чином, завдяки ізоферментам цитохрому P450 (3A4) до десметильних метаболітів, М 1 і М2. Ці активні метаболіти далі метаболізуються шляхом гідроксилювання й сполучення з фармакологічно неактивними метаболітами, М5 і М6. Період напівжиття терапевтично активних первинних і вторинних метаболітів М1 і М2 становить 14 і 16 годин, відповідно. Як видно з ряду літературних даних, метаболізм, опосередкований цитохромом Р450, і тривалий час напівжиття активних метаболітів (M1 і М2) у значній мірі відповідальні за несприятливі ефекти, такі як підвищений кров'яний тиск і інші побічні ефекти, що виникають з лікарських взаємодій сібутраміну. Таким чином, існує потреба та великий попит на більш безпечні й ефективні засоби придушення апетиту наступного покоління для лікування ожиріння. Ідеальний лікарський засіб у даному класі повинен мати високу активність відносно придушення апетиту, доведений ефект за втратою жиру, повинен добре переноситися під час уведення при гострому і хронічному стані й мати знижені побічні ефекти у порівнянні з сібутраміном і фентерміном. КОРОТКИЙ ОПИС ВИНАХОДУ Даний винахід спрямований на створення композицій нових похідних фенілциклоалкілметиламіну і застосування зазначених композицій для лікування ожиріння й пов'язаних із ним супутніх станів, і депресії й пов'язаних з нею супутніх станів. У даному винаході запропоновані способи синтезу таких похідних фенілциклоалкілметиламіну. Згідно з даним винаходом також запропоновані способи застосування похідних фенілциклоалкілметиламіну і фармацевтичної композиції похідних фенілциклоалкілметиламіну для лікування або запобігання ожиріння й супутніх захворювань і/або розладів, і для лікування або запобігання депресії й супутніх захворювань і/або розладів. Сполуки згідно з даним винаходом мають переваги завдяки їхнім переважним метаболічним, фармакокінетичним і фармакологічним профілям. У даному винаході запропоновані похідні фенілциклоалкілметиламіну структурної формули (I): , або їх ізомер або фармацевтично прийнятна сіль, де: n становить 0, 1, 2, 3, 4 або 5; SP являє собою спейсер, де зазначений спейсер являє собою C 1-6 алкілен, і при цьому один або більше атомів вуглецю зазначеного C1-6 алкілену необов'язково містять в якості замісників 6 6 O, S або NR , де R являє собою H або C1-6 алкіл; 6 X являє собою O, S, NR або S(O)(O); 1 2 3 4 5 кожний з R , R , R , R і R незалежно являє собою водень, C1-6 алкіл, арил, арилалкіл, циклоалкіл, циклогетероалкіл, гетероарил, гетероарилалкіл, ацилалкілоксикарбоніл, ацилоксіалкілоксикарбоніл, ацилалкілоксикарбоніламіно, ацилоксіалкілоксикарбоніламіно, C1-6 алкокси, алкоксикарбоніл, алкоксикарбонілалкокси, алкоксикарбонілалкіламіно, алкілсульфініл, алкілсульфоніл, алкілтіо, аміно, алкіламіно, арилалкіламіно, діалкіламіно, арилалкокси, арилалкоксикарбонілалкокси, арилалкоксикарбонілалкіламіно, арилоксикарбоніл, арилоксикарбонілалкокси, арилоксикарбонілалкіламіно, карбокси, карбамоїл, карбамат, карбонат, ціано, галоген, гетероарилоксикарбоніл, гідрокси, фосфат, фосфонат, сульфат, 1 2 3 4 5 сульфонат або сульфонамід; R , R , R , R , і R необов'язково містять в якості замісників ізотопи 2 3 13 15 17 18 18 31 32 35 36 H (дейтерій), H (тритій), C, N, O, O, F, P, P, S і Cl; 2 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 «*» означає атом вуглецю, який може бути оптично активним. Сполуки згідно з даним винаходом включають (R)-ізомери, (S)-ізомери і суміші (R)- і (S)ізомерів. ДОКЛАДНИЙ ОПИС У даному винаході запропоновані сполуки, фармацевтичні композиції й способи фармакологічного лікування ожиріння й пов'язаних із ним захворювань і/або розладів. У даному винаході також запропоновані способи синтезу нових речовин для придушення апетиту. Визначення Сполуки згідно з даним винаходом можуть містити один або більше хіральних центрів і/або подвійних зв'язків і тому можуть існувати в якості стереоізомерів, таких як ізомери за подвійним зв'язком (тобто геометричні ізомери), енантіомери або діастереоізомери. Відповідно, хімічні структури, зображені в даному документі, охоплюють усі можливі енантіомери і стереоізомери наведених в якості ілюстрації сполук, включаючи стереоізомерно чисту форму (наприклад, геометрично чисту, енантіомерно чисту або діастереомерно чисту) і суміші енантіомерів і стереоізомерів. Суміші енантіомерів і стереоізомерів можуть бути розділені на складові енантіомери або стереоізомери із застосуванням методик поділу або методик хірального синтезу, добре відомих фахівцям у даній області. Сполуки згідно з даним винаходом можуть також існувати у декількох таутомерних формах, включаючи енольну форму, кетоформу і їх суміші. Відповідно, хімічні структури, зображені в даному документі, охоплюють усі можливі таутомерні форми наведених в якості ілюстрації сполук. Сполуки згідно з даним винаходом також включають мічені ізотопами сполуки, в яких один або більше атомів мають атомну масу, відмінну від атомної маси атомів, що зазвичай зустрічаються у природі. Приклади ізотопів, які можуть бути включені в сполуки згідно з даним винаходом, включають, але не обмежуються 2 3 13 15 18 17 31 32 35 18 36 ними H, H, C, N, O, O, P, P, S, F і Cl. "Алкіл" означає насичений або ненасичений, розгалужений, лінійний або циклічний моновалентний вуглеводневий радикал, отриманий шляхом видалення одного атома водню від одного атома вуглецю вихідного алкану, алкену або алкіну. Типові алкільні групи включають, але не обмежуються ними, метил; етили, такі як етаніл, етеніл, етиніл; пропіли, такі як пропан-1іл, пропан-2-іл, циклопропан-1-іл, проп-1-ен-1-іл, проп-1-ен-2-іл, проп-2-ен-1-іл (аліл), циклопроп-1-ен-1-іл, циклопроп-2-ен-1-іл, проп-1-ін-1-іл, проп-2-ін-1-іл і т.п.; бутили, такі як бутан-1-іл, бутан-2-іл, 2-метил-пропан-1-іл, 2-метил-пропан-2-іл, циклобутан-1-іл, бут-1-ен-1-іл, бут-1-ен-2-іл, 2-метил-проп-1-ен-1-іл, бут-2-ен-1-іл, бут-2-ен-2-іл, бута-1,3-дієн-1-іл, бута-1,3дієн-2-іл, циклобут-1-ен-1-іл, циклобут-1-ен-3-іл, циклобута-1,3-дієн-1-іл, бут-1-ин-1-іл, бут-1-ин3-іл, бут-3-ин-1-іл і т.п. Термін "C1-6 алкіл" охоплює C1 алкіл, C2 алкіл, C3 алкіл, C4 алкіл, C5 алкіл і С6 алкіл. Термін "алкіл", як передбачається, конкретно включає радикали, що мають будь-який ступінь або рівень насичення, тобто групи, що мають винятково одинарні зв'язки вуглецьвуглець, групи, що мають один або більше подвійних зв'язків вуглець-вуглець, групи, що мають один або більше потрійних зв'язків вуглець-вуглець і групи, що мають комбінацію одинарних, подвійних і потрійних зв'язків вуглець-вуглець. У випадку коли передбачається конкретний рівень насичення, використовують вираження "алканіл", "алкеніл" і "алкініл". Переважно алкільна група містить 1-20 атомів вуглецю, більш переважно від 1 до 10 атомів вуглецю. Термін "алкілен" означає видалення атома водню з "алканілу". "Алканіл" означає насичений розгалужений, лінійний або циклічний алкільний радикал, отриманийшляхом видалення одного атома водню від одного атома вуглецю вихідного алкану. Типові алканільні групи включають, але не обмежуються ними, метаніл, етаніл, пропаніли, такі як пропан-1-іл, пропан-2-іл (ізопропіл), циклопропан-1-іл і т.п.; бутаніли, такі як бутан-1-іл, бутан2-іл (втор-бутил), 2-метил-пропан-1-іл (ізобутил), 2-метил-пропан-2-іл (т-бутил), циклобутан-1-іл і т.п. "Алкеніл" означає ненасичений розгалужений, лінійний або циклічний алкільний радикал, що має щонайменше один подвійний зв'язок вуглець-вуглець, отриманий шляхом видалення одного атома водню від одного атома вуглецю вихідного алкену. Дана група може мати конформацію цис або транс щодо подвійного(их) зв'язку(ів). Типові алкенільні групи включають, але не обмежуються ними, етаніл; пропеніли, такі як проп-1-ен-1-іл, проп-1-ен-2-іл, проп-2-ен-1іл (аліл), проп-2-ен-2-іл, циклопроп-1-ен-1-іл, циклопроп-2-ен-1-іл; бутеніли, такі як бут-1-ен-1-іл, бут-1-ен-2-іл, 2-метилпроп-1-ен-1-іл, бут-2-ен-1-іл, бут-2-ен-2-іл, бута-1,3-дієн-1-іл, бута-1,3-дієн2-іл, циклобут-1-ен-1-іл, циклобут-1-ен-3-іл, циклобута-1,3-дієн-1-іл і т.п. "Алкілен" означає бівалентний радикал, який являє собою розгалужений або нерозгалужений вуглеводневий фрагмент, що містить конкретну кількість атомів вуглецю та має дві точки приєднання. Алкілени необов'язково містять один, два або три замісники. Термін "C 1-6 3 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 алкілен" охоплює C1 алкілен, С2 алкілен, C3 алкілен, C4 алкілен, C5 алкілен, С6 алкілен, і будьякий їх піддіапазон. Приклади алкіленів включають, без обмеження: метилен (-CH2-, C1 алкілен), етилен (-CH2CH2-, С2 алкілен), пропілен (-CH2CH2CH2-, C3 алкілен), і бутилен (-CH2CH2CH2CH2-, C4 алкілен). "Алкініл" означає ненасичений розгалужений, лінійний або циклічний алкільний радикал, що містить щонайменше один потрійний зв'язок вуглець-вуглець, отриманий шляхом видалення одного атома водню від одного атома вуглецю вихідного алкіну. Типові алкільні групи включають, але не обмежуються ними, етиніл; пропініли, такі як проп-1-ін-1-іл, проп-2-ін-1-іл і т.п.; бутиніли, такі як бут-1-ин-1-іл, бут-1-ин-3-іл, бут-3-ин-1-іл і т.п. "Ацил" означає радикал -C(O)R, де R являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, форміл, ацетил, циклогексилкарбоніл, циклогексилметилкарбоніл, бензоїл, бензилкарбоніл. "Ацилоксіалкілоксикарбоніл" означає радикал -C(O)OCR'R”OC(O)R’’’, де кожний з R", R" і R’’’ незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, -С(O)OСН2OC(O)СН3, С(O)OСН2OC(O)СН2СН3, -С(O)OСН(СН3)OC(O)СН2СН3, -С(O)OСН(СН3)OC(O)С6Н5. "Ацилалкілоксикарбоніл" означає радикал -C(O)OCR'R”C(O)R’’’, де кожний з R", R" і R’’’ незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, -С(O)OСН2С(O)СН3, -С(O)OСН2С(O)СН2СН3, С(O)OСН(СН3)С(O)СН2СН3, -С(O)OСН(СН3)С(O)С6Н5. "Ацилоксіалкілоксикарбоніламіно" означає радикал -NRC(O)OCR'R”OC(O)R’’’, де кожний з R, R", R" і R’’’ незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, -NHC(O)OCH2OC(O)CH3, NHC(O)OCH2 OC(O)CH2CH3, -NHC(O)OCH(CH3)OC(O)CH2CH3, -NHC(O)OCH(CH3)OC(O)C6H5. "Ацилалкілоксикарбоніламіно" означає радикал -NRC(O)OCR'R”C(O)R”’, де кожний з R, R", R" і R’” незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, -NHC(O)OCH2C(O)CH3, NHC(O)OCH2C(O)CH2CH3, -NHC(O)OCH(CH3)C(O)CH2CH3, -NHC(O)OCH(CH3)C(O)C6H5. "Алкіламіно" означає радикал -NHR, де R являє собою алкільну або циклоалкільну групу, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, метиламіно, етиламіно, 1-метилетиламіно, циклогексиламіно. "Алкокси" означає радикал -OR, де R являє собою алкільну або циклоалкільну групу, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними метокси, етокси, пропокси, бутокси, циклогексилокси. "Алкоксикарбоніл" означає радикал -C(O)-алкокси, де алкокси визначений у даному документі. "Алкоксикарбонілалкокси" означає радикал -OCR'R'C(O)-алкокси, де алкокси визначений у даному документі. Аналогічним чином, кожний з R" і R" незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, OCH2C(O)OCH3, -OCH2C(O)OCH2CH3, -OСН(СН3)С(O)OСН2СН3, -OСН(C6Н5)С(O)OСН2СН3, OCH(CH2C6H5)C(O)OCH2CH3, -OC(CH3)(CH3)C(O)OCH2CH3. "Алкоксикарбонілалкіламіно" означає радикал -NRCR'R'C(O)-алкокси, де алкокси визначений у даному документі. Аналогічним чином, кожний з R, R", R" і R" незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не 4 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 обмежуються ними, -NHCH2C(O)OCH3, -N(CH3)CH2C(O)OCH2CH3, -NHCH(CH3)C(O)OCH2CH3, NHCH(C6H5)C(O)OCH2CH3, -NHCH(CH2C6H5)C(O)OCH2CH3 і -NHC(CH3)(CH3)C(O)OCH2CH3. "Алкілсульфоніл" означає радикал -S(O)2R, де R являє собою алкільну або циклоалкільну групу, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, метилсульфоніл, етилсульфоніл, пропілсульфоніл і бутилсульфоніл. "Алкілсульфініл" означає радикал -S(O)R, де R являє собою алкільну або циклоалкільну групу, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, метилсульфініл, етилсульфініл, пропілсульфініл і бутилсульфініл. "Алкілтіо" означає радикал -SR, де R являє собою алкільну або циклоалкільну групу, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, метилтіо, етилтіо, пропілтіо й бутилтіо. "Арил" означає моновалентний ароматичний вуглеводневий радикал, отриманий шляхом видалення одного атома водню від одного атома вуглецю вихідної ароматичної кільцевої системи. Типові арильні групи включають, але не обмежуються ними, групи, отримані з ацеантрилену, аценафтилену, ацефенантрилену, антрацену, азулену, бензолу, хризену, коронену, флуорантену, флуорену, гексацену, гексафену, гексалену, ас-індацену, вторіндацену, індану, індену, нафталіну, октацену, октафену, окталену, овалену, пента-2,4-дієну, пентацену, пенталену, пентафену, перилену, феналену, фенантрену, піцену, плеїдену (pleidene), пірену, пірантрену, рубіцену, трифенілену, тринафталіну (trinaphthalene). Переважно арильна група містить від 6 до 20 атомів вуглецю, більш переважно від 6 до 12 атомів вуглецю. "Арилалкіл" означає ациклічний алкіл, у якому один із атомів водню пов'язаний з атомом 3 вуглецю, як правило кільцевим атомом вуглецю або атомом вуглецю в sp -гібридизації, замінений на арильну групу. Як правило, арилалкільні групи включають, але не обмежуються ними, бензил, 2-фенілетан-1-іл, 2-фенілетен-1-іл, нафтилметил, 2-нафтилетан-1-іл, 2нафтилетен-1-іл, нафтобензил, 2-нафтофенілетан-1-іл. Якщо передбачаються конкретні алкільні фрагменти, застосовується номенклатура арилалканіл, арилалкеніл і/або арилалкініл. Переважно арилалкільна група являє собою (C6-С30)арилалкіл, наприклад алканільний, алкенільний або алкінільний фрагмент арилалкільної групи являє собою (C1-C10), а арильний фрагмент являє собою (C6-С20), більш переважно арилалкільна група являє собою (C6-С20) арилалкільний, наприклад алканільний, алкенільний або алкінільний фрагмент арилалкільної групи являє собою (C1-C8), а арильний фрагмент являє собою (C6-C12). "Арилалкокси" означає -O-арилалкільний радикал, де арилалкіл визначений в даному документі й необов'язково може містити один або більше замісників, визначених у даному документі. "Арилалкоксикарбонілалкокси" означає радикал -OCR'R”C(O)-арилалкокси, де арилалкокси визначений в даному документі. Аналогічним чином, R" і R" незалежно являють собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, OCH2C(O)OCH2C6H5, -OCH(CH3)C(O)OCH2C6H5, -OCH(C6H5)C(O)OCH2C6H5, OCH(CH2C6H5)C(O)OСН2C6Н5, -OC(СН3)(СН3)С(O)OCH2C6H5. "Арилалкоксикарбонілалкіламіно" означає радикал -NRCR'R'C(O)-арилалкокси, де арилалкокси визначений в даному документі. Аналогічним чином, кожний з R, R", R" і R" незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, -NHCH2C(O)OCH2C6H5, N(CH3)CH2C(O)OCH2C6H5, -NHCH(CH3)C(O)OCH2C6H5, -NHCH(C6H5)C(O)OCH2C6H5, NHCH(CH2C6H5)C(O)OCH2C6H5, -NHC(CH3)(CH3)C(O)OCH2C6H5. "Арилоксикарбоніл" означає радикал -C(O)-O-арил, де арил визначений в даному документі та необов'язково може містити один або більше замісників, визначених у даному документі. "Арилоксикарбонілалкокси" означає радикал -OCR'R'C(O)-арилокси, де арилокси визначений в даному документі. Аналогічним чином, кожний з R" і R" незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, -OCН2С(O)OC6Н5, -OCH(СН3)С(O)OC6Н5, -OCН(C6Н5)С(O)OC6Н5, 5 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 OCH(СН2C6Н5)С(O)OC6Н5, -OC(СН3)(СН3)С(O)OС6Н5. "Арилоксикарбонілалкіламіно" означає радикал -NRCR'R'C(O)-арилокси, де арилокси визначений в даному документі. Аналогічним чином, кожний з R, R", R" і R" незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, -NHCH2C(O)OC6H5, -N(CH3)CH2C(O)OC6H5, -NHCH(CH3)C(O)OC6H5, NHCH(C6H5)C(O)OC6H5, -NHCH(CH2C6H5)C(O)OC6H5, -NHC(CH3)(CH3)C(O)OC6H5. "Карбамоїл" означає радикал -C(O)NRR, де кожна група R незалежно являє собою, водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. "Карбамат" означає радикал-NR'C(O)OR", де кожний з R" і R" незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, метилкарбамат (-NHC(O)OCH3), етилкарбамат (-NHC(O)OCH2CH3), бензилкарбамат (-NHC(O)OCH2C6H5). "Карбонат" означає радикал -OC(O)OR, де R являє собою алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними, метилкарбонат (-C(O)OCH3), циклогексилкарбонат (-С(O)OC6Н11), фенілкарбонат (-C(O)OC6H5), бензилкарбонат (-C(O)OCH2C6H5). "Діалкіламіно" означає радикал -NRR", де R і R' незалежно являють собою алкільну або циклоалкільну групи, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. Ілюстративні приклади включають, але не обмежуються ними диметиламіно, метилетиламіно, ди-(1-метилетил)аміно, (циклогексил)(метил)аміно, (циклогексил)(етил) аміно, (циклогексил)(пропіл)аміно. "Галоген" означає фтор, хлор, бром або йод. "Гетероарил" означає одновалентний гетероароматичний радикал, отриманий шляхом видалення одного атома водню від одного атома вихідної гетероароматичної кільцевої системи. Типові гетероарильні групи включають, але не обмежуються ними, групи, отримані з акридину, арсиндолу, карбазолу, карболіну, хроману, хромену, цинноліну, фурану, імідазолу, індазолу, індолу, індоліну, індолізину, ізобензофурану, ізохромену, ізоіндолу, ізоіндоліну, ізохіноліну, ізотіазолу, ізоксазолу, нафтиридину, оксадіазолу, оксазолу, перимідину, фенантридину, фенантроліну, феназину, фталазину, птеридину, пурину, пірану, піразину, піразолу, піридазину, піридину, піримідину, піролу, піролізину, хіназоліну, хіноліну, хінолізину, хіноксаліну, тетразолу, тіадіазолу, тіазолу, тіофену, триазолу, ксантену. Переважно гетероарильна група являє собою 5-20 членний гетероарил, де 5-10 членний гетероарил є особливо переважним. Переважними гетероарильними групами є гетероарильні групи, отримані з тіофену, піролу, бензотіофену, бензофурану, індолу, піридину, хіноліну, імідазолу, оксазолу і піразину. "Гетероарилоксикарбоніл" означає радикал -C(O)-OR, де R являє собою гетероарил, визначений в даному документі, який необов'язково може містити один або більше замісників, визначених у даному документі. "Гетероарилалкіл" означає ациклічний алкільний радикал, в якому один із атомів водню, 3 пов'язаних із атомом вуглецю, як правило кільцевим атомом вуглецю або атомом вуглецю в sp гібридизації, замінений на гетероарильну групу. Переважно гетероарилалкільний радикал являє собою гетероарилалкіл з 6-30 атомами вуглецю, наприклад алканільний, алкенільний або алкінільний фрагмент гетероарилалкілу є 1-10-членним, а гетероарильний фрагмент являє собою 5-20-членний гетероарил, більш переважно 6-20-членний гетероарилалкіл, наприклад алканільний, алкенільний або алкінільний фрагмент гетероарилалкілу є 1-8-членним, а гетероарильний фрагмент являє собою 5-12-членний гетероарил. "Ізомер" означає сполуки згідно з даним винаходом, до складу яких входять асиметричні атоми вуглецю (оптичні центри) або подвійні зв'язки, при цьому передбачається, що рацемати, діастереомери, енантіомери, геометричні ізомери, структурні ізомери й індивідуальні ізомери, охоплені обсягом даного винаходу. У даному документі термін "пацієнт" охоплює пацієнтів, що є ссавцями. Приклади ссавців включають, але не обмежуються ними, будь-яких представників класу ссавців: людей, приматів, що не відносяться до людей, таких як шимпанзе, і інших мавп (apes) і видів мавп (monkey); 6 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 сільськогосподарських тварин, таких як велика рогата худоба, коні, вівці, кози, свині; свійських тварин, таких як кролики, собаки і кішки; лабораторних тварин, включаючи гризунів, таких як пацюки, миші й морські свинки. "Фармацевтично прийнятний" означає схвалений або підлягаючий схваленню регулювальним органом Федерального або державного уряду або наведений у Фармакопеї США або будь-якій іншій загальновизнаній фармакопеї для застосування для тварин і, більш конкретно, для людей. "Фармацевтично прийнятна сіль" означає сіль сполуки згідно з даним винаходом, яка є фармацевтично прийнятною та має необхідну фармакологічну активність вихідної сполуки. Такі солі включають: (1) солі приєднання кислоти, утворені неорганічними кислотами, такими як соляна кислота, бромистоводнева кислота, сірчана кислота, азотна кислота, фосфорна кислота; або утворені органічними кислотами, такими як оцтова кислота, пропіонова кислота, гексанова кислота, циклопентанпропіонова кислота, гліколева кислота, піровиноградна кислота, молочна кислота, малонова кислота, бурштинова кислота, яблучна кислота, малеїнова кислота, фумарова кислота, винна кислота, лимонна кислота, бензойна кислота, 3-(4гідроксибензоїл)бензойна кислота, корична кислота, мигдальна кислота, метансульфонова кислота, етансульфонова кислота, 1,2-етандисульфонова кислота, 2-гідроксіетансульфонова кислота, бензолсульфонова кислота, 4-хлорбензолсульфонова кислота, 2-нафталінсульфонова кислота, 4-толуолсульфонова кислота, камфорсульфонова кислота, 4-метилбіцикло[2,2,2]-окт2-ен-1-карбонова кислота, глюкогептонова кислота, 3-фенілпропіонова кислота, триметилоцтова кислота, трет-бутилоцтова кислота, лаурилсірчана кислота, глюконова кислота, глутамінова кислота, гідроксинафтойна кислота, саліцилова кислота, стеаринова кислота, муконова кислота; або (2) солі, утворені таким чином, що кислотний протон, який присутній у вихідній сполуці, замінений іоном металу, наприклад, іоном лужного металу, іоном лужноземельного металу або іоном алюмінію; або координується з органічною основою, такою як етаноламін, діетаноламін, триетаноламін або N-метилглюкамін. "Фармацевтично прийнятний формотворний компонент" означає розріджувач, ад'ювант, допоміжну речовину або носій, з яким уводять сполуку згідно з даним винаходом. "Фосфат" означає радикал-OP(O)(OR")(OR"), де кожний з R' і R" незалежно являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. "Фосфонат" означає радикал -P(O)(OR")(OR"), де кожний з R' і R" незалежно являють собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. "Запобігаючий" або "запобігання" означає зменшення ризику виникнення захворювання або розладу (тобто забезпечення того, що щонайменше один із клінічних симптомів захворювання не розвивається у пацієнта, який підданий або схильний до захворювання, але ще не відчуває симптомів захворювання або в нього ще не проявляються симптоми захворювання). "Захисна група" означає групу атомів, яка при приєднанні до реакційноздатної групи молекули маскує, зменшує або запобігає її реакційну здатність. Приклади захисних груп можуть nd бути виявлені в джерелах Green et al., "Protective Groups in Organic Chemistry", (Wiley, 2 ed. 1991) і Harrison et al., "Compendium of Synthetic Organic Methods", vols. 1-8 (John Wiley і Sons, 1971-1996). Ілюстративні амінозахисні групи включають, але не обмежуються ними, форміл, ацетил, трифторацетил, бензил, бензилоксикарбоніл ("CBZ"), трет-бутоксикарбоніл ("Boc"), триметилсиліл ("TMS"), 2-триметилсилілетансульфоніл ("SES"), тритильні та заміщені тритильні групи, алілоксикарбоніл, 9-флуоренілметилоксикарбоніл ("FMOC"), нітровератрилоксикарбоніл ("NVOC"). Ілюстративні гідроксизахисні групи включають, але не обмежуються ними, групи, в яких гідроксильна група або ацилована, або алкілована, такі як бензил і триалкілсилільні прості ефіри й алільні прості ефіри. "Рацемат" означає еквімолярну суміш енантіомерів хіральної молекули. "Спейсер" означає C1-6 алкілен, у якому один або більше атомів вуглецю зазначеного C 1-6 6 6 алкілену необов'язково може бути замінений на O, S або NR , де R може являти собою H або C1-6 алкіл. C1-6 алкілен необов'язково містить замісники. У деяких аспектах C 1-6 алкілен необов'язково містить в якості замісників ацилалкілоксикарбоніл, ацилоксіалкілоксикарбоніл, ацилалкілоксикарбоніламіно, алкокси, алкоксикарбоніл, ацилоксіалкілоксикарбоніламіно, алкоксикарбонілалкокси, алкоксикарбонілалкіламіно, алкілсульфініл, алкілсульфоніл, алкілтіо, аміно, алкіламіно, арилалкіламіно, діалкіламіно, арилалкокси, арилалкоксикарбонілалкокси, арилалкоксикарбонілалкіламіно, арилоксикарбоніл, арилоксикарбонілалкокси, 7 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 арилоксикарбонілалкіламіно, карбокси, карбамоїл, карбамат, карбонат, ціано, галоген, гетероарилоксикарбоніл, гідрокси, фосфат, фосфонат, сульфат, сульфонат або сульфонамід. "Заміщений" ("містить замісники") означає групу, в якій один або більше атомів водню кожний незалежно замінений на однаковий(і) або різний(і) замісник(и). Типові замісники 54 54 54 54 55 54 включають, але не обмежуються ними, -X, -R , -O-, =O, -OR , -SR , -S, =S, -NR R , =NR , 54 31 CX3, -CF3, -CN, -OCN, -SCN, -NO, -NO2, =N2, -N3, -S(O)2O-, -S(O)2OH, -S(O)2OR , -OS(O)2O , 54 14 31 54 55 54 54 54 OS(O)2R , -P(O)(O-)2, -P(O)(OR )(O ), -OP(O)(OR )(OR ), -C(O)R , -C(S)R , -C(O)OR , 54 55 54 56 54 55 56 54 55 57 56 54 55 C(O)NR R , -C(O)O-, -C(S)OR , -NR C(O)NR R , -NR C(S)NR R , -NR C(NR )NR R і 56 54 55 54 55 56 57 C(NR )NR R , де кожний X незалежно являє собою галоген; кожний з R , R , R і R незалежно являє собою водень, алкіл, заміщений алкіл, арил, заміщений арил, арилалкіл, заміщений арилалкіл, циклоалкіл, заміщений циклоалкіл, циклогетероалкіл, заміщений циклогетероалкіл, гетероалкіл, заміщений гетероалкіл, гетероарил, заміщений гетероарил, гетероарилалкіл, заміщений гетероарилалкіл. "Сульфат" означає радикал -OS(O)(O)OR, де R являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. "Сульфонамід" означає радикал -S(O)(O)NR'R", де R' і R" незалежно являють собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі, або необов'язково R' і R", разом із атомом, до якого вони обидва приєднані, утворюють циклогетероалкільне або заміщене циклогетероалкільне кільце. Ілюстративні приклади включають, але не обмежуються ними, азетидинільну, піролідинільну, піперидинільну, морфолінільну, 4-(NR’”)-піперазинільну або імідазолільну групу, де зазначена група необов'язково може містити один або більше замісників, визначених у даному документі. R'” являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. "Сульфонат" означає радикал -S(O)(O)OR, де R являє собою водень, алкіл, циклоалкіл, циклогетероалкіл, арил, арилалкіл, гетероалкіл, гетероарил, гетероарилалкіл, визначені в даному документі, які необов'язково можуть містити один або більше замісників, визначених у даному документі. "Тіо" означає радикал -SH. "Лікуючий" або "лікування" будь-якого захворювання або стану означає, в одному з варіантів реалізації даного винаходу, полегшення захворювання або розладу (тобто припинення або зменшення розвитку захворювання або щонайменше одного з його клінічних симптомів). В іншому варіанті реалізації "лікуючий" або "лікування" означає поліпшення щонайменше одного фізичного параметра, який може не бути помітним для пацієнта. У ще одному варіанті реалізації даного винаходу "лікуючий" або "лікування" означає придушення захворювання або розладу, фізично (наприклад, шляхом стабілізації помітного симптому), психологічно (наприклад, шляхом стабілізації фізичного параметра) або обома зі зазначених способів. "Терапевтично ефективна кількість" означає кількість сполуки, яка при введенні пацієнту для лікування захворювання достатня для забезпечення ефекту такого лікування захворювання. "Терапевтично ефективна кількість" змінюється залежно від сполуки, захворювання і його тяжкості, а також віку, ваги й інших характеристик пацієнта, що зазнає лікування, і може бути визначена фахівцем без зайвих експериментів. Сполуки згідно з винаходом У даному винаході запропоновані похідні фенілциклоалкілметиламіну формули (I): , або їх ізомер або фармацевтично прийнятна сіль, де: n становить 0, 1, 2, 3, 4 або 5; переважно n становить 0 (циклопропіл), 1 (циклобутил), 2 (циклопентил) або 3 (циклогексил), і більш переважно n становить 1. SP являє собою спейсер, де зазначений спейсер являє собою C 1-6 алкілен, і при цьому один 6 або більше атомів вуглецю зазначеного C1-6 алкілену необов'язково заміщені O, S або NR , де 6 R являє собою H або C1-6 алкіл; 8 UA 114807 C2 6 5 10 15 20 25 30 35 40 45 50 55 60 X являє собою O, S, NR або S(O)(O); 1 2 3 4 5 кожний R , R , R , R і R незалежно являє собою водень, C1-6 алкіл, арил, арилалкіл, циклоалкіл, циклогетероалкіл, гетероарил, гетероарилалкіл, ацилалкілоксикарбоніл, ацилоксіалкілоксикарбоніл, ацилалкілоксикарбоніламіно, ацилоксіалкілоксикарбоніламіно, C1-6 алкокси, алкоксикарбоніл, алкоксикарбонілалкокси, алкоксикарбонілалкіламіно, алкілсульфініл, алкілсульфоніл, алкілтіо, аміно, алкіламіно, арилалкіламіно, діалкіламіно, арилалкокси, арилалкоксикарбонілалкокси, арилалкоксикарбонілалкіламіно, арилоксикарбоніл, арилоксикарбонілалкокси, арилоксикарбонілалкіламіно, карбокси, карбамоїл, карбамат, карбонат, ціано, галоген, гетероарилоксикарбоніл, гідрокси, фосфат, фосфонат, сульфат, 1 2 3 4 5 2 сульфонат або сульфонамід; R , R , R , R і R необов'язково заміщений ізотопами H 3 13 15 17 18 18 31 32 35 36 (дейтерій), H (тритій), C, N, O, O, F, P, P, S і Cl; і «*» означає атом вуглецю, який може бути оптично активним. Сполуки згідно з даним винаходом включають (R)-ізомери, (S)-ізомери і суміші (R)- і (S)ізомерів. В одному з варіантів реалізації даного винаходу сполуки являють собою оптично чисті (R)-ізомери, оскільки вони часто є більш активними. В іншому варіанті реалізації сполуки являють собою оптично чисті (S)-ізомери. В іншому варіанті реалізації сполуки є рацемічними сполуками. 1 2 В одному з переважних варіантів реалізації даного винаходу R і R незалежно являють собою H, C1-6 алкокси (наприклад, метокси, етокси), галоген (наприклад, фтор, хлор) або гідроксил. 3 В одному з переважних варіантів реалізації даного винаходу R являє собою H або C1-6 алкіл (наприклад, ізобутил). 4 В одному з переважних варіантів реалізації даного винаходу R являє собою H. В одному з переважних варіантів реалізації даного винаходу SP являє собою C 1-6 алкілен. 5 В одному з переважних варіантів реалізації даного винаходу R являє собою C1-6 алкіл. 6 В одному з переважних варіантів реалізації даного винаходу R являє собою C1-6 алкіл. Описані в даному документі сполуки згідно з даним винаходом можуть мати одну або більше наступних характеристик або властивостей: 1. Сполуки згідно з даним винаходом можуть мати властивості інгібування переносника допаміну (DAT), переносника норепінефрину (NET) і переносника серотоніну (SERT); 2. Пероральна біодоступність сполуки відповідає пероральному введенню із застосуванням стандартних фармакологічних сполук для перорального введення, однак сполуки і їх композиції також можна вводити із застосуванням будь-якої системи доставки, яка забезпечує постійний та контрольований рівень у крові протягом часу. У деяких варіантах реалізації даного винаходу в даному винаході запропоновані сполуки, що мають дві або більше зі зазначених вище характеристик або властивостей. У переважному варіанті реалізації сполуки згідно з даним винаходом мають всі чотири характеристики або властивості. Фахівцями можуть бути легко зроблені додаткові модифікації сполук, запропонованих у даному винаході. Таким чином, аналоги і солі наведених в якості прикладів сполук входять в обсяг даного винаходу. Знаючи сполуки згідно з даним винаходом, кваліфікований хімік може використовувати відомі методики для синтезу даних сполук із доступних джерел. У даному документі термін "похідні" означає сполуки, які є по суті такими самими, як інша сполука, але можуть бути модифіковані, наприклад, шляхом уведення додаткових бічних груп. Термін "похідні" у даному документі також може означати сполуки, які є по суті такими самими, як інша сполука, але мають атомне або молекулярне заміщення у певних місцях сполуки. Даний винахід також відноситься до енантіомерно виділених сполук і композицій, що містять дані сполуки. Виділені енантіомерні форми сполуки згідно з даним винаходом по суті не містять інших форм (тобто перебувають в енантіомерному надлишку). Інакше кажучи, R-форми сполуки по суті не містять S-форм сполуки і, таким чином, перебувають в енантіомерному надлишку стосовно S-форм. Навпроти, S-форми сполуки по суті не містять R-форм сполуки і, таким чином, перебувають в енантіомерному надлишку стосовно R-форм. В іншому варіанті реалізації даного винаходу виділені енантіомерні сполуки перебувають щонайменше в 80 % енантіомерному надлишку. У переважному варіанті реалізації сполуки перебувають щонайменше приблизно в 90 %, 95 %, 97 % або 99 % енантіомерному надлишку. Синтез сполук згідно з даним винаходом Сполуки згідно з даним винаходом можуть бути отримані за допомогою способів синтезу, представлених на схемах 1. У рівні техніки описані різні способи синтезу аналогів циклоалкілметиламінів (див., наприклад, патент США № 5596019; WO 2004/096202; WO 02/083631; WO 02/36540; WO 02/060424; Jeffery, J. E. et al., J. Chem. Soc. Perkin Trans 1, 1996, 9 UA 114807 C2 5 10 15 20 25 30 35 2583-2589.). У рівні техніки відомі й інші способи синтезу циклоалкілметиламінів, які легко доступні фахівцю в даній області. Вихідні речовини і проміжні сполуки, застосовувані в синтезі цільових молекул (схеми 1-8), доступні у продажі або можуть бути отримані за допомогою встановлених методик (див., наприклад, Green et al., "Protective Groups in Organic Synthesis, rd ’’(Wiley, 4 ed., 2006); Harrison et al "Compendium of Synthetic Organic Methods, ” vols. 1-8 (John Wiley and Sons, 1971-1996); "Beilstein Handbook of Organic Chemistry, Frankfurt, Germany; Feiser et al, "Reagents for Organic Synthesis, ” Volumes 1-45, Karger, 1991; March, Advanced Organic th Chemistry, ” Wiley Interscience, 4 ed., 1992; Larock "Comprehensive Organic Transformations, ” nd Wiley-vch Publishers, 2 ed., 1999; Paquette, "Encyclopedia of Reagents for Organic Synthesis, ” st John Wiley and Sons, 1 ed., 1995). Відповідно, вихідні речовини, які підходять для одержання сполук згідно з даним винаходом і їх проміжних сполук, доступні у продажі або можуть бути отримані за допомогою добре відомих способів синтезу. Інші способи синтезу циклоалкілметиламінів, описаних у даному документі, або описані в рівні техніки, або очевидні фахівцю в даній області з урахуванням наведених вище посилань та можуть бути застосовані для синтезу сполук згідно з даним винаходом. Відповідно, способи, представлені на схемах у даному описі, є ілюстративними, але не обмежуючими. Способи Відповідно до одного зі способів, похідні фенілциклоалкілметиламіну (7, 8) формули (I) одержують, як описано на схемі 2. Вихідні блоки фенілциклоалкіламіну (6) одержують шляхом модифікації методики, описаної Джеффері зі співавторами (Jeffery et al.) (J. Chem. Soc., Perkin Trans. 1, 1996, 2583-2589), як показано на схемі 1. Типова методика включає реакцію 3 циклоалкілнітрилу (3) з відповідним реактивом Гріньяра (R MgBr) у присутності толуолу при температурі початку кипіння (gentle reflux) протягом від 10 до 24 годин із наступною обробкою отриманої проміжної сполуки боргідридом натрію в метанолі або етанолі з одержанням відповідного циклоалкілметиламіну (6). Циклоалкілнітрили (3), які використовуються для одержання циклоалкіламінів (6), або здобували в Sigma-Aldrich, або синтезували з відповідних фенілацетонітрилів (1) із використанням стандартних хімічних прийомів. Обрані рацемічні аміни (6) розділяють на відповідні оптично чисті (R)- і (S)-ізомери за допомогою стандартного методу хіральної кристалізації із застосуванням оптично чистої винної кислоти. Фенілциклоалкілметиламіни (6) алкілують відповідними 4-нітрофенілсульфонільними ефірами (9) із застосуванням карбонару цезію в розчиннику, що являє собою N, Nдиметилформамід (ДМФA), при кімнатній температурі з одержанням відповідних циклоалкілметиламінефірних похідних (7, 8) із виходами від помірного до гарного, як показано на схемі 2. Вихідні блоки 4-нітрофенілсульфонільних ефірів (9) синтезують, як показано на схемі 6. 40 10 UA 114807 C2 5 10 Згідно з іншим способом, ефірні похідні фенілциклоалкілметиламіну (7, 8) одержують за допомогою комбінації з відповідними алкоксіалкілкарбоновими кислотами (10) з наступним відновленням амідних проміжних сполук (11) алюмогідридом літію (LAH) у безводному ТГФ із помірними виходами, як показано на схемі 2. Алкоксіалкілкарбонові кислоти (10) одержують, як показано на схемі 7. Згідно з іншим способом, похідні фенілциклоалкілметиламіну (12, 13) формули (I) одержують, як описано на схемі 3. Фенілциклоалкіламіни (6) піддають реакції комбінації з відповідними алкілтіоалкілкарбоновими кислотами (14) з одержанням амідів (15), які після відновлення алюмогідридом літію дозволяють одержати відповідні тіоефірні похідні фенілциклоалкілметиламіну (12, 13). Алкілтіоалкілкарбонові кислоти (14) синтезують, як показано на схемі 8. 15 20 Згідно з іншим способом, похідні фенілциклоалкілметиламіну (17) формули (I) одержують, як описано на схемі 4. Фенілциклоалкіламіни (15) окисляють з використанням м-хлорпербензойної кислоти (mcpba) з одержанням амідів (16), які після відновлення алюмогідридом літію дозволяють одержати відповідні похідні фенілциклоалкілметиламіну (17). 11 UA 114807 C2 5 Згідно з іншим способом, похідні фенілциклоалкілметиламіну (19) формули (I) одержують, як описано на схемі 5. Фенілциклоалкіламіни (6) піддають реакції комбінації з відповідними складними ефірами алкіламіноалкілкарбонової кислоти (20) у присутності триметилалюмінію в толуолі з одержанням амідів (21), які після відновлення з використанням розчину комплексу борану з диметилсульфідом (BH3-DMS) у толуолі або LAH у ТГФ дозволяють одержати відповідні похідні фенілциклоалкілметиламіну (19). 10 15 20 25 Оптично чисті похідні (R)- і (S)-фенілциклоалкілметиламіну, що мають формулу I, одержують або з відповідних оптично чистих амінів (6), або піддаючи відповідні рацемічні похідні фенілциклоалкілметиламіну (7, 8, 12, 13, 17 і 19) із застосуванням методів поділу за допомогою хіральної ВЕРХ. Усі похідні фенілциклоалкілметиламіну (7, 8, 12, 13, 17 і 19) перетворюють у відповідні гідрохлоридні солі за допомогою обробки 2 н. розчином HСl в ефірі при стандартних умовах. Вихідні блоки п-нітрофенілсульфонілзахищених ефірів (9), які використовують в синтезі похідних фенілциклоалкілметиламіну, синтезують у чотири стадії, як показано на схемі 6. Монобензилзахищені діоли (24) синтезують шляхом бензилування відповідних діолів (23) із використанням гідриду натрію як основа в безводному тетрагідрофурані (ТГФ) при 0 °C з наступним кип'ятінням реакційної суміші зі зворотним холодильником із забезпеченням гарного виходу. Зазначені бензилзахищені спирти (24) алкілують відповідним алкілгалогенідом із застосуванням як основа гідриду натрію в безводному N, N-диметилформаміді (ДМФА) з одержанням простих ефірів (25). Захисну групу, що захищає бензильну групу, відщеплюють у стандартних умовах гідрування з одержанням відповідного спирту (26), який піддають реакції з п-нітрофенілсульфонілхлоридом із використанням слабкої основи – триетиламіну – у дихлорметановому розчиннику з одержанням п-нітрофенілсульфонілзахищених простих ефірів (9) у загальному з гарними виходами. 30 12 UA 114807 C2 5 Вихідні блоки 4-алкоксіалкілкарбонової кислоти (10) синтезують у дві стадії, як показано на схемі 7. Гамма-бутиролактон (28) піддають реакції з етилортоформіатом (29) у присутності етанолу і сірчаної кислоти з одержанням відповідного складного ефіру 4-етоксибутанової кислоти (30) з гарним виходом. Омилення складного ефіру (30) у стандартних умовах реакції дозволяє одержати відповідну 4-етоксибутанову кислоту (10) з гарним виходом. 10 Вихідні блоки алкілтіоалкілкарбонових кислот (14) синтезують у дві стадії, як показано на схемі 8. Тіолати натрію (32) алкілують бромалкілкарбоновими кислотами (31) у безводному ДМФ із одержанням складних ефірів (33), які після омилення дозволяють одержати відповідні алкілтіоалкілкарбонові кислоти (14). 15 20 25 30 Терапевтичне застосування сполук формули (I) Згідно з різними аспектами, у даному винаході запропоновані способи лікування або запобігання ожиріння, депресії, і пов'язаних супутніх захворювань у хворого. Спосіб включає введення пацієнту, що потребує такого лікування, ефективної кількості будь-якої зі сполук структурної формули (I). В інших аспектах спосіб дозволяє лікувати ожиріння, депресію й пов'язані з ними супутні симптоми. Даний винахід відноситься до способів лікування та профілактики ожиріння й пов'язаних супутніх захворювань. Термін "пов'язані з ожирінням супутні захворювання", який використовується у даному документі, означає медичні стани, які, як відомо фахівцям у даній області, пов'язані з ожирінням. Даний термін включає наступні стани, але не обмежується ними: діабет, включаючи інсулінонезалежний цукровий діабет, порушену толерантність до глюкози, гіпертензію, тромбоз коронарних артерій, інсульт, депресію, тривожність, психози (наприклад шизофренію), пізню дискінезію, наркотичну залежність, зловживання наркотиками, когнітивні розлади, хворобу Альцгеймера, церебральну ішемію, обсесивно-компульсивну поведінку, панічні атаки, соціальні фобії, розлади харчової поведінки, такі як булімія, анорексія, перекуси й 13 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 обжерливість, ліпідні синдроми, гіперглікемію, гіперліпідемію й стрес у ссавців, зокрема людей. Крім того, сполуки, композиції та способи згідно з даним винаходом можуть бути застосовані для лікування або запобігання метаболічних захворювань та виникаючих внаслідок них станів або, наприклад, не пов'язаного з фізичною активністю термогенезу і підвищеної швидкості метаболізму, сексуальної дисфункції, апное в сні, предменструального синдрому, нетримання сечі, включаючи стресове нетримання, гіперактивних розладів, хіатальних гриж і рефлюксезофагіту, болю, особливо невропатичного болю, збільшення ваги, пов'язане з медикаментозним лікуванням, синдрому хронічної втоми, остеоартриту і подагри, раку, пов'язаного зі збільшенням ваги, порушення менструального циклу, жовчних каменів, ортостатичної гіпотензії та легеневої гіпертензії. Сполуки, композиції та способи згідно з даним винаходом можуть бути застосовані для запобігання серцево-судинних захворювань і для зниження адгезивності тромбоцитів, для сприяння зниженню ваги після вагітності, зменшенню тяги до паління та для сприяння зниженню ваги після припинення паління. Даний винахід також може бути застосований для зниження рівня сечової кислоти і рівня ліпідів у ссавців, зокрема людей. Відповідно до винаходу, сполуку і/або композицію, що містить сполуку структурної формули (I) вводять пацієнту, переважно людині, що страждає ожирінням і пов'язаними з ним супутніми захворюваннями і/або розладами. У деяких варіантах реалізації даного винаходу сполуки і/або композиції згідно з даним винаходом вводять пацієнту, переважно людині, в якості превентивного заходу проти різних захворювань або розладів. Таким чином, сполуки і/або композиції, що містять сполуку(и) структурної формули (I), можуть бути введені в якості превентивного заходу пацієнту, що має схильність до ожиріння та пов'язаних із ним супутніх захворювань та/або розладів (див. WO 2004/058237; WO 2004/096202; WO 02/060424; WO 01/51453; WO 01/00205; WO 01/00187; Mueller, P., публікація міжнародної заявки WO 00/32178; WO 98/11884; WO 98/13034). Таким чином, фахівці в даній області можуть легко досліджувати і застосовувати сполуки і/або композиції, що містять сполуку(и) формули (I) для лікування ожиріння й пов'язаних із ним супутніх захворювань та/або розладів. Терапевтичне/профілактичне введення Сполуки і/або композиції згідно з даним винаходом можуть бути введені або нанесені пацієнту окремо або в комбінації з іншими фармацевтично активними агентами. Сполуки і/або композиції згідно з даним винаходом переважно вводять перорально. Сполуки і/або композиції згідно з даним винаходом також можуть бути введені будь-яким іншим зручним шляхом, наприклад за допомогою інфузії або болюсної ін'єкції, за допомогою усмоктування через епітеліальні або слизуваті оболонки (наприклад, слизувату оболонку порожнини рота, ректальну або слизувату оболонку кишечнику і т.п.). Уведення може бути системним або місцевим. Відомі різні системи доставки (наприклад, інкапсулювання в ліпосоми, мікрочастинки, мікрокапсули, капсули тощо), які можуть бути використані для введення сполуки і/або композиції згідно з даним винаходом. Способи введення включають, але не обмежуються ними, внутрішньошкірний, внутрішньом'язовий, внутрішньочеревинний, внутрішньовенний, підшкірний, інтраназальний, епідуральний, пероральний, сублінгвальний, інтраназальний, внутрішньомозковий, інтравагінальний, черезшкірний, ректальний, шляхом інгаляції або місцевий, зокрема для вух, носа, ока або шкіри. Зокрема, у переважних варіантах реалізації даного винаходу сполуки і/або композиції згідно з даним винаходом можуть бути доставлені за допомогою систем із тривалим вивільненням, переважно систем пероральної доставки з уповільненим вивільненням. В одному з варіантів реалізації може бути використаний насос (див. Langer вище; Sefton, 1987, CRC Crit. Ref Biomed. Eng. 14:201; Saudek et al., 1989, N. Engl. J. Med. 321:574). В іншому варіанті реалізації даного винаходу можуть бути використані полімерні матеріали (див. "Medical Applications of Controlled Release, ” Langer and Wise (eds.), Wiley, New York (1984); Ranger and Peppas, 1983, J. Macromol. Sci. Rev. Macromol Chem. 23:61; див. також Levy et al., 1985, Science 228:190; During et al., 1989, Ann. Neurol. 25:351; Howard et al, 1989, J. Neurosurg. 71:105). У переважному варіанті реалізації полімерні матеріали використовують для пероральної доставки з уповільненим вивільненням. Переважні полімери включають карбоксиметилцелюлозу натрію, гідроксипропілцелюлозу, гідроксипропілметилцелюлозу і гідроксіетилцелюлозу (більш переважна гідроксипропілметилцелюлоза). Інші переважні прості ефіри целюлози описані в рівні техніки (Bamba et al., Int. J. Pharm., 1979, 2, 307). В іншому варіанті реалізації для перорального введення з уповільненим вивільненням можуть бути застосовані покриті ентеросолюбільним покриттям препарати. Переважні матеріали для покриття включають полімери із залежною від рН розчинністю (тобто рН 14 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 контрольованим вивільненням), полімери з повільною або залежною від рН швидкістю набрякання, розчинення або ерозії (тобто з контрольованим за часом вивільненням), полімери, які розкладаються ферментами (тобто з контрольованим ферментами вивільненням) і полімери, які утворюють плівкові шари, що руйнуються при збільшенні тиску (тобто з контрольованим тиском вивільненням). У ще одному варіанті реалізації для перорального введення з уповільненим вивільненням застосовують осмотичні системи доставки (Verma et al., Drug Dev. Ind. Pharm., 2000, 26:695708). У переважному варіанті реалізації для пристроїв пероральної доставки з уповільненим вивільненням застосовують осмотичні системи доставки OROS® (Alza Corporation, Mountain View, CA) (див., наприклад, патенти США №№ 3845770 і 3916899). У ще одному варіанті реалізації система з контрольованим вивільненням може бути розміщена в безпосередній близькості до мішені сполуки і/або композиції згідно з даним винаходом, таким чином, потрібна тільки частина системної дози (див., наприклад, Goodson // Medical Applications of Controlled Release, вище, vol. 2, pp. 115-138 (1984)). Також можна застосовувати інші системи з контрольованим вивільненням, описані в джерелі Langer, 1990, Science 249:1527-1533. Сполуки і/або композиції, що містять сполуку(и) формули (I) згідно з даним винаходом можуть бути піддані хімічному і/або ферментативному розщепленню. Один або більше ферментів, які присутні у шлунку, просвіті кишечнику, кишкової тканини, крові, печінки, мозку або будь-якій іншій підходящій тканині ссавця, можуть ферментативно розщеплювати сполуки і/або композиції згідно з даним винаходом. Композиції згідно з даним винаходом У різних аспектах даного винаходу запропоновані фармацевтичні композиції, що містять будь-яку зі сполук структурної формули (I) і фармацевтично прийнятний формотворний компонент. Для введення пацієнту сполуки згідно з даним винаходом і фармацевтично прийнятні формотворні компоненти переважно є стерильними. Вода є переважним формотворним компонентом, якщо сполуку згідно з даним винаходом вводять внутрішньовенно. Сольові розчини і водні розчини декстрози і гліцерину також можуть бути використані в якості рідких формотворних компонентів, зокрема для ін'єкційних розчинів. Придатні фармацевтичні формотворні компоненти також включають допоміжні речовини, такі як крохмаль, глюкоза, лактоза, сахароза, желатин, солод, рис, борошно, крейда, силікагель, стеарат натрію, моностеарат гліцерину, тальк, хлорид натрію, сухе знежирене молоко, гліцерин, пропіленгліколь, воду, етанол або буферні агенти для забезпечення необхідного pН. Крім того, можуть бути використані допоміжні, стабілізуючі, загущуючі, змазуючі і забарвлювальні агенти. Фармацевтичні композиції можуть бути приготовлені за допомогою звичайного процесу змішування, розчинення, гранулювання, а також емульгування, інкапсулювання, захоплювання або ліофілізації. Фармацевтичні композиції можуть бути приготовлені звичайним способом із використанням одного або більше фізіологічно прийнятних носіїв, розріджувачів, наповнювачів або допоміжних речовин, які полегшують готування зі сполук згідно з даним винаходом препаратів, які можуть мати фармацевтичне застосування. Точний склад залежить від обраного шляху введення. Композиції згідно з даним винаходом можуть мати форму розчинів, суспензій, емульсій, таблеток, пігулок, пелет і капсул, капсул, що містять рідини, порошків, сполук із уповільненим вивільненням, супозиторіїв, емульсій, аерозолів, спреїв, суспензій або будь-яку іншу форму, що підходить для застосування. В одному з варіантів реалізації даного винаходу фармацевтично прийнятний формотворний компонент дозволяє одержати капсулу (див., наприклад, патент США № 5698155). Інші приклади придатних фармацевтичних формотворних компонентів були описані в рівні техніки (див. Remington's Pharmaceutical Sciences, Philadelphia College of th Pharmacy and Science, 17 Edition, 1985). Переважні композиції згідно з даним винаходом готовлять для пероральної доставки, зокрема для перорального застосування з уповільненим вивільненням. Композиції для пероральної доставки можуть бути представлені, наприклад, у формі таблеток, пастилок, водних або масляних суспензій, гранул, порошків, емульсій, капсул, сиропів або еліксирів. Композиції, що вводяться перорально, можуть містити один або більше необов'язкових агентів, наприклад, підсолоджувачів, таких як фруктоза, аспартам або сахарин; ароматизаторів, таких як перцева м'ята, масло грушанки, або барвників кольору вишні й консервантів для забезпечення препарату з фармацевтично приємним смаком. У випадку таблетованої форми або форми пігулок композиції можуть мати покриття для того, щоб відстрочити розкладання й усмоктування в шлунково-кишковому тракті, забезпечуючи тим 15 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 самим уповільнену дію протягом тривалого періоду часу. Селективно проникні мембрани, що оточують осмотично активну рушійну сполуку, також підходять для сполук, що вводяться перорально, згідно з даним винаходом. Для цих останніх платформ, рідина з середовища, що оточує капсулу, усмоктується рушійною сполукою, яка набухає, витісняючи агент або композицію агента через отвір. Такі платформи доставки можуть забезпечувати профіль доставки по суті нульового порядку, на відміну від профілів із негайним вивільненням, що містять піки. Також може бути використана речовина, що забезпечує відстрочку за часом, така як моностеарат гліцерину або стеарат гліцерину. Композиції для перорального введення можуть містити стандартні формотворні компоненти, такі як маніт, лактоза, крохмаль, стеарат магнію, сахарин натрію, целюлозу, карбонат магнію та т.п. Такі формотворні компоненти переважно мають фармацевтичну якість. Для перорально рідких препаратів, таких як суспензії, еліксири і розчини, придатні носії, наповнювачі або розріджувачі включають воду, сольовий розчин, алкіленгліколі (наприклад, пропіленгліколь), поліалкіленгліколі (наприклад, поліетиленгліколь), масла, спирти, слабокислі буфери з pН від 4 до 6 (наприклад, ацетатний, цитратний, аскорбатний з концентрацією від приблизно 1 мМ до приблизно 50 мМ) і т.п. Крім того, можуть бути додані ароматизатори, консерванти, барвники, і солі жовчних кислот. Також передбачаються композиції для введення за допомогою інших шляхів. Для трансбуккального введення композиції можуть мати форму таблеток, пастилок тощо, приготовлених звичайним способом. Рідкі склади лікарських засобів для застосування з розпилювачами і пристроями для розпилення рідин й еластичними гідродинамічними (ЕГД) аерозольними пристроями, як правило, містять сполуку згідно з даним винаходом із фармацевтично прийнятним формотворним компонентом. Переважно фармацевтично прийнятний формотворний компонент являє собою рідину, таку як спирт, воду, поліетиленгліколь або перфторвуглець. Необов'язково може бути додана інша речовина для зміни аерозольних властивості розчину або суспензії сполук згідно з даним винаходом. Переважно, дана речовина являє собою рідину, таку як спирт, гліколь, полігліколь або жирна кислота. Інші способи приготування рідких розчинів або суспензій лікарських засобів, що підходять для застосування в аерозольних пристроях, відомі фахівцям у даній області (див., наприклад, патенти США №№. 5112598 і 5556611). Сполуки згідно з даним винаходом можуть бути також приготовлені у вигляді ректальних або вагінальних композицій, таких як супозиторії або утримуючі клізми, наприклад, що містять звичайні основи для супозиторіїв, такі як масло какао або інші гліцериди. Крім описаних вище складів сполуки згідно з даним винаходом можуть бути також приготовлені у вигляді депо-препарату. Такі склади тривалої дії можуть бути введені шляхом імплантації (наприклад, підшкірно або внутрішньом'язово) або шляхом внутрішньом'язової ін'єкції. Так, наприклад, сполуки згідно з даним винаходом можуть бути приготовлені з прийнятними полімерними або гідрофобними речовинами (наприклад, у вигляді емульсії у прийнятному маслі) або іонообмінними смолами або у вигляді помірно розчинних похідних, наприклад у вигляді помірно розчинної солі. Якщо сполука згідно з даним винаходом є кислотною, вона може бути включена в будь-який з вищеописаних складів у вигляді вільної кислоти, фармацевтично прийнятної солі, сольвату або гідрату. Фармацевтично прийнятні солі, які по суті зберігають активність вільної кислоти, можуть бути отримані шляхом реакції з основами і, як правило, більш розчинні у водних й інших протонних розчинниках, ніж відповідна форма вільної кислоти. Способи застосування та дози У даному винаході запропоновані способи лікування або запобігання ожиріння у пацієнта, які включають введення пацієнту, що потребує такого лікування, ефективної кількості будь-якої зі сполук структурної формули (I). Кількість сполуки згідно з даним винаходом, ефективна для лікування конкретного розладу або стану, описаного в даному документі, буде залежати від природи стану або розладу, і може бути визначена стандартними клінічними методами, відомими в даній області, як описано раніше. Крім того, для визначення оптимальних діапазонів доз необов'язково можуть бути використані дослідження in vitro або in vivo. Кількість сполуки, що вводиться, згідно з даним винаходом залежить, серед інших факторів, від суб'єкта, що зазнає лікування, а також ваги суб'єкта, тяжкості захворювання, способу введення та рішення лікаря. Наприклад, доза може бути доставлена у фармацевтичній композиції шляхом однократного введення за допомогою декількох уведень або з контрольованим вивільненням. У переважному варіанті реалізації даного винаходу сполуки згідно з даним винаходом доставляють за допомогою перорального 16 UA 114807 C2 5 10 15 20 25 введення з уповільненим вивільненням. Переважно, у цьому варіанті, сполуки згідно з даним винаходом вводять двічі на добу (або переважно один раз на добу). Дозування може повторюватися з перервами, введення може бути зроблене окремо або в комбінації з іншими лікарськими засобами і може тривати доти, поки потрібне ефективне лікування хворобливого стану або розладу. Сполуки структурної формули (I) можуть бути введені в діапазоні доз 0,1-500 мг, переважно 1-100 мг на добу, у вигляді однієї або більше доз, і більш переважно 5 мг, 10 мг, 15 мг, 20 мг, 25 мг, 35 мг або 50 мг на добу, і найбільше переважно 25 мг. Сполуки згідно з даним винаходом перед застосуванням для людей переважно досліджують in vitro й in vivo на необхідну терапевтичну або профілактичну активність. Також ефективність та безпека сполук згідно з даним винаходом може бути продемонстрована із застосуванням тваринних модельних систем. Терапевтично ефективна доза сполук згідно з даним винаходом, описаних у даному документі, буде забезпечувати терапевтичний кращий ефект, не викликаючи істотної токсичності. Токсичність сполук згідно з даним винаходом може бути визначена із застосуванням стандартних фармацевтичних методик і може бути легко встановлена фахівцем у даній області. Співвідношення доз, що забезпечують токсичний та терапевтичний ефекти, являє собою терапевтичний індекс. Дозування сполуки згідно з винаходами, описаними у даному документі, перебуває в межах діапазону циркулюючих концентрацій, які включають ефективну дозу з невеликою токсичністю або з відсутністю токсичності. Далі даний винахід описаний з посиланням на наступні приклади, в яких докладно описані сполуки і композиції згідно з даним винаходом, а також дослідження для застосування сполук і композицій згідно з даним винаходом. Фахівцям у даній області очевидно, що не виходячи за рамки обсягу даного винаходу можуть бути здійснені численні модифікації як матеріалів, так і способів. ПРИКЛАДИ У наведених нижче прикладах наступні абревіатури мають наступні значення. Якщо абревіатура не розшифрована, вона має загальноприйняте значення. CDI = ДХМ = DMAP = ДМФА = год. = HATU = РХ/МС = M= МТБЕ = к. т. = ТЕА = ТГФ = ТФО = 1,1’-Карбонілдіімідазол дихлорметан 4-N, N-Диметиламінопіридин N, N-Диметилформамід години O-(7-азабензотриазол-1-іл)-N, N,N",N’-тетраметилуронію гексафторфосфат рідинна хроматографія/мас-спектроскопія молярний метил-трет-бутиловий ефір кімнатна температура триетиламін тетрагідрофуран трифтороцтова кислота 30 35 40 45 Загальна методика синтезу фенілциклоалкілметиламіну 6 (Схема 1) До перемішуваного розчину реактиву Гріньяра (2 M розчин в ефірі, 0,065 моль) в атмосфері азоту по краплях додавали фенілциклоалкілкарбонітрил (3) (0,026 моль) в 50 мл толуолу при 0 °C. Далі реакційну суміш повільно нагрівали при 92 °C протягом 18 год. Хід реакції контролювали за допомогою тонкошарової хроматографії (ТШХ). Реакційну суміш охолоджували до кімнатної температури і концентрували при зниженому тиску. Залишок розбавляли 30 мл безводного метанолу, охолоджували при 0 °C і повільно частинами додавали NaBH4 (2,5 г). Отриману суміш перемішували до повного перетворення імінової проміжної сполуки у відповідний амін. Після завершення реакції, видаляли метанол за допомогою випарювання. Залишок розбавляли етилацетатом, промивали насиченим розчином бікарбонату натрію, сушили над MgSO4 і випарювали при зниженому тиску з одержанням відповідного фенілциклобутилметиламіну (6), який очищали за допомогою колоночної хроматографії на силікагелі з використанням градієнта гексану й етилацетату. Чисті продукти 6a-m демонстрували задовільні результати 1H ЯМР і/або мас-спектрометричного аналізу. Приклад 1 1 3-Метил-1-(1-(n-толіл)циклопропіл)бутан-1-амін (6a). Безбарвне масло (1,66 г, 61 %). H ЯМР (400 МГц, CDCl3): δ 0,65-0,70 (m, 3H); 0,77-0,80 (m, 1H); 0,85 (d, J=6,8 Гц, 6H); 0,98-1,11 (m, 2H); 17 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 1,22-1,30 (m, 2H); 1,70-1,77 (m, 1H); 2,10-1,13 (m, 1H); 2,28 (s, 3H); 7,09 (d, J=8,0 Гц, 2H); 7,20 (d, + J=8,0 Гц, 2H). МС (ІЕР): m/z=218,20 (M+H ). Приклад 2 1-(1-(4-Хлорфеніл)циклопропіл)-3-метилбутан-1-амін (6b). Безбарвне масло (1,60 г, 60 %). 1 H ЯМР (400 МГц, CDCl3): δ 0,65-0,70 (m, 3H); 0,77-0,80 (m, 1H); 0,85 (d, J=6,8 Гц, 6H); 0,87-1,01 (m, 1H); 1,18-1,27 (m, 3H); 1,69-1,73 (m, 1H);2,16 (d, J=10,4 Гц, 1H); 7,23- 7,24 (m, 4H). МС (ІЕР): + m/z=238,20 (M+H ). Приклад 3 1 1-(1-(4-Фторфеніл)циклобутил)-3-метилбутан-1-амін (6c). Безбарвне масло (2,2 г, 70 %). H ЯМР (400 МГц, CDCl3): δ 0,58-0,65 (m, 1H); 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,15-1,21 (m, 1H); 1,67-1,70 (m, 1H); 1,80-1,86 (m, 1H); 1,93-1,98 (m, 1H); 2,12-2,18 (m, 1H); 2,28-2,37 (m, 3H); 2,97 (dd, J=2,0 Гц; 10,8 Гц, 1H); 6,93-7,08 (m, 3H); 7,12-7,16 (m, 1H). Приклад 4 1 1-(1-(4-Хлорфеніл)циклобутил)-3-метилбутан-1-амін (6d). Безбарвне масло (4,7 г, 72 %). H ЯМР (400 МГц, CDCl3): δ 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,13-1,23 (m, 2H); 1,66-1,68 (m, 1H); 1,79-1,84 (m, 1H); 1,90-1,96 (m, 1H); 2,15-2,16 (m, 1H); 2,25-2,33 (m, 3H); 2,98 (d, J=10,8 Гц, 1H); 7,06 (dd, J=1,6; 8,4 Гц, 2H); 7,24 (dd, J=1,6; 8,4 Гц, 2H). Приклад 5 1-(1-(3,4-Дихлорфеніл)циклобутил)-3-метилбутан-1-амін (6e). Безбарвне масло (3,6 г, 70 %). 1 H ЯМР (400 МГц, CDCl3): δ 0,53-0,60 (m, 1H); 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,101,13 (m, 1H); 1,63-1,67 (m, 1H); 1,77-1,83 (m, 1H); 1,91-1,97 (m, 1H); 2,12-2,16 (m, 1H); 2,21-2,33 (m, 3H); 2,97 (d, J=10,8 Гц, 1H); 6,96 (dd, J=2,0 Гц; 8,4 Гц, 1H); 7,19 (d, J=2 Гц; 1H); 7.32 (d, J=8,4 Гц, 1H). Приклад 6 1-(1-(2,4-Дихлорфеніл)циклобутил)-3-метилбутан-1-амін (6f). Безбарвне масло (1,5 г, 72 %). 1 H ЯМР (400 МГц, CDCl3): δ 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,13-1,15 (m, 1H); 1,231,26 (m, 1H) 1,71-1,81 (m, 2H); 1,92-2,03 (m, 1H); 2,35-2,43 (m, 4H); 3,24 (dd, J=2,0 Гц; 10,8 Гц, 1H); 7,02 (d, J=8,4 Гц, 1H); 7,16 (dd, J=2 Гц; 8,4 Гц, 1H); 7,29 (d, J=2,4 Гц, 1H). Приклад 7 1-(1-(3,4-Диметоксифеніл)циклобутил)-3-метилбутан-1-амін (6g). Безбарвне масло (3,6 г, 1 70 %). H ЯМР (400 МГц, CDCl3): δ 0,53-0,60 (m, 1H); 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,10-1,13 (m, 1H); 1,63-1,67 (m, 1H); 1,77-1,83 (m, 1H); 1,91-1,97 (m, 1H); 2,12-2,16 (m, 1H); 2,212,33 (m, 3H); 2,97 (d, J=10,8 Гц, 1H); 3,87 (s, 6H); 6,77-6,82 (m, 3H). Приклад 8 1-(1-(4-Етоксифеніл)циклобутил)-3-метилбутан-1-амін (6h). Безбарвне масло (1,06 г, 72 %). 1 H ЯМР (400 МГц, CDCl3): δ 0,57-0,64 (m, 1H); 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,151,21 (m, 1H); 1,40 (t J=6,8 Гц, 3H); 1,67-1,69 (m, 1H); 1,79-1,84 (m, 1H); 1,90-1,96 (m, 1H); 2,142,16 (m, 1H); 2,27-2,36 (m, 3H); 2,98 (dd, J=2,0 Гц; 10,8 Гц, 1H); 4,02 (q, J=6,8 Гц, 2H); 6,83 (d, J=8,4 Гц, 2H); 7,05 (dd, J=8,4 Гц, 2H). Приклад 9 3-Метил-1-(1-(4-(метилтіо)феніл)циклобутил)бутан-1-амін (6i). Безбарвне масло (1,7 г, 34 %). 1 H ЯМР (400 МГц, CDCl3): δ 0,56-0,62 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,041,06 (s ушир., 2H); 1,13-1,20 (m, 1H); 1,64-1,68 (m, 1H); 1,79-1,83 (m, 1H); 1,90-1,95 (m, 1H); 2,112,17 (m, 1H); 2,26-2,37 (m, 3H); 2,46 (s, 3H); 2,96 (d, J=10,8 Гц, 1H); 7,05 (d, J=8,4 Гц, 2H); 7,19 (d, + J=8,4 Гц, 2H). МС (ІЕР): m/z=264,20 (M+H ). Приклад 10 1 3-Метил-1-(1-(n-толіл)циклопентил)бутан-1-амін (6j). Безбарвне масло (1,46 г, 60 %). H ЯМР (400 МГц, CDCl3): δ 0,68-0,78 (m, 1H); 0,83 (d, J=6,8 Гц, 6H); 0,99 (s ушир., 2H); 1,20-1,24 (m, 1H); 1,50-1,56 (m, 2H); 1,58-1,68 (m, 3H); 1,72-1,78 (m, 1H); 1,84-1,91 (m, 1H); 2,02-2,08 (m, 2H); 2,28 (s, 3H); 2,73 (d, J=10,8 Гц, 1H); 7,09 (d, J=8,0 Гц, 2H); 7,20 (d, J=8,0 Гц, 2H). МС (ІЕР): m/z=246,20 + (M+H ). Приклад 11 1-(1-(4-Метоксифеніл)циклопентил)-3-метилбутан-1-амін (6k). Безбарвне масло (1,43 г, 1 55 %). H ЯМР (400 МГц, CDCl3): δ 0,66-0,77 (m, 2H); 0,81 (d, J=6,8 Гц, 6H); 0,97- 1,02 (s ушир., 2H); 1,12-1,18 (m, 1H); 1,48-1,55 (m, 1H); 1,58-1,68 (m, 3H); 1,71-1,77 (m, 1H); 1,82-1,89 (m, 2H); 2,07-2,06 (m, 1H); 2,70 (d, J=10,8 Гц, 1H); 3,78 (s, 3H); 6,82 (d, J=8,8 Гц, 2H); 7,23 (d, J=8,8 Гц, + 2H). МС (ІЕР): m/z=262,20 (M+H ). Приклад 12 1 3-Метил-1-(1-(n-толіл)циклогексил)бутан-1-амін (6l). Безбарвне масло (1,46 г, 60 %). H ЯМР (400 МГц, CDCl3): δ 0,63-0,76 (m, 1H); 0,77 (d, J=6,8 Гц, 3H); 0,83 (d, J=6,8 Гц, 3H); 1,17-1,32 (m, 18 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 5H); 1,37-1,66 (m, 6H); 2,24-2,36 (m, 4H); 2,52 (d, J=10,4 Гц, 1H); 7,09 (d, J=8,0 Гц, 2H); 7,20 (d, + J=8,0 Гц, 2H). МС (ІЕР): m/z=260,20 (M+H ). Приклад 13 1 1-(1-(4-Хлорфеніл)циклогексил)-3-метилбутан-1-амін (6m). Безбарвне масло (0,8 г, 32 %). H ЯМР (400 МГц, CDCl3): δ 0,60-0,66 (m, 1H); 0,75 (d, J=6,8 Гц, 3H); 0,81 (d, J=6,8 Гц, 3H); 0,95-1,00 (s ушир., 2H); 1,11-2,25 (m, 5H); 1,41-1,62 (m, 5H); 2,20-2,30 (m, 2H); 2,53 (d, J=10,8 Гц, 1H); 7,22 + (d, J=8,8 Гц, 2H); 7,27 (d, J=8,8 Гц, 2H). МС (ІЕР): m/z=280,20 (M+H ). Загальна методика синтезу простих ефірних похідних фенілциклобутилметиламіну 7 і 8 (Схема 2) До перемішуваного розчину карбонату цезію (1,4 г, 5,0 екв.) в 10 мл ДМФ додавали відповідний фенілциклобутилметиламін (6) (0,0009 моль) і отриману суміш перемішували при кімнатній температурі протягом 4 год. Далі додавали розчин придатного 4нітробензолсульфонату (0,0045 моль, 5 екв.) в 5 мл ДМФА протягом періоду, що становить 5 хвилин. Отриману суміш перемішували при кімнатній температурі протягом ночі. Хід реакції контролювали за допомогою тонкошарової хроматографії (ТШХ). Реакційну суміш фільтрували, розбавляли 10 мл етилацетату, промивали сольовим розчином і сушили над Na 2SO4, випарювали з одержанням відповідних простих ефірних похідних фенілциклобутилметиламіну (7, 8), які очищали за допомогою колоночної хроматографії на силікагелі із застосуванням градієнта гексану й етилацетату. Чисті продукти (7,8) демонстрували задовільні результати 1H ЯМР і/або мас-спектрометричного аналізу. Вибрані прості ефірні похідні (7, 8) піддавали хіральній ВЕРХ із одержанням оптично чистих (R)- і (S)-ізомерів. Умови хіральної ВЕРХ: колонка - CHIRAL PAKIA 4,6 × 250 мм, 5 мкМ; рухома фаза - 0,1 % ДЕА в гексані й етанолі; ізократичний метод зі швидкістю потоку 0,8 мл на хвилину; об'єм проби 1,00 мкл; і час проведення аналізу 20 хв. Усі прості ефірні похідні (7, 8) перетворювали у відповідні HCl солі за допомогою їхньої обробки 1 н. HCl у діоксані/воді з наступною ліофілізацією. Гідрохлоридні солі простих ефірних похідних (7, 8) тестували на переносниках моноамінів (MATs) у фармакологічних дослідженнях in vitro. Приклад 14 1-(1-(4-Етоксифеніл)циклобутил)-N-(2-метоксіетил)-3-метилбутан-1-амін (7a). 1 Безбарвне масло (100 мг, вихід 28 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,08-1,12 (m, 1H); 1,41 (t, J=9,2 Гц, 3H); 1,59- 1,68 (m, 1H); 1,71-1,89 (m, 2H); 2,16-2,38 (m, 4H); 2,73 (d ушир., J=3,2 Гц, 1H); 2,88 (t, J=6,8 Гц, 2H); 3,32 (s, 3H); 3,45 (t, J=7,2 Гц, 2H); 4,03 (q, J=7,2 Гц, 2H); 6,83 (d, J=8,4 Гц, 2H); 7,16 (d, J=8,4 Гц, 2H). МС + (ІЕР): m/z=320,61 (M+H ). Приклад 15 N-(2-Етоксіетил)-1-(1-(4-етоксифеніл)циклобутил)-3-метилбутан-1-амін (7b). 1 Безбарвне масло (70 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,08-1,12 (m, 1H); 1,21 (t, J=9,6 Гц, 3H); 1,38- 1,44 (m, 4H); 1,59-1,66 (m, 1H); 1,75-1,86 (m, 2H); 2,15-2,18 (m, 1H); 2,28-2,37 (m, 3H); 2,73 (d ушир., J=11,6 Гц, 1H); 2,73-2,92 (m, 2H); 3,43-3,50 (m, 3H); 4,03 (q, J=7,2 Гц, 2H); 6,83 (d, J=8,4 Гц, 2H); 7,16 (d, + J=8,4 Гц, 2H). МС (ІЕР): m/z=334,72 (M+H ). Приклад 16 1-(1-(4-Етоксифеніл)циклобутил)-3-метил-N-(2-пропоксіетил)бутан-1-амін (7c). 1 Безбарвне масло (80 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 0,91-0,92 (m, 6H); 1,00-1,08 (m, 1H); 1,39-1,46 (m, 4H); 1,521,64 (m, 3H); 1,73-1,86 (m, 2H); 2,17-2,40 (m, 4H); 2,73 (s ушир., 1H); 2,88-2,94 (m, 2H); 3,36 (t, J=6,8 Гц, 2H); 3,48 (d, J=10,8 Гц, 2H); 4,03 (q, J=7,2 Гц, 2H); 6,83 (d, J=8,4 Гц, 7,16 (d, J=8,4 Гц, + 1H). МС (ІЕР): m/z=348,40 (M+H ). Приклад 17 N-(2-Бутоксіетил)-1-(1-(4-етоксифеніл)циклобутил)-3-метилбутан-1-амін (7d). 1 Безбарвне масло (100 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 0,92 (t, J=9,6 Гц, 3H); 1,08-1,12 (m, 1H); 1,32- 1,44 (m, 5H); 1,49-1,64 (m, 3H); 1,78-1,86 (m, 1H); 2,04-2,15 (m, 1H); 2,26-2,39 (m, 2H); 2,73 (d ушир., J=11,6 Гц, 1H); 2,86-2,91 (m, 2H); 3,38-3,48 (m, 4H); 3,64 (t, J=7,2 Гц, 1H); 4,03 (q, J=7,2 Гц, 2H); 4,277 (t, + J=6,8 Гц, 1H); 6,82 (d, J=8,4 Гц, 2H); 7,15 (d, J=8,4 Гц, 2H). МС (ІЕР): m/z=362,57 (M+H ). Приклад 18 1-(1-(4-Етоксифеніл)циклобутил)-N-(2-ізобутоксіетил)-3-метилбутан-1-амін (7e). 1 Безбарвне масло (90 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 0,90-1,04 (m, 6H); 1,08-1,12 (m, 1H); 1,38-1,44 (m, 4H); 1,601,68 (m, 1H); 1,70-1,91 (m, 3H); 2,13-2,20 (m, 1H); 2,27-2,42 (m, 3H); 2,71 (d, J=8,4 Гц, 1H); 2,85 19 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 2,92 (m, 2H); 3,17 (d, J=6,4 Гц, 2H); 3,58 (t, J=7,2 Гц, 1H); 4,03 (q, J=7,2 Гц, 2H); 6,82 (d, J=8,4 Гц, + 2H); 7,15 (d, J=8,4 Гц, 2H). МС (ІЕР): m/z=362,57 (M+H ). Приклад 19 N-(2-Етоксіетил)-3-метил-1-(1-(4-(метилтіо)феніл)циклобутил)бутан-1-амін (7f). 1 Безбарвне масло (0,20 г, 20 %). H ЯМР (400 МГц, CDCl3): δ 0,60-0,66 (m, 1H); 0,82 (d, J = 6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 1,06-1,09 (m, 1H); 1,17 (t, J=7,2 Гц, 3H); 1,61-1,60 (m, 1H); 1,70-1,77 (m, 1H); 1,82-1,88 (1H); 2,14-2,19 (m, 3H); 2,23-2,29 (m, 2H); 2,35-2,41 (m, 1H); 2,46 (s, 3H); 2,72 (d, J=10 Гц, 1H); 2,88 (t, J=7,2 Гц, 2H); 3,42-3,48 (m, 3H); 7,02 (d, J=8,8 + Гц, 2H); 7,20 (d, J=8,8 Гц, 2H). МС (ІЕР): m/z=336,20 (M+H ). Приклад 20 N-(4-Етоксибутил)-3-метил-1-(1-(4-(метилтіо)феніл)циклобутил)бутан-1-амін (7g). 1 Безбарвне масло (0,21 г, 20 %). H ЯМР (400 МГц, CDCl3): δ 0,60-0,66 (m, 1H); 0,82 (d, J = 6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 1,87 (t, J=7,2 Гц, 3H); 1,47-1,83 (m, 6H); 2,04-2,22 (m, 3H); 2,27-2,32 (m, 2H); 2,46 (s, 3H); 3,40-3,49 (m, 5H); 4,10-4,15 (m, 4H); 7,02 (d, J=8,8 Гц, + 2H); 7,20 (d, J=8,8 Гц, 2H). МС (ІЕР): m/z=364,20 (M+H ). Приклад 21 1-(1-(4-Хлорфеніл)циклобутил)-N-(2-етоксіетил)-3-метилбутан-1-амін (7h). 1 H ЯМР (400 МГц, CDCl3): δ 0,63-0,71 (m, 1H); 0,81 (d, J=6,8 Гц, 3H); 0,86 (d, J=6,8 Гц, 3H); 1,01-1,07 (m, 1H); 1,17 (t, J=7,2 Гц, 3H); 1,59-1,66 (m, 1H); 1,70-1,77 (m, 1H); 1,83- 1,90 (m, 1H); 2,12-2,17 (m, 1H); 2,22-2,29 (m, 2H); 2,36-2,43 (m, 1H); 2,73 (dd, J=2,4 Гц; 10,0 Гц, 1H); 2,88 (t, J=5,6 Гц, 2H); 3,43-3,48 (m, 4H); 7,16 (d J=8,4 Гц, 2H); 7,23 (d, J=8,4 Гц, 2H). МС (ІЕР): m/z=325,10 + (M+H ). Приклад 22 N-(2-Етоксіетил)-1-(1-(4-фторфеніл)циклобутил)-3-метилбутан-1-амін (7i). 1 H ЯМР (400 МГц, CDCl3): δ 0,64-0,71 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,86 (d, J=6,8 Гц, 3H); 1,02-1,08 (m, 1H); 1,17 (t, J=7,2 Гц, 3H); 1,59-1,66 (m, 1H); 1,70-1,78 (m, 1H); 1,83- 1,92 (m, 1H); 2,12-2,17 (m, 2H); 2,21-2,31 (m, 2H); 2,36-2,43 (m, 1H); 2,72 (dd, J=2,4 Гц; 10,0 Гц, 1H); 2,88 (t, J=5,6 Гц, 2H); 3,43-3,44 (m, 4H); 6,95 (t, J=8,8 Гц, 2H); 7,18 (dd, J=5,2 Гц; 8,8 Гц, 2H). МС (ІЕР): + m/z=308,67 (M+H ). Приклад 23 N-(2-Етоксіетил)-3-метил-1-(1-(n-толіл)циклопропіл)бутан-1-амін (7j). 1 Безбарвне масло (0,24 г, 22 %). H ЯМР (400 МГц, CDCl3): δ 0,46-0,50 (m, 1H); 0,67-0,72 (m, 1H); 0,75-0,79 (m, 1H); 0,80 (d, J=6,8 Гц, 3H); 0,83 (d, J=6,8 Гц, 3H); 1,04-1,13 (m, 1H); 1,16-1,20 (m, 4H); 1,23-1,31 (m, 1H); 1,70-1,76 (m, 1H); 1,94-1,98 (m, 1H); 2,30 (s, 3H); 2,75- 2,80 (m, 1H); 3,21-3,27 (m, 1H); 3,45-3,54 (m, 4H); 7,06 (d, J=7,2 Гц, 2H); 7,20 (d, J=7,2 Гц, 2H). МС (ІЕР): + m/z=290,20 (M+H ). Приклад 24 1-(1-(4-Хлорфеніл)циклопропіл)-N-(2-етоксіетил)-3-метилбутан-1-амін (7k). 1 Безбарвне масло (0,22 г, 24 %). H ЯМР (400 МГц, CDCl3): δ 0,47-0,52 (m, 1H); 0,65-0,71 (m, 1H); 0,75-0,89 (m, 7H); 1,02-1,09 (m, 1H); 1,18 (t, J=7,2 Гц, 3H); 1,19-1,27 (m, 1H); 1,44 (s ушир., 2H); 1,68-1,73 (m, 1H); 1,95-1,98 (m, 1H); 2,73-2,79 (m, 1H); 3,17-3,23 (m, 1H); 3,47-3,53 (m, 2H); + 7,06 (d, J=7,2 Гц, 2H); 7,17 (d, J=7,2 Гц, 2H). МС (ІЕР): m/z=310,20 (M+H ). Приклад 25 N-(2-Етоксіетил)-3-метил-1-(1-(n-толіл)циклопентил)бутан-1-амін (7l). 1 Безбарвне масло (0,27 г, 22 %). H ЯМР (400 МГц, CDCl3): δ 0,60-0,75 (m, 1H); 0,75 (d, J=6,8 Гц, 3H); 0,78 (d, J=6,8 Гц, 3H); 1,06-1,21 (m, 1H); 1,18 (t, J=7,2 Гц, 3H); 1,26-1,47 (m, 3H); 1,57-1,65 (m, 3H); 1,72-1,80 (m, 1H); 1,84-2,00 (m, 3H); 2,34 (s, 3H); 2,54 (d, J=8,4 Гц, 1H); 2,78-2,85 (m, 1H); 2,86-2,90 (m, 1H); 3,15-3,49 (m, 4H); 6,81 (d, J=8,8 Гц, 2H); 7,26 (d, J=8,8 Гц, 2H). МС (ІЕР): + m/z=317,20 (M+H ). Приклад 26 N-(2-Етоксіетил)-1-(1-(4-метоксифеніл)циклопентил)-3-метилбутан-1-амін (7m). 1 Безбарвне масло (0,27 г, 22 %). H ЯМР (400 МГц, CDCl3): δ 0,60-0,75 (m, 1H); 0,75 (d, J=6,8 Гц, 3H); 0,78 (d, J=6,8 Гц, 3H); 1,06-1,21 (m, 1H); 1,18 (t, J=7,2 Гц, 3H); 1,26-1,47 (m, 3H); 1,57-1,65 (m, 3H); 1,72-1,80 (m, 1H); 1,84-2,00 (m, 3H); 2,51 (d, J=8,4 Гц, 1H); 2,78- 2,85 (m, 1H); 2,86-2,90 (m, 1H); 3,15-3,45 (m, 4H); 3,77 (s, 3H); 6,81 (d, J=8,8 Гц, 2H); 7,26 (d, J=8,8 Гц, 2H). МС (ІЕР): + m/z=334,20 (M+H ). Приклад 27 N-(4-Етоксибутил)-3-метил-1-(1-(п-толіл)циклогексил)бутан-1-амін (7n). 1 Безбарвне масло (0,18 г, 20 %). H ЯМР (400 МГц, CDCl3): δ 0,67-0,72 (m, 1H); 0,75 (d, J=6,8 Гц, 3H); 0,78 (d, J=6,8 Гц, 3H); 1,13-1,26 (m, 8H); 1,36-1,44 (m, 3H); 1,49-1,59 (m, 7H); 2,16 (d, 20 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 J=12,8 Гц, 1H); 2,21-2,35 (m, 5H); 2,44-2,50 (m, 1H); 2,65-2,69 (m, 1H); 3,34-3,48 (m, 4H); 7,23 (d, + J=8,8 Гц, 2H); 7,28 (d, J=8,8 Гц, 2H). МС (ІЕР): m/z=360,20 (M+H ). Приклад 28 1-(1-(4-Хлорфеніл)циклогексил)-N-(4-етоксибутил)-3-метилбутан-1-амін (7o). 1 Безбарвне масло (0,18 г, 20 %). H ЯМР (400 МГц, CDCl3): δ 0,58-0,65 (m, 1H); 0,75 (d, J=6,8 Гц, 3H); 0,78 (d, J=6,8 Гц, 3H); 1,07-1,13 (m, 1H); 1,56-1,26 (m, 6H); 1,38-1,63 (m, 10H); 2,13 (d, J=14,0 Гц, 1H); 2,21 (d, J=10 Гц, 1H); 2,28 (d, J=13,6 Гц, 1H); 2,45-2,51 (m, 1H); 2,68-2,74 (m, 1H); + 3,36-3,48 (m, 4H); 7,23 (d, J=8,8 Гц, 2H); 7,28 (d, J=8,8 Гц, 2H). МС (ІЕР): m/z=381,20 (M+H ). Приклад 29 1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(2-етоксіетил)-3-метилбутан-1-амін (8a). 1 Безбарвне масло (87 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,61-0,68 (m, 1H); 0,84 (d, J=6,8 Гц, 3H); 0,89 (d, J=6,8 Гц, 3H); 1,03-1,04 (m, 1H); 1,08 (t, J=7,2 Гц, 3H); 1,62- 1,63 (m, 1H); 1,75-1,78 (m, 1H); 1,88-1,91 (m, 1H); 2,21-2,38 (m, 4H); 2,75 (dd, J=2,4 Гц; 10,0 Гц, 1H); 2,96-3,02 (m, 2H); 3,41 (q, J=7,2 Гц, 2H); 3,44 (t, J=4,4 Гц, 2H); 7,06 (dd, J=2,4 Гц; 8,4 Гц, 1H); 7,31 (d, J=2,0 + Гц, 1H); 7,34 (d, J=8,4 Гц, 1H). МС (ІЕР): m/z=360,10 (M+H ). Приклад 30 (R)-1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(2-метоксіетил)-3-метилбутан-1-амін (8b). 1 Безбарвне масло (60 мг, вихід 28 %). H ЯМР (400 МГц, CDCl3): δ 0,64-0,71 (m, 1H); 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,04 (t, J=12 Гц, 1H); 1,53 (s ушир., 1H); 1,62- 1,65 (m, 1H); 1,73-1,81 (m, 1H); 1,88-1,91 (m, 1H); 2,15-2,25 (m, 3H); 2,37-2,44 (m, 1H); 2,74 (d, J=8,4 Гц, 1H); 2,75-2,94 (m, 2H); 2,96 (s, 3H); 3,44 (t, J=10,8 Гц, 2H); 7,06 (d, J=8,0 Гц, 1H); 7,33 (s, 1H); 7,34 (d, + J=8,0 Гц, 1H). МС (ІЕР): m/z=346,03 (M+H ). Приклад 31 (S)-1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(2-метоксіетил)-3-метилбутан-1-амін (8c). 1 Безбарвне масло (100 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,64-0,71 (m, 1H); 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,04 (t, J=12 Гц, 1H); 1,53 (s ушир., 1H); 1,62- 1,65 (m, 1H); 1,73-1,81 (m, 1H); 1,88-1,91 (m, 1H); 2,15-2,25 (m, 3H); 2,37-2,44 (m, 1H); 2,74 (d, J=8,4 Гц, 1H); 2,75-2,94 (m, 2H); 2,96 (s, 3H); 3,44 (t, J=10,8 Гц, 2H); 7,06 (d, J=8,0 Гц, 1H); 7,33 (s, 1H); 7,34 (d, + J=8,0 Гц, 1H). МС (ІЕР): m/z=346,03 (M+H ). Приклад 32 (R)-1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(3-пропоксипропіл)-3-метилбутан-1-амін (8d). 1 Безбарвне масло (87 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 0,91 (t, J=9,6 Гц, 3H); 1,00-1,08 (m, 1H); 1,56- 1,64 (m, 5H); 1,66-1,80 (m, 2H); 1,83-1,96 (m, 1H); 2,09-2,30 (m, 3H); 2,37-2,46 (m, 1H); 2,72-2,94 (m, 3H); 3,37 (t, J=10,8 Гц, 2H); 3,49 (t, J=10,8 Гц, 2H); 7,07 (dd, J=3,2 Гц, 11,2 Гц, 1H); 7,32 (s, 1H); 7,33 (d, J=8,4 + Гц, 1H). МС (ІЕР): m/z=388,30 (M+H ). Приклад 33 (S)-1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(3-пропоксипропіл)-3-метилбутан-1-амін (8e). 1 Безбарвне масло (60 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 0,91 (t, J=9,6 Гц, 3H); 1,00-1,08 (m, 1H); 1,56- 1,64 (m, 5H); 1,66-1,80 (m, 2H); 1,83-1,96 (m, 1H); 2,09-2,30 (m, 3H); 2,37-2,46 (m, 1H); 2,72-2,94 (m, 3H); 3,37 (t, J=10,8 Гц, 2H); 3,49 (t, J=10,8 Гц, 2H); 7,07 (dd, J=3,2 Гц, 11,2 Гц, 1H); 7,32 (s, 1H); 7,33 (d, J=8,4 + Гц, 1H). МС (ІЕР): m/z=388,30 (M+H ). Приклад 34 (R)-N-(3-Бутоксипропіл)-1-(1-(3,4-дихлорфеніл)циклобутил)-3-метилбутан-1-амін (8f). 1 Безбарвне масло (130 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,59-0,64 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 0,91 (t, J=9,6 Гц, 3H); 1,04-1,07 (m, 1H); 1,32- 1,40 (m, 2H); 1,50-1,56 (m, 3H); 1,57-1,79 (m, 4H); 1,87-1,92 (m, 1H); 2,10-2,27 (m, 3H); 2,38-2,42 (m, 1H); 2,722,94 (m, 3H); 3,37 (t, J=10,8 Гц, 2H); 3,49 (t, J=10,8 Гц, 2H); 7,07 (dd, J=2,0 Гц, 8,0 Гц, 1H); 7,32 (s, + 1H); 7,33 (d, J=8,0 Гц, 1H). МС (ІЕР): m/z=402,03 (M+H ). Приклад 35 (S)-N-(3-Бутоксипропіл)-1-(1-(3,4-дихлорфеніл)циклобутил)-3-метилбутан-1-амін (8g). 1 Безбарвне масло (130 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,59-0,64 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 0,91 (t, J=9,6 Гц, 3H); 1,04-1,07 (m, 1H); 1,32- 1,40 (m, 2H); 1,50-1,56 (m, 3H); 1,57-1,79 (m, 4H); 1,87-1,92 (m, 1H); 2,10-2,27 (m, 3H); 2,38-2,42 (m, 1H); 2,722,94 (m, 3H); 3,37 (t, J=10,8 Гц, 2H); 3,49 (t, J=10,8 Гц, 2H); 7,07 (dd, J=2,0 Гц, 8,0 Гц, 1H); 7,32 (s, + 1H); 7,33 (d, J=8,0 Гц, 1H). МС (ІЕР): m/z=402,03 (M+H ). Приклад 36 (R)-1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(4-метоксибутил)-3-метилбутан-1-амін (8h). 1 Безбарвне масло (60 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,84 (d, 21 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 J=8,8 Гц, 3H); 0,89 (d, J=8,8 Гц, 3H); 1,00-1,08 (m, 1H); 1,43-1,68 (m, 6H); 1,71-1,94 (m, 2H); 2,102,45 (m, 4H); 2,66-2,84 (m, 3H); 3,31 (s, 3H); 3,37 (t, J=10,8 Гц, 2H); 7,07 (dd, J=3,2 Гц, 11,6 Гц, + 1H); 7,32 (s, 1H); 7,34 (d, J=11,6 Гц, 1H). МС (ІЕР): m/z=374,26 (M+H ). Приклад 37 (S)-1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(4-метоксибутил)-3-метилбутан-1-амін (8i). 1 Безбарвне масло (60 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,84 (d, J=8,8 Гц, 3H); 0,89 (d, J=8,8 Гц, 3H); 1,00-1,08 (m, 1H); 1,43-1,68 (m, 6H); 1,71-1,94 (m, 2H); 2,102,45 (m, 4H); 2,66-2,84 (m, 3H); 3,31 (s, 3H); 3,37 (t, J=10,8 Гц, 2H); 7,07 (dd, J=3,2 Гц, 11,6 Гц, + 1H); 7,32 (s, 1H); 7,34 (d, J=11,6 Гц, 1H). МС (ІЕР): m/z=374,26 (M+H ). Приклад 38 (R)-1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(4-етоксибутил)-3-метилбутан-1-амін (8j). 1 Безбарвне масло (100 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,84 (d, J=9,2 Гц, 3H); 0,89 (d, J=9,2 Гц, 3H); 1,01-1,08 (m, 1H); 1,20 (t, J=9,2 Гц, 3H); 1,43- 1,64 (m, 6H); 1,71-1,94 (m, 2H); 2,09-2,41 (m, 4H); 2,66-2,84 (m, 3H); 3,40-3,51 (m, 4H); 7,08 (dd, J=2,8 Гц, 10,8 + Гц, 1H); 7,32 (s, 1H); 7,34 (d, J=10,8 Гц, 1H). МС (ІЕР): m/z=388,26 (M+H ). Приклад 39 (S)-1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(4-етоксибутил)-3-метилбутан-1-амін (8k). 1 Безбарвне масло (100 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,66 (m, 1H); 0,84 (d, J=9,2 Гц, 3H); 0,89 (d, J=9,2 Гц, 3H); 1,01-1,08 (m, 1H); 1,20 (t, J=9,2 Гц, 3H); 1,43- 1,64 (m, 6H); 1,71-1,94 (m, 2H); 2,09-2,41 (m, 4H); 2,66-2,84 (m, 3H); 3,40-3,51 (m, 4H); 7,08 (dd, J=2,8 Гц, 10,8 + Гц, 1H); 7,32 (s, 1H); 7,34 (d, J=10,8 Гц, 1H). МС (ІЕР): m/z=388,26 (M+H ). Приклад 40 1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(4-ізобутоксибутил)-3-метилбутан-1-амін (8l). 1 Безбарвне масло (87 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,59-0,64 (m, 1H); 0,84 (d, J=9,2 Гц, 3H); 0,89 (d, J=9,2 Гц, 3H); 0,91 (s ушир., 6H); 1,01-1,07 (m, 1H); 1,45-1,63 (m, 6H); 1,661,92 (m, 3H); 2,10-2,31 (m, 2H); 2,37-2,49 (m, 2H); 2,68-2,82 (m, 3H); 3,16 (d, J=6,4 Гц, 2H); 3,40 (t, J=6,4H, 2H); 7,08 (dd, J=2,8 Гц, 10,8 Гц, 1H); 7,32 (s, 1H); 7,33 (d, J=10,8 Гц, 1H). МС (ІЕР): + m/z=416,26 (M+H ). Приклад 41 1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(2-етоксіетил)пропан-1-амін (8n). 1 H ЯМР (400 МГц, CDCl3): δ 0,69-0,74 (m, 1H); 0,89 (d, J=6,8 Гц, 3H); 1,19 (t, J=6,8 Гц, 3H); 1,39-1,47 (m, 1H); 1,71-1,78 (m, 1H); 1,86-1,96 (m, 1H); 2,17-2,27 (m, 3H); 2,36-2,43 (m, 1H); 2,54 (dd, J=2,4 Гц; 10,0 Гц, 1H); 2,79-2,85 (m, 1H); 2,88-2,94 (m, 1H); 3,43-3,49 (m, 4H); 7,06 (dd, J=2,4 + Гц; 8,4 Гц, 1H); 7,30 (s, 1H); 7,32 (d, J=8,4 Гц, 1H). МС (ІЕР): m/z=332,60 (M+H ). Приклад 42 1-(1-(3,4-Диметоксифеніл)циклобутил)-N-(2-метоксіетил)-3-метилбутан-1-амін (8o). 1 Безбарвне масло (100 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,72-0,78 (m, 1H); 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,06-1,12 (m, 1H); 1,60-1,68 (m, 1H); 1,77-1,91 (m, 2H); 2,132,20 (m, 1H); 2,28-2,40 (m, 3H); 2,72 (d ушир., J=9,2 Гц, 1H); 2,89 (t, J=5,6 Гц, 2H); 3,32 (s, 3H); + 3,45 (t, J=7,2 Гц, 2H); 3,87 (s, 6H); 6,77-6,82 (m, 3H). МС (ІЕР): m/z=336,70 (M+H ). Приклад 43 1-(1-(3,4-Диметоксифеніл)циклобутил)-N-(2-етоксіетил)-3-метилбутан-1-амін (8p). 1 Безбарвне масло (88 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,72-0,78 (m, 1H); 0,84 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,06-1,12 (m, 1H); 1,18 (t, J=6,8 Гц, 3H); 1,52 (s ушир., 1H); 1,62-1,67 (m, 1H); 1,77-1,89 (m, 2H); 2,15-2,18 (m, 1H); 2,29-2,32 (m, 2H); 2,36-2,40 (m, 1H); 2,72 (dd, J=3,2 Гц; 6,8 Гц, 1H); 2,88 (t, J=1,6 Гц, 2H); 3,45-3,49 (m, 3H); 3,87 (s, 6H); 6,77-6,82 (m, 3H). + МС (ІЕР): m/z=350,80 (M+H ). Приклад 44 1-(1-(3,4-Диметоксифеніл)циклобутил)-N-(3-метоксипропіл)-3-метилбутан-1-амін (8q). 1 Безбарвне масло (80 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,70-0,74 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,06-1,12 (m, 1H); 1,63-1,72 (m, 3H); 1,76-1,88 (m, 2H); 2,132,16 (m, 1H); 2,27-2,32 (m, 2H); 2,37-2,40 (m, 1H); 2,71 (dd, J=2,4 Гц; 9,6 Гц, 1H); 2,80-2,84 (m, 2H); + 3,32 (s, 3H); 3,45 (t, J=6,4 Гц, 2H); 3,87 (s, 6H); 6,76-6,82 (m, 3H). МС (ІЕР): m/z=350,80 (M+H ). Приклад 45 1-(1-(3,4-Диметоксифеніл)циклобутил)-N-(3-етоксипропіл)-3-метилбутан-1-амін (8r). 1 Безбарвне масло (100 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,70-0,74 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,08-1,12 (m, 1H); 1,19 (t, J=6,8 Гц, 3H); 1,63- 1,72 (m, 3H); 1,76-1,88 (m, 2H); 2,13-2,16 (m, 1H); 2,27-2,32 (m, 2H); 2,37-2,40 (m, 1H); 2,71 (dd, J=2,4 Гц; 9,6 Гц, 1H); 2,82 (t, J=6,4 Гц, 2H); 3,43-3,50 (m, 4H); 3,87 (s, 6H); 6,76- 6,82 (m, 3H). МС (ІЕР): + m/z=364,62 (M+H ). 22 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 Приклад 46 1-(1-(3,4-Диметоксифеніл)циклобутил)-N-(4-метоксибутил)-3-метилбутан-1-амін (8s). 1 Безбарвне масло (130 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,70-0,74 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,08-1,12 (m, 1H); 1,57-1,64 (m, 6H); 1,78-1,89 (m, 3H); 2,132,16 (m, 1H); 2,27-2,32 (m, 2H); 2,37-2,40 (m, 1H); 2,74 (s ушир., 1H); 3,27 (s ушир., 3H); 3,36 (t, + J=5,6 Гц, 2H); 3,87 (s, 6H); 6,76-6,82 (m, 3H). МС (ІЕР): m/z=364,62 (M+H ). Приклад 47 1-(1-(3,4-Диметоксифеніл)циклобутил)-N-(4-етоксибутил)-3-метилбутан-1-амін (8t). 1 Безбарвне масло (100 мг, вихід 27 %). H ЯМР (400 МГц, CDCl3): δ 0,69-0,74 (m, 1H); 0,83 (d, J=6,8 Гц, 3H); 0,88 (d, J=6,8 Гц, 3H); 1,04-1,12 (m, 1H); 1,19 (t, J=6,8 Гц, 3H); 1,24- 1,30 (m, 3H); 1,45-1,51 (m, 2H); 1,58-1,65 (m, 2H); 2,14-2,18 (m, 1H); 2,27-2,40 (m, 3H); 2,69-2,78 (m, 3H); 3,39+ 3,42 (m, 4H); 3,87 (s, 6H); 6,76-6,82 (m, 3H). МС (ІЕР): m/z=378,20 (M+H ). Загальна методика синтезу тіоефірних похідних фенілциклобутилметиламіну 12 і 13 (Схема 3) До перемішуваного розчину фенілциклоалкілметиламіну (6) (1 екв.), алкілтіоалкілкарбонової кислоти (14) (1,2 екв.) і DMAP (0,6 г, 1 екв.) в 20 мл при 0 °C в атмосфері азоту по краплях додавали розчин дициклогексилкарбодііміду (DCC) (1,4 г, 0,0070 моль, 1,2 екв.) в 10 мл ДХМ. Після завершення додавання, реакційну суміш перемішували при кімнатній температурі протягом 15 год. Хід реакції контролювали за допомогою тонкошарової хроматографії (ТШХ). Реакційну суміш фільтрували, і фільтрат концентрували при зниженому тиску. Залишок очищали за допомогою колоночної хроматографії на силікагелі з одержанням відповідних амідів (15) у вигляді білих твердих речовин із виходом 70-90 %. До суспензії алюмогідриду літію (LAH) (0,417 г, 4,2 екв.) в 20 мл безводного ТГФ по краплях додавали розчин аміду (15) (1 екв.) в 20 мл ТГФ при 0 °C в атмосфері азоту. Після завершення додавання, реакційну суміш доводили до к. т. і потім кип'ятили зі зворотним холодильником протягом 24 год. Хід реакції контролювали за допомогою тонкошарової хроматографії (ТШХ). Реакційну суміш охолоджували до 0 °C, і реакцію зупиняли шляхом послідовного додавання 2,5 мл води, 4,5 мл 10 % NaOH і, нарешті, 2 мл води. Після перемішування протягом деякого часу додавали простий ефір. Осад фільтрували через целітний фільтр і промивали етилацетатом. Об'єднані фільтрати випарювали, і залишок очищали за допомогою хроматографії на силікагелі із застосуванням градієнта гексану й етилацетату в якості елюентів із одержанням відповідних чистих тіоефірних похідних (12, 13). Чисті тіоефіри (12, 13) демонстрували задовільні результати 1H ЯМР і/або мас-спектрометричного аналізу. Вибрані рацемічні прості ефірні похідні (12, 13) піддавали хіральній ВЕРХ із одержанням відповідних оптично чистих (R)- і (S)-ізомерів із застосуванням умов, описаних для простих ефірних похідних (7, 8) на схемі 2. Усі тіоефірні похідні (12, 13) перетворювали у відповідні HCl солі за допомогою їхньої обробки 1 н. HCl у діоксані/воді з наступною ліофілізацією. Гідрохлоридні солі тіоефірних похідних (12, 13) тестували на переносниках моноамінів (MATs) у фармакологічних дослідженнях in vitro. Приклад 48 N-(4-(Етилтіо)бутил)-1-(1-(4-фторфеніл)циклобутил)-3-метилбутан-1-амін (12a). 1 Безбарвне масло (0,47 г, вихід 51 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,63 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 1,03-1,06 (m, 1H); 1,26 (t, J=7,2 Гц, 3H); 1,47- 1,54 (m, 2H); 1,56-1,67 (m, 3H); 1,71-1,77 (m, 1H); 1,84-1,92 (m, 1H); 2,10-2,17 (m, 1H); 2,20-2,26 (m, 2H); 2,342,38 (m, 1H); 2,50-2,55 (m, 3H); 2,65-2,72 (m, 2H); 2,74-2,80 (m, 2H); 6,97 (dd, J=8,4 Гц; 11,6 Гц, + 1H); 7,06 (dd, J=1,6 Гц; 7,6 Гц, 1H); 7,12-7,17 (m, 2H). МС (ІЕР): m/z=352,20 (M+H ). Приклад 49 1-(1-(4-Хлорфеніл)циклобутил)-N-(4-(етилтіо)бутил)-3-метилбутан-1-амін (12b). 1 Безбарвне масло (0,48 г, вихід 51 %). H ЯМР (400 МГц, CDCl3): δ 0,60-0,66 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 1,03-1,09 (m, 3H); 1,25 (t, J=7,2 Гц, 3H); 1,47- 1,54 (m, 2H); 1,58-1,65 (m, 2H); 1,73-1,78 (m, 1H); 1,84-1,91 (m, 1H); 2,11-2,18 (m, 1H); 2,21-2,29 (m, 2H); 2,352,42 (m, 1H); 2,50-2,55 (m, 4H); 2,67-2,77 (m, 3H); 7,16 (d, J=8,8 Гц, 2H); 7,25 (d, J=8,8 Гц, 2H). МС + (ІЕР): m/z=369,20 (M+H ). Приклад 50 1-(1-(4-Етоксифеніл)циклобутил)-N-(2-(етилтіо)етил)-3-метилбутан-1-амін (12c). 1 Безбарвне масло (0,37 г, вихід 52 %). H ЯМР (400 МГц, CDCl3): δ 0,69-0,75 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 1,05-1,11 (m, 1H); 1,26 (t, J=7,2 Гц, 3H); 1,40 (t, J=7,2 Гц, 3H); 1,54-1,66 (m, 2H); 1,72-1,74 (m, 1H); 1,82-1,88 (m, 1H); 2,03-2,18 (m, 1H); 2,25-2,26 (m, 2H); 2,52 (q, J=7,6 Гц, 2H); 2,61 (t, J=6,8 Гц, 2H); 2,70 (dd, J=2,0 Гц; 9,6 Гц, 1H); (t, J=6,8 Гц, 2H); 4,01 (q, + J=7,2 Гц, 2H); 6,82 (d, J=8,4 Гц, 2H); 7,15 (d, J=8,4 Гц, 2H). МС (ІЕР): m/z=350,20 (M+H ). Приклад 51 23 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 4-(Бутилтіо)-N-(1-(1-(4-етоксифеніл)циклобутил)пропіл)бутан-1-амін (12d). 1 Безбарвне масло (0,47 г, вихід 53 %). H ЯМР (400 МГц, CDCl3): δ 0,72-0,80 (m, 1H); 0,840,91 (m, 6H); 1,34-1,46 (m, 6H); 1,48-1,65 (m, 6H); 1,71-1,80 (m, 1H); 1,82-1,89 (m, 1H); 2,15-2,37 (m, 4H); 2,46-2,51 (m, 5H); 2,63-2,75 (m, 2H); 4,01 (q, J=7,2 Гц, 2H); 6,82 (d, J=8,4 Гц, 2H); 7,15 (d, + J=8,4 Гц, 2H). МС (ІЕР): m/z=378,20 (M+H ). Приклад 52 1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(2-(етилтіо)етил)-3-метилбутан-1-амін (13a). 1 Безбарвне масло (0,41 г, вихід 53 %). H ЯМР (400 МГц, CDCl3): δ 0,60-0,67 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 1,03-1,06 (m, 2H); 1,26 (t, J=7,2 Гц, 3H); 1,55- 1,61 (m, 1H); 1,70-1,74 (m, 1H); 1,80-1,86 (m, 1H); 2,08-2,14 (m, 1H); 2,18-2,23 (m, 2H); 2,30-2,35 (m, 1H); 2,432,50 (m, 2H); 2,53-2,60 (m, 2H); 2,68 (d, J=10,0 Гц, 1H); 2,81-2,91 (m, 2H); 7,04 (dd, J=2,0 Гц; 8,4 + Гц, 1H); 7,30 (d, J=2,0 Гц, 1H); 7,32 (d, J=8,4 Гц, 1H). МС (ІЕР): m/z=376,20 (M+H ). Приклад 53 N-(2-(Бутилтіо)етил)-1-(1-(3,4-дихлорфеніл)циклобутил)-3-метилбутан-1-амін (13b). 1 Безбарвне масло (0,27 г, вихід 50 %). H ЯМР (400 МГц, CDCl3): δ 0,60-0,67 (m, 1H); 0,810,92 (m, 9H); 1,04-1,10 (m, 1H); 1,34-1,45 (m, 2H); 1,50-1,58 (m, 2H); 1,60-1,65 (m, 1H); 1,73-1,78 (m, 1H); 1,85-1,91 (m, 1H); 2,15-2,19 (m, 1H); 2,23-2,30 (m, 2H); 2,35-2,40 (m, 1H); 2,46-2,50 (m, 2H); 2,58-2,62 (m, 2H); 2,68 (dd, J=2,4 Гц; 10,0 Гц, 1H); 2,85-2,93 (m, 2H); 7,04 (dd, J=2,0 Гц; 8,4 + Гц, 1H); 7,30 (d, J=2,0 Гц, 1H); 7,32 (d, J=8,4 Гц, 1H). МС (ІЕР): m/z=403,20 (M+H ). Приклад 54 1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(4-(етилтіо)бутил)-3-метилбутан-1-амін (13c). 1 Безбарвне масло (0,37 г, вихід 52 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,63 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 1,03-1,06 (m, 1H); 1,26 (t, J=7,2 Гц, 3H); 1,47- 1,54 (m, 2H); 1,56-1,67 (m, 3H); 1,71-1,77 (m, 1H); 1,84-1,92 (m, 1H); 2,10-2,17 (m, 1H); 2,20-2,26 (m, 2H); 2,342,38 (m, 1H); 2,50-2,55 (m, 3H); 2,65-2,72 (m, 2H); 2,74-2,80 (m, 2H); 7,04 (dd, J=2,0 Гц; 8,4 Гц, 1H); + 7,30 (d, J=2,0 Гц, 1H); 7,32 (d, J=8,4 Гц, 1H). МС (ІЕР): m/z=403,20 (M+H ). Приклад 55 N-(4-(Бутилтіо)бутил)-1-(1-(3,4-дихлорфеніл)циклобутил)-3-метилбутан-1-амін (13d). 1 Безбарвне масло (0,45 г, вихід 55 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,63 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 0,88 (t, J=7,2 Гц, 3H); 1,02-1,05 (m, 1H); 1,36- 1,43 (m, 2H); 1,48-1,65 (m, 7H); 1,73-1,77 (m, 1H); 1,85-1,90 (m, 1H); 2,10-2,16 (m, 1H); 2,18-2,25 (m, 2H); 2,342,39 (m, 1H); 2,48-2,52 (m, 4H); 2,65-2,80 (m, 3H); 7,04 (dd, J=2,0 Гц; 8,4 Гц, 1H); 7,30 (d, J=2,0 Гц, + 1H); 7,32 (d, J=8,4 Гц, 1H). МС (ІЕР): m/z=431,20 (M+H ). Приклад 56 1-(1-(2,4-Дихлорфеніл)циклобутил)-N-(4-(етилтіо)бутил)-3-метилбутан-1-амін (13e). 1 Безбарвне масло (0,57 г, вихід 51 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,63 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 1,03-1,06 (m, 1H); 1,26 (t, J=7,2 Гц, 3H); 1,47- 1,54 (m, 2H); 1,56-1,67 (m, 3H); 1,71-1,77 (m, 1H); 1,84-1,92 (m, 1H); 2,10-2,17 (m, 1H); 2,20-2,26 (m, 2H); 2,342,38 (m, 1H); 2,50-2,55 (m, 3H); 2,65-2,72 (m, 2H); 2,74-2,80 (m, 2H); 7,02 (d, J=8,4 Гц, 1H); 7,16 + (dd, J=2 Гц; 8,4 Гц, 1H); 7,29 (d, J=2,4 Гц, 1H). МС (ІЕР): m/z=403,20 (M+H ). Приклад 57 1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(2-(етилтіо)етил)пропан-1-амін (13f). 1 Безбарвне масло (0,27 г, вихід 52 %). H ЯМР (400 МГц, CDCl3): δ 0,72-0,79 (m, 1H); 0,92 (t, J=7,6 Гц, 3H); 1,23 (t, J=7,6 Гц, 3H); 1,42-1,48 (m, 1H); 1,72-1,79 (m, 1H); 1,86-1,93 (m, 1H); 2,182,30 (m, 3H); 2,34-2,41 (m, 1H); 2,49-2,55 (m, 3H); 2,60-2,69 (m, 2H); 2,80-2,89 (m, 1H); 2,86-2,97 (m, 1H); 7,04 (dd, J=2,0 Гц; 8,4 Гц, 1H); 7,30 (d, J=2,0 Гц, 1H); 7,32 (d, J=8,4 Гц, 1H). МС (ІЕР): + m/z=347,20 (M+H ). Приклад 58 4-(Бутилтіо)-N-(1-(1-(3,4-дихлорфеніл)циклобутил)пропіл)бутан-1-амін (13g). 1 Безбарвне масло (0,37 г, вихід 50 %). H ЯМР (400 МГц, CDCl3): δ 0,69-0,83 (m, 1H); 0,840,91 (m, 6H); 1,03-1,05 (m, 1H); 1,34-1,41 (m, 4H); 1,51-1,65 (m, 6H); 1,72-1,77 (m, 1H); 1,85- 1,92 (m, 1H); 2,17-2,30 (m, 2H); 2,34-2,41 (m, 1H); 2,45-2,50 (m, 4H); 2,62-2,68 (m, 1H); 2,72-2,78 (m, 1H); 7,04 (dd, J=2,0 Гц; 8,4 Гц, 1H); 7,30 (d, J=2,0 Гц, 1H); 7,32 (d, J=8,4 Гц, 1H). МС (ІЕР): + m/z=403,20 (M+H ). Загальна методика синтезу алкілсульфонільних похідних фенілциклобутилметиламіну 17 (Схема 4) Синтез амідних похідних (16, Стадія 1): До перемішуваного розчину m-CPBA (мхлорпербензойної кислоти) (0,94 г, 2,1 екв.) в 10 мл ТГФ по краплях додавали при -30 °C (сухий лід/ацетон) протягом 30 хвилин розчин аміду (15) (0,0026 моль) в 10 мл ТГФ. Хід реакції контролювали за допомогою ТШХ. Після завершення реакції, додавали 3 мл триетиламіну 24 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 (ТЕА), після чого додавали розчин 10 мл насиченого бікарбонату натрію. Органічний шар відокремлювали, промивали сольовим розчином, сушили над Na 2SO4 і випарювали. Залишок очищали за допомогою хроматографії на силікагелі із застосуванням градієнта гексану й етилацетату в якості елюентів із одержанням відповідних чистих амідів (16). Синтез алкілсульфонільних похідних (17, Стадія 2): До суспензії алюмогідриду літію (LAH) (0,3 г, 4,2 екв.) в 20 мл безводного ТГФ по краплях додавали амід (16) (1 екв.) в 10 мл ТГФ при 0 °C в атмосфері азоту. Після завершення додавання, реакційну суміш доводили до кімнатної температури і потім кип'ятили зі зворотним холодильником протягом 15 год. Хід реакції контролювали за допомогою тонкошарової хроматографії (ТШХ). Реакційну суміш охолоджували до 0 °C, і реакцію зупиняли шляхом послідовного додавання 5 мл води, 9 мл 10 % NaOH і, нарешті, 4 мл води. Після перемішування протягом деякого часу додавали простий ефір. Осад фільтрували через целітний фільтр і промивали етилацетатом. Об'єднані фільтрати випарювали, і залишок очищали за допомогою колоночної хроматографії на силікагелі із застосуванням градієнта гексану й етилацетату з одержанням відповідних сульфонільних похідних (17). Чисті сульфонільні похідні (17) демонстрували задовільні результати 1H ЯМР і/або мас-спектрометричного аналізу. Усі сульфонільні похідні (17) перетворювали у відповідні HCl солі за допомогою їхньої обробки 1 н. HCl у діоксані/воді з наступною ліофілізацією. Гідрохлоридні солі алкілсульфонільних похідних (17) тестували на переносниках моноамінів (MATs) у фармакологічних дослідженнях in vitro. Приклад 59 N-(1-(1-(3,4-Дихлорфеніл)циклобутил)-3-метилбутил)-4-(етилсульфоніл)бутанамід (16a). 1 Безбарвне масло (0,85 г, вихід 73 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,71 (m, 1H); 0,80 (d, J=6,8 Гц, 3H); 0,90 (d, J=6,8 Гц, 3H); 1,13-1,19 (m, 1H); 1,24 (t, J=7,2 Гц, 3H); 1,78- 1,84 (m, 1H); 2,05-2,23 (m, 5H); 2,25-2,32 (m, 2H); 2,37-2,47 (m, 2H); 2,96-3,07 (m, 4H); 4,47-4,53 (m, 1H); 4,93 (d, J=10,4 Гц, 1H); 6,94 (dd, J=2,0 Гц; 8,4 Гц, 1H); 7,16 (d, J=2,0 Гц, 1H); 7,38 (d, J=8,4 Гц, 1H). МС + (ІЕР): m/z=449,20 (M+H ). Приклад 60 4-(Бутилсульфоніл)-N-(1-(1-(3,4-дихлорфеніл)циклобутил)-3-метилбутил)бутанамід (16b). 1 Безбарвне масло (0,85 г, вихід 73 %). H ЯМР (400 МГц, CDCl3): δ 0,57-0,71 (m, 1H); 0,80 (d, J=6,8 Гц, 3H); 0,91 (t, J=7,2 Гц, 3H); 0,95 (d, J=6,8 Гц, 3H); 1,13-1,19 (m, 1H); 1,38- 1,50 (m, 3H); 1,75-1,85 (m, 3H); 2,05-2,23 (m, 5H); 2,25-2,32 (m, 2H); 2,37-2,47 (m, 2H); 2,93-2,97 (m, 2H); 3,013,05 (m, 2H); 4,47-4,53 (m, 1H); 4,93 (d, J=10,4 Гц, 1H); 6,94 (dd, J=2,0 Гц; 8,4 Гц, 1H); 7,16 (d, + J=2,0 Гц, 1H); 7,38 (d, J=8,4 Гц, 1H). МС (ІЕР): m/z=477,20 (M+H ). Приклад 61 1-(1-(3,4-Дихлорфеніл)циклобутил)-N-(4-(етилсульфоніл)бутил)-3-метилбутан-1-амін (17a) 1 Безбарвне масло (0,11 г, вихід 31 %). H ЯМР (400 МГц, CDCl3): δ 0,58-0,65 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 1,03-1,08 (m, 1H); 1,38 (t, J=7,2 Гц, 3H); 1,52- 1,59 (m, 3H); 1,74-1,78 (m, 1H); 1,84-1,93 (m, 3H); 2,08-2,15 (m, 1H); 2,17-2,28 (m, 2H); 2,31-2,36 (m, 1H); 2,662,71 (m, 2H); 2,78-2,83 (m, 1H); 2,93-3,00 (m, 4H); 7,04 (dd, J=2,0 Гц; 8,4 Гц, 1H); 7,30 (d, J=2,0 Гц, + 1H); 7,32 (d, J=8,4 Гц, 1H). МС (ІЕР): m/z=435,20 (M+H ). Приклад 62 N-(4-(Бутилсульфоніл)бутил)-1-(1-(3,4-дихлорфеніл)циклобутил)-3-метилбутан-1-амін (17b). 1 Безбарвне масло (0,07 г, вихід 37 %). H ЯМР (400 МГц, CDCl3): δ 0,59-0,65 (m, 1H); 0,82 (d, J=6,8 Гц, 3H); 0,87 (d, J=6,8 Гц, 3H); 0,95 (t, J=7,2 Гц, 3H); 1,03-1,05 (m, 1H); 1,43- 1,51 (m, 2H); 1,52-1,62 (m, 3H); 1,72-1,86 (m, 4H); 1,88-1,93 (m, 3H); 2,08-2,38 (m, 4H); 2,66-2,71 (m, 2H); 2,782,84 (m, 1H); 2,91-2,97 (m, 4H); 7,04 (dd, J=2,0 Гц; 8,4 Гц, 1H); 7,30 (d, J=2,0 Гц, 1H); 7,32 (d, J=8,4 + Гц, 1H). МС (ІЕР): m/z=463,20 (M+H ). Загальна методика синтезу фенілциклоалкіламінових похідних 19 (Схема 5) Синтез амідів (21, Стадія 1): До перемішуваного розчину 2M розчина триметилалюмінію (4 мл, 0,008 моль) у толуолі по краплях додавали розчин фенілциклоалкіламіну (6) (0,0053 моль, 1 екв.) і складного ефіру (20) (0,0053 моль, 1 екв.) у толуолі в атмосфері азоту при 0 °C у герметично закритій пробірці. Реакційну суміш перемішували при 80 °C протягом 5 год. Хід реакції контролювали за допомогою ТШХ. Після завершення реакції суміш концентрували під вакуумом, реакцію зупиняли шляхом додавання дробленого льоду й екстрагували етилацетатом (15 мл x 3). Об'єднаний екстракт сушили над сульфатом натрію та концентрували при зниженому тиску. Залишок пропускали через коротку колонку з одержанням чистого аміду (21). Аміди (21a-d) одержували відповідно до цього протоколу. Вихідні складні ефіри (20) одержували шляхом алкілування циклічного піролідину і піперидину відповідними складними ефірами бромалкілкарбонових кислот у стандартних умовах із застосуванням триетиламіну (ТЕА) як основа в ДХМ в якості розчинника з гарними виходами. Аміди (21e-f) одержували 25 UA 114807 C2 5 10 15 20 25 30 35 40 45 50 55 60 шляхом комбінації 4-N, N-диметилбутанової кислоти з фенілциклоалкіламіном (6) із застосуванням HATU як агент для комбінації. До перемішуваного розчину аміну (6) (1 екв.), 4-N, N-диметилбутанової кислоти (1 екв.) і розчину HATU (2 екв.) у ДХМ по краплях додавали розчин N, N-діізопропілетиламіну (ДІЕА) (3 екв.) в атмосфері азоту при 0 °C. Реакційну суміш перемішували при кімнатній температурі протягом 5 год. Хід реакції контролювали за допомогою ТШХ. Після завершення реакції для її зупинки у суміш додавали воду й екстрагували ДХМ, об'єднані екстракти сушили над Na2SO4 і потім випарювали при зниженому тиску. Залишок очищали за допомогою колоночної хроматографії на силікагелі із застосуванням градієнта ДХМ і метанолу в якості елюентів із одержанням чистих амідів (21e-f). Аміди (21a-f) демонстрували задовільні результати 1H ЯМР і мас-спектрометричного (РХ/МС) аналізу. В якості типового прикладу в даній заявці наведені результати 1H ЯМР і МС аміду (21d). Синтез амінів (19, Стадія 2): Комплекс борану з диметилсульфідом (DMS) (1,5 екв.) у ТГФ по краплях додавали до охолодженого за допомогою льоду розчину аміду (21) (1 екв.) у ТГФ. Реакційну суміш перемішували при 60 °C протягом 3 год. Після завершення реакції для її зупинки у реакційну суміш додавали крижану воду і потім двічі екстрагували EtOAc. Об'єднані органічні шари промивали сольовим розчином і сушили над Na2SO4. Органічний шар випарювали при зниженому тиску. Неочищений продукт перебував у формі аміноборанового адукту або комплексу. Похідну аміну у формі вільної основи (19) одержували шляхом обробки аміноборанового комплексу відповідно до описаних способів із застосуванням нікелю Ренея в метанолі (Couturier, M. et al, Organic Letters, 2001, vol 3 (No. 3), 465-467) або піперазину в метанолі (Zhou, Q. et al, Organic letters 2011, vol 13 (No. 3), 526-529). Неочищені похідні аміну у формі вільної основи (19) очищали за допомогою препаративної ВЕРХ із застосуванням градієнта гексану й етанолу в якості елюентів із одержанням чистих похідних амінів (19). Приклад 63 N-(1-(1-(3,4-Диметоксифеніл)циклобутил)-3-метилбутил)-4-(піперидин-1-іл) бутанамід (21d) 1 Безбарвне масло (0,85 г, вихід 39 %). H ЯМР (300 МГц, ДМСОd6): δ 0,73-0,76 (m, 6H); 0,850,98 (m, 2H); 1,39-1,59 (m, 8H); 1,71 (b, 3H); 1,83-1,89 (m, 2H); 2,11-2,17 (m, 6H); 2,27- 2,49 (m, 4H); 3,73 (s, 3H); 3,74 (s, 3H); 4,19-4,25 (m, 1H), 6,62 (s, 1H), 6,64 (s ушир., 1H), 6,89 (d, J=7,8 Гц, + 1H); 7,30 (d ушир., 1H, обмінюється в D2O); МС (ІЕР): m/z=431,17 (M+H ). Приклад 64 1-(1-(3,4-Дихлорфеніл)циклобутил)-3-метил-N-(4-(піролідин-1-іл)бутил)бутан-1-амін (19a) 1 Безбарвне масло (0,092 г, вихід 18,7 %). H ЯМР (300 МГц, ДМСОd6): δ 0,61-0,67 (m, 1H); 0,85 (d, J=7,2 Гц, 3H); 0,90 (d, J=6,4 Гц, 3H); 1,04-1,10 (m, 1H); 1,36-1,43 (m, 3H); 1,56- 1,62 (m, 2H); 1,67-1,78 (m, 2H); 1,80-1,90 (m, 4H); 1,95-2,30 (m, 4H); 2,67-2,84 (m, 7H); 3,21 (t ушир., 2H); 7,07 (dd, J=2 Гц, 8 Гц, 1H), 7,31 (d, J=2 Гц, 1H); 7,34 (d, J=8,4 Гц, 1H); МС (ІЕР): m/z=411,16 (M+). Приклад 65 1-(1-(3,4-Диметоксифеніл)циклобутил)-3-метил-N-(4-(піролідин-1-іл)бутил)бутан-1-амін (19b) 1 Безбарвне масло (0,085 г, вихід 17,7 %). H ЯМР (300 МГц, CDCl3): δ 0,69-0,75 (m, 1H); 0,84 (d, J=6,6 Гц, 3H); 0,88 (d, J=6,6 Гц, 3H); 1,07-1,14 (m, 1H); 1,35-1,48 (m, 5H); 1,80- 1,86 (m, 6H); 2,14-2,17 (m, 2H); 2,30-2,35 (m, 2H); 2,67-2,77 (m, 7H); 3,19 (t ушир., 2H); 3,87 (s, 6H); 6,79-6,81 + (m, 3H); МС (ІЕР): m/z=403,23 (M+H ). Приклад 66 1-(1-(3,4-Дихлорфеніл)циклобутил)-3-метил-N-(4-(піперидин-1-іл)бутил)бутан-1-амін (19c) 1 Безбарвне масло (0,015 г, вихід 15,6 %); H ЯМР (300 МГц, ДМСОd6): δ 0,59-0,62 (m, 1H); 0,79 (d, J=6,6 Гц, 3H); 0,84 (d, J=6,6 Гц, 3H); 0,94-1,02 (m, 1H); 1,33-1,38 (m, 2H); 1,46- 1,48 (m, 3H); 1,59-1,75 (m, 8H); 2,11-2,16 (m, 2H); 2,43-2,50 (m, 2H); 2,65-2,77 (m, 9H); 7,20 (dd, J=5,1 Гц; 8,4 Гц, 1H); 7,42 (d, J=1,8 Гц, 1H); 7,51 (d, J=8,1 Гц, 1H). МС (ІЕР): m/z=425,13 (M+). Приклад 67 1-(1-(3,4-Диметоксифеніл)циклобутил)-3-метил-N-(4-(піперидин-1-іл)бутил)бутан-1-амін (19d). 1 Безбарвне масло (0,060 г, вихід 15,5 %). H ЯМР (400 МГц, CDCl3): δ 0,61-0,67 (m, 1H); 0,85 (d, J=6,8 Гц, 3H); 0,97 (d, J=6,8 Гц, 3H); 1,07-1,14 (m, 1H); 1,22-1,28 (m, 2H); 1,33- 1,47 (m, 3H); 1,58-1,71 (m, 2H); 1,61-1,67 (m, 2H); 1,73-2,30 (m, 6H); 2,35-2,42 (m, 1H); 2,67-2,84 (m, 8H); 3,23 (s + ушир., 2H); 3,87 (s, 6H); 6,79-6,81 (m, 3H). МС (ІЕР): m/z=417,20 (M+H ). Приклад 68 4 4 N1-(1-(1-(3,4-Дихлорфеніл)циклобутил)-3-метилбутил)-N ,N -диметилбутан-1,4-діамін (19e) 1 Безбарвне масло (0,045 г, вихід 11,6 %). H ЯМР (400 МГц, CDCl3): δ 0,59-0,65 (m, 1H); 0,80 (d, J=6,8 Гц, 3H); 0,84 (d, J=6,8 Гц, 3H); 0,95-1,02 (m, 1H); 1,22-1,28 (m, 1H); 1,33- 1,47 (m, 3H); 1,59-1,71 (m, 4H); 1,81-1,87 (m, 2H); 1,73-2,30 (m, 3H); 2,35-2,42 (m, 2H); 2,36-2,58 (m, 6H); 2,602,74 (m, 2H); 7,06 (dd, J=2,0 Гц; 8,4 Гц, 1H); 7,31 (d, J=2,0 Гц, 1H); 7,35 (d, J=8,4 Гц, 1H). МС (ІЕР): 26 UA 114807 C2 + 5 10 15 20 25 30 35 40 45 50 55 60 m/z=386,20 (M+H ). Приклад 69 4 4 N1-(1-(1-(3,4-Диметоксифеніл)циклобутил)-3-метилбутил)-N ,N -диметилбутан-1,4-діамін (19f) 1 Безбарвне масло (0,08 г, вихід 20 %). H ЯМР (400 МГц, CDCl3): δ 0,59-0,65 (m, 1H); 0,80 (d, J=6,8 Гц, 3H); 0,84 (d, J=6,8 Гц, 3H); 0,95-1,02 (m, 1H); 1,22-1,28 (m, 1H); 1,33-1,47 (m, 3H); 1,591,71 (m, 4H); 1,81-1,87 (m, 2H); 1,73-2,30 (m, 3H); 2,35-2,42 (m, 2H); 2,36-2,58 (m, 6H); 2,60-2,74 + (m, 2H); 3,87 (s, 6H); 6,79-6,81 (m, 3H). МС (ІЕР): m/z=377,20 (M+H ). Загальна методика синтезу алкоксіалкіл-4-нітробензолсульфонатів 9 (Схема 6) Синтез монобензилоксикарбінолів (24, Стадія 1): До перемішуваної суспензії NaH (3,5 г, 1,04 екв.) у сухому ТГФ (50 мл) додавали діол (23) (3 екв.) протягом 0,5 год. при 0 °C. Після завершення додавання суміш доводили до кипіння та по краплях додавали бензилбромід (10 мл, 0,084 моль, 1 екв.). Реакційну суміш кип'ятили зі зворотним холодильником при перемішуванні протягом 12 год. Хід реакції контролювали за допомогою тонкошарової хроматографії (ТШХ). Після завершення реакції суміш залишали охолоджуватися до кімнатної температури і розбавляли ефіром. Об'єднані екстракти сушили над MgSO 4, фільтрували і концентрували при зниженому тиску. Залишок пропускали через коротку колонку з силікагелем із застосуванням градієнта гексану й етилацетату в якості елюентів із одержанням чистого монобензилоксикарбінолу (24) у вигляді безбарвного масла з середніми виходами. Синтез алкоксіалкілбензилових ефірів (25, Стадія 2): До перемішуваної суспензії NaH (0,75 г, 1,5 екв.) у сухому ДМФА (20 мл) додавали монобензилоксикарбінол (24) (1 екв.) в 10 мл ДМФА при 0 °C. Після завершення додавання суміш перемішували протягом 1 год., і потім у неї по краплях додавали розчин відповідного алкілброміду або йодиду (2 екв.). Реакційну суміш перемішували протягом 15 год., і хід реакції контролювали за допомогою тонкошарової хроматографії (ТШХ). Після завершення реакції суміш розбавляли 25 мл води, екстрагували етилацетатом, сушили над безводним MgSO4, фільтрували і концентрували при зниженому тиску. Отримане масло очищали за допомогою колоночної хроматографії на силікагелі із застосуванням градієнта гексану й етилацетату в якості елюентів із одержанням відповідних алкоксіалкілбензилових ефірів (25) у вигляді безбарвного масла. Алкоксіалкілсульфонати (9, Стадія 3): До перемішуваної суспензії Pd/C (10 %) (активованого) (0,8 г) в етанолі (10 мл) додавали розчин алкоксіалкілбензилового ефіру (25) (0,001 моль) в 10 мл етанолу. Реакційну суміш витримували під тиском водню протягом 15 год. Хід реакції контролювали за допомогою тонкошарової хроматографії (ТШХ). Після завершення реакції суміш фільтрували через целітний фільтр, промивали етилацетатом і розчин фільтрату концентрували при зниженому тиску. Залишок пропускали через коротку колонку з силікагелем із застосуванням градієнта гексану і діетилового ефіру в якості елюентів із одержанням відповідного простого ефіру карбінолу (26) у вигляді безбарвного масла. Простий ефір карбінолу (26) піддавали обробці 4-нітросульфонілхлоридом у присутності м'якої основи триетиламіну (ТЕА) у ДХМ при температурі від 0 °C до 5 °C. Хід реакції контролювали за допомогою ТШХ. Після завершення реакції суміш промивали водою, сушили над безводним сульфатом магнію та концентрували при зниженому тиску. Залишок очищали за допомогою хроматографії на силікагелі із застосуванням градієнта гексану й етилацетату в якості елюентів із одержанням алкоксіалкілсульфонатів (9). Приклад 70 1 2-Етоксіетил-4-нітробензолсульфонат (9a). Біла тверда речовина (1,87 г, вихід 93 %). H ЯМР (400 МГц, CDCl3): δ 1,08 (t, J=7,2 Гц, 3H); 3,41 (q, J=7,2 Гц, 2H); 3,61 (t, J=4,4 Гц, 2H); 4,28 (t, J=4,4 Гц, 2H); 8,16 (d, J=8,8 Гц, 2H); 8,37 (d, J=8,8 Гц, 2H). Приклад 71 1 2-Метоксіетил-4-нітробензолсульфонат (9b). Біла тверда речовина (1,87 г, вихід 93 %). H ЯМР (400 МГц, CDCl3): δ 3,28 (s, 3H); 3,59 (t, J=4,4 Гц, 2H); 4,30 (t, J=4,4 Гц, 2H); 8,13 (d, J=8,8 Гц, 2H); 8,40 (d, J=8,8 Гц, 2H). Приклад 72 1 2-Етоксибутил-4-нітробензолсульфонат (9c). Біла тверда речовина (1,87 г, вихід 93 %). H ЯМР (400 МГц, CDCl3): δ 1,08 (t, J=6,8 Гц, 3H); 1,59-1,63 (m, 2H); 1,76-1,83 (m, 2H); 3,37-3,45 (m, 4H); 4,19 (t, J=6,4 Гц, 2H); 8,11 (d, J=8,8 Гц, 2H); 8,40 (d, J=8,8 Гц, 2H). Приклад 73 1 2-Метоксибутил-4-нітробензолсульфонат (9d). Біла тверда речовина (1,87 г, вихід 93 %). H ЯМР (400 МГц, CDCl3): δ 1,57-1,63 (m, 2H); 1,72-1,82 (m, 2H); 3,28 (s, 3H); 3,33- 3,44 (m, 3H); 4,10 (t, J=6,4 Гц, 2H); 8,11 (d, J=8,8 Гц, 2H); 8,40 (d, J=8,8 Гц, 2H). Приклад 74 27 UA 114807 C2 1 5 10 15 20 25 30 35 40 45 50 55 60 4-Пропоксибутил-4-нітробензолсульфонат (9e). Біла тверда речовина (1,87 г, вихід 93 %). H ЯМР (400 МГц, CDCl3): δ 0,84 (t, J=7,2 Гц, 3H); 1,44-1,51 (m, 2H); 1,91-1,97 (m, 2H); 3,28 (t, J=6,8 Гц, 2H); 3,43 (t, J=5,6 Гц, 2H); 4,26 (t, J=6,4 Гц, 2H); 8,11 (d, J=8,8 Гц, 2H); 8,40 (d, J=8,8 Гц, 2H). Приклад 75 1 4-Бутоксипропіл-4-нітробензолсульфонат (9f). Біла тверда речовина (1,87 г, вихід 93 %). H ЯМР (400 МГц, CDCl3): δ 0,88 (t, J=7,2 Гц, 3H); 1,25-1,31 (m, 2H); 1,41-1,47 (m, 2H); 1,94 (t, J=6,0 Гц, 2H); 3,31 (t, J=6,4 Гц, 2H); 3,42 (t, J=5,6 Гц, 2H); 4,26 (t, J=6,4 Гц, 2H); 8,11 (d, J=8,8 Гц, 2H); 8,40 (d, J=8,8 Гц, 2H). Приклад 76 Етил-4-Етоксибутаноат (30) (Схема 7). До охолодженого за допомогою льоду розчину γбутиролактону (28) (11,2 г, 0,13009 ммоль, 1,0 екв.), триетилортоформіату (29) (41,1 мл, 0,2497 ммоль, 1,92 екв.) в 100 мл етанолу додавали 0,25 мл (0,0045 ммоль, 0,035 екв.) сірчаної кислоти. Суміш нагрівали при 50 °C протягом 12 год. при контролі ходу реакції за допомогою ТШХ. Реакційну суміш охолоджували до кімнатної температури і більшу частину розчинника випарювали при зниженому тиску. Концентровану реакційну суміш гасили холодним насиченим розчином NaHCO3 і двічі піддавали екстракції етилацетатом. Об'єднані органічні екстракти сушили над безводним Na2SO4 і концентрували під вакуумом із одержанням 20 г (95 %) етил-41 етоксибутаноату (30) у вигляді світло-жовтого масла. H ЯМР (400 МГц, CDCl3): δ 1,16-1,28 (m, 6H); 1,87-1,91 (m, 2H); 2,39(t, J=9,6 Гц; 2H); 3,42-3,50 (m, 2H); 3,57-3,64 (m, 2H); 4,13 (q, J=6 Гц, 2H). Приклад 77 3-Етоксибутанова кислота (10) (Схема 7). До охолодженого за допомогою льоду розчину етил-4-етоксибутаноату (30) (~1 г) в 10 мл тетрагідрофурану (ТГФ) додавали водний розчин NaOH (0,62 г в 7 мл H2O) і проводили перемішування при кімнатній температурі протягом 12 год., контролюючи хід реакції за допомогою ТШХ. Більшу частину розчинника випарювали при зниженому тиску, і залишок розбавляли водою (10 мл). Водний шар підкисляли розчином 1 н. HCl (pH ~ 2) і потім піддавали екстракції етилацетатом (15 мл x 3). Об'єднані органічні екстракти сушили над безводним Na2SO4 і концентрували під вакуумом із одержанням 0,6 г (73,14) 41 етоксибутанової кислоти у вигляді світло-жовтого масла. H ЯМР (400 МГц, CDCl3): δ 1,20 (t, J=9,2 Гц, 3H); 1,87-1,95 (m, 2H); 2,47 (t, J=10 Гц; 2H); 3,48 (q, J=9,2 Гц, 4H). Загальна методика синтезу складних ефірів алкілтіоалкілкарбонової кислоти (33) (Схема 8) До перемішуваного розчину алкантіолату натрію (32) (1 екв.) у безводному ДМФА (10 мл) при 0 °C додавали складний ефір бромалкілкарбонової кислоти (31) (1 екв.) протягом 5 хв. Реакційну суміш перемішували протягом 15 год. при кімнатній температурі. Хід реакції контролювали за допомогою тонкошарової хроматографії (ТШХ). Реакційну суміш розбавляли етилацетатом (20 мл) і промивали насиченим розчином NaHCO 3 (водний шар гасили гіпохлоритом натрію (bleach)). Органічний шар сушили над безводним Na 2SO4 із одержанням відповідного складного ефіру алкілтіоефіркарбонової кислоти (33), який очищали за допомогою колоночної хроматографії на силікагелі із застосуванням градієнта гексану й етилацетату і виділяли у вигляді безбарвного масла. Приклад 78 1 Етил-4-(етилтіо)бутанoат (33a). Безбарвне масло (6,87 г, вихід 100 %). H ЯМР (400 МГц, CDCl3): δ 1,20-1,26 (m, 6H); 1,84-1,92 (m, 2H); 2,40 (t, J=9,6 Гц, 2H); 2,47-2,55 (m, 4H); 4,12 (q, J=7,2 Гц, 2H). Приклад 79 1 Етил-2-(етилтіо)ацетат (33b). Безбарвне масло (5,87 г, вихід 90 %). H ЯМР (400 МГц, CDCl3): δ 1,20-1,29 (m, 6H); 2,63 (q, J=7,6 Гц, 2H); 3,19 (s, 2H); 4,15 (q, J=7,2 Гц, 2H). Приклад 80 1 Етил-4-(бутилтіо)бутанoат (33c). Безбарвне масло (14,12 г, вихід 100 %). H ЯМР (400 МГц, CDCl3): δ 0,89 (t, J=7,6 Гц, 3H); 1,22 (t, J=7,6 Гц, 3H); 1,34-1,36 (m, 2H); 1,48- 1,54 (m, 2H); 1,871,90 (m, 2H); 2,39 (t, J=7,6 Гц, 2H); 2,44-2,51 (m, 4H); 4,10 (q, J=7,6 Гц, 2H). Приклад 81 1 Етил-2-(бутилтіо)ацетат (33d). Безбарвне масло (5,80 г, вихід 100 %). H ЯМР (400 МГц, CDCl3): δ 0,89 (t, J=6,8 Гц, 3H); 1,26 (t, J=7,2 Гц, 3H); 1,36-1,41 (m, 2H); 1,52- 1,61 (m, 2H); 2,61 (t, J=7,6 Гц, 2H); 3,18 (s, 2H); 4,15 (q, J=7,2 Гц, 2H). Загальна методика синтезу алкілтіоефірів карбонових кислот (14) (Схема 8) До перемішуваного розчину складного ефіру алкілтіоефіркарбонової кислоти (33) (0,1 моль, 1 екв.) в етанолі (20 мл) по краплях додавали 2 н. водн. NaOH (1,5 екв.). Реакційну суміш перемішували при кімнатній температурі протягом 30 хв. (хід реакції контролювали за допомогою ТШХ). Після завершення реакції реакційну суміш концентрували на роторному 28
ДивитисяДодаткова інформація
Назва патенту англійськоюCompositions, synthesis, and methods of using phenylcycloalkylmethylamine derivatives
Автори англійськоюBhat, Laxminarayan, Adiey, Kouacou, Bhat, Seema Rani
Автори російськоюБхат Лаксминараян, Адиэй Коуакоу, Бхат Сима Рани
МПК / Мітки
МПК: A61K 31/13, C07C 211/26, C07C 211/25
Мітки: способи, застосування, фенілциклоалкілметиламіну, композиції, похідних, синтез
Код посилання
<a href="https://ua.patents.su/32-114807-kompozici-sintez-i-sposobi-zastosuvannya-pokhidnikh-fenilcikloalkilmetilaminu.html" target="_blank" rel="follow" title="База патентів України">Композиції, синтез і способи застосування похідних фенілциклоалкілметиламіну</a>
Попередній патент: Система для утворення аерозолю з відстежуванням споживання та зворотним зв’язком
Наступний патент: Фармацевтична діагностика
Випадковий патент: Спосіб контролю чисельності популяцій плодожерок (lepidoptera, tortricidae)