2,4-діамінопіримідини, фармацевтична композиція, що їх містить, та спосіб лікування малярії
Номер патенту: 105759
Опубліковано: 25.06.2014
Автори: Тарнчомпу Бонгкоч, Чарман Сьюзан, Ютхавонг Йонгіют, Чітнумсуб Пенчіт, Тонгпанчанг Чавані, Чарман Уільям, Вівас Лівія, Меттьюз Дейвід, Камчонвонгпайсан Сумалі, Вілаїван Тірают, Катіяр Санджай Бабу, Юваніяма Джірундон
Формула / Реферат
1. Сполука формули І:
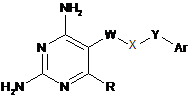 (I),
(I),
де R — водень або С1-4-алкіл;
W-X-Y — О(СН2)2-4О;
Аr — ароматичний цикл, вибраний з-посеред заміщеного фенілу та факультативно заміщеного нафтилу, або факультативно заміщений гетероароматичний цикл, вибраний з групи, до якої входять хінолініл, ізохінолініл, хіназолініл, хіноксалініл, піридил, індоліл, триазоліл, бензоксазоліл, бензімідазоліл, індолініл та бензотриазоліл;
причому, якщо Аr — ароматичний цикл, то термін “заміщений” означає групи, заміщені щонайменше одним замісником, вибраним з групи, до якої входять ацил, бензоксазоліл, карбоксил, карбоксі-С1-3-алкіл, карбоксі-С1-3-алкілоксигрупа, С1-3-алкілоксикарбоніл-С1-3-алкіл, С1-3-алкілоксикарбоніл-С1-3-алкілоксигрупа, тетразоліл, тетразоліл-С1-3-алкіл та тетразоліл-С1-3-алкілоксигрупа; та, якщо Аr — факультативно заміщений гетероароматичний цикл, то термін “заміщений” означає групи, заміщені одним або кількома замісниками, вибраними з групи, яку складають алкіл, заміщений алкіл, циклоалкіл, заміщений циклоалкіл, трифторметил, арил, заміщений арил, галоген, аміногрупа, заміщена аміногрупа, алкоксигрупа, арилоксигрупа, гідроксил та нітрогрупа;
або фармацевтично прийнятна сіль такої сполуки.
2. Сполука за п. 1, яка відрізняється тим, що R — С1-4-алкіл.
3. Сполука за п. 1 або п.2, яка відрізняється тим, що R — етил.
4. Сполука за будь-яким з попередній пунктів, де Аr — феніл, заміщений щонайменше одним замісником, вибраним з групи, до якої входять ацил, бензоксазоліл, карбоксил, карбоксі-С1-3-алкіл, карбоксі-С1-3-алкілоксигрупа, С1-3-алкілоксикарбоніл-С1-3-алкіл, С1-3-алкілоксикарбоніл-С1-3-алкілоксигрупа, тетразоліл, тетразоліл-С1-3-алкіл та тетразоліл-С1-3-алкілоксигрупа.
5. Сполука за будь-яким з пп. 1-3, де Аr — 4-хінолініл або заміщений 4-хінолініл, де термін “заміщений” означає один або кілька замісників, вибраних з групи, яку складають алкіл, заміщений алкіл, циклоалкіл, заміщений циклоалкіл, трифторметил, арил, заміщений арил, галоген, аміногрупа, заміщена аміногрупа, алкоксигрупа, арилоксигрупа, гідроксил та нітрогрупа.
6. Сполука за п. 1, де R — етил, W-X-Y — О(СН2)3О, та Аr — хінолініл або заміщений 4-хінолініл, де термін “заміщений” означає один або кілька замісників, вибраних з групи, яку складають алкіл, заміщений алкіл, циклоалкіл, заміщений циклоалкіл, трифторметил, арил, заміщений арил, галоген, аміногрупа, заміщена аміногрупа, алкоксигрупа, арилоксигрупа, гідроксил та нітрогрупа.
7. Сполука за п. 1, вибрана з групи, яку складають:

2,4-діаміно-6-етил-5-(3-(хінолін-4-ілокси)пропокси)піримідин (Р113);

2,4-діаміно-6-етил-5-(3-(6-хлорхінолін-4-ілокси)пропокси)піримідин (Р149);

2,4-діаміно-6-етил-5-(3-(6-фторхінолін-4-ілокси)пропокси)піримідин (Р153);
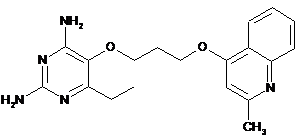
2,4-діаміно-6-етил-5-(3-(2-метилхінолін-4-ілокси)пропокси)піримідин (Р154);

2,4-діаміно-6-етил-5-(3-(7-фтор-2-метилхінолін-4-ілокси)пропокси)піримідин (Р157);

2,4-діаміно-6-етил-5-(3-(2-(3-карбоксипропокси)фенокси)пропокси)піримідин (Р135); 
етиловий складний ефір 2,4-діаміно-6-етил-5-(3-(2-(3-карбоксипропокси)фенокси)пропокси)піримідину (Р217);

2,4-діаміно-6-етил-5-(3-(2-(2-карбоксіетил)фенокси)пропокси)піримідин (Р218);

етиловий складний ефір 2,4-діаміно-6-етил-5-(3-(2-(2-карбоксіетил)фенокси)пропокси)піримідину (Р195);

2,4-діаміно-6-етил-5-(3-(6-(3-карбоксипропокси)-2-метилхінолін-4-ілокси)пропокси)піримідин (Р169); та

етиловий складний ефір 2,4-діаміно-6-етил-5-(3-(6-(3-карбоксипропокси)-2-метилхінолін-4-ілокси)пропокси)піримідину (Р219);
або фармацевтично прийнятна сіль такої сполуки.
8. Сполука за п. 1, якою є сполука Р195 або її фармацевтично прийнятна сіль.
9. Сполука за п. 1, якою є сполука Р218 або її фармацевтично прийнятна сіль.
10. Сполука за п. 9, якою є гідрохлорид 2,4-діаміно-6-етил-5-(3-(2-(2-карбоксіетил)фенокси)пропокси)піримідину (сіль Р218).
11. Сполука за будь-яким з пп. 1-10 для застосування як лікарського засобу.
12. Фармацевтична композиція, яка містить щонайменше одну сполуку за будь-яким з пп. 1-10 у поєднанні із щонайменше одним фармацевтично прийнятним наповнювачем.
13. Спосіб лікування малярії, який включає введення сполуки за формулою І
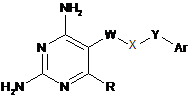 (I),
(I),
де R — водень або С1-4-алкіл;
W-X-Y — О(СН2)2-4О;
Аr — ароматичний цикл, вибраний з-посеред заміщеного фенілу та факультативно заміщеного нафтилу, або факультативно заміщений гетероароматичний цикл, вибраний з групи, до якої входять хінолініл, ізохінолініл, хіназолініл, хіноксалініл, піридил, індоліл, триазоліл, бензоксазоліл, бензімідазоліл, індолініл та бензотриазоліл;
причому, якщо Аr — ароматичний цикл, то термін “заміщений” означає групи, заміщені щонайменше одним замісником, вибраним з групи, до якої входять ацил, бензоксазоліл, нітрогрупа, карбоксил, карбоксі-С1-3-алкіл, карбоксі-С1-3-алкілоксигрупа, С1-3-алкілоксикарбоніл-С1-3-алкіл, С1-3-алкілоксикарбоніл-С1-3-алкілоксигрупа, тетразоліл, тетразоліл-С1-3-алкіл та тетразоліл-С1-3-алкілоксигрупа; та, якщо Аr — факультативно заміщений гетероароматичний цикл, то термін “заміщений” означає групи, заміщені одним або кількома замісниками, вибраними з групи, яку складають алкіл, заміщений алкіл, циклоалкіл, заміщений циклоалкіл, трифторметил, арил, заміщений арил, галоген, аміногрупа, заміщена аміногрупа, алкоксигрупа, арилоксигрупа, гідроксил та нітрогрупа;
або фармацевтично прийнятної солі такої сполуки.
14. Спосіб за п.13, який відрізняється тим, що сполука вибрана з-посеред сполук за будь-яким з пп.7-10.
15. Спосіб за п. 13 або 14, який відрізняється тим, що штам малярії є резистентним до щонайменше одного антифолатного лікарського засобу.
16. Спосіб за п. 15, який відрізняється тим, що резистентний до антифолатного лікарського засобу штам малярії є резистентним до щонайменше одного антифолатного лікарського засобу, вибраного з групи, до якої входять циклогуаніл, хлорциклогуаніл, піриметамін та інші інгібітори DHFR.
17. Спосіб за будь-яким з пп. 13-16, який відрізняється тим, що сполуку вводять перорально.
Текст
Реферат: Цей винахід стосується нових сполук, які є інгібіторами природних та мутантних дигідрофолатредуктаз (DHFR) Plasmodium falciparum, корисних для лікування малярії. Винахід стосується також способів одержання та застосування таких сполук. Протималярійні сполуки за UA 105759 C2 (12) UA 105759 C2 цим винаходом є малотоксичними для організму-хазяїна, інфікованого малярійним паразитом, та є ефективними при вживанні у складі фармацевтичних композицій. NH2 W N H2N N R X Y Ar UA 105759 C2 5 10 15 20 25 30 35 40 45 50 55 60 Перехресне посилання на споріднену заявку [0001] Ця заявка претендує на пріоритет за попередньою патентною заявкою США № 60/978,375, поданою 8 жовтня 2007 р. Галузь винаходу [0002] Цей винахід стосується протималярійних сполук або антифолатів для лікування малярії та способів одержання та застосування цих сполук. Передумови створення винаходу [0003] Малярія - це захворювання, яке переноситься комарами і є причиною понад 2,7 мільйонів смертельних випадків на рік, згідно з оцінками Всесвітньої Організації охорони здоров'я (ВООЗ, WHO). Малярія є потенціально фатальним захворюванням крові, причиною якого є паразит, що переноситься в організми людей та тварин комаром виду анофелес (Anopheles). Існує чотири види паразитів, які уражають людей, в тому числі Plasmodium falciparum (P. falciparum), Plasmodium vivax (P. vivax), Plasmodium malariae (P. malariae) та Plasmodium ovale (P. ovale), причому більшість смертельних випадків у людей спричиняє P. falciparum. P. falciparum є небезпечним не тільки тому, що він перетравлює гемоглобін червоних кров'яних тілець (еритроцитів), але й тому, що він змінює адгезивні властивості клітини, яку він інфікував, що спричиняє зчеплення клітин зі стінками кровоносних судин. Таке явище стає небезпечним, коли інфіковані клітини крові прилипають до кровоносних судин, утруднюючи кровотік. [0004] Життєвий цикл малярійного паразита в організмі людини або тварини починається, коли заражений комар вводить малярійні спорозоїти в організм нового хазяїна під час всмоктування крові. Спорозоїти рухаються до печінки, де вони проникають у гепатоцити (клітини печінки) і зазнають стадії реплікації, яка спричиняє вивільнення у кровотік тисяч мерозоїтів, що відбувається приблизно через два тижні. Потім вивільнені мерозоїти проникають в еритроцити, де відбувається внутрішньоеритроцитний цикл їх розвитку. На протязі перших 48 год. після зараження еритроцита паразит проходить кілька стадій розвитку. Першою стадією є циклічна стадія, під час якої паразит починає розкладати гемоглобін. Наступною стадією є трофозоїтна стадія, під час якої паразит споживає більшу частину гемоглобіну, збільшується в розмірі та готується до продукування більшої кількості паразитів. Нарешті, паразит зазнає нестатевого поділу і утворює багатоядерний шизонт. Наприкінці циклу еритроцит розривається, і вивільнені мерозоїти заражають нові еритроцити (дивись MicroWorlds™ electronic science magazine; Lawrence Berkeley National Laboratory, University of California). Коли паразит досягає зрілості всередині еритроцита, він змінює адгезивні властивості клітини в її оточенні, що стає особливо небезпечним, оскільки ці заражені кров'яні клітини прилипають до стінок капілярів головного мозку, заважаючи кровотоку та викликаючи стан, що зветься церебральною малярією. Крім того, безперервне руйнування заражених та незаражених еритроцитів (останнє явище є результатом механізму, опосередкованого імунною системою), у сполученні з послабленням продукування нових еритроцитів кістковим мозком (дисеритропоез) неминуче призводить до анемії. [0005] Резистентна до лікарських засобів малярія стала однією з найважливіших проблем у галузі боротьби з малярією. Є відомості про клінічну резистентність in vivo щодо всіх протималярійних лікарських засобів, за винятком артемізиніну та його похідних. Рекомендації ВООЗ щодо лікування резистентних до лікарських засобів інфекцій включають застосування артемізинінів у комбінації з іншими класами протималярійних засобів. Однак доступність цих засобів для бідних країн обмежена їхньою високою вартістю. У деяких регіонах світу артемізинінові ліки складають першочергову групу лікувальних засобів і масово застосовуються як засоби монотерапії при самолікуванні підозрюваної неускладненої малярії, що, у свою чергу, збільшує ризик розвитку резистентності мікроорганізмів до лікарського засобу. Проблему резистентності мікроорганізмів до лікарського засобу можна пояснити передусім підвищеним селективним впливом, зокрема, на P. falciparum внаслідок нерозбірливого застосування ліків при самолікуванні та незавершення такого лікування. Резистентність P. falciparum до хлорохіну, вперше зафіксована у таїланді в 1961 р., на цей час поширена у більшості ендемічних малярійних країн. Резистентність до антифолатів - піриметаміну та циклогуанілу - швидко виникла після розгортання їх застосування як протималярійних засобів. Віднайдення сульфасполук уможливило створення комбінацій лікарських засобів, ефективних проти резистентних до лікарських засобів паразитів, однак внаслідок застосування таких комбінацій також виникла резистентність. Зміни чутливості малярійних паразитів до лікарських засобів можуть викликатися кількома механізмами, наприклад, фізіологічною адаптацією як наслідком негенетичних змін, селекцією існуючих резистентних до лікарських засобів паразитів зі змішаної популяції під впливом лікарських засобів, спонтанними мутаціями, мутацією внутрішньоядерних 1 UA 105759 C2 5 10 15 20 25 30 35 40 45 50 55 60 генів або наявністю плазмідоподібних факторів. [0006] Важливим механізмом виявилася селекція мутантів під впливом самих лікарських засобів. В навколишньому середовищі, де присутні протималярійні засоби у субтерапевтичних концентраціях, паразити, резистентні до лікарських засобів внаслідок своєї природної варіативності або внаслідок мутацій, набувають значної біологічної переваги. Це означає, що навіть якщо резистентні до лікарських засобів штами спочатку становлять незначну меншість, безперервне пригнічення міжвидової конкуренції збоку нерезистентних до лікарських засобів штамів під впливом лікарських засобів забезпечує досягнення чисельної переваги організмів резистентних до лікарських засобів штамів, тобто розвиток та поширення резистентності до звичайних протималярійних засобів, наприклад, хлорохіну та сульфадоксин-піриметаміну (SP). У Південно-східній Азії, Південній Америці та в Африці переважають види малярії, спричинені резистентним до багатьох лікарських засобів паразитом P. Falciparum. Африка, що є континентом, найбільш обтяженим цим захворюванням, відрізняється також підвищеною смертністю від нього (дивись Roll Back Malaria, Facts on ACTs, WHO, January 2006). Більшість досліджень свідчить, що у виникненні резистентної до лікарських засобів малярії слід звинувачувати селекцію паразитів під впливом лікарських засобів. При генетично визначеній резистентності має місце передача гаметоцитів від популяцій резистентних до лікарських засобів паразитів, яка сприяє поширенню резистентних до лікарських засобів штамів. Паразити Plasmodium мають дуже складні геноми, і легкість їх перебудови залежно від мікрооточення в організмах різних хазяїв та необхідних змін метаболізму ілюструє складність дослідження точних способів впливу протималярійних засобів на метаболізм паразитів (дивись The Biology of Malaria Parasites: Report of a WHO Scientific Group. WHO Technical Report Series, 1987). Прикладами протималярійних засобів, які пов'язують із резистентністю паразитів до лікарських засобів, є антибіотик доксициклін, деякі антифолати, наприклад, прогуаніл, піриметамін та сульфаміди, хіноліни, такий як хлорохін, мефлохін та хінін, та нафтохінони, такі як атовахон. [0007] Деякі сполуки, такі як 1,2-дигідротриазини, 2,4-діамінопіримідини та 2,4діамінохіназоліни, широко досліджувалися як інгібітори дигідрофолатредуктази (DHFR), яка є ключовим ферментом у процесі підтримання загальної кількості редукованих фолатів. В організмі малярійних паразитів DHFR є складовою частиною біфункціонального ферменту дигідрофолатредуктази-тимідилатсинтази (DHFR-TS) та діє шляхом перетворення дигідрофолату в тетрагідрофолат, який потім перетворюється у 5,10-метилентетрагідрофолат. Цей кофактор використовується тимідилатсинтазою (TS) для продукування деокситимідилату компонента ДНК, який має істотне значення для синтезу ДНК та росту клітин. Результатом інгібування DHFR є інгібування синтезу ДНК та смерть паразита. Отже ці інгібітори, відомі також під назвою антифолатів, є потенціально корисними лікарськими засобами проти інфекційних агентів за умови, що вони здатні селективно інгібувати DHFR паразита-мішені без помітного впливу на клітини організму-хазяїна. [0008] До інгібіторів DHFR, загальновідомих під назвами антифолатів або антифолів, у яких було виявлено високу протималярійну ефективність, належать циклогуаніл (Cyc) - 1,2дигідротриазин, та піриметамін (Pyr) - 2,4-діамінопіримідин, а також їх похідні з різними замісниками у положеннях 1 та 2 дигідротриазину та у положеннях 5 та 6 діамінопіримідину. Деякі сполуки цих класів є також ефективними інгібіторами бактеріальної DHFR і мають антибактеріальну активність. Циклогуаніл, піриметамін та інші описані похідні 1,2дигідротриазину, 2,4-діамінопіримідину та 2,4-діамінохіназоліну ефективні проти природних типів малярійних паразитів, однак вони при пероральному вживанні не є ефективними in vivo проти резистентних до антифолатів паразитів, щодо яких показано наявність мутацій у DHFR та дигідроптероатсинтазі (DHPS). Ступінь резистентності, як правило, зростає з кількістю мутацій DHFR, стимулюючи потребу у нових лікарських засобах, ефективних як проти нерезистентних, так і резистентних штамів малярійних паразитів. Оскільки в організмі людини-хазяїна також присутня DHFR, такі лікарські засоби мають бути селективними щодо DHFR паразита у порівнянні з відповідним ферментом організму-хазяїна або інгібувати його значно слабше, оскільки в іншому разі вони можуть бути токсичними для організму-хазяїна. Інші властивості лікарських засобів також не повинні спричиняти токсичність для організму-хазяїна. Бажано також, щоб такі лікарські засоби не мали значної антибактеріальної дії, оскільки вони мають призначатися для частого вживання у малярійно-ендемічних регіонах для лікування повторних малярійних інфекцій, отже, бажано виключити розвиток резистентних штамів співіснуючих мікроорганізмів під час протималярійного лікування. [0009] Відомо, що певні похідні 1,2-дигідротриазину, такі як WR99210, та його проліки PS-15 є ефективними інгібіторами деяких резистентних до лікарських засобів штамів малярії in vitro, однак вони також виявляють токсичність у тваринних моделях (дивись Найт та ін. - Knight et al., 2 UA 105759 C2 5 10 15 20 Ann. Trop. Med. Parasitol. (1982) 76:1-7), та їх виготовлення включає утворення високотоксичного -1 побічного продукту TCDD, концентрація якого має жорстко підтримуватися на рівні млрд . Синтезовано кілька сполук, аналогічних PS-15, і деякі з них проходили клінічні випробування (Йєнсен та ін. - Jensen et al., J. Med. Chem. (2001) 44:3925-3931; патент США № 5,322,858 (1994); та Ширер та ін. - Shearer et al., J. Med. Chem. (2005) 48:2805-2813). Припускалося, що WR99210 зв'язується з DHFR, однак реальні подробиці такого з'єднання лишалися невідомими до публікації повідомлення про кристалічну структуру комплексу фермент-інгібітор, де було виявлено молекулярну взаємодію між WR99210 та DHFR Plasmodium falciparum (Юваніяма та ін. - Yuvaniyama et al., Nat. Struct. Biol. (2003) 10:357-365). Незважаючи на високу активність in vitro проти нерезистентних та резистентних до антифолатів штамів P. falciparum, лишається неясним, чи будуть коли-небудь на основі таких сполук створені ефективні засоби лікування малярії, у зв'язку з їхньою низькою біодоступністю при пероральному застосуванні. [0010] Внаслідок зростаючої смертності, пов'язаної з малярією, існує потреба в удосконалених та більш ефективних способах боротьби із цим захворюванням. Зокрема, існує потреба у удосконалених та більш ефективних способах лікування та профілактики резистентної до лікарських засобів малярії, тобто у засобах, які є ефективними інгібіторами багатомутантної дигідрофолатредуктази Plasmodium falciparum. Цей винахід спрямований на задоволення цієї потреби, а також інших потреб. Суть винаходу [0011] Цей винахід стосується протималярійних сполук або антифолатів для лікування та профілактики малярії та способів одержання та застосування таких сполук. Ці антифолати діють як нові інгібітори дигідрофолатредуктази (DHFR) Plasmodium falciparum при лікуванні малярії, в тому числі нерезистентної та резистентної до лікарських засобів малярії. [0012] Цей винахід пропонує сполуку Формули I, показаної нижче: 25 NH2 W N H2N 30 35 40 45 50 N X Y Ar (I), R де R - водень або C1-4-алкіл, W-O або CH2, X - (CH2)2-4, факультативно заміщений однією або кількома гідроксильними групами, та Y-CH2, O, S, N(Z), де Z-H або факультативно заміщений ацил, алкіл чи арил або їх похідне; і Ar - факультативно заміщений арил або гетероарил або їх похідне; або фармацевтично прийнятну сіль такої сполуки. [0013] За одним із варіантів здійснення цього винаходу Ar - факультативно заміщений ароматичний цикл, такий як заміщений феніл або нафтил, або факультативно заміщений гетероароматичний цикл, факультативно вибраний з групи, до якої входять хінолініл, ізохінолініл, хіназолініл, хіноксалініл, піридил, індоліл, триазоліл, бензоксазоліл, бензимідазоліл, індолініл та бензотриазоліл. Якщо Аr - ароматичний цикл, то він факультативно заміщений щонайменше одним замісником, вибраним з групи, до якої входять ацил, бензоксазоліл, нітрогрупа, карбоксил, карбокси-С1-3-алкіл, карбокси-С1-3-алкілоксигрупа, С1-3-алкілоксикарбонілС1-3-алкіл, С1-3-алкілоксикарбоніл-С1-3-алкілоксигрупа, тетразоліл, тетразоліл-С1-3-алкіл та тетразоліл-С1-3-алкілоксигрупа. Ar факультативно заміщений додатковими замісниками. За іншим варіантом здійснення цього винаходу Ar заміщений при одному або кількох заміщуваних положеннях щонайменше одним замісником, вибраним з групи, до якої входять алкіл, заміщений алкіл, циклоалкіл, заміщений циклоалкіл, трифторметил, арил, заміщений арил, галоген, аміногрупа, заміщена аміногрупа, алкоксигрупа, арилоксигрупа, гідроксил та нітрогрупа. [0014] За одним із варіантів здійснення цього винаходу R-C1-4-алкіл. За іншим варіантом здійснення цього винаходу R - етил. [0015] За одним із варіантів здійснення цього винаходу сукупністю W-X-Y є група O(CH2)2-4O. За іншим варіантом здійснення цього винаходу W-X-Y є група O(CH2)2-4S. За ще одним варіантом здійснення цього винаходу W-X-Y є O(CH2)2-4NZ. За подальшим варіантом здійснення цього винаходу W-X-Y є група O(CH2)2-4 або (CH2)3-5O. [0016] Крім того, цей винахід охоплює спосіб лікування пацієнта, який потребує лікування від малярії, причому згаданий спосіб включає введення в організм пацієнта ефективної кількості 3 UA 105759 C2 5 10 15 20 25 30 35 40 45 50 55 60 сполуки I або її похідних. За одним із варіантів здійснення цього винаходу, пацієнт потребує лікування від резистентного до лікарських засобів або нерезистентного штаму малярії. За іншим варіантом здійснення цього винаходу резистентним до лікарських засобів (наприклад, резистентним до антифолатів) штамом малярії є штам, резистентний до щонайменше одного лікарського засобу (наприклад, засобу проти DHFR). До таких антифолатних лікарських засобів належать (але без обмеження поданим нижче переліком) циклогуаніл, хлорциклогуаніл та піриметамін. За одним із варіантів здійснення цього винаходу, якому віддається перевага, резистентний до антифолатів штам малярії містить у протеїновій послідовності своєї DHFR щонайменше одну мутацію, в тому числі 16(AlaVal), 51(AsnIle), 59(CysArg), 108(SerAsn), 108(SerThr) та 164(IleLeu). За іншим варіантом здійснення цього винаходу, якому віддається перевага, резистентним до антифолатів штамом малярії є штам малярії, який містить у протеїновій послідовності своєї DHFR щонайменше дві мутації, в тому числі 16(AlaVal), 51(AsnIle), 59(CysArg), 108(SerAsn), 108(SerThr) та 164(IleLeu). За іншим варіантом здійснення цього винаходу, якому віддається перевага, резистентним до антифолатів штамом малярії є штам малярії, який містить у протеїновій послідовності своєї DHFR щонайменше дві мутації, в тому числі 16(AlaVal) та 108(SerThr). Лікування неускладненої малярії, в тому числі переміжне та/або запобіжне лікування, за варіантом, якому віддається перевага, виконується шляхом перорального введення лікарських засобів. Лікування ускладненої або тяжкої малярії за варіантом, якому віддається перевага, виконується шляхом парентерального введення. Однак мається на увазі можливість інших форм застосування лікарських засобів. Короткий опис фігур [0017] Найкраще розуміння цього винаходу досягається при читанні цього опису з фігурами, що додаються, які призначені для ілюстрування варіантів здійснення винаходу, яким віддається перевага. Однак слід мати на увазі, що винахід не обмежується конкретними варіантами здійснення, показаними на фігурах. Хімічні структури, показані на фігурах, додатково обговорюються у Прикладі 1 цього опису. [0018] На Фіг. 1 показано хімічну структуру сполуки P113. [0019] На Фіг. 2 показано хімічну структуру сполуки P149. [0020] На Фіг. 3 показано хімічну структуру сполуки P153. [0021] На Фіг. 4 показано хімічну структуру сполуки P154. [0022] На Фіг. 5 показано хімічну структуру сполуки P157. [0023] На Фіг. 6 показано хімічну структуру сполук P135 (R=H) та P217 (R=Et). [0024] На Фіг. 7 показано хімічну структуру сполук P195 (R=Et) та P218 (R=H). [0025] На Фіг. 8 показано хімічну структуру сполук P169 (R=H) та P219 (R=Et). [0026] На Фіг. 9 показано концентрацію сполуки P218 у плазмі самців мишей Swiss Outbred після внутрішньовенного введення сполуки P218 (вільної кислоти) та перорального введення сполуки P195 (складноефірних проліків). Детальний опис винаходу i) Загальний огляд [0027] Цей винахід пропонує нові інгібітори, ефективні проти малярії, зокрема, проти резистентної до антифолатів малярії, яка є наслідком мутацій у дигідрофолатредуктазі (DHFR) Plasmodium falciparum (P. falciparum). Відомі штами P. Falciparum, резистентні до антифолатів, мають мутації у положеннях 108 (заміна серину на аспарагін), 51 (заміна аспарагіну на ізолейцин), 59 (заміна цистеїну на аргінін) та/або 164 (заміна ізолейцину на лейцин). Інший резистентний до антифолатів штам P. falciparum має мутації у положеннях 16 (заміна аланіну на валін) та 108 (заміна серину на треонін). Можливо, що вони впливають не тільки на дигідрофолатредуктазу, але й на інші мішені в організмі малярійного паразита або на реакції організму-хазяїна, які спричиняють ефективне знищення паразитів. Протималярійні сполуки за цим винаходом є відносно низькотоксичними для хазяїна-ссавця та мають достатню ефективність при вживанні у складі фармацевтичних композицій. Значною перевагою цього винаходу є те, що нові сполуки мають незначну антибактеріальну дію або взагалі не мають такої дії і, отже, дуже малоймовірно, що вони можуть сприяти розвитку резистентних до лікарських засобів штамів бактерій. ii) Визначення [0028] Терміни "антифолати", "антифоли" та "інгібітори DHFR" в цьому описі є взаємозамінними і для цілей цього винаходу означають сполуки, які можуть бути застосовані для лікування або профілактики малярії. Ці сполуки є ефективними інгібіторами мутантної та природної дигідрофолатредуктази (DHFR) Plasmodium falciparum (P. falciparum). [0029] Терміни "Plasmodium falciparum" та "P. falciparum" в цьому описі є взаємозамінними та стосуються паразита, який передається хазяям - людям та тваринам, внаслідок чого хазяїн 4 UA 105759 C2 5 10 15 20 25 30 35 40 45 50 55 60 виявляє один або кілька симптомів малярії. Більш конкретно, P. falciparum є представником найпростіших, який викликає малярію. [0030] Термін "ацил" у значенні, вживаному в цьому описі, означає групу формули R'C(=O)-, де R" є, наприклад, H, C1-6-алкіл, арил, C1-6-алкоксигрупа, OH, NH2, NHR' або N(R')2, де R' - C1-6алкіл або арил. [0031] У значенні, вживаному в цьому описі, терміни "алкіл", "алкеніл" та "алкініл" охоплюють одновалентні вуглеводневі радикали нерозгалуженої, розгалуженої та циклічної структури та їх комбінації, які містять тільки атоми C та H, якщо вони є незаміщеними. Їх прикладами є метил, етил, ізобутил, циклогексил, циклопентилетил, 2-пропеніл, 3-бутиніл тощо. Загальна кількість вуглецевих атомів у кожній з таких груп подекуди вказується в цьому описі; наприклад, якщо група може містити до 10 атомів вуглецю, вона може бути представлена як 1-10C або як C1-C10, або C1-10. Якщо можливою є заміна атомів вуглецю гетероатомами (у типових випадках N, O та S), наприклад, у гетероалкільних групах, то числа, які характеризують групу, хоч і записуються, наприклад, як C1-C6, означають суму кількості вуглецевих атомів у групі та кількості таких гетероатомів, які замінюють вуглецеві атоми у циклі або ланцюжку, який описується. [0032] У типових випадках алкільні, алкенільні та алкінільні замісники містять 1-10C (алкіли) або 2-10C (алкеніли або алкініли). Відповідно до варіантів здійснення винаходу, яким віддається перевага, вони містять 1-8C (алкіли) або 2-8C (алкеніли або алкініли). У деяких випадках вони містять 1-4C (алкіли) або 2-4C (алкеніли або алкініли). Окрема група може містити кілька типів кратних зв'язків або кілька кратних зв'язків; такі групи охоплюються терміном "алкеніл", якщо вони містять щонайменше один подвійний вуглець-вуглецевий зв'язок, та охоплюються терміном "алкініл", якщо вони містять щонайменше один потрійний вуглець-вуглецевий зв'язок. [0033] Алкільні, алкенільні та алкінільні групи часто є заміщеними до такої міри, в якій таке заміщення має хімічний сенс. До типових замісників належать (але без обмеження поданим нижче переліком) галоген, =O, =N-CN, =N-OR, =NR, OR, NR2, SR, SO2R, SO2NR2, NRSO2R, NRCONR2, NRCOOR, NRCOR, CN, COOR, CONR2, OOCR, COR та NO2, де кожний R незалежно від інших є H, C1-C8-алкіл, C2-C8-гетероалкіл, C1-C8-ацил, C2-C8-гетероацил, C2-C8-алкеніл, C2C8-гетероалкеніл, C2-C8-алкініл, C2-C8-гетероалкініл, C6-C10-арил або C5-C10-гетероарил, і кожний R факультативно заміщений такими замісниками: галоген, =O, =N-CN, =N-OR', =NR', OR', NR'2, SR', SO2R', SO2NR'2, NR'SO2R', NR'CONR'2, NR'COOR', NR'COR', CN, COOR', CONR'2, OOCR', COR' та NO2, причому кожний R' незалежно від інших є H, C1-C8-алкіл, C2-C8гетероалкіл, C1-C8-ацил, C2-C8-гетероацил, C6-C10-арил або C5-C10-гетероарил. Алкільні, алкенільні та алкінільні групи можуть також бути заміщені такими замісниками: C 1-C8-ацил, C2C8-гетероацил, C6-C10-арил або C5-C10-гетероарил, кожний з яких може бути заміщений замісниками, які відповідають конкретній групі. [0034] В той час як термін "алкіл" у значенні, вживаному в цьому описі, охоплює циклоалкільні та циклоалкілалкільні групи, термін "циклоалкіл" може вживатися для позначення карбоциклічної неароматичної групи, яка приєднана до решти молекули через вуглецевий атом циклу, а термін "циклоалкілалкіл" може вживатися для позначення карбоциклічної неароматичної групи, яка приєднана до решти молекули через алкільну з'єднувальну ланку. Аналогічно, термін "гетероцикліл" може вживатися для позначення циклічної неароматичної групи, яка містить як член циклу щонайменше один гетероатом та приєднана до решти молекули через атом циклу, який може бути атомом C або N; а термін "гетероциклілалкіл" може вживатися для позначення такої групи, яка приєднана до решти молекули через з'єднувальну ланку. Розміри та замісники, придатні для циклоалкільних, циклоалкілалкільних, гетероциклільних та гетероциклілалкільних груп, є такими самими, як описано вище для алкільних груп. У значенні, вживаному в цьому описі, ці терміни охоплюють також цикли, які містять один або два подвійні зв'язки, за умови, що такий цикл не є ароматичним. [0035] Термін "ароматична група" або "арильна група" ("арил") означає моноциклічну або конденсовану біциклічну групу, яка має добре відомі ознаки ароматичності; прикладами таких груп є феніл та нафтил. Аналогічно, терміни "гетероароматичний" та "гетероарил" означають таку моноциклічну або конденсовану біциклічну систему, яка містить як члени циклу один або декілька гетероатомів, вибраних із групи, до якої входять O, S та N. Включення гетероатома надає ароматичності 5-членним циклам, а також 6-членним циклам. До типових гетероароматичних систем належать моноциклічні C 5-C6 ароматичні групи, такі як піридил, піримідил, піразиніл, тієніл, фураніл, піроліл, піразоліл, тіазоліл, оксазоліл та імідазоліл, та згадані конденсовані біциклічні групи, утворені в результаті конденсації однієї з вищезгаданих моноциклічних груп із фенільним циклом або з будь-якою гетероароматичною моноциклічною групою з утворенням біциклічної групи C8-C10, якою може бути, наприклад, індоліл, бензимідазоліл, індазоліл, бензотриазоліл, ізохіноліл, хіноліл, бензотіазоліл, бензофураніл, 5 UA 105759 C2 5 10 15 20 25 30 35 40 45 піразолопіридил, хіназолініл, хіноксалініл, цинолініл тощо. Це визначення охоплює будь-яку моноциклічну або конденсовану біциклічну систему, яка має ознаки ароматичності з точки зору розподілу електронів по циклічній системі. Воно охоплює також біциклічні групи, де щонайменше один цикл, безпосередньо приєднаний до решти молекули, має ознаки ароматичності. У типових випадках циклічні системи містять 5-12 атомів - членів циклів. Перевага віддається моноциклічним гетероарилам, які містять 5-6 членів циклу, та біциклічним гетероарилам, які містять 8-10 членів циклів. [0036] Арильні та гетероарильні групи можуть бути заміщені різноманітними замісниками, до яких належать, наприклад, C1-C8-алкіл, C2-C8-алкеніл, C2-C8-алкініл, C5-C12-арил, C1-C8-ацил та гетероформи цих груп, кожна з яких може мати додаткові замісники; до інших замісників арильних та гетероарильних груп належать галоген, OR, NR 2, SR, SO2R, SO2NR2, NRSO2R, NRCONR2, NRCOOR, NRCOR, CN, COOR, CONR2, OOCR, COR та NO2, де кожний R незалежно від інших є H, C1-C8-алкіл, C2-C8-гетероалкіл, C2-C8-алкеніл, C2-C8-гетероалкеніл, C2-C8-алкініл, C2-C8-гетероалкініл, C6-C10-арил, C5-C10-гетероарил, C7-C12-арилалкіл або C6-C12гетероарилалкіл, і кожний R факультативно заміщений, як описано вище для алкільних груп. Замісники при арильній або гетероарильній групі можуть, звичайно, бути додатково заміщені групами, описаними вище як придатні для кожного типу таких замісників або для кожного компонента замісника. Таким чином, наприклад, арилалкільний замісник може бути заміщений при арильному фрагменті замісниками, описаними в цьому документі як типові для арильних груп, і може бути додатково заміщений при алкільному фрагменті замісниками, описаними в цьому документі як типові або придатні для алкільних груп. [0037] Термін "факультативно заміщений" у значенні, вживаному в цьому описі, вказує, що конкретна описана група або групи можуть не мати інших замісників, окрім атомів водню, або ця група чи групи можуть мати один або кілька відмінних від атомів водню замісників. Якщо не зазначено інше, загальна кількість таких замісників, які можуть бути присутніми, дорівнює кількості атомів H, присутніх у незаміщеній формі описуваної групи. У випадку, коли факультативний замісник приєднаний через подвійний зв'язок, як, наприклад, карбонільний кисень (=O), то така група займає дві наявні валентності, отже, загальна кількість замісників, які можуть бути приєднані, зменшується відповідно до кількості наявних валентностей. [0038] Термін "штам" означає конкретний генетичний варіант конкретного організму. Стосовно до хіміотерапії мікроорганізми можуть бути охарактеризовані як резистентні або нерезистентні до лікарських засобів штами, залежно від їх чутливості до конкретного лікарського засобу або способу терапії. Резистентний до лікарських засобів штам часто має одну або кілька генетичних мутацій. Нерезистентним до лікарських засобів штамом є штам, який за нормальних умов повною мірою реагує на конкретний лікарський засіб або спосіб терапії. Такий штам може мати або не мати генетичні мутації. Резистентним штамом є штам, який меншою мірою ніж нерезистентний штам реагує на той самий лікарський засіб або спосіб терапії. [0039] Терміни "нерезистентний" та "природний" в цьому описі є взаємозамінними та стосуються штамів паразита, які за нормальних умов повною мірою реагують на конкретний лікарський засіб або спосіб терапії. iii) Протималярійні сполуки [0040] Згідно з одним з аспектів цей винахід пропонує серію нових протималярійних сполук, ефективних як проти природної, так і резистентної до лікарських засобів, в тому числі резистентної до антифолатів, малярії, спричиненої Plasmodium falciparum (P. falciparum). Ці сполуки належать до класу інгібіторів дигідрофолатредуктази. Нові сполуки мають загальну формулу I, показану нижче: NH2 W N H2N 50 N R X Y Ar (I) , [0041] R у сполуках формули (I) - H або C1-4-алкіл, у деяких варіантах здійснення цього винаходу він є C1-4-алкіл. У деяких варіантах здійснення цього винаходу R - етил або метил, іноді перевага віддається етилу. [0042] W іноді є O, а іноді - CH2. У деяких варіантах здійснення цього винаходу, яким віддається перевага, W є O. 6 UA 105759 C2 5 10 15 20 25 30 35 40 45 50 55 60 [0043] Y часто є CH2, O, S або NZ. [0044] X - алкіленовий ланцюг, який містить від 2 атомів до 4 атомів вуглецю, (CH2)2-4, який може бути заміщений гідроксильною групою. [0045] Ar іноді, відповідно до варіантів здійснення цього винаходу, яким віддається перевага, - гетероциклічна ароматична група, така як хінолініл, ізохінолініл, хіназолініл або хіноксалініл. Відповідно до деяких варіантів здійснення цього винаходу, яким віддається перевага, Ar хінолініл, а в конкретних варіантах здійснення - 4-хінолініл. [0046] Якщо Ar є ароматичним циклом, а не гетероароматичною групою, то він має бути заміщеним щонайменше однією групою, і відповідно до деяких варіантів він заміщений щонайменше одним замісником, вибраним з групи, до якої входять ацил, бензоксазоліл, нітрогрупа, карбоксил, карбокси-С1-3-алкіл, карбокси-С1-3-алкілоксигрупа, С1-3-алкілоксикарбонілС1-3-алкіл, С1-3-алкілоксикарбоніл-С1-3-алкілоксигрупа, тетразоліл, тетразоліл-С1-3-алкіл та тетразоліл-С1-3-алкілоксигрупа; і Ar факультативно заміщений додатковими замісниками; або мова йде про фармацевтично прийнятну сіль описаної сполуки. Відповідно до деяких варіантів здійснення цього винаходу Ar заміщений щонайменше одним замісником, вибраним з групи, до якої входять CO2R', (CH2)1-3COOR', O(CH2)1-3COOR', тетразоліл, (CH2)1-3-тетразоліл та O(CH2)1-3тетразоліл, де R' - H або C1-4-алкіл. За іншим варіантом здійснення цього винаходу Ar може бути додатково заміщений при одному або кількох заміщуваних положеннях факультативним замісником, вибраним із групи, до якої входять алкіл, заміщений алкіл, циклоалкіл, заміщений циклоалкіл, трифторметил, арил, заміщений арил, галоген, аміногрупа, заміщена аміногрупа, алкоксигрупа, арилоксигрупа, гідроксил, нітрогрупа тощо. До факультативних замісників Ar, яким віддається перевага, належать галоген, CF3, метоксигрупа та метил, і Ar у типових випадках має 0-2 такі факультативні замісники, а у варіантах здійснення цього винаходу, яким віддається перевага, - 0 або 1 такий факультативний замісник. [0047] Якщо Ar - гетероароматичний цикл, то він може бути заміщений при одному або кількох заміщуваних положеннях замісником, вибраним із групи, до якої входять алкіл, заміщений алкіл, циклоалкіл, заміщений циклоалкіл, трифторметил, арил, заміщений арил, галоген, аміногрупа, заміщена аміногрупа, алкоксигрупа, арилоксигрупа, гідроксил, нітрогрупа тощо. Серед замісників при Ar, якщо він є гетероароматичним циклом, перевага віддається галогену, CF3, метоксигрупі та метилу, а у деяких варіантах здійснення цього винаходу гетероароматична група, позначена Ar, є незаміщеною. [0048] До протималярійних сполук за цим винаходом належать також їхні таутомери та фармацевтично прийнятні солі. Винахід охоплює також фармацевтичні композиції, які містять щонайменше одну сполуку формули (I) у суміші із щонайменше одним фармацевтично прийнятним наповнювачем. У варіантах здійснення цього винаходу, яким віддається перевага, наповнювач не є водою. У випадках, коли у сполуці формули (I) присутній хіральний центр, цей винахід охоплює кожний індивідуальний енантіомер або діастереомер сполуки, а також суміші енантіомерів або діастереомерів, в тому числі рацемічні суміші. [0049] Цей винахід охоплює також проліки, які легко перетворюються in vivo у сполуки формули (I). До прикладів таких проліків належать заміщені похідні, в яких азот аміногрупи заміщений ацилом, у типових випадках C1-C6-ацилом, який може бути заміщеним, та сполуки, в яких карбоксильна група естерифікована з утворенням C1-C6-алкоксикарбонільної групи. Пролікам, заміщеним при N ацилом, який являє собою C 1-C4-ацил або ацил, що походить від амінокислоти, такої як гліцин, аланін, серин, глутамін, валін, лейцин, ізолейцин, глутамат, аспартат тощо, або дипептидів чи трипептидів, які містять ці амінокислоти, часто віддається перевага, оскільки вони легко деацилюються ендогенними амідазами та естеразами. [0050] Крім того, винахід охоплює синтетичні способи одержання вищезгаданих сполук. Синтетичні способи одержання 5-алкокси-6-заміщених 2,4-діамінопіримідинів у деяких варіантах здійснення цього винаходу включають O-алкілування 5-гідрокси-6-заміщеного 2,4діамінопіримідину галогеналкілом або алкілмезилатом у присутності основи. [0051] За іншим аспектом цей винахід пропонує способи застосування згаданих сполук для лікування малярії, в тому числі нерезистентних та резистентних до лікарських засобів штамів малярії. Відповідно до варіанта здійснення цього винаходу, якому віддається перевага, запропоновані сполуки є ефективними інгібіторами як природної, так і резистентної до лікарських засобів дигідрофолатредуктази Plasmodium falciparum (pf DHFR). Крім того, мається на увазі застосування описаних сполук або фармацевтичних композицій чи солей таких сполук при лікуванні резистентної до лікарських засобів малярії, викликаної Plasmodium falciparum, який містить природну або мутантну дигідрофолатредуктазу (pf DHFR), наприклад, мутантних штамів, описаних у цьому документі, які мають щонайменше одну мутацію у протеїновій послідовності DHFR, або інших штамів, які мають щонайменше одну з точкових мутацій, 7 UA 105759 C2 5 описаних у цьому документі, і більша перевага віддається мутантним штамам, які мають щонайменше дві мутації, описані у цьому документі. iv) Синтез протималярійних сполук [0052] Змінюваний бічний ланцюг сполук, де Ar - гетероароматична група, за варіантом, якому віддається перевага, створюється шляхом проведення реакції алкілування Ar або ArOH алкілувальним засобом, як показано нижче на Схемі 1. Схема 1 10 15 20 25 30 35 40 45 [0053] Прийнятні алкілувальні засоби, які забезпечують одержання алкілованих сполук, корисних при синтезі сполук формули (I), добре відомі. Наприклад, у реакціях, показаних вище, можна застосувати 1,3-дибромпропан або 1-бром-3-хлорпропан для одержання сполук, які мають формулу Ar-(CH2)3-Br або Ar-O-(CH2)3-Br. Ці проміжні продукти прийнятні для алкілування 5-гідроксильної групи 2,4-діамінопіримідину з одержанням сполук формули (I). До прийнятних відщеплюваних груп LG належать (однак без обмеження поданим нижче переліком), наприклад, хлорид, бромід, йодид, мезилат, бензолсульфонат, тозилат та трифлат. Різновиди реакцій цього типу є очевидними для фахівця у галузі. До прийнятних нуклеофілів належать (однак без обмеження поданим нижче переліком) феноли, інші арил- та гетероарилзаміщені спирти, арилта гетероарилзаміщені тіоли, тіофенол, арил- та гетероарилзаміщені аміни та гетероароматичні сполуки, які легко піддаються алкілуванню при атомах циклів, такі як індоли, триазоли, імідазоли та їх заміщені похідні та спряжені основи. [0054] Якщо селективне моноалкілування є більш складним процесом, то можна також застосовувати як вихідні сполуки замість біс-електрофілів ω-галогеновані спирти, такі як 2брометанол, 3-бромпропанол або 3-хлорпропанол. В такому разі OH-групу проміжного спирту слід заміняти відщеплюваною групою з підвищеною реакційною здатністю за умови, що вона є сумісною зі структурами інших частин молекули. Наприклад, бромування можна здійснювати із застосуванням PBr3, водного розчину HBr, Ph3PBr2, CBr4/Ph3P, NBS/Ph3P, тоді як для мезилування можна застосовувати MsCl/Et3N. За альтернативним варіантом реакція Міцунобу (DEAD/Ph3P або DIAD/Ph3P) між галогенованим спиртом та нуклеофільною сполукою (ArYH) забезпечує прямий синтез необхідного проміжного продукту, який містить приєднаний до Ar реакційноздатний бічний ланцюг. [0055] Після синтезу Ar, який містить реакційноздатний бічний ланцюг, подальше алкілування молекули Ar-(CH2)1-4-LG 5-гідрокси-6-заміщеними 2,4-діамінопіримідинами у присутності основи уможливлює одержання сполук за цим винаходом. 5-гідрокси-6-заміщені 2,4діамінопіримідини наявні на ринку. Основу можна вибрати з групи, до якої входять LiH, LiOH, KOH, NaH та K2CO3, при цьому найбільша перевага серед основ віддається LiOH. Основу можна додавати в кількості 1-10 екв. відносно гідроксипіримідину. Перевага віддається проведенню реакції в інертному розчиннику, серед розчинників перевага віддається N, Nдиметилформаміду. Реакцію можна проводити при температурі від приблизно 25C до 80C, але перевага віддається температурі 25-30C. Більш детальний опис реакції подано у нижчезгаданих патентах та публікаціях, включених до цього опису у повному обсязі шляхом посилання (а саме у патентах США № 4,179,562 та № 4,374,136; у патенті Великої Британії № 2086386). Інші способи одержання сполук вищезазначеної загальної структури добре відомі в галузі, і досвідченому практику неважко адаптувати їх до одержання згаданих сполук. [0056] Кінцеві продукти можна виділяти та очищати звичайними способами, такими як випарювання, екстрагування, кристалізація та/або колонкова хроматографія. Гідрохлориди та інші фармацевтично прийнятні солі сполук формули (I) легко одержати шляхом змішування сполуки з прийнятною кислотою, яка відповідає бажаній солі, як добре відомо в галузі. Кислоту 8 UA 105759 C2 5 10 15 часто додають до розчину або суспензії сполуки формули (I) у розчиннику, який містить воду, метанол та/або етанол, з подальшим випарюванням для видалення небажаного розчинника. Діамінопіридини часто перетворюють у двозаміщені солі, такі як дигідрохлориди. v) Фармацевтичні композиції та лікарські форми протималярійних сполук [0057] Протималярійні сполуки або антифолати можуть бути виготовлені у формі фармацевтичних препаратів для застосування у способах за цим винаходом. Така композиція або сполука може стимулювати біологічну реакцію, пов'язану зі зв'язуванням протималярійної сполуки з природною або мутантною (наприклад, одномутантною, багатомутантною) дигідрофолатредуктазою (DHFR) P. falciparum при резистентній до лікарських засобів та нерезистентній малярії та може застосовуватися згідно з винаходом як фармацевтичний препарат. Приклади загальних подробиць способів виготовлення та застосування детально описані у науковій літературі (дивись Remington's Pharmaceutical Sciences, Maack Publishing Co., Easton, Pa.). Антифолатні фармацевтичні препарати можна виготовляти за будь-яким способом, відомим у галузі виробництва фармацевтичних засобів. Антифолати, які застосовуються у способах за цим винаходом, можна виготовляти у вигляді лікарських форм, призначених для вживання будь-яким прийнятним звичайним шляхом, в тому числі для перорального та парентерального застосування. При лікуванні неускладненої малярії перевага віддається пероральному застосуванню, в той час як для лікування ускладненої (тяжкої) малярії перевага віддається парентеральному введенню. Ілюстративні приклади подано нижче. 20 Таблиця 1 Протималярійна активність та біодоступність триазинів при пероральному введенні у порівнянні з піримідином IC50 проти P. falciparum in vitro (мкM) Природний WR99210 Циклогуаніл Піриметамін 25 0,0006 0,037 0,079 ED90 P. chabaudi AS (мг/кг) Резистентний мутант 0,018 >100 >100 підшкірно перорально 1,1 3,7 0,25 74,2 6,2 0,88 Пероральна біодоступність у пацюків (%) 10 5,33 >10 1,25 0,42 Відношення IC50 Vero/TM4 Vero/V1/S 549 6000 >260 1380 nd >1620 nd 500 18 1405 134 nd=не визначалося 15 20 25 30 35 40 Приклад 15. Активність іn vivo у моделях малярії на гризунах [00120] Протималярійна активність досліджуваних сполук in vivo оцінювалася із застосуванням моделей Plasmodium chabaudi та Plasmodium berghei шляхом виконання стандартного 4-добового тесту Петерса (Peters) при використанні в кожному експерименті піриметаміну як лікарського засобу порівняння. За загальною методикою, самців мишей лінії CD1 з масою тіла 20 г (Charles Rivers, UK) витримували у спеціальних безпатогенних умовах при вільному доступі до корму. Для перорального введення досліджувані сполуки розчиняли у стандартному суспендувальному середовищі (SSV) [0,5 % натрієвої карбоксиметилцелюлози, 0,5 % бензилового спирту, 0,4 % Tween 80, 0,9 % NaCl (усі реактиви виробництва Sigma)], а для внутрішньоочеревинного або підшкірного введення - у суміші 0,5 % (маса/об'єм) гідроксипропілметилцелюлози, 0,4 % (об'ємн.) Tween 80, 0,5 % (об'ємн.) бензилового спирту у 6 деіонізованій воді. Мишей інфікували внутрішньовенним введенням 410 інфікованих еритроцитів і лікували перорально (p.o.) 0,2 мл розчину випробовуваних сполук через 2 год. (у день 0) та у 1, 2 та 3 дні після інфікування. Паразитемію визначали шляхом мікроскопічного дослідження плівок крові, забарвлених за Гімза (Giemsa), проби для яких брали на 4-й день. Мікроскопічні підрахунки показників для плівок крові від кожної миші обробляли із застосуванням програми GraphPad Prism 4 (GraphPad Software, Inc., Каліфорнія, США) та виражали у відсотках інгібування середньоарифметичних показників паразитемії для кожної групи у порівнянні з необробленою групою. При початковому скринінгу сполуки випробовувалися у дозах 30 мг/кг на добу проти штаму P. chabaudi AS (нерезистентного) протягом вищезазначеного періоду з обчисленням відсотків інгібування відносно необроблюваних контрольних груп. Сполуки, які давали інгібування 80 % або більше, потім випробовували на тій самій моделі у певному діапазоні доз на протязі вищезгаданого періоду для визначення кривих доза-реакція та обчислення значень ED50 та ED90. Сполуки, які давали значення ED90 на рівні сполуки порівняння або нижче (Таблиця 6), потім відбирали для тестування на P. chabaudi ASP (резистентному до піриметаміну штамі) та на летальному штамі P. berghei ANKA (нерезистентному). Результати випробувань in vivo на P. chabaudi AS показано в Таблиці 7. Із одержаних значень ED90 видно, що деякі сполуки виявляють у цьому випробуванні найвищу активність, і вони випробовувалися також на штамах P. chabaudi ASP та 22 UA 105759 C2 5 P. berghei ANKA. [00121] Як видно з Таблиці 6, низка цих сполук має значення ED 90 у 2-90 разів нижче (ED90=0,01-0,36 мг/кг), ніж відомий лікарський засіб піриметамін, який має значення ED90 відносно P. chabaudi AS 0,88 мг/кг. У Таблиці 7 показано ефективність деяких описаних сполук у трьох різних моделях малярії на гризунах, в тому числі викликаних P. chabaudi ASP та летальним P. berghei ANKA. У порівнянні з піриметаміном, який має у 15 разів нижчу ефективність (ED90=13,5 мг/кг) щодо резистентного до піриметаміну штаму P. chabaudi ASP, сполука P113 зберігає свою ефективність щодо цього штаму (ED 90=0,01 мг/кг) та щодо летального P. berghei ANKA (ED90=0,03 мг/кг). 10 Таблиця 6 Протималярійна активність сполук щодо P. chabaudi AS при пероральному застосуванні у стандартному 4-добовому тесті Петерса P. chabaudi AS (мг/кг) ED50 * ED90* 0,9 1,5 0,03 7,3 0,006 0,01 nd nd 0,025 0,076 2 5,2 0,3 3,4 0,7 1,3 0,8 2,8 nd nd 0,06 0,65 nd nd 0,54 3,08 0,03 0,12 3,8 28,8 1,96 11,8 2,21 14,1 0,01 0,02 0,006 0,013 0,006 0,043 nd nd 0,14 0,36 0,008 0,012 0,17 1,4 0,03 0,08 0,39 2,33 1,78 9,57 nd nd nd nd >29 >29 nd nd 0,16 0,9 0,22 1,74 >10 >10 0,21 0,69
ДивитисяДодаткова інформація
Назва патенту англійськоюAntimalarial compounds with flexible side-chains
Автори російськоюTarnchompoo, Bongkoch, Yuthavong, Yongyuth, Vilaivan, Tirayut, Chitnumsub, Penchit, Thongpanchang, Chawanee, Kamchonwongpaisan, Sumalee, Matthews, David, Vivas, Livia, Yuvaniyama, Jirundon, Charman, Susan, Charman, William, Katiyar, Sanjay Babu
МПК / Мітки
МПК: A61K 31/496, A61K 31/495
Мітки: фармацевтична, композиція, 2,4-діамінопіримідини, містить, малярії, спосіб, лікування
Код посилання
<a href="https://ua.patents.su/33-105759-24-diaminopirimidini-farmacevtichna-kompoziciya-shho-kh-mistit-ta-sposib-likuvannya-malyari.html" target="_blank" rel="follow" title="База патентів України">2,4-діамінопіримідини, фармацевтична композиція, що їх містить, та спосіб лікування малярії</a>
Попередній патент: 5-членні гетероциклічні аміди та споріднені сполуки
Наступний патент: Антитіло проти bst2
Випадковий патент: Лікарський препарат кардіологічної дії