2′,4′-дифтор-2′-метилзаміщені нуклеозидні похідні як інгібітори реплікації phk вірусу гепатиту c
Формула / Реферат
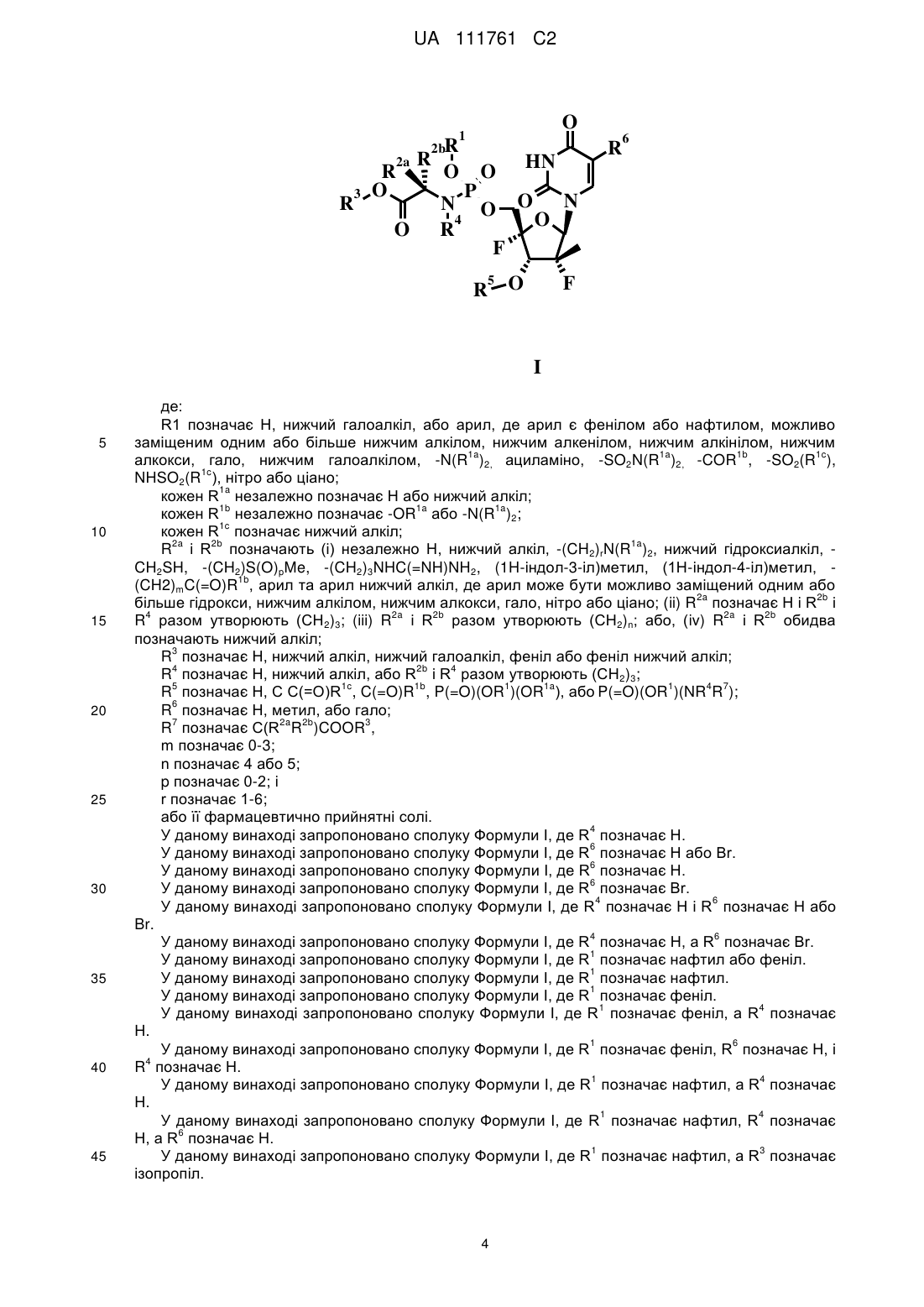
1. Сполука формули І
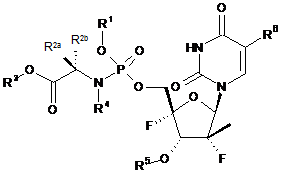 , I
, I
де:
R1 позначає Н, нижчий галоалкіл або арил, де арил є фенілом або нафтилом, можливо заміщеним одним або більше нижчим алкілом, нижчим алкенілом, нижчим алкінілом, нижчим алкокси, гало, нижчим галоалкілом, -N(R1a)2, ациламіно, -SO2N(R1a)2, -COR1b, -SO2(R1c), NHSO2(R1c), нітро або ціано;
кожен R1а незалежно позначає Н або нижчий алкіл;
кожен R1b незалежно позначає -OR1a або -N(R1a)2;
кожен R1c позначає нижчий алкіл;
R2а і R2b позначають (i) незалежно Н, нижчий алкіл, -(CH2)rN(R1a)2, нижчий гідроксіалкіл, -CH2SH, -(CH2)S(O)pMe, -(CH2)3NHC(=NH)NH2, (1H-індол-3-іл)метил, (1H-індол-4-іл)метил, -(CH2)mC(=O)R1b, арил та арилнижчий алкіл, де арил може бути можливо заміщений одним або більше гідрокси, нижчим алкілом, нижчим алкокси, гало, нітро або ціано; (ii) R2a позначає Н і R2b і R4 разом утворюють (СН2)3; (iii) R2a і R2b разом утворюють (СH2)n; або (iv) R2a і R2b обидва позначають нижчий алкіл;
R3 позначає Н, нижчий алкіл, нижчий галоалкіл, феніл або фенілнижчий алкіл;
R4 позначає Н, нижчий алкіл, або R2b і R4 разом утворюють (СН2)3;
R5 позначає Н, C(=O)R1c, C(=O)R1b, P(=O)(OR1)(OR1a) aбo P(=O)(OR1)(NR4R7);
R6 позначає Н, метил або гало;
R7 позначає C(R2aR2b)COOR3,
m позначає 0-3;
n позначає 4 або 5;
р позначає 0-2;і
r позначає 1-6;
або її фармацевтично прийнятні солі.
2. Сполука за п. 1, де R4 позначає Н.
3. Сполука за п. 2, де R6 позначає Н або Вr.
4. Сполука за п. 3, де R1 позначає нафтил або феніл.
5. Сполука за п. 4, де R2a позначає Н.
6. Сполука за п. 5, де R2b позначає метил.
7. Сполука за п. 6, де R3 позначає ізопропіл.
8. Сполука за п. 7, де R5 позначає Н.
9. Сполука за п. 7, де R5 позначає C(=O)R1c.
10. Сполука за п. 9, де R1с позначає етил.
11. Сполука за п. 7, де R5 позначає P(=O)(OR1)(NR4R7).
12. Сполука за п. 11, де R1 позначає нафтил.
13. Сполука за п. 12, де R4 позначає Н і R7 позначає СН(СН3)С(=О)ОСН(СН3)2.
14. Сполука, вибрана з групи, що складається з:
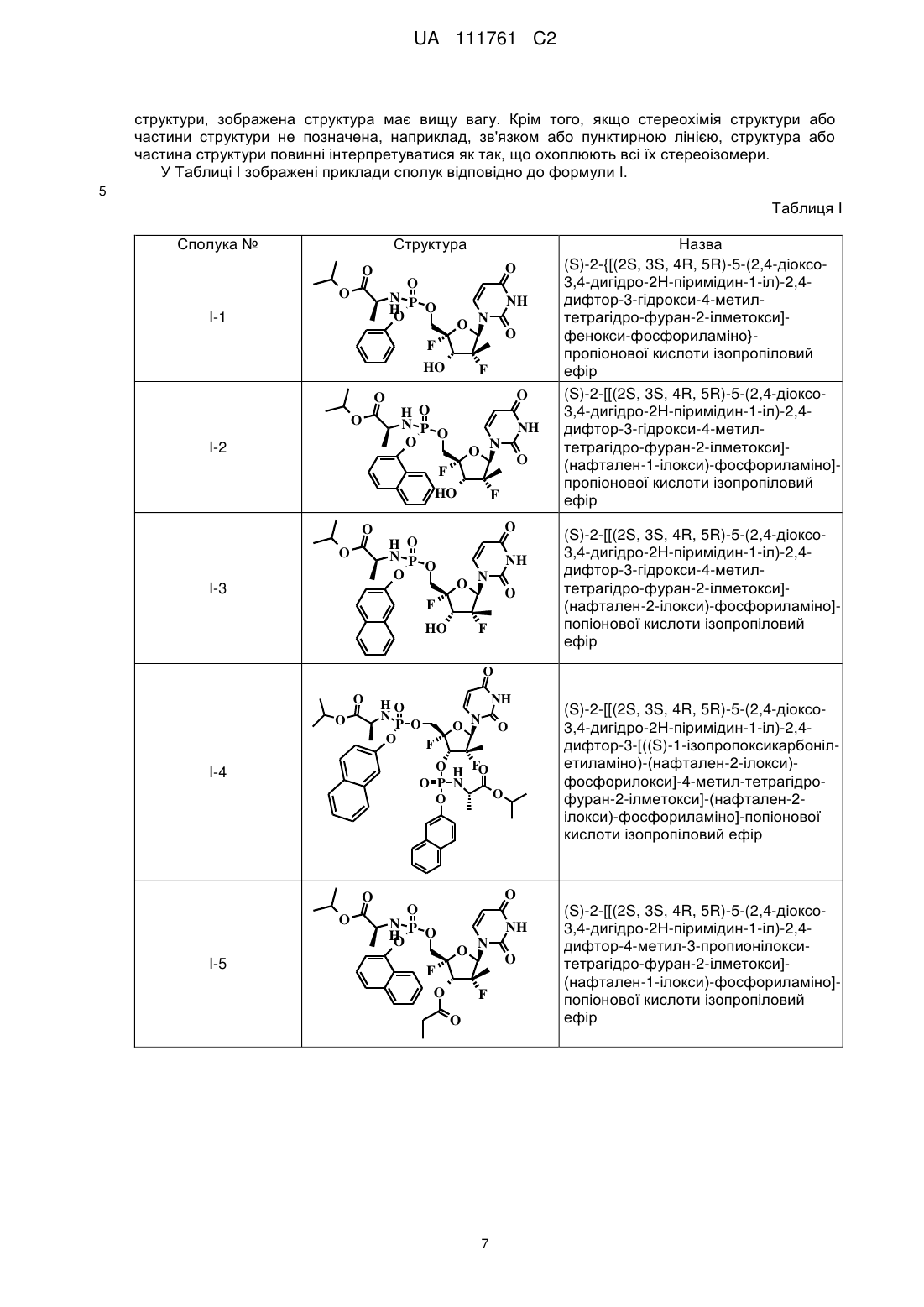
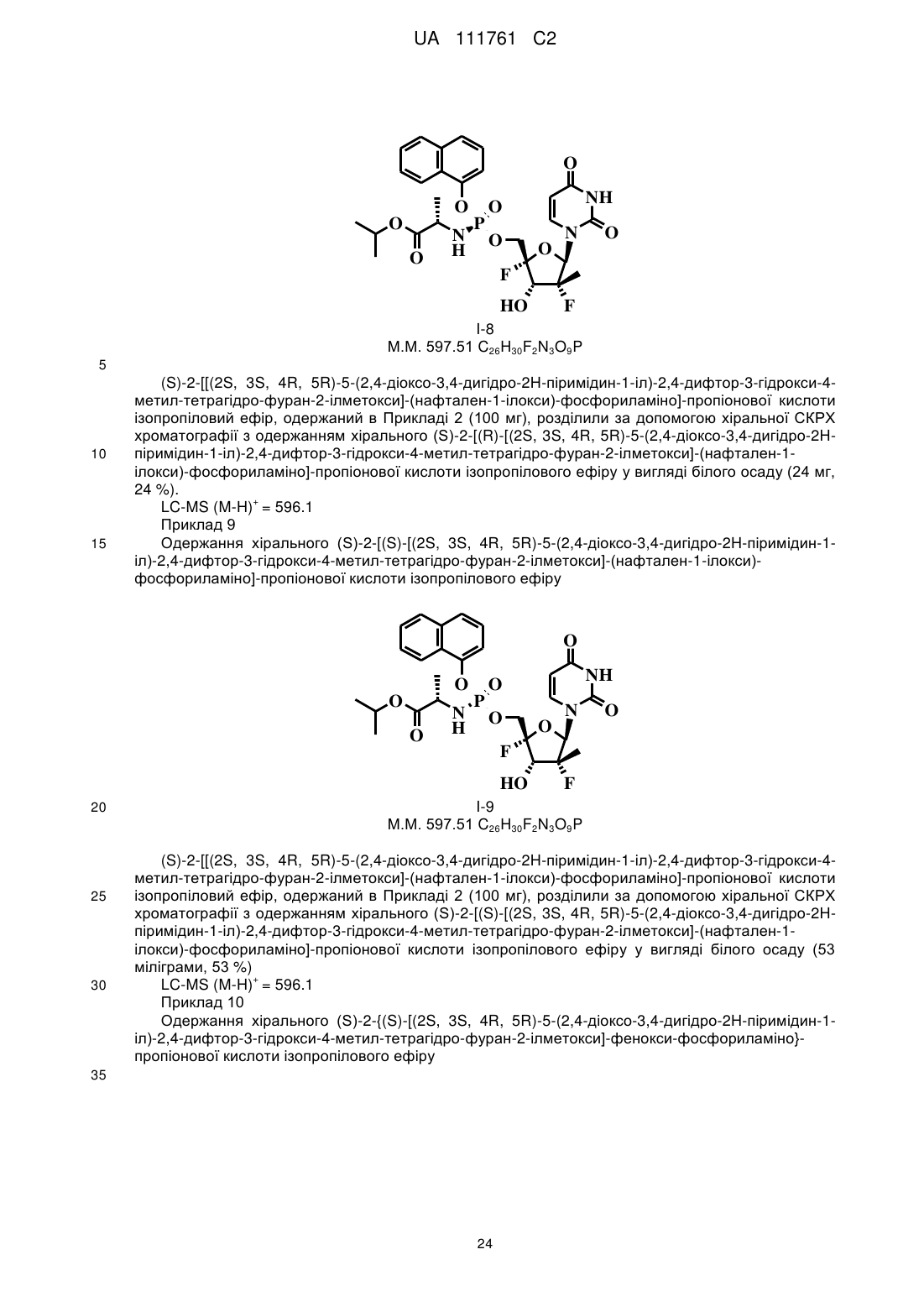
(S)-2-{[(2S,3S,4R,5R)-5-(2,4-діоксо-3,4-дигідро-2Н-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-феноксифосфориламіно}-пропіонової кислоти ізопропілового ефіру;
(S)-2-[[(2S,3S,4R,5R)-5-(2,4-дioкco-3,4-дигiдpo-2H-пipимiдин-1-iл)-2,4-дифтop-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
(S)-2-[[(2S,3S,4R,5R)-5-(2,4-діокco-3,4-дигiдpo-2H-пipимiдин-l-iл)-2,4-дифтop-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
(S)-2-[[(2S,3S,4R,5R)-5-(2,4-дioкco-3,4-дигiдpo-2H-пipимiдин-l-iл)-2,4-дифтop-3-[((S)-l-ізопропоксикарбонілетиламіно)-(нафтален-2-ілокси)-фосфорилокси]-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
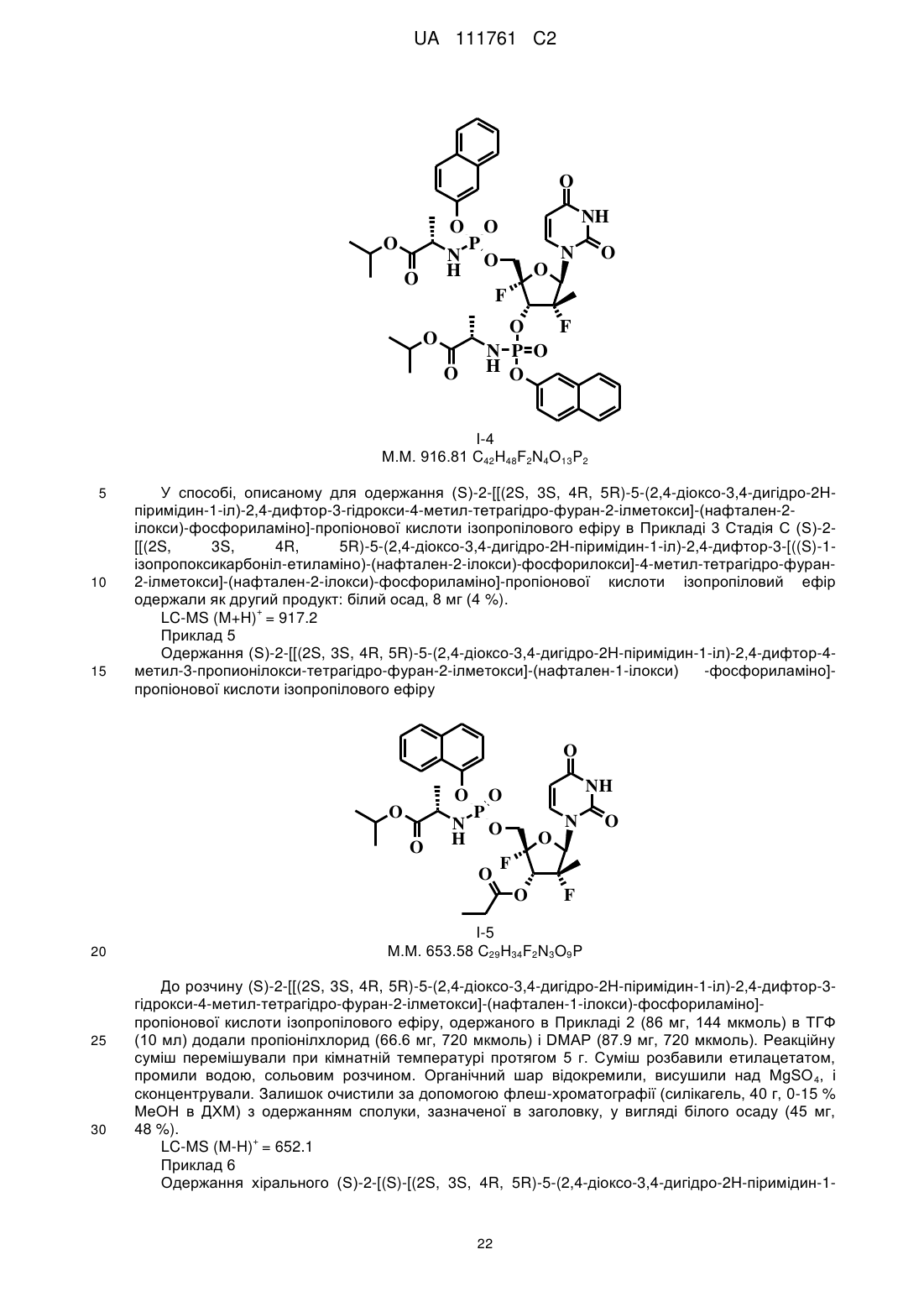
(S)-2-[[(2S,3S,4R,5R)-5-(2,4-дioкco-3,4-дигiдpo-2H-пipимiдин-l-iл)-2,4-дифтop-4-мeтил-3-пропіонілокситетрагідрофуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
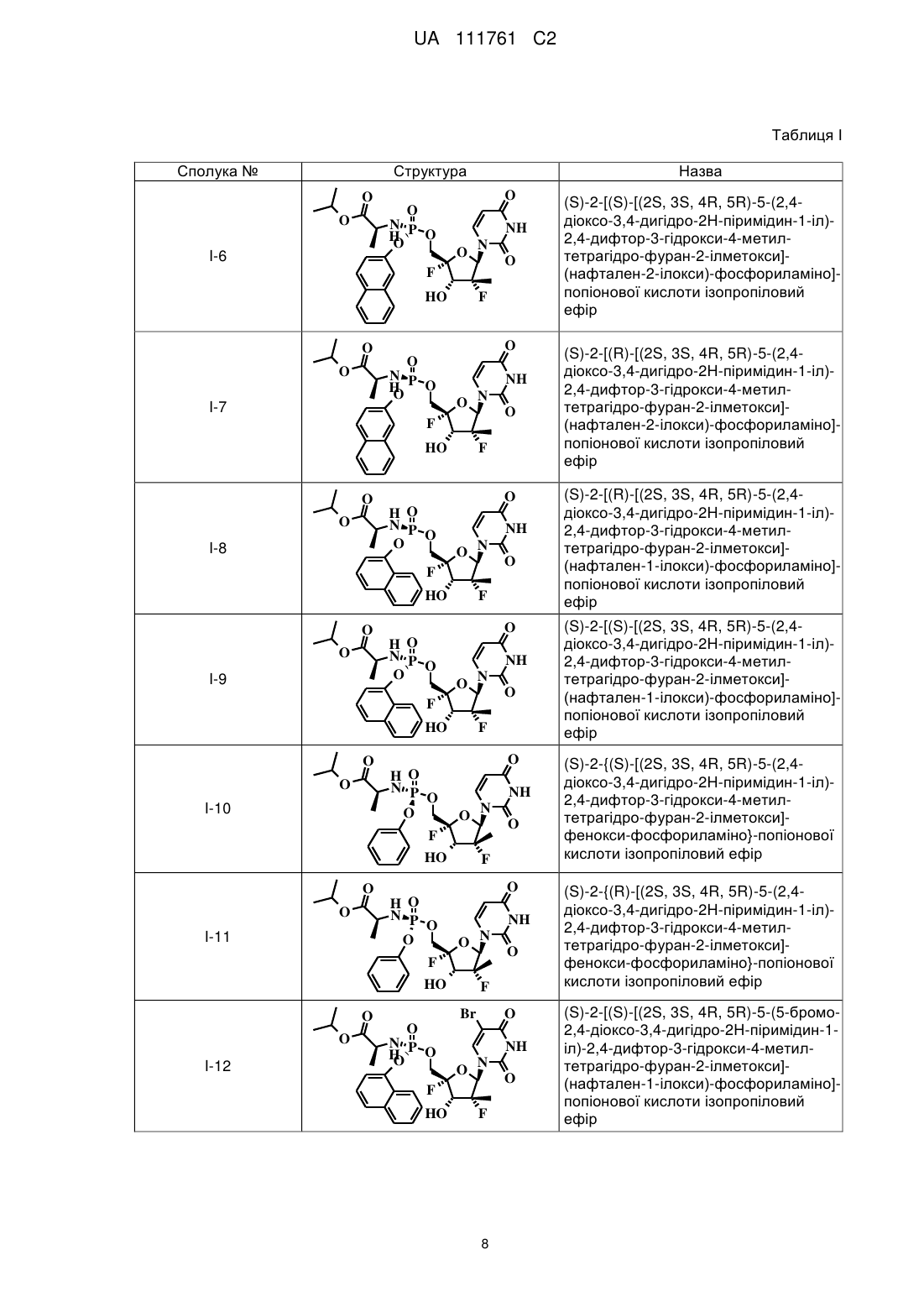
(S)-2-[(S)-[(2S,3S,4R,5R)-5-(2,4-дioкco-3,4-дигiдpo-2H-пipимiдин-l-iл)-2,4-дифтop-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
(S)-2-[(R)-[(2S,3S,4R,5R)-5-(2,4-дioкco-3,4-дигiдpo-2H-пipимiдин-l-iл)-2,4-дифтop-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
(S)-2-[(R)-[(2S,3S,4R,5R)-5-(2,4-діоксо-3,4-дигідро-2Н-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
(S)-2-[(S)-[(2S,3S,4R,5R)-5-(2,4-діоксо-3,4-дигідро-2Н-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
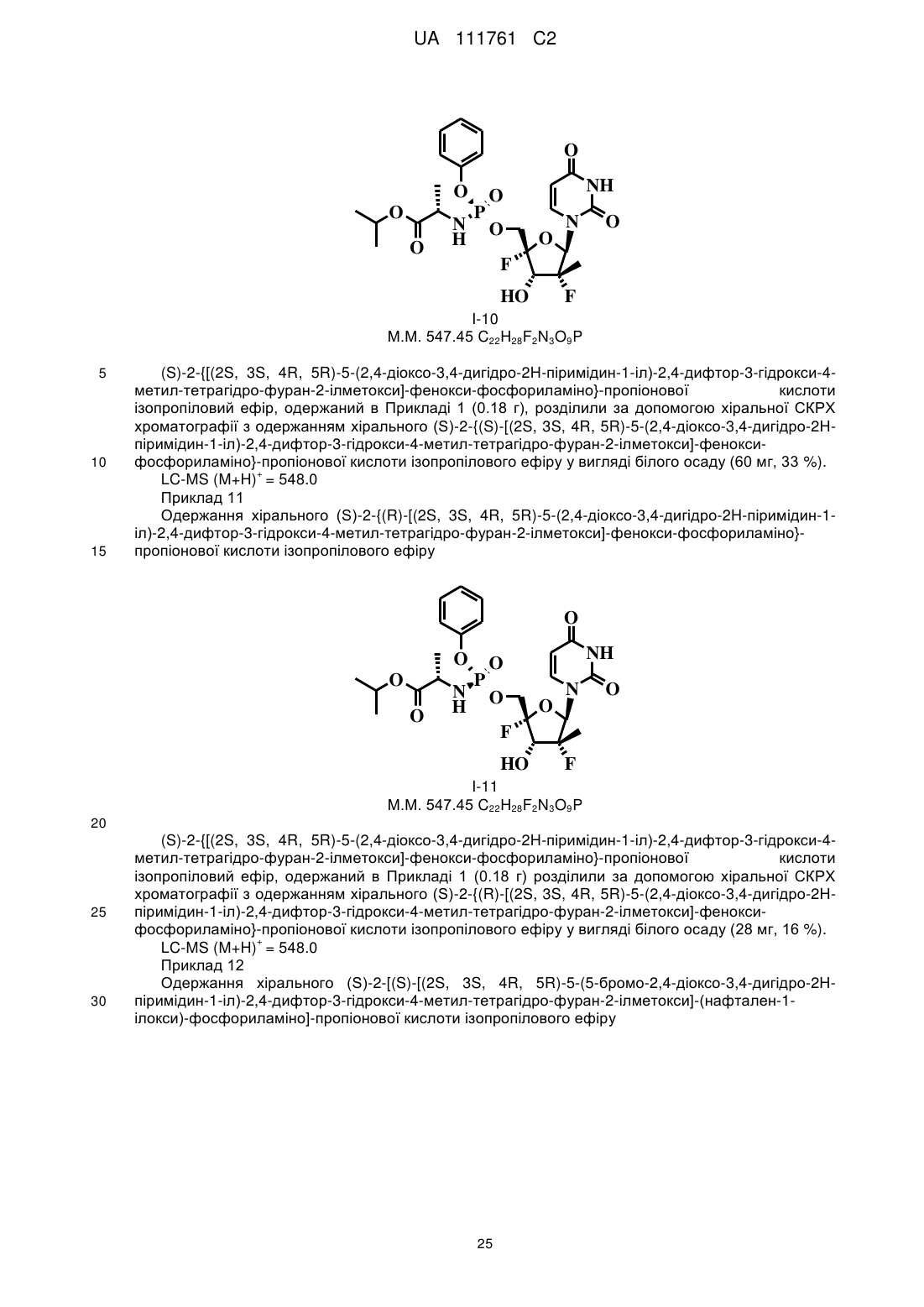
(S)-2-{(S)-[(2S,3S,4R,5R)-5-(2,4-діоксо-3,4-дигідро-2Н-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-феноксифосфориламіно}-пропіонової кислоти ізопропілового ефіру;
(S)-2-{(R)-[(2S,3S,4R,5R)-5-(2,4-діоксо-3,4-дигідро-2Н-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-феноксифосфориламіно}-пропіонової кислоти ізопропілового ефіру;
(S)-2-[(S)-[(2S,3S,4R,5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2Н-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
(S)-2-[(S)-[(2S,3S,4R,5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2Н-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
(S)-2-[(R)-[(2S,3S,4R,5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру;
(S)-2-[(R)-[(2S,3S,4R,5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру; і
(S)-2-[[(2S,3S,4R,5R)-5-(5-бpoмo-2,4-дioкco-3,4-дигiдpo-2H-пipимiдин-l-iл)-2,4-дифтop-3-гідрокси-4-метилтетрагідрофуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру.
15. Сполука за будь-яким з пп. 1-14 для застосування як терапевтично активної речовини.
16. Фармацевтична композиція, що містить сполуку за будь-яким з пп. 1-14 і терапевтично інертний носій.
17. Застосування сполуки за будь-яким з пп. 1-14 для лікування або профілактики інфекції вірусу гепатиту С (ВГС).
18. Застосування сполуки за будь-яким з пп. 1-14 при одержанні лікарського засобу для лікування або профілактики інфекції вірусу гепатиту С (ВГС).
19. Сполука за будь-яким з пп. 1-14 для лікування або профілактики інфекції вірусу гепатиту С (ВГС).
20. Спосіб лікування інфекції вірусу гепатиту С (ВГС), що включає введення пацієнтові, що потребує цього, терапевтично ефективної кількості сполуки за будь-яким з пп. 1-14.
Текст
Реферат: Даний винахід стосується сполук Формули І: R R2a R 3 O R2b O R R HN O 6 P N O O 1 O O 4 O N F R 5 O F I. Також розкриті фармацевтичні композиції, що містять сполуки Формули І, способи застосування сполук Формули І та/або композицій, що містять сполуки Формули І, для лікування ВГС. UA 111761 C2 (12) UA 111761 C2 UA 111761 C2 5 10 15 20 25 30 ОБЛАСТЬ, ДО ЯКОЇ ВІДНОСИТЬСЯ ВИНАХІД Даний винахід відноситься до нуклеозидних похідних як інгібіторів реплікації РНК реплікона ВГС. Зокрема, винахід відноситься до застосування пуринових і піримидинових нуклеозидних похідних як інгібіторів реплікації субгеному РНК вірусу гепатиту С (ВГС) і фармацевтичним композиціям, що містять такі сполуки. Вірус гепатиту С є основною причиною хронічних захворювань печінки у всьому світі. Пацієнти, інфіковані ВГС, піддаються ризику розвитку цирозу печінки і подальшої гепатоцелюлярної карциноми і, отже, ВГС є основним показанням для трансплантації печінки. Тільки два затверджені способи лікування в даний час доступні для лікування ВГС-інфекції (R. G. Gish, Sem. Liver. Dis., 1999, 19, 35). Це монотерапія інтерфероном-α і, зовсім недавня, комбінована терапія нуклеозидним аналогом рибавірином (Virazole) з інтерфероном-α. Багато з ліків, схвалених для лікування вірусних інфекцій є нуклеозидами або аналогами, і більшість з цих препаратів нуклеозидних аналогів інгібують реплікацію вірусу, унаслідок перетворення у відповідні трифосфати, через інгібування ферментів вірусної полімерази. Це перетворення в трифосфат зазвичай опосередковане клітинними кіназами і, отже, пряму оцінку нуклеозидів як інгібіторів реплікації ВГС зручно проводити тільки з використанням клітинного аналізу. Для ВГС немає дійсного клітинного аналізу реплікації вірусу або тваринної моделі інфекції. Вірус гепатиту С відноситься до сімейства Flaviridae. Він є РНК вірусом, РНК-геном, що кодує великий поліпротеїн, який після процесингу проводить необхідний комплекс реплікації для синтезу спадкової РНК. Вважається, що більшість з неструктурних білків, що кодуються РНК геномом ВГС, беруть участь в реплікації РНК. Lohmann і соавт. [V. Lohmann et al., Science, 1999, 285, 110-113] описали конструкцію клітинної лінії гепатоми людини (Huh7), в яку, як було показано, вводили молекули субгеномів РНК ВГС і вони реплікувалися з високою ефективністю. Вважається, що механізм реплікації РНК в цих клітинних лініях ідентичний реплікації повногеномом РНК ВГС в інфікованих гепатоцитах. Клони субгеномів кДНК ВГС, використовувані для виділення цих клітинних ліній, лягли в основу розробки клітинного аналізу для ідентифікації нуклеозидних аналогів - інгібіторів ВГС реплікації. СТИСЛИЙ ВИКЛАД ВИНАХОДУ Сполуки Формули I корисні для лікування захворювань, опосередкованих вірусом гепатиту C (ВГС) і для фармацевтичних композицій, що містять такі сполуки. У даному винаході запропоновано сполуку Формули І O 1 6 2bR 2a 3 R R O O R O O R HN P N O O N 4 O R F 5 R O F I 35 40 45 де: R1 позначає H, нижчий галоалкіл, або арил, де арил є фенілом або нафтилом, можливо заміщеним одним або більше нижчим алкілом, нижчим алкенілом, нижчим алкінілом, нижчим 1a 1a 1b 1c алкокси, гало, нижчим галоалкілом, -N(R )2, ациламіно, -SO2N(R )2, -COR , -SO2(R ), 1c NHSO2(R ), нітро або ціано; 1a кожен R незалежно позначає H або нижчий алкіл; 1b 1a 1a кожен R незалежно позначає -OR або -N(R )2; 1c кожен R позначає нижчий алкіл; 2a 2b 1a R і R позначають (i) незалежно Н, нижчий алкіл, -(CH2)rN(R )2, нижчий гідроксиалкіл, -CH2SH, -(CH2)S(O)pMe, -(CH2)3NHC(=NH)NH2, (1H-індол-3-іл)метил, (1H-індол-4-іл)метил, 1b -(CH2)mC(=O)R , арил та арил нижчий алкіл, де арил може бути можливо заміщений одним 1 UA 111761 C2 2a 5 10 15 20 25 30 35 40 45 50 55 60 або більше гідрокси, нижчим алкілом, нижчим алкокси, гало, нітро або ціано; (ii) R позначає H і 2b 4 2a 2b 2a 2b R і R разом утворюють (CH2)3; (iii) R і R разом утворюють (CH2)n; або, (iv) R і R обидва позначають нижчий алкіл; 3 R позначає H, нижчий алкіл, нижчий галоалкіл, феніл або феніл нижчий алкіл; 4 2b 4 R позначає H, нижчий алкіл, або R і R разом утворюють (CH2)3; 5 1c 1b 1 1a 1 4 7 R позначає H, C(=O)R , C(=O)R , P(=O)(OR )(OR ), або P(=O)(OR )(NR R ); 6 R позначає H, метил, або гало; 7 2a 2b 3 R позначає C(R R )COOR , m позначає 0-3; n позначає 4 або 5; p позначає 0-2; і r позначає 1-6; або її фармацевтично прийнятні солі. У даному винаході запропоновано спосіб лікування інфекції вірусу гепатиту С (ВГС), що включає введення пацієнтові, що потребує цього, терапевтично ефективної кількості сполуки Формули I. У даному винаході запропонована композиція, що містить сполуку Формули I і фармацевтично прийнятний ексципієнт. ДОКЛАДНИЙ ОПИС ВИНАХОДУ Було показано, що сполуки Формули I є інгібіторами субгеномної реплікації вірусу гепатиту С в клітинній лінії гепатоми. Ці сполуки мають потенціал ефективності як противірусні препарати для лікування ВГС-інфекції у людини. Термін "алкіл", використовуваний тут, позначає лінійний або з розгалуженим ланцюжком вуглеводневий залишок, що містить від 1 до 12 атомів вуглецю. Переважно, термін "алкіл" означає лінійний або з розгалуженим ланцюжком вуглеводневий залишок, що містить від 1 до 7 атомів вуглецю. Найбільш переважними є метил, етил, пропіл, ізопропіл, н-бутил, ізобутил, трет-бутил або пентил. Алкіл може бути незаміщеним або заміщеним. Замісники вибрані з одного або більше циклоалкілу, нітро, аміно, алкіл аміно, діалкіламіно, алкіл карбонілу і циклоалкіл карбонілу. Термін "циклоалкіл", використовуваний тут, позначає можливо заміщений циклоалкіл, що містить від 3 до 7 атомів вуглецю, наприклад, циклопропіл, циклобутил, циклопентил, циклогексил або циклогептил. Термін "алкокси", використовуваний тут, позначає можливо заміщену лінійну або з розгалуженим ланцюжком алкіл-окси групу, де "алкільна" частина визначена вище, таку як метокси, етокси, н-пропілокси, ізопропілокси, н-бутилокси, ізобутилокси, трет-бутилокси, пентилокси, гексилокси, гептилокси, включаючи їх ізомери. Термін "алкоксиалкіл", використовуваний тут, позначає алкоксигрупу, як визначено вище, яка приєднана до алкільної групи, визначеної вище. Прикладами є метоксиметил, метоксиетил, метоксипропіл, етоксиметил, етоксиетил, етоксипропіл, пропілоксипропіл, метоксибутил, етоксибутил, пропілоксибутил, бутилоксибутил, трет-бутилоксибутил, метоксипентил, етоксипентил, пропілоксипентил, включаючи їх ізомери. Термін "алкеніл", використовуваний тут, позначає незаміщений або заміщений вуглеводневий радикал, що має від 2 до 7 атомів вуглецю, переважно від 2 до 4 атомів вуглецю, і такий, що має одну або два олефінові подвійні зв'язки, переважно один олефіновий подвійний зв'язок. Прикладами є вініл, 1-пропеніл, 2-пропеніл (аліл) або 2-бутеніл (кротил). Термін "алкиніл", використовуваний тут, позначає незаміщений або заміщений вуглеводневий радикал, що має від 2 до 7 атомів вуглецю, переважно від 2 до 4 атомів вуглецю, і такий, що має одну або, де можливо, два потрійні зв'язки, переважно один потрійний зв'язок. Прикладами є етиніл, 1-пропініл, 2-пропініл, 1-бутиніл, 2-бутиніл або 3-бутиніл. Термін "гідроксиалкіл", використовуваний тут, позначає лінійну або з розгалуженим ланцюжком алкільну групу, як визначено вище, де 1, 2, 3 або більше атомів водню заміщені гідроксигрупою. Прикладами є гідроксиметил, 1-гідроксиетил, 2-гідроксиетил, 1-гідроксипропіл, 2-гідроксипропіл, 3-гідроксипропіл, гідроксиізопропіл, гідроксибутил і тому подібне. Термін "галогеналкіл", використовуваний тут, означає лінійну або з розгалуженим ланцюжком алкільну групу, як визначено вище, де 1, 2, 3 або більше атомів водню заміщені галогеном. Прикладами є 1-фторметил, 1-хлорметил, 1-бромметил, 1-йодметил, трифторметил, трихлорметил, трибромметил, трийодометил, 1-фторетил, 1-хлоретил, 1-брометил, 1-йодетил, 2-фторетил, 2-хлоретил, 2-брометил, 2-йодетил, 2,2-дихлоретил, 3-бромпропіл або 2,2,2трифторетил і тому подібне. Термін "алкілтіо", використовуваний тут, позначає лінійну або з розгалуженим ланцюжком 2 UA 111761 C2 5 10 15 20 25 30 35 40 45 50 55 (алкіл)S- групу, в якій "алкільна" частина така, як визначено вище. Прикладами є метилтіо, етилтіо, н-пропілтіо, ізопропілтіо, н-бутилтіо, ізобутилтіо або трет-бутилтіо. Термін "арил", використовуваний тут, позначає можливо заміщений феніл і нафтил (наприклад, 1-нафтил, 2-нафтил або 3-нафтил). Відповідні замісники для арилу можуть бути вибрані з тих, які зазначені для алкілу; крім того, проте, галоген, гідрокси і можливо заміщений алкіл, галогеналкіл, алкеніл, алкиніл і арилокси є замісниками, які можуть бути включені в список замісників. Термін "гетероцикліл", використовуваний тут, позначає можливо заміщені насичені, частково ненасичені або ароматичні моноциклічні, біциклічні або трициклічні гетероциклічні системи, які містять один або більше гетероатомів, вибраних з азоту, кисню і сірки, які також можуть конденсувати з можливо заміщеним насиченим, частково ненасиченим або ароматичним моноциклічним карбоциклом або гетероциклом. Прикладами відповідних гетероциклів є оксазоліл, ізоксазоліл, фурил, тетрагідрофурил, 1,3діоксоланіл, дигідропіраніл, 2-тієніл, 3-тієніл, піразиніл, ізотіазоліл, дигідрооксазоліл, піримидиніл, тетразоліл, 1-піролідиніл, 2-піролідиніл, 3-піролідиніл, піролідиноніл, (N-оксид) піридиніл, 1-піроліл, 2-піроліл, триазоліл, наприклад 1,2,3-триазоліл або 1,2,4-триазоліл, 1піразоліл, 2-піразоліл, 4-піразоліл, піперидиніл,морфолініл (наприклад, 4-морфолініл), тіоморфолініл (наприклад, 4-тіоморфолініл), тіазоліл, піридиніл, дигідротіазоліл, імідазолідиніл, піразолініл, піперазиніл, 1-імідазоліл, 2-імідазоліл, 4-імідазоліл, тіадіазоліл, наприклад, 1,2,3тіадіазоліл, 4-метилпіперазиніл, 4-гідроксипіперидин-1-іл. Відповідні замісники для гетероциклілу можуть бути вибрані із замісників, зазначених для алкілу; на додаток, проте, можливо заміщений алкіл, алкеніл, алкиніл, оксогрупа (= O) або аміносульфоніл позначають замісники, які можуть бути включені в список замісників. Термін "ацил" ("алкілкарбоніл"), використовуваний тут, позначає групу формули C(=O)R, де R позначає водень, незаміщений або заміщений лінійний або розгалужений залишок вуглеводневого ланцюга, що містить від 1 до 7 атомів вуглецю, або фенільної групи. Найбільш переважними ацильними групами є такі, в яких R позначає водень, незаміщений лінійним або розгалуженим вуглеводневим залишком, що містить від 1 до 4 атомів вуглецю, або фенільну групу. Термін галоген означає фтор, хлор, бром або йод, переважно фтор, хлор, бром. В зображеннях зазначених сполук в даній заявці, потовщена конічна лінія ( ) позначає замісник, який знаходиться вище площини кільця, якому належить асиметричний атом вуглецю і пунктирна лінія ( ) позначає замісник, який знаходиться нижче площини кільця, якому належить асиметричний атом вуглецю. Сполуки формули I мають стереоізомерію. Ці сполуки можуть бути будь-якими ізомерами сполуки формули I або сумішами цих ізомерів. Сполуки і проміжні сполуки за даним винаходом, які мають один або більше асиметричних атомів вуглецю, можуть бути одержані у вигляді рацемічних сумішей стереоізомерів, які можуть бути розділені. Сполуки формули I демонструють таутомерію, що означає, що сполуки за даним винаходом можуть існувати у вигляді двох або більше хімічних сполук, які здатні легко взаємоперетворюватися. У багатьох випадках це означає просто обмін атома водню між двома іншими атомами, з будь-яким з яких він утворює ковалентний зв'язок. Таутомерні сполуки існують в динамічній рівновазі одна з одною, так що спроби одержати окремі речовини зазвичай приводять до утворення суміші, яка проявляє всі хімічні і фізичні властивості, очікувані на основі структур її компонентів. Найбільш поширеним типом таутомерії є такий, в який залучені карбонільні або кетосполуки і ненасичені гідроксильні сполуки, або еноли. Структурними змінами є зсув атома водню між атомами вуглецю і кисню, з перебудовою зв'язків. Наприклад, у багатьох аліфатичних альдегідів і кетону, таких як ацетальдегід, кетоформа є переважаючою; у фенолів енольна форма є основним компонентом. Сполуки формули I, які є основними, можуть утворювати фармацевтично прийнятні солі з неорганічними кислотами, такими як галогенводневі кислоти (наприклад, хлористоводнева кислота і бромистоводнева кислота), сірчана кислота, азотна кислота і фосфорна кислота і т. п., а також з органічними кислотами (наприклад, оцтовою кислотою, винною кислотою, янтарною кислотою, фумаровою кислотою, малеїновою кислотою, яблучною кислотою, саліциловою кислотою, лимонною кислотою, метансульфоновою кислотою і п-толуолсульфокислотою і т. п.). Утворення і виділення таких солей може бути здійснене способами, відомими в даній області. Інгібітори ВГС У даному винаході запропоновано сполуку Формули I 60 3 UA 111761 C2 O 1 6 2bR 2a 3 R R O O R O O R HN P N O O N 4 O R F 5 R O F I 5 10 15 20 25 30 35 40 45 де: R1 позначає H, нижчий галоалкіл, або арил, де арил є фенілом або нафтилом, можливо заміщеним одним або більше нижчим алкілом, нижчим алкенілом, нижчим алкінілом, нижчим 1a 1a 1b 1c алкокси, гало, нижчим галоалкілом, -N(R )2, ациламіно, -SO2N(R )2, -COR , -SO2(R ), 1c NHSO2(R ), нітро або ціано; 1a кожен R незалежно позначає H або нижчий алкіл; 1b 1a 1a кожен R незалежно позначає -OR або -N(R )2; 1c кожен R позначає нижчий алкіл; 2a 2b 1a R і R позначають (i) незалежно Н, нижчий алкіл, -(CH2)rN(R )2, нижчий гідроксиалкіл, CH2SH, -(CH2)S(O)pMe, -(CH2)3NHC(=NH)NH2, (1H-індол-3-іл)метил, (1H-індол-4-іл)метил, 1b (CH2)mC(=O)R , арил та арил нижчий алкіл, де арил може бути можливо заміщений одним або 2a 2b більше гідрокси, нижчим алкілом, нижчим алкокси, гало, нітро або ціано; (ii) R позначає H і R і 4 2a 2b 2a 2b R разом утворюють (CH2)3; (iii) R і R разом утворюють (CH2)n; або, (iv) R і R обидва позначають нижчий алкіл; 3 R позначає H, нижчий алкіл, нижчий галоалкіл, феніл або феніл нижчий алкіл; 4 2b 4 R позначає H, нижчий алкіл, або R і R разом утворюють (CH2)3; 5 1c 1b 1 1a 1 4 7 R позначає H, C C(=O)R , C(=O)R , P(=O)(OR )(OR ), або P(=O)(OR )(NR R ); 6 R позначає H, метил, або гало; 7 2a 2b 3 R позначає C(R R )COOR , m позначає 0-3; n позначає 4 або 5; p позначає 0-2; і r позначає 1-6; або її фармацевтично прийнятні солі. 4 У даному винаході запропоновано сполуку Формули I, де R позначає H. 6 У даному винаході запропоновано сполуку Формули I, де R позначає H або Br. 6 У даному винаході запропоновано сполуку Формули I, де R позначає H. 6 У даному винаході запропоновано сполуку Формули I, де R позначає Br. 4 6 У даному винаході запропоновано сполуку Формули I, де R позначає H і R позначає H або Br. 4 6 У даному винаході запропоновано сполуку Формули I, де R позначає H, а R позначає Br. 1 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил або феніл. 1 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил. 1 У даному винаході запропоновано сполуку Формули I, де R позначає феніл. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає феніл, а R позначає H. 1 6 У даному винаході запропоновано сполуку Формули I, де R позначає феніл, R позначає H, і 4 R позначає H. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, а R позначає H. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 H, а R позначає H. 1 3 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, а R позначає ізопропіл. 4 UA 111761 C2 1 5 10 15 20 25 30 35 40 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 3 H, а R позначає ізопропіл. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 3 H, R позначає H, а R позначає ізопропіл. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 3 H, R позначає H, R позначає H, а R позначає ізопропіл. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 2b 3 H, R позначає H, R позначає H, R позначає метил, а R позначає ізопропіл. 5 У даному винаході запропоновано сполуку Формули I, де R позначає H. 1 5 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, а R позначає H. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 5 H, а R позначає H. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 5 H, R позначає H, а R позначає H. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 5 H, R позначає H, R позначає H, а R позначає H. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 2b 5 H, R позначає H, R позначає H, R позначає метилом, а R позначає H. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 2b 3 5 H, R позначає H, R позначає H, R позначає метил, R позначає ізопропіл, а R позначає H. 5 1c У даному винаході запропоновано сполуку Формули I, де R позначає C(=O)R . 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 2b 3 5 H, R позначає H, R позначає H, R позначає метил, R позначає ізопропіл, а R позначає 1c C(=O) R . 1c У даному винаході запропоновано сполуку Формули I, де R позначає етил. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 2b 3 5 H, R позначає H, R позначає H, R позначає метил, R позначає ізопропіл, а R позначає C(=O)CH2CH3. 5 1 4 7 У даному винаході запропоновано сполуку Формули I, де R позначає P(=O)(OR )(NR R ). 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 2b 3 5 H, R позначає H, R позначає H, R позначає метил, R позначає ізопропіл, а R позначає 1 4 7 P(=O)(OR )(NR R ). 1 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 2b 3 5 H, R позначає H, R позначає H, R позначає метил, R позначає ізопропіл, R позначає 1 4 7 1 P(=O)(OR )(NR R ), а R позначає нафтил. 4 7 У даному винаході запропоновано сполуку Формули I, де R позначає H, а R позначає CH(CH3)C(=O)OCH(CH3)2. 1 4 У даному винаході запропоновано сполуку Формули I, де R позначає нафтил, R позначає 6 2a 2b 3 5 H, R позначає H, R позначає H, R позначає метил, R позначає ізопропіл, R позначає 1 4 7 1 4 7 P(=O)(OR )(NR R ), R позначає нафтил, R позначає H, а R позначає CH(CH3)C(=O)OCH(CH3)2. У даному винаході запропоновано сполуку, вибрану з групи, що складається з: (S)-2-{[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4метил-тетрагідро-фуран-2-ілметокси]-фенокси-фосфориламіно}-пропіонової кислоти ізопропілового ефіру; (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру; (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру; (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-[((S)-1ізопропоксикарбоніл-етиламіно)-(нафтален-2-ілокси)-фосфорилокси]-4-метил-тетрагідро-фуран2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру; (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-4-метил-3пропионілокси-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру; 45 5 UA 111761 C2 (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру; (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру; (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру; (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру; (S)-2-{(S)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси4-метил-тетрагідро-фуран-2-ілметокси]-фенокси-фосфориламіно}-пропіонової кислоти ізопропілового ефіру; (S)-2-{(R)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси4-метил-тетрагідро-фуран-2-ілметокси]-фенокси-фосфориламіно}-пропіонової кислоти ізопропілового ефіру; (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]пропіонової кислоти ізопропілового ефіру; (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]пропіонової кислоти ізопропілового ефіру; (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]пропіонової кислоти ізопропілового ефіру; (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]пропіонової кислоти ізопропілового ефіру; і (S)-2-[[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]пропіонової кислоти ізопропілового ефіру. 5 10 15 20 25 У даному винаході запропоновано спосіб лікування інфекції вірусу гепатиту С (ВГС), що включає введення пацієнтові, що потребує цього, терапевтично ефективної кількості сполуки Формули I. У даному винаході запропоновано вищезазначений спосіб, що додатково включає введення модулятора імунної системи або противірусного засобу, який інгібує реплікацію ВГС, або їх комбінацій. У даному винаході запропоновано вищезазначений спосіб, де модулятором імунної системи є інтерферон або хімічне похідне інтерферону. У даному винаході запропоновані вищезазначені способи, де противірусний засіб вибраний з групи, що складається з інгібітору протеази ВГС, інгібітору гелікази ВГС, інгібітору праймази ВГС, інгібітору злиття ВГС, та їх комбінації. У даному винаході запропоновано спосіб інгібування реплікації ВГС в клітині, що включає введення сполуки Формули I. У даному винаході запропонована композиція, що містить сполуку Формули I і фармацевтично прийнятний ексципієнт. У даному винаході запропоновано застосування сполуки Формули I при виготовленні лікарського засобу для лікування ВГС. У даному винаході запропоновано сполуку, композицію або спосіб, як тут описано. Сполуки Приклади індивідуальних сполук, які охоплюються даним винаходом і які знаходяться в його об'ємі, представлені в наступній таблиці. Ці приклади і способи наведені далі для чіткішого розуміння і здійснення даного винаходу кваліфікованими фахівцями. Вони не повинні розглядатися як винаходи, що обмежують об'єм, а лише як його ілюстрація і втілення. В основному, номенклатура, використана в даному винаході, заснована на AUTONOMTM v.4.0, комп'ютеризованій системі генерації назв хімічних сполук по ІЮПАК інституту Бельштейн. Якщо спостерігається невідповідність між зображеною структурою і назвою, даним для цієї 6 UA 111761 C2 структури, зображена структура має вищу вагу. Крім того, якщо стереохімія структури або частини структури не позначена, наприклад, зв'язком або пунктирною лінією, структура або частина структури повинні інтерпретуватися як так, що охоплюють всі їх стереоізомери. У Таблиці I зображені приклади сполук відповідно до формули I. 5 Таблиця I Сполука № Структура O O O N P O H O O I-1 NH O N O F HO O O I-2 F O H O N P O O NH O N O F HO O O I-3 F O H O N P O O NH O N O F HO F Назва (S)-2-{[(2S, 3S, 4R, 5R)-5-(2,4-діоксо3,4-дигідро-2H-піримідин-1-іл)-2,4дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси]фенокси-фосфориламіно}пропіонової кислоти ізопропіловий ефір (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо3,4-дигідро-2H-піримідин-1-іл)-2,4дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-1-ілокси)-фосфориламіно]пропіонової кислоти ізопропіловий ефір (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо3,4-дигідро-2H-піримідин-1-іл)-2,4дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-2-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір O O O NH O N O O H FO O P N O O I-4 O O I-5 HO N P O O F (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо3,4-дигідро-2H-піримідин-1-іл)-2,4дифтор-3-[((S)-1-ізопропоксикарбонілетиламіно)-(нафтален-2-ілокси)фосфорилокси]-4-метил-тетрагідрофуран-2-ілметокси]-(нафтален-2ілокси)-фосфориламіно]-попіонової кислоти ізопропіловий ефір O O N P O H O NH O N F O F O 7 O (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо3,4-дигідро-2H-піримідин-1-іл)-2,4дифтор-4-метил-3-пропионілокситетрагідро-фуран-2-ілметокси](нафтален-1-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір UA 111761 C2 Таблиця I Сполука № Структура O O I-6 Назва O O N P O H O NH O N F HO O O I-7 F O O N P O H O NH O N F HO O O I-8 O H O N P O O NH O N HO O I-9 O H O N P O O NH O N HO O I-10 O I-11 O H O N P O O NH O N O I-12 O F O H O N P O O NH O N F HO O O F F HO O O F F O O F F O O F O Br O N P O H O NH O N F HO O F 8 O (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(2,4діоксо-3,4-дигідро-2H-піримідин-1-іл)2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-2-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(2,4діоксо-3,4-дигідро-2H-піримідин-1-іл)2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-2-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(2,4діоксо-3,4-дигідро-2H-піримідин-1-іл)2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-1-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(2,4діоксо-3,4-дигідро-2H-піримідин-1-іл)2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-1-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір (S)-2-{(S)-[(2S, 3S, 4R, 5R)-5-(2,4діоксо-3,4-дигідро-2H-піримідин-1-іл)2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси]фенокси-фосфориламіно}-попіонової кислоти ізопропіловий ефір (S)-2-{(R)-[(2S, 3S, 4R, 5R)-5-(2,4діоксо-3,4-дигідро-2H-піримідин-1-іл)2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси]фенокси-фосфориламіно}-попіонової кислоти ізопропіловий ефір (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(5-бромо2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-1-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір UA 111761 C2 Таблиця I Сполука № Структура O O I-13 O Br O N P O H O NH O N F HO O O I-14 F O Br O N P O H O NH O N F HO O O I-15 O NH O N F HO O O I-16 O NH O N F HO 5 10 15 20 25 O F Br H O N P O O O F Br O N P O H O O F O Назва (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(5-бромо2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-2-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(5-бромо2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-1-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(5-бромо2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-2-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір (S)-2-[[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4діоксо-3,4-дигідро-2H-піримідин-1-іл)2,4-дифтор-3-гідрокси-4-метилтетрагідро-фуран-2-ілметокси](нафтален-2-ілокси)-фосфориламіно]попіонової кислоти ізопропіловий ефір Синтез Загальні Схеми Вищеописані способи розкриті детальніше далі: Початкова сполука 1 може бути одержана відповідно до способів, описаних Sofia, M. J. і соавт, J. Med. Chem. (2010), 53(19),7202-7218 і Clark, J. L. і соавт, J. Med. Chem. (2005), 48(17),5504-5508. Йодування, з подальшим видаленням йоду в лужному середовищі може привести до проміжної сполуки 3, в якій захист 3’-гідроксилу за допомогою бензоїльної групи приводить до проміжної сполуки 4. Стереоспецифічна реакція перетворення проміжної сполуки 4 в 5 є ключовою стадією. Аналогічне перетворення для введення фтору в 4’α положенні описано раніше Ajmera, S. і соавт, J. Med. Chem. (1988), 31(6),1094-1098 і Moffatt, J.g. і соавт., J. Am. Chem. Soc. (1971), 93(17), 4323-4324. Заміщення 5" йоду бензоатом натрію дає проміжну сполуку 6. Завершально, депротекція 3", 5" бензоїльних груп в проміжній сполуці 6 дає нуклеозидну проміжну сполуку 7 (Схема 1). 1 У наведених нижче Загальних Схемах, R може бути H, нижчим галоалкілом або арилом, де арил може бути фенілом або нафтилом, можливо заміщеним одним або більше нижчим алкілом, нижчим алкенілом, нижчим алкинілом, нижчим алкокси, гало, нижчим галоалкілом, 1a 1a 1b 1c 1c 1a -N(R )2, ациламіно, -SO2N(R )2, -COR , -SO2(R ), -NHSO2(R ), нітро або ціано, кожен R 1b 1a 1a може бути незалежно H або нижчим алкілом, кожен R може бути незалежно -OR або -N(R )2, 1c 2a 2b кожен R може бути нижчим алкілом, R і R позначають (i) незалежно Н, нижчий алкіл, 1a -(CH2)rN(R )2, нижчий гідроксиалкіл, CH2SH, -(CH2)S(O)pMe, -(CH2)3NHC(=NH)NH2, (1H-індол1b 3-іл)метил, (1H-індол-4-іл)метил, -(CH2)mC(=O)R , арил і арил нижчий алкіл, де арил може бути можливо заміщений одним або більше гідрокси, нижчим алкілом, нижчим алкокси, гало, нітро 2a 2b 4 2a 2b або ціано; (ii) R може бути H, і R і R разом утворюють (CH2)3; (iii) R і R разом утворюють 2a 2b 3 (CH2)n; або, (iv) R і R обидва позначають нижчий алкіло, R може бути H, нижчим алкілом, 4 нижчим галоалкілом, фенілом або феніл нижчим алкілом, R може бути H, нижчим алкілом, або 9 UA 111761 C2 2b 4 5 1c 1b 1 1a R і R разом утворюють (CH2)3, R може бути H, C(=O)R , C(=O)R , P(=O)(OR )(OR ), або 1 4 7 6 7 2a 2b 3 P(=O)(OR )(NR R ), R може бути H, метилом або гало, R може бути C(R R )COOR , m може бути 0-3, n може бути 4 або 5, p може бути 0-2, а r може бути 1-6. Схема 1. NaOMe I2, PPh3 ТГФ, 15 oC 18 г MeOH, 65 oC 4г 3 2 1 I2, AgF BzCl, DMAP PhCOONa ДХМ, 25 oC 3г ТГФ, 0 oC 10 хв ДМСО, 100 oC 18 г 5 4 NH3 MeOH, КТ 18 г 7 6 5 Нуклеозид 7 також може бути благополучно конвертований в 5’-галогеновану проміжну сполуку 8 за допомогою взаємодії з NCS, NBS, або NIS у відповідних умовах (Схема 2). Схема 2. NBX ДМФ, мікрохвил. 80 oC, 10 хв 10 7 X, R6 = Cl, Br, I 8 Фосфорамідатні сполуки даного винаходу можуть бути одержані за допомогою конденсації нуклеозиду 7 або 8 з відповідним чином заміщеним фосфохлоридатною сполукою 11 у присутності сильної основи (Схема 3). Конденсація може бути проведена відносно незахищених 10 UA 111761 C2 нуклеозидів 7 або 8. Зв'язаний продукт 12 у формулі I може бути додатково дериватизований в продукт 13. Обидві сполуки 12 або 13 у формулі I спочатку виходять у вигляді суміші двох діастереомерів в реакції зв'язування і можуть бути розділені на відповідні хіральні енантіомери за допомогою хіральних колонок, хіральної ВЕРХ, або хіральною СКРХ хроматографією. 5 Схема 3. R1OH NEt3, ефір КТ, 18 г 9 NEt3 11 10 трет-BuMgCl R5Cl, DMAP ТГФ ІІ, ТГФ КТ, 3г R5=C(=O)C1-6алкіл 7 or 8 12 R6 = H, Cl, Br, I 13 10 15 20 Дозування і введення: Як показано в наведеній Таблиці, сполуки формули I мають потенціал ефективності як противірусних препаратів для лікування ВГС інфекції в організмі людини або метаболізуються в сполуку, яка проявляє таку активність. В іншому варіанті здійснення винаходу активну сполуку або її похідне або солі можна вводити в комбінації з іншим противірусним засобом, таким як протигепатитний засіб, зокрема сполуку формули I. Коли активну сполуку або її похідне або сіль вводять в комбінації з іншим противірусним засобом активність може бути збільшена в порівнянні з початковою сполукою. Це може бути легко оцінено шляхом одержання похідного і тестування його анти-ВГС активності відповідно до способу, описаному в даному винаході. Введення активної сполуки може знаходитися в діапазоні від безперервного (краплинне внутрішньовенне вливання) до декількох пероральних введень на день (наприклад, чотири рази на день) і може включати пероральне, місцеве парентеральне, внутрішньом'язове, внутрішньовенне, підшкірне, трансдермальне (яке може включати засіб, що підсилює проникність), букальне і супозиторне введення, серед інших шляхів введення. 4'-F заміщені похідні нуклеозидів, а також їх фармацевтично прийнятні солі можуть 11 UA 111761 C2 5 10 15 20 25 30 35 40 45 50 55 60 застосовуватися як лікарські засоби у вигляді будь-якого фармацевтичного препарату. Фармацевтичний препарат можна вводити ентерально, або перорально, наприклад, у вигляді пігулок, пігулок з покриттям, драже, твердих і м'яких желатинових капсул, розчинів, емульсій, сиропів або суспензій, або ректально, наприклад, у вигляді супозиторіїв. Вони також можуть бути введені парентерально (внутрішньом'язово, внутрішньовенно, підшкірно або внутрішньом'язовими ін'єкціями або інфузіями), наприклад, у вигляді розчинів для ін'єкцій, назально, наприклад, у формі назальних спреїв або інгаляційних спреїв, місцево і так далі. Для виготовлення фармацевтичних препаратів, 4'-заміщені похідні нуклеозидів, а також їх фармацевтично прийнятні солі можуть бути приготовані разом з терапевтично інертним неорганічним або органічним наповнювачем для виробництва пігулок, пігулок з покриттям, драже, твердих і м'яких желатинових капсул, розчинів, емульсій або суспензій. Сполуки формули I можуть бути сформульовані в суміші з фармацевтично прийнятним носієм. Наприклад, сполуки за даним винаходом можна вводити перорально у вигляді фармакологічно прийнятних солей. Оскільки сполуки за даним винаходом є переважно розчинними у воді, їх можна вводити внутрішньовенно у фізіологічному сольовому розчині (наприклад, забуференому до рН близько 7,2 до 7,5). З цією метою можуть застосовуватися звичайні буфери, такі як фосфати, бікарбонати або цитрати. Звичайно, будь-який фахівець в даній області може змінити препарати в рамках розкриття даного винаходу з метою одержати численні препарати для конкретного чину введення без додання композиціям за даним винаходом нестійкості або зниження їх терапевтичної активності. Зокрема, модифікація даних сполук з метою зробити їх більш розчинними у воді або іншому носієві, наприклад, може бути легко досягнута шляхом незначних змін (утворення солей, етерифікації і так далі), які прийняті в межах звичайної кваліфікації в даній області техніки. Крім того, в межах звичайної кваліфікації в даній області, можна модифікувати шляхи введення і режим дозування конкретної сполуки з метою контролювання фармакокінетику даних сполук для максимально корисного ефекту у пацієнтів. Для парентеральних препаратів, носій зазвичай включає стерильну воду або водний розчин хлориду натрію, хоча інші інгредієнти, включаючи ті, які допомагають диспергуванню, можуть бути включені. Звичайно, у разі, коли необхідно використовувати стерильну воду і підтримувати її стерильність, композиції і носії також повинні бути стерилізовані. Також можуть бути одержані суспензії для ін'єкцій, в яких можуть застосовуватися відповідні рідкі носії, агенти, що суспендують, і тому подібне. Відповідними ексципієнтами для пігулок, пігулок з покриттям, драже, та твердих желатинових капсул є, наприклад, лактоза, кукурудзяний крохмаль та його похідні, тальк і стеаринова кислота або її солі. Якщо необхідно, пігулки або капсули можуть бути покриті ентеросолюбільною оболонкою або мати сповільнене вивільнення за допомогою стандартних методик. Відповідними ексципієнтамі для м'яких желатинових капсул є, наприклад, рослинні масла, віск, жири, напівтверді і рідкі поліоли. Відповідними наповнювачами для ін'єкційних розчинів є, наприклад, вода, фізіологічний розчин, спирти, поліоли, гліцерин або рослинні масла. Відповідними наповнювачами для супозиторіїв є, наприклад, природні і отверджені масла, віск, жири, напіврідкі або рідкі поліоли. Відповідними наповнювачами для розчинів і сиропів для ентерального застосування є, наприклад, вода, поліоли, сахароза, інвертний цукор і глюкоза. Фармацевтичні препарати за даним винаходом також можуть бути представлені у вигляді препаратів із сповільненим вивільненням або інших відповідних препаратів. Фармацевтичні препарати можуть також містити консерванти, солюбілізатори, стабілізатори, змочуючі агенти, емульгатори, підсолоджувачі, барвники, ароматизатори, солі для регулювання осмотичного тиску, буфери, маскуючі агенти або антиоксиданти. Фармацевтичні препарати можуть також містити інші терапевтично активні засоби, відомі в даній області. Дозування може варіюватися в широких межах і, звичайно, буде адаптоване до індивідуальних вимог у кожному конкретному випадку. Для перорального введення добова доза, що складає від приблизно 0,01 до приблизно 100 мг/кг ваги тіла на день, повинна бути відповідною при монотерапії та/або комбінованій терапії. Переважна добова доза складає від приблизно 0,1 до приблизно 500 мг/кг маси тіла, переважніше від приблизно 0,1 до приблизно 100 мг/кг ваги тіла і найпереважніше від 1,0 до приблизно 100 мг/кг ваги тіла на день. Типовий препарат міститиме від приблизно 5 % до приблизно 95 % активної сполуки (мас/мас). Добову дозу можна вводити у вигляді одноразової дози або в розділених дозах, як правило, від 1 до 5 12 UA 111761 C2 5 10 15 20 25 30 35 40 45 50 55 60 доз на день. У деяких фармацевтичних лікарських формах, пролікарські форми сполук, особливо ациловані (ацетильовані або інші) похідні, піридинові ефіри і різні сольові форми даних сполук є переважними. Фахівцеві в даній області буде зрозуміло, як легко модифікувати дані сполуки в пролікарські форми з метою полегшення доставки активних сполук в цільові ділянки організмухазяїна або пацієнта. Фахівець в даній області також скористається сприятливими фармакокінетичними параметрами пролікарських форм, у відповідних випадках, для доставки даних сполук в цільові ділянки в організмі хазяїна або пацієнта, щоб максимізувати очікуваний ефект сполуки. Показання і спосіб лікування Сполуки за даним винаходом та їх ізомерні форми, а також їх фармацевтично прийнятні солі корисні при лікуванні і профілактиці ВГС інфекції. У даному винаході запропонований спосіб лікування інфекції вірусу гепатиту С (ВГС), що включає введення пацієнтові, що потребує цього, терапевтично ефективної кількості сполуки Формули I. У даному винаході запропонований спосіб інгібування реплікації ВГС в клітинах, що включає введення сполуки Формули I. Комбінована терапія Сполуки за винаходом та їх ізомерні форми, а також їх фармацевтично прийнятні солі корисні при лікуванні і профілактики ВГС інфекції самі по собі або при використанні в комбінації з іншими сполуками, направленими на вірусні або клітинні елементи або функції, що беруть участь в життєвому циклі ВГС. Класи сполук, використовуваних у винаході, включають, без обмеження, всі класи ВГС противірусних препаратів. Для комбінованої терапії, класи засобів за механізмом хімічної реакції, які можуть бути корисні в комбінації із сполуками за даним винаходом, включають, наприклад, нуклеозидні і ненуклеозидні інгібітори полімерази ВГС, інгібітори протеази, інгібітори гелікази, інгібітори NS4B і лікарські засоби, які функціонально інгібують внутрішній сайт зв'язування рибосом (IRES) і інші лікарські засоби, які інгібують приєднання ВГС клітин або зв'язування вірусів, трансляцію РНК ВГС, транскрипцію ВГС РНК, реплікацію або дозрівання ВГС, збірку або вивільнення вірусу. Конкретні сполуки в цих класах і використовувані у винаході, включають, без обмеження, макроциклічні, гетероциклічні і лінійні інгібітори протеази ВГС, такі як телапревір (VX-950), боцепревір (SCH-503034), нарлапревір (SCH-9005 18), ITMN-191 (R-7227), TMC-435350 (тобто TMC-435), MK-7009, BI-201335, Bi-2061 (цилупревір), BMS-650032, ACH-1625, ACH-1095 (інгібітор NS4A кофактора ВГС протеази), VX-500, VX-8 13, PHX-1766, PHX2054, IDX-136, IDX-3 16, ABT-450 EP-0 13420 (і споріднені сполуки) і VBY-376; нуклеозидні інгібітори ВГС полімерази (реплікази), корисні для даного винаходу включають, без обмеження, R7128, PSI-785 1, IDX-184, IDX-102, R1479, UNX-08 189, PSI-6130, PSI-938 і PSI-879 та різні інші нуклеозидні і нуклеотидні аналоги та інгібітори ВГС, включаючи (без обмеження), одержані як 2'-С-метил модифіковані нуклеоз(т)иди, 4'-аза модифіковані нуклеоз(т)иди, і 7'-деазамодифіковані нуклеоз(т)иди. Ненуклеозидні інгібітори ВГС полімерази (реплікази), використовувані у винаході, включають, без обмеження, ВГС-796, ВГС-371, VCH-759, VCH-916, VCH-222, ANA-598, MK-3281, ABT-333, ABT-072, PF-00868554, BI-207127, GS-9190, A-837093, JKT-109, Gl-59728 і Gl-60667. Крім того, сполуки за винаходом можуть застосовуватися в комбінації з антагоністами циклофіліну та імунофіліну (наприклад, без обмеження, сполуки Debio, NM-811, а також циклоспорин та його похідні), інгібіторами кінази, інгібіторами білків теплового шоку (наприклад, HSP90 і HSP70), іншими імуномодулюючими засобами, які можуть включати, без обмеження, інтерферони (альфа-, бета-, омега-, гама-, -лямбда або синтетичні), такі як Інтрон A, Роферон-a, Канферон-A300, Адваферон, Інферген, Хумоферон, Суміферон MP, Альфаферон, ІФН- β, Ферон і т.п.; поліетиленгліколевими (ПЕГ-ілірованими похідними інтерферону) сполуками, такими як ПЕГ-інтерферону α-2a (Пегасис), Пег-інтерферон-α-2b (PEGINTRON), пегільований інтерферон-α-con1 і т. п.; препаратами і похідними інтерферону тривалої дії, таких як альбумін, злитий інтерферон, Альбуферон, Локтерон, і т. п.; інтерферонами з різними типами систем контрольованої доставки (наприклад, ITCA-638, омега-інтерферон, що доставляється підшкірною системою доставки Duros); сполуками, які стимулюють синтез інтерферону в клітинах, такими як Ресихімод і т. п.; інтерлейкінами; сполуками, які підсилюють розвиток відповіді Т клітин-хелперів типу 1, такими як SCV-07 і т. п.; агоністами Толл-подібних рецепторів, такими як CpG-10101 (актилон), ізоторабамін, ANA773 і т. п.; тимозин α-1; ANA-245 і ANA-246; гістамін дигідрохлорид; пропагерманій; тетрахлородкаоксидом; амплігеном; IMP-321; КРН-7000; антитілами, такими як цивацир, XTL-6865 і тому подібне та профілактичними і терапевтичними вакцинами, такими як Інновак С, ВГС E1E2/MF59 і т. п. Крім того, будь-який з 13 UA 111761 C2 5 10 15 20 25 30 35 40 45 50 55 60 вищеописаних способів, що включають введення інгібітору NS5A, тип агоніста рецептора інтерферону типу I (наприклад, IFN-α) і агоніста рецептора інтерферону типу II (наприклад, IFNγ) може бути доповнений введенням ефективної кількості антагоніста TNF-α. Ілюстративні, без обмеження, TNF-α антагоністи, які підходять для використання в таких комбінованих препаратах включають ENBREL, REMICADE, і HUMIRA. Крім того, сполуки за винаходом можуть застосовуватися в комбінації з антипротозойними засобами та іншими противірусними препаратами, які вважаються ефективними в лікуванні ВГС інфекції, такі як, без обмеження, проліки нітазоксанід. Нітазоксанід може бути використаний як засіб в комбінації із сполуками, описаними в даному винаході, а також в комбінації з іншими засобами, використовуваними при лікуванні ВГС інфекції, такими як ПЕГінтерфероном α -2a і рибавірином. Сполуки за винаходом також можуть застосовуватися з альтернативними формами інтерферонів і обробленими поліетиленгліколем інтерферонами, рибавірином або його аналогами (наприклад, тарабаварин, льововорин), мікроРНК, сполуки малих інтерферуючих РНК (наприклад, SIRPLEX-140-N і т. п.), нуклеотидними або нуклеозидними аналогами, імуноглобулінами, гепатопротекторами, протизапальними засобами та іншими інгібіторами NS5A. Інгібітори інших мішеней життєвого циклу ВГС включають інгібітори NS3 гелікази; інгібітори кофактора NS4A; антисмислові олігонуклеотидні інгібітори, такі як ISIS-14803, AVI4065 і т. п.; вектор-кодуємі короткі шпильки РНК (shRNA); ВГС специфічні рибозими, такі як гептазим, RPI, 13919 і т.п.; інгібітори вбудовування, такі як ХЕПЕКС-C, HuMax-HepC і т. п.; інгібітори альфа-глюкозидази, такі як цельгозивір, UT-231B і т. п.; KPE-02003002 і BIVN 401 і IMPDH інгібітори. Інші ілюстративні сполуки - інгібітори ВГС включають ті, які описані в наступних публікаціях: патенти США №. 5,807,876; 6,498,178; 6,344,465; і 6,054,472; публікаціях PCT № WO97/40028; WO98/4038 1; WO00/56331, WO02/04425; WO03/007945; WO03/010141; WO03/000254; WO01/32153; WO00/06529; WO00/18231; WO00/10573; WO00/13708; WO01/85172; WO03/037893; WO03/037894; WO03/037895; WO02/100851; WO02/100846; WO99/01582; WO00/09543; WO02/18369; WO98/17679, WO00/056331; WO98/22496; WO99/07734; WO05/073216, WO05/073195 і WO08/021927. Крім того, комбінації, наприклад, рибавірину і інтерферону, можна вводити у вигляді множинної комбінованої терапії з щонайменше одною із сполук за винаходом. Даний винахід не обмежується вищезазначеними класами або сполуками і передбачає відомі та нові сполуки і комбінації біологічно активних агентів. Передбачається, що комбінована терапія за даним винаходом включає будь-яку хімічно сумісну комбінацію сполуки групи даного винаходу з іншими сполуками групи за винаходом або іншими сполуками зовнішніх щодо винаходу груп, за умови, що комбінація не знижує противірусної активності сполуки групи даного винаходу, або противірусної активності самої фармацевтичної композиції. Комбінована терапія може бути послідовною, тобто лікування за допомогою спочатку одного агента, а потім другого агента (наприклад, де кожне лікування включає різні сполуки за даним винаходом або де одне лікування включає сполуку згідно винаходу та інше включає одну або більше біологічно активну речовину) або це може бути лікування обома агентами одночасно (паралельно). Послідовна терапія може включати достатньо часу після завершення першої терапії перед початком другої терапії. Лікування обома агентами одночасно може проводитися однією добовою дозою або роздільними дозами. Комбінована терапія не обов'язково повинна бути обмежена двома агентами і може включати три або більше агентів. Дозування як для одночасної, так і для послідовної комбінованої терапії залежатимуть від швидкостей всмоктування, розподілу, метаболізму і виведення компонентів комбінованої терапії, а також інших чинників, відомих фахівцям в даній області техніки. Значення дозування також змінюватимуться залежно від тяжкості стану, що підлягає полегшенню. Слід також розуміти, що для будь-якого конкретного суб'єкта конкретні режими і схеми дозування можуть бути скоректовані з часом відповідно до потреби індивіда і висновку фахівця в даній області, що призначає або спостерігає за проведенням комбінованої терапії. У даному винаході запропоновано спосіб лікування інфекції вірусу гепатиту С (ВГС), що включає введення пацієнтові, що потребує цього, терапевтично ефективної кількості сполуки Формули I. У даному винаході запропоновано вищезазначений спосіб, що додатково включає введення модулятора імунної системи або противірусного засобу, який інгібує реплікацію ВГС, або їх комбінацій. У даному винаході запропоновано вищезгаданий спосіб, де модулятором імунної системи є інтерферон або хімічне похідне інтерферону. У даному винаході запропоновані вищезгадані способи, де противірусний засіб вибраний з 14 UA 111761 C2 5 10 15 20 25 30 35 40 45 50 55 60 групи, що складається з інгібітору протеази ВГС, інгібітору гелікази ВГС, інгібітору праймази ВГС, інгібітору злиття ВГС, та їх комбінації. ПРИКЛАДИ Скорочення, використовувані в даній заявці, включають: ацетил (Ac), оцтова кислота (HOAc), азо-біс-ізобутирилнітрил (AIBN), 1-N-гідроксибензотриазол (HOBt), атмосфера (атм), високоефективна рідинна хроматографія (ВЕРХ), 9 -борабіцикло[3.3.1]нонан (9-BBN або BBN), метил (Me), трет-бутоксикарбоніл (Boc), ацетонітрил (MeCN), ди-трет-бутил пірокарбонат або Boc ангідрид (BOC2O), 1-(3-диметиламінопропіл)-3-етилкарбодіімид (EDCI), бензоїл (Bz), бензил (Bn), м-хлорпербензойна кислота (MCPBA), бутил (Bu), метанол (MeOH), бензилоксикарбоніл (Cbz або Z), температура плавлення (ТП), карбонілдіімідазол (CDI), MeSO 2-(метилсульфоніл або Ms), 1,4-діазабіцикло[2,2,2]октан (DABCO), мас-спектр (ms), діетиламіносератрифторид (DAST), метил-трет-бутиловий ефір (МТБЕ), дибензиліденацетон (DBA), N-карбоксиангідрид (NCA), 1,5-діазабіцикло[4.3.0]нон-5-ен (DBN), N-бромсукцинімід (NBS), 1,8діазабіцикло[5.4.0]ундец-7-ен (DBU), N-метилморфолін (NMM), N-метилпіролідон (NMP), 1,2дихлоретан (ДХЕ), піридинійхлорхромат (PCC), N, N'-дициклогексилкарбодіімід (DCC), дихромат піридину (PDC), дихлорметан (ДХМ), пропіл (Pr), діетилазодикарбоксилат (DEAD), феніл (Ph), ди-ізо-пропілазодикарбоксилат, DIAD, фунтів на квадратний дюйм (psi), ди-ізо-пропілетиламін (DIPEA), піридин (пир), ди-ізо-бутилалюмінійгідрид, DIBAL-H, кімнатна температура або КТ, час утримування або RT, N, N-диметилацетамід (DMA), трет-бутилдиметилсиліл або трет- BuMe2Si, (TBDMS), 4-N, N-диметиламінопіридин (DMAP), триетиламін (Et 3N або TEA), N, Nдиметилформамід (ДМФ), трифлат або CF3SO2-(Tf), диметилсульфоксид (ДМСО), трифтороцтова кислота (ТФО), 1,1'-біс-(дифенілфосфіно)етан (ДФФЕ), 2,2,6,6тетраметилгептан-2,6-діон (TMHD), 1,1'-біс-(дифенілфосфіно)фероцен (DPPF), тонкошарова хроматографія (ТШХ), етилацетат (EtOAc), тетрагідрофуран (ТГФ), діетиловий ефір (Et 2O), триметилсиліл або Me3Si (TMS), етил (Et), моногідрат п-толуолсульфонової кислоти (TsOH або pTsOH), літій гексаметилдисилазан (LIHMDS), 4-Me-C6H4SO2- або тозил (Ts), ізопропіл (I-Pr), Nуретан-N-карбоксиангідрид (UNCA), етанол (EtOH). Звичайні номенклатури, включаючи префікси нормальний (N), ізо (I-), вторинний (втор-), третинний (трет-) і нео мають свої звичайні значення при використанні їх з алкільною частиною. (J. Rigaudy і D. P. Klesney, Nomenclature in Organic Chemistry, IUPAC 1979 Pergamon Press, Oxford). Основні умови Сполуки за даним винаходом можуть бути одержані за допомогою різних способів, зображених в ілюстративних реакціях, описаних нижче в розділі Приклади. Початкові матеріали і реагенти, використовувані при одержанні цих сполук, як правило, або доступні від комерційних постачальників, таких як Aldrich Chemical Со, або їх одержують способами, відомими фахівцям в даній області, слідуючи методикам, описаним у посиланнях, таким як Fieser and Fieser's Reagents for Organic Synthesis; Wiley & Sons: New York, 1991, Volumes 1-15; Rodd's Chemistry of Carbon Compounds, Elsevier Science Publishers, 1989, Volumes 1-5 and Supplementals; and Organic Reactions, Wiley & Sons: New York, 1991, Volumes 1-40. Необхідно розуміти, що схеми реакцій синтезу, показані в розділі Приклади, просто ілюструють деякі способи, якими можуть бути синтезовані сполуки за даним винаходом, кваліфікованими фахівцями в даній області техніки можуть бути зроблені або запропоновані різні модифікації цих реакційних схем з посиланням на розкриття відомостей що містяться в даному винаході. Початкові речовини і проміжні сполуки реакційних схем синтезу можуть бути виділені і очищені, якщо необхідно, з використанням звичайних способів, включаючи, але не обмежуючись ними, фільтрування, дистиляція, кристалізація, хроматографія і тому подібне. Такі речовини можуть бути охарактеризовані звичайними параметрами, включаючи фізичні константи і спектральні дані. Якщо не зазначене інше, описані тут реакції зазвичай проводять в інертній атмосфері при атмосферному тиску в діапазоні реакційних температур від -78 °C до приблизно 150 °C, часто, від близько 0 °C до приблизно 125 °C, або, найчастіше і зазвичай, при кімнатній температурі (або температурі навколишнього середовища), наприклад, близько 20 °C. Різні замісники сполук за винаходом, можуть бути присутніми в початкових сполуках, додаватися до будь-якої з проміжних сполук або додаватися після утворення кінцевих продуктів відомими способами за допомогою реакцій заміщення або конверсії. Якщо самі замісники є реактивними, то замісники можуть бути захищені самі по собі відповідно до способів, відомих в даній області. Різні захисні групи відомі в даній області і можуть бути використані. Приклади багатьох можливих груп можна знайти в "Protective Groups in Organic Synthesis" під авторством Green і соавт., John Wiley and Sons, 1999. Наприклад, нітрогрупи можуть бути додані нітруванням і нітрогрупа може бути перетворена в інші групи, такі як аміно відновленням і 15 UA 111761 C2 5 10 галоген діазотуванням аміногрупи і заміною діазогрупи на галоген. Ацильні групи можуть бути додані ацилуванням Фріделя-Крафтса. Ацильні групи можуть бути потім перетворені у відповідні алкільні групи різними способами, зокрема відновленням Вольфа-Кіжнера і відновленням за Клемменсоном. Аміногрупи можна алкілувати з утворенням моно-і диалкіламіногруп; а меркапто і гідроксильні групи можна алкілувати з утворенням відповідних ефірів. Первинні спирти можна окислити за допомогою окислювачів, відомих в даній області, з утворенням карбонових кислот або альдегідів, а вторинні спирти можуть бути окислені з утворенням кетону. Таким чином, реакції заміщення або модифікації можуть бути використані для одержання різних замісників по всій молекулі початкового матеріалу, проміжних сполук або кінцевих продуктів, зокрема виділених продуктів. Приклади одержання Одержання 1. Одержання проміжної сполука хірального 1-((2R, 3R, 4R, 5S)-3-фтор-4-гідрокси-5(йодометил)-3-метил-тетрагідрофуран-2-іл)піримідин-2,4(1H, 3H)-діону 15 O NH I N O HO O F М.М. 370.12 C10H12FIN2O4 20 25 30 Хіральний 1-((2R, 3R, 4R, 5R)-3-фтор-4-гідрокси-5-гідроксиметил-3-метил-тетрагідро-фуран2-іл)-1H-піримідин-2,4-діон (6.14 г, 23.6 ммоль), PPh3 (9 г, 34.4 ммоль), імідазол (2.4 г, 34.4 ммоль) і безводний ТГФ (100 мл) додали в 3-горлову колбу (500 мл), суміш перемішували при 20 °C в атмосфері азоту протягом 20 хв. Потім I 2 (6.6 г, 26 ммоль), розчинений в безводному ТГФ (100 мл), додали в суміш по краплях при 20 °C протягом 30 хв, після додавання, всю суміш перемішували при 20 °C в атмосфері азоту протягом 18 годин. ТШХ показало, що початковий матеріал був витрачений, потім в неї додали воду (50 мл), суміш екстрагували етилацетатом (150 мл×3), органічний шар промили сольовим розчином, висушили над Na 2SO4, видалили розчинник за допомогою зниженого тиску, осад очистили за допомогою хроматографічної колонки з силікагелем (ДХМ: MeOH=100: 1 до 50: 1) з одержанням сполука, зазначеної в заголовку, у вигляді білого осаду (8.2 г, 94 %). + LC-MS (M+H) = 371.0 Одержання 2. Одержання проміжної сполуки хірального 1-((2R, 3R, 4R)-3-фтор-4-гідрокси-3-метил-5метилен-тетрагідрофуран -2-іл)піримідин-2,4(1H, 3H)-діону O NH O 35 HO N O F М.М. 242.21 C10H11FN2O4 40 Хіральний 1-((2R, 3R, 4R, 5S)-3-фтор-4-гідрокси-5-(йодометил)-3-метил-тетрагідрофуран-2ил)піримідин-2,4(1H, 3H)-діон (8.2 г, 22 ммоль) розчинили в MeOH (100 мл) і в нього додали NaOMe (3.73 г, 69 ммоль) в атмосфері азоту, після додавання суміш нагрівали до 65 °C і перемішували в атмосфері азоту протягом 14 годин, ТШХ показало, що початковий матеріал був витрачений, потім суміш охолодили до КТ, в неї додали іонообмінну смолу IR-120 (H) для 16 UA 111761 C2 5 вирівнювання pH до 8, відфільтрували і видалили розчинник за допомогою зниженого тиску, неочищений продукт очистили за допомогою хроматографічної колонки з силікагелем (ДХМ: MeOH=15: 1) з одержанням сполуки, зазначеної в заголовку, у вигляді білого осаду (3.3 г, 59 %). + LC-MS (M+H) = 243.1 Одержання 3. Одержання проміжної сполуки хірального бензойної кислоти (3R, 4R, 5R)-5-(2,4-діоксо-3,4дигідро-2H-піримідин-1-іл)-4-фтор-4-метил-2-метилен-тетрагідро-фуран-3-ілового ефіру O NH O N O O O 10 15 20 F М.М. 346.32 C17H15FN2O5 До суміші хірального 1-((2R, 3R, 4R)-3-фтор-4-гідрокси-3-метил-5-метилен-тетрагідрофуран 2-іл)піримідин-2,4(1H, 3H)-діону (18.3 г, 75.6 ммоль) і DMAP (27.7 г, 227 ммоль) в безводному ТГФ (900 мл) при 0 °C додали BzCl (15.9 г, 113.4 ммоль) по краплях. Реакційну суміш перемішували при 0 °C протягом 0.5 г, потім додали насичений NaHCO3, щоб погасити реакцію. Суміш екстрагували етилацетатом (300 мл×3). Об'єднаний органічний екстракт промили H2O, сольовим розчином, висушили над Na2SO4, і сконцентрували. Залишок очистили за допомогою хроматографічної колонки з силікагелем (ДХМ: MeOH=160: 1 до 120: 1) з одержанням сполуки, зазначеної в заголовку, у вигляді білого осаду (17 г, 65 %). + LC-MS (M+H) = 347.1 Одержання 4. Одержання проміжної сполуки хірального (2R, 3S, 4R, 5R)-5-(2,4-діоксо-3,4дигідропіримідин-1(2H)-іл)-2,4-дифтор-O-2-(йодометил)-4-метил-тетрагідрофуран-3-іл бензоату O NH N I O F O 25 30 35 O O F М.М. 492.22 C17H15F2IN2O5 До суміші хірального бензойної кислоти (3R, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин1-іл)-4-фтор-4-метил-2-метилен-тетрагідро-фуран-3-ілового ефіру (17 г, 49 ммоль) і AgF (31 г, 245 ммоль) в безводному ТГФ (600 мл) при 0 °C додали ТГФ розчин (600 мл) I2 (24.8 г, 98 ммоль) по краплях. Після завершення додавання, реакційну суміш нагрівали до кімнатної температури і перемішували протягом 3 г. ТШХ аналіз показав, що початковий матеріал був повністю витрачений і відбулося утворення необхідного продукту. Реакційну суміш погасили водним розчином NaS2O3 (5 %, 300 мл). Суміш екстрагували етилацетатом (350 мл×3). Об'єднаний органічний екстракт промили сольовим розчином, висушили над Na 2SO4, і сконцентрували. Залишок очистили за допомогою хроматографічної колонки з силікагелем (ДХМ: MeOH=120: 1) з одержанням сполуки, зазначеної в заголовку, у вигляді білого осаду (11 г, 17 UA 111761 C2 5 45 %). + LC-MS (M+H) = 493.0 Одержання 5. Одержання проміжної сполуки хірального (2R, 3S, 4R, 5R r)-5-(2,4-діоксо-3,4дигідропіримідин-1(2H)-іл)-2,4-дифтор-O-2-бензоїлметил-4-метил-тетрагідрофуран-3-іл бензоату O NH O O O O N O F O F М.М. 486.46 C24H20F2N2O7 10 15 20 Хіральний (2R, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідропіримідин-1(2H)-іл)-2,4-дифтор-O-2(йодометил)-4-метил-тетрагідрофуран-3-іл бензоат (0.56 г, 1.15 ммоль), бензоат натрію (0.825 г, 5.73 ммоль) і 18-crown-6 (0.03 г, 0.115 ммоль) суспендували в ДМСО (20 мл), розчин нагрівали до 100 °C і перемішували в атмосфері азоту протягом 18 г, потім охолодили до КТ, в нього додали воду (30 мл), суміш екстрагували етилацетатом (30 мл×3), органічний шар промили H 2O, сольовим розчином і H2O, видалили розчинник за допомогою зниженого тиску, залишок очистили за допомогою колоночной хроматографії на силікагелі (PE: EA=1: 2) з одержанням сполуки, зазначеної в заголовку, у вигляді безбарвного масла (0.34 г, 61 %). + LC-MS (M+Na) = 509.1 Одержання 6. Одержання проміжної сполуки хірального 1-((2R, 3R, 4S, 5S)-3,5-дифтор-4-гідрокси-5(гідроксиметил)-3-метил-тетрагідрофуран-2-іл)піримідин-2,4(1H, 3H)-діону O NH HO O N O F HO 25 30 35 F М.М. 278.21 C10H12F2N2O5 Хіральний (2R, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідропіримідин-1(2H)-іл)-2,4-дифтор-O-2бензоїлметил-4-метил-тетрагідрофуран-3-іл бензоат (0.34 г, 0.7 ммоль) розчинили в метанолі, і додали розчин амонію в метанолі (7 н, 20 мл). Реакційну суміш перемішували при кімнатній температурі протягом ночі. Суміш сконцентрували, а залишок очистили за допомогою колоночной хроматографії на силікагелі (ДХМ: MeOH=20: 1) і препаратівної ВЕРХ з одержанням сполуки, зазначеної в заголовку, у вигляді білого осаду (0.074 г, 38 %). + 1 LC-MS (M+H) = 279.1; H NMR (300MHz, ДМСО-d6) δ 11.575 (s, 1 H), 7.666-7.639 (d, 1 H, J=8.1 Hz), 6.324-6.266 (d, 1 H, J=17.4 Hz), 6.056-6.037 (d, 1 H, J=5.7 Hz), 5.821 (brs, 1 H), 5.7135.686 (d, 1H, J=8.1 Hz), 4.057-4.023 (m, 1H), 3.636 (s, 2 H), 1.313-1.238 (d, 3H, J=22.5 Hz). Одержання 7. Одержання проміжної сполуки хірального 5-бромо-1-((2R, 3R, 4S, 5S)-3,5-дифтор-4-гідрокси5-гідроксиметил-3-метил-тетрагідро-фуран-2-іл)-1H-піримідин-2,4-діону 18 UA 111761 C2 O Br HO NH O N O F HO F М.М. 357.11 C10H11BrF2N2O5 5 10 15 У 2 мл пробірці для мікрохвильової печі хіральний 1-((2R, 3R, 4S, 5S)-3,5-дифтор-4-гідрокси5-(гідроксиметил)-3-метил-тетрагідрофуран-2-іл)піримідин-2,4(1H, 3H)-діон (70 мг, 0.252 ммоль), NBS (67.2 мг, 0.377 ммоль), розчинили в ДМФ (0.7 мл). Реакційну суміш закрили і нагрівали в умовах мікрохвильового випромінювання при 80 °C протягом 10 хв. РХ/МС аналіз показав повне витрачання початкового матеріалу і утворення необхідного продукту як основного. Розчинник евапорірувалі, а залишок очистили за допомогою 2 × 4г силікагельового картриджа, елююючи 070 % EtOAc в гексанах з одержанням сполуки, зазначеної в заголовку, у вигляді білого осаду (94 мг, 90 %) + 1 MS (M) = 358; H NMR (300 MHz, CD3OD): δ(ppm) 8.41 (s, 1H),6.40-6.35 (d, 1H),4.28-4.18 (m, 1H), 3.80-3.76 (d, 2H), 1.45-1.37(d, 3H) Приклад 1. Одержання (S)-2-{[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-фенокси-фосфориламіно}-пропіонової кислоти ізопропілового ефіру O O O O N H P O 25 30 35 40 O N O F HO 20 NH O F I-1 М.М. 547.45 C22H28F2N3O9P Стадія A. (S)-ізопропіл 2-амінопропаноату гідрохлорид (Oakwood, 500 мг, 2.98 ммоль) і фенілфосфородихлоридат (Aldrich, 662 мг, 2.98 ммоль) суспендували в безводному ДХМ (25 мл). Реакційну суміш охолодили до -78 °C. Триетиламін (604 мг, 830 мкл, 5.97 ммоль) додали по краплях. Реакційну суміш перемішували при -78 °C протягом 1 г, потім дали нагрітися до кімнатної температури і перемішували протягом ночі. Розчинник видалили, залишок промили безводним ефіром. Фільтрат сконцентрували з одержанням неочищеного (2S)-ізопропіл 2(хлор(фенокси)фосфориламіно)пропаноату у вигляді світло-жовтого масла (0.8 г, 88 %) і використовували без додаткового очищення. Стадія B. До розчину хірального 1-((2R, 3R, 4S, 5S)-3,5-дифтор-4-гідрокси-5-(гідроксиметил)-3метилтетрагідрофуран-2-іл)піримідин-2,4(1H, 3H)-діону (42 мг, 151 мкмоль), одержаного в Одержанні 6 в ТГФ (8.00 мл) додали ТГФ розчин (Aldrich, 1 M) трет-бутилмагнію хлориду (377 мкл, 377 мкмоль) по краплях. Суміш перемішували при кімнатній температурі протягом 15 хв. з подальшим додаванням ТГФ розчину (0.5 M) (2S)-ізопропіл 2-(хлор(фенокси)фосфориламіно) пропаноату (755 мкл, 377 мкмоль). Реакційну суміш перемішували при кімнатній температурі протягом 1 г, з подальшим додаванням ТГФ розчину (Aldrich, 1 M) трет-бутилмагнію хлориду (189 мкл, 189 мкмоль) ТГФ розчину (0.5 M) (2S)-ізопропіл 2-(хлор(фенокси)фосфориламіно) пропаноату (378 мкл, 189 мкмоль). Реакційну суміш потім перемішували при кімнатній температурі протягом 2 г. Метанол (2 мл) додали щоб погасити реакцію, суміш очистили за 19 UA 111761 C2 5 допомогою флеш-хроматографії (силікагель, 0-15 % MeOH в ДХМ) і висушили під вакуумом з одержанням сполуки, зазначеної в заголовку, у вигляді світло-жовтого осаду (18 мг, 22 %). + LC-MS (M+H) = 548.1 Приклад 2 Одержання (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]пропіонової кислоти ізопропілового ефіру O O O O N H P O 15 20 25 30 35 40 45 O N O F HO 10 NH O F I-2 М.М. 597.51 C26H30F2N3O9P Стадія A. Нафтален-1-ол (Aldrich, 1.5 г, 10.4 ммоль) і оксихлорид фосфору (V) (Aldrich, 1.6 г, 0.97 мл, 10.4 ммоль) суспендували в безводному ефірі (37.5 мл), і температуру знизили до -78 °C. Триетиламін (1.05 г, 1.45 мл, 10.4 ммоль) додали по краплях і реакційну суміш перемішували при -78 °C протягом 1 г. Реакційну суміш нагрівали до кімнатної температури і перемішували протягом ночі. Суміш відфільтрували, а фільтрат сконцентрували з одержанням неочищеного нафтален-1-іл фосфородихлоридату у вигляді світло-жовтого масла (2 г, 74 %) і використовували на наступній стадії без додаткового очищення. Стадія B. (S)-ізопропіл 2-амінопропаноату гідрохлорид (Oakwood, 1.28 г, 7.64 ммоль) і нафтален-1-іл фосфородихлоридат (2 г, 7.66 ммоль) суспендували в безводному ДХМ (35 мл). Реакційну суміш охолодили до -78 °C. Триетиламін (1.55 г, 2.13 мл, 15.3 ммоль) додали по краплях. Реакційну суміш перемішували при -78 °C протягом 1 г, потім нагрівали до кімнатної температури і перемішували протягом 5 г. Розчинник видалили, а залишок промили безводним етиловим ефіром і відфільтрували. Фільтрат сконцентрували з одержанням неочищеного (2S)ізопропіл 2-(хлор(нафтален-1-ілокси)фосфориламіно)пропаноату у вигляді світло-жовтого масла (2.5 г, 92 %) і використовували без додаткового очищення. Стадія C. До розчину хірального 1-((2R, 3R, 4S, 5S)-3,5-дифтор-4-гідрокси-5-(гідроксиметил)-3метилтетрагідрофуран-2-іл)піримідин-2,4(1H, 3H)-діону (150 мг, 539 мкмоль) одержаного в Одержанні 6 в ТГФ (24 мл) додали ТГФ розчин (Aldrich, 1 M) трет-бутилмагнію хлориду (1.35 мл, 1.35 ммоль) по краплях. Суміш перемішували при кімнатній температурі протягом 15 хв, з подальшим додаванням ТГФ розчину (0.5 M) (2S)-ізопропіл 2-(хлор(нафтален-1-ілокси) фосфориламіно) пропаноату (2.7 мл, 1.35 ммоль). Реакційну суміш перемішували при кімнатній температурі протягом 1 г, потім додали додаткову кількість ТГФ розчину (Aldrich, 1 M) третбутилмагнію хлориду (0.68 мл, 0.68 ммоль) і ТГФ розчину (0.5 M) (2S)-ізопропіл 2(хлор(нафтален-1-ілокси)фосфориламіно)пропаноату (1.35 мл, 0.68 ммоль). Реакційну суміш потім перемішували при кімнатній температурі протягом 3 г. Метанол (6 мл) додали, щоб погасити реакцію, суміш очистили за допомогою флеш-хроматографії (силікагель, 0-15 % MeOH в ДХМ) і висушили під вакуумом з одержанням сполуки, зазначеної в заголовку, у вигляді білого осаду (0.2 г, 62 %). + LC-MS (M-H) = 596.0 Приклад 3 Одержання (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]пропіонової кислоти ізопропілового ефіру 20 UA 111761 C2 O O O O N H NH O P O O N O F HO F I-3 М.М. 597.51 C26H30F2N3O9P 5 10 15 20 25 30 35 40 Стадія A. Нафтален-2-ол (Aldrich, 2 г, 13.9 ммоль) і оксихлорид фосфору (V) (Aldrich, 2.13 г, 1.29 мл, 13.9 ммоль) суспендували в безводному ефірі (50 мл), і температуру знизили до -78 °C. Триетиламін (1.4 г, 1.93 мл, 13.9 ммоль) додали по краплях і реакційну суміш перемішували при -78 °C протягом 1 г. Реакційну суміш нагрівали до кімнатної температури і перемішували протягом ночі. Суміш відфільтрували, а фільтрат сконцентрували з одержанням неочищеного нафтален-2-іл фосфородихлоридату у вигляді світло-жовтого масла (2.5 г, 69 %) і використовували на наступній стадії без додаткового очищення. Стадія B. (S)-ізопропіл 2-амінопропаноату гідрохлорид (Oakwood, 500 мг, 2.98 ммоль) і нафтален-2-іл фосфородихлоридат (724 мг, 2.98 ммоль) суспендували в безводному ДХМ (25 мл). Реакційну суміш охолодили до -78 °C. Триетиламін (604 мг, 830 мкл, 5.97 ммоль) додали по краплях. Реакційну суміш перемішували при -78 °C протягом 1 г, потім дали нагрітися до кімнатної температури і перемішували протягом 5 г. Розчинник видалили, а залишок промили безводним етиловим ефіром і відфільтрували. Фільтрат сконцентрували з одержанням неочищеного (2S)ізопропіл 2-(хлор(нафтален-2-ілокси)фосфориламіно)пропаноату у вигляді світло-жовтого масла (0.8 г, 75 %) і використовували без додаткового очищення. Стадія C. До розчину хірального 1-((2R, 3R, 4S, 5S)-3,5-дифтор-4-гідрокси-5-(гідроксиметил)-3метилтетрагідрофуран-2-іл)піримідин-2,4(1H, 3H)-діону (60 мг, 216 мкмоль) одержаного в Одержанні 6 в ТГФ (8 мл) додали ТГФ розчин (Aldrich, 1 M) трет-бутилмагнію хлориду (539 мкл, 539 мкмоль) по краплях. Суміш перемішували при кімнатній температурі протягом 15 хв. з подальшим додаванням ТГФ розчину (0.5 M) (2S)-ізопропіл 2-(хлор(нафтален-2-ілокси) фосфориламіно)пропаноату (1.08 мл, 539 мкмоль). Реакційну суміш перемішували при кімнатній температурі протягом 1 г, потім додали додаткову кількість ТГФ розчину (Aldrich, 1 M) третбутилмагнію хлориду (270 мкл, 270 мкмоль) і ТГФ розчину (0.5 M) (2S)-ізопропіл 2(хлор(нафтален-2-ілокси)фосфориламіно)пропаноату (0.54 мл, 270 мкмоль). Реакційну суміш потім перемішували при кімнатній температурі протягом 18 г. Метанол (2 мл) додали, щоб погасити реакцію, суміш очистили за допомогою флеш-хроматографії (силікагель, 1-18 % MeOH в ДХМ) і висушили під вакуумом з одержанням сполуки, зазначеної в заголовку, у вигляді білого осаду (75 міліграм, 58 %). + LC-MS (M-H) = 596.1 Приклад 4 Одержання (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3[((S)-1-ізопропоксикарбоніл-етиламіно)-(нафтален-2-ілокси)-фосфорилокси]-4-метил-тетрагідрофуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру 21 UA 111761 C2 O O O N H O NH O P O N O O F O F N P O H O O O I-4 М.М. 916.81 C42H48F2N4O13P2 5 10 15 У способі, описаному для одержання (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру в Прикладі 3 Стадія C (S)-2[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-[((S)-1ізопропоксикарбоніл-етиламіно)-(нафтален-2-ілокси)-фосфорилокси]-4-метил-тетрагідро-фуран2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропіловий ефір одержали як другий продукт: білий осад, 8 мг (4 %). + LC-MS (M+H) = 917.2 Приклад 5 Одержання (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-4метил-3-пропионілокси-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси) -фосфориламіно]пропіонової кислоти ізопропілового ефіру O O O O N H NH O P O O O 25 30 O F O 20 N F I-5 М.М. 653.58 C29H34F2N3O9P До розчину (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]пропіонової кислоти ізопропілового ефіру, одержаного в Прикладі 2 (86 мг, 144 мкмоль) в ТГФ (10 мл) додали пропіонілхлорид (66.6 мг, 720 мкмоль) і DMAP (87.9 мг, 720 мкмоль). Реакційну суміш перемішували при кімнатній температурі протягом 5 г. Суміш розбавили етилацетатом, промили водою, сольовим розчином. Органічний шар відокремили, висушили над MgSO 4, і сконцентрували. Залишок очистили за допомогою флеш-хроматографії (силікагель, 40 г, 0-15 % MeOH в ДХМ) з одержанням сполуки, зазначеної в заголовку, у вигляді білого осаду (45 мг, 48 %). + LC-MS (M-H) = 652.1 Приклад 6 Одержання хірального (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1 22 UA 111761 C2 іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)фосфориламіно]-пропіонової кислоти ізопропілового ефіру O O O O N H NH O P O O 10 15 O F HO 5 N F I-6 М.М. 597.51 C26H30F2N3O9P (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропіловий ефір, одержаний в Прикладі 3 (50 мг), розділили за допомогою хіральної СКРХ хроматографії з одержанням хірального (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру у вигляді білого осаду (27 мг, 54 %) + LC-MS (M-H) = 596.1 Приклад 7 Одержання хірального (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)фосфориламіно]-пропіонової кислоти ізопропілового ефіру 20 O O O O N H NH O P O O N O F HO F I-7 М.М. 597.51 C26H30F2N3O9P 25 30 35 (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропіловий ефір, одержаний в Прикладі 3 (50 мг), розділили за допомогою хіральної СКРХ хроматографії з одержанням хірального (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру у вигляді білого осаду (12 мг, 24 %). + LC-MS (M-H) = 596.1 Приклад 8 Одержання хірального (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)фосфориламіно]-пропіонової кислоти ізопропілового ефіру 23 UA 111761 C2 O O O O N H NH O P O O N O F HO F I-8 М.М. 597.51 C26H30F2N3O9P 5 10 15 (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропіловий ефір, одержаний в Прикладі 2 (100 мг), розділили за допомогою хіральної СКРХ хроматографії з одержанням хірального (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру у вигляді білого осаду (24 мг, 24 %). + LC-MS (M-H) = 596.1 Приклад 9 Одержання хірального (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)фосфориламіно]-пропіонової кислоти ізопропілового ефіру O O O O N H P O 25 30 O N O F HO 20 NH O F I-9 М.М. 597.51 C26H30F2N3O9P (S)-2-[[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропіловий ефір, одержаний в Прикладі 2 (100 мг), розділили за допомогою хіральної СКРХ хроматографії з одержанням хірального (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру у вигляді білого осаду (53 міліграми, 53 %) + LC-MS (M-H) = 596.1 Приклад 10 Одержання хірального (S)-2-{(S)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-фенокси-фосфориламіно}пропіонової кислоти ізопропілового ефіру 35 24 UA 111761 C2 O O O O N H NH O P O O N O F HO F I-10 М.М. 547.45 C22H28F2N3O9P 5 10 15 (S)-2-{[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4метил-тетрагідро-фуран-2-ілметокси]-фенокси-фосфориламіно}-пропіонової кислоти ізопропіловий ефір, одержаний в Прикладі 1 (0.18 г), розділили за допомогою хіральної СКРХ хроматографії з одержанням хірального (S)-2-{(S)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-феноксифосфориламіно}-пропіонової кислоти ізопропілового ефіру у вигляді білого осаду (60 мг, 33 %). + LC-MS (M+H) = 548.0 Приклад 11 Одержання хірального (S)-2-{(R)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-фенокси-фосфориламіно}пропіонової кислоти ізопропілового ефіру O O O O N H NH O P O O N O F HO F I-11 М.М. 547.45 C22H28F2N3O9P 20 25 30 (S)-2-{[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4метил-тетрагідро-фуран-2-ілметокси]-фенокси-фосфориламіно}-пропіонової кислоти ізопропіловий ефір, одержаний в Прикладі 1 (0.18 г) розділили за допомогою хіральної СКРХ хроматографії з одержанням хірального (S)-2-{(R)-[(2S, 3S, 4R, 5R)-5-(2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-феноксифосфориламіно}-пропіонової кислоти ізопропілового ефіру у вигляді білого осаду (28 мг, 16 %). + LC-MS (M+H) = 548.0 Приклад 12 Одержання хірального (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру 25 UA 111761 C2 O Br O O O N H NH O P O O O N F HO F I-12 М.М. 676.41 C26H39Br2N3O9P 5 10 15 20 25 Стадія A. До розчину хірального 5-бромо-1-((2R, 3R, 4S, 5S)-3,5-дифтор-4-гідрокси-5-гідроксиметил-3метил-тетрагідро-фуран-2-іл)-1H-піримідин-2,4-діону (50 мг, 0.14 ммоль), одержаного в Одержанні 7, в ТГФ (3 мл) при 0 °C додали ТГФ розчин (Aldrich, 1 M) трет-бутилмагнію хлориду (0.35 мл, 0.35 ммоль) по краплях. Суміш перемішували при 0 °C протягом 15 хв, з подальшим додаванням ТГФ розчину (0.5 M) (2S)-ізопропіл 2-(хлор(нафтален-1-ілокси)фосфориламіно) пропаноату, одержаного в Прикладі 2 Стадія B (0.7 мл, 0.35 ммоль). Реакційну суміш нагрівали до кімнатної температури і перемішували протягом 2 г. Метанол (2 мл) додали, щоб погасити реакцію. Суміш очистили за допомогою флеш-хроматографії (5-10 % MeOH в ДХМ) з одержанням (S)-2-[[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)фосфориламіно]-пропіонової кислоти ізопропілового ефіру у вигляді білого осаду (50 мг, 52 %). Стадія B. (S)-2-[[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси) -фосфориламіно]пропіонової кислоти ізопропіловий ефір (50 мг) розділили за допомогою хіральної СКРХ хроматографії з одержанням хірального (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси](нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру у вигляді білого осаду (11 мг, 22 %). LC-MS (M)+ = 676.0 Приклад 13 Одержання хірального (S)-2-[(S)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру 30 O Br O O O N H NH O P O O N O F HO F I-13 М.М. 676.41 C26H39Br2N3O9P 35 (S)-2-[[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]пропіонової кислоти ізопропіловий ефір, одержаний в Прикладі 16 (50 мг), розділили за допомогою хіральної СКРХ хроматографії з одержанням хірального (S)-2-[(S)-[(2S, 3S, 4R, 5R)5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро 26 UA 111761 C2 5 фуран-2-ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру у вигляді білого осаду (27 мг, 54 %). + LC-MS (M) = 676.0 Приклад 14 Одержання хірального (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру O Br O O O N H NH O P O O F HO 10 15 20 O N F I-14 М.М. 676.41 C26H39Br2N3O9P В процесі розділення (S)-2-[[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-1-ілокси)фосфориламіно]-пропіонової кислоти ізопропілового ефіру (50 мг) за допомогою хіральної СКРХ хроматографії в Прикладі 12 Стадія B, хіральний (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2ілметокси]-(нафтален-1-ілокси)-фосфориламіно]-пропіонової кислоти ізопропіловий ефір одержали як другий продукт: білий осад (8 мг, 16 %). + LC-MS (M) = 676.0 Приклад 15 Одержання хірального (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2Hпіримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру 25 O Br O O O N H NH O P O O N O F HO F I-15 М.М. 676.41 C26H39Br2N3O9P 30 35 В процесі розділення (S)-2-[[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H-піримідин1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2-ілокси)фосфориламіно]-пропіонової кислоти ізопропілового ефіру, одержаного в Прикладі 16 (50 мг), за допомогою хіральної СКРХ хроматографії, хіральний (S)-2-[(R)-[(2S, 3S, 4R, 5R)-5-(5-бромо2,4-діоксо-3,4-дигідро-2H-піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2ілметокси]-(нафтален-2-ілокси)-фосфориламіно]-пропіонової кислоти ізопропіловий ефір одержали як другий продукт: білий осад (16 мг, 32 %). + LC-MS (M) = 675.9 Приклад 16 Одержання хірального (S)-2-[[(2S, 3S, 4R, 5R)-5-(5-бромо-2,4-діоксо-3,4-дигідро-2H 27 UA 111761 C2 піримідин-1-іл)-2,4-дифтор-3-гідрокси-4-метил-тетрагідро-фуран-2-ілметокси]-(нафтален-2ілокси)-фосфориламіно]-пропіонової кислоти ізопропілового ефіру O Br O O O N H P O 10 15 20 25 30 35 40 45 O N O F HO 5 NH O F I-16 М.М. 676.41 C26H39Br2N3O9P До розчину хірального 5-бромо-1-((2R, 3R, 4S, 5S)-3,5-дифтор-4-гідрокси-5-гідроксиметил-3метил-тетрагідро-фуран-2-ил)-1H-піримідин-2,4-диона (92 мг, 0.26 ммоль), одержаного в Одержанні 7, в ТГФ (3 мл) при 0 °C додали ТГФ розчин (Aldrich, 1 M) трет-бутилмагнію хлориду (0.64 мл, 0.64 ммоль) по краплях. Суміш перемішували при 0 °C протягом 15 хв, з подальшим додаванням ТГФ розчину (0.5 M) (2S)-ізопропіл 2-(хлор(нафтален-2-ілокси)фосфориламіно) пропаноату, одержаного в Прикладі 3 Стадія B (1.29 мл, 0.64 ммоль). Реакційну суміш нагрівали до кімнатної температури і перемішували протягом 2 г. Метанол (2 мл) додали щоб погасити реакцію. Суміш очистили за допомогою флеш-хроматографії (5-10 % MeOH в ДХМ) з одержанням сполуки, зазначеної в заголовку, у вигляді білого осаду (56 мг, 32 %). + LC-MS (M) = 676.0 Біологічні приклади Аналіз реплікона ВГС Цей аналіз вимірює здатність сполук формули I інгібувати реплікацію РНК ВГС, і таким чином їх потенційну цінність для лікування ВГС інфекцій. Даний аналіз використовує репортер як єдиний показник внутриклітинного рівня РНК реплікона ВГС. Ген люциферази Renilla ввели в першу відкриту рамку зчитування генотипованого конструкта реплікона 1b Nk5.1 (N. Krieger et al., J. Virol. 2001 75(10):4614), відразу після внутрішньої послідовності сайту зв'язування рибосоми (IRES), злитого з геном неоміцинфосфотрансферази (NPTII) через саморозщеплюваний пептид 2A з вірусу ящура (M.d. Ryan & J. Drew, EMBO 1994 13(4):928-933). Після in vitro транскрипції РНК електропорувалі в клітини гепатоми людини Huh7, стійкі до G418 колонії були відокремлені і розмножені. Стабільно виділена клітинна лінія 2209-23 містила реплікативну субгеномну РНК ВГС, і активність люциферази Renilla, що експресується репліконом, відображала його рівень РНК в клітинах. Аналіз проводили в повторних планшетах, один в матово-білих та один в прозорих, з метою вимірювання противірусної активності і цитотоксичності хімічних сполук в паралелях, щоб бути упевненим, що спостережувана активність не є результатом пониженої проліферації клітин або загибелі клітин. Клітини ВГС реплікона (2209-23), які експресують репортер люциферази Renilla, культивували в середовищі Дульбекко MEM (Invitrogen cat no. 10569-010) з 5 % фетальною бичачою сироваткою (FBS, Invitrogen cat. no. 10082-147) та висівали на 96-лункові планшети в кількості 5000 клітин на лунку, та інкубували протягом ночі. Двадцять чотири години опісля, різні розведення хімічних сполук в ростовому середовищі додали до клітин, які потім інкубували при 37 °C протягом трьох днів. Після закінчення часу інкубації, клітини в білих планшетах зібрали і люциферазну активність вимірювали за допомогою системи аналізу люциферази R. luciferase (Promega cat no. E2820). Всі реагенти, описані в наступному абзаці знаходилися у складі набору виробника, і для одержання реагентів слідували інструкціям виробника. Клітини один раз промили 100 мкл фосфатно-сольового буфера (pH 7.0) (PBS) на лунку і лізували за допомогою 20 мкл 1x R. luciferase Assay лікуючим буфером перед інкубацією при кімнатній температурі протягом 20 хв. Планшет потім помістили в мікропланшетний люмінометр Centro LB 960 (Berthold Technologies), в кожну лунку додали 100 мкл R. luciferase Assay буфера і сигнал вимірювали з використанням 2-секундної затримки, 2-секундна програма вимірювань. IC50, концентрація ліків, необхідна для зниження рівня репліконів на 50 % в порівнянні з контрольним 28
ДивитисяДодаткова інформація
Назва патенту англійською2',4'-difluoro-2'-methyl substituted nucleoside derivatives as inhibitors of hcv rna replication
Автори англійськоюZhang, Jing, Zhang, Zhuming
Автори російськоюЧжан Цзин, Чжан Чжумин
МПК / Мітки
МПК: A61K 31/7072, A61P 31/14, C07H 19/06
Мітки: реплікації, інгібітори, 2',4'-дифтор-2'-метилзаміщені, гепатиту, вірусу, похідні, нуклеозидні
Код посилання
<a href="https://ua.patents.su/33-111761-24-diftor-2-metilzamishheni-nukleozidni-pokhidni-yak-ingibitori-replikaci-phk-virusu-gepatitu-c.html" target="_blank" rel="follow" title="База патентів України">2′,4′-дифтор-2′-метилзаміщені нуклеозидні похідні як інгібітори реплікації phk вірусу гепатиту c</a>
Попередній патент: Пристрій для електродугового напилення композиційних покриттів
Наступний патент: Спосіб отримання фармакологічно активного ліпосомального засобу, що містить кверцетин
Випадковий патент: Механізм відтяжки полотна круглов'язальної машини