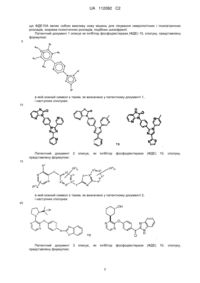
Кристалічна форма конденсованої гетероциклічної сполуки
Формула / Реферат
1. Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3Н-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2Н-імідазо[4,5-b]піридин-2-ону, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки з міжплощинними відстанями (d) 13,59±0,2, 9,22±0,2, 7,88±0,2, 6,76±0,2, 6,21±0,2, 6,13±0,2, 5,73±0,2, 4,64±0,2, 3,79±0,2, 3,75±0,2 ангстреми в порошковій рентгенівській дифракції.
2. Кристалічна форма за пунктом 1, яка демонструє порошкову рентгенівську дифрактограму, що має додаткові характеристичні піки з міжплощинними відстанями (d) 7,48±0,2, 5,24+0,2, 5,13±0,2, 4,27±0,2, 4,16±0,2, 4,06±0,2, 3,99±0,2, 3,93±0,2, 3,60±0,2, 3,41±0,2, 3,16±0,2, 3,10±0,2, 3,06±0,2, 2,89±0,2, 2,83±0,2, 2,73±0,2 та 2,58±0,2 ангстреми в порошковій рентгенівській дифракції.
3. Кристалічна форма за пунктом 1, яка показує початкову температуру приблизно 222 °C - приблизно 224 °C ендотермічної поведінки, викликаної плавленням в ДСК-вимірюваннях (швидкість зростання температури 5 °C/хв.).
4. Лікарський засіб, який містить кристалічну форму за пунктом 1.
5. Лікарський засіб за пунктом 4, який є інгібітором фосфодіестерази 10А.
6. Лікарський засіб за пунктом 4, який є профілактичним або терапевтичним агентом при шизофренії.
7. Спосіб попередження або лікування шизофренії у ссавців, за яким ссавцю вводять ефективну кількість кристалічної форми за пунктом 1.
8. Застосування кристалічної форми за пунктом 1 для отримання профілактичного або терапевтичного лікарського засобу для лікування шизофренії.
9. Кристалічна форма за пунктом 1 для застосування в профілактиці або лікуванні шизофренії.
Текст
Реферат: Представлений винахід стосується кристалічної форми 1-етил-7-метил-3-{4-[(3-метил-3Німідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2Н-імідазо[4,5-b]піридин-2-ону, придатної для використання як профілактичного або терапевтичного засобу для лікування шизофренії, який демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,2 і 6,76±0,2 ангстреми у порошковій рентгенівській дифракції. UA 112082 C2 (12) UA 112082 C2 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 60 Галузь техніки, до якої відноситься винахід Представлений винахід стосується кристалічної форми конденсованої гетероциклічної сполуки, яка проявляє надзвичайну інгібувальну активність відносно фосфодіестерази 10A, і є придатною для використання як засіб для лікуванння або профілактики шизофренії і т.д., та подібних захворювань. Рівень техніки Фосфодіестерази (ФДЕи) є суперродиною ферментів, які кодуються 21 генами, та поділяються на 11 окремих родин у відповідності до структурних та функціональних властивостей. Ці ферменти метаболічно інактивують убіквітарні внутрішньоклітинні вторинні месенджери, циклічний аденозин-монофосфат (цАМФ) і циклічний гуанозин-монофосфат (цГМФ); ФДЕи селективно каталізують гідроліз 3’-естерного зв'язку, створюючи інактивований 5’-монофосфат. На основі субстратної специфічності, ФДЕ родини можут бути також класифіковані на три групи: i) цАМФ-ФДЕи (ФДЕ4, ФДЕ7, ФДЕ8), ii) цГМФ-ФДЕи (ФДЕ5, ФДЕ6 та ФДЕ9) та iii) ФДЕи подвійної субстратної специфічності (ФДЕ1, ФДЕ2, ФДЕ3, ФДЕ10 та ФДЕ11). цАМФ та цГМФ залучаються у регуляцію практично кожного фізіологічного процесу, такого як вироблення протизапального медіатора і дію, функцію іонного каналу, м'язову релаксацію, утворення здатності до навчання та запам'ятовування, диференціювання, апоптоз, ліпогенез, глікогеноліз і глюконеогенез. Особливо у нейронах ці вторинні месенджери відіграють важливо роль у регуляції синаптичної трансмісії, а також у нейрональному диференціюванні і виживанні (не патентний документ1). Регуляція цих процесів за допомогою цАМФ і цГМФ супроводжується активацією протеїнкінази A (ПК-A) і протеїнкінази G (ПК-G), які в свою чергу фосфорилюють різноманітні субстрати, включаючи фактори транскрипції, іонні канали і рецептори, які регулюють різноманітні фізіологічні процеси. Очевидно, що внутрішньоклітинні концентрації цАМФ і цГМФ розділені у часі, просторі та функціонально регуляцією систем аденілат- і гуанілатциклаз у відповідь на позаклітинну сигналізацію та їх деградацію за допомогою ФДЕз (не патентний документ 2). ФДЕи є єдиними засобами, що забезпечують деградацію циклічних нуклеотидів цАМФ і цГМФ у клітинах, таким чином, ФДЕи відіграють суттєву роль у сигнальній трансдукції циклічного нуклеотиду. Таким чином, ФДЕи можуть бути перспективними мішенями для різноманітних терапевтичних лікарських засобів. Фосфодіестераза 10A (ФДЕ10A) була відкрита у 1999 (не патентні документи 3-5). Дослідження експресії продемонстрували, що ФДЕ10A має найбільш обмежене розповсюдження серед всіх відомих родин ФДЕ; мРНК ФДЕ10A є у значній мірі експресованою тільки у головному мозку і яєчках (не патентні 6 і 7). У головному мозку, мРНК і білок ФДЕ10A чисельно представлені у серединних шипикових нейронах (МШНи) смугастого тіла (не патентні 8 і 9). МШНи класифікуються на дві групи: МШН, які експресують дофамінові рецептори Д1, що відповідають за прямий (стріонігральний) шлях і МШН, які експресують дофамінові рецептори Д2, що відповідають за непрямий (стріопалідарний) шлях. Функцією прямого шляху є планування і виконання рухів, в той час як функцією непрямого шляху є дія на поведінкову активацію як гальмування. Оскільки ФДЕ10A експресується у обидвох групах МШН, інгібітори ФДЕ10A могли б активувати обидва ці шляхи. Антипсихотична ефективність сучасних медикаментів, антагоністів Д2 або Д2/5-HT2A рецепторів, в основному є наслідком їх активування непрямого шляху у смугастому тілі. Оскільки інгібітори ФДЕ10A здатні активувати цей шлях, це передбачає, що інгібітори ФДЕ10A є перспективними як антипсихотичні лікарські засоби. Надлишково виражений антагонізм по відношенню до Д2 рецептора у головному мозку антагоністами Д2 викликає проблеми екстрапірамідальних побічних ефектів і гіперпролактинемії. Однак, експресія ФДЕ10A обмежується цими стріарними шляхами у головному мозку, таким чином, очікується, що побічні ефекти від інгібіторів ФДЕ10A є слабшими, у порівнянні з існуючими антагоністами Д2. Щодо гіперпролактинемії, інгібітори ФДЕ10A не будуть підвищено продукувати пролактин через відсутність вираженого антагонізма по відношенню до Д2 рецептора у гіпофізі. Крім того, присутність ФДЕ10A у прямому шляху забезпечує можливість того, що інгібітори ФДЕ10A будуть мати деяку перевагу, у порівнянні з існуючими антагоністами Д2; вважається, що прямий шлях сприятиме бажаній дії, а активація цього шляху інгібіторами ФДЕ10A може перешкоджати екстрапірамідальним симптомам, викликаним надлишково вираженим антагонізмом по відношенню до Д 2 рецептора. Крім того, активація цього шляху могла б полегшити таламо-стріарний відтік, сприяючи виконанню комплексів процедурних комплексів заходів. Крім того, підсилення рівнів вторинного месенджера без блокади дофаміну та/або інших нейротрансмітерних рецепторів може також забезпечити терапевтичні переваги, відзначені незначною кількістю негативних побічних ефектів, у порівнянні з існуючими антипсихотичними засобами (наприклад, гіперпролактинемія і збільшення маси тіла). Це унікальне розподілення і функція у головному мозку вказують на те, 1 UA 112082 C2 що ФДЕ10A являє собою важливу нову мішень для лікування неврологічних і психіатричних розладів, зокрема психотичних розладів, подібних шизофренії. Патентний документ 1 описує як інгібітор фосфодіестерази (ФДЕ) 10, сполуку, представлену формулою: 5 в якій кожний символ є таким, як визначено у патентному документі 1, і наступних сполуках: 10 . Патентний документ представлену формулою: 2 описує, як інгібітор фосфодіестерази (ФДЕ) 10, сполуку, 10, сполуку, 15 в якій кожний символ є таким, як визначено у патентному документі 2, і наступних сполуках: 20 . Патентний документ представлену формулою: 3 описує, як інгібітор 2 фосфодіестерази (ФДЕ) UA 112082 C2 в якій кожний символ є таким, як визначено у патентному документі 3, і наступних сполуках: . 5 Патентний документ представлену формулою: 4 описує, як інгібітор фосфодіестерази (ФДЕ) 10, сполуку, в якій кожний символ є таким, як визначено у патентному документі 4, Патентний документ 5 описує, як інгібітор фосфодіестерази (ФДЕ) представлену формулою: 10, сполуку, в якій Z є 10 15 в якій кожний символ є таким, як визначено у патентному документі 5. 3 UA 112082 C2 Патентний документ представлену формулою: 6 описує, як інгібітор фосфодіестерази (ФДЕ) 10, сполуку, 5 10 15 20 25 30 35 40 45 в якій кожний символ є таким, як визначено у патентному документі 6. [Перелік документів] [патентні документи] патентний документ 1: WO2008/004117 патентний документ 2: WO2010/057121 патентний документ 3: WO2010/057126 патентний документ 4: WO2006/072828 патентний документ 5: WO2008/001182 патентний документ 6: WO2010/090737 [не патентні документи] не патентний документ 1: Nat. Rev. Drug Discov. 2006, vol. 5, p. 660-670 не патентний документ 2: Circ. Res. 2007, vol. 100(7), p. 950-966 не патентний документ 3: Proc. Natl. Acad. Sci. USA, 1999, vol. 96, p. 8991-8996 не патентний документ 4: J. Biol. Chem. 1999, vol. 274, p. 18438-18445 не патентний документ 5: Gene, 1999, vol. 234, p. 109-117 не патентний документ 6: Eur. J. Biochem. 1999, vol. 266, p. 1118-1127 не патентний документ 7: J. Biol. Chem. 1999, vol. 274, p. 18438-18445 не патентний документ 8: Eur. J. Biochem. 1999, vol. 266, p. 1118-1127 не патентний документ 9: Brain Res. 2003, vol. 985, p. 113-126 Cкорочений опис винаходу Проблеми, що вирішуються даним винаходом Існує потреба у розробці сполуки, що має надзвичайну інгібувальну дію по відношенню до ФДЕ10A, яка є придатною для використання як засіб для лікуванння або профілактики шизофренії і т.д. і подібних захворювань, і має надзвичайні властивості у стабільності. Способи вирішення проблеми Винахідники представленого винаходу провели інтенсивні дослідження у спробі вирішити визначені вище проблеми і успішно одержали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он у вигляді кристалічної форми, яка є термодинамічно, хімічно і фізично високо стабільною. На додаток, винахідники виявили, що кристалічна форма має надзвичайну інгібувальну дію по відношенню до ФДЕ10A, і є в достатній мірі задовільною для використання як медикамент для лікування або профілактики шизофренії і подібних захворювань. Винахідники завершили представлений винахід на основі даних, отриманих в результаті цих досліджень. Таким чином, представлений винахід стосується [1] кристалічної форми 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону, що демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,2 і 6,76±0,2 ангстремів у порошковій рентгенівській дифракції (що тут і надалі іноді згадується як кристалічна форма, згідно з представленим винаходом); [2] кристалічної форми, визначеної вище у пункті [1], яка демонструє порошкову рентгенівську дифрактограму, що має також характеристичні піки при значеннях міжплощинних відстаней (d) 9,22±0,2, 7,88±0,2, 6,21±0,2, 6,13±0,2, 5,73±0,2, 4,64±0,2, 3,79±0,2 і 3,75±0,2 ангстремів у порошковій рентгенівській дифракції; 4 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 60 [3] кристалічної форми, визначеної вище у пункті [2], яка демонструє порошкову рентгенівську дифрактограму, що має також характеристичні піки, при значеннях міжплощинних відстаней (d) 7,48±0,2, 5,24±0,2, 5,13±0,2, 4,27±0,2, 4,16±0,2, 4,06±0,2, 3,99±0,2, 3,93±0,2, 3,60±0,2, 3,41±0,2, 3,16±0,2, 3,10±0,2, 3,06±0,2, 2,89±0,2, 2,83±0,2, 2,73±0,2 і 2,58±0,2 ангстремів у порошковій рентгенівській дифракції; [4] кристалічної форми, визначеної вище у пункті [1], яка демонструє температуру початку ендотермічного переходу, викликаного плавленням, від приблизно 222 до приблизно 224C, при вимірюванні за допомогою ДСК (диференційної скануючої калориметрії) (швидкість підвищення температури складає 5C/хв.); [5] медикаменту, що містить кристалічну форму, визначену вище у пункті [1]; [6] медикаменту, визначеного вище у пункті [5], який є інгібітором фосфодіестерази 10A; [7] медикаменту, визначеного вище у пункті [5], який є профілактичним або терапевтичним засобом проти шизофренії; [8] способу запобігання або лікування шизофренії у ссавця, що включає введення ссавцеві ефективної кількості кристалічної форми, визначеної вище у пункті [1]; [9] застосування кристалічної форми, визначеної вище у пункті [1], для одержання профілактичного або терапевтичного лікарського засобу від шизофренії; [10] кристалічної форми, визначеної вище у пункті [1], для застосування для профілактики або лікування шизофренії; та подібного. Ефект винаходу Оскільки кристалічна форма, згідно з представленим винаходом, демонструє надзвичайну інгібувальну дію по відношенню до ФДЕ10A, проявляє низьку токсичність та надзвичайну стабільність, вона є придатною для використання як фармацевтичний продукт. Скорочений опис фігур Фіг. 1 демонструє порошкову рентгенівську дифрактограму кристалічної форми Допоміжного прикладу 1-1. Фіг. 2 демонструє порошкову рентгенівську дифрактограму кристалічної форми Допоміжного прикладу 2. Фіг. 3 демонструє порошкову рентгенівську дифрактограму кристалічної форми Допоміжного прикладу 3. Фіг. 4 демонструє порошкову рентгенівську дифрактограму кристалічної форми Допоміжного прикладу 4, Фіг. 5 демонструє порошкову рентгенівську дифрактограму кристалічної форми Допоміжного прикладу 5. Фіг. 6 демонструє порошкову рентгенівську дифрактограму кристалічної форми Допоміжного прикладу 6. Фіг. 7 демонструє порошкову рентгенівську дифрактограму кристалічної форми Допоміжного прикладу 7, Фіг. 8 демонструє порошкову рентгенівську дифрактограму кристалічної форми Прикладу 1(2). Фіг. 9 демонструє термоаналітичні дані ДСК кристалічної форми Прикладу 1(2). Опис втілень (Детальний опис винаходу) Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону у представленому винаході може бути сольватом, таким як гідрат і т. п., або не сольватом, таким як не гідрат (ангідрид) і т. п… Приклади "гідрату" включають від 0,5 гідрату до 5,0 гідрату. Серед них перевага надається 0,5 гідрату, 1,0 гідрату, 1,5 гідрату, 2,0 гідрату і 2,5 гідрату. Особлива перевага надається 0,5 гідрату, 1,0 гідрату і 1,5 гідрату. Крім того, визначений вище "гідрат" може бути також "гідратом змінного складу", що містить змінну кількість води у кристалічній структурі у відповідності до вологості оточуючого середовища. Вміст води гідрату змінного складу змінюється в межах діапазону від приблизно 4,0 до приблизно 14,5 мас. %. 1-Етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2Hімідазо[4,5-b]піридин-2-он у представленому винаході може також бути його дейтеридом. Крім того, кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону у представленому винаході може також бути сольватом, іншим ніж гідрат. Приклади сольватованої кристалічної форми 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону включають кристали 5 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 60 сольвату спирту, такі як кристал метанольного сольвату, кристал етанольного сольвату і т. п. (переважно кристал сольвату C1-6 спирту), кристалогідрат з органічним розчинником, до якого додають воду і органічний розчинник (наприклад, кристалогідрати спирту, такі як метанологідрат, етанологідрат і т.д., переважно кристалогідрат C 1-6 спирту) і т. п… Кристалічна форма,згідно з представленим винаходом, може бути одержана кристалічним перетворенням аморфної форми 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону або інших кристалічних форм (включаючи гідрат кристалічної форми) 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону. Кристалічне перетворення є явищем, де кристалічна структура змінюється, коли температура або тиск перевищує певний рівень. Оскільки "спосіб кристалічного перетворення" є відомим по суті, то можуть бути зазначені способи такі як, наприклад, кристалізація з розчину (наприклад, спосіб концентрування, спосіб повільного охолодження, спосіб за допомогою реакції (дифузійний метод, електролізний метод, метод гідротермального синтезу, розчин-розплавний метод і т. п.), кристалізація на основі зазначеного вище (наприклад, метод сублімації (метод запаяної кювети, метод у потоці газу), метод реакції в газовій фазі, метод хімічних транспортних реакцій), кристалізація з розплавленої форми (наприклад, метод нормальної спрямованої кристалізації (метод витягування з розплаву, метод температурного перепаду, метод Бріджмена), метод зонного плавлення (метод горизонтального зонного плавлення, метод плаваючої зони), спеціальний метод вирощування кристалів (метод VLS (пара-рідина-кристал) метод рідинно-фазної епітаксії), метод транспірації (спосіб, що включає розчинення кристалу у розчиннику, фільтрування і випаровування розчинника в умовах оточуючого середовища), метод затравочної зависі (спосіб, що включає додавання кристалу до розчинника, таким чином, щоб залишився надлишок твердої речовини для створення суспензії, перемішування суспензії при кімнатній температурі або при нагріванні, або при охолодженні, і збирання твердої речовини), сушіння при пониженому тиску, подрібнення, перетворення на порошок, обпресування та їм подібні. Для одержання кристалічної форми, згідно з представленим винаходом, з наведених вище способів перевага надається методу затравочної зависі. Для аналізування одержаної кристалічної форми стандартно використовують рентгенодифракційний кристалографічний аналіз. Крім того, кристалічна орієнтація може бути також визначена за допомогою механічного способу, оптичного методу (наприклад, Фур'єРаман спектр, спектр ЯМР твердого тіла) і т.д… Крім того, відповідно до стандартних способів можуть бути також здійснені термічний аналіз кристалу (диференційна скануюча калориметрія (ДСК)), аналіз інфрачервоного спектра поглинання (KBr) і т. п… Пік спектра, одержаного за допомогою способу вищезазначеного аналізу, обов'язково містить певну похибку вимірювання, в силу своєї природи. Кристалічна форма, що має пік у спектрі в межах діапазону похибки також охоплюється кристалічною формою, згідно з представленим винаходом. Наприклад, “±0,2" або “±0,1" у міжплощинній відстані (d) порошкової рентгенівської дифракції означає, що похибка є допустимою. Кристалічна форма, згідно з представленим винаходом, одержана за допомогою визначеного вище способу, є новою кристалічною формою, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,2 і 6,76±0,2 ангстремів, у порошковій рентгенівській дифракції, і є переважно несольватованою кристалічною формою (наприклад, ангідридом). Кристалічна форма, згідно з представленим винаходом, є переважно кристалічною формою, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,2, 9,22±0,2, 7,88±0,2, 6,76±0,2, 6,21±0,2, 6,13±0,2, 5,73±0,2, 4,64±0,2, 3,79±0,2 і 3,75±0,2 ангстремів у порошковій рентгенівській дифракції, та є переважно несольватованою кристалічною формою (наприклад, ангідридом). Кристалічна форма, згідно з представленим винаходом, більш переважно є кристалічною формою, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,2, 9,22±0,2, 7,88±0,2, 7,48±0,2, 6,76±0,2, 6,21±0,2, 6,13±0,2, 5,73±0,2, 5,24±0,2, 5,13±0,2, 4,64±0,2, 4,27±0,2, 4,16±0,2, 3,99±0,2, 3,93±0,2, 3,79±0,2, 3,75±0,2, 3,60±0,2, 3,41±0,2, 2,89±0,2, 2,73±0,2 і 2,58±0,2 ангстремів у порошковій рентгенівській дифракції, та є переважно несольватованою кристалічною формою (наприклад, ангідридом). Кристалічна форма, згідно з представленим винаходом, ще більш переважніше є кристалічною формою, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,2, 9,22±0,2, 7,88±0,2, 6 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 60 7,48±0,2, 6,76±0,2, 6,21±0,2, 6,13±0,2, 5,73±0,2, 5,24±0,2, 5,13±0,2, 4,64±0,2, 4,27±0,2, 4,16±0,2, 4,06±0,2, 3,99±0,2, 3,93±0,2, 3,79±0,2, 3,75±0,2, 3,60±0,2, 3,41±0,2, 3,16±0,2, 3,10±0,2, 3,06±0,2, 2,89±0,2, 2,83±0,2, 2,73±0,2 і 2,58±0,2 ангстремів у порошковій рентгенівській дифракції, та є переважно несольватованою кристалічною формою (наприклад, ангідридом). Як інше втілення, кристалічна форма, згідно з представленим винаходом, одержана за допомогою вищезазначеного способу, є новою кристалічною формою, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,1 і 6,76±0,1 ангстремів у порошковій рентгенівській дифракції, та є переважно несольватованою кристалічною формою (наприклад, ангідридом). Кристалічна форма, згідно з представленим винаходом, є переважно кристалічною формою, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,1, 9,22±0,1, 7,88±0,1, 6,76±0,1, 6,21±0,1, 6,13±0,1, 5,73±0,1, 4,64±0,1, 3,79±0,1 і 3,75±0,1 ангстремів у порошковій рентгенівській дифракції, та є переважно несольватованою кристалічною формою (наприклад, ангідридом). Кристалічна форма, згідно з представленим винаходом, більш переважно є кристалічною формою, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,1, 9,22±0,1, 7,88±0,1, 7,48±0,1, 6,76±0,1, 6,21±0,1, 6,13±0,1, 5,73±0,1, 5,24±0,1, 5,13±0,1, 4,64±0,1, 4,27±0,1, 4,16±0,1, 3,99±0,1, 3,93±0,1, 3,79±0,1, 3,75±0,1, 3,60±0,1, 3,41±0,1, 2,89±0,1, 2,73±0,1 і 2,58±0,1 ангстремів у порошковій рентгенівській дифракції, та є переважно несольватованою кристалічною формою (наприклад, ангідридом). Кристалічна форма, згідно з представленим винаходом, ще більш переважніше є кристалічною формою, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки при значеннях міжплощинних відстаней (d) 13,59±0,1, 9,22±0,1, 7,88±0,1, 7,48±0,1, 6,76±0,1, 6,21±0,1, 6,13±0,1, 5,73±0,1, 5,24±0,1, 5,13±0,1, 4,64±0,1, 4,27±0,1, 4,16±0,1, 4,06±0,1, 3,99±0,1, 3,93±0,1, 3,79±0,1, 3,75±0,1, 3,60±0,1, 3,41±0,1, 3,16±0,1, 3,10±0,1, 3,06±0,1, 2,89±0,1, 2,83±0,1, 2,73±0,1 і 2,58±0,1 ангстремів у порошковій рентгенівській дифракції, та є переважно несольватованою кристалічною формою (наприклад, ангідридом). Кристалічна форма, згідно з представленим винаходом, є переважно безводною кристалічною формою. Кристалічна форма, згідно з представленим винаходом, демонструє температуру початку ендотермічного переходу, викликаного плавленням, від приблизно 222 до приблизно 224C, переважно приблизно 223C, при вимірюванні за допомогою ДСК за умов швидкості підвищення температур 5C/хв., де термін "приблизно" в цьому документі означає ±1C. Кристалічна форма, згідно з представленим винаходом, демонструє максимальну температуру ендотермічного переходу, викликаного плавленням, від приблизно 223 до приблизно 225C, переважно приблизно 224C, при вимірюванні за допомогою ДСК за умов швидкості підвищення температур 5C/хв., де термін "приблизно" в цьому документі означає ±1C. Максимальна температура ендотермічного переходу є вищою, ніж температура початку. Кристалічна форма, згідно з представленим винаходом, не має двох або декількох ендотермічних характеристик в діапазоні від кімнатної температури до приблизно 240C (вона має тільки пік ендотермічного переходу, викликаного одним плавленням), при вимірюванні за допомогою ДСК за умов швидкості підвищення температур 5C/хв., де термін "приблизно" в цьому документі означає ±1C. Чистота кристалічної форми, згідно з представленим винаходом, складає приблизно 95 % 100 %, переважно приблизно 97 % - 100 %, більш переважно приблизно 99 % - 100 %. Одержана в такий спосіб кристалічна форма, згідно з представленим винаходом, має надзвичайну інгібувальну дію по відношенню до ФДЕ10A, проявляє низьку токсичність та є придатною для використання як фармацевтичний продукт. Крім того, оскільки кристалічна форма, згідно з представленим винаходом, є надзвичайно стабільною, вона може легко піддаватись обробці і може бути перетворена на тверду фармацевтичну композицію з гарною відтворюваністю. Кристалічна форма, згідно з представленим винаходом, є придатною для використання для профілактики та/або лікування, наприклад, наступних захворювань або симптомів у ссавців (наприклад, людей, корів, коней, собак, кішок, мавп, мишей, щурів і т.д., головним чином людей): психотичного розладу (наприклад, короткочасного психотичного розладу, індукованого психотичного розладу); психозу, викликаного вживанням алкоголю, амфетаміну, маріхуани, кокаїну, галюціногенів, ожирінням, леткими речовинами наркотичної дії, опіоїдами або фенциклідином; маячного розладу; 7 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 60 тривожного розладу; розладу руху; розладу настрою; великого депресивного розладу; великого депресивного розладу на фоні психотичного розладу, що включає маячний розлад або шизофренію; епізоду глибокої депресії легкого, помірного або тяжкого типу; епізоду маніакальної поведінки або розладу змішаного характеру; епізоду гіпоманіакальної поведінки; депресивного епізоду з атиповими ознаками; депресивного епізоду з ознаками меланхолічного розладу; депресивного епізоду з кататонічними ознаками; епізоду розладу настрою з післяпологовим початком; постінсультної депресії; дистимічного розладу; малого депресивного розладу; аутизму; звикання до надмірного вживання лікарських засобів; нейродегенеративного захворювання; нейродегенерації, пов'язаної з травмою головного мозку; нейродегенерації, пов'язаної з інсультом; нейродегенерації, пов'язаної з церебральним інфарктом; нейродегенерації, індукованої гліпоглікемією; нейродегенерації, пов'язаної з нападом епілепсії; нейродегенерації, пов'язаної з отруєнням нейротоксинами; мультисистемної атрофії; хвороби Альцгеймера; деменції; мультиінфарктної деменції; алкогольної деменції або іншої, пов'язаної з вживанням наркотиків деменції; деменції, пов'язаної з внутрішньочерепними пухлинами або травмою головного мозку; деменції, пов'язаної з хворобою Хантінгтона або хворобою Паркінсона; СНІД-асоційованої деменції; лобно-скроневої деменції; делірію; амнестичного розладу; посттравматичного стресового розладу; розумової відсталості; порушення здатності до навчання (наприклад, розладу читання, розладу математичних навичок або розладу здатності до письмового вираження); синдрому дефіциту уваги і гіперактивності; зниження когнітивної здатності, пов'язаної з віком; передменструального дисфоричного розладу; постпсихотичного депресивного розладу при шизофренії; біполярних розладів, що включають біполярний розлад І типу і біполярний розлад ІІ типу; циклотимічного розладу; хвороби Паркінсона; хвороби Хантінгтона; параноїдного розладу; шизофренії (наприклад, параноїдної шизофренії, гебефренічної шизофренії, кататонічної шизофренії, шизофренії недиференційованого типу, залишкової шизофренії); шизофреноформного розладу; шизоафективного розладу маячного типу або депресивного типу; розладу особистості параноїдального типу; розладу особистості шизоїдного типу; ожиріння; метаболічного синдрому; інсулінонезалежного цукрового діабету (НІЗЦД); порушення толерантності до глюкози; та їм подібних, зокрема для профілактики та/або лікування шизофренії. 8 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 Кристалічна форма, згідно з представленим винаходом, проявляє низьку токсичність і може бути безпечно введена пероральним шляхом або не пероральним шляхом (наприклад, місцевим, ректальним і внутрішньовенним шляхом введення, і т.д.), як сама по собі або у формі фармацевтичних композицій, створених за допомогою загально відомого способу, з фармакологічно прийнятним носієм, наприклад, таблеток (включаючи таблетки з цукровим покриттям і таблетки з плівковим покриттям), порошків, гранул, капсул (включаючи м'які капсули), таблеток, що розпадаються у ротовій порожнині, плівок, що розпадаються у ротовій порожнині, рідин, ін'єкційних лікарських форм, супозиторіїв, лікарських форм пролонгованої дії та пластирів. Вміст кристалічної форми, згідно з представленим винаходом, у фармацевтичній композиції складає від приблизно 0,01 до 100 мас. % відносно маси всієї композиції. В той же час доза змінюється в залежності від суб'єкта, якому вводиться, шляху введення, цільового захворювання, симптому і т. п., наприклад, для перорального введення пацієнту з шизофренією (дорослій людині, з масою тіла приблизно 60 кг), одинична доза загалом знаходиться в межах діапазону від приблизно 0,1 до приблизно 20 мг/кг маси тіла, переважно від приблизно 0,2 до приблизно 10 мг/кг маси тіла, більш переважно від приблизно 0,5 до приблизно 10 мг/кг маси тіла. Таку дозу вводять переважно від одного до декількох разів (наприклад, 3 рази) у день. Фармакологічно прийнятні носії, які можуть використовуватись для одержання фармацевтичної композиції, згідно з представленим винаходом, включають різноманітні органічні або неорганічні речовини-носії, що загально прийнятно використовуються як фармацевтичні матеріали, включаючи ексціпієнти, змащувальні речовини, зв'язувальні речовини, дезінтегранти, водорозчинні полімери та основні неорганічні солі для твердих препаративних лікарських форм; та розчинники, солюбілізувальні агенти, суспендувальні агенти, ізотонічні агенти, буфери та заспокійливі засоби для рідких препаративних лікарських форм. При необхідності можуть також використовуватись інші стандартні фармацевтичні добавки, такі як консерванти, антиоксиданти, барвники, підсолоджувачі, підкислюючі агенти, шипучі агенти, коригенти смаку і запаху, і т. п… Такі "ексціпієнти" включають, наприклад, лактозу, цукрозу, D-маніт, крохмаль, кукурудзяний крохмаль, кристалічну целюлозу, світлу безводну кремнієву кислоту, оксид титану і т. п… Такі "змащувальні речовини" включають, наприклад, стеарат магнію, естер цукрози і жирних кислот, поліетиленгліколь, тальк і стеаринову кислоту. Такі "зв'язувальні речовини" включають, наприклад, гідроксипропілцелюлозу, гідроксипропілметилцелюлозу, кристалічну целюлозу, α-крохмаль, полівінілпіролідон, порошок гуміарабіку, желатин, пулулан, низько-заміщену гідроксипропілцелюлозу і т. п… Такі "дезінтегранти" включають (1) кросповідон, (2) так звані супер-дезінтегранти, такі як кроскармелоза натрію (FMC-Asahi Chemical) і кармелоза кальцію (GOTOKU CHEMICAL CO., LTD.), (3) натрій-карбоксиметилкрохмаль (наприклад, продукт виробництва Matsutani Chemical), (4) низько-заміщену гідроксипропілцелюлозу (наприклад, продукт виробництва Shin-Etsu Chemical), (5) кукурудзяний крохмаль, і т.д. Згаданий "кросповідон" може бути будь-яким поперечно-зшитим полімером, що має хімічну назву 1-етеніл-2-піролідиноновий гомополімер, включаючи полівінілполіпіролідон (ПВПП) і 1-вініл-2-піролідиноновий гомополімер, і прикладом якого є Колідон CL (виробництва BASF), Поліпласдон XL (виробництва ISP), Поліпласдон XL-10 (виробництва ISP), Поліпласдон INF-10 (виробництва ISP) і т. п… Такі "водорозчинні полімери" включають, наприклад, розчинні в етанолі водорозчинні полімери і т. п. [наприклад, похідні целюлози, такі як гідроксипропілцелюлоза (тут і надалі також згадується як ГПЦ), полівінілпіролідон] та нерозчинні в етанолі водорозчинні полімери [наприклад, похідні целюлози, такі як гідроксипропілметилцелюлоза (тут і надалі також згадується як ГПМЦ), метилцелюлоза і натрійкарбоксиметилцелюлоза, поліакрилат натрію, полівініловий спирт, альгінат натрію, гуарова камедь і т. п.]. Такі "основні неорганічні солі" включають, наприклад, основні неорганічні солі натрію, калію, магнію та/або кальцію. Перевага надається основним неорганічним солям магнію та/або кальцію. Більша перевага надається основним неорганічним солям магнію. Такі основні неорганічні солі натрію включають, наприклад, карбонат натрію, гідрокарбонат натрію, вторинний кислий фосфат натрію і т.д… Такі основні неорганічні солі калію включають, наприклад, карбонат калію, гідрокарбонат калію і т.д… Такі основні неорганічні солі магнію включають, наприклад, карбонат магнію важкий, карбонат магнію, оксид магнію, гідроксид магнію, алюмометасилікат магнію, силікат магнію, алюмінат магнію, синтетичний гідроталькіт [Mg6Al2(OH)16·CO3·4H2O] і алюмомагнієвий гідроксид. Серед інших, перевага надається карбонату магнію важкому, карбонату магнію, оксиду магнію, магнію гідроксиду, і т.д… Такі 9 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 60 основні неорганічні солі кальцію включають, наприклад, осаджений карбонат кальцію, гідроксид кальцію і т.д… Такі "розчинники" включають, наприклад, воду для ін'єкції, спирт, пропіленгліколь, макроголь, сезамову олію, кукурудзяну олію, оливову олію і т.д… Такі "солюбілізувальні агенти" включають, наприклад, поліетиленгліколь, пропіленгліколь, Dманіт, бензилбензоат, етанол, тріс-амінометан, холестерин, триетаноламін, карбонат натрію, цитрат натрію і т. п… Такі "суспендувальні агенти" включають, наприклад, поверхнево-активні речовини, такі як стеарилтриетаноламін, лаурилсульфат натрію, лаурил-амінопропіонова кислота, лецитин, безалконій хлорид, бензетонію хлорид, гліцеринмоностеарат і т. п.; гідрофільні полімери, такі як полівініловий спирт, полівінілпіролідон, натрійкарбоксиметилцелюлоза, метилцелюлоза, гідроксиметилцелюлоза, гідроксиетилцелюлоза, гідроксипропілцелюлоза і т.д… та т. п… Такі "ізотонічні агенти" включають, наприклад, глюкозу, D-сорбит, хлорид натрію, гліцерин, D-маніт і т. п… Такі "буфери" включають, наприклад, буферні розчини фосфатів, ацетатів, карбонатів, цитратів і т.д… Такі "заспокійливі засоби" включають, наприклад, бензиловий спирт і т. п… Такі "консерванти" включають, наприклад, естери п-оксибензойної кислоти, хлорбутанол, бензиловий спирт, фенетиловий спирт, дегідрооцтову кислоту, сорбінову кислоту і т. п… Такі "антиоксиданти" включають, наприклад, сульфіти, аскорбінову кислоту, α-токоферол і т. п… Такі "барвники" включають, наприклад, харчові барвники, такі як харчовий барвник жовтий № 5, харчовий барвник червоний № 2 та харчовий барвник синій № 2; та харчові забарвлюючі лаки, оксид заліза червоний і т. п… Такі "підсолоджувачі" включають, наприклад, сахарин натрію, дикалій гліцеризинат, аспатам, стевію, тауматин і т. п… Такі "підкислюючі агенти" включають, наприклад, лимонну кислоту (безводну лимонну кислоту), винну кислоту, яблучну кислоту і т. п… Такі "шипучі агенти" включають, наприклад, бікарбонат натрію і т. п… Такі "коригенти смаку і запаху" можуть бути синтетичними речовинами або речовинами природного походження, і включають, наприклад, лимон, лайм, помаранча, ментол, полуницю і т. п… Кристалічна форма, згідно з представленим винаходом, може бути одержана як препаративна форма для перорального введення відповідно до загально відомого способу, наприклад, шляхом формування під тиском у присутності ексціпієнта, дезінтегранта, зв'язувальної речовини, змащувальної речовини або їм подібних, а потім при необхідності нанесення покриття за допомогою загально відомого способу з метою маскування смаку, розчинення у кишковому тракті або пролонгованого вивільнення. Для ентеросолюбільної препаративної лікарської форми, за допомогою загально відомого способу може забезпечуватись проміжний шар між ентеросолюбільним шаром і шаром, що містить лікарську речовину, з ціллю відокремлення двох шарів. Для одержання кристалічної форми, згідно з представленим винаходом, у вигляді таблетки, що розпадається у ротовій порожнині, доступні способи включають, наприклад, спосіб, в якому ядро, що містить кристалічну целюлозу і лактозу покривають кристалічною формою, згідно з представленим винаходом і основною неорганічною сіллю, і також покривають покривним шаром, що містить водорозчинний полімер, одержуючи композицію, яку покривають ентеросолюбільним покривним шаром, що містить поліетиленгліколь, додатково покривають ентеросолюбільним покривним шаром, що містить триетилцитрат, більше того, покривають ентеросолюбільним покривним шаром, що містить поліетиленгліколь, і більш того, ще покривають манітом, одержуючи гранули тонкого помелу, які змішують з добавками і формують, і т. п… Згаданий вище "ентеросолюбільний покривний шар" включає, наприклад, водні субстрати розчинного у кишковому тракті полімеру, такі як ацетат-фталат целюлози (АФЦ), фталат гідроксипропілметилцелюлози, ацетат-сукцинат гідроксиметилцелюлози, спів-полімери метакрилової кислоти [наприклад, Eudragit L30D-55 (торгова марка; виробництва Rohm), Colicoat MAE30DP (торгова марка; виробництва BASF), Polykid PA30 (торгова марка; виробництва San-yo Chemical) і т. п.], карбоксиметилетилцелюлоза, шелак і т. п.; субстрати пролонгованого вивільнення, такі як спів-полімери метакрилової кислоти [наприклад, Eudragit NE30D (торгова марка), Eudragit RL30D (торгова марка), Eudragit RS30D (торгова марка), і т.д…] і т. п.; водорозчинні полімери; пластифікатори, такі як триетилцитрат, поліетиленгліколь, ацетильовані моногліцериди, триацетин, рицинова олія і т. п.; і їх суміші, і т. п… Зазначена вище 10 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 60 "добавка" включає, наприклад, водорозчинні цукрові спирти (наприклад, сорбіт, маніт, мальтит, сахариди з низьким вмістом крохмалю, ксиліт, відновлену палатинозу, еритрит і т.д…), кристалічну целюлозу [наприклад, Ceolas KG 801, Avicel PH 101, Avicel PH 102, Avicel PH 301, Avicel PH 302, Avicel RC-591 (кристалічна целюлоза і натрієва сіль кармелози) і т. п.], низькозаміщену гідроксипропілцелюлозу [наприклад, LH-22, LH-32, LH-23, LH-33 (Shin-Etsu Chemical) та їх суміші і т. п.] і т. п.; також використовують зв'язувальні речовини, заспокійливі засоби, шипучі агенти, підсолоджувачі, коригенти смак і запаху, змащувальні речовини, барвники, стабілізатори, ексціпієнти, дезінтегранти і т.д… Кристалічна форма, згідно з представленим винаходом, може вводитись як окремий активний агент або у комбінації з іншими медикаментами, такими як інші засоби використовувані у лікуванні психозу, особливо шизофренії і біполярного розладу, обсесивнокомпульсивного розладу, великої депресії, хвороби Паркінсона, хвороби Альцгеймера, когнітивного порушення та/або втрати пам'яті [наприклад, агоністи α7 нікотинового рецептора, часткові агоністи α7 нікотинового рецептора, позитивні алостеричні модулятори α7 нікотинового рецептора, інгібітори ФДЕ2, інгібітори ФДЕ4, інгібітори ФДЕ5, інші інгібітори ФДЕ, блокатори кальцієвих каналів, модулятори m1 і m2 мускаринових рецепторів, модулятори рецептора аденозину, ампакіни, інгібітори транспортеру гліцину 1 типу, модулятори NMDA-рецепторів, модулятори mGlu-рецепторів, модулятори дофаміну, модулятори серотоніну, селективні інгібітори зворотного захоплення серотоніну, інгібітори зворотного захоплення серотоніну і норепінефрину, інгібітори зворотного захоплення норепінефрину і дофаміну, потрійні інгібітори зворотного захоплення, модулятори канабіноїдів і інгібітори холінестерази (наприклад, донепізил, ривастигмін і галантамін)]. В таких комбінаціях, кожний активний інгредієнт може бути введений або згідно з їх звичайним діапазоном доз, або дозою, що є нижчою від їх звичайного діапазону доз, і може бути введений або одночасно або послідовно. Лікарські засоби, прийнятні для використання у комбінації з кристалічною формою, згідно з представленим винаходом, включають, але не обмежуються ними, інші прийнятні лікарські засоби проти шизофренії, такі як Галоперидол, Клозапін, Оланзапін, Рисперидон, Арипіпразол, Зипрасидон, Паліперидон і Кветіапіну фумарат; лікарські засоби проти біполярного розладу, включаючи, але не обмежуючись ними, Літій, Оланзапін, Арипіпразол і Вальпроєву кислоту; лікарські засоби проти хвороби Паркінсона, включаючи, але не обмежуючись ними, Леводопу, Бромкриптин, Перголід, Праміпексол, Толкапон, Проциклідин, Тригексифенідил і Бензатропін; засоби, використовувані у лікуванні великої депресії, включаючи, але не обмежуючись ними, Амітриптилін, Протриптилін, Дезіпрамін, Нортриптилін, Пароксетин, Флуоксетин, Сертралін, Бупропіон, Есциталопрам, Міртазапін, Венлафаксин, Дулоксетин; засоби, використовувані у лікуванні хвороби Альцгеймера, включаючи, але не обмежуючись ними, Галантамін, Такрин, Донепезил, Ривастигмін, Мемантин, Неотропін, Селегілін, Естроген і Йодхінол; засоби використовувані у лікуванні деменції, включаючи, але не обмежуючись ними, Тіоридазин, Галоперидол, Римперидон, Такрин, Донепезил і Ривастигмін; засоби, використовувані у лікуванні епілепсії, включаючи, але не обмежуючись ними, Фенітоїн, Фенобарбітал, Карбамазепін, Вальпроєву кислоту, Етосуксимід, Габапентин, Фенобарбітал, Солфетон і Фелбатол; засоби, використовувані у лікуванні розсіяного склерозу, включаючи, але не обмежуючись ними, Толтеродин, Оксибутинін, Оксикодон, Інтерферон β-1b, Інтерферон β-1a, Азатіоприн, Метотрексат і Глатирамер; засоби використовувані у лікуванні хвороби Хантінгтона, включаючи, але не обмежуючись ними, Амітриптилін, Протриптилін, Дезіпрамін, Нортриптилін, Пароксетин, Флуоксетин, Сертралін, Тетрабеназин, Галоперидол, Хлорпрмазин, Тіоридазин, Сульпірид, Кветіапін, Клозапін і Рисперидон; засоби, використовувані у лікуванні діабету, включаючи, але не обмежуючись ними, ліганди PPAR (наприклад, агоністи, антагоністи, такі як Росиглітазон, Троглітазон і Піоглітазон), засіб, що підсилює секрецію інсуліну (наприклад, засоби на основі сульфонілсечовини, такі як Глібурид, Глімеперид, Хлорпропамід, Толбутамід і Гліпізид і засоби, що не містять сульфонілсечовини), інгібітори α-глюкозидази (наприклад, Акарбоза, Міглітол і Воглібоза), підсилювачі чутливості рецепторів до інсуліну (такі як агоністи PPAR-γ, наприклад, глітазони; бігуаніди, інгібітори PTP-1B, інгібітори DPP-IV і інгібітори 11βHSD), сполуки, що знижують утворення глюкози печінкою (такі як антагоністи глюкагону і метформін, наприклад, Глюкофаг і Глюкофаг XR), інсулін і похідні інсуліну (обидві форми тривалої та короткочасної активності, та композиції інсуліну); і лікарські засоби проти ожиріння, включаючи, але не обмежуючись ними, агоністи β-3, агоністи CB-1, інгібітори нейропептиду Y5, Ціліарний Нейротрофічний Фактор і похідні (наприклад, аксокін), пригнічувачі апетиту (наприклад, Сибутрамін) і інгібітори ліпази (наприклад, Орлістат). Форма введення супутніх лікарських засобів з кристалічною формою, згідно з представленим винаходом, спеціальним чином не обмежується, і є прийнятною за умов, що 11 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 60 кристалічну форму, згідно з представленим винаходом, комбінують з супутніми лікарськими засобами під час введення. Приклади таких форм введення є наступними: (1) введення єдиного препарату, одержаного шляхом виготовлення рецептури, яка одночасно включає кристалічну форму, згідно з представленим винаходом, і супутній лікарський засіб, (2) одночасне введення двох видів препаратів, одержаних шляхом окремого виготовлення кристалічної форми, згідно з представленим винаходом, і супутнього лікарського засобу, при використанні ідентичного шляху введення, (3) введення в різні проміжки часу двох видів препаратів, одержаних шляхом окремого виготовлення кристалічної форми, згідно з представленим винаходом, і супутнього лікарського засобу, при використанні ідентичного шляху введення, (4) одночасне введення двох видів препаратів, одержаних шляхом окремого виготовлення кристалічної форми, згідно з представленим винаходом, і супутнього лікарського засобу, при використанні різних шляхів введення, (5) введення в різні проміжки часу двох видів препаратів, одержаних шляхом окремого виготовлення кристалічної форми, згідно з представленим винаходом, і супутнього лікарського засобу при використанні різних шляхів введення (наприклад, введення у наступному порядку: кристалічна форма, згідно з представленим винаходом, а потім супутній лікарський засіб, або введення у зворотному порядку. Ці форми введення узагальнюються нижче і вводиться наступне скорочення, таке як: препарат комплексної терапії, згідно з представленим винаходом. У випадку призначення препарату комплексної терапії, згідно з представленим винаходом, супутній лікарський засіб і кристалічна форма, згідно з представленим винаходом, можуть вводитись одночасно, альтернативно спочатку може вводитись супутній лікарський засіб, а потім може бути введена кристалічна форма, згідно з представленим винаходом, або спочатку може вводитись кристалічна форма, згідно з представленим винаходом, а потім може бути введений супутній лікарський засіб. При введенні у різні проміжки часу, різниця у часі введення змінюється в залежності від використовуваного активного інгредієнта, лікарської форми та способу введення. Наприклад, коли спочатку вводять супутній лікарський засіб, кристалічна форма, згідно з представленим винаходом, може бути введена протягом проміжку часу від 1 хв. до 3 днів, переважно у проміжку від 10 хв. до 1 дня і більш переважно у проміжку від 15 хв. до 1 години після введення супутнього лікарського засобу. Однак, якщо спочатку вводять кристалічну форму, згідно з представленим винаходом, супутній лікарський засіб може бути введений протягом від 1 хв. до 1 дня, переважно у проміжку від 10 хв. до 6 годин і більш переважно у проміжку від 15 хв. до 1 години після введення кристалічної форми, згідно з представленим винаходом. Якщо не виникає проблем, пов'язаних з побічними ефектами супутніх лікарських засобів, можуть встановлюватись будь-які дозування. Добова доза щодо супутнього лікарського засобу залежить від режиму дозування, суб'єкта введення, шляху введення, захворювання, що піддають лікуванню, симптомів і т.д… Наприклад, у випадку перорального введення у пацієнтів з шизофренією (дорослих людей, з масою тіла орієнтовно 60 кг), діапазони нормальної добової дози складають від приблизно 0,1 до приблизно 20 мг/кг маси тіла, переважно від приблизно 0,2 до приблизно 10 мг/кг маси тіла і більш переважно від приблизно 0,5 до приблизно 10 мг/кг маси тіла. Перевага надається введенню цієї дози від одного разу на добу до декількох разів на добу (наприклад, 3 рази). Якщо кристалічну форму, згідно з представленим винаходом, використовують у комбінації з супутнім лікарським засобом, відповідний режим дозування, з міркувань усунення протилежних ефектів відповідних лікарських засобів, може бути знижений в межах безпечного діапазону. Препарат комплексної терапії, згідно з представленим винаходом, демонструє низьку токсичність. Наприклад, кристалічна форма, згідно з представленим винаходом, та/або вищезазначений супутній лікарський засіб можуть бути скомбіновані з фармацевтично прийнятним носієм відповідно до відомого способу, з одержанням фармацевтичної композиції, такої як таблетки (включаючи таблетки з цукровим покриттям і таблетки з плівковим покриттям), порошкоподібні засоби, гранули, капсули (включаючи м'які капсули), рідини, ін'єкційні розчини, супозиторії, засоби пролонгованого вивільнення і т.д… Ці композиції можуть бути безпечно введені оральним або не оральним шляхом (наприклад, включаючи місцевий, ректальний і внутрішньовенний шляхи). Фармацевтично прийнятними носіями, які можуть використовуватись для виробництва препарату комплексної терапії, згідно з представленим винаходом, можуть бути ті ж самі, що використовувались у фармацевтичній композиції, згідно з представленим винаходом, як було зазначено вище. 12 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 60 Співвідношення у суміші між кристалічною формою, згідно з представленим винаходом, і супутнього лікарського засобу у препараті комплексної терапії, згідно з представленим винаходом, може вибиратись відповідним чином у залежності від суб'єкта введення, шляхів введення і типу захворювання. Визначені вище супутні лікарські засоби, можуть комбінуватись у відповідному співвідношенні, якщо поєднуються два або декілька лікарських засобів. Дозування лікарського засобу може вибиратись відповідним чином на основі режиму дозування, використовуваного у клінічній практиці. Крім того, співвідношення у суміші між кристалічною формою, згідно з представленим винаходом, і супутнім лікарським засобом може вибиратись відповідним чином у залежності від суб'єкта введення, шляхів введення, типу захворювання, симптомів, комбінацій і т.д… Наприклад, якщо суб'єктом введення є людина, супутній лікарський засіб може використовуватись у кількісному діапазоні від 0,01 до 100 мас. частин по відношенню до 1 мас. частини кристалічної форми, згідно з представленим винаходом. Наприклад, вміст кристалічної форми, згідно з представленим винаходом, у препараті комплексної терапії, згідно з представленим винаходом, змінюється в залежності від форми препаратів. Загалом, її вміст знаходиться у діапазоні від приблизно 0,01 до 99,9 мас. %, переважно від приблизно 0,1 до 50 мас. % і більш переважно від приблизно 0,5 до 20 мас. % відносно загальної маси препарату. Вміст супутнього лікарського засобу у препараті комплексної терапії, згідно з представленим винаходом, змінюється в залежності від форми препаратів. Загалом, його вміст знаходиться у діапазоні від приблизно 0,01 до 99,9 мас. %, переважно від приблизно 0,1 до 50 мас. % і більш переважно від приблизно 0,5 до 20 мас. % відносно загальної маси препарату. Вміст добавки, такої як носії у препараті комплексної терапії, згідно з представленим винаходом, змінюється в залежності від форми препаратів. Загалом, їх вміст знаходиться у діапазоні від приблизно 1 до 99,99 мас. % і переважно від приблизно 10 до 90 мас. % відносно загальної маси препарату. Коли кристалічна форма, згідно з представленим винаходом, і супутній лікарський засіб виготовляються окремо, може застосовуватись ідентичний вміст. Оскільки режими дозування можуть коливатись за різних умов, як визначено вище, може бути достатнім режим дозування менший, ніж зазначені вище режими дозування, або може виникнути необхідність призначення дозування, що перевищує діапазон. Приклади Представлений винахід детально пояснюється посиланням на наступні Допоміжні приклади, Приклади, Приклади одержання і Експериментальні приклади. Ці приклади є тільки варіантами, які не обмежують представлений винахід, і можуть бути модифіковані в межах діапазону, що не виходить за рамки представленого винаходу. "Кімнатна температура" в наступних Допоміжних прикладах і Прикладах становить загалом від 10C до приблизно 35C. % у виході означає моль/моль%, % розчинника, використовуваного для хроматографії, означає об. %, і % використовуваний для іншого, означає мас. %. У спектрі протонного ЯМР, OH і NH протони і т. п., які не можуть бути ідентифіковані, оскільки вони мають широкі смуги, не реєструються у даних. У хроматографії на силікагелі, використовувався силікагель 60 (230-400 меш), виробництва Merk & Co., Inc., і амінопропілсилан-зв'язаний силікагель (Chromatorex NH, виробництва Fuji Silysia Chemical Ltd.) використовувався для хроматографії на основному силікагелі, описаний як "NH силікагель". Інші скорочення, використовувані у тексті, означають наступне. с: синглет д: дублет дд: дублет дублетів дт: дублет триплетів т: триплет тт: триплет триплетів тд: триплет дублетів к: квартет с: септет м: мультиплет ш: широкий J: константа спін-спінової взаємодії Гц: Герц CDCl3: дейтерований хлороформ 13 UA 112082 C2 5 10 15 20 25 30 35 ДМСО-d6: дейтерований диметилсульфоксид 1 H ЯМР: протонний ядерний магнітний резонанс ВЕРХ: високоефективна рідинна хроматографія ТГФ: тетрагідрофуран DMF: N, N-диметилформамід ДМСО: диметилсульфоксид ІПЕ: ізопропіловий етер DMA: N, N-диметилацетамід DIPEA: N, N-діізопропілетиламін Pd2(dba)3: тріс(дибензиліденацетон)дипаладій(0) РХ-МС: спектр рідинної хроматографічної-мас-спектрометрії ESI: метод мас-спектрометрії з іонізацією електророзпиленням API: метод мас-спектрометрії з хімічною іонізацією при атмосферному тиску Всі реагенти і розчинники були комерційної якості і використовувались без додаткового очищення. Сполуки та/або проміжні сполуки очищували за допомогою препаративної високоефективної рідинної хроматографії (преп. ВЕРХ), з використанням системи очищення Gilson High through Put. Використовували колонки для обернено-фазової хроматографії YMC CombiPrep Pro C18, S5 мкм, 19 × 50 мм. Використовували градієнтне елюювання (швидкість потоку 20 мл/хв.), типово починаючи з суміші 5 % ацетонітрил/95 % вода і з досяганням до 100 % ацетонітрилу протягом періоду 7 хвилин. Всі розчинники містили 0,1 % трифтороцтову кислоту (ТФК). Мас-спектрометричний аналіз здійснювали відповідно до методів рідинної хроматографії/мас-спектрометрії (РХ-МС). У методі застосовували систему Waters РХ-МС (Agilent HP1100 ВЕРХ і мас-спектрометр Micromass ZMD для інструмента РХ-МС, CAPCELL PAK C18, UG120, S-3 мкм, 1,5 × 35 мм хроматографічної колонки), і систему розчинників, яка являла собою 5-95 % градієнт ацетонітрилу у воді з 0,04 % ТФК (швидкість потоку 0,5 мл/хв.; діапазон молекулярної маси 200-800; напруга на конусі 20 В; температура в колонці 40C). Всі маси наведені як маси протонованих родоначальних іонів. Аналіз порошкової рентгенівської дифракції здійснювали, використовуючи RINT Ultima-IV (виробництва Rigaku Corporation). Диференційну скануючу калориметрію (ДСК) здійснювали, використовуючи калориметр для диференційної скануючої калориметрії (ДСК1 (виробництва Mettler-Toledo)) при швидкості підвищення температури 5C/хв., в діапазоні температур 25C-240C. Нагрівання здійснювали, використовуючи термоблок (виробництва TAITEC Co., Ltd.). Допоміжний приклад 1-1 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) a) 3-[4-(бензилокси)феніл]-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он 40 45 50 Суміш трет-бутил (2-хлор-4-метилпіридин-3-іл)карбамату (2,00 г), гідрохлориду 4(бензилокси)аніліну (2,91 г), 9,9-диметил-4,5-біс(дифенілфосфіно)ксантену (381 мг), третбутоксиду натрію (1,90 г) і Pd2(dba)3 (302 мг) у 2-пропанолі (6 мл) і толуолі (24 мл) перемішували в атмосфері азоту при 100C протягом 24 годин. Реакційну суміш концентрували при пониженому тиску. Залишок розчиняли у метанолі і осад відфільтровували. Фільтрат концентрували і залишок очищували за допомогою колонкової хроматографії (NH силікагель, елюйований 15 % - 50 % етилацетатом у гексані), одержуючи 3-[4-(бензилокси)феніл]-7-метил1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (988 мг), у вигляді безбарвної твердої речовини. МС (API+): [M+H]+ 332,3. 1 H ЯМР (300 МГц, CDCl3) δ 2,39 (3H, с), 5,12 (2H, с), 6,87 (1H, д, J=5,3 Гц), 7,12 (2H, д, J=9,0 Гц), 7,28-7,50 (5H, м), 7,57 (2H, д, J=8,7 Гц), 7,96 (1H, д, J=5,3 Гц), 9,93 (1H, шс). b) 3-[4-(бензилокси)феніл]-1-етил-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он 14 UA 112082 C2 5 10 15 До суміші 3-[4-(бензилокси)феніл]-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (998 мг) і карбонату цезію (1,96 г) у ДМФ (10 мл) додавали йодетан (0,289 мл) при кімнатній температурі. Суміш перемішували при 50C протягом 4 годин. Суміш розбавляли водою при кімнатній температурі і суміш екстрагували етилацетатом. Органічний шар відокремлювали, промивали водою і сольовим розчином, сушили над сульфатом магнію і потім концентрували при пониженому тиску. Залишок очищували за допомогою колонкової хроматографії (силікагель, елюйований 15 % - 30 % етилацетатом у гексані), одержуючи 3-[4(бензилокси)феніл]-1-етил-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (801 мг), у вигляді твердої речовини білого кольору. МС (API+): [M+H]+ 360.4. 1 H ЯМР (300 МГц, CDCl3) δ 1,41 (3H, т, J=7,2 Гц), 2,61 (3H, с), 4,19 (2H, к, J=7,2 Гц), 5,11 (2H, с), 6,81 (1H, д, J=5,3 Гц), 7,10 (2H, д, J=8,7 Гц), 7,30-7,47 (5H, м), 7,53 (2H, д, J=9,1 Гц), 7,91 (1H, д, J=5,3 Гц). c) 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2Hімідазо[4,5-b]піридин-2-он 20 25 30 35 40 45 Суміш 3-[4-(бензилокси)феніл]-1-етил-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (800 мг) і 10 % Pd-C (118 мг) у етанолі (20 мл) гідрували протягом ночі з використанням балонного водню при кімнатній температурі. Каталізатор відфільтровували і фільтрат концентрували у вакуумі, одержуючи 1-етил-3-(4-гідроксифеніл)-7-метил-1,3-дигідро-2Hімідазо[4,5-b]піридин-2-он, у вигляді безбарвної твердої речовини. До суміші одержаної твердої речовини і 3-метил-2-(метилсульфоніл)-3H-імідазо[4,5-b]піридину (480 мг) у ДМФ (10 мл) додавали 60 % гідрид натрію (58,9 мг) при 100C. Суміш нагрівали при мікрохвильовому випромінюванні при 180C протягом 30 хв. Реакційну суміш розбавляли метанолом і концентрували у вакуумі. Залишок очищували за допомогою колонкової хроматографії (NH силікагель, елюйований 30 % - 50 % етилацетатом у гексані, і силікагель, елюйований 15 % 30 % етилацетатом у гексані). Неочищену речовину очищували за допомогою ВЕРХ (C18, елюйований сумішшю вода/ацетонітрил, що містить 0,1 % трифтороцтову кислоту). До одержаного розчину додавали водний насичений гідрокарбонат натрію і суміш екстрагували етилацетатом. Екстракт сушили над сульфатом магнію і потім концентрували у вакуумі, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро2H-імідазо[4,5-b]піридин-2-он (119 мг), у вигляді безбарвних кристалів (Форма A). МС (API+): [M+H]+ 401,3. Допоміжний приклад 1-2 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) a) 1-етил-3-(4-гідроксифеніл)-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он Суміш 3-[4-(бензилокси)феніл]-1-етил-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (21,4 г) і 10 % Pd-C (3,17 г) у етанолі (400 мл) гідрували з використанням балонного водню при 15 UA 112082 C2 5 кімнатній температурі протягом 2 годин. Каталізатор відфільтровували і фільтрат концентрували у вакуумі. Тверду речовину промивали сумішшю ТГФ-гексан, одержуючи 1-етил3-(4-гідроксифеніл)-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (10,90 г), у вигляді твердої речовини. МС (API+): [M+H]+ 270,4. b) 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2Hімідазо[4,5-b]піридин-2-он 10 15 20 25 До розчину 3-метил-2-(метилсульфоніл)-3H-імідазо[4,5-b]піридину (1,0 г) і 1-етил-3-(4гідроксифеніл)-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (1,3 г) у ДМФ (10 мл) додавали 60 % гідрид натрію (0,23 г) при кімнатній температурі і суміш перемішували при мікрохвильовому випромінюванні, при 180C протягом 30 хв. До суміші додавали етанол (10 мл). Утворені кристали збирали за допомогою фільтрування і промивали етанолом. Цю реакцію під дією мікрохвильового випромінювання повторювали додатково два рази, використовуючи однакову кількість вихідних матеріалів. Об'єднані кристали перекристалізовували з етанолу, що містить 5 % дистильованої води (270 мл) і сушили при пониженому тиску, одержуючи 1-етил-7метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5b]піридин-2-он (3,3 г), у вигляді білих кристалів (Форма A). МС (API+): [M+H]+ 401,3. 1 H ЯМР (300 МГц, ДМСО-d6) δ 1,32 (3H, т, J=7,2 Гц), 2,61 (3H, с), 3,77 (3H, с), 4,12 (2H, к, J=7,2 Гц), 7,00 (1H, д, J=5,7 Гц), 7,20 (1H, дд, J=7,9, 4,9 Гц), 7,58-7,66 (2H, м), 7,71-7,78 (2H, м), 7,80 (1H, дд, J=7,9, 1,1 Гц), 7,87 (1H, д, J=4,9 Гц), 8,22 (1H, дд, J=4,9, 1,5 Гц). Ел. аналіз разрахов. для C22H20N6O2: C, 65,99; H, 5,03; N, 20,99. Знайдено: C, 65,76; H, 5,07; N, 20,85. Результати вимірювання порошкової рентгенівської дифракції кристалів Форми A, одержаних у Допоміжному прикладі 1-1 наведені у наступних Таблиці 1 і Фіг. 1. Таблиця 1 Дані порошкової рентгенівської дифракції (кристали форми A) 0) 2θ( 7,88 9,5 10,9 14,06 14,58 15,74 16,14 16,76 18,3 19,6 20,3 21,22 21,84 22,3 22,76 23,72 24,68 25,36 26,32 27,1 27,7 значення d (Å) 11,2103 9,302 8,1102 6,2937 6,0704 5,6255 5,487 5,2854 4,8439 4,5255 4,371 4,1835 4,0661 3,9833 3,9038 3,7479 3,6043 3,5092 3,3833 3,2877 3,2178 16 відносна інтенсивність (%) 5 26 38 8 11 67 22 10 81 6 61 6 12 10 14 19 58 23 11 6 100 UA 112082 C2 Продовження таблиці 1 28,36 29,94 30,48 30,9 31,7 32,84 33,14 33,94 5 10 3,1444 2,982 2,9304 2,8915 2,8203 2,725 2,701 2,6391 12 3 3 5 5 3 3 4 Допоміжний приклад 2 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма B) Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) (20 мг, 0,05 ммоль), одержані у Допоміжному прикладі 1-1, змішували з ацетонітрилом (3 мл) і розчиняли при температурі всередині 60C. Одержаний розчин фільтрували через фільтр з розміром пор 0,22 мкм і охолоджували до 0-5C, перемішуючи. Суміш перемішували протягом 8 годин в охолодженому стані при температурі 05C. Кристали збирали за допомогою фільтрування, одержуючи 1-етил-7-метил-3-{4-[(3-метил3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (кристали Форми B). Результати вимірювання порошкової рентгенівської дифракції одержаних кристалів наведені у наступній Таблиці 2 і Фіг. 2. 15 Таблиця 2 Дані порошкової рентгенівської дифракції (кристали форми B) 0) 2θ( 4,82 5,12 5,6 5,7 6,08 9,26 9,62 10,22 11,34 11,36 11,92 15,7 15,9 17,18 18,64 22,88 24,58 24,72 25 26,02 29,86 29,98 30,1 30,26 значення d (Å) 18,3182 17,2455 15,7684 15,492 14,5245 9,5425 9,1862 8,6482 7,7965 7,7828 7,4184 5,6398 5,5693 5,1571 4,7563 3,8836 3,6187 3,5985 3,5589 3,4216 2,9898 2,9781 2,9665 2,9512 відносна інтенсивність (%) 37 19 12 11 7 20 17 13 96 100 23 5 5 4 6 12 7 11 5 6 6 6 5 7 Допоміжний приклад 3 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма D) 17 UA 112082 C2 5 Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) (20 мг, 0,05 ммоль), одержані у Допоміжному прикладі 1-1, змішували з трифторетанолом (0,5 мл) і розчиняли при кімнатній температурі. Трифторетанол випаровували в умовах потоку азоту під час охолодження до 0-5C. Кристали збирали за допомогою фільтрування, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (кристали Форми D). Результати вимірювання порошкової рентгенівської дифракції одержаних кристалів наведені у наступній Таблиці 3 і Фіг. 3. Таблиця 3 Дані порошкової рентгенівської дифракції (кристали форми D) 0) 2θ( 5,72 11,52 11,96 12,4 15,62 16,26 16,52 19,28 23,26 24,18 24,56 24,68 25,54 26,28 26,5 28,14 29,82 29,92 30,2 31,18 значення d (Å) 15,4378 7,675 7,3937 7,1323 5,6685 5,4468 5,3616 4,5999 3,821 3,6777 3,6216 3,6043 3,4848 3,3884 3,3607 3,1685 2,9937 2,9839 2,9569 2,8661 відносна інтенсивність (%) 12 100 13 24 14 8 11 7 18 29 11 10 10 13 18 10 8 79 4 10 15 20 Допоміжний приклад 4 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма E) Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) (20 мг, 0,05 ммоль), одержані у Допоміжному прикладі 1-1, змішували з ацетоном (4 мл) і розчиняли при температурі всередині 50C. Одержаний розчин фільтрували через фільтр з розміром пор 0,22 мкм, додавали воду (3 мл), нагріту до 50C, і охолоджували до температури 0-5C, перемішуючи. Суміш перемішували протягом 8 годин в охолодженому стані при температурі 0-5C. Кристали збирали за допомогою фільтрування, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (кристали Форми E). Результати вимірювання порошкової рентгенівської дифракції одержаних кристалів наведені у наступній Таблиці 4 і Фіг. 4. Таблиця 4 Дані порошкової рентгенівської дифракції (кристали форми E) 2 θ () 5,64 11,32 11,9 15,4 17,02 Значення d (Å) 15,6566 7,8102 7,4308 5,749 5,2052 18 Відносна інтенсивність (%) 15 100 4 1 3 UA 112082 C2 Продовження таблиці 4 20,06 20,32 22,76 23,92 24,5 25,52 26,04 28,6 29,96 30,26 30,9 34,48 5 10 4,4227 4,3667 3,9038 3,7171 3,6304 3,4875 3,419 3,1186 2,98 2,9512 2,8915 2,599 1 1 4 1 1 2 1 1 3 2 2 2 Допоміжний приклад 5 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма F) Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) (20 мг, 0,05 ммоль), одержані у Допоміжному прикладі 1-1, змішували з 2-пропанолом (10 мл) і розчиняли при температурі всередині 60C. Одержаний розчин фільтрували через фільтр з розміром пор 0,22 мкм, додавали н-гептан (10 мл), нагрітий до 60C, і охолоджували до температури 0-5C, перемішуючи. Суміш перемішували протягом 8 годин в охолодженому стані при температурі 0-5C. Кристали збирали за допомогою фільтрування, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (кристали Форми F). Результати вимірювання порошкової рентгенівської дифракції одержаних кристалів наведені у наступній Таблиці 5 і Фіг. 5. 15 Таблиця 5 Дані порошкової рентгенівської дифракції (кристали форми F) 0) 2θ( 7,38 10,42 14,32 14,86 16,56 20,92 20,98 22,28 23,5 23,78 25,5 25,98 26,82 27,62 31,66 33,44 20 значення d (Å) 11,9687 8,4827 6,18 5,9566 5,3488 4,2428 4,2308 3,9868 3,7825 3,7386 3,4902 3,4268 3,3214 3,2269 2,8238 2,6774 відносна інтенсивність (%) 5 100 3 2 3 6 5 2 6 4 2 2 18 2 12 2 Допоміжний приклад 6 Кристалічна форма гідрату змінного складу 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма H) Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) (20 мг, 0,05 ммоль), одержані у Допоміжному прикладі 1-1, змішували з сумішшю ацетонітрил/вода (9:1) (1 мл) і суміш перемішували при кімнатній температурі протягом тижня. Кристали збирали за допомогою фільтрування, одержуючи гідрат змінного складу 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2 19 UA 112082 C2 іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (вміст води гідрату змінного складу змінювався у межах діапазону від приблизно 4 до приблизно 14 мас. %) (кристали Форми H). Результати вимірювання порошкової рентгенівської дифракції одержаних кристалів наведені у наступній Таблиці 6 і Фіг. 6. 5 Таблиця 6 Дані порошкової рентгенівської дифракції (кристали форми H) 0) 2θ( 6,06 7,9 9,24 10,96 15,86 16,2 17,14 17,76 18,62 20,42 24,04 24,8 26,54 27,2 27,54 29,28 29,6 31,46 33,48 10 15 значення d (Å) 14,5724 11,182 9,5631 8,0659 5,5832 5,4668 5,1691 4,99 4,7614 4,3456 3,6988 3,5871 3,3558 3,2758 3,2361 3,0477 3,0154 2,8413 2,6743 відносна інтенсивність (%) 23 4 18 28 29 5 5 4 9 12 8 100 29 24 6 3 9 6 5 Допоміжний приклад 7 Кристалічна форма моногідрату 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма I) Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) (20 мг, 0,05 ммоль), одержані у Допоміжному прикладі 1-1, змішували з сумішшю етанол/вода (9:1) (1 мл) і суміш перемішували при кімнатній температурі протягом тижня. Кристали збирали за допомогою фільтрування, одержуючи моногідрат 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро2H-імідазо[4,5-b]піридин-2-ону (кристали Форми I). Результати вимірювання порошкової рентгенівської дифракції одержаних кристалів наведені у наступній Таблиці 7 і Фіг. 7. Таблиця 7 Дані порошкової рентгенівської дифракції (кристали Форми I) 0) 2θ( 8,24 10,6 11,44 12,64 13,72 13,94 14,7 15,64 17,68 18,46 18,96 20,62 значення d (Å) 10,7213 8,339 7,7285 6,9974 6,4489 6,3476 6,0211 5,6613 5,0124 4,8023 4,6768 4,3039 20 відносна інтенсивність (%) 11 41 33 5 17 12 16 50 20 31 6 19 UA 112082 C2 Продовження таблиці7 20,92 22,62 22,92 23,16 24,5 25,52 26,1 27,72 29,6 29,78 5 10 15 20 25 30 35 40 45 4,2428 3,9277 3,8769 3,8373 3,6304 3,4875 3,4113 3,2155 3,0154 2,9976 6 12 8 5 10 100 37 42 8 22 Приклад 1 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G) (1) Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A: 100 мг) розчиняли у етанолі (20 мл) при 80C і розчин залишали охолоджуватись до кімнатної температури. Суміш перемішували при кімнатній температурі протягом 350 годин. Тверді речовини збирали за допомогою фільтрування, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро2H-імідазо[4,5-b]піридин-2-он (50 мг), у вигляді кристалів (Форма G). (2) Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A: 40,0 г) розчиняли у ДМСО (400 мл) при 95C і розчин залишали охолоджуватись до 85C. До розчину повільно додавали етанол (400 мл) при 85C і суміш залишали охолоджуватись до 80C. До розчину додавали затравку кристалу (Форма G, 50 мг) при 80C. Суміш перемішували і тримали при температурі 73C протягом 20 годин. Тверді речовини збирали за допомогою фільтрування і промивали етанолом (500 мл), одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро2H-імідазо[4,5-b]піридин-2-он (19,5 г), у вигляді білих кристалів (Форма G). Приклад 2 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G) Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A: 600 мг) перемішували у етанолі (60 мл) при кімнатній температурі протягом 168 годин. Тверді речовини збирали за допомогою фільтрування, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (350 мг), у вигляді кристалів (Форма G). МС (API+): [M+H]+ 401,1. 1 H ЯМР (400 МГц, ДМСО-d6) δ 1,25-1,38 (3H, м), 2,61 (3H, с), 3,78 (3H, с), 4,04-4,18 (2H, м), 6,96-7,04 (1H, м), 7,17-7,25 (1H, м), 7,59-7,66 (2H, м), 7,71-7,77 (2H, м), 7,78-7,83 (1H, м), 7,857,91 (1H, м), 8,16-8,28 (1H, м). Ел. анал. розрахов. для C22H20N6O2: C, 65,99; H, 5,03; N, 20,99. Знайдено: C, 65,73; H, 5,12; N, 20,85. Приклад 3 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G) Кристали (3,0 г) 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону, одержані у Прикладі 7 a) розчиняли у ДМСО (33 мл) при 90C. До розчину повільно додавали етанол (30 мл) при 80-90C. Кристал (Форма G), одержаний у Прикладі 2 додавали як затравку кристалу при температурі 80-90C. Суміш перемішували при 60-65C протягом 6 годин і при кімнатній температурі протягом 18 годин. Тверді речовини збирали за допомогою фільтрування і промивали етанолом (15 мл), одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро2H-імідазо[4,5-b]піридин-2-он (1,3 г), у вигляді білих кристалів (Форма G). Приклад 4 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G) 21 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 Кристали (3,0 г) 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону, одержані у Прикладі 7 a) розчиняли у ДМСО (33 мл) при 90-95C. До розчину повільно додавали етилацетат (30 мл) при температурі 70-90C. Кристал (Форма G), одержаний у Прикладі 3, додавали як затравку кристалу при 80-90C. Суміш перемішували при 45-50C протягом 25 хв. і при 70-75C протягом 3 годин. Суміш охолоджували до 0-5C і перемішували протягом 1 години. Тверді речовини збирали за допомогою фільтрування і промивали етилацетатом (15 мл), одержуючи 1-етил-7-метил-3-{4[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (2,6 г), у вигляді кристалів (Форма G). Приклад 5 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G) Розчин 3-метил-2-(метилсульфоніл)-3H-імідазо[4,5-b]піридину (20,4 г, 96,55 ммоль) у DMA (117 мл) додавали до розчину 1-етил-3-(4-гідроксифеніл)-7-метил-1,3-дигідро-2H-імідазо[4,5b]піридин-2-ону (26,0 г, 96,55 ммоль) і трет-бутоксиду калію (11,4 г) у DMA (96 мл) при кімнатній температурі. Суміш перемішували при 95-100C протягом 1,5 годин. Додавали воду (221 мл) при температурі 80-100C. Осад збирали при кімнатній температурі і сушили при пониженому тиску, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-он (35,8 г), у вигляді неочищеного продукту. Неочищений 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-он (10,0 г) розчиняли у ДМСО (150 мл) при 90-100C. Розчин фільтрували через паперовий фільтр і промивали, використовуючи ДМСО (10 мл). Об'єднаний фільтрат повільно додавали до суміші кристалів (Форма G: 100 мг) (як затравку кристалу), одержаних у Прикладі 4, у етилацетаті (100 мл) при 5-30C. Суміш перемішували при кімнатній температурі протягом 17 годин і при 70C протягом 1 години. Суміш повільно охолоджували до 25C і перемішували протягом 2 годин. Суміш перемішували при 0-10C протягом 1 години і при кімнатній температурі протягом 1 години. Тверді речовини збирали за допомогою фільтрування і сушили при пониженому тиску при 50C, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3Hімідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (8,0 г), у вигляді білих кристалів (Форма G). Приклад 6 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G) Розчин 3-метил-2-(метилсульфоніл)-3H-імідазо[4,5-b]піридину (40,8 г, 193,09 ммоль) у DMA (234 мл) додавали до розчину 1-етил-3-(4-гідроксифеніл)-7-метил-1,3-дигідро-2H-імідазо[4,5b]піридин-2-ону (52,0 г, 193,09 ммоль) і трет-бутоксиду калію (22,8 г) у DMA (192 мл) при кімнатній температурі. Суміш перемішували при 90-100C протягом 1 години. Додавали воду (442 мл) при температурі 80-100C. Осад збирали при кімнатній температурі і сушили при пониженому тиску, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (72,4 г), у вигляді неочищеного продукту. Неочищений 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-он (60,0 г) розчиняли у ДМСО (900 мл) при 90-100C. Розчин фільтрували через паперовий фільтр і промивали, використовуючи ДМСО (60 мл). Об'єднаний фільтрат повільно додавали до суміші кристалів (Форма G: 600 мг) (як затравку кристалу), одержаних у Прикладі 5, у етилацетаті (600 мл) при 0-30C. Суміш перемішували при 70C протягом 0,5 годин і охолоджували до кімнатної температури. Суміш перемішували при кімнатній температурі протягом 1 години, при 0-10C протягом 1 години і при кімнатній температурі протягом 1 години. Тверді речовини збирали за допомогою фільтрування і сушили при пониженому тиску при 50C, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (47,9 г), у вигляді білих кристалів (Форма G). МС (ESI+): [M+H]+ 401,2. 1 H ЯМР (500 МГц, CDCl3) δ 1,42 (3H, т), 2,62 (3H, с), 3,84 (3H, с), 4,15-4,27 (2H, м), 6,81-6,92 (1H, м), 7,10-7,18 (1H, м), 7,52-7,61 (2H, м), 7,73-7,80 (1H, м), 7,82-7,87 (2H, м), 7,91-7,95 (1H, м), 8,20-8,29 (1H, м). Приклад 7 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G) 22 UA 112082 C2 5 10 15 20 25 30 35 40 45 50 55 a) Розчин 3-метил-2-(метилсульфоніл)-3H-імідазо[4,5-b]піридину (78,4 г, 371,33 ммоль) у DMA (420 мл) додавали до розчину 1-етил-3-(4-гідроксифеніл)-7-метил-1,3-дигідро-2Hімідазо[4,5-b]піридин-2-ону (100,0 г, 371,33 ммоль) і трет-бутоксиду калію (51,5 г) у DMA (370 мл) при кімнатній температурі. Суміш перемішували при 90-100C протягом 1 години. Додавали воду (780 мл) при температурі 90-100C. Осад збирали при кімнатній температурі і сушили при пониженому тиску, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (127,7 г), у вигляді кристалів. Одержані кристали (125,0 г) розчиняли у ДМСО (1375 мл) при 90-95C. До розчину повільно додавали етанол (1250 мл) при 80-95C і суміш залишали охолоджуватись до кімнатної температури. Тверді речовини збирали за допомогою фільтрування, промивали етанолом (625 мл), одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро2H-імідазо[4,5-b]піридин-2-он (103,9 г), у вигляді кристалів. b) Суміш одержаних кристалів (55,0 г) у розчині ДМСО (275 мл) і етанолу (275 мл) перемішували при 70-75C протягом 0,5 години і суміш залишали охолоджуватись до кімнатної температури. Тверді речовини збирали за допомогою фільтрування і промивали етанолом (165 мл), одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-он (52,2 г), у вигляді кристалів. Одержані кристали (5,0 г) розчиняли у ДМСО (50 мл) при 95C. Розчин фільтрували через паперовий фільтр і промивали, використовуючи ДМСО (5 мл). До об'єднаного фільтрату повільно додавали етанол (50 мл) при 73-95C. До розчину додавали кристали, одержані у Прикладі 4 (Форма G: 5 мг), як затравочний кристал при 73C. Суміш залишали охолоджуватись до кімнатної температури. Суміш перемішували при 70-75C протягом 7 годин і залишали охолоджуватись до кімнатної температури. Суміш перемішували при 70-75C протягом 8 годин, і охолоджували до кімнатної температури. Суміш перемішували при 70-75C протягом 2 годин і суміш перемішували при кімнатній температурі протягом 1 години, і при 0-10C протягом 1 години. Тверді речовини збирали за допомогою фільтрування і сушили при пониженому тиску при 50C, одержуючи 1етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5b]піридин-2-он (4,5 г), у вигляді білих кристалів (Форма G). Приклад 8 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G) 3-Mетил-2-(метилсульфоніл)-3H-імідазо[4,5-b]піридин (8,62 г, 40,8 ммоль) додавали до суміші 1-етил-3-(4-гідроксифеніл)-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (10,0 г, 37,1 ммоль), карбонату калію (6,15 г) і води (4,25 мл) у DMA (75 мл) при кімнатній температурі. Суміш перемішували при 80-90C протягом 1 години. Додавали воду (135 мл) при температурі 45C. Осад збирали при кімнатній температурі і сушили при пониженому тиску, одержуючи 1етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5b]піридин-2-он (14,13 г), у вигляді неочищеного продукту. Неочищений 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-он (12,0 г) розчиняли у ДМСО (228 мл) при 90C. Розчин фільтрували через скляний фільтр. Фільтрат нагрівали до 90C і перемішували при 30C протягом 1 години. Додавали етанол (72 мл) і суміш перемішували протягом 1 години. Після перемішування при 60C протягом 4,5 годин, суміш охолоджували до кімнатної температури. Після перемішування при 10C протягом 4,5 годин, осад збирали і сушили при пониженому тиску, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-он (10,2 г), у вигляді білих кристалів (Форма G). Приклад 9 Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G) 3-Mетил-2-(метилсульфоніл)-3H-імідазо[4,5-b]піридин (258,9 г, 1,22 ммоль) додавали до суміші 1-етил-3-(4-гідроксифеніл)-7-метил-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону (300,0 г, 1,11 ммоль), карбонату калію (184,7 г) і води (127,5 мл) у DMA (1950 мл) при кімнатній температурі. Потім додавали DMA (300 мл) і суміш перемішували при 86-87C протягом 1 години. Додавали воду (4050 мл) при температурі 45C. Осад збирали при 25C і сушили при пониженому тиску, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (435,87 г), у вигляді неочищеного продукту. Неочищений 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-он (400,0 г) розчиняли у ДМСО (7600 мл) при 80-90C. Розчин 23 UA 112082 C2 5 10 фільтрували через скляний фільтр. Фільтрат нагрівали до 80-90C і кристали (Форма G: 4 г), одержані у Прикладі 8 додавали до розчину при 50C як затравку кристалу. Після охолодження до 30C, додавали етанол (2400 мл). Суміш нагрівали до 60-70C і охолоджували до кімнатної температури. Після перемішування при охолодженні на льоду, осад збирали і сушили при пониженому тиску, одержуючи 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-он (344,04 г), у вигляді білих кристалів (Форма G). Результати вимірювання порошкової рентгенівської дифракції кристалів Форми G, одержаних у Прикладі 1(2), наведені у наступній Таблиці 8 і Фіг. 8. Крім того, дані термічного аналізу ДСК кристалів наведені у Фіг. 9. Таблиця 8 Дані порошкової рентгенівської дифракції (кристали Форми G) 0) 2θ( 6,5 9,58 11,22 11,82 13,08 14,26 14,44 15,46 16,9 17,28 19,12 20,8 21,32 21,88 22,24 22,58 23,44 23,27 24,74 26,12 28,24 28,82 29,18 30,88 31,64 32,78 34,68 15 20 25 значення d (Å) 13,5869 9,2245 7,8796 7,4809 6,763 6,2059 6,1289 5,7268 5,2419 5,1275 4,638 4,267 4,1641 4,0588 3,9939 3,9345 3,7921 3,7479 3,5957 3,4088 3,1575 3,0953 3,0579 2,8933 2,8255 2,7298 2,5845 відносна інтенсивність (%) 8 38 82 17 25 47 49 58 12 29 45 25 16 5 30 44 100 100 15 17 5 10 20 13 6 7 7 Приклад одержання 1 (1) Кристалічна форма Прикладу 1 10,0 г (2) Лактоза 70,0 г (3) Кукурудзяний крохмаль 50,0 г (4) Розчинний крохмаль 7,0 г (5) Стеарат магнію 3,0 г Після того як 10,0 г кристалічної форми Прикладу 1 і 3,0 г стеарату магнію гранулюють у 70 мл водного розчину розчинного крохмалю (7,0 г як розчинний крохмаль) і потім сушать, одержану суміш змішують з 70,0 г лактози і 50,0 г кукурудзяного крохмалю (лактоза, кукурудзяний крохмаль, розчинний крохмаль і стеарат магнію, всі є продуктами, переліченим у Японській Фармакопеї). Суміш пресують, одержуючи таблетку. Експериментальний приклад 1 Дослідження кристалізації з різних розчинників Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) (20 мг, 0,05 ммоль), одержані у Допоміжному прикладі 1-1, витримували при 55C і додавали різні розчинники до тих пір, доки майже вся 24 UA 112082 C2 5 кількість не розчинялася. Одержаний розчин фільтрували через фільтр з розміром пор 0,22 мкм і охолоджували до температури 0-5C, перемішуючи. Суміш перемішували протягом 8 годин з охолодженням при 0-5C. Утворені кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону збирали за допомогою фільтрування і кристалічну форму кристалічних продуктів підтверджували. Результати наведені у Таблиці 9. Таблиця 9 розчинник метанол етанол 2-пропанол ацетон метилетилкетон етилацетат ацетонітрил толуол хлороформ тетрагідрофуран трифторетанол 10 15 20 розчинність при 55C (мг/мл) 5,6 2,6 200 26 >200 кристалічна форма Форма A Форма A Форма A Форма A Форма A Форма A Форма B Форма G Форма A Форма A Форма D Як продемонстровано вище, при кристалізації з різних розчинників, переважним чином кристалізувались кристали Форми A, а кристали Форми G кристалізувались тільки за умов присутності толуолу, де використання для одержання лікарської речовини для фармацевтичних продуктів обмежується з точки зору залишку розчинника. Експериментальний приклад 2 Тест на розчинність, суспендованої суміші кристалічних форм Суміші кристалічних форм, що містять однакову масу кожної кристалічної форми 1-етил-7метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5b]піридин-2-ону, одержаного у Допоміжних прикладах 1-1, 3 і 4, і Прикладі 1 одержували в загальній кількості 20 мг. Суміші кристалічних форм змішували з етанолом (1 мл) і суміші перемішували при кімнатній температурі. Після перемішування протягом одного тижня і після перемішування протягом 2 тижнів, утворені кристали 1-етил-7-метил-3-{4-[(3-метил-3Hімідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону збирали за допомогою фільтрування і кристалічну форму кристалічних продуктів підтверджували. Результати наведені у Таблиці 10. Таблиця 10 суміш кристалічних форм Форма A+Форма G Форма A+Форма E Форма A+Форма D+Форма E+Форма G кристалічна форма через 1 тиждень через 2 тижня Форма G Форма G Форма A + Форма G Форма G Форма G Форма G 25 30 35 Як проілюстровано вище, суміші різних кристалічних форм перетворювались на кристалічну Форму G через 2 тижня при кімнатній температурі і при суспендуванні в етанолі. Результати показали, що кристалічна форма (Форми G), згідно з представленим винаходом, є термодинамічно стабільною за умов суспендування в етанолі при кімнатній температурі. Експериментальний приклад 3 Тест на розчинність кристалічної Форми A, суспендованої у різних розчинниках Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма A) (20 мг, 0,05 ммоль), одержані у Допоміжному прикладі 1-1, змішували з різними розчинниками (1 мл) і суміш перемішували при кімнатній температурі. Після перемішування протягом одного тижня і після перемішування протягом 2 тижнів, кристали утворені 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону, збирали за допомогою фільтрування і кристалічну форму кристалічних продуктів підтверджували. Результати наведені у Таблиці 11. 25 UA 112082 C2 Таблиця 11 кристалічна форма через 1 тиждень через 2 тижня Форма G Форма G Форма A Форма A Форма G Форма G Форма G Форма G Форма A+Форма G Форма G Форма G Форма G Форма G Форма G Форма A Форма A розчинник метанол ізопропіловий спирт ацетон метилетилкетон етилацетат толуол тетрагідрофуран 1-бутанол 5 10 Як проілюстровано вище, кристалічна Форма A перетворювалась на кристалічну Форму G, при суспендуванні у багатьох розчинниках. Результати виявили, що кристалічна форма (Форми G), згідно з представленим винаходом, є термодинамічно більш стабільною, коли суспендована у різних розчинниках при кімнатній температурі, ніж кристалічна Форма A, переважно одержана за допомогою кристалізації з розчину. Експериментальний приклад 4 Тест на стабільність при збереженні Кристали 1-етил-7-метил-3-{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3дигідро-2H-імідазо[4,5-b]піридин-2-ону (Форма G, 5-10 мг), одержані у Прикладі 1, поміщали до скляної колби, герметично закупореної металевої кришечкою і зберігали при 80C. Через 1 тиждень і через 2 тижня зразок забирали, розчиняли у суміші розчинників вода/ацетонітрил при концентрації 0,2 мг/мл і аналоги вимірювали за допомогою Alliance ВЕРХ 2695 (Waters Corporation). Результати наведені у Таблиці 12. 15 Таблиця 12 умови зберігання до зберігання 80C, 1 тиждень 80C, 2 тижні 20 25 30 35 вигляд процент площі (%) ВЕРХ площі під піком головної форми білий кристалічний порошок без змін без змін кристалічна форма 99,7 Форма G 99,7 99,6 Форма G Форма G З наведених вище результатів, чітко видно, що кристалічна (Форма G), згідно з представленим винаходом, має дуже високу хімічну і фізичну стабільність. Експериментальний приклад 5 Інгібування ферменту ФДЕ Фермент ФДЕ10A людини одержували з Sf9 або COS-7 клітин, трансфектованих повнорозмірним геном. Клонований фермент екстрагували з гомогенезованого клітинного конгломерату. Екстрагований фермент з Sf9 клітин частково очищували, використовуючи Histag колонку афінної хроматографії. Фермент зберігали при -70C до використання. ФДЕ активність вимірювали, використовуючи SPA (сцинтиляційний аналіз зближення) (GE Healthcare). Для оцінки інгібувальної активності, 10 мкл серійно розведеного 1-етил-7-метил-3{4-[(3-метил-3H-імідазо[4,5-b]піридин-2-іл)окси]феніл}-1,3-дигідро-2H-імідазо[4,5-b]піридин-2-ону інкубували з 20 мкл ферменту ФДЕ у буфері для досліджень (50 мМ HEPES-NaOH, 8,3 мМ MgCl2, 1,7 мМ EGTA, 0,1 % BSA (pH 7,4)) протягом 30 хв. при кімнатній температурі. Кінцева концентрація ДМСО в дослідженні складала 1 відсоток відносно сполук, що досліджували у двох паралельних дослідженнях з використанням 96-лункових планшетів з половинною площею 3 заповнення лунок (Corning). Для початку реакції, 10 мкл субстрату [ H] цГМФ (25 або 50 нМ; поміщені у набори для SPA від GE Healthcare або придбані у PerkinElmer, відповідно) додавали до кінцевого досліджуваного об'єму 40 мкл. Після 60 хв. інкубування при кімнатній температурі, додавали крупинки ітрію SPA, що містять сульфат цинку, (6 мг/мл, 20 мкл) до заключної реакції ФДЕ. Після стояння ще протягом 60 хвилин, планшети для досліджень підраховували на сцинтиляційному лічильнику (PerkinElmer) і обчислювали ступінь інгібування. Ступінь інгібування обчислювали засновуючись на лунках з контролем, що містять ДМСО як 0 %, і на лунках з контролем без ферменту як 100 %. Результати наведені у Таблиці 13. 26 UA 112082 C2 Таблиця 13 Ступінь інгібування (%) (10 мкМ) 106 5 10 15 Ступінь інгібування (%) (1 мкМ) 109 Промислова придатність Оскільки кристалічна форма, згідно з представленим винаходом, демонструє надзвичайну інгібувальну дію по відношенню до ФДЕ10A, вона може забезпечити профілактичний або терапевтичний лікарський засіб придатний для використання в клінічній практиці для захворювання, такого як шизофренія і т. п… Крім того, оскільки кристалічна форма, згідно з представленим винаходом, проявляє надзвичайну ефективність, низьку токсичність, стабільність, фармакокинетичні параметри в умовах in vivo і т.д… (зокрема, стабільність), вона є придатною для використання як медикамент. Хоча деякі з втілень представленого винаходу, були описані детально вище, однак, для фахівців даної галузі існує можливість внесення різних модифікацій і змін у окремі втілення, без проявлення суттєвого відступу від концепції та переваг представленого винаходу. Такі модифікації і зміни охоплюються у суті та об'ємі представленого винаходу, як викладено у доданій формулі винаходу. Дана заявка заснована на патентній заявці № 2011-138920 поданій в Японії, вміст якої включений до цього документу у всій його повноті. ФОРМУЛА ВИНАХОДУ 20 25 30 35 40 1. Кристалічна форма 1-етил-7-метил-3-{4-[(3-метил-3Н-імідазо[4,5-b]піридин-2-іл)окси]феніл}1,3-дигідро-2Н-імідазо[4,5-b]піридин-2-ону, яка демонструє порошкову рентгенівську дифрактограму, що має характеристичні піки з міжплощинними відстанями (d) 13,59±0,2, 9,22±0,2, 7,88±0,2, 6,76±0,2, 6,21±0,2, 6,13±0,2, 5,73±0,2, 4,64±0,2, 3,79±0,2, 3,75±0,2 ангстреми в порошковій рентгенівській дифракції. 2. Кристалічна форма за пунктом 1, яка демонструє порошкову рентгенівську дифрактограму, що має додаткові характеристичні піки з міжплощинними відстанями (d) 7,48±0,2, 5,24+0,2, 5,13±0,2, 4,27±0,2, 4,16±0,2, 4,06±0,2, 3,99±0,2, 3,93±0,2, 3,60±0,2, 3,41±0,2, 3,16±0,2, 3,10±0,2, 3,06±0,2, 2,89±0,2, 2,83±0,2, 2,73±0,2 та 2,58±0,2 ангстреми в порошковій рентгенівській дифракції. 3. Кристалічна форма за пунктом 1, яка показує початкову температуру приблизно 222 °C приблизно 224 °C ендотермічної поведінки, викликаної плавленням в ДСК-вимірюваннях (швидкість зростання температури 5 °C/хв.). 4. Лікарський засіб, який містить кристалічну форму за пунктом 1. 5. Лікарський засіб за пунктом 4, який є інгібітором фосфодіестерази 10А. 6. Лікарський засіб за пунктом 4, який є профілактичним або терапевтичним агентом при шизофренії. 7. Спосіб попередження або лікування шизофренії у ссавців, за яким ссавцю вводять ефективну кількість кристалічної форми за пунктом 1. 8. Застосування кристалічної форми за пунктом 1 для отримання профілактичного або терапевтичного лікарського засобу для лікування шизофренії. 9. Кристалічна форма за пунктом 1 для застосування в профілактиці або лікуванні шизофренії. 27 UA 112082 C2 28
ДивитисяДодаткова інформація
Назва патенту англійськоюCrystal of fused heterocyclic compound
Автори англійськоюYamamoto, Katsuhiko
Автори російськоюЯмамото Кацухико
МПК / Мітки
МПК: C07D 471/04, A61P 25/18, A61K 31/437
Мітки: кристалічна, форма, сполуки, гетеро)циклічно, конденсованої
Код посилання
<a href="https://ua.patents.su/33-112082-kristalichna-forma-kondensovano-geterociklichno-spoluki.html" target="_blank" rel="follow" title="База патентів України">Кристалічна форма конденсованої гетероциклічної сполуки</a>
Попередній патент: Ротаційні протези суглоба, які мають посилену опорну втулку
Наступний патент: Капсульована лікарська форма, яка містить монтелукаст і левоцетиризин
Випадковий патент: Багатодисковий розкидач мінеральних добрив