Сполуки бензімідазолону, які мають 5-нт4 рецепторну агоністичну активність
Номер патенту: 86204
Опубліковано: 10.04.2009
Автори: Утіда Тікара, Кацу Ясухіро, Соне Хірокі, Ігуті Сатору, Кодзіма Такасі
Формула / Реферат
1 .Сполука формули (І):
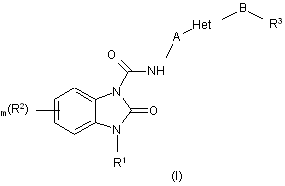 ,
,
в якій
Het являє собою гетероциклічну групу, яка має один атом азоту, з яким В зв'язується безпосередньо, і від 4 до 7 атомів вуглецю, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 4 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() ;
;
А являє собою алкіленову групу, яка має від 1 до 4 атомів вуглецю;
В являє собою ковалентний зв'язок або алкіленову групу, яка має від 1 до 5 атомів вуглецю, і вказана алкіленова група є незаміщеною або заміщеною оксогрупою, коли R3 являє собою гетероциклічну групу;
R1 являє собою ізопропільну групу або циклопентильну групу;
R2 незалежно являє собою атом галогену або алкільну групу, яка має від 1 до 4 атомів вуглецю;
m являє собою 0, 1, 2, 3 або 4; і
R3 являє собою
(і) циклоалкільну групу, яка має від 3 до 8 атомів вуглецю, і вказана циклоалкільна група є заміщеною від 1 до 5 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() , або
, або
(іі) гетероциклічну групу, яка має від 3 до 8 атомів, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 5 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() ,
,
вказані замісники ![]() незалежно вибирають з гідроксигрупи і аміногрупи;
незалежно вибирають з гідроксигрупи і аміногрупи;
вказані замісники ![]() незалежно вибирають з гідроксигрупи, аміногрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю, карбоксильної групи і алкоксигрупи, яка має від 1 до 4 атомів вуглецю; і
незалежно вибирають з гідроксигрупи, аміногрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю, карбоксильної групи і алкоксигрупи, яка має від 1 до 4 атомів вуглецю; і
вказані замісники ![]() незалежно вибирають з гідроксигрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю, карбоксильної групи, аміногрупи, алкільної групи, яка має від 1 до 4 атомів вуглецю, амінозаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю і карбамоїльної групи,
незалежно вибирають з гідроксигрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю, карбоксильної групи, аміногрупи, алкільної групи, яка має від 1 до 4 атомів вуглецю, амінозаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю і карбамоїльної групи,
або її фармацевтично прийнятні солі.
2. Сполука або її фармацевтично прийнятна сіль за п. 1, в якій
Het являє собою гетероциклічну групу, яку вибирають з:
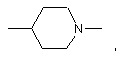
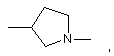
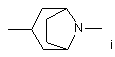
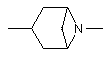 ,
,
вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 3 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() ; і
; і
А являє собою алкіленову групу, яка має від 1 до 3 атомів вуглецю.
3. Сполука або її фармацевтично прийнятна сіль за п. 1, в якій
Het являє собою групу формули

і ця група є незаміщеною або заміщеною одним із замісників, які вибирають з групи, яка складається із замісників ![]() ;
;
А являє собою алкіленову групу, яка має від 1 до 2 атомів вуглецю,
В являє собою алкіленову групу, яка має від 1 до 4 атомів вуглецю, і вказана алкіленова група є незаміщеною або заміщеною оксогрупою, коли R3 являє собою гетероциклічну групу;
R2 незалежно являє собою атом галогену або алкільну групу, яка має від 1 до 2 атомів вуглецю;
m являє собою 0, 1 або 2; і
R3 являє собою
(і) циклоалкільну групу, яка має від 4 до 7 атомів вуглецю, і вказана циклоалкільна група є заміщеною від 1 до 3 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() , або
, або
(іі) гетероциклічну групу, яка має від 4 до 7 атомів, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 3 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() .
.
4. Сполука або її фармацевтично прийнятна сіль за п. 1, в якій
Het являє собою групу формули

і ця група є незаміщеною або заміщеною одним із замісників, які вибирають з групи, яка складається із замісників ![]() ;
;
А являє собою метиленову групу;
В являє собою алкіленову групу, яка має від 1 до 2 атомів вуглецю;
R1 являє собою ізопропільну групу;
R2 незалежно являє собою атом фтору, атом хлору або метил; і
R3 являє собою
(і) циклоалкільну групу, яка має від 5 до 7 атомів вуглецю, і вказана циклоалкільна група є заміщеною від 1 до 2 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() , або
, або
(іі) гетероциклічну групу, яка має від 5 до 7 атомів, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 2 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() ,
,
вказані замісники ![]() незалежно вибирають з гідроксигрупи, аміногрупи і алкоксигрупи, яка має від 1 до 2 атомів вуглецю; і
незалежно вибирають з гідроксигрупи, аміногрупи і алкоксигрупи, яка має від 1 до 2 атомів вуглецю; і
вказані замісники ![]() незалежно вибирають з гідроксигрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 2 атомів вуглецю, карбоксильної групи, аміногрупи, амінозаміщеної алкільної групи, яка має від 1 до 2 атомів вуглецю і карбамоїльної групи.
незалежно вибирають з гідроксигрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 2 атомів вуглецю, карбоксильної групи, аміногрупи, амінозаміщеної алкільної групи, яка має від 1 до 2 атомів вуглецю і карбамоїльної групи.
5. Сполука або її фармацевтично прийнятна сіль за п. 1, в якій
Het являє собою групу формули

А являє собою метиленову групу;
В являє собою метиленову групу;
R1 являє собою ізопропільну групу;
R2 являє собою атом фтору;
m являє собою 0 або 1; і
R3 являє собою
(і) циклоалкільну групу, яка має від 5 до 6 атомів вуглецю, і вказана циклоалкільна група є заміщеною від 1 до 2 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() , або
, або
(іі) гетероциклічну групу, яка має від 5 до 6 атомів, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 2 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() ,
,
вказані замісники ![]() незалежно вибирають з гідроксигрупи і аміногрупи; і вказані замісники
незалежно вибирають з гідроксигрупи і аміногрупи; і вказані замісники ![]() незалежно вибирають з гідроксигрупи і аміногрупи.
незалежно вибирають з гідроксигрупи і аміногрупи.
6. Сполука або її фармацевтично прийнятна сіль за п. 1, в якій
Het являє собою групу формули

А являє собою метиленову групу;
В являє собою метиленову групу;
R1 являє собою ізопропільну групу;
R2 являє собою атом фтору;
m являє собою 0; і
R3 являє собою
(і) циклоалкільну групу, заміщену від 1 до 2 замісниками, які незалежно вибирають з гідроксигрупи або аміногрупи, або
(іі) гетероциклічну групу, яка має від 6 атомів, і вказана гетероциклічна група є заміщеною гідроксигрупою або аміногрупою.
7. Сполука або її фармацевтично прийнятна сіль за п. 6, в якій
R3 являє собою
(і) циклогексильну групу, заміщену від 1 до 2 гідроксигрупами, або
(іі) групу тетрагідропірану, заміщену від 1 до 2 гідроксигрупами.
8. Сполука або її фармацевтично прийнятна сіль за п. 7, в якій
R3 являє собою гідрокситетрагідропіраніл або дигідроксициклогексил.
9. Сполука за п. 1, яку вибирають з:
N-({1-[(4-гідрокситетрагідро-2Н-піран-4-іл)метил]піперидин-4-іл}метил)-3-ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1-карбоксаміду;
N-({1-[(транс-1,4-дигідроксигексил)метил]піперидин-4-іл}метил)-3-ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1-карбоксаміду;
N-({1-[(цис-1,4-дигідроксигексил)метил]піперидин-4-іл}метил)-3-ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1-карбоксаміду і
6-фтор-N-({1-[(4-гідрокситетрагідро-2Н-піран-4-іл)метил]піперидин-4-іл}метил)-3-ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1-карбоксаміду,
або її фармацевтично прийнятна сіль.
10. Сполука або її фармацевтично прийнятна сіль за будь-яким з пп. 1-9, де фармацевтично прийнятна сіль являє собою гідрохлорид або геміедизилат.
11. Фармацевтична композиція, яка містить сполуку або її фармацевтично прийнятну сіль за будь-яким з пп. 1-10 разом з фармацевтично прийнятним ексципієнтом.
12. Спосіб лікування хворобливих станів, опосередкованих 5-НТ4 рецепторною активністю, у ссавців, який включає введення вказаному суб'єкту, який потребує такого лікування, терапевтично ефективної кількості сполуки або її фармацевтично прийнятної солі за будь-яким з пп. 1-10.
13. Спосіб лікування захворювань, які вибирають із захворювання шлунково-стравохідного рефлюксу, захворювання шлунково-кишкового тракту, розладу шлункової моторності, невиразкової диспепсії, функціональної диспепсії, синдрому подразненої кишки (IBS), запору, диспепсії, езофагіту, шлунково-стравохідного захворювання, нудоти, захворювання центральної нервової системи, хвороби Альцгеймера, когнітивного розладу, блювання, мігрені, неврологічного захворювання, болю, серцево-судинних розладів, серцевої недостатності, аритмії серця, діабетів і синдрому апное, який включає введення вказаному суб'єкту терапевтично ефективної кількості сполуки або її фармацевтично прийнятної солі за будь-яким з пп. 1-10.
14. Застосування сполуки або її фармацевтично прийнятної солі за будь-яким з пп. 1-10 для виробництва ліків для лікування хворобливих станів, опосередкованих 5-НТ4 рецепторною активністю, у ссавців.
15. Застосування сполуки за п. 14, де вказаний стан вибирають із захворювання шлунково-стравохідного рефлюксу, захворювання шлунково-кишкового тракту, розладу шлункової моторності, невиразкової диспепсії, функціональної диспепсії, синдрому подразненої кишки (IBS), запору, диспепсії, езофагіту, шлунково-стравохідного захворювання, нудоти, захворювання центральної нервової системи, хвороби Альцгеймера, когнітивного розладу, блювання, мігрені, неврологічного захворювання, болю, серцево-судинних розладів, серцевої недостатності, аритмії серця, діабетів і синдрому апное.
16. Сполука формули (2-А'):
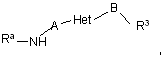 2-А'
2-А'
в якій
Rа являє собою атом водню або N-захисну групу;
Het являє собою гетероциклічну групу, яка має один атом азоту, з яким В зв'язується безпосередньо, і від 4 до 7 атомів вуглецю, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 4 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() ;
;
А являє собою алкіленову групу, яка має від 1 до 4 атомів вуглецю:
В являє собою ковалентний зв'язок або алкіленову групу, яка має від 1 до 5 атомів вуглецю, і вказана алкіленова група є незаміщеною або заміщеною оксогрупою, коли R3 являє собою гетероциклічну групу;
R3 являє собою
(і) циклоалкільну групу, яка має від 3 до 8 атомів вуглецю, і вказана циклоалкільна група є заміщеною від 1 до 5 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() , або
, або
(іі) гетероциклічну групу, яка має від 3 до 8 атомів, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 5 замісниками, які незалежно вибирають з групи, яка складається із замісників ![]() ,
,
вказані замісники ![]() незалежно вибирають з гідроксигрупи і аміногрупи;
незалежно вибирають з гідроксигрупи і аміногрупи;
вказані замісники ![]() незалежно вибирають з гідроксигрупи, аміногрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю, карбоксильної групи і алкоксигрупи, яка має від 1 до 4 атомів вуглецю; і
незалежно вибирають з гідроксигрупи, аміногрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю, карбоксильної групи і алкоксигрупи, яка має від 1 до 4 атомів вуглецю; і
вказані замісники ![]() незалежно вибирають з гідроксигрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю, карбоксильної групи, аміногрупи, алкільної групи, яка має від 1 до 4 атомів вуглецю, амінозаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю і карбамоїльної групи,
незалежно вибирають з гідроксигрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю, карбоксильної групи, аміногрупи, алкільної групи, яка має від 1 до 4 атомів вуглецю, амінозаміщеної алкільної групи, яка має від 1 до 4 атомів вуглецю і карбамоїльної групи,
або її сіль.
17. Сполука або її сіль за п. 16, де Rа являє собою атом водню або t-бутоксикарбонільну групу;
Het являє собою групу формули

А являє собою метиленову групу;
В являє собою метиленову групу; і
R3 являє собою гідрокситетрагідропіраніл або дигідроксициклогексил.
18. Комбінація сполуки або її фармацевтично прийнятної солі за будь-яким з пп. 1-10 та іншого фармакологічно активного агента.
19. Фармацевтична композиція, яка містить сполуку або її фармацевтично прийнятну сіль за будь-яким з пп. 1-10 та інший фармакологічно активний агент.
Текст
1 .Сполука формули (І): C2 2 (19) 1 3 86204 4 Het являє собою гетероциклічну групу, яку вибирають з групи, яка складається із замісників a2 , рають з: або N N N N , вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 3 замісниками, які незалежно вибирають з групи, яка складається із замісників a1 ; і А являє собою алкіленову групу, яка має від 1 до 3 атомів вуглецю. 3. Сполука або її фармацевтично прийнятна сіль за п. 1, в якій Het являє собою групу формули N (іі) гетероциклічну групу, яка має від 5 до 7 атомів, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 2 замісниками, які незалежно вибирають з групи, яка складається із замісників b, вказані замісники a2 незалежно вибирають з гідроксигрупи, аміногрупи і алкоксигрупи, яка має від 1 до 2 атомів вуглецю; і вказані замісники b незалежно вибирають з гідроксигрупи, гідроксизаміщеної алкільної групи, яка має від 1 до 2 атомів вуглецю, карбоксильної групи, аміногрупи, амінозаміщеної алкільної групи, яка має від 1 до 2 атомів вуглецю і карбамоїльної групи. 5. Сполука або її фармацевтично прийнятна сіль за п. 1, в якій Het являє собою групу формули , і ця група є незаміщеною або заміщеною одним із замісників, які вибирають з групи, яка складається 1 із замісників a ; А являє собою алкіленову групу, яка має від 1 до 2 атомів вуглецю, В являє собою алкіленову групу, яка має від 1 до 4 атомів вуглецю, і вказана алкіленова група є незаміщеною або заміщеною оксогрупою, коли R3 являє собою гетероциклічну групу; R2 незалежно являє собою атом галогену або алкільну групу, яка має від 1 до 2 атомів вуглецю; m являє собою 0, 1 або 2; і R3 являє собою (і) циклоалкільну групу, яка має від 4 до 7 атомів вуглецю, і вказана циклоалкільна група є заміщеною від 1 до 3 замісниками, які незалежно вибирають з групи, яка складається із замісників a2 , або (іі) гетероциклічну групу, яка має від 4 до 7 атомів, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 3 замісниками, які незалежно вибирають з групи, яка складається із замісників b. 4. Сполука або її фармацевтично прийнятна сіль за п. 1, в якій Het являє собою групу формули N , А являє собою метиленову групу; В являє собою метиленову групу; R1 являє собою ізопропільну групу; R2 являє собою атом фтору; m являє собою 0 або 1; і R3 являє собою (і) циклоалкільну групу, яка має від 5 до 6 атомів вуглецю, і вказана циклоалкільна група є заміщеною від 1 до 2 замісниками, які незалежно вибирають з групи, яка складається із замісників a2 , або (іі) гетероциклічну групу, яка має від 5 до 6 атомів, і вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 2 замісниками, які незалежно вибирають з групи, яка складається із замісників b, вказані замісники a2 незалежно вибирають з гідроксигрупи і аміногрупи; і вказані замісники b незалежно вибирають з гідроксигрупи і аміногрупи. 6. Сполука або її фармацевтично прийнятна сіль за п. 1, в якій Het являє собою групу формули N , N , і ця група є незаміщеною або заміщеною одним із замісників, які вибирають з групи, яка складається із замісників a1 ; А являє собою метиленову групу; В являє собою алкіленову групу, яка має від 1 до 2 атомів вуглецю; R1 являє собою ізопропільну групу; R2 незалежно являє собою атом фтору, атом хлору або метил; і R3 являє собою (і) циклоалкільну групу, яка має від 5 до 7 атомів вуглецю, і вказана циклоалкільна група є заміщеною від 1 до 2 замісниками, які незалежно виби А являє собою метиленову групу; В являє собою метиленову групу; R1 являє собою ізопропільну групу; R2 являє собою атом фтору; m являє собою 0; і R3 являє собою (і) циклоалкільну групу, заміщену від 1 до 2 замісниками, які незалежно вибирають з гідроксигрупи або аміногрупи, або (іі) гетероциклічну групу, яка має від 6 атомів, і вказана гетероциклічна група є заміщеною гідроксигрупою або аміногрупою. 7. Сполука або її фармацевтично прийнятна сіль за п. 6, в якій R3 являє собою 5 86204 6 розладу, блювання, мігрені, неврологічного захво(і) циклогексильну групу, заміщену від 1 до 2 гідрорювання, болю, серцево-судинних розладів, серксигрупами, або цевої недостатності, аритмії серця, діабетів і син(іі) групу тетрагідропірану, заміщену від 1 до 2 гіддрому апное. роксигрупами. 16. Сполука формули (2-А'): 8. Сполука або її фармацевтично прийнятна сіль за п. 7, в якій B R3 являє собою гідрокситетрагідропіраніл або диA Het R3 2- (А') Ra NH гідроксициклогексил. , 9. Сполука за п. 1, яку вибирають з: в якій N-({1-[(4-гідрокситетрагідро-2Н-піран-4Rа являє собою атом водню або N-захисну групу; іл)метил]піперидин-4-іл}метил)-3-ізопропіл-2-оксоHet являє собою гетероциклічну групу, яка має 2,3-дигідро-1Н-бензімідазол-1-карбоксаміду; один атом азоту, з яким В зв'язується безпосередN-({1-[(транс-1,4ньо, і від 4 до 7 атомів вуглецю, і вказана гетеродигідроксигексил)метил]піперидин-4-іл}метил)-3циклічна група є незаміщеною або заміщеною від ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-11 до 4 замісниками, які незалежно вибирають з карбоксаміду; N-({1-[(цис-1,4-дигідроксигексил)метил]піперидингрупи, яка складається із замісників a1 ; 4-іл}метил)-3-ізопропіл-2-оксо-2,3-дигідро-1НА являє собою алкіленову групу, яка має від 1 до 4 бензімідазол-1-карбоксаміду і атомів вуглецю: 6-фтор-N-({1-[(4-гідрокситетрагідро-2Н-піран-4В являє собою ковалентний зв'язок або алкіленову іл)метил]піперидин-4-іл}метил)-3-ізопропіл-2-оксогрупу, яка має від 1 до 5 атомів вуглецю, і вказана 2,3-дигідро-1Н-бензімідазол-1-карбоксаміду, алкіленова група є незаміщеною або заміщеною або її фармацевтично прийнятна сіль. оксогрупою, коли R3 являє собою гетероциклічну 10. Сполука або її фармацевтично прийнятна сіль групу; за будь-яким з пп. 1-9, де фармацевтично прийняR3 являє собою тна сіль являє собою гідрохлорид або геміедизи(і) циклоалкільну групу, яка має від 3 до 8 атомів лат. вуглецю, і вказана циклоалкільна група є заміще11. Фармацевтична композиція, яка містить сполуною від 1 до 5 замісниками, які незалежно вибику або її фармацевтично прийнятну сіль за будьрають з групи, яка складається із замісників a2 , яким з пп. 1-10 разом з фармацевтично прийнятабо ним ексципієнтом. (іі) гетероциклічну групу, яка має від 3 до 8 атомів, 12. Спосіб лікування хворобливих станів, опосереі вказана гетероциклічна група є незаміщеною або дкованих 5-НТ4 рецепторною активністю, у ссавзаміщеною від 1 до 5 замісниками, які незалежно ців, який включає введення вказаному суб'єкту, вибирають з групи, яка складається із замісників який потребує такого лікування, терапевтично b, ефективної кількості сполуки або її фармацевтичвказані замісники a1 незалежно вибирають з гідно прийнятної солі за будь-яким з пп. 1-10. 13. Спосіб лікування захворювань, які вибирають роксигрупи і аміногрупи; із захворювання шлунково-стравохідного рефлюквказані замісники a2 незалежно вибирають з гідсу, захворювання шлунково-кишкового тракту, роксигрупи, аміногрупи, гідроксизаміщеної алкільрозладу шлункової моторності, невиразкової дисної групи, яка має від 1 до 4 атомів вуглецю, карпепсії, функціональної диспепсії, синдрому подрабоксильної групи і алкоксигрупи, яка має від 1 до 4 зненої кишки (IBS), запору, диспепсії, езофагіту, атомів вуглецю; і шлунково-стравохідного захворювання, нудоти, вказані замісники b незалежно вибирають з гідрозахворювання центральної нервової системи, хвоксигрупи, гідроксизаміщеної алкільної групи, яка роби Альцгеймера, когнітивного розладу, блюванмає від 1 до 4 атомів вуглецю, карбоксильної груня, мігрені, неврологічного захворювання, болю, пи, аміногрупи, алкільної групи, яка має від 1 до 4 серцево-судинних розладів, серцевої недостатноатомів вуглецю, амінозаміщеної алкільної групи, сті, аритмії серця, діабетів і синдрому апное, який яка має від 1 до 4 атомів вуглецю і карбамоїльної включає введення вказаному суб'єкту терапевтичгрупи, но ефективної кількості сполуки або її фармацевабо її сіль. тично прийнятної солі за будь-яким з пп. 1-10. 17. Сполука або її сіль за п. 16, де Rа являє собою 14. Застосування сполуки або її фармацевтично атом водню або t-бутоксикарбонільну групу; прийнятної солі за будь-яким з пп. 1-10 для виробHet являє собою групу формули ництва ліків для лікування хворобливих станів, опосередкованих 5-НТ4 рецепторною активністю, у ссавців. 15. Застосування сполуки за п. 14, де вказаний стан вибирають із захворювання шлунковостравохідного рефлюксу, захворювання шлунковокишкового тракту, розладу шлункової моторності, невиразкової диспепсії, функціональної диспепсії, синдрому подразненої кишки (IBS), запору, диспепсії, езофагіту, шлунково-стравохідного захворювання, нудоти, захворювання центральної нервової системи, хвороби Альцгеймера, когнітивного N , А являє собою метиленову групу; В являє собою метиленову групу; і R3 являє собою гідрокситетрагідропіраніл або дигідроксициклогексил. 18. Комбінація сполуки або її фармацевтично прийнятної солі за будь-яким з пп. 1-10 та іншого фармакологічно активного агента. 7 86204 8 19. Фармацевтична композиція, яка містить сполуяким з пп. 1-10 та інший фармакологічно активний ку або її фармацевтично прийнятну сіль за будьагент. Даний винахід відноситься до нових сполук бензімідазолону. Ці сполуки володіють селективною 5-НТ4 рецепторною агоністичною активністю. Даний винахід також відноситься до фармацевтичної композиції, способу лікування і застосування, які включають вищезазначені сполуки для лікування станів захворювань, опосередкованих 5-НТ4 рецепторною активністю. Взагалі, 5-НТ4 рецепторні агоністи є корисними для лікування різноманітності захворювань, таких як захворювання шлунково-стравохідного рефлюксу, захворювання шлунково-кишкового тракту, розлад шлункової моторності, невиразкова диспепсія, функціональна диспепсія, синдром подразненої кишки (IBS), запор, диспепсія, езофагіт, шлунково-стравохідне захворювання, нудота, захворювання центральної нервової системи, хвороба Альцгеймера, когнітивний розлад, блювота, мігрень, неврологічне захворювання, біль, серцево-судинні розлади, серцева недостатність, аритмія серця, діабети і синдром апное [Дивіться TiPs, 1992, 13, 141; Ford A. P. D. W. et al., Med. Res. Rev., 1993, 13, 633; Gulfflcson G. W. et ah. DrugDev. Res., 1992, 26, 405; Richard M. Eglen et al, TiPS, 1995,16,391; Bockaert J. Et al., CNSDrugs, 1, 6; Romanelli M. N. et al., Arzheim Forsch./Drug Res., 1993, 43, 913; Kaumann A. et al., NaunynSchmiedeberg's. 1991, 344. 150, and Romanelli M. N. et al., Arzheim Forsch./Drug Res., 1993, 43, 913]. Також, Мозаприд, як відомо, є корисним для лікування діабету. Буде бажаним, якщо б були забезпечені 5-НТ4 рецепторні агоністи, які володіють більшими 5НТ4 рецепторними агоністичними активностями. [US5223511] розкриває сполуки бензімідазолу як 5-НТ4 рецепторні антагоністи. Більш конкретно, розкриті сполуки, які представлені наступною формулою: [WO93/18027] розкриває сполуки бензімідазолону як 5-НТ4 рецепторні антагоністи. Більш конкретно, розкриті сполуки, які представлені наступною формулою: [WO99/17772] розкриває сполуки бензімідазолону як 5-НТ4 рецепторні агоністи і/або антагоніс ти. Більш конкретно, розкриті сполуки, які представлені наступною формулою: [WO94/00449] розкриває сполуки бензімідазолону як 5-НТ4 агоністи або антагоністи і/або 5-НТ3 антагоністи. Більш конкретно, розкриті сполуки, які представлені наступною формулою: Є потреба у забезпеченні нових 5-НТ4 агоністів, які являють собою хороші лікарські кандидати. Зокрема, переважні сполуки повинні зв'язуватись міцно до 5-НТ4 рецептора, в той же час показуючи невелику афінність для інших рецепторів, і показувати функціональну активність як агоністи. Вони повинні добре абсорбуватись з шлунковокишкового тракту, бути метаболічно стійкими і володіти прийнятними фармакокінетичними властивостями. Коли їх націлюють проти рецепторів в центральній нервовій системі, вони повинні перетинати кров'яний бар'єр мозку вільно, і коли їх націлюють селективно проти рецепторів в периферійній нервовій системі, вони не повинні перетинати кров'яний бар'єр мозку. Вони повинні бути нетоксичними і демонструвати невелику кількість побічних ефектів. До того ж, ідеальний лікарський кандидат існуватиме у фізичній формі, яка є стабільною, негігроскопічною і яка легко формується у композиції. На сьогоднішній день несподівано було виявлено, що сполуки даного винаходу володіють сильною селективною 5-НТ4 агоністичною активністю, і таким чином вони є корисними для лікування хворобливих станів, опосередкованих 5-НТ4 активністю, таких як захворювання шлунковостравохідного рефлюксу, захворювання шлунковокишкового тракту, розлад шлункової моторності, невиразкова диспепсія, функціональна диспепсія, синдром подразненої кишки (IBS), запор, диспепсія, езофагіт, шлунково-стравохідне захворювання, нудота, захворювання центральної нервової системи, хвороба Альцгеймера, когнітивний розлад, блювота, мігрень, неврологічне захворювання, біль, серцево-судинні розлади, серцева недостатність, аритмія серця, діабети і синдром апное (особливо викликаний введенням опіоїду). 9 86204 10 Надалі, сполуки даного винаходу показують вказані замісники α2 незалежно вибирають з зменшене QT пролонгування за допомогою предгідроксигрупи, аміногрупи, гідрокси-заміщеної алставлення полярної групи в R3 формули (І). QT кільної групи, яка має від 1 до 4 атомів вуглецю, пролонгування, як відомо, має потенційну відповікарбоксильної групи і алкоксигрупи, яка має від 1 дальність за продукування фатальних серцевих до 4 атомів вуглецю; і аритмій Torsades de Pointes (TdP). Здатність провказані замісники β незалежно вибирають з гілонгувати потенційну тривалість серцевої дії була дроксигрупи, гідрокси-заміщеної алкільної групи, ідентифікована як така, що існує завдяки дії в каяка має від 1 до 4 атомів вуглецю, карбоксильної налі калію HERG. Наприклад, медикаменти, які групи, аміногрупи, алкільної групи, яка має від 1 до виходять з ринку завдяки пролонгуванню QT, такі 4 атомів вуглецю, аміно-заміщеної алкільної групи, як Цизаприд і Терфенадин, як відомо, є могутніми яка має від 1 до 4 атомів вуглецю і карбамоїльної блокаторами каналу калію HERG (Expert Opinion of групи. Pharmacotherapy.; 2, pp.947-973,2000) Інгібіторна Також, даний винахід забезпечує фармацевактивність в каналі HERG була оцінена з афінності тичну композицію для лікування станів захворюдля каналу калію типу HERG, було досліджено за вань, опосередкованих 5-НТ4 рецептором, у ссавдопомогою перевірки зв'язування [3 Н]дофетиліду, ців, яка включає введення вказаному суб'єкту що може передбачити інгібіторну активність в катерапевтично ефективну кількість сполуки формуналі HERG [Eur. J. Pharmacol, 430, pp.147ли (1) або її фармацевтично прийнятних солей. 148,2001]. Надалі, даний винахід також забезпечує фарСполуки даного винаходу можуть показати мацевтичну композицію для лікування захворюменшу токсичність, хорошу абсорбцію, розподіл, вань, які вибирають із захворювання шлунковохорошу розчинність, низьку афінність зв'язування стравохідного рефлюксу, захворювання шлунковобілка, меншу взаємодію між ліками і хорошу метакишкового тракту, розладу шлункової моторності, болічну стабільність. невиразкової диспепсії, функціональної диспепсії, Даний винахід забезпечує сполуку наступної синдрому подразненої кишки (IBS), запору, диспеформули (І) або фармацевтично її прийнятні солі. псії, езофагіту, шлунково-стравохідного захворювання, нудоти, захворювання центральної нервової системи, хвороби Альцгеймера, когнітивного розладу, блювоти, мігрені, неврологічного захворювання, болю, серцево-судинних розладів, сер(I) цевої недостатності, аритмії серця, діабетів і синдрому апное, або подібного, яка включає терапевтично ефективну кількість сполуки бензімідазолону формули (І) або її фармацевтично прив якій йнятної солі разом з фармацевтично прийнятним Het являє собою гетероциклічну групу, яка має носієм. один атом азоту, з яким В зв'язується безпосередТакож, даний винахід забезпечує спосіб лікуньо, і від 4 до 7 атомів вуглецю, і вказана гетеровання ссавця, включаючи людину, щоб лікувати циклічна група є незаміщеною або заміщеною від стани захворювань, опосередковані 5-НТ4 рецеп1 до 4 замісниками, які незалежно вибирають з тором, у ссавців, який включає введенні згаданому групи, яка складається із замісників а1; суб'єкту терапевтично ефективної кількості сполуА являє собою алкіленову групу, яка має від 1 ки формули (І) або її фармацевтично прийнятних до 4 атомів вуглецю; солей. Надалі, даний винахід забезпечує спосіб В являє собою ковалентний зв'язок або алкілікування хворобливих станів, як згадано вище. До ленову групу, яка має від 1 до 5 атомів вуглецю, і того ж, даний винахід забезпечує застосування вказана алкіленова група є незаміщеною або засполуки формули (І) або її фармацевтично прийнміщеною оксогрупою, коли R3 являє собою гетероятних солей у виробництві ліків для лікування стациклічну групу; нів захворювань, опосередкованих 5-НТ4 рецептоR1 являє собою ізопропільну групу або циклорною активністю, у ссавців. Стани, опосередковані пентильну групу; 5-НТ4 рецепторною активністю, включають ті заR незалежно являє собою атом галогену або хворювання або розлади, які описані вище. алкільну групу, яка має від 1 до 4 атомів вуглецю; Також, даний винахід забезпечує сполуку наm являє собою 0, 1, 2, 3 або 4; і ступної формули (2-А') або її сіль: R3 являє собою (і) циклоалкільну групу, яка має від 3 до 8 ато(2-A') мів вуглецю, і вказана циклоалкільна група є заміщеною від 1 до 5 замісниками, які незалежно вив якій бирають з групи, яка складається із замісників α2, Ra являє собою атом водню або N-захисну або групу; (іі) гетероциклічну групу, яка має від 3 до 8 Het являє собою гетероциклічну групу, яка має атомів, і вказана гетероциклічна група є незаміщеодин атом азоту, до якого В зв'язується безпосеною або заміщеною від 1 до 5 замісниками, які редньо, і від 4 до 7 атомів вуглецю, і вказана гетенезалежно вибирають з групи, яка складається із роциклічна група є незаміщеною або заміщеною замісників β, від 1 до 4 замісниками, які незалежно вибирають з вказані замісники α1 незалежно вибирають з групи, яка складається із замісників α1; гідроксигрупи і аміногрупи; 11 86204 12 А являє собою алкіленову групу, яка має від 1 Як використано тут, термін "галоген" у "R2" до 4 атомів вуглецю; означає фтор, хлор, бром і йод, переважно фтор В являє собою ковалентний зв'язок або алкіабо хлор. ленову групу, яка має від 1 до 5 атомів вуглецю, і Як використано тут, термін "алкіл" в "R2"; "алвказана алкіленова група є незаміщеною або закіл" "гідрокси-заміщеної алкільної групи" і "алкоксиміщеною оксогрупою, коли R3 являє собою гетерогрупа, яка має від 1 до 4 атомів вуглецю" в "замісциклічну групу; никах α 2", "алкіл" в "замісниках β"; і "алкіл" R3 являє собою "гідрокси-заміщеної алкільної групи" і "аміно(і) циклоалкільну групу, яка має від 3 до 8 атозаміщена алкільна група" в "замісниках β" означамів вуглецю, і вказана циклоалкільна група є заміють насичені радикали з прямим або розгалужещеною від 1 до 5 замісниками, які незалежно виним ланцюгом, які мають від 1 до 4 атомів вуглебирають з групи, яка складається із замісників α2, цю, включаючи, але не обмежуючись цим, метил, або етил, n-пропіл, ізопропіл, n-бутил, ізобутил, втор(іі) гетероциклічну групу, яка має від 3 до 8 бутил, трет-бутил. атомів, і вказана гетероциклічна група є незаміщеЯк використано тут, термін "циклоалкіл" в "R3" ною або заміщеною від 1 до 5 замісниками, які означає циклічну алкільну групу, яка має 3 до 8 незалежно вибирають з групи, яка складається із атомів вуглецю, таку як циклопрошл, циклобутил, замісників β, циклопентил, циклогексил, циклогептил, циклооквказані замісники α1 незалежно вибирають з тил і т.д. гідроксигрупи і аміногрупи; Як використано тут, термін "гетероциклічний" вказані замісники α2 незалежно вибирають з "R3" означає гетероциклічне кільце, яке має один гідроксигрупи, аміногрупи, гідрокси-заміщеної алабо більше гетероатомів в кільці, переважно має кільної групи, яка має від 1 до 4 атомів вуглецю, від 2 до 6 атомів вуглецю і від 1 до 3 гетероатомів, карбоксильної групи і алкоксигрупи, яка має від 1 включаючи азиридиніл, азетидиніл, піперидиніл, до 4 атомів вуглецю; і морфолініл (включаючи морфоліно), піролідиніл, вказані замісники β незалежно вибирають з гіпіразолідиніл, піперазиніл, тетрагідропіразоліл, дроксигрупи, гідрокси-заміщеної алкільної групи, піразолініл, тетрагідропіраніл і т.д. яка має від 1 до 4 атомів вуглецю, карбоксильної Термін "лікування", як використано тут, відногрупи, аміногрупи, алкільної групи, яка має від 1 до ситься до змінювання, полегшення, інгібування 4 атомів вуглецю, аміно-заміщеної алкільної групи, прогресу, або запобігання розладу або стану, до яка має від 1 до 4 атомів вуглецю і карбамоїльної якого такий термін застосовується, або один або групи. більше симптомів такого розладу або стану. ТерЯк використано тут, термін "гетероциклічний" мін "лікування", як використано тут, відноситься до "Het" означає гетероциклічну групу, яка має один дії лікування, оскільки "лікування" тільки-но визнаатом азоту і від 4 до 7 атомів вуглецю, така як чено вище. Переважна сполука формули (І) даного є тією, де Het являє собою гетероциклічну групу, яку вибирають з Як використано тут, термін "алкілен" в "А" означає насичені радикали з прямим або розгалуженим ланцюгом, які мають від 1 до 4 атомів вуглецю, включаючи, але не обмежуючись цим, метилен, етилен, η-пропілен, ізопропілен, n-бутилен, ізобутилен, втор-бутилен, трет-бутилен. "Алкілен" в "А" являє собою переважно метиленову групу, етиленову групу або пропіленову групу; більш переважно метиленову групу або етиленову групу; найбільш переважно метиленову групу. Як використано тут, термін "алкілен" в "В" означає насичені радикали з прямим або розгалуженим ланцюгом, які мають від 1 до 5 атомів вуглецю, включаючи, але не обмежуючись цим, метилен, етилен, η-пропілен, ізопропілен, n-бутилен, ізобутилен, втор-бутилен, трет-бутилен, nпентилен, ізопентилен, втор-пентилен. третпентилен. "Алкілен" в "В" являє собою переважно алкіленову групу, яка має від 1 до 4 атомів вуглецю; більш переважно алкіленову групу, яка має від 1 до 3 атомів вуглецю; ще більш переважно метиленову групу або етиленову групу; навіть більш переважно метиленову групу. вказана гетероциклічна група є незаміщеною або заміщеною від 1 до 3 замісниками, які незалежно вибирають з групи, яка складається із замісників α 1; і А являє собою алкіленову групу, яка має від 1 до 3 атомів вуглецю. Більш переважна сполука формули (І) даного винаходу є тією, де Het являє собою групу формули , і ця група є незаміщеною або заміщеною одним із замісників, які вибирають з групи, яка складається із замісників α1; А являє собою алкіленову групу, яка має від 1 до 2 атомів вуглецю; В являє собою алкіленову групу, яка має від 1 до 4 атомів вуглецю, і вказана алкіленова група є незаміщеною або заміщеною оксогрупою, коли R3 являє собою гетероциклічну групу; R2 незалежно являє собою атом галогену або алкільну групу, яка має від 1 до 2 атомів вуглецю; m являє собою 0, 1 або 2; і 13 86204 14 R1 являє собою (іі) гетероциклічну групу, яка має від 5 до 6 (і) циклоалкільну групу, яка має від 4 до 7 атоатомів, і вказана гетероциклічна група є незаміщемів вуглецю, і вказана циклоалкільна група є заміною або заміщеною від 1 до 2 замісниками, які щеною від 1 до 3 замісниками, які незалежно винезалежно вибирають з групи, яка складається із бирають з групи, яка складається із замісників α2, замісників β, або вказані замісники α незалежно вибирають з гі(іі) гетероциклічну групу, яка має від 4 до 7 дроксигрупи і аміногрупи; і атомів, і вказана гетероциклічна група є незаміщевказані замісники β незалежно вибирають з гіною або заміщеною від 1 до 3 замісниками, які дроксигрупи і аміногрупи. незалежно вибирають з групи, яка складається із Більш переважні сполуки формули (І) даного замісників β. винаходу являють собою сполуку або її фармацеТакож, більш переважна сполука формули (І) втично прийнятну сіль, де даного винаходу являє собою сполуку або її фарHet являє собою групу формули мацевтично прийнятну сіль, де Het являє собою групу формули , А являє собою метиленову групу; В являє собою метиленову групу; , R1 являє собою ізопропільну групу; і ця група є незаміщеною або заміщеною одR2 являє собою атом фтору; m являє собою 0; ним із замісників, які вибирають з групи, яка скла1 і дається із замісників α ; R3 являє собою А являє собою метиленову групу; (і) циклоалкільну групу, заміщену від 1 до 2 В являє собою алкіленову групу, яка має від 1 замісниками, які незалежно вибирають з гідроксигдо 2 атомів вуглецю; рупи або аміногрупи, або R1 являє собою ізопропільну групу; (іі) гетероциклічну групу, яка має від 6 атомів, і R2 незалежно являє собою атом фтору, атом вказана гетероциклічна група є заміщеною гідрохлору або метил; і ксигрупою або аміногрупою. R3 являє собою Найбільш переважні сполуки формули (І) да(і) циклоалкільну групу, яка має від 5 до 7 атоного винаходу являють собою сполуку або її фармів вуглецю, і вказана циклоалкільна група є замімацевтично прийнятну сіль, де щеною від 1 до 2 замісниками, які незалежно виHet являє собою групу формули бирають з групи, яка складається із замісників α2, або (іі) гетероциклічну групу, яка має від 5 до 7 , атомів, і вказана гетероциклічна група є незаміщеА являє собою метиленову групу; ною або заміщеною від 1 до 2 замісниками, які В являє собою метиленову групу; незалежно вибирають з групи, яка складається із R1 являє собою ізопропільну групу; замісників β, R2 являє собою атом фтору; m являє собою 0; вказані замісники α незалежно вибирають з гіі дроксигрупи, аміногрупи, і алкоксигрупи, яка має R3 являє собою від 1 до 2 атомів вуглецю; і (і) циклогексильну групу, заміщену від 1 до 2 вказані замісники β незалежно вибирають з гігідроксигрупами (особливо дигідроксициклогексидроксигрупи, гідрокси-заміщеної алкільної групи, лом), або яка має від 1 до 2 атомів вуглецю, карбоксильної (іі) групу тетрагідропірану, заміщену від 1 до 2 групи, аміногрупи, аміно-заміщеної алкільної гругідроксигрупами (особливо гідрокситетрагідропірапи, яка має від 1 до 2 атомів вуглецю і карбамоїнілом). льної групи. У сполуках формули (І) або їх фармацевтично Більш переважна сполука формули (І) даного прийнятній солі, R2 переважно являє собою атом винаходу являє собою сполуку або її фармацевтифтору, атом хлору, метильну групу або етиленову чно прийнятну сіль, де групу; більш переважно атом фтору, атом хлору, Het являє собою групу формули метильну група; найбільш переважно атом фтору. У сполуках формули (І) або фармацевтично прийнятній солі, m являє собою переважно 0, 1 , або 2; більш переважно 0 або 1; ще більш переваА являє собою метиленову групу; жно 0. В являє собою метиленову групу; Переважна індивідуальна сполука даного виR1 являє собою ізопропільну групу; находу являє собою: R2 являє собою атом фтору; m являє собою 0 N-({1-[(4-гiдpoкcитeтpaгiдpo-2H-піpaн-4або 1; і iл)мeтил]пiпepидин-4-iл}мeтил)-3-ізопропіл-2-оксоR3 являє собою 2,3-дигідро-1Н-бензімідазол-1-карбоксамід; (і) циклоалкільну групу, яка має від 5 до 6 атоN-({1-[(транс-1,4мів вуглецю, і вказана циклоалкільна група є замідигідроксигексил)метил]піперидин-4-іл}метил)-3щеною від 1 до 2 замісниками, які незалежно виізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1бирають з групи, яка складається із замісників α2, карбоксамід; або N-({1-[(цис-1,4дигідроксигексил)метил]піперидин-4-іл}метил)-3 15 86204 16 ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1, одержують відповідно до наступного синтезу. карбоксамід; і І сполука формули (І), де Het інший, ніж 6-фтор-N-({1-[(4-гідрокситетрагідро-2Н-піран-4іл)метил]піперидин-4-іл}метил)-3-ізопропіл-2-оксо2,3-дигідро-1Н-бензімідазол-1-карбоксамід, , може бути одержана подібним способом або або їх фармацевтично прийнятна сіль. способом, відомим кваліфікованому в даній галузі Переважна сполука формули (2-А') даного вифахівцю. находу являє собою ту, в якій Ra являє собою атом На Стадіях 1a, 1b, 1d, 2а, 2с, 2е, 3а, 3с, 3d наводню або t-бутоксикарбонільну групу; ступних схем, кожну реакцію переважно проводять Het являє собою групу формули у присутності основи. Немає специфічного обмеження відносно природи основ, які використовують, і будь-яка основа, яку звичайно використову, ють в реакціях цього типу, може однаково бути А являє собою метиленову групу; В являє совикористана тут. Основи, які залучають, включабою метиленову групу; і ють, наприклад, гідрооксиди лужних металів, такі R3 являє собою гідрокситетрагідропіраніл або як гідроксид літію, гідроксид натрію і гідроксид кадигідроксициклогексил. лію; карбонати лужних металів, такі як карбонат Загальний синтез натрію і карбонат калію; гідриди лужних металів, Сполуки даного винаходу можуть бути одертакі як гідрид натрію, гідрид калію і гідрид літію; жані множиною способів, добре відомих для одералкоксиди лужних металів, такі як метоксид нажання сполук даного типу, наприклад, як показано трію, етоксид натрію, t-бутоксид калію і метоксид на наступних реакційних Схемах. Якщо інше не літію; алкіллітії, такі як бутиллітій і метиллітій; літій вказано R1 - R3 і m на наступних реакційних Схеаміди, такі як літій діетиламіди, літій діізопропіламах і в подальшому обговоренні є такими, як вимід і літій біс(триметилсиліл)амід; гідрогенкарбозначено вище. Термін "захисна група", як викориснати лужних металів, такі як гідрогенкарбонат натано надалі, означає гідрокси або аміно захисну трію і гідрогенкарбонат калію; і третинні органічні групу, яку вибирають з типових гідрокси або аміно аміни, такі як триетиламін, диметиланілін, піридин, захисних груп, які описані в [Protective Groups in 4-диметиламінопіридин, 1,5Organic Synthesis edited by T. W. Greene et al. діазабіцикло[4.3.0]нон-5-ен, 1,8(John Wiley & Sons, 1991)]. Всі вихідні матеріали у діазабіцикло[5.4.0]ундец-7-ен і Ν,Νнаступних загальних синтезах можуть бути комердіізопропілетиламін. ційно доступними або одержані звичайними споСинтез Бензімідазолону (1-А): собами, відомими кваліфікованим в даній галузі Наступні реакційні схеми ілюструють одерфахівцям. жання сполук бензімідазолону формули 1-А. Сполуку формули (І), де Het являє собою Схема 1а: У вищезазначених формулах, Ζ являє собою "гало", такий як атом хлору, брому або йоду. Стадія 1а На стадії 1а, аміносполуку формули 1-3 можна одержати відновлювальним амінуванням сполуки алканону (яка має від 1 до 4 атомів вуглецю) амі 17 86204 18 носполукою формули 1-1 у присутності або за відНа цій стадії сполуку формули 1-3 можна одесутності відновлювального агента або металевого ржати алкілуванням сполуки формули 1-2 сполуагента в інертному розчиннику. кою формули R'-NH2. Реакцію звичайно і переважно виконують у Реакція може мати місце при широкому діапаприсутності розчинника. Немає специфічного обзоні температур, і точна температура реакції не є меження щодо природи розчинника, який залучакритичною умовою для даного винаходу. Перевають, за умови, що він не має несприятливого жна температура реакції залежатиме від таких впливу на реакцію або на залучені реагенти і що факторів, як природа розчинника і вихідний матевін може розчинити реагенти щонайменше до деріал або реагент, які використовують. Однак, взаякої міри. Приклади прийнятних водних або невогалі, зручно проводити реакцію при температурі дних органічних розчинників включають: спирти, від 0°С до 150°С, більш переважно від 20°С до такі як метанол, етанол або ізопропінол; ефіри, 120°С. Час, який вимагається для реакції, може такі як тетрагідрофуран (THF), диметоксіетан або також широко змінюватись, залежно від багатьох діоксан; ацетонітрил; Ν,Ν'-диметилформамід; дифакторів, особливо від температури реакції і приметилсульфоксид; оцтова кислота і галогенований роди реагентів і розчинника, які залучають. Однак, вуглеводень, такий як дихлорметан, дихлоретан за умови, що реакцію виконують у переважних або хлороформ. умовах, які зазначені вище, період від 5 хвилин до Реакція може мати місце при широкому діапа48 годин, більш переважно від 30 хвилин до 24 зоні температур, і точна температура реакції не є годин, звичайно буде достатнім. критичною умовою для даного винаходу. ПереваСтадія 1с жна температура реакції залежатиме від таких Сполука формули 1-4 може бути одержана факторів, як природа розчинника і вихідний матевідновленням сполуки формули 1-3 прийнятним ріал або реагент, які використовують. Однак, взавідновлювальним агентом, таким як боргідрид нагалі, зручно проводити реакцію з відновлювальнитрію (NaBH4 ), літій алюмінійгідрид (LAH), диборан, ми агентами при температурі від -78°С до 100°С, водень і металевий каталізатор, залізо і хлористобільш переважно від близько -20°С до 60°С. Час, воднева кислота, хлорид олова і хлористоводнева який вимагається для реакції, може також широко кислота, цинк і хлористоводнева кислота, муразмінюватись, залежно від багатьох факторів, осошина кислота, боран диметилсульфідний комбливо від температури реакції і природи реагентів плекс, боран-THF, (переважно водень і металевий і розчинника, які залучають. Однак, за умови, що каталізатор), звичайно в надлишку, в реакційно реакцію виконують у переважних умовах, які заінертному розчиннику, такому як метанол, етанол, значені вище, період від 5 хвилин до 1 тижня, пропанол, бутанол, тетрагідрофуран (THF) (перебільш переважно від 30 хвилин до 24 годин, звиважно метанол або етанол), звичайно при темпечайно буде достатнім. У випадку реакції з металературі від -78°С до 60°С, переважно від близько вими реагентами, зручно проводити реакцію при 0°С до 45°С протягом від 5 хвилин до 24 годин, температурі від 20°С до 100°С, переважно від переважно від 60 хвилин до 12 годин. близько 20°С до 60°С протягом від 10 хвилин до Стадія 1d 48 годин, переважно від 30 хвилин до 24 годин. На стадії 1d, аміносполуку формули 1-4 можна Прийнятні відновлювальні реагенти являють одержати за допомогою відновлювального амінусобою ті, які звичайно використовують при відноввання сполуки алканону аміносполукою формули ленні, наприклад, боргідрид натрію, ціаноборгід1-5 у подібних умовах, що і на стадії 1а. рид натрію або триацетоксиборгідрид натрію. Альтернативно, сполуку формули 1-4 можна Поєднання металевих реагентів і водневого одержати алкілуванням сполуки формули 1-5 спогазу може бути також залучене як відновлювальлукою формули Z-R1. ний реагент. Приклади прийнятних металевих реаРеакція може мати місце при широкому діапагентів включають паладій-вуглець, паладійгідрокзоні температур, і точна температура реакції не є сид-вуглець, платино-оксид, платино-вуглець, критичною умовою для даного винаходу. Переварутеній-вуглець, родій-алюмінооксид і жна температура реакції залежатиме від таких трис[трифенілфосфін]родійхлорид. Відновлення факторів, як природа розчинника і вихідний матеметалевими реагентами може бути проведене у ріал або реагент, які використовують. Однак, взаатмосфері водню при тиску від 1 до 100атм., перегалі, зручно проводити реакцію при температурі важно від 1 до 10атм. від 0°С до 120°С, більш переважно від 0°С до Це відновлення може бути проведене після 70°С. Час, який вимагається для реакції, може утворення відповідного енаміну сполуки алканону також широко змінюватись, залежно від багатьох або аміну сполуки алканону в реакційно інертному факторів, особливо від температури реакції і прирозчиннику, такому як бензол, толуол або ксилол роди реагентів і розчинника, які залучають. Однак, при температурі в діапазоні від 20 до 130°С протяза умови, що реакцію виконують у переважних гом від 1 години до 1 тижня. умовах, які зазначені вище, період від 5 хвилин до Альтернативно, сполуку формули 1-3 можна 48 годин, більш переважно від 30 хвилин до 24 одержати алкілуванням сполуки формули 1-1 алгодин, звичайно буде достатнім. кіл галідом формули Z-R1, де Ζ являє собою гало Стадія 1е (гало являє собою хлор, бром або йод), що по суті Сполука формули 1-А може бути одержана є тією ж умовою, що і зазначена нижче (Стадія 1d), циклізацією сполуки формули 1-4 з прийнятним переважно у присутності основи. карбонілуючим агентом, таким як карбонілдіімідаСтадія 1b зол, трихлорметил хлорформіат, трифосген і сечовина (переважно карбонілдіімідазол), звичайно 19 86204 20 Альтернативно, сполука формули 1-А (в якій в надлишку, в реакційно інертному розчиннику, R1 являє собою ізопропіл, як показано на Схемі 1b) такому як диметоксіетан, діоксан, ацетонітрил, може бути одержана зі сполуки алкенілΝ,Ν'-диметилформамід, диметилсульфоксид, дихбензімідазолону формули 1-6 відповідно до настулорметан, дихлоретан, хлороформ або тетрагідпної Схеми 1b в реакційних умовах, відомих кварофуран (THF) (переважно THF), звичайно при ліфікованому в даній галузі фахівцю. температурі -78°С до 120°С, переважно від близько 20°С до 100°С протягом від 5 хвилин до 24 годин, переважно від 60 хвилин до 12 годин. Схема Ib Синтез частини аміну (2-А): Наступні реакційні схеми ілюструють одержання сполук піперидину формули (2-А). Схема 2a У вищезазначених формулах, PG являє собою захисну групу. Термін "захисна група", як використано тут, означає аміно захисну групу, яку вибирають з типових аміно захисних груп, які розкриті в [Protective Groups in Organic Synthesis edited by T. W. Greene et al. (John Wiley & Sons, 1991)]. Типові аміно захисні групи включають бензил, С2Н5О(С )-, = О СН= )-, О трет3(С бутилдиметилсиліл (TBS), третбутилдифенілсиліл, бензилоксикарбоніл, представлений як Z, і трет-бутоксикарбоніл, представлений як t-Boc або Вос. Сполука формули 2-2 може бути одержана алкілуванням або відновлювальним амінуванням сполуки формули 2-1 сполукою формули алкіл R3, гало-R3 або H(C=O)-R3 у подібних умовах, що і на стадії 1а. Коли -B-R3 являє собою 4гідрокситетрагідропіранілметил, це алкілування може бути здійснено за допомогою використання сполуки 1,6-діоксаспіро[2,5]октану. Потім, цю реакцію продовжують зняттям захисту з тим, щоб одержати сполуку формули 1-А. Це зняття захисту може бути проведено відповідно до методик, відомих кваліфікованим в даній галузі фахівцям, щоб одержати сполуку формули 2-А. Альтернативно, сполука формули (2-А) може бути одержана зі сполуки піперидину формули 23 відповідно до наступної Схеми 2b з реакційними умовами, відомими кваліфікованим фахівцям. Схема 2b (А1 являє собою ковалентний зв'язок або С13алкілeн). Наприклад, на стадії 2с, сполука 2-4 може бути одержана алкілуванням або відновлювальним амінуванням по суті в тих же умовах, що і розкриті на стадії 2а Схеми 2а. Потім, відновлення на стадії 2d може бути проведене у присутності відновлювального реагенту, такого як LiAlH4 в реак ційно інертному розчиннику, такому як THF. Прийнятна температура реакції варіює від близько 78°С до близько 100°С, переважно від близько 30°С до близько 40°С. Сполука формули (1-А) може бути одержана за сполуки піперидину формули 2-5 відповідно до наступної Схеми 2с в реакційних умовах, відомих кваліфікованому фахівцю. 21 86204 22 Схема 2c (А1 являє собою ковалентний зв'язок або С13алкілен) Наприклад, на стадії 2е, сполуки 2-6 можуть бути одержані алкілуванням або відновлювальним амінуванням в подібних умовах, що розкриті на стадії 2а Схеми 2а. Потім, відновлення на стадії 2f може бути проведене у присутності Н2 і каталізатора гідрогенізації, такого як PtO2, в реак ційно інертному розчиннику, такому як THF. Прийнятна температура реакції варіює від близько -78°С до близько 100°С, переважно від близько -30°С до близько 40°С. Синтез сполуки формули (І): Наступні реакційні схеми ілюструють одержання сполук бензімідазолону формули І. Схема 3a Стадія 3а Сполука формули 3-1 може бути одержана карбонілуванням сполуки формули 1-А сполукою формули 2-А у присутності прийнятного карбонілуючого агента, такого як карбонілдіімідазол, трихлорметил хлорформіат, трифосген, 4нітрофеніл хлорформіат або сечовина (переважно трифосген), звичайно в надлишку, в реакційно інертному розчиннику, такому як диметоксіетан, діоксан, ацетонітрил, Ν,Ν'-диметилформамід, диметилсульфоксид, дихлорметан, дихлоретан, тетрагідрофуран (THF), бензол, толуол або хлороформ (переважно THF), звичайно при температурі від -78°С до 120°С, переважно від близько 0°С до 90°С протягом від 5 хвилин до 24 годин, переважно від 60 хвилин до 12 годин. Стадія 3b: Сполуку формули 3-2 одержують зняттям захисту сполуки формули 3-1 кислотою, такою як хлористоводнева кислота. Стадія 3с: Сполука формули (Іа) може бути одержана алкілуванням або відновлювальним амінуванням в подібних умовах, що розкриті на стадії 2а Схеми 2а. Альтернативно, сполука формули (Іа) може бути одержана зі сполук алкіл-бензімідазолону відповідно до наступної Схеми 3b в реакційних умовах, відомих кваліфікованому фахівцю. Схема 3b Наприклад, на стадії 3d, сполука формули 1А може бути піддана реакції зі сполукою формули 2-А у присутності карбонілуючого агента, такого як карбонілдіімідазол, трихлорметил хлорформі ат, трифосген, 4-нітрофеніл хлорформіат або сечовина (переважно трифосген), звичайно в надлишку, в реакційно інертному розчиннику, такому як диметоксіетан, діоксан, ацетонітрил, 23 86204 24 Ν,Ν'-диметилформамід, диметилсульфоксид, Сполука формули 7 може бути одержана за дихлорметан, дихлоретан, тетрагідрофуран допомогою використання реакції, відомої кваліфі(THF), бензол, толуол або хлороформ (переважкованому фахівцю. Наприклад, сполука формули но THF), звичайно при температурі від -78°С до 7 може бути одержана за сполуки формули 3 120°С, переважно від близько 0°С до 90°С протявідповідно до наступної Схеми 3с в реакційних гом від 5 хвилин до 24 годин, переважно від 60 умовах, відомих кваліфікованому фахівцю. хвилин до 12 годин. Схема 3с На вищезазначених Схемах від la до 3с, приклади прийнятних розчинників включають суміш будь-яких двох або більше тих розчинників, які описані на кожній Стадії. Сполуки формули (І) і проміжні сполуки вищезазначених способів одержання можуть бути виділені і очищені звичайними методиками, такими як дистиляція, перекристалізація або хроматографічне очищення. Оптично активні сполуки даного винаходу можуть бути одержані декількома способами. Наприклад, оптично активні сполуки даного винаходу можуть бути одержані хроматографічним розділенням, ферментативним розщепленням або фракціонованою кристалізацією з кінцевих сполук. Різні сполуки даного винаходу мають асиметричний центр. Тому, сполуки можуть існувати у відокремленій (+)- і (-)-оптично активній формах, також як і в рацемічній формі. Даний винахід включає всі такі форми в своєму об'ємі. Індивідуальні ізомери можуть бути одержані відомими способами, такими як оптично селективна реакція або хроматографічне розділення у приготуванні кінцевого продукту або його проміжної сполуки. Даний винахід також включає ізотопічномічені сполуки, які ідентичні до тих, які викладені у формулі (І), але з тим, що один або більше атомів заміщені атомом, який має атомну масу або масове число, яке відрізняється від атомної маси або масового числа, яке звичайно знаходять у природі. Приклади ізотопів, які можуть бути включені у сполуки винаходу включають ізотопи водню, вуглецю, азоту, кисню, фосфору, фтору і хлору, такі як 2Н, 3Н, 13С, 14С, 15 N, 18О, 17 31 0, Р, 32Р, 35S, 18F і 36Сl, відповідно. Сполуки даного винаходу, їх проліки, фармацевтично прийнятні ефіри вказаних сполук і фармацевтич но прийнятні солі вказаних сполук, вказаних ефірів або вказаних проліків, які містять зазначені вище ізотопи і/або інші ізотопи інших атомів знаходяться в об'ємі даного винаходу. Конкретні ізотопічно-мічені сполуки даного винаходу, наприклад ті, в які включені радіоактивні ізотопи, такі як 3H і 14С, є корисними у дослідженні розподілу ліків та/або субстрату у тканині. Тритійовані, тобто, 3Н, і вуглець-14, тобто, 14С, ізотопи є зокрема переважними через легкість їх представлення і здатність до виявлення. Надалі, заміна більш важкими ізотопами, такими як дейтерій, тобто, 2Н, може привести до терапевтичної переваги, яка виникає через більшу метаболічну стабільність, наприклад, збільшений in vivo час півжиття або зменшена вимога до дозування і, тому, можуть бути переважними за деяких обставин. Ізотопічно-мічені сполуки формули (І) даного винаходу і їх проліки можуть бути звичайно одержані за допомогою проведення процедури, розкритої у вищезазначених Схемах і/або Прикладах і Приготуваннях, викладених нижче, за допомогою представлення легкодоступного ізотопічноміченого реагенту для неізотопічно-міченого реагенту. Даний винахід включає сольові форми сполук (І), як одержано. Фармацевтично прийнятні солі сполук формули (І) включають їх кислотно-адитивні і основно-адитивні солі (включаючи дисолі). Фармацевтично прийнятні нетоксичні солі сполук формули (І) можуть бути одержані звичайними методиками за допомогою, наприклад, контактування вказаної сполуки зі стехіометричною кількістю гідроксиду або алкоксиду відповідного лужного або лужноземельного металу (натрію, калію, кальцію і магнію) у воді або відповідному органічному розчиннику, такому як етанол, ізопропанол, їх суміші, або подібне. 25 86204 26 (2-А'), являють собою ті, які утворюють основноОснови, які використовують для одержання адитивні солі. Такі основно-адитивні солі вклюфармацевтично прийнятних основно-адитивних чають фармацевтично прийнятні основносолей сполук даного винаходу формули (І), явадитивні солі, як описано вище, і солі, які містять ляють собою ті, які утворюють нетоксичні основкатіони, такі як триетиламін, піридин і аміак. но-адитивні солі, тобто, солі, які містять фармаСполуки формули (2-А') здатні до утворення цевтично прийнятні катіони, такі як аденін, широкої різноманітності різних солей з різними аргінін, цитозин, лізин, бенетамін (тобто, Nнеорганічними і органічними кислотами. бензил-2-фенілетиламін), бензатин (тобто, Ν,ΝКислоти, які використовують, щоб одержати дибензилетилендіамін), холін, діоламін (тобто, кислотно-адитивні солі сполуки формули (2-А'), діетаноламін), етилендіамін, глюкозамін, гліцин, являють собою ті, які утворюють кислотногуанідин, гуанін, меглюмін (тобто, Nадитивні солі. Такі кислотно-адитивні солі вклюметилглюкамін), нікотинамід, оламін (тобто, етачають фармацевтично прийнятні кислотноноламін), орнітин, прокаїн, пролін, піридоксин, адитивні солі, як описано вище, і солі, які містять серин, тирозин, валін та трометамін (тобто, трис аніони, такі як ціанід. або трим(гідроксиметил)амінометан). ОсновноТакож включені в об'єм даного винаходу біоадитивні солі можуть бути одержані звичайними попередники (також названі проліками) сполук методиками. формули (І). Біопопередник сполуки формули (І) В тій мірі, як конкретні сполуки даного винаявляє собою її хімічну похідну, яка легко може ходу являють собою основні сполуки, вони здатні бути перетворена назад в батьківську сполуку до утворення широкої різноманітності різних соформули (І) в біологічних системах. Зокрема, лей з різними неорганічними і органічними кислобіопопреденик сполуки формули (І) перетворютами. ють назад в батьківську сполуку формули (І) пісКислоти, які використовують для одержання ля того, як біопопередник був введений до, і абфармацевтично прийнятних кислотно-адитивних сорбувався, ссавцю, наприклад, людині. солей основних сполук даного винаходу формули Наприклад, можливо зробити біопопередник спо(І), являють собою ті, які утворюють нетоксичні лук формули (І), в якій один або обидва L і W кислотно-адитивні солі, тобто, солі, які містять включають гідроксигрупи, утворюючи ефір гідрофармацевтично прийнятні аніони, такі як хлорид, кисигрупи. Коли тільки один з L і W включає гідбромід, йодид, нітрат, сульфат або бісульфат, роксигрупу, тільки моноефір є можливим. Коли як фосфат або кислотний фосфат, ацетат, лактат, L, так і W включають гідрокси, моно- і ді-ефіри цитрат або кислотний цитрат, тартрат або бі(які можуть бути однаковими або різними) можуть тартрат, сукцинат, малат, фумарат, глюконат, бути одержані. Типові ефіри являють собою просахарат, бензоат, метансульфонат, етансульфості ефіри алканоату, такі як ацетат, пропіонат, нат, бензолсульфонат, р-толуолсульфонат, адибутират і т.д. Крім того, коли L або W включає пат, аспарат камзилат, едизилат (тобто 1,2гідроксигрупу, біопопередники можуть бути одеретандисульфонат), естолат (тобто лаурил сульжані за допомогою перетворення гідроксигрупи в фат), глюцептат (тобто глюкогептонат), глюконат, похідне ацилоксиметилу (наприклад, похідне пів3-гідрокси-2-нафтоат, ксионофоат (тобто 1алоїлоксиметилу) реакцією з галідом ацилоксигідрокси-2-нафтоат), ізетіонат (тобто 2метилу (наприклад, хлоридом півалоїлоксиметигідроксіетансульфонат), мукат (тобто галактарат), лу). 2-нафзилат (тобто нафталенсульфонат, стеарат, Коли сполуки формули (І) даного винаходу холат, глюкоронат, глутамат, гіпурат, лактобіоможуть утворювати сольвати, такі як гідрати, такі нат, лізинат, малеат, манделат, нападизилат, сольвати включені в об'єм даного винаходу. нікатинат, полігалактуронат, саліцилат, сульфоСполуки формули (І), які містять один або бісаліцилат, танат, триптофанат, борат, карбонат, льше асиметричних атомів вуглецю, можуть існуолеат, фталат і памоат (тобто 1,1'-метилен-біс-(2вати як два або більше стереоізомерів. Там, де гідрокси-3-нафтоат). З них перевага віддається сполука формули (І) містить алкенільну або аледизилату (включаючи гемі-едизилат) і гідрохлокеніленільну групу, можливі геометричні риду. Кислотно-адитивні солі можуть бути одерцис/транс (або Ζ/Ε) ізомери. Там, де сполука місжані звичайними методиками. тить, наприклад, групу кето або оксиму або ароДля огляду прийнятних солей дивіться [Berge матичну частину, може виникнути таутомерний et аl., J. Pharm. Sci., 66, 1-19, 1977]. ізомеризм ("таутомеризм"). Це є наслідком того, Даний винахід включає сольові форми сполук що окрема сполука може проявляти більше ніж формули (2-А'), як одержано. один тип ізомеризму. Сполуки формули (2-А') можуть бути здатні Включеними в об'єм даного винаходу є всі до утворення катіонів. Катіони сполук формули стереоізомери, геометричні ізомери і таутомерні (2-А') можуть бути одержані звичайними методиформи сполук формули (І), включаючи сполуки, ками за допомогою, наприклад, контактування які проявляють більше ніж один тип ізомеризму, і сказаної сполуки зі стехіометричною гідроксиду суміші одного або більше з них. Також включениабо алкоксиду відповідного лужного або лужноми є кислотно-адитивні або основно-адитивні земельного металу (натрію, калію, кальцію і магсолі, де протиіон є оптично активним, наприклад, нію) у воді або відповідному органічному розчинD-лактат або L-лізин; або рацемічним, наприклад, нику, такому як етанол, ізопропанол, їх суміші, DL-тартрат або DL-аргінін. або подібне. Цис/транс ізомери можуть бути розділені Основи, які використовують, щоб одержати звичайною методикою, добре відомою кваліфікоосновно-адитивні солі кислотних сполук формули 27 86204 28 мульти- і нано-частинки, гелі, твердий розчин, ваним в даній галузі фахівцям, наприклад, хроліпосом, плівки (включаючи муко-адгезивні), овуматографією і фракціонованою кристалізацією. лі, спреї і рідкі склади. Звичайні методики для одержання/виділення Рідкі склади включають суспензії, розчини, індивідуальних енантіомерів включають хіральсиропи і еліксири. Такі склади можуть бути залуний синтез з прийнятного оптично чистого попечені як наповнювачі в м'яких або твердих капсуредника або розщеплення рацемату (або рацелах і звичайно містять носій, наприклад, воду, мату солі або похідного), наприклад, хіральна етанол, поліетилен гліколь, пропілен гліколь, мерідинна хроматографія високого тиску (РХВТ). тилцелюлозу або прийнятну олію, і один або біАльтернативно, рацемат (або рацемічний польше емульгуючих агентів і/або суспендуючих передник) можуть бути піддані реакції з прийнятагентів. Рідкі склади можуть також бути одержані ною оптично активною сполукою, наприклад, відновленням вологовмісту твердої речовини, спиртом, або, у випадку, де сполука формули (І) наприклад, з саше. містить кислотну або основну частину, кислота Сполуки винаходу можуть бути також викориабо основа, така як винна кислота або 1стані у швидко розчинних, швидко дезинтегруюфенілетиламін. Одержана ліастереомерна суміш чих дозованих формах, такі як описані в [Expert може бути розділена хроматографією і/або фракOpinion in Therapeutic Patents, 11 (6), 981-986 by ціонованою кристалізацією і одним або обидва Liang and Chen (2001)]. стереоізмери, які перетворюють у відповідний Для дозованих форм у формі таблеток, зачистий енантіомер(и) способами, добре відомими лежно від дози, лікарський засіб може складати кваліфікованому фахівцю. від 1ваг.% до 80ваг.% дозованої форми, більш Стереоізомерні конгломерати можуть бути звичайно від 5ваг.% до 60ваг.% дозованої форрозділені звичайними методиками, відомими квами. В доповнення до лікарського засобу, таблетліфікованим в даній галузі фахівцям, дивіться, ки звичайно дезинтегрант. Приклади дезинтегранаприклад, ["Stereochemistry of Organic Comнтів включають натрій крохмаль гліколят, натрій pounds" by Ε L Eliel (Wiley, New York, 1994)]. карбоксиметил целюлозу, кальцій карбоксиметил Сполуки даного винаходу, призначені для целюлозу, натрій кроскармелозу, кросповідон, фармацевтичного використання, можуть вводиполівінілпіролідон, метил целюлозу, мікрокристатись як кристалічні або аморфні продукти. Вони лічну целюлозу, нижчу алкіл-заміщену гідроксипможуть бути одержані, наприклад, як тверді проропіл целюлозу, крохмаль, прежелатинізований бки, порошки або плівки способами, такими як крохмаль і натрій альгінат. Звичайно, дезинтегосадження, кристалізація, сушіння виморожуванрант буде містити від 1ваг. 1% до 25ваг.%, переням, розпилювальне сушіння або сушіння випаважно від 5ваг.% до 20ваг.% дозованої форми. рюванням. Індукційне або радіочастотне сушіння Зв'язувальні речовини звичайно використоможе бути використане з цією метою. вують, щоб надати когезійні властивості складам Вони можуть бути ведені окремо або в поєду формі таблеток. Прийнятні зв'язувальні речонанні з однією або більше іншими сполуками вивини включають мікрокристалічну целюлозу, женаходу або в поєднанні з одним або більше інлатин, цукор, поліетилен гліколь, природні і синшими лікарськими засобами (або як будь-яка їх тетичні камеді, полівінілпіролідон, комбінація). Звичайно, їх будуть вводити як склад прежелатинізований крохмаль, гідроксипропіл у поєднанні з одним або більше фармацевтично целюлозу і гідроксипропіл метилцелюлозу. Табприйнятними ексципієнтами. Термін "ексципієнт" летки можуть також містити розріджувачі, такі як використовують тут, щоб описати будь-який інглактоза (моногідрат, висушують розпилюванням редієнт, інший, ніж сполука(и) винаходу. Вибір моногідрат, ангідрид і тому подібне), маніт, ксиліексципієнта буде у великій мірі залежати від татол, глюкозу, сахарозу, сорбіт, мікрокристалічну ких факторів, як конкретний спосіб введення, целюлозу, крохмаль і двоосновний кальцій фосвплив ексципієнта на розчинність і стабільність і фат дигідрат. природи форми дозування. Таблетки можуть також необов'язково містиФармацевтичні композиції, прийнятні для доти поверхнево-активні агенти, такі як лаурил суставки сполук даного винаходу і способів їх одельфат натрію і полісорбат 80, і гліданти, такі як ржання, легко будуть очевидні для кваліфіковадіоксид кремнію і тальк. Коли присутні, поверхнених в даній галузі фахівців. Такі композиції і во-активні агенти можуть включати від 0,2ваг.% способи їх одержання можуть бути знайдені, надо 5ваг.% таблетки, і гліданти можуть містити від приклад, в ['Remington's Pharmaceutical Sciences', 0,2ваг.% до 1ваг.% таблетки. 19th Edition (Mack Publishing Company, 1995)]. Таблетки також звичайно містять змащувачі, Оральне введення такі як стеарат магнію, стеарат кальцію, стеарат Сполуки даного винаходу можуть бути ввецинку, стеариловий фумарат натрію, і суміші стедені орально. Оральне введення може включити арату магнію з лаурил сульфатом натрію. Змаковтання, так, щоб сполука потрапляли у шлунщувачі звичайно містять від 0,25ваг.% до ково-кишковий тракт, або може бути залучене 10ваг.%, переважно від 0,5ваг.% до 3ваг.% таббукальне або під'язикове введення, за допомогою летки. якого сполука входить в потік крові безпосередІнші можливі інгредієнти включають антиокньо з рота. сиданти, барвники, смакові агенти, консерванти і Склади, прийнятні для орального введення, агенти, які маскують смак. включають тверді склади, такі як таблетки, капТаблетки для прикладу містять до близько сули, які містять частинки, рідини або порошки, 80% лікарського засобу, від близько 10ваг.% до коржики (включаючи наповнені рідиною), гумки, 29 86204 30 близько 90ваг.% зв'язувальної речовини, від блиСклади для парентерального введення мозько 0ваг.% до близько 85ваг.% розріджувача, від жуть бути складені таким чином, щоб бути склаблизько 2ваг.% до близько 10ваг.% дезинтеграндами негайного і/або зміненого вивільнення. та, і від близько 0,25ваг.% до близько 10ваг.% Склади зміненого вивільнення включають склади змащувача. затриманого, тривалого, імпульсного, контрольоСуміші таблеток можуть бути ущільнені безваного, спрямованого і програмованого вивільпосередньо або роликом, щоб створити таблетки. нення. Так, сполуки винаходу можуть складатись Суміші таблеток або порції сумішей можуть альяк тверда речовина, напівтверда речовина або тернативно бути волого-, сухо- або плавкотиксотропна рідина для введення як імплантовагранульованими, плавко-замороженими або ексний склад, що забезпечує змінене звільнення трудованими перед таблетуванням. Остаточний активної сполуки. Приклади таких складів вклюсклад може містити один або більше шарів і може чають покриті лікарським засобом ендопротези бути покритий або непокритий; він може навіть судини і PGLA мікросфери. бути інкапсульований. Місцеве введення Склад таблеток обговорюється у ["PharmaСполуки винаходу можуть також бути введені ceutical Dosage Forms: Tablets, Vol.1", by H. Lieмісцево у шкіру або слизову оболонку, тобто, berman and L. Lachman, Marcel Dekker, N.Y.. N.Y., шкірно або черезшкірно. Типові склади для цього 1980 (ISBN 0-8247-6918-Х)]. включають гелі, гідрогелі, лосьйони, розчини, Тверді склади для орального введення мокреми, мазі, опудрювальні засоби, пов'язки, піни, жуть бути складені таким чином, щоб бути склаплівки, шкірні пластирі, губки, імплантати, тамподами негайного і/або зміненого вивільнення. ни, волокна, бинти і мікроемульсії. Ліпосоми таСклади зміненого вивільнення включають склади кож можуть бути використані. Типові носії вклюзатриманого, тривалого, імпульсного, контрольочають спирт, воду, мінеральне масло, рідкий ваного, спрямованого і програмованого вивільвазелін, білий вазелін, гліцерин, поліуетиленглінення. коль і пропіленгліколь. Підсилювачі проникнення Прийнятні склади зміненого вивільнення для можуть бути введені, дивіться, наприклад, [J. цілей даного винаходу розкриті у в [US Патенті Pharm Sci, 88 (10), 955-958 by Finnin and Morgan №6,106,864]. Деталі інших прийнятних технологій (October 1999)]. вивільнення, так як високоенергійні дисперсії і Інші засоби місцевого введення включають осмотичні і покриті частинки розкриті у [Verma et доставку електропорацією, іонтофорезом, фоноal., Pharmaceutical Technology On-line. 25(2), 1-14 форезом, сонофорезом і мікроколговою або без(2001)]. Застосування жувальної гумки, щоб досяголковою (наприклад Powderject™, Bioject™ і т.д.) гнути контрольованого вивільнення, розкрите у ін'єкцією. [WO 00/35298]. Склади для місцевого введення можуть бути Парентеральне введення складені таким чином, щоб бути складами негайСполуки винаходу можуть бути також введені ного і/або зміненого вивільнення. Склади змінебезпосередньо в потік крові, в м'яз або у внутріного вивільнення включають склади затриманого, шній орган. Прийнятні засоби для парентеральтривалого, імпульсного, контрольованого, спряного введення включають внутрішньовенні, внутмованого і програмованого вивільнення. рішньоартеріальні, внутрішньочеревинні, Вдихуване/штраназальне введення інтратекальні, внутрішньошлункові, внутрішньоСполуки винаходу можуть бути також введені уретральні, інтрастемальні, інтраакраніальні, інтраназально або інгаляцією, звичайно у формі внутрішньом'язові і підшкірні. Прийнятні пристосухого порошку (або одного, або як суміш, наприсування для парентерального введення включаклад, в сухій суміші з лактозою, або як частинка зі ють голкові (включаючи мікроголкові) інжектори, змішаних компонентів, наприклад, змішана з фоінжектори, вільні від голок, і пристрої вливання. сфоліпідами, як фосфатидилхолін) з порошковоПарентеральні склади звичайно являють сого інгалятора або, як аерозольний спрей з аеробою водні розчини, які можуть містити ексципієнзольного контейнера, насосу, спрею, ти, такі як солі, вуглеводні і буферні агенти (пепульверизатора (переважно пульверизатора, реважно до рН від 3 до 9), але, для деяких використовуючи електродинаміки, щоб виробити застосувань, вони можуть бути більш прийнятно тонкоподрібнену димку), або розпилювача, з або складені як стерильний неводний розчин або як без використання прийнятного пропеленту, таковисушена форма, для використання у поєднанні з го як 1,1,1,2-тетрафторетан або 1,1,1,2,3,3,3прийнятним носієм, таким як стерильна вільна від гептафторетан. Для інтраназального застосуванпірогену вода. ня, порошок може містити біоадгезивний агент, Одержання парентеральних складів у стеринаприклад, цитозан або циклодекстрин. льних умовах, наприклад, ліофілізацією, може Аерозольний контейнер, насос, спрей, пульохоче легко проведене стандартними фармацевверизатор або розпилювач містить розчин або тичними методиками, добре відомими кваліфікосуспензію сполук(и) винаходу, що містить, наприваним в даній галузі фахівцям. клад, етанол, водний етанол або прийнятний Розчинність сполук формули (І), які викорисальтернативний агент для диспергування, солютовують в одержання паретнтеральних розчинів білізування або продовженого вивільнення від може бути збільшена використанням відповідних активної речовини, пропелент(и) як розчинник і методик складання у склади, таких як введення необов'язковий суфрактант, такий як сорбіт триоагентів, які збільшують розчинність. леат, олейнова кислота або олігомолочна кислота. 31 86204 32 бути складами негайного і/або зміненого вивільПеред тим, як використовувати у складі сухонення. Склади зміненого вивільнення включають го порошку або суспензії, лікарський продукт міксклади затриманого, тривалого, імпульсного, конронізують до розміру, прийнятного для доставки трольованого, спрямованого і програмованого інгаляцією (звичайно менше ніж 5 мікронів). Це вивільнення. може бути досягнуте будь-яким відповідним споОчне/вушне введення собом подрібнення у порошок, таким як подрібСполуки винаходу можуть також бути введені нення спіральним струменем, струминне подріббезпосередньо в око або вухо, звичайно у формі нення псевдозрідженим шаром, обробка крапель мікронізованої суспензії або розчину в понадкритичним середовищем з тим, щоб сфорізотонічному, рН-регульованому стерильному мувати наночастинки, гомогенізація високого тиссольовому розчині. Інші склади, прийнятні для ку або розпилювальне сушіння. очного і вушного введення, включають мазі, біоКапсули (зроблені, наприклад, з желатину раскладані (наприклад абсорбовані гелеві губки, або НРМС), витяжні пластирі та картриджі для колаген) і небіораскладані (наприклад силікон) застосування в інгаляторі або інсуфляторі моімплантати, облатки, лінзи і гранульовані або жуть бути складені таким чином, щоб містити везикулярні системи, такі як ніосоми або ліпосопорошкову суміш сполуки винаходу, прийнятну ми. Полімер, такий як зшита поліакрилова кислопорошкову основу, таку як лактоза або крохмаль і та, полівінілспирт, гіалуронова кислота, целюломодифікатор швидкодії, такий як 1-лейцин, маніт зний полімер, наприклад, або стеарат магнію. Лактоза може бути ангідридгідроксипропілметилцелюлоза, гідроксіетилценою або у формі моногідрату, переважно останлюлоза, або метилцелюлоза, або гетерополісанє. Інші прийнятні ексципієти включають декхаридний полімер, наприклад, геланова камедь, стран, глюкозу, мальтозу, сорбіт, ксилітол, можуть бути введені разом з консервантом, тафруктозу, сахарозу і трегалозу. ким як бензалконій хлорид. Такі склади можуть Склад прийнятного розчину для застосування також бути введені іонтофорезом. в пульверизаторі, використовуючи електродинаСклади для очного/вушного введення можуть міку, щоб виробити тонкоподрібнену димку, може бути складені таким чином, щоб бути складами містити від 1мкг до 20мг сполуки винаходу за принегайного і/або зміненого вивільнення. Склади ведення у дію і об'єм приведення у дію може змізміненого вивільнення включають склади затринюватись від 1мкл до 100мкл. Типовий склад моманого, тривалого, імпульсного, контрольованоже містити сполуку формули (І), пропіленгліколь, го, спрямованого і програмованого вивільнення. стерильну воду, етанол і хлорид натрію. АльтерІнші технології нативні розчинники, які можуть використовуваСполуки винаходу можуть бути об'єднані з тись замість пропіленгліколю, включають гліцерозчинними макромолекулярними об'єктами, тарин і поліетиленгліколь. кими як циклодекстрин і його прийнятні похідні Прийнятні смакові домішки, такі як ментол і або поліетилен гліколь-вмісні полімери, для того, левоментол, або підсолоджувачі, такі як сахарин щоб вдосконалити міру їх розчинності, розклаабо сахарин натрій, можуть бути додані до таких дання, маскування смаку, біодоступності і/або складів винаходу, призначених для вдихуваностабільності для застосування у будь-яких вищего/інтраназального введення. зазначених способах введення. Склади для вдихуваного/інтраназального Комплекси лікарський засіб-циклодекстрин, введення можуть бути складені таким чином, щоб наприклад, звичайно корисні для більшості дозобути складами негайного і/або зміненого вивільваних форм і шляхів введення. Можуть бути винення, наприклад, полі(DL-молочна-співгліколева користані як адукти, так і неадукти. Як альтернакислота (PGLA). Склади зміненого вивільнення тива до прямого утворення комплексу з включають склади затриманого, тривалого, імпулікарським засобом, циклодекстрин може бути льсного, контрольованого, спрямованого і провикористаний як допоміжна домішка, тобто, як грамованого вивільнення. носій, розріджувач або солюбілізатор. Найбільш У випадку сухих порошкових інгаляторів і аечасто використовують для цих цілей альфа-, берозолів, одиниця дозування визначається за дота- і гама-циклодекстрини, приклади яких можуть помогою клапана, який доставляє дозовану кільбути знайдені у [патентних заявках №№WO 91 кість. Одиниці відповідно до винаходу звичайно /11172, WO 94/02518 і WO 98/55148]. приладжують так, щоб вводити дозовану кількість Набори або "вдих", що містить від 1 до 100мкг сполуки Оскільки може бути бажаним введення комформули (І). Загальна щоденна доза звичайно бінації активних сполук, наприклад, з метою лікубуде знаходитись в діапазоні від 50мкг до 20мг, вання конкретного захворювання або стану, в що може бути введене як єдина доза або, більш об'ємі даного винаходу лежить те, що дві або звичайно, як розділені дози протягом дня. більше фармацевтичних композицій, щонайменРектальне/інтравагінальне введення ше одна з яких містить сполуку відповідно до виСполуки винаходу можуть вводитись ректанаходу, можуть зручно бути об'єднані у формі льно або вагінально, наприклад,ув формі супозинабору, прийнятного для співведення композицій. торію, песарію або клізми. Масло-какао є традиТак, набір за винаходом включає дві або біційною осоновою супозиторію, але різні льше окремі фармацевтичні композиції, щонайальтернативи можуть такою бути використані, де менше одна з яких містить сполуку формули (І) прийнятно. відповідно до винаходу, і засоби для окремого Склади для ректального/вагінального ввезберігання згаданих композицій, такі як контейдення можуть бути складені таким чином, щоб 33 86204 34 (іх) антагоністів кальцію, наприклад, аранідинер, розділена пляшка або розділений фольговий пін, лацидипін, фалодипін, азелнідипін, клінідипакет. Приклад такого набору являє собою добре пін, ломеризин, дилтіазем, галопаміл, ефонідипін, знайому блістерну упаковку, яка використовуєтьнізолдипін, амлодипін, лерканідипін, бевантоло, ся для пакування таблеток, капсул і тому подібне. нікардипін, ізрадипін, бенідипін, верапаміл, нітреНабір за винаходом зокрема прийнятний для ндипін, барнідипін, пропафенон, манідипін, бепвведення різних дозованих форм, наприклад, ридил, ніфедипін, нілвадипін, німодипін, ніфедиоральних і парентеральних, для введення окрепін іфазудил; мих композицій з різними інтервалами дозування, (х) агоністи бензодіазепіну, наприклад, діазеабо для титрування окремих композицій одна пам, залеплон, золпідем, галоксазолам, клоназепроти іншої. Щоб сприяти відповідності, набір пам, празепам, квазепам, флутазолам, триазозвичайно містить керівництва для введення і молам, лорметазепам, мідазолан, тофізопам, же бути забезпечений так званою пам'яткою. клобазам, флунітразепам і флутопразепам; Дозування (хі) аналоги простагландину, наприклад ПроДля введення людині, загальна щоденна достагландин, мізопростол, трепростиніл, езопросза сполук винаходу звичайно знаходиться в діатенол, латанопрост, ілопрост, берапрост, енпроспазоні від 0,05мг до 100мг залежно, звичайно, від тил, ібудиласт і озагрел; способу введення, переважно в діапазоні від (хіі) гістамін Н3 агоністи, наприклад, R-альфа0,1мг до 50мг і більш переважно в діапазоні від метилгістамін і ВР-294; 0,5мг до 20мг. Наприклад, оральне введення мо(хііі) протишлункові агенти, наприклад, Проже вимагати загальну щоденну дозу від 1мг до тишлункова вакцина, ітриглумід і Z-360; 20мг, в той час як внутрішньовенна доза може (xiv) 5-НТ3 антагоністи, наприклад, долазеттільки вимагати від 0,5мг до 10мг. Загальна щорон, палонозетрон, алозетрон, азазетрон, ламоденна доза може бути введена як єдина або роззетрон, мітразапін, гранізетрон, тропізетрон, Еділені дози. 3620, онданзетрон і індизетрон; Такі дозування базуються на середній люди(xv) трициклічні антидепресанти, наприклад, ні, яка має вагу від близько 65кг до 70кг. Тераіміпрамін, амітриптилін, кломіпрамін, амоксамін і певт легко зможе визначити дози для тих, чия лофепрамін; вага виходить за межі цього діапазону, як напри(xvi) агоністи GABA, наприклад, габапентин, клад для дитини і людей похилого віку. топірамат, цинолазепам, клоназепам, прогабід, Для уникнення сумніву, посилання тут на "лібротизолам, зопіклон, прегабалін і езопіклон; кування" включають посилання на радикальне, (xvii) опіоїдні анальгетики, наприклад, морпаліативне і профілактичне лікування. фін, героїн, гідроморфон, оксиморфон, леворфа5-НТ4 агоніст даного винаходу може бути конол, левалорфам, метадон, меперидин, фентарисно поєднаний з іншою фармакологічно активніл, кокаїн, кодеїн, дигідрокодехн, оксикодон, ною сполукою або з двома або більше іншими гідрокодон, пропоксифен, налмефен, налорфін, фармакологічно активними сполуками, особливо налоксон, налтрексон, бупренорфін, буторфанол, у лікуванні захворювання шлунковоналбуфін і пентазоцин; стравохідного рефлюксу. Наприклад, 5-НТ4 аго(xviii) аналоги соматостатину, наприклад, окніст, особливо сполука формули (І), або її фартреотид, AN-238 і PTR-3173; мацевтично прийнятна сіль або сольват, як ви(хіх) активатор СІ каналів: наприклад лубіпзначено вище, може вводитись одночасно, ростон; послідовно або окремо у поєднанні з одним або (хх) селективні інгібітори оберненого захопбільшими агентами, які вибирають з: лення серетоніну, наприклад сертралін, есцита(і) антагоністів гістамін Н2 рецептора, наприлопрам, флуоксетин, нефазодон, флувоксамін, клад ранітидин, лафутидин, нізатидин, циметициталопрам, мілнаципран, пароксетин, венлафадин, фамотидин і роксатидин; ксин, трамадол, сибутрамін, дулоксетин, дезфен(іі) інгібіторів протонового насосу, наприклад, лафаксин і депоксетин; омепразол, езомепразол, пантопразол, рабепра(ххі) антихолінергічні засоби, наприклад, дизол, тенатопразол, ілапразол і ланзопразол; цикломін і гіосціамін; (ііі) антагоністів кислотного насосу, напри(ххіі) проносні засоби, наприклад, Trifyba®, клад, сорапразан, ревапразан(YН-1885), AZDFybogel®, Konsyl®, Isogel®, Regulan®, Celevac® і 0865, CS-526, AU-2064 і YJA-20379-8; Normacol®; (iv) оральних антацидних сумішей, наприклад (xxiii) скловолоконні продукти, наприклад Maalox*, Aludrox* і Gaviscon*; Metamucil®; (ν) захисних засобів слизової оболонки, на(xxiv) антиспазматичні засоби, наприклад, приклад, полапрецинк, екабет натрій, ребаміпід, мебеверин; тепренон, цетраксат, сукралфат, хлорпілін-мідь і (xxv) антагоністи допаміну, наприклад, метоплаунотол; клопрамід, домперидон і левосульпірид; (vi) GABAg агоністів, наприклад, баклофен і (xxvi) холінергічні засоби, наприклад, неостиAZD-3355; гмін (νϋ) α2 агоністів, наприклад, клонідин, меде(xxvii) інгібітор AChE: галантамін, метрифотомідин, лофексидин, моксонідин, тизанідин, гуанат, ривастигмін, ітоприд і донепезил; нфацин, гуанабенз, таліпексол і дексмедетомі(xxviii) Антагоністи тазікініну (NK), особливо, дин; NK-3, NK-2 і NK-1, наприклад, антагоністи, непа(viii) похідних ксантину, наприклад, теофілін, дутант, саредутант, талнетант, (αR,9R)-7-[3,5амінофілін і доксофілін; 35 86204 36 спендованих в кінцевому об'ємі 500мкл 50мМ тіс(трифторметил)бензил]-8,9,10,11-тетрагідро-9Tris-HCl (pH7,5). Неспецифічне зв'язування виметил-5-(4-метилфеніл)-7Н-[1,4]діазоцино[2,1значали з 10мкМ 5-НТ. g][1,7]нафтиридин-6-13-діон (ТАК-637), 5Планшети інкубували при кімнатній темпера[[(2R,3S)-2-[(1R)-1-[3,5турі на планшетному шейкері протягом 30хв. Вибіс(трифторметил)феніл]етокси-3-(4-фторфеніл)пробування припиняли швидким фільтруванням, 4-морфолініл]метил]-1,2-дигідро-3Н-1,2,4використовуючи Brandell харвестер клітин через триазол-3-он (МК-869), ланепітант, дапітант і 3фільтри Wallac-B, попередньо вимочені в 0,2% [[2-метокси-5полі(етиленімін) при 4°С протягом 60-90хв. Філь(трифторметокси)феніл]метиламіно]-2-фенілтри промивали тричі 1мл льодяного 50мМ піперидин (2S, 3S). HEPES, і висушували у мікрохвильовому приСпосіб оцінки біологічних активностей: строї або при кімнатній температурі. їх пакували і 5-НТ4 рецептор зв'язувальні властивості спонагрівали за допомогою сцинтилятора "Meltilex" лук даного винаходу визначають відповідно до (Wallac) або вимочували в BetaplateScint (Wallac). наступних методик. Рецепторзв'язану радіоактивність вимірювали, Одержання Мембрани використовуючи лічильник "Big-spot", лічильник Голови свиней поставляли з бойні. Стриарні Betaplate (Wallac) або LS лічильник (Packard). тканини розтинали, зважували і гомогенізували у Зв'язування людського 5-НТ4 (1) 15 об'ємах 50мМ льодяного HEPES (рН7,5) в гоЛюдські 5-HT4(d) трансфековані НЕК293 клімогенізаторі Polytron (30сек. на повній швидкості). тини одержували і вирощували власного виготоСуспензію центрифугували при 48,000g і 4°С провлення. Зібрані клітини суспендували в 50мМ тягом 5хв. Одержану гранулу ресуспендували у HEPES (рН7,4 при 4°С), доповнюючи протеаза відповідному об'ємі 50мМ льодяного HEPES, інгібіторним коктейлем (Boehringer, 1:1000 розбарозподіляли в аліквоти і зберігали при -80°С, до влення) і гомогенізували, використовуючи ручний використання. Polytron PT 1200 подрібнювач, встановлений на Бичачі голови також поставляли з бойні. повну потужність, протягом 30сек. на льоду. ГоСтриарні тканини розтинали, зважували і гомогенізували у 20 об'ємах 50мМ льодяного Tris-HCl могенати центрифугували при 40,000´g при 4°С (рН7,4) в гомогенізаторі Polytron (30сек. на повній протягом 30хв. Гранули ресуспендували в 50мМ швидкості). Суспензію центрифугували при HEPES (pH7,4 при 4°С) і центрифугували ще раз 20,000g і 4°С протягом 30хв. Одержану гранулу таким же чином. Кінцеві гранули ресуспендували ресуспендували у 15 об'ємах 50сМ льодяного у відповідному об'ємі 50мМ HEPES (рН7,4 при Tris-HCl, гомогенізували і центрифугували знову 25°С), гомогенізували, аліквотували і зберігали таким же чином. Кінцеву гранулу ресуспендували при -80°С, до використання. Аліквоту мембрану відповідному об'ємі 50мМ Tris-HCl, розподіляли них частинок використовували для визначення в аліквоти і зберігали при -80°С, до використання. концентрації білку, використовуючи набір ВСА Тканини кори головного мозку видаляли з білкового аналізу (PIERCE) і ARVOsx планшетний самців щурів Sprague-Dawley (SD) (Japan SLC), зчитувач (Wallac). зважували і вміщували у 10 об'ємів 50мМ льодяДля експериментів на зв'язування інкубували ного Tris-HCl (рН7,5). Їх гомогенізували в гомоге25мкл тестованих сполук з 25мкл [3H]-GR113808 нізаторі Polytron (30сек. на повній швидкості) і (Amersham, кінцеве 0,2нМ) і 150мг мембранного згодом центрифугували при 48,000g і 4°С протягомогенату і WGA-SPA гранульованих гом 15хв. Одержану гранулу ресуспендували в (Amersham) суспензійних розчинів (10мкг протеї50mМ льодяного Tris-HCl, гомогенізували і ну і 1мг SPA шариків/клітину) протягом 60 хвилин центрифугували знову таким же чином. Кінцеву при кімнатній температурі. Неспецифічне зв'язугранулу ресуспендували у відповідному об'ємі вання визначали 1мкМ GR113808 (Tocris) при 50мМ Tris-HCl, розподіляли в аліквоти і зберігали кінцевій концентрації. Інкубацію припиняли при -80°С, до використання. центрифугуванням при 1000 rpm. РецепторПротеїнові концентрації гомогенатів визначазв'язувальну радіоактивність визначали за дополи способом Бредфорда або ВСА протеїновим могою підрахування з планшетним лічильником способом (Пірс) з BSA як стандартом. MicroBeta (Wallac). Випробування на зв’язування Всі сполуки, одержані у робочих прикладах, Властивості сполук для 5-НТ4 рецепторів як описано нижче, були тестовані цим способом, і свиней або биків і 5-НТ3 рецепторів щурів оцінювони показали значення Kі від 0,3нМ до 30нМ вали з використанням радіомічених специфічних щодо інгібування зв'язування у 5-НТ5 рецепторі. лігандів, GR 113808 ({1-[2Зв'язування людського 5-НТ4 (2) (метилсульфоніл)етил]-4-піперидиніл}[метил-3Н]Людські 5-HT4(d) трансфековані НЕK293 клі1Н-індол-8-карбоксилат) і BRL 43694 (1-Метил-Nтини одержували і вирощували власного вигото(9-[метил-3Н]-9-азабіцикло[3,3,1]нон-3-іл)-1Hвлення. Зібрані клітини суспендували в 50мМ Tris індазол-3-карбоксамід). Сполуки інкубували з 25буфері (рН7,4 при 4°С), доповнюючи протеаза 100рМ [3H]-GR 113 808 (Amersham) і 0,6-1мг білка інгібіторним коктейлем (Boehringer, 1:1000 розбасвинячих або бичачих стриарних мембран, сувлення) і гомогенізували, використовуючи ручний спендованих в кінцевому об'ємі 0,8-1мл 50мМ Polytron PT 1200 подрібнювач, встановлений на Tris-HCl (рН7,5). Неспецифічне зв'язування виповну потужність, протягом 30сек. на льоду. Гозначали з 10-50мкМ 5-НТ. Зв'язування 0,3нМ [3H]могенати центрифугували при 40,000´g при 4°С BRL 43694 (NEN) вимірювали, використовуючи протягом 10хв. Гранули ресуспендували в 50мМ 400нг білка кортикальних мембран щурів, суTris буфері (рН7,4 при 4°С) і центрифугували ще 37 86204 38 тягом 1 хвилини. Як тільки виникало максимальраз таким же чином. Кінцеві гранули ресуспендуне розслаблення і здійснювалось вимірювання, вали у відповідному об'ємі 50мМ Tris буферу тканини промивали при максимальній швидкості (рН7,4 при 25°С), який містить 10мМ MgCl2, гомо(66мл/хв.) протягом щонайменше 1 хвилини і генізували, аліквотували і зберігали при -80°С, до поки базовий вихідний рівень не був встановлевикористання. Аліквоту мембранних частинок ний (пре-карбохолін і 5-НТ) (звичайно, вихідний використовували для визначення концентрації рівень падає нижче первинного, що слідує за білку, використовуючи набір ВСА білкового аналіпочатковим урівноваженням). Швидкість потоку зу (PIERCE) і ARVOsx планшетний зчитувач (Walнасосу зменшували до 2мл/хв. і тканини залишаlac). ли на 60 хвилин. Для експериментів на зв'язування інкубували Кумулятивна крива концентрація-ефект 50мкл тестованих сполук з 50мкл [3Н] 5-НТ (СЕС) до 5-НТ будували для діапазону від 0,1нМ (Amersham, кінцеве 8,0нМ) і 400мкл мембранного до 1мкМ, з шагом збільшення одиниці наполовигомогенату (300мкг білок/канал) протягом 60 хвину (5-НТ крива 1 для аналізу даних). Час контаклин при кімнатній температурі. Неспецифічне тування між дозами був 3 хвилини або доти, доки зв'язування визначали 50мкМ GR113808 (Tocris) не встановлювалось плато. Тканини відповідали при кінцевій концентрації. Всі інкубації припиняли швидше, коли концентрація 5-НТ у ванні збільшушвидким вакуумним фільтруванням над 0,2% РЕІ валась. У кінці кривої, тканини промивали (при просоченим скловолоконним фільтрувальним максимальній швидкості) якомога швидше, щоб папером, використовуючи харвестер BRANDEL, з уникнути десинсибілізації рецепторів. Швидкість наступними трьома промиваннями 50мМ Tris бупотоку насосу зменшували до 2мл/хв. і тканини фером (рН7,4 при 25°С). Рецептор-зв'язувальну залишали на 60 хвилин радіоактивність визначали рідинним сцинтиляДругий СЕС був проведений - або для 5-НТ ційним лічінням, використовуючи лічильник Pack(для тканин контрольованого часу), інших агонісard LS. тів 5-НТ4 (стандарт) або тестованої сполуки (криВсі сполуки Прикладів показали 5НТ4 рецепва 2 для аналізу даних). Час контактування зміторну афінність. нювався для інших 5-НТ4 агоністів і тестованих Функціональне випробування: сполук і адаптований відповідно до індивідуальНаявність 5-НТ4 рецепторів у стравоході щуних відповідей тканин для кожного конкретного рів і здатність демонструвати частковий агонізм в агента. У тканинах, які піддаються дії тестованої одержання ТММ повідомляються в літературі сполуки, висока концентрація (1мкМ) 5-НТ4 анта[Див. G.S. Baxter et al. Naunyn-Schmiedeberg's гоніста (SB 203,186: 1H-індол-3-карбонова кислоArch Pharmacol (1991) 343: 439-446; M. Yukiko et та, 2-(1-піперидиніл)етиловий ефір, Tocris) була al. JPET (1997) 283:1000-1008; and JJ. Reeves et додана до бані, після останньої концентрації тесal. Br. J. Pharmacol. (1991) 103: 1067-1072)]. тованої сполуки. Це було зроблено з тим, щоб Більш конкретно, часткова агоністична активність побачити, чи буде змінене будь-яке агоністможе бути виміряна відповідно до наступних індуковане розслаблення (якщо присутнє). SB процедур. 203,186 змінював 5-НТ індуковане розслаблення, Самців SD щурів (Charles River), які важать відновлюючи первинний ступінь тканини карба250-350г, оглушали і потім вбивали шийним вихолін-індукованого тонусу тканини. вихом. Стравохід розтинали від безпосередньо Агоністична активність тестованих сполук бупроксимального до шлунку (включаючи частину ла підтверджена за допомогою попереднього шлунку, щоб позначити дистальний відділ) до інкубування тканин з 100нМ стандартним 5НТ4 рівня трахеї і потім вміщували у свіжий розчин антагоністом, таким як SB 203,186. SB 203,186 Кребса. додавали до бані за 5 хвилин перед додаванням Зовнішній скелетний м'язовий шар видаляли карбахінолу до кривої 2. Тканини повинні бути в один хід за допомогою очищення його від шару "спарені" для аналізу даних, тобто тестовану гладкого м'язу, який лежить нижче, використовусполуку за відсутності SB 203,186 в одній тканині ючи хірургічні щипці (до напряму трахеї). Залишпорівнювали з тестованою сполукою у присутносковий внутрішній канал гладкого м'язу був відоті SB 203,186 в окремій тканині. Було неможлимий як ТММ. Його відрізали на 2см від вим провести криву 3, тобто 5-НТ криву 1, з напервинного "кінця шлунку" і залишок відкидали. ступною кривою 2 тестованої сполуки (-SB ТММ вкладали як цільні "відкриті" канали в 203,186), з наступною кривою 2 тестованої споподовжньому напрямі в 5мл органні бані, заповлуки (+SB 203,186). нені теплим (32°С) аерованим Кребс. Тканини Агоніст-індуковане зростання сАМР в людсьвміщували під початковою напругою 750мг і було ких 5-НТ4(d) трансфекованих НЕK293 клітинах дозволяли урівноважитись протягом 60 хвилин. Людські 5-HT4(d) трансфековані НЕK293 кліТканини перенапружували двічі з 15 хвилинними тини одержували і вирощували власного виготопроміжками протягом періоду урівноваження. влення. Клітини вирощували при 37°С і 5% СО2 в Швидкість потоку насосу встановлювали на DMEM, доповненим 10% PCS, 20мМ HEPES 2мл/хв. протягом цього часу. (рН7,4), 200мкг/мл гігроміцину В (Gibco), Після урівноваження насос відключали. Тка100одиниць/мл пеніциліну і 100мкг/мл стрептомінини піддавали дії 1мкМ карбохоліну і скорочувацину. ли і досягали до стійкого рівня скорочення протяКлітини вирощували до 60-80% конфлюентгом 15 хвилин. Тканини потім піддавали дії 1мкМ ності. У попередній день до обробки сполуками 5-НТ (щоб затравити тканини). Тканини розслаблялись у відповідь на 5-НТ досить швидко - про 39 86204 40 діоактивне зв'язування до фільтра визначали діалізований FCS (Gibco) заміщували на нормалічильником Wallac Betaplate. льний і клітини інкубували протягом ночі. Випробування Iherg Сполуки готували в 96-ямкові планшети Клітини НЕК 293, які стабільно експресують (12,5мкл/ямку). Клітини збирали з PBS/1мМ калієвий канал HERG, використовували для елеEDTA, центрифугували і промивали PBS. На поктрофізіологічного дослідження. Методологія для чатку випробування, клітинну гранулу ресуспенстабільної трансфекції цього каналу в клітинах дували в DMEM, доповненому 20мМ HEPES, НЕК може бути знайдена в іншому джерелі 10мкМ паргіліну (Sigma) і 1мМ 3-ізобутил-1[Z.Zhou et al., 1998, Biophysical journal, 74, pp.230метилксантину (Sigma) у концентрації 241]. Перед днем експериментування, клітини 1,6´10клітин/мл і залишали на 15 хвилин при збирали з клітинних колб і вміщували на покривкімнатній температурі. Реакцію ініціювали додане скло у стандартному середовищі MEM з 10% ванням клітин в планшети (12,5мкл/ямку). Після PCS. Покриті клітини зберігали в інкубаторі при інкубування протягом 15 хвилин при кімнатній 37°С, який підтримується в атмосфері температурі, додавали 1% Тритон Х-100, щоб 95%O2/5%СO2. Клітини досліджували між 15зупинити реакцію (25мкл/ямку) і планшети зали28год. після збирання. шали протягом 30 хвилин при кімнатній темпераСтруми HERG досліджували, використовуючи турі. Гомогенне основане на флуоресценції виявстандартний метод "відкриття-закриття" в повнолення з часовим розділенням cAMP (Schering) клітинній формі. Протягом експерименту клітини здійснювали відповідно до інструкцій виробника. переохолоджували стандартним зовнішнім розARVOsx мультимічений лічильник (Wallac) викочином наступної композиції (мМ); NaCl, 130; KСI, ристовували, щоб виміряти HTRF (збудження 4; СаСl2, 2; MgCl2, 1; Глюкоза, 10; HEPES, 5; 320нм, виділення 665нм/620нм, час затримання рН7,4 з NaOH. Повноклітинні записи здійснювали, 50мксек., вікно 400мксек.). використовуючи петч-піпетковий ампліфікатор і Дані аналізували, основуючись на співвіднопетч-піпетки, які мають опір 1-3MOhm, коли запошенні інтенсивності флуоресценції кожної ямки внені стандартним внутрішнім розчином наступпри 620нм і 665нм, з наступним кількісним аналіного складу (мМ); KСI, 130; MgATP, 5; MgCl2, 1,0; зом сАМР, використовуючи стандартну криву HEPES, 10; EGTA 5, рН7,2 з KОН. Тільки ці клітисАМР. Збільшення вироблення сАМР, яке виклини з опорами доступу нижче 15ΜΩ та опорами кається кожною сполукою, було нормалізоване ущільнення >1GΩ були прийняті для подальшого до кількості сАМР, продукованої 1000нМ серотоекспериментування. Компенсація послідовних ніну (Sigma). опорів була прийнята аж до максимально 80%. Всі сполуки Прикладів показали 5НТ4 рецепНе було здійснено видалення витоку. Однак, торну агоністичну активність. прийнятний опір доступу залежав від розміру Зв'язування людського дофетиліду записаних струмів і рівня компенсації послідовЛюдські 5-HT4(d) трансфековані НЕK293 кліних опорів, що може безпечно використовуватини одержували і вирощували власного вигототись. Слідуючи досягненню повноклітинної конфівлення. Зібрані клітини суспендували в 50мМ гурації і достатнього для клітинного діалізу з Tris-HCl (pH7,4 при 4°С) і гомогенізували, викорипіпеточним розчином (>5хв.), стандартний протостовуючи ручний Polytron PT 1200 подрібнювач, кол напруги застосовували до клітини, щоб вивстановлений на повну потужність, протягом кликати мембранні струми. Протокол напруги є 20сек. на льоду. Гомогенати центрифугували при таким, як зазначено нижче. Мембрану деполяри40,000´g при 4°С протягом 20хв. Гранули ресусзували з вихідного потенціалу у -80мВ до +20мВ пендували, гомогенізували і центрифугували ще протягом 1000мс. Це закінчувалось падінням ліраз таким же чином. Кінцеві гранули ресуспендунійного вимірювання напруги (швидкість 0,5мв в вали у відповідному об'ємі 50мМ Tris-HCl, 10мМ мсек.-1) назад до вихідного потенціалу. Протокол KСI, 1мМ MgCl2 (pH7,4 при 25°С), гомогенізували, напруги застосовували до клітини безперервно розділяли на аліквоти і зберігали при -80°С, до протягом експерименту кожні 4 секунди (0,25Гц). використання. Аліквоту мембранних частинок Амплітуда максимального струму встановлювавикористовували для визначення концентрації лась близько 40мВ протягом вимірювання лінійбілку, використовуючи набір ВСА білкового аналіної зміни. Як тільки одержували стійкі викликані зу (PIERCE) і ARVOsx планшетний зчитувач (Walструмові відповіді у зовнішньому розчині, носій lac). (0,5% DMSO у стандартному зовнішньому розчиВипробування на зв'язування проводили в ні) застосовували протягом 10-20хв. за допомоповному об'ємі 200мкл в 96-ямкових планшетах. гою перистальтичного насосу. Забезпечувались Двадцять мкл тестованих сполук інкубували з мінімальні зміни в амплітуді викликаної струмової 20мкл [3Н]-дофетиліду (Amersham, кінцевий 5нМ) відповіді у стані контролю носієм, тестовану споі 160мкл мембранного гомогенату (25мг білка) луку або 0, 3, 1, 3, 10мкМ застосовували протяпротягом 60 хвилин при кімнатній температурі. гом 10-хвилинного періоду 10-хвилинний період Неспецифічне зв'язування визначали 10мкМ довключав час, який розчин, який постачається, фетиліду при кінцевій концентрації. Інкубування проходив через трубу з резервуару розчину до припиняли швидким вакуумним фільтруванням зчитувальної камери через насос. Час піддавання над 0,5% попередньо вимоченим GF/B Betaplate клітин дії розчину сполук був більше, ніж 5хв. фільтром, використовуючи Skatron харвестер після того, як концентрація лікарського засобу в клітин з 50мМ Tris-HCl, 10мМ KСI, 1мМ MgCl2, рН ямці камери досягла бажаної концентрації. Спо7,4 при 4°С. Фільтри висушували, вкладали в стерігалася оборотність. Нарешті, клітини піддатипові пакети і наповнювали Betaplate Scint. Ра 41 86204 42 щурами води. За п'ять хвилин до введення тесвали дії високої дози дофетиліду (5мкМ), специтованої їжі, тестовані сполуки, цизаприд або нофічного блокатора ІKr, щоб оцінити інтенсивний сій дозували відповідним шляхом щурам (n=8-10) ендогенний струм. в об'ємі 0,1мл на 100г ваги тіла. Цизаприд (3мг/кг) Всі експерименти були виконані при кімнатній використовували як позитивний контроль для температурі (23±1°С). Викликані мембранні струексперименту. Щурам давали 3мл тестованої їжі ми зчитувати on-line на комп'ютері, фільтрували шляхом примусового харчування і повертали у при 500-1КГц (Бессель -3дБ) і відбирали зразки клітки. Через тридцять хвилин після введення їжі, при 1-2КГц, використовуючи петч-піпетковий амщурів вибраковували піддаванням дії СО2. Після пліфікатор і специфічне програмне забезпечення серединної лапаратомії, шлунок лігували в нижаналізування даних. Амплітуду максимального чому стравохідному сфінктері (LES) і пілорусі. струму, яка виникала при близько 40мВ, вимірюПотім шлунок видаляли і зважували (А). Після вали незалежно на комп'ютері. того, як шлунок відкривали і промивали 0,9% соСереднє арифметичне десяти значень ампльовим розчином, його блотували спереду ткалітуди підраховували в контрольних умовах і у ниною, щоб видалити будь-яку надмірну рідину, і присутності лікарського засобу. Відсоткове знизважували знову (В). Після вивільнення щурів, які ження I N в кожному експерименті одержували з'їли випорожнення або наданий штучний пронормалізованим значенням струму, використомах, ступінь шлункового вивільнення для індивівуючи наступну формулу: I N=(I-I D/I C)´100, де ID дуальних тварин підраховували за формулою: являє собою середнє значення струму у присутСтупінь шлункового вивільнення (%) =(Аності лікарського засобу і І C являє собою середнє В)/вага тестованої їжі. значення струму у контрольних умовах. Окремі Шлункова моторика у свідомих собак: експерименти виконували для кожної концентраХірургічну операцію на собаках виконували ції лікарського засобу або узгодженого у часі конмодифікованим способом Z. Itoh et al. [Gastroenтролю, і середнє арифметичне в кожному експеterol. Jpn., 12,275-283 (1977)]. Впливи тестованих рименті визначали як результат дослідження. сполук на шлункову моторику у собаках досліПівжиття у мікросомах печінки людини (HLM) джували модифікованим способом N. Toshida et Тестовані сполуки (1мкМ) інкубували з 3,3мМ al. [J. Pharmacol.Exp/Ther., 257, 781-787 (1991)]. MgCl2 і 0,78мг/мл HLM (HL101) в 100мМ кальцій Оцінка в голодному стані: Тваринам хронічно фосфатного буферу (рН7,4) при 37°С на 96імплантували тензометричний датчик сили в тіло ямковому планшеті. Реакційну суміш розділяли шлунку, і піддавали голодуванню протягом ночі на дві групи, не-Р450 групу і Р450 групу. NADPH перед експериментом. Шлункову моторику бездодавали тільки до реакційної суміші групи Р450. перервно зчитували системою телеметрії протяАліквоту зразків групи Р450 збирали у точці часу гом 8год. після введення сполуки. Щоб кількісно в 0, 10, 30, і 60 хвилин, де 0 хвилинна точка часу визначити зміну у моториці травного тракту, інвказувала на час, коли NADPH додавали в реакдекс моторики визначали як ділянку під кривими ційну суміш групи Р450. Аліквоту зразків не-Р450 скорочення протягом кожного 2-годинного перігрупи збирали в точці часу у -10 і 65 хвилин. Зіоду, розділеного піковою висотою інтердигестивбрані аліквоти екстрагували розчином ацетонітного мігруючого скорочення. рилу, який містить внутрішній стандарт. ОсаджеОцінка в післяобідньому стані: Тваринам хроний білок центрифугували в центрифузі нічно імплантували тензометричний датчик сили (2000об./хв, 15хв.). Концентрацію сполуки в супев тіло шлунку, і голодували протягом ночі перед рнатанті вимірювали системою PX/MS/MS. експериментом. Післяобідню моторику індукуваЗначення півжиття одержували за допомогою ли годуванням твердою їжею (100 грамів), і спопобудови натурального логарифму співвіднолуку вводили через 2год. Шлункову моторику шення максимальної зони сполук/внутрішнього безперервно зчитували системою телеметрії стандарту проти часу. Нахил прямої найкращого протягом 8год. після введення сполуки. Індекс узгодження через точки дає ступінь метаболізму моторики визначали, щоб кількісно визначити (k). Це перетворювали у значення півжиття, визміну у моториці травного тракту як ділянку під користовуючи наступні рівняння: кривими скорочення протягом кожного 1Півжиття =In 2/k годинного періоду, розділеного ділянкою під криСпосіб моделі шлункового вивільнення у щувими скорочення протягом 1год. до введення рів: сполуки. Впливи сполук на шлункове вивільнення у Сполуки формули (І) даного винаходу можуть щурів досліджували модифікованим способом бути введені або оральним, парентеральним або [D.A. Droppleman et al., J. Pharmacol. Methods 4, місцевим шляхом ссавцям. Звичайно, ці сполуки 227-230 (1980)]. Тестовану їжу, знежирену калонайбільш переважно вводять людині в дозах, які рійну їжу одержували відповідно до способу [S. знаходяться в діапазоні від 0,3мг до 750мг на Ueki et al., Arzneim.-Forsch./Drug Res. 49 (Π), 618день, переважно від 10мг до 500мг на день, хоча 625 (1999)]. IGS-SD щурів (самець, 7w, 230-270г) можуть виникнути неминуче варіації, в залежноспридбавали у Charles River Japan (Atsugi). Цих ті від ваги і стана суб'єкта, якого лікують, стану щурів використовували в експериментах через хвороби, який лікують і конкретного шляху ввеодин тиждень акліматизації. В експериментах дення, який обирають. Однак, наприклад, рівень щури голодували за 15 годин перед експеримендозування, який знаходиться в межах від 0,06мг тами, але дозволяли вільний доступ до води. За до 2мг на кг ваги тіла на день, є найбільш пересорок п'ять хвилин до початку експерименту, воважним для лікування запалення. ду вилучали з клітки, щоб запобігти одержання 43 86204 44 реважно зроблене за допомогою кремів, желе, Сполуки даного винаходу можуть бути ввегелів, паст, мазей і тому подібне, відповідно до дені одні або у поєднанні з фармацевтично пристандартної фармацевтичної практики йнятними носіями або розріджувачами будь-яких Приклади із вищезазначених шляхів, і таке введення може Винахід проілюстрований наступними необбути проведене в єдиній або багаторазовій дозах. межувальними прикладами, в яких, якщо не вкаБільш конкретно, нові терапевтичні агенти виназано інакше: всі дії були проведені при кімнатній ходу можуть бути введені в широкій різноманітабо температурі навколишнього середовища, ності різних форм дозування, тобто, вони можуть тобто, в діапазоні 18-25°С; випаровування розбути об'єднані з різними фармацевтично прийнячинника проводили, використовуючи роторний тними інертними носіями у формі таблеток, капвипарник під зниженим тиском з температурою сул, коржиків, таблеток, твердих льодяників, побані до 60°С; реакції контролювали тонкошаророшків, спреїв, кремів, бальзамів, супозиторіїв, вою хроматографією (ТШХ) і часи реакції навежеле, гелів, паст, лосьйонів, мазей, водних судені лише для ілюстрації; точки плавлення (т.пл.) спензій, ін'єктованих розчинів, еліксирів, сиропів і дані невиправленими (поліморфізм може привестому подібне. Такі носії включають тверді розріти до різних точок плавлення); структуру і чистоту джувачі або наповнювачі, стерильні водні засоби всіх виділених сполук засвідчували щонайменше і різні нетоксичні органічні розчинники і т.д. Крім однією з наступних технік: ТШХ (Merck силікагель того, оральні фармацевтичні композиціїможуть 60 F254 покриті ТШХ планшети або Merck NH2 бути прийнятно підсолоджені і/або їм може бути F254S покриті HPTLC планшети), маснадано смаку. Зазвичай, терапевтично ефективні спектрометрія, ядерний магнітний резонанс сполуки даного винаходу присутні в таких фор(ЯМР), інфрачервоні спектри поглинання (14), мах дозування при рівнях концентрації, які варімікроаналіз або порошкова рентгенограма юють від 5% до 70% за вагою, переважно від 10% (PXRD). Виходи надані лише для ілюстративних до 50% за вагою. цілей. Колонкову флеш-хроматографію проводиДля орального введення, таблетки, які місли, використовуючи Merck силікагель 60 (230тять різні ексципієнти, такі як мікрокристалічна 400меш ASTM) або Fuji Silysia Chromatorex® целюлоза, цитрат натрію, карбонат кальцію, фоDU3050 (Аміно Тип, 30-50мкМ). Масспектральні сфат дикальцію і гліцин, можуть бути залучені дані низького розділення (ЕІ) одержували на масразом з різними дезінтегрантами, такими як кроспектрометрі Integrity (Waters) або масхмаль і переважно краще кукурудзяний, картоспектрометрі Automass 120 (JEOL). Macпляний або тапіоковий крохмаль, альгінова кисспектральні дані низького розділення (ESI) одерлота і конкретні комплексні силікати, разом з жували на мас-спектрометрі ZMD2 (Waters) або гранулюючими зв'язувальними речовинами, тамас-спектрометрі Quattro II (Micromass). Дані кими як полівінілпіролідон, сахароза, желатин і ЯМР визначали при 270МГц (JNM-LA JEOL 270 акація. Додатково, змащувальні агенти, такі як спектрометр) або 300МГц (JEOL JNM-LA300), наприклад, стеарат магнію, лаурил сульфат навикористовуючи дейтрований хлороформ (99,8% трію і тальк часто є дуже корисними з метою табD) або диметилсульфоксид (99,9% D) як розчинлетування. Тверді композиції подібного типу таник, якщо не вказано інакше, відносно тетрамекою можуть бути залучені як наповнювачі в тилсилану (TMS), як внутрішній стандарт в частжелатинових капсулах; переважні матеріали в ках на мільйон (м.ч.); умовні скорочення, які цьому випадку також включають лактозу або мовикористовуються: s= синглет, d= дуплет, t= трилочний цукор також як і високомолекулярні полілет, q= квартет, m= мультиплет, br.= ушир, і т.д. етиленгліколі. Коли водні суспензії і/або еліксири ІЧ спектри вимірювали інфрачервоним спектроє бажаними для орального введення, активний метром Shimazu (ІЧ-470). Оптичне обертання інгредієнт може бути поєднаний з різними підсовимірювали, використовуючи JASCO DP-370 Digiлоджувальними або смаковими агентами, барвtal Polarimeter (Japan Spectroscopic CO, Ltd.). Пониками, і, якщо бажано, емульгуючими а/або сурошкову рентгенограму PXRD визначали, викоспендуючими агентами також, разом з такими ристовуючи Rigaku RTNT-TTR порошковий розріджувачами, як вода, етанол, пропіленглідифректометр, оснащений автоматичним відбірколь, гліцерин і їх різні подібні комбінації. ним перетворювачем, 2 тета-тета гоніометром, Для парентерального введення розчини спощілинами розходимості пучка, вторинним монолуки даного винаходу або в кунжутній або арахіхроматором і сцинтиляційним лічильником. Зрасовій олії або у водному пропіленгліколі можуть зок одержували для аналізу за допомогою пакубути залучені. Водні розчини повинні бути прийнвання порошку на алюмінієвий тримач зразків. ятно буферовані (переважно рН>8), якщо необЗразок обертали 60,00об./хв. і сканували 4°/хв.. хідно, і рідкий розріджувач, має бути ізотонічним. Хімічні символи мають їх звичайні значення; т.к. Ці водні розчини є прийнятними з метою внутрі(точка кипіння), т.пл. (точка плавлення), л шньовенних ін'єкцій Маслянисті розчини є прийн(літр(и)),мл (мілілітр(и)),г (грам(и)), ятними для внутрішньосуглобових, внутрішньомг(міліграм(и)), моль (молі),мМоль (мілімолі), екв. м'язових і підшкірних ін'єкцій Одержання всіх цих (еквіваленти)). розчинів у стерильних умовах можуть бути легко Приклад 1: здійснені стандартними фармацевтичними метоN-({1-[(4-Гiдpoкcитeтpaгiдpo-2H-пipaн-4диками, добре відомими кваліфікованим в даній iл)мeтил]пiпepидин-4-iл}мeтил)-3-ізопропіл-2галузі фахівцям. Додатково, також можливо ввооксо-2,3-дигідро-1H-бунзімідазол-1-карбоксамід дити сполуки даного винаходу місцево при лікугідрохлорид ванні запальних станів шкіри і це може бути пе Стадія 1. трет-Бутил ({1-[(4-гідрокситетрагідро-2Н-піран-4-іл)метил]-піперидин-4-іл}метил)карбамат До перемішуваного розчину трет-бутил (піперидин-4-ілметил)карбамату (22,3г, 104ммоль) в метанолі додають 1,6-діоксаспіро[2,5]октан (14,2г, 124ммоль, [Satyamurthy, Nagichettiar et al., Phosphorus Suljur, 1984, 19, 113]) при температурі навколишнього середовища. Потім суміш нагрівають при 60°С протягом 4год. Леткі компоненти видаляють випаровуванням і одержану в'язку олію осаджують сумішшю гексану і діетилового ефіру. Осад збирають фільтруванням і перекристалізовують сумішшю гекса ну і 2-пропанолу, щоб дати 14,2г вказаної у заголовку сполуки (42%) як безбарвний порошок. MS (ESI) m/z: 329 (М+Н+). т.пл.: 104°С. 1 H-ЯМР (CDCI 3) δ: 1,23-1,31 (2Η, м), 1,44 (9Η, с), 1,51-1,69 (8Η, м), 2,27-2,38 (4Η, м), 2,83-2,88 (2Η, м), 3,00 (2Η, т, J=6,2Гц), 3,70-3,85 (4Η, м). Підраховано аналізом для C17H32N2O4: С, 62,17; Η, 9,82; Ν, 8,53. Знайдено: С, 62,07; Η, 9,92; Ν, 8,58. Стадія 2. 4-{[4-(Амінометил)піперидин-1іл]метил}тетрагідро-2Н-піран-4-ол До розчину трет-бутил ({1-[(4гідрокситетрагідро-2Н-піран-4іл)метил]піперидин-4-іл}метил)карбамату (50,28г, 153ммоль) в метанолі додають 4Ν НСІ в діоксані (200мл, 800ммоль) при кімнатній температурі. Через 4год. леткі матеріали видаляють випаровуванням. Одержану аморфну речовину осаджують сумішшю діетиловий ефір/метанол (5:1). Осад збирають і додають до льодяного 6Ν NaOH водн. (200мл) поступово. Суміш екстрагують сумішшю дихлорметан/метанол (10:1) протягом 4 годин. Об'єднану органічну фазу промивають розсолом, висушують над MgSO4 і концентрують, щоб одержати 24,90г (99%) вказаної у заголовку сполуки як блідо-коричневу аморфну речовину. MS (ESI) m/z: 229 (М+Н+). 1 H-ЯМР (CDCI 3) δ: 1,19-1,28 (2Η, м), 1,44-1,63 (8Η, м), 1,65-1,71 (2Η, м), 2,32 (2Η, с). 2,35 (2Η, т, J=11,0Гц), 2,57 (2Η, д, J=5,7Гц), 2,85-2,90 (2Η, м), 3,70-3,81 (4Η, м) Стадія 3. Ν-({1-[(4-Гідрокситетрагідро-2Нпіран-4-іл)метил]піперидин-4-іл}метил)-3ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1карбоксамід До перемішуваної суміші 1-ізопропіл-1,3дигідро-2Н-бензімідазол-2-ону [J. Med. Chem. 1999, 42, 2870-2880] (23,0г, 130ммоль) і триетиламіну (54,6мл, 392ммоль) в тетрагідрофурані (300мл) додають трифосген (38,8г, 130ммоль) в тетрагідрофурані (200мл) поступово при кімнатній температурі. Потім суміш нагрівають при 80°С протягом 4год. Після охолодження розчин 4-{[4(амінометил)піперидин-1-іл]метил}тетрагідро-2Нпіран-4-олу (стадія 2 Прикладу 1) (24,9г, 109ммоль) і триетиламіну (45мл, 109ммоль) в тетрагідрофурані (500мл) додають до суміші. Потім, суміш нагрівають 80°С протягом 6год. Після охолодження насич. NaHCO3 водн. додають до суміші Суміш екстрагують етилацетатом (500мл´4). Екстракти промивають розсолом, висушують над MgSO4 і концентрують. Залишок хроматографують на колонці амінопропілсилікагелю, елююючи етилацетатом/гексаном (3:1), щоб дати 31,3г (67%) вказаної у заголовку сполуку як тверду речовину білого кольору. 1HЯМР (DMSO-d6) δ: 8,80 (1Η, ушир. т, J=6,0Гц). 8,06 (1Η, м), 7,41 (1Η, м), 7,19 (1Η, дт, J=1,5, 7,7Гц), 7,12 (1Η, дт, J=1,3, 7,7Гц), 4,64 (1Η, септет, J=7,0Гц), 4,08 (1Η, ушир, с), 3,68-3,44 (4Η, м), 3,19 (2Η, т, J=6,0Гц), 2,89 (2Η, м), 2,20 (2Η, ушир, с), 2,09 (2Η, м), 1,68-1,10 (9Η, м), 1,47 (6Н, д, J=7,0Гц). MS (ESI) m/z: 431 (М+Н+). Підраховано аналізом для C23H34N4O4: С, 64,16; Η, 7,96; Ν, 13,01. Знайдено: С, 64,13; Η, 7,97; Ν, 12,99. Стадія 4 Ν-({1-[(4-Гідрокситетрагідро-2Нпіран-4-іл)метил]піперидин-4-іл}метил)-3 47 86204 48 м), 3,00-3,12 (3Η, м), 3,15-3,45 (3Η, м), 3,60-3,70 ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1(6Η, м), 4,61-4,69 (1Η, м), 5,46-5,49 (1Η, м), 7,13 карбоксамід гідрохлорид (1Η, т, J=7,8Гц) 7,20 (1Η, т, J=7,8Гц), 7,42 (1Η, д, До перемішуваного розчину N-({1-[(4J=7,9Гц), 8,07 (1Η, д, J-8,0Гц), 8,86 (1Η, м), 9,61гідрокситетрагідро-2Н-піран-49,81 (1Η, м). іл)метил]піперидин-4-іл}метил)-3-ізопропіл-2MS (ESI) m/z: 431 (M+H+). оксо-2,3-дигідро-1H-бензімідазол-1-карбоксаміду Підраховано аналізом для C23H35N4O4CI: С, (27,0г, 62ммоль) в метанолі (150мл) додавали 59,15; Η, 7,55; Ν, 2,00. Знайдено: С, 58,81; Η, 10% НСІ-метанол (100мл) при температурі на7,57; Ν, 11,85. вколишнього середовища. Через 30 хвилин леткі Альтернативний шлях, щоб синтезувати 4матеріали видаляли випаровуванням. Одержану {[4-(амінометил)піперидин-1-іл]метил}тетрагідроаморфну речовину осаджували сумішшю ета2Н-піран-4-ол описаний нижче. нол/діетиловий ефір. Осад перекристалізовували Стадія 1. Бензил ({1-[(4-гідрокситетрагідроз суміші етанол/діетиловий ефір (1:1), щоб одер2Н-піран-4-іл)метил]піперидин-4'жати 26,5г (90%) вказаної у заголовку сполуки як іл}метил)карбамат безбарвний порошок. 1H-ЯМР (DMSO-d6) δ: 1,49 (6Η, д, J=6,9Гц), 1,50-1,70 (4Η, м), 1,76-1,91 (5Η, Суміш бензил (піперидин-4ілметил)карбамату (7,77г, 31,3ммоль, [Bose, D. Subhas et al, Tetrahedron Lett., 1990, 31, 6903]) і 1,6-діоксаспіро[2,5]октану (4,29г, 37,6ммоль, Saryamurthy, Nagichettiar et ah, [Phosphorus Sulfur, 1984, 19, 113]) в метанолі (93мл) перемішували при кімнатній температурі протягом 20год. Потім суміш нагрівали зі зворотним холодильником протягом 8год. Після охолодження до кімнатної температури, розчинник видаляли у вакуумі. Залишок хроматографували на колонці силікагелю, елююючи сумішшю метанол/дихлорметан (1:20), щоб одержати 5,60г (49%) вказаної у заголовку сполуки як безбарвну олію. Стадія 2. 4-{[4-(Амінометил)піперидин-1іл]метил}тетрагідро-2Н-піран-4-ол Суміш бензил ({1-[(4-гідрокситетрагідро-2Нпіран-4-іл)метил]піперидин-4-іл}метил)карбамату (5,60г, 15,5ммоль, стадія 1) і паладію на активованому вугіллі (10ваг.%, 1,20г) в метанолі (250мл) гідрогенізують при кімнатній температурі протягом 20год. Потім, сполуку фільтрують через подушку целіту, і фільтрат концентрують у вакуумі, щоб одержати 3,30г (94%) вказаної у заголовку сполуки як злегка жовту олію. Наступне являє собою інший шлях, щоб синтезувати 4-{[4-(амінометил)піперидин-1іл]метил}тетрагідро-2Н-піран-4-ол. Стадія 1. 1-[(4-гідрокситетрагідро-2Н-піран-4іл)метил]піперидин-4-карбоксамід Суміш йодиду триметилсульфоксонію (0,791г, 3,52ммоль) і 2N-NaOH водн. (1,76мл, 3,52ммоль) в ацетонітрилі (1,62мл) перемішували при 50°С протягом 30хв. Потім до суміші додавали тетрагідро-4Н-піран-4-он (0,324г, 3,20ммоль) і одержану суміш перемішували при 50°С протягом 3год. Насчич. NaCl водн. (10мл) додають до реакційної суміші при кімнатній температурі і органічний шар екстрагують СН2СІ 2 (20мл), висушують над Na2SO4, фільтрують і концентрують. Після видалення розчинника, МеОН (1,62мл) та ізоніпекотамід (0,381г, 2,88ммоль) додають до залишку, суміш перемішують при 75°С протягом 14год. під N2. Реакційну суміш концентрують і залишок перекристалізовують з МеОНацетонітрилу, щоб одержати 0,484г (2,00ммоль) вказаної у заголовку сполуки як тверду речовину білого кольору. 1H-NMR (300МГц, DMSO-d6) δ 7,19 (ушир, с, 1Н), 6,69 (ушир, с, 1Η), 4,10 (с, 1Η), 3,70-3,50 (м, 4Η), 2,95-2,85 (м, 2Η), 2,20 (с, 2Η), 2,15-1,85 (м, 3Η), 1,65-1,50 (м, 6Н), 1,40-1,25 (м, 2Н). Стадія 2. 4-{[4-(Амінометил)піперидин-1іл]метил}тетрагідро-2Н-піран-4-ол тозилат До перемішуваної суспензії NaBH4 (0,505г, 13,2г) в триетилен гліколь диметиловому ефірі (12,8мл) додають розчин 1-[(4-гідрокситетрагідро2Н-піран-4-іл)метил]піперидин-4-карбоксаміду (0,640г, 2,64ммоль) і АсОН (0,765мл, 13,2ммоль) в триетилен гліколь диметиловому ефірі (3,2мл) краплями при 80°С під N2. Реакційну суміш гасять 2N-HCI водн. доти, доки значення рН не досягне 10. Органічний шар екстрагують СН2СІ 2 тричі, і об'єднаний органічний шар висушують над Na2SO4, фільтрують і концентрують. До залишкового розчину (вказана у заголовку сполука в триетиленгліколь диметиловому ефірі) додають розчин моногідрату р 49 86204 50 (ушир, с, 1Η), 3,70-3,45 (м, 4Η), 2,95-2,85 (м, 2Η), толуолсульфонової кислоти (0,408г, 2,11ммоль) в 2,68 (д, J=7,0, 2Η), 129 (с, 3Η), 2,22 (с, 2Η), 2,07 МеОН (1,28мл) при 60°С, потім суміш охолоджу(т, J=11,0, 2Η), 1,65-1,45 (м, 4Η), 1,55-1,35 (м, 1Η), ють до кімнатної температури. Виявлені тверді 1,40-1,25 (м, 2Н), 1,30-1,10 (м, 2Н). речовини збирають всмоктуванням і промивають Приклад 2. гексаном, щоб одержати вказану у заголовку Ν-({1-[(4-Гідрокситетрагідро-2Н-піран-4сполуку (0,340г, 0,849ммоль) як тверду речовину іл)метил]піперидин-4-іл}метил)3-ізопропіл-2-оксобілого кольору. 1 2,3-дигідро-1Н-бензімідазол-1-карбоксамід геміH-NMR (300МГц, DMSO-d6) δ 7,61 (ушир, с, едизилат 2Η), 7,55-7,40 (м, 2Η), 7,15-7,05 (м, 1Η), 4,11 До перемішуваного розчину N-({1-[(4гідрокситетрагідро-2Н-піран-4іл)метил]піперидин-4-іл}метил)-3-ізопропіл-2оксо-2,3-дигідро-1Н-бензімідазол-1-карбоксаміду 1,51г (3,51ммоль) в етилацетаті (10мл) і метанолу (10мл) додають розчин 1,2етандисульфонової кислоти 397мг (1,75ммоль) в метанолі (5,0мл) і одержану суспензію перемішують протягом 5год. при кімнатній температурі. Суміш фільтрують і перший урожай висушують під вакуумом протягом 5год. при 100°С, щоб одержати 1,78г сирого продукту. 1,61г сирого продукту розчиняють в метанолі (20мл) і додають до розчину етилацетат (20мл). Одержану суспензію перемішують протягом 2год. при кімнатній температурі. Суміш фільтрують і урожай висушують під вакуумом протягом 4год. при 100°С, щоб одержати вказану у заголовку сполуку 1,13г (61%) як безбарвні кристали. MS (ESI) m/z: 431 (M+H)+. т.пл.: 233°С. ІЧ (KВr) ν: 2866, 1738, 1683, 1558, 1373, 1217, 1028, 756см-1. 1 H-ЯМР (DMSO-d6) δ 8,96 (0,25 Η, ушир, с), 8,85 (1Η, ушир, т, J=6,0Гц), 8,61 (0,75Η, ушир, с), 8,06 (1Η, м), 7,43 (1Η, м), 7,21 (1Η, дт, J=13,7,7Гц), 7,13 (1Η, дт, J=1,2, 7,7Гц), 5,26 (1Η, ушир, с), 4,65 (1Η, септет, J=7,0Гц), 3,74-2,92 (12 Η, м), 2,64 (2Η, с), 2,00-1,35 (9Η, м), 1,47 (6Η, д, J=7,0Гц). Підраховано аналізом для C23H34N4O4·0,5 C2H6O6S2: С, 54,84; Η, 7,09; Ν, 10,66; S, 6,10. Знайдено: С, 54,50, Η, 7,24; Ν, 10,60; S, 6,08. Кут рентгенограми PXRD (2-Theta°): 10,2, 11,9, 16,3, 17,3, 17,6, 21,8, 24,2. Приклад 3 3-Ізопропіл-N-{[1-(2-морфолін-4-іл-2оксоетил)піперидин-4-іл]метил}-2-оксо-2,3дигідро-1Н-бензімідазол-1-карбоксамід монооксолат Вказану у заголовку сполуку одержують подібним способом, показаним на Стадії 3 Приготування 1, використовуючи 4(хлорацетил)морфолін [В. G. Hazra; V. S. Pore; S. P. Maybhate, Org. Prep. Proced. Int., 1989, 21, 3558]. MS (ESI) m/z: 440 (M+H)+. т.пл.: 194,2°C. ІЧ (KВr) v: 3443, 2934, 1765, 1728, 1686, 1659, 1612, 1551см-1. 1 H-ЯМР (CDCI 3) (вільна основа) δ: 9,00-8,88 (1H, м) 8,30-8,22 (1H, м), 7,23-7,12 (3Н, м), 4,784,62 (1Н, м), 3,66 (4H, с), 3,70-3,58 (4Н, м), 3,32 (2Н, т, J=6,3Гц), 3,15 (2Н, с), 2,94-2,84 (2Н, м), 2,14-2,01 (2Н, м), 1,86-1,23 (5Н, м), 1,56 (6Н, д, J=7,0Гц). 1 H-ЯМР (DMSO-d6) (сольова форма) δ: 8,928,80 (1Н, м) 8,07 (1H, д, J=7,7Гц), 7,45 (1H, д, J=7,5Гц), 7,26-7,06 (2Н, м), 4,76-4,56 (1H, м), 4,102,60 (18Н, м), 1,90-1,40 (3Н, м), 1,49 (6Н, д, J=6,9Гц). Підраховано аналізом для C25H35N5O8: С, 56,27; Η, 6,61; Ν, 13,13. Знайдено: С, 56,25; Η, 6,82; Ν, 12,98. Приклад 4. 3-Ізопропіл-N-{[1-(3-морфолін-4-іл-3оксопропіл)піперидин-4-іл]метил}-2-оксо-2,3Дигідро-1Н-бензімідазол-1-карбоксамід монооксолат 51 До суміші 3-ізопропіл-2-оксо-N-(піперидин-4ілметил)-2,3-дигідро-1Н-бензімідазол-1карбоксаміду (150мг, 0,474ммоль) і 4-(3-хлорпропаноїл)-морфоліну [G. Mattalia,; С. Serafmi; U. Bucciarelli, Farmaco, Ed. Sri., 1976, 31, 457-67] (300мг, 1,185ммоль) в 4,7мл Ν,Νдиметилформаміду додають триетиламін (0,23мл, 1,659ммоль) і йодид натрію (178мл, 1,185ммоль). Реакційну суміш перемішують при 90°С протягом 6 днів. Реакційну суміш потім концентрують випаровуванням. Залишок розбавляють водним NaHCO3 10мл, екстрагують дихлорметаном 30мл тричі. Об'єднаний екстракт висушують над MgSO4 і концентрують. Препаративна ТШХ (елюент: СН2Сl2/метанол=10/1) дає коричневу аморфну олію 130мг (60%). Аморфну речовину (130мг) розчиняють в 3мл метанолу і ацилюють розчином 24мг щавлевої кислоти в 2мл МеОН. Суміш концентрують. Кристалізація одержаного залишку з AcOEt-EtOH дає білу аморфну речовину 107мг як вказану у заголовку сполуку. Вказану у заголовку сполуку одержують подібним способом, показаним у прикладі 4, використовуючи 4-(хлор-бутирил)морфолін [Schlesinger, Prill; В. G. Hazra; J.Amer.Chem.Soc, 1956, 78, 6123-6124]. MS (ESI) m/z: 472 (M+H)+. ІЧ (KBr) v: 3443, 1728, 1686, 1647-1616, 1551см-1. 1 H-ЯМР (CDCI 3) (вільна основа) δ: 9,02-8,88 (1H, м), 8,31-8,20 (1H, м), 7,22-7,04 (3Н, м), 4,804,60 (1Н, м), 3,66-3,56 (8H, м), 3,40-3,22 (2Н, м), 3,00-2,88 (2Н, м), 2,50-2,30 (6Н, м), 2,00-120 (7Н, м), 1,57 (6Н, д, J=7,1Гц). 86204 52 MS (ESI) m/z: 458 (М+Н)+. ІЧ IR (KBr) v: 3443, 2941, 1732, 1697, 1686, 1647, 1638, 1558см-1. 1 H-ЯМР (CDCI 3) (вільна основа) δ: 9,06-8,94 (1H, ушир.) 8,24-8,19 (1Н, м), 7,26-7,10 (3Н, м), 4,76-4,64 (1H, м), 3,75-2,80 (10Н, м), 2,60-1,30 (13Н, м), 1,56 (6Н, д, J=7,0Гц). 1 H-ЯМР (CDCI 3) (сольова форма) δ: 9,10-9,00 (1Н, м) 8,27-8,17 (1H, м), 7,33-7,12 (3Н, м), 4,874,62 (1H, м), 3,78-2,65 (16Н, м), 2,20-1,60 (7Н, м), 1,56 (6Н, д, J=6,9Гц). Підраховано аналізом для С26H37N5О8×0,9С2Н2О4×1,3Н2О: С, 51,21; Η, 6,40; Ν, 10,74. Знайдено: С, 50,90; Η, 6,26; Ν, 11,13. Приклад 5. 3-Ізопропіл-N-{[1-(4-морфолін-4-іл-4охобутил)піперидин-4-іл]метил}-2-оксо-2,3Дигідро-1Н-бензімідазол-1-карбоксамід монооксолат 1 H-ЯМР (DMSO-d6) (сольова форма) δ: 8,938,79 (1H, м) 8,07 (1H, д, J=7,5Гц), 7,44 (1H, д, J=7,5Гц), 7,27-7,08 (2Н, м), 4,75-4,58 (1H, м), 4,472,30 (18Н, м), 1,90-0,90 (7Н, м), 1,49 (6Н, д, J=6,9Гц). Підраховано аналізом для C27H39N5O8: С, 57,74; Η, 7,00; Ν, 12,47. Знайдено: С, 57,52; Η, 7,03; Ν, 12,32. Приклад 6. Ν-({1-[(транс-1,4Дигідроксигексил)метил]піперидин-4-іл}метил)-3ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1карбоксамід гідрохлорид Стадія 1. трет-Бутил(1-оксаспіро[2,5]окт-6-ілокси)дифенілсилан 53 86204 54 До перемішуваної суспензії гідриду натрію (60% в мінеральній олії, 441мг, 11,0ммоль) в DMSO (7мл) додають триметилсульфоксоній йодид (2,53г, 11,5ммоль) при кімнатній температурі, і суміш перемішують при кімнатній температурі протягом 30 хвилин. До цієї суміші додають розчин 4-{[третбутил(дифеніл)силіл]окси}циклогексанону ([Okamura, William H. et al, J.Org.Chem., 1993, 58, 600610], 3,53г, 10,0ммоль) в DMSO (35мл) краплями при кімнатній температурі, суміш перемішують при кімнатній температурі протягом для 2год. Потім суміш розбавляють водою (600мл) і екстрагують діетиловим ефіром (200мл´4). Об'єднаний органічний шар висушують над сульфатом магнію і концентрують у вакуумі. Залишок хроматографують на колонці силікагелю, елююючи сумішшю n-гексан/етилацетат (1:10), і потім очищують препаративною ТШХ, елююючи сумішшю п-гексан/етилацетат (1:15), щоб одержати 459мг (13%, транс) і 390мг (11%, цис) вказаної у заголовку сполуки як безбарвну олію відповідно. (транс) 1 H-ЯМР (CDCI 3) δ: 7,70-7,66 (4Η, м), 7,46-7,35 (6Η, м), 4,03-3,97 (1Η, м), 2,63 (2Η, с), 2,07-1,63 (8Η, м), 1,08 (9Η, с). (цис) 1 H-ЯМР (CDCI 3) δ: 7,70,7,65 (4Η, м), 7,46-7,35 (6Η, м), 3,97-3,83 (1Η, м), 2,58 (2Η, с), 1,83-1,37 (8Η, м), 1,07 (9Η, с). Стадія 2. N-({1-[(транс-4-[третБутил(дифеніл)силіл]окси-1гідроксициклогексил)метил]піперидин-4іл]метил}-3-ізопропіл-2-оксо-2,3-дигідро-1Нбензімідазол-1-карбоксамід гідрохлорид Суміш трет-бутил[(3R,6R)-1-оксаспіро[2,5]окт6-ілокси]диіфенілсилану (Стаді 1, транс-ізомер, 283,0мг, 0,772ммоль) і 3-ізопропіл-2-оксо-N(піперидин-4-ілметил)-2,3-дигідро-1Нбензімідазол-1-карбоксаміду (Приготування 1, стадія 2, 2,48г, 0,0194моль) в МеОН (4мл) нагрівають при 50°С з перемішуванням протягом 2 днів. Після охолодження реакційну суміш випаровують, щоб видалити розчинник, і залишок хроматографують на колонці силікагелю, елююючи сумішшю етилацетат/n-гексан (1:10), потім сумішшю метанол/дихлорметан (1:20). щоб одержати 308,1мг (58%) вказаної у заголовку сполуки як безбарвний сироп. MS (ESI) m/z: 683 (М+Н)+. H-ЯМР (CDCI 3) δ: 8,93 (1Η, м), 8,32-8,23 (1Η, м), 7,72-7,60 (4Η, м), 7,46-7,32 (6Η, м), 7,22-7,10 (3Η, м), 4.80-4,62 (1Η, м), 3,96 (1Η, м), 331 (2Η, т, J=6,26Гц), 2,92 (2Η, д, J=10,88Гц), 2,45-2,29 (4Η, м), 1,85-1,65 (6Η, м), 1,65-1,43 (9Η, м, включаючи 6Η, д, J=7,09Гц в 1,56м.ч.), 1,43-1,25 (4Н, м), 1,06 (9Н, с). Стадія 3. N-({1-[(транс-1,4Дигідроксициклогексил)метил]піперидин-4іл}метил)-3-ізопропіл-2-оксо-2,3-дигідро-1Нбензімідазол-1-карбоксамід гідрохлорид Суміш трет-бутил N-{1-({транс-4-[третбутил(дифеніл)силіл]окси-1гідроксициклогексил}метил)піперидин-4іл]метил}-3-ізопропіл-2-оксо-2,3-дигідро-1Hбензімідазол-1-карбоксаміду (234мг, 0,343 мол) і НСІ розчину МеОН (50мл) перемішують при кімнатній температурі протягом 4год. Потім розчинник видаляють у вакуумі. Залишок роблять основним насиченим водним NaHCO3 (30мл), екстрагують СН2СІ 2 (30мл´3 рази) і об'єднаний органічний шар висушують над Na2SO4. Видалення розчинника дає залишок, який хроматографують на колонці NH-силікагелю, елююючи сумішшю етилацетат/n-гексан (1:1-2:1), щоб одержати 140,1мг (92%) вказаної у заголовку сполуки як безбарвний сироп. MS (ESI) m/z: 445 (М+Н)+. 1 1 H-ЯМР (CDCI 3) δ: 8,93 (1Η, ушир, т, J=5,87Гц), 8,32-8,20 (1Η, м), 7,25-7,03 (3Η, м), 4,80-4,62 (1Η, м), 3,94 (1Η, м), 3,31 (2Η, т, J=6,10Гц), 2,89 (2Η, ушир, д, J=11,53Гц), 2,36 (2Η, с), 2,34 (2Η, т, J=11,86Гц), 2,00-1,85 (2Η, м), 1,821,25 (18Η, м, включаючи 6Η, д, J=7,09Гц в 1,56м.ч.). 140,1мг цього сиропу розчиняють у розчині НСІ в МеОН (4мл), концентрують і висушують у вакуумі при 50°С протягом 5год., щоб одержати 139,2мг вказаної у заголовку сполуки, як жовту аморфну тверду речовину. MS (ESI) m/z: 445 (М+Н)+. 1 H-ЯМР (DMSO-d6) δ: 9,35-8,75 (1H, м), 8,86 (1Η, т, J=6,59Гц), 8,07 (1Η, д, J=7,74Гц), 7,44 (1Η, д, J=7,58Гц), 7,22 (1Η, дт, J=1,15 Гц, 7,42Гц), 7,14 (1Η, дт, J=1,32 Гц, 7,74Гц), 5,04 (1Η, ушир, с), 55 86204 56 Кут рентгенограми PXRD (2-Theta°): 8,3, 14,5, 4,75-4,45 (1Η, м), 3,70 (1Η, ушир, с), 3,59 (2Η, д, 17,7, 18,3, 19,1, 26,4, 27,5. J=11,70Гц), 3,50-2,90 (8Η, м), 1,90-1,57 (8Η, м), Приклад 7 1,57-1,30 (10Η, м, включаючи 6Η, д, J=6,92Гц в N-({1-[(цис-1,41,49м.ч.). Дигідроксигексил)метил]піперидин-4-іл}метил)-3ІЧ (KВr): 3285, 2936, 2677, 1728, 1686, 1611, ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-11549, 1481, 1375, 1298, 1204, 1157, 1101, 1018, карбоксамід гідрохлорид 762см-1. Підраховано аналізом для C24H36N4O4-HCI2H2O: С, 57,76; Н, 7,88; N, 11,23. Знайдено: С, 57,54; Н, 7,90; N, 11,21. Стадія 1. Н-({1-[(цис-4-[трет-Бутил(дифеніл)силіл]окси-1-гідроксициклогексил)метил]піперидин-4іл]метил}-3-ізопропіл-2-оксо-2,3-дигідро-1H-бензімідазол-1-карбоксамід. Вказану у заголовку сполуку одержують відповідно до методики, яка розкрита на Стадії 2 у Прикладі 6, використовуючи тpeт-бутил[(3S,6S)-1оксаспіро[2,5]окт-6-ілокси]дифенілсилан (Приклад 6, Стадія 1, цис-ізомер, 311,0мг, 0,848ммоль) замість трет-бутил[(3R,6R)-1оксаспіро[2,5]окт-6-ілокси]дифенілсилан. MS (ESI) m/z: 683 (М+Н)+. 1 H-ЯМР (CDCI 3) δ: 8,91 (1Η, т, J=5,87Гц), 8,30-8,22 (1Η, м), 7,72-7,63 (4Η, м), 7,45-7,30 (6Η, м), 7,20-7,10 (3Η, м), 4,80-4,63 (1Η, м), 3,59 (1Η, м), 3,29 (2Η, т, J=6,24Гц), 2,83 (2Η, д, J=11,74Гц), 2,26 (2Η, т, J=11,55Гц), 2,18 (2Η, с), 1,85-1,65 (4Η, м), 1,65-1,50 (11Η, м, включаючи 6Η, д, J=7,15Гц в 1,56м.ч.), 1,40-1,30 (2Η, м), 1,15-1,00(11Η, м, включаючи 9Η, с, 1,05м.ч.). Стадія 2. Ν-({1-[(цис-1,4Дигідроксициклогексил)метил]піперидин-4іл}метил)-3-ізопропіл-2-оксо-2,3-дигідро-1Нбензімідазол-1-карбоксамід гідрохлорид Вказану у заголовку сполуку одержують відповідно до методики, яка розкрита на Стадії 3 у Прикладі 6, використовуючи N-{[1-({цис-4-[третбутил(дифеніл)силіл]окси-1гідроксициклогексил}метил)піперидин-4іл]метил}-3-ізопропіл-2-оксо-2,3-дигідро-1Нбензімідазол-1-карбоксамід (295,0мг, 0,432ммоль) замість Ν-{[1-({транс-4[дифеніл(триметилсиліл)метокси]-1гідроксициклогексил}метил)піперидин-4іл]метил}-3-ізопропіл-2-оксо-2,3-дигідро-1Нбензімідазол-1-карбоксамід. MS (ESI) m/z: 445 (М+Н)+. 1 H-ЯМР (CDCI 3) δ: 8,93 (1Η, ушир, т, J=5,60Гц), 8,31-8,22 (1Η, м), 7,25-7,10 (3Η, м), 4,80-4,62 (1Η, м), 3,63-3,49 (1Η, м), 3,31 (2Η, т, J=6,10Гц), 2,89 (2Η, ушир, д, J=11,54Гц), 2,33 (2Η, дт, J=1,81Гц, 11,70Гц), 1,85-1,60 (16Η, м, вклю чаючи 6Η, д, J=7,09Гц при 1,57м.ч.), 1,45-1,18 (4Η, м). 165,7мг цього сиропу розчиняють у розчині НСІ в МеОН (4мл), концентрують і висушують у вакуумі при 50°С протягом 5год., щоб одержати 164,7мг вказаної у заголовку сполуки як жовту аморфну тверду речовину. MS (ESI) m/z: 445 (М+Н)+. 1 H-ЯМР (DMSO-d6) δ: 9,30-8,90 (1Η, м), 8,86 (1Η, т, J=5,93Гц), 8,07 (1Η, д, J=7,58Гц), 7,44 (1Η, д, J=7,58Гц), 7,22 (1Η, дт, J=1,48Гц, 7,75Гц), 7,15 (1Η, дт, J=1,15Гц, 7,74Гц), 4,75-4,58 (1Н, м), 3,702,90 (11Н, м), 1,90-1,67 (6 Н, м), 1,67-1,20 (12Н, м, включаючи 6Η, д, J=6,92Гц в 1,49м.ч.). ІЧ (KВr): 3294, 2936, 2673, 1728, 1686, 3611, 1545, 1479, 1375, 1298, 1203, 1158, 1134,1101, 1051, 762см-1. 57 86204 58 Підраховано аналізом для C24H36N4O4-HCI6-Фтор-N-({1-[(4-гідрокситетрагідро-2Н-піран5H2O: С, 54,79; Н, 8,05; N, 10,65, Знайдено: С, 4-іл)метил]піперидин-4-іл}метил)-3-ізопропіл-254,75; Н, 7,88; N, 10,56. оксо-2,3-дигідро-1H-бензімідазол-1-карбоксамід Приклад 8: гідро хлорид Стадія 1. 6-Φтορ-Ν-({1-[(4-гідрокситетрагідро-2Н-піран-4-іл)метил]-піперидин-4-іл}метил)-3-ізопропіл-2оксо-2,3-дигідро-1Н-бензімідазол-1-карбоксамід Вказану у заголовку сполуку одержують відповідно до методики, яка розкрита на Стадії 3 Прикладу 1, з 5-фтор-1-ізопропіл-1,3-дигідро-2Нбензімідазол-2-ону [І. Tapia et al, J. Med. Chem., 1999, 42, 2880] і 4-{[4-(амінометил)піперидин-1іл]метил}тетрагідро-2Н-піран-4-олу (стадія 2 Прикладу 1). MS (ESI) m/z: 449 (М+Н+). 1 H-ЯМР (CDCI 3) δ: 1,12-1,70 (8Η, м), 1,55 (6Η, д, J=7,0Гц), 1,74 (2Н, ушир, д, 12,8 Н2), 2,31 (2Н, с), 2,35 (2Н, ушир, т, J=11,9Гц), 2,88 (2Η, ушир, д, J=11,7Гц), 3,30 (2Η, т, J=6,2Гц), 3,70-3,85 (4Η, м), 4,62-4,75 (1Η, м), 6,90 (1Η, тд, J=9,0,2,4Гц), 7,027,07 (1Η, м), 8,05 (1Η, дд, J=9,5, 2,6Гц), 8,85-8,92 (1Η, м). Стадія 2. 6-Φтορ-Ν-({1-[(4-гідрокситетрагідро2Н-піран-4-іл)метил]-піперидин-4-іл}метил)-3ізопропіл-2-оксо-2,3-дигідро-1H-бензімідазол-1карбоксамід гідрохлорид Вказану у заголовку сполуку одержують відповідно до методики, яка розкрита на Стадії 4 Прикладу 1, з 6-фтор-N-{1-[(4-гідрокситетрагідро2Н-піран-4-іл)метил]піперидин-4-іл}метил)-3ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1карбоксаміду (стадія 1 Прикладу 8). MS (ESI) m/z: 449 (М+Н+). 1 H-ЯМР (DMSO-d6) δ: 1,46 (6Η, д, J=6,9Гц), 1,55-1,65 (4Η, м), 1,70-1,91 (4Η, м), 2,90-3,28 (8Η, м), 3,50-3,67 (6Η, м), 4,56-4,69 (1Η, м), 5,30-5,37 (1Η, м), 5,76 (1Η, с), 7,08 (1Η, тд, J=9,0,2,4Гц), 7,44-7,49 (1Η, м), 7,85 (1Η, дд, J=9,5, 2,5Гц), 8,818,85 (1Η, м). Підраховано аналізом для C23H34FN4O4CI: С, 56,96; Η, 7,07; Ν, 11,55. Знайдено: С, 57,00; Η, 7,20; Ν, 11,43. Кут рентгенограми PXRD (2-Theta°): 10,0, 14,6, 16,2, 18,5, 23,2, 25,3, 27,3. Приклад 9: 5-фтор-N-({1-[(4-гідрокситетрагідро-2Н-піран4-іл)метил]піперидин-4-іл}метил)-3-ізопропіл-2оксо-2,3-дигідро-1Н-бензімідазол-1-карбоксамід Стадія 1. (5-фтор-2-нітрофеніл)ізопропіламін До перемішуваної суміші 2,4-дифтор-1нітробензолу (4,77г, 30ммоль) і K2СО3 (4,14г, 30ммоль) в THF (30мл) додають ізопропіламін (1,77г, 30ммоль) в THF (10мл) при 0°С. Після перемішування протягом 13год. нерозчинні матеріали видаляють подушкою целіту і фільтрат концентрують під зниженим тиском, щоб одержати вказану у заголовку сполуку (5,25г, 88%) як блідожовту олію. MS (ESI) m/z: 405 (М+Н+). 1 H-ЯМР (CDCI 3): δ 8,21 (1Η, дд, J=9,3, 6,0Гц), 6,48 (1Η, дд, J=11,7, 2,6Гц), 6,39-6,29 (1Η, м), 3,81-3,66 (1Η, м), 1,33 (6Η, д, J=6,4Гц). Стадія 2. 6-фтор-1-ізопропіл-1,3-дигідро-2Нбензімідазол-2-он Суміш (5-фтор-2-нітрофеніл)ізопропіламіну (Стадія 1 Прикладу 9, 5,85г, 30ммоль) і 10% Pd-C (600мг) в МеОН перемішують під атмосферою водневого газу при кімнатній температурі протягом 12год. Каталізатор відфільтровують на подушці целіту, і фільтрат випаровують під зниженим тиском. До залишку додають 1, Гкарбонілдіімідазол (4,5г, 28ммоль) і THF (100мл) і потім перемішують при 100°С протягом 10год. Після охолодження леткі матеріали видаляють під зниженим тиском і залишок розподіляють між етилацетатом і Н2О. Після екстрагування етилацетатом (3 рази), об'єднану органічну фазу промивають розсолом, висушують над MgSO4 і концентрують. Залишок хроматографують на колонці силікагелю, елююючи сумішшю гексан/етилацетат (2:1), щоб одержати 3,47г (60%) вказаної у заголовку сполуки як тверду речовину білого кольору. MS (ESI) m/z: 195 (М+Н+), 193 (М-Н+). 1 H-ЯМР (CDCI 3): δ 7,06-6,99 (1Η, м), 6,90 (1Η, дд, J=9,2, 2,4Гц), 6,82-6,72 (1Η, с), 4,83-4,62 (1Η, м), 1,54 (6Η, д, J=7,1Гц). 59 86204 60 Стадія 3 5-фтор-Ν-({1-[(4-гідрокситетрагідроПрикладу 9, з 4,5-дифтор-N-ізопропіл-22Н-піран-4-іл)метил]-піперидин-4-іл}метил)-3нітроаніліну (Стадія 1 Прикладу 10). ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-1MS (ESI) m/z: 213 (М+Н+), 211 (М+Н+). 1 карбоксамід H-ЯМР (CDCI 3): δ 7,00-6,89 (2Η, м), 4,76-4,57 До перемішуваної суміші 6-фтор-1-ізопропіл(1Η, м), 3,86-3,69 (4Η, м), 3,31 (2Η, т, J=7,0Гц), 1,3-дигідро-2Н-бензімідазол-2-ону (Стадія 2 При2,95-2,82 (2Η, м), 2,35 (2Η, т, J=13,7Гц), 2,31 (2Η, кладу 9, 0,58г, 3ммоль) і рс), 1,67-1,25 (10Η, м), 1,55 (6Η, д, J=7,7Гц). нітрофенілхлорформіату (0,66г, 3,3ммоль) в дихСтадія 3. 5,6-дифтор-N-({1-[(4лоргоетані (15мл) додають триетиламін (1,25мл, гідрокситетрагідро-2Н-піран-4-іл)метил]9,0ммоль) при кімнатній температурі. Після пепіперидин-4-іл}метил)-3-ізопропіл-2-оксо-2,3ремішування протягом 2год., розчин 4-{[4дигідро-1H-бензімідазол-1-карбоксамід (амінометил)піперидин-1-іл]метил}тетрагідро-2НВказану у заголовку сполуку одержують відпіран-4-олу (Стадія 2 Прикладу 1, 0,75г, повідно до методики, яка розкрита на Стадії 3 3,3ммоль) в дихлорметані (15мл) додають до Прикладу 9, з 5,6-дифтор-1-ізопропіл-1,3-дигідросуміші. Після перемішування протягом 4год., су2Н-бензімідазол-2-ону (Стадія 2 Прикладу 10) і 4міш розбавляють етилацетатом (100мл). Потім {[4-(амінометил)піперидин-1-іл]метил}тетрагідроорганічний шар промивають 0,5N NaOH водн. 2Н-піран-4-олу (Стадія 2 Прикладу 1). (10мл) 5 разів і розсолом, висушують над MgSO4 і MS (ESI) m/z·467 (М+Н+). 1 концентрують. Залишок хроматографують на H-ЯМР (CDCI 3): δ 8,88-8,78 (1Η, м), 8,25-8,15 колонці амінопропіл-силікагелю, елююючи сумі(1Η, м), 6,94-6,79 (2Η, м), 4,73-4,57 (1Η, м), 3,86шшю гексан/етилацетат (3:1), щоб одержати 3,69 (4Η, м), 3,31 (2Η, т, J=7,0Гц), 2,95-2,82 (2Η, 0,97г (79%) вказаної у заголовку сполуки як тверм), 2,35 (2Η, т, J=13,7Гц), 2,31 (2Η, с), 1,67-1,25 ду речовину білого кольору. (10Η, м), 1,55 (6Η, д, J=7,7Гц). MS (ESI) m/z: 449 (М+Н+). Стадія 4. 5,6-дифтор-N-({1-[(41 H-ЯМР (CDCI 3): δ 8,84-8,74 (1Η, м), 8,21-8,11 гідрокситетрагідро-2Н-піран-4-іл)метил](2Η, м), 7,02-6,91 (2Η, м), 4,68-4,56 (1Η, м), 3,87піперидин-4-іл}метил)-3-ізопропіл-2-оксо-2,33,72 (4Η, м), 3,34-3,25 (2Η, м), 2,93-2,82 (2Η, м), дигідро-1Н-бензімідазол-1-карбоксамід гідрохло2,42-2,25 (4Η, м), 1,79-1,68 (2Η, м), 1,67-1,29 рид (13Η, м). Суміш 5,6-дифтор-N-({-1-[(4Підраховано аналізом для C23H33N4O4F: С, гідрокситетрагідро-2Н-піран-4-іл)метил]61,59; Η, 7,42; Ν, 12,49. Знайдено: С, 61,45; Η, піперидин-4-іл}метил)-3-ізопропіл-2-оксо-2,37,33; Ν, 12,40. дигідро-1Н-бензімідазол-1-карбоксаміду (Стадія 3 Приклад 10: Прикладу 10, 113мг, 0,242ммоль) і 10% НСІ5,6-дифтор-N-({1-[(4-гідрокситетрагідро-2Нметанолу (5мл) перемішують протягом 1год. Попіран-4-іл)метил]тперидин-4-іл}метил)-3тім леткі компоненти видаляють під зменшеним ізопропіл-2-оксо-2,3 -дигідро-1Н-бензімідазол-1тиском і залишок перекристалізовують з етанолкарбоксамід гідрохлорид діетилового ефіру, щоб одержати 88мг (72%) вказаної у заголовку сполуки як безбарвний порошок. MS (ESI) m/z: 467 (М+Н+). 1 H-ЯМР (DMSO-d6): δ 8,82-8,71 (1Η, м), 8,087,93 (1Η, м), 7,78-7,67 (1Η, м), 5,35-5,26 (1Η, м), 4,69-4,52 (1Η, м), 3,70-3,51 (6Η, м), 3,41-2,91 (7Η, Стадія 1. 4,5-дифтор-N-ізопропіл-2м), 1,94-1,53 (8Η, м), 1,45 (6Н, д, J=7,0Гц). нітроанілін Підраховано аналізом для 4,5-дифтор-2-нітроанілін (3,48г, 20ммоль), С23Н33N4O4F2Cl×1H2O: С, 53,96; Η, 6,69; Ν, 10,94. 2,2-диметоксипропан (11,9мл, 100ммоль) і триЗнайдено: С, 53,67; Η, 6,64; Ν, 10,89. фтороцтову кислоту (1,6мл, 21ммоль) розчиняПриклад 11: ють в толуолі (40мл) і перемішують при кімнатній 6-хлор-N-({1-[(4-гідрокситетрагідро-2Н-пірантемпературі протягом 1год. Додають повільно 4-іл)метил]піперидин-4-іл}метил)-3-ізопропіл-2комплекс бор-піридину (2,12мл, 21ммоль). Реакоксо-2,3 -дигідро-1Н-бензімідазол-1-карбоксамід ційну суміш перемішують протягом 20год. Розгідро хлорид чинник випаровують у вакуумі, і залишок вміщують у воду і екстрагують дихлорметаном. Органічний екстракт висушують (Na2SO4) і концентрують у вакуумі. Залишок хроматографують на колонці амінопропіл-силікагелю, елююючи сумішшю гексан/етилацетат (30:1), щоб одержати 2,42г (56%) вказаної у заголовку сполуки як світСтадія 1. 6-хлор-N-({1-[(4-гідрокситетрагідро2Н-піран-4-іл)метил]-піперидин-4-іл}метил)-3ло-оранжеву тверду речовину. 1 H-ЯМР (CDCI 3): δ 8,05 (1Η, дд, J=10,8, ізопропіл-2-оксо-2,3-дигідро-1Н-бензімідазол-18,6Гц), 6,61 (1Η, дд, J=12,6, 6,8Гц), 3,77-3,62 (1Η, карбоксамід м), 1,33 (6Η, д, J=6,2Гц). Вказану у заголовку сполуку одержують відСтадія 2. 5,6-дифтор-1-ізопропіл-1,3-дигідроповідно до методики, яка розкрита на Стадії 3 Прикладу 9, з 5-хлор-1-ізопропіл-1,3-дигідро-2Н2Н-бензімідазол-2-он Вказану у заголовку сполуку одержують відбензімідазол-2-ону [І. Tapia et al, J. Med. Chem., 42, 2880 (1999)] і 4-{[4-(амінометил)піперидин-1повідно до методики, яка розкрита на Стадії 2
ДивитисяДодаткова інформація
Назва патенту англійськоюBenzimidazolone compounds having 5-ht4 receptor agonistic activity
Автори англійськоюIguchi Satoru, Katsu Yasuhiro, Sone Hiroki, Uchida Chikara, Kojima Takashi
Назва патенту російськоюСоединения бензимидазолона, которые имеют 5-нт4 рецепторную агонистическую активность
Автори російськоюИгути Сатору, Кацу Ясухиро, Сонэ Хироки, Утида Тикара, Кодзима Такаси
МПК / Мітки
МПК: C07D 413/14, A61P 1/04, C07D 405/06, A61K 31/4184, C07D 401/12, C07D 405/14
Мітки: активність, бензимідазолону, рецепторну, агоністичну, сполуки, мають, 5-нт4
Код посилання
<a href="https://ua.patents.su/34-86204-spoluki-benzimidazolonu-yaki-mayut-5-nt4-receptornu-agonistichnu-aktivnist.html" target="_blank" rel="follow" title="База патентів України">Сполуки бензімідазолону, які мають 5-нт4 рецепторну агоністичну активність</a>
Попередній патент: Термінал для керування потужністю передачі на основі оцінки біта зворотної активності і заданих лінійно-зростаючих/спадних функцій потоків даних (варіанти)
Наступний патент: Система збору та обробки даних
Випадковий патент: Лінія виготовлення деревинних композиційних матеріалів із шпону