Нітрофеніліпритні і нітрофенілазиридинові спирти і їх відповідні фосфати, і їх застосування як націлених цитотоксичних засобів
Номер патенту: 89363
Опубліковано: 25.01.2010
Автори: Етвелл Грехем Джон, Ян Шанцзинь, Хелзбі Нуала Анн, Уілсон Уілльям Роберт, Денні Уілльям Александер, Петтерсон Адам Ворн
Формула / Реферат
1. Фосфатна сполука формули (І)
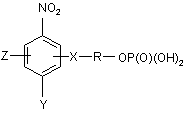 , (I)
, (I)
де:
X представляє в будь-якому доступному положенні кільця -CONH;
R представляє нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди;
Y представляє -N-азиридиніл, -N(CH2CH2W)2 або -N(CH2СНMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me;
Z представляє в будь-якому доступному положенні кільця -NO2, галоген, -CN, -CF3 або -SO2Me;
і її фармацевтично прийнятні солі й похідні.
2. Фосфатна сполука формули (І) за п. 1, яка вибрана зі сполуки, представленої формулами (Ia), (Ib) або (Іс)
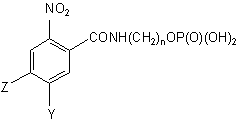 , (Ia)
, (Ia)
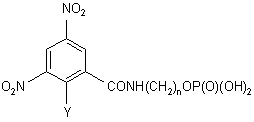 , (Ib)
, (Ib)
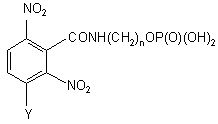 , (Ic)
, (Ic)
де Y представляє
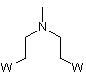 або
або ![]() ,
,
і де
n дорівнює 1-6;
Z представляє -NO2, галоген, -CN, -CF3 або -SO2Me; і
де кожний W незалежно вибраний з галогену або -OSO2Me;
і її фармацевтично прийнятних солей і похідних.
3. Фосфатна сполука формули (І) за п. 1 або п. 2, яка вибрана із групи, що включає:
2-[[2-[біс(2-брометил)аміно]-3,5-динітробензоїл]аміно]етилдигідрофосфат;
3-[[5-[біс(2-хлоретил)аміно]-2,4-динітробензоїл]аміно]пропілдигідрофосфат;
3-[[5-[біс(2-брометил)аміно]-2,4-динітробензоїл]аміно]пропілдигідрофосфат;
2-[[2-[біс(2-хлоретил)аміно]-3,5-динітробензоїл]аміно]етилдигідрофосфат;
2-[(2-хлоретил)-2,4-динітро-6-[[[2-(2-фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфонат;
2-({2-[біс(2-бромпропіл)аміно]-3,5-динітробензоїл}аміно)етилдигідрофосфат;
2-[(2-брометил)-2,4-динітро-6-[[[2-(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфонат;
2-[[2-[біс(2-йодетил)аміно]-3,5-динітробензоїл]аміно]етилдигідрофосфат;
2-[(2-йодетил)-2,4-динітро-6-({[2-(фосфонооксі)етил]аміно}карбоніл)аніліно]етилметансульфонат;
2-[(2-хлоретил)-2,4-динітро-3-[[[3-(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфонат;
3-({3-[біс(2-брометил)аміно]-2,6-динітробензоїл}аміно)пропілдигідрофосфат;
2-[(2-брометил)-2,4-динітро-3-[[[2-(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфонат;
2-[(2-брометил)-2,4-динітро-3-[[[3-(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфонат і
2-[(2-йодетил)-2,4-динітро-3-[[[3-(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфонат.
4. Спосіб одержання фосфату, представленого загальною формулою (І)
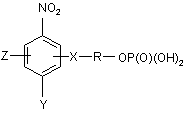 , (I)
, (I)
де:
X представляє в будь-якому доступному положенні кільця -CONH;
R представляє нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди;
Y представляє -N-азиридиніл або -N(CH2CH2W)2, де кожний W незалежно вибраний з галогену або -OSO2Me;
Z представляє в будь-якому доступному положенні кільця -NO2, галоген, -CN, -CF3 або -SO2Me;
і його фармацевтично прийнятних солей і похідних;
при якому здійснюють таку стадію
(і) фосфорилування сполуки формули (II)
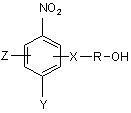 , (II)
, (II)
де:
X представляє в будь-якому доступному положенні кільця -CONH;
Y представляє в будь-якому доступному положенні кільця -N-азиридиніл, -N(CH2CH2W)2 або -N(CH2СНMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me;
Z представляє в будь-якому доступному положенні кільця -NO2, галоген, -CN, -CF3 або -SO2Me; і
R представляє нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди.
5. Спосіб одержання сполуки формул (Ia), (Ib) або (Іс)
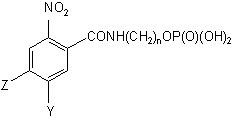 , (Ia)
, (Ia)
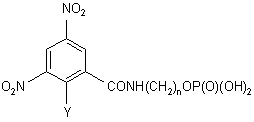 , (Ib)
, (Ib)
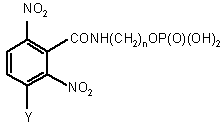 , (Ic)
, (Ic)
де Y може представляти
 або
або ![]() ,
,
і де
n дорівнює 1-6;
Z представляє -NO2, галоген, -CN, -CF3 або -SО2Me; і
де кожний W незалежно вибраний з галогену або -OSO2Me;
і її фармацевтично прийнятних солей і похідних,
при якому здійснюють стадію
фосфорилування сполуки, представленої формулами (ІІа), (ІІb) або (ІІс)
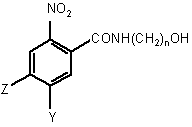 , (ІIa)
, (ІIa)
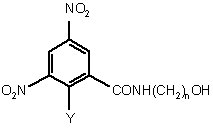 , (ІIb)
, (ІIb)
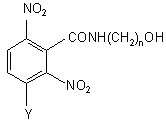 , (IІc)
, (IІc)
де Y представляє
 або
або ![]() ,
,
і де
n дорівнює 1-6;
Z представляє -NO2, галоген, -CN, -CF3 або -SО2Me; і
де W незалежно вибраний з галогену або -OSO2Me; і
її фармацевтично прийнятних солей і похідних.
6. Спосіб протиракового лікування, при якому здійснюють стадію введення суб'єкту ефективної кількості сполуки формули (І), як визначено в будь-якому з пп. 1-3.
7. Спосіб знищення гіпоксичних клітин пухлини, при якому здійснюють введення суб'єктові з пухлиною ефективної кількості сполуки формули (І), як визначено в будь-якому з пп. 1-3.
8. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки формули (І), як визначено за будь-яким з пп. 1-3, і фармацевтично прийнятний ексципієнт, ад'ювант, носій, буфер або стабілізатор.
9. Сполука, вибрана з:
2-[(2-брометил)-2,4-динітро-6-[[[2-(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфонату;
2-[(2-брометил)-2,4-динітро-3-[[[2-(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфонату;
2-[(2-брометил)-2,4-динітро-3-[[[3-(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфонату й
2-[(2-йодетил)-2,4-динітро-3-[[[3-(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфонату.
10.Сполука 2-[(2-брометил)-2,4-динітро-6-[[[2-(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфонат.
11. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за п. 10 і фармацевтично прийнятний ексципієнт, ад'ювант, носій, буфер або стабілізатор.
12. Застосування ефективної кількості сполуки формули (І) за п. 10 при виготовленні лікарського засобу для лікування раку в суб'єкта.
Текст
1. Фосфатна сполука формули (І) 2 3 89363 4 4. Спосіб одержання фосфату, представленого загальною формулою (І) NO2 NO2 CONH(CH2)nOP(O)(OH)2 (Ic) NO2 Z Y де Y представляє N W або R (I) OP(O)(OH)2 , N W X , і де n дорівнює 1-6; Z представляє -NO2, галоген, -CN, -CF3 або SO2Me; і де кожний W незалежно вибраний з галогену або OSO2Me; і її фармацевтично прийнятних солей і похідних. 3. Фосфатна сполука формули (І) за п. 1 або п. 2, яка вибрана із групи, що включає: 2-[[2-[біс(2-брометил)аміно]-3,5динітробензоїл]аміно]етилдигідрофосфат; 3-[[5-[біс(2-хлоретил)аміно]-2,4динітробензоїл]аміно]пропілдигідрофосфат; 3-[[5-[біс(2-брометил)аміно]-2,4динітробензоїл]аміно]пропілдигідрофосфат; 2-[[2-[біс(2-хлоретил)аміно]-3,5динітробензоїл]аміно]етилдигідрофосфат; 2-[(2-хлоретил)-2,4-динітро-6-[[[2-(2фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфона т; 2-({2-[біс(2-бромпропіл)аміно]-3,5динітробензоїл}аміно)етилдигідрофосфат; 2-[(2-брометил)-2,4-динітро-6-[[[2(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфона т; 2-[[2-[біс(2-йодетил)аміно]-3,5динітробензоїл]аміно]етилдигідрофосфат; 2-[(2-йодетил)-2,4-динітро-6-({[2(фосфонооксі)етил]аміно}карбоніл)аніліно]етилметансульфона т; 2-[(2-хлоретил)-2,4-динітро-3-[[[3(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфо нат; 3-({3-[біс(2-брометил)аміно]-2,6динітробензоїл}аміно)пропілдигідрофосфат; 2-[(2-брометил)-2,4-динітро-3-[[[2(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфона т; 2-[(2-брометил)-2,4-динітро-3-[[[3(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфо нат і 2-[(2-йодетил)-2,4-динітро-3-[[[3(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфо нат. Y , де: X представляє в будь-якому доступному положенні кільця -CONH; R представляє нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди; Y представляє -N-азиридиніл або -N(CH2CH2W)2, де кожний W незалежно вибраний з галогену або OSO2Me; Z представляє в будь-якому доступному положенні кільця -NO2, галоген, -CN, -CF3 або -SO2Me; і його фармацевтично прийнятних солей і похідних; при якому здійснюють таку стадію (і) фосфорилування сполуки формули (II) NO2 Z X R OH (II) Y , де: X представляє в будь-якому доступному положенні кільця -CONH; Y представляє в будь-якому доступному положенні кільця -N-азиридиніл, -N(CH2CH2W)2 або N(CH2СНMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me; Z представляє в будь-якому доступному положенні кільця -NO2, галоген, -CN, -CF3 або -SO2Me; і R представляє нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди. 5. Спосіб одержання сполуки формул (Ia), (Ib) або (Іс) NO2 CONH(CH2)nOP(O)(OH)2 (Ia) Z Y , NO2 (Ib) O2N CONH(CH2 )nOP(O)(OH)2 Y , 5 89363 6 NO2 N N CONH(CH2)nOP(O)(OH)2 W (Ic) NO2 Y , де Y може представляти N N W W або , і де n дорівнює 1-6; Z представляє -NO2, галоген, -CN, -CF3 або SО2Me; і де кожний W незалежно вибраний з галогену або OSO2Me; і її фармацевтично прийнятних солей і похідних, при якому здійснюють стадію фосфорилування сполуки, представленої формулами (ІІа), (ІІb) або (ІІс) NO2 CONH(CH2)nOH (ІIa) Z Y , NO2 (ІIb) O2N CONH(CH2)nOH Y , NO2 CONH(CH2)nOH (IІc) NO2 Y , W або , і де n дорівнює 1-6; Z представляє -NO2, галоген, -CN, -CF3 або SО2Me; і де W незалежно вибраний з галогену або OSO2Me; і її фармацевтично прийнятних солей і похідних. 6. Спосіб протиракового лікування, при якому здійснюють стадію введення суб'єкту ефективної кількості сполуки формули (І), як визначено в будьякому з пп. 1-3. 7. Спосіб знищення гіпоксичних клітин пухлини, при якому здійснюють введення суб'єктові з пухлиною ефективної кількості сполуки формули (І), як визначено в будь-якому з пп. 1-3. 8. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки формули (І), як визначено за будь-яким з пп. 1-3, і фармацевтично прийнятний ексципієнт, ад'ювант, носій, буфер або стабілізатор. 9. Сполука, вибрана з: 2-[(2-брометил)-2,4-динітро-6-[[[2(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфона ту; 2-[(2-брометил)-2,4-динітро-3-[[[2(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфона ту; 2-[(2-брометил)-2,4-динітро-3-[[[3(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфо нату й 2-[(2-йодетил)-2,4-динітро-3-[[[3(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфо нату. 10.Сполука 2-[(2-брометил)-2,4-динітро-6-[[[2(фосфонооксі)етил]аміно]карбоніл]аніліно]етилметансульфона т. 11. Фармацевтична композиція, що містить терапевтично ефективну кількість сполуки за п. 10 і фармацевтично прийнятний ексципієнт, ад'ювант, носій, буфер або стабілізатор. 12. Застосування ефективної кількості сполуки формули (І) за п. 10 при виготовленні лікарського засобу для лікування раку в суб'єкта. де Y представляє Даний винахід відноситься до нових нітрофеніліпритних і нітрофенілазиридинових спиртів, до їх відповідних фосфатів, до їх застосування як націлених цитотоксичних засобів; як біовідновлювальних препаратів при гіпоксичних пухлинах і до їх застосування при деструкції клітин, включаючи направлену на гени ферментно-пролікарську те рапію (GDEPT) і направлену на антитіла ферментно-пролікарську терапію (ADEPT) в поєднанні з нітроредуктазними ферментами. Застосування селективних до пухлин проліків (відносно неактивних сполук, які можуть бути селективно перетворені в більш активні сполуки in vivo), являє собою цінну концепцію при терапії 7 89363 8 раку (див., наприклад, Denny, Eur. J. Med. Chem. 4-нітроароматичні сполуки відновлюються (2001) 36, 577). флавопротеїдними ферментами як ссавців, так і Наприклад, проліки можуть бути перетворені в бактерій, які впливають на ступінчасте додавання протипухлинний засіб під впливом ферменту, який електронів в кількості до 6. Основний ферментний може з'єднуватись з моноклональним антитілом, метаболіт являє собою звичайно 4-електронний яке буде зв'язуватись з антигеном, асоційованим з відновлений вид (гідроксиламін). пухлиною. Комбінація таких проліків з таким ферПовідомлялось про ряд нітрофеніліпритів і німентом і кон'югатом моноклонального антитіла трофенілазиридинів як проліків для застосування являє собою дуже активний клінічний засіб. Цей при направленій на гени ферментно-пролікарській підхід до терапії раку, що часто іменується як «натерапії (GDEPT) в поєднанні з ферментами нітроправлена на антитіла ферментно-пролікарська редуктази. Зокрема, повідомляється, що СВ 1954 терапія» (ADEPT), розкритий у WO88/07378. [5-(азиридин-1-іл)-2,4-динітробензамід] (1) [покаЩе один терапевтичний підхід, названий «назано нижче] являє собою субстрат для аеробної правлена на вірус ферментно-пролікарська теранітроредуктази NTR (продукт гена nfsB), виділений пія» (VDEPT), був запропонований як спосіб оброз Е.coli В (Boland et al., Biochem. Pharmacol. 1991, бки пухлинних клітин у пацієнтів, використовуючи 41, 867-875; Anlezark et al., Biochem. Pharmacol, проліки. Пухлинні клітини націлюються вірусним 1992, 44, 2289-2295; Parkinson et al., J. Med. Chem. вектором, який несе ген, що кодує фермент, здат2000, 43, 3624). Ця сполука застосовувалась як ний активувати проліки. Ген може бути транскриппроліки, що застосовуються як при ADEPT (Knox et ційно регульованим тканеспецифічними промотоal., Biochem. Pharmacol, 1995, 49, 1641-1647), так і рними або підсилювальними послідовностями. при GDEPT (Bridgewater et al., Eur. J. Cancer, 1995, Вірусний вектор входить в пухлинні клітини та екс31A, 2362-2370; Bailey et al., Gene Ther, 1996, 3, пресує фермент, щоб проліки перетворились в 1143-1150; Bailey and Hart, Gene Ther, 1997, 4,80активний препарат всередині пухлинних клітин 81; Green et al., Cancer Gene Ther, 1997, 4, 229(Huber et al., Proc. Natl. Acad. Sci. USA (1991) 88, 238), включаючи клінічне випробування (Chung8039). Альтернативно, використовувались невіруFaye et al., Clin. Cancer Res, 2001, 7, 2662-2668). сні способи доставки генів. Такі способи включаАналогічним чином, динітрофеніліприт SN ють спільне осадження фосфату кальцію, мікро23862 (2) являє собою також субстрат для NTR і ін'єкцію, ліпосоми, пряме захоплення ДНК і виявляє селективну токсичність відносно ліній кліопосередковане рецепторами перенесення ДНК. їх тин, які експерсують фермент. Він активується огляд представлений у публікації Morgan & French, відновленням нітрогрупи (Palmer et al., J. Med. Annu. Rev. Biochem., 1993, 62; 191. Термін Chem, 1995, 38, 1229; Kestell et al., Cancer «GDEPT» (направлена на гени ферментноChemother. Pharmacol, 2000, 46, 365-374). Похідне пролікарська терапія) використовується для вклю4-SO2Me (3) також являло собою субстрат (Atwell чення як вірусних, так і невірусних систем доставet al., Anti-Cancer Drug Des, 1996, 11, 553), як і реки (Denny et al., US 6310237). гіоізомери (4) і (5) (Friedlos et al., J. Med. Chem, 1997,40, 1270). Однак сполуки цього типу не були дуже ефективними як біовідновлювальні проліки, коли ці сполуки активувались в гіпоксичній пухлинній тканині ферментами ендогенної редуктази, що виявляють співвідношення активності 2-5 в гіпоксичних умовах відносно гіпоксичних умов в лінії клітин дикого типу АА8, використовуючи клоногенний аналіз (Palmer et al., J. Med. Chem. 1996, 39, 25182528). Були описані деякі фосфатні аналоги іприту, призначені для солюбілізації сполук. Найбільш відомим є естрамустинфосфат (естрацит; 6), який, як було показано, зв'язується з доменами, зв'язуючими тубулін, на різних білках, пов'язаних з мікротрубочками (Moraga et al., Biochem. Biophys. Acta, 1992, 1121, 97-103), і які, як було показано, активні при запущеному раку молочної залози (Keren-Rosenberg et al., Semin. Oncol., 1997, 24 (Suppl. 3), 26-29), але, як було показано, активується NTR або гіпоксією. Інше дослідження також показало, що естрамустинфосфат є сенсибілізатором до опромінення (Kim et al., Int. J. Radiat. Oncol. Biol. Phys., 1994, 29, 555-557). Аналог феноліпритфосфату 7 являє собою субстрат карбоксипептидази, яка не активується в гіпоксичних умовах (Matsui et al., патент Японії 07082280 А2, 1995), і солюбілізований іприт 8 був описаний як інгібітор фосфатази, але не було показано, що він активується в гіпоксичних умовах (Workman, Chem.-Biol. Interact., 1978, 20, 103-112). 9 Метою даного винаходу є надання специфічного класу нітрофеніліпритів і азиридинів, які несуть коротколанцюгові спирти і їх відповідних фосфатів для застосування як націлюваних цитотоксичних засобів або біовідновлювальних проліків, або, щонайменше, надання громадськості корисної альтернативи. У першому аспекті даний винахід надає нові фосфатні сполуки формули І де: де Υ може являти собою і де n дорівнює 1-6 Ζ являє собою -ΝΟ2, галоген, -CN, -CF3 або SO2Me; і де кожний W незалежно вибраний з галогену або -OSO2Me; і її фармацевтично прийнятних солей і похідних. 89363 10 X являє собою в будь-якому доступному положенні кільця -CONH-, -SO2NH-, -О-, -СН2-, NHCO - або -NHSO2-; R являє собою нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди; Υ являє собою в будь-якому доступному положенні кільця -N-азиридиніл, -N(CH2CH2W)2 або N(CH2CHMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me; Ζ являє собою в будь-якому доступному положенні кільця -ΝΟ2, галоген, -CN, -CF3 або -SO2Me; і їх фармацевтично прийнятні солі і похідні. У переважному варіанті здійснення фосфатна сполука формули (І) вибрана зі сполуки, представленої формулами (la), (Ib) або (Іс) Переважно, фосфатна сполука формули (І) вибрана з групи, що включає: 2-[[2-[біс(2-брометил)аміно]-3,5динітробензоїл]аміно]етилдигідрофосфат; 3-[[5-[біс(2-хлоретил)аміно]-2,4динітробензоїл]аміно]пропілдигідрофосфат; 3-[[5-[біс(2-брометил)аміно]-2,4динітробензоїл]аміно]пропілдигідрофосфат; 2-[[2-[біс(2-хлоретил)аміно]-3,5динітробензоїл]аміно]етилдигідрофосфат; 11 2-[(2-хлоретил)-2,4-динітро-6-[[[2-(2фосфоноокси)етил]аміно]карбоніл]аніліно]етилметансульфонат; 2-({2-[біс(2-бромпропіл)аміно]-3,5динітробензоїл}аміно)етилдигідрофосфат; 2-[(2-брометил)-2,4-динітро-6-[[[2(фосфоноокси)етил]аміно]карбоніл]аніліно]етилметансульфонат; 2-[[2-[біс(2-йодетил)аміно]-3,5динітробензоїл]аміно]етилдигідрофосфат; 2-[(2-йодетил)-2,4-динітро-6-({[2(фосфоноокси)етил]аміно]карбоніл)аніліно]етилметансульфонат; 2-[(2-хлоретил)-2,4-динітро-3-[[[3(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфонат; 3-({3-[біс(2-брометил)аміно]-2,6динітробензоїл}аміно)пропілдигідрофосфат; 2-[(2-брометил)-2,4-динітро-3-[[[2(фосфоноокси)етил]аміно]карбоніл]аніліно]етилметансульфонат; 2-[(2-брометил)-2,4-динітро-3-[[[3(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфонат і 2-[(2-йодетил)-2,4-динітро-3-[[[3(фосфоноокси)пропіл]аміно]карбоніл]аніліно]етилметансульфонат. 89363 12 У другому аспекті даний винахід надає спиртові сполуки формули (II) де: X являє собою в будь-якому доступному положенні кільця -CONH-, -SO2NH-, -О-, -СН2-, NHCO - або -NHSO2-; Υ являє собою в будь-якому доступному положенні кільця -N-азиридиніл, -N(CH2CH2W)2 або N(CH2CHMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me; Ζ являє собою в будь-якому доступному положенні кільця -ΝΟ2, галоген, -CN, -CF3 або -SO2Me; R являє собою нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди; і їх фармацевтично прийнятні солі і похідні, за умови, що, коли Ζ являє собою ΝΟ2, і Υ являє собою -N(CH2CH2Cl)2, X і R разом не можуть являти собою -CONHCH2(CHOH)CH2-, і, крім того, за умови, що наступні сполуки 13 виключаються. У переважному варіанті здійснення сполука, яка містить спиртову групу, формули (II), вибрана де Υ може являти собою і де n дорівнює 1-6 89363 14 зі сполуки, представленої формулами (IIа), (IIb або (IIс) Ζ являє собою -ΝΟ2, галоген, -CN, -CF3 або SO2Me; і де кожний W незалежно вибраний з галогену або -OSO2Me; і їх фармацевтично прийнятні солі і похідні, за умови, що коли Ζ являє собою -ΝΟ2, і Υ являє собою -N(CH2CH2CI)2, X і R разом не можуть являти собою -CONHCH2(CHOH)CH2-, і, крім того, за умови, що наступні сполуки 15 виключаються. Переважно, сполука формули (II) вибрана із групи, що включає: N-(2-гідроксіетил)-5-[біс(2-брометил)аміно]2,4-динітробензамід; N-(4-гідроксибутил)-5-[біс(2-брометил)аміно]2,4-динітробензамід; N-(5-гідроксипентил)-5-[біс(2брометил)аміно]-2,4-динітробензамід; N-(6-гідроксигексил)-5-[біс(2-брометил)аміно]2,4-динітробензамід; 5-[біс(2-брометил)аміно]-N-(2-гідроксіетил)-4(метилсульфоніл)-2-нітробензамід; 2-[(2-брометил)-5-[[(3гідроксипропіл)аміно]карбоніл]-2,4динітроаніліно]етилметансульфонат; 5-[біс(2-йодетил)аміно]-N-(2-гідроксіетил)-2,4динітробензамід; 2-[біс(2-хлоретил)аміно]-N-(2-гідроксіетил)3,5-динітробензамід; 2-[біс(2-брометил)аміно]-N-(2-гідроксіетил)3,5-динітробензамід; 2-[біс(2-хлоретил)аміно]-N-(3-гідроксипропіл)3,5-динітробензамід; 2-[біс(2-брометил)аміно]-N-(3-гідроксипропіл)3,5-динітробензамід; 2-[біс(2-хлоретил)аміно]-N-(4-гідроксибутил)3,5-динітробензамід; 2-[біс(2-брометил)аміно]-N-(4-гідроксибутил)3,5-динітробензамід; 2-[біс(2-хлоретил)аміно]-N-(5гідроксипентил)-3,5-динітробензамід; 2-[біс(2-брометил)аміно]-N-(5гідроксипентил)-3,5-динітробензамід; 2-[біс(2-хлоретил)аміно]-N-(6-гідроксигексил)3,5-динітробензамід; 2-[біс(2-брометил)аміно]-N-(6-гідроксигексил)3,5-динітробензамід; 2-[біс(2-бромпропіл)аміно]-N-(2-гідроксіетил)3,5-динітробензамід; 2-((2-брометил)-2-{[(2гідроксипропіл)аміно]карбоніл}-4,6динітроаніліно)етилметансульфонат; 2-((2-брометил)-2-{[(2гідроксипропіл)аміно]карбоніл}-4,6динітроаніліно)етилметансульфонат; 2-((2-хлоретил)-2-{[(2гідроксіетил)аміно]карбоніл}-4,6динітроаніліно)етилметансульфонат; 2-[біс(2-йодетил)аміно]-N-(2-гідроксіетил)-3,5динітробензамід; 2-((2-йодетил)-2-{[(2гідроксиетил)аміно]карбоніл}-4,6динітроаніліно)етилметансульфонат; 2-[біс(2-брометил)аміно]-N-(2-гідроксіетил)2,6-динітробензамід; 2-((2-брометил)-3-{[(2гідроксіетил)аміно]карбоніл}-2,4динітроаніліно)етилметансульфонат; 3-[біс(2-брометил)аміно]-N-(3-гідроксипропіл)2,6-динітробензамід; 2-((2-брометил)-3-{[(3гідроксипропіл)аміно]карбоніл}-2,4динітроаніліно)етилметансульфонат; 89363 16 3-[біс(2-брометил)аміно]-N-(4-гідроксибутил)2,6-динітробензамід; 2-((2-брометил)-3-{[(4гідроксибутил)аміно]карбоніл}-2,4динітроаніліно)-етилметансульфонат; 2-((2-хлоретил)-3-{[(3гідроксипропіл)аміно]карбоніл}-2,4динітроаніліно)-етилметансульфонат і 2-((2-йодетил)-3-{[(3гідроксипропіл)аміно]карбоніл}-2,4динітроаніліно)-етилметансульфонат. У третьому аспекті винаходу надається спосіб одержання фосфатів, представлених загальною формулою (І) де: X являє собою в будь-якому доступному положенні кільця -CONH-, -SO2NH-, -О-, -СН2-, NHCO - або -NHSO2-; R являє собою нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди; Υ являє собою в будь-якому доступному положенні кільця -N-азиридиніл, або -N(CH2CH2W)2, де кожний W незалежно вибраний з галогену або -OSO2Me; Ζ являє собою в будь-якому доступному положенні кільця -ΝΟ2, галоген, -CN, -CF3 або SO2Me; і їх фармацевтично прийнятних солей і похідних; який включає стадії (і) фосфорилування сполуки формули (II) де: X являє собою в будь-якому доступному положенні кільця -CONH-, -SO2NH-, -О-, -СН2-, NHCO - або -NHSO2-; Υ являє собою в будь-якому доступному положенні кільця -N-азиридиніл, -N(CH2CH2W)2 або -N(CH2CHMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me; Ζ являє собою в будь-якому доступному положенні кільця -ΝΟ2, галоген, -CN, -CF3 або SO2Me; і R являє собою нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди. У четвертому аспекті надається спосіб одержання сполук формул (IIa), (IIb) або (IIc) 17 де Υ може являти собою і де n дорівнює 1-6 де Υ може являти собою де кожний W'1 і W'2 являє собою галоген; з ефективною кількістю метансульфонату срібла (AgOMs) в розчиннику з одержанням вказаної вище сполуки формул (IIa), (IIb) або (IIc). 89363 18 Ζ являє собою -ΝΟ2, галоген, -CN, -CF3 або SO2Me; і де W 1 являє собою галоген, і W2 являє собою -OSO2Me; і їх фармацевтично прийнятних солей і похідних; який включає стадію взаємодії сполуки формул (IIа'), (IIb') або (IIc'), необов'язково при нагріванні Потрібно розуміти, що в способі, визначеному безпосередньо вище, де W'1 і W'2 являють собою або йод, і/або бром, вказаний йод і/або бром може бути частково або повністю заміщений OSO2Me. У ситуації, де кожний або обидва з W'1 і W'2 являють собою хлор, вказаний хлор є інертним і не може бути заміщений OSO2Me. Переважно, розчинник вибирають з MeCN або іншого полярного апротонного розчинника. У п'ятому аспекті надається спосіб одержання сполуки формул (la), (Ib) або (Іс) 19 де Υ може являти собою і де n дорівнює 1-6 де Υ являє собою і де n дорівнює 1-6 Ζ являє собою -ΝΟ2, галоген, -CN, -CF3 або SO2Me; і де W незалежно вибраний з галогену або OSO2Me; і її фармацевтично прийнятних солей і похідних. У шостому аспекті надається сполука формули (І), формули (la), (Ib) або (Іс) або формули (IIa), (IIb) або (IIc), одержана будь-яким з визначених вище способів одержання. 89363 20 Ζ являє собою -ΝΟ2, галоген, -CN, -CF3 або SO2Me; і де кожний W незалежно вибраний з галогену або -OSO2Me; і її фармацевтично прийнятних солей і похідних, який включає стадію фосфорилування сполуки, представленої формулами (IIа), (IIb) або (IIc) У сьомому аспекті даний винахід надає спосіб застосування як проліків, придатних для (і) GDEPT (направленої на гени ферментнопролікарської терапії) або ADEPT (направленої на антитіла ферментно-пролікарської терапії) в поєднанні, щонайменше, з одним нітроредуктазним ферментом; або (іі) застосування як одного або декількох селективних для гіпоксії цитотоксинів, який включає стадію введення сполуки формули (І), як визначено вище, або сполуки формули (II) де: 21 89363 22 X являє собою в будь-якому доступному поми у значних концентраціях зовні клітин. Передложенні кільця -CONH-, -SO2NH-, -О-, -СН2-, бачається, що синтетичний ко-фактор можна виNHCO - або -NHSO2-; користати для стимуляції активації проліків Υ являє собою в будь-якому доступному поаналогами внутрішньоклітинного ферменту. Аналоженні кільця -N-азиридиніл, -N(CH2CH2W)2 або логічна проблема не виникає при GDEPT, тому -N(CH2CHMeW)2, де кожний W незалежно вибращо у значних концентраціях є декілька внутрішний з галогену або -OSO2Me; ньоклітинних відновлювальних ко-факторів, таких Ζ являє собою в будь-якому доступному пояк аналоги NADH і NADPH. ложенні кільця -ΝΟ2, галоген, -CN, -CF3 або У дев'ятому аспекті даний винахід надає споSO2Me; сіб забезпечення протиракового лікування, де R являє собою нижчий С1-6алкіл, необов'язсполуку формули (І), як визначено вище, вводять ково заміщений однією або декількома групами, в ефективній кількості суб'єкту. включаючи гідрокси, аміно і їх N-оксиди або діалПереважно, кількість вказаної сполуки склакіламіно і їх N-оксиди; і їх фармацевтично прийндає приблизно від 20% до 100% від максимально ятних солей і похідних; переносимої дози для вказаного суб'єкта. або їх суміш в терапевтично ефективній кільПереважно, спосіб включає ще одну стадію кості для націлювання на пухлинні клітини у сувпливу на пухлинні клітини опроміненням або б'єкта. хіміотерапевтичними засобами. Переважно, нітроредуктазний фермент кодуУ десятому аспекті даного винаходу надаєтьється геном nfsB або Е.coli, або ортологічними ся спосіб деструкції клітин з використанням, щогенами у виду Clostridia. найменше, одного нітроредуктазного ферменту, Переважно, спосіб включає додаткову стадію який включає стадію введення сполуки формули опромінення пухлинних клітин. (І), як визначено вище, або сполуки формули (II) У восьмому аспекті даний винахід надає спосіб застосування як проліків, придатних для GDEPT (направленої на гени ферментнопролікарської терапії) або ADEPT (направленої на антитіла ферментно-пролікарської терапії) в поєднанні, щонайменше, з одним нітроредуктазним ферментом, як протираковим засобом, який включає стадію введення сполуки формули (І), як де: визначено вище, або сполуки формули (II) X являє собою в будь-якому доступному положенні кільця -CONH-, -SO2NH-, -О-, -СН2-, NHCO - або -NHSO2-; Υ являє собою в будь-якому доступному положенні кільця -N-азиридиніл, -N(CH2CH2W)2 або -N(CH2CHMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me; Ζ являє собою в будь-якому доступному положенні кільця -ΝΟ2, галоген, -CN, -CF3 або де: SO2Me; X являє собою в будь-якому доступному поR являє собою нижчий С1-6алкіл, необов'язложенні кільця -CONH-, -SO2NH-, -О-, -СН2-, ково заміщений однією або декількома групами, NHCO - або -NHSO2-; включаючи гідрокси, аміно і їх N-оксиди або діалΥ являє собою в будь-якому доступному покіламіно і їх N-оксиди; і їх фармацевтично прийнложенні кільця -N-азиридиніл, -N(CH2CH2W)2 або ятних солей і похідних; або їх суміш в кількості, -N(CH2CHMeW)2, де кожний W незалежно вибраефективній для руйнування клітин, де вказані ний з галогену або -OSO2Me; клітини експресують, щонайменше, один нітроΖ являє собою в будь-якому доступному поредуктазний фермент. ложенні кільця -ΝΟ2, галоген, -CN, -CF3 або Переважно, клітини, які є мішенню для деSO2Me; струкції, являють собою пухлинні клітини в тканиR являє собою нижчий С1-6алкіл, необов'язні у суб'єкта. ково заміщений однією або декількома групами, Переважно, спосіб деструкції клітин з викоривключаючи гідрокси, аміно і їх N-оксиди або діалстанням, щонайменше, одного нітроредуктазного кіламіно і їх N-оксиди; і їх фармацевтично прийнферменту забезпечується технологією ADEPT ятних солей і похідних; або GDEPT. або їх суміш в терапевтично ефективній кільВ одинадцятому аспекті даного винаходу накості для націлювання на пухлинні клітини у судається фармацевтична композиція, яка включає б'єкта. терапевтично ефективну кількість сполуки форПереважно, нітроредуктазний фермент кодумули (І) або сполуки формули (II) ється геном nfsB або Е.coli, або онтологічними генами у виду Clostridia. Переважно, спосіб включає додаткову стадію опромінення пухлинних клітин. Потрібно розуміти, що при ADEPT може бути необхідною подача відновлювального кофактора, оскільки вони можуть не бути присутні 23 де: X являє собою в будь-якому доступному положенні кільця -CONH-, -SO2NH-, -О-, -СН2-, NHCO - або -NHSO2-; Υ являє собою в будь-якому доступному положенні кільця -N-азиридиніл, -N(CH2CH2W)2 або -N(CH2CHMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me; Ζ являє собою в будь-якому доступному положенні кільця -ΝΟ2, галоген, -CN, -CF3 або SO2Me; R являє собою нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди; і їх фармацевтично прийнятних солей і похідних, або їх суміші і фармацевтично прийнятний ексципієнт, ад'ювант, носій, буфер або стабілізатор. Фармацевтично прийнятний ексципієнт, ад'ювант, носій, буфер або стабілізатор повинен бути переважно нетоксичним і не повинен заважати ефективності активності інгредієнта. Точна природа носія або іншої речовини буде залежати від шляху введення, який може бути пероральним або шляхом ін'єкції, такої як шкірна, підшкірна або внутрішньовенна. Потрібно розуміти, що ці фактори можуть бути легко визначені фахівцем в даній галузі без непотрібного експериментування. Фармацевтичні композиції для перорального введення можуть бути у формі таблетки, капсули, порошку або рідин. Таблетка може включати твердий носій або ад'ювант. Рідкі фармацевтичні композиції загалом включають рідкий носій, такий як воду, вазелінове масло, тваринні масла або рослинні олії, мінеральне масло або синтетичне масло. Можуть бути включені фізіологічний сольовий розчин, декстроза або інший розчин сахариду або гліколі, такі як етиленгліколь, пропіленгліколь або поліетиленгліколь. Капсула може включати твердий носій, такий як желатин. Для внутрішньовенної, шкірної або підшкірної ін'єкції активний інгредієнт повинен бути у формі парентерально прийнятного водного розчину, який вільний від пірогенів і має відповідні рН, ізотонічність і стійкість. Фахівці в даній галузі цілком здатні одержати відповідні розчини, використовуючи, наприклад, ізотонічні носії, такі як розчин хлориду натрію для ін'єкцій, розчин Рінгера для ін'єкцій, молочнокислий розчин Рінгера для ін'єкцій. За необхідності можуть бути включені консерванти, стабілізатори, буфери, антиоксиданти і/або інші домішки. У дванадцятому аспекті даного винаходу надається застосування при виготовленні лікарського засобу ефективної кількості сполуки формули (І), як визначено вище, або сполуки формули (II) де: 89363 24 X являє собою в будь-якому доступному положенні кільця -CONH-, -SO2NH-, -О-, -СН2-, NHCO - або - NHSO2-; Υ являє собою в будь-якому доступному положенні кільця -N-азиридиніл, -N(CH2CH2W)2 або -N(CH2CHMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me; Ζ являє собою в будь-якому доступному положенні кільця -ΝΟ2, галоген, -CN, -CF3 або SO2Me; R являє собою нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди; і їх фармацевтично прийнятних солей і похідних, або їх суміші для застосування при (і) GDEPT або (іі) ADEPT як селективного для гіпоксії цитотоксину для націлювання на ракові клітини у потребуючого цього суб'єкта. У тринадцятому аспекті даного винаходу надається застосування при виготовленні лікарського засобу ефективної кількості сполуки формули (І), як визначено вище, або сполуки формули (II) де: X являє собою в будь-якому доступному положенні кільця -CONH-, -SO2NH-, -О-, -СН2-, NHCO - або -NHSO2-; Υ являє собою в будь-якому доступному положенні кільця -N-азиридиніл, -N(CH2CH2W)2 або -N(CH2CHMeW)2, де кожний W незалежно вибраний з галогену або -OSO2Me; Ζ являє собою в будь-якому доступному положенні кільця -ΝΟ2, галоген, -CN, -CF3 або SO2Me; R являє собою нижчий С1-6алкіл, необов'язково заміщений однією або декількома групами, включаючи гідрокси, аміно і їх N-оксиди або діалкіламіно і їх N-оксиди; і їх фармацевтично прийнятних солей і похідних, або їх суміші для застосування при терапії для деструкції клітин для націлювання на ракові клітини у потребуючого цього суб'єкта. Хоча сполуки даного винаходу звичайно використовуються для націлювання на пухлинні клітини або пухлинні тканини у людей, їх можна застосовувати для націлювання на пухлинні клітини або тканини у інших суб'єктів теплокровних тварин, таких як інші примати, сільськогосподарські тваринні, такі як велика рогата худоба, спортивні тварини і домашні тваринні, такі як коні, собаки і кішки. Термін «терапевтично ефективна кількість», що використовується у всьому описі, потрібно розуміти як кількість сполуки формули (І) або формули (II), як визначено вище, або будь-якої зі сполук Іа-Іс або IIа-ІІс, як визначено вище, або їх суміші, яка достатня для вияву сприятливого ефекту на суб'єкта з раковими клітинами. Дійсна 25 89363 26 кількість, частота і динаміка введення буде залеструкції певних клітин або тканин-мішеней жати від природи і тяжкості захворювання, що (Gusterson et al., Endocrine Related Cancer, 1997, піддається лікуванню. Призначення лікування 4, 67-74). знаходиться в сфері відповідальності лікарів заВираз «по суті мінімальний побічний ефект» гальної практики та інших лікарів. потрібно розуміти як такий, що означає, що зниТермін «галоген», що використовується у щення примикаючих клітин, які не є мішенню, є всьому описі, включає хлор, бром або йод. мінімальним, через наявність невеликої або відПотрібно розуміти, що сполуки винаходу, висутність дифузії між клітинами, що є і що не є значені вище, можна вводити окремо або в коммішенню активованого метаболіту, який виникає бінації з іншими видами лікування, зокрема, провнаслідок ферментативної активації сполуки фоменевою терапією і цитотоксичними рмули (І) або формули (II), визначеної вище, або хіміотерапевтичними препаратами, або одночасбудь-якої зі сполук Іа-Іс або IIa-IIс, визначених но, або послідовно, в залежності від підлягаючого вище, або їх суміші. лікуванню стану. Фармацевтично прийнятні солі формули (І) Термін «їх фармацевтично прийнятні похідні і включають основні або кислотні сполуки формусолі», що використовується у всьому описі, вклюли (І), які утворюють фармацевтично прийнятні чають солі, похідні кислот, утворені з хлористосолі і з органічними, і з неорганічними кислотами водневої, сірчаної, фосфорної, оцтової, лимоні/або органічними і неорганічними основами. Приної, щавлевої, малонової, саліцилової, яблучної, кладами відповідних кислот для утворення солей фумарової, янтарної, аскорбінової, малеїнової, є хлористоводнева, сірчана, фосфорна, оцтова, метансульфонової, ізетіонової кислот і ним поділимонна, щавлева, малонова, саліцилова, яблубних, і солі, похідні основ, утворені з карбонату чна, фумарова, янтарна, аскорбінова, малеїнова, натрію і калію, гідроксиду натрію і калію, аміаку, метансульфонова, ізетіонова кислоти і ним подітриетиламіну, триетаноламіну і ним подібних. бні. Прикладами відповідних основ для утворенТермін «деструкція клітин», що використовуня солі є карбонат натрію і калію, гідроксид нається у всьому описі, потрібно розуміти як знитрію і калію, аміак, триетиламін, триетаноламін і щення клітин, які були піддані генній інженерії ним подібні. для експресії ферменту, такого як нітроредуктаПодальші аспекти даного винаходу стануть за, введенням проліків, які активовані цим ферочевидними з наступного опису, представленого ментом. В результаті, деструкцію клітин можна тільки у вигляді прикладу і з посиланням на сувикористати для селективної деструкції певних проводжуючі схеми синтезу. клітин або тканин-мішеней за допомогою, наприПриклади сполук формули (І), де X являє соклад, специфічної ферментативної експресії нітбою -CONH-, можна одержати способами, привероредуктази, яка специфічно експресована ткаденими на схемі 1, де Ζ є таким, як визначено ниною, і яку потім можна використати для вище для формули (І). активації проліків в активний метаболіт для де У наступних таблицях 1a і 2а представлені фізичні дані для сполук загальної формули (І) і (II), що представляють їх і здатних бути одержаними способами винаходу. 27 89363 28 де Υ може являти собою Примітки Посилання на відомі сполуки. 1. Khan AH, Ross WC J. Tumor-growth inhibitory nitrophenylaziridines and related compounds. Structure-activity relations. II. Chem.-Biol. Int., 1971, 4, 11-22. 2. NZ Patent No.240785. 3. Co-pending NZ Application No. 521851. 29 89363 30 4. Wilson WR, Pullen SM, Hogg A, Helsby NA, Hicks КО, Denny WA. Quantitation of bystander effects in nitroreductase suicide gene therapy using three-dimensional cell. Cancer Res., 2002, 62, 1425-1432. Сполуки таблиці la можна одержати загальними способами, представленими на схемах 2а-2k і проілюстрованими нижче в прикладах 1-20. де Υ може являти собою Сполуки таблиці lb можна одержати загальними способами, представленими на схемі 3, і проілюстрованими нижче в прикладах 26-39. 31 89363 32 33 89363 34 35 89363 36 37 На схемі 3X, Υ, Ζ і R є такими, як визначено вище для формули (І) і (II). Приклади Винахід і кращий спосіб його здійснення проілюстровані наступними прикладами 1-25 (спирти) і прикладами 26-39 (фосфати). Приклад 1 (схема 2а). N(3-гідроксипропіл)-5[біс(2-хлоретил)аміно]-2,4-динітробензамід (IIa-3) Суспензію 5-[біс(2-хлоретил)аміно]-2,4динітробензойної кислоти [Palmer et al., J. Med. Chem., 1994, 37, 2175] (1) (2,50r, 7,1ммоль) в SOCl2 (20мл), що містить ДМФА (2 краплі) нагрівають при кип'ятінні зі зворотним холодильником протягом 1год., потім концентрують досуха при зниженому тиску і повторно випаровують з бензолом. Одержаний неочищений бензоїлхлорид розчиняють в Ме2СО (50мл) і охолоджений (-5°С) розчин обробляють холодним розчином 3-аміно1-пропанолу (1,09г, 14,5ммоль) у воді (25мл). Реакційну суміш струшують при кімнатній температурі протягом 5хв., потім розбавляють водою (25мл), концентрують до половини об'єму і екстрагують СН2СІ2 (2х). Органічний екстракт промивають 0,1н. НCl і водою, потім піддають подальшій обробці з одержанням твердої речовини, якому хроматографують на силікагелі, елююючи EtOAc, з одержанням сполуки IIa-3 (2,37г, 82%): т.пл. (EtOAc/і-Рr2О) 90-91°С; 1H ЯМР [(CD3)2SO] d 8,63 (т, J=5,6Гц, 1Н, CONH), 8,53 (с, 1Н, Н-3), 7,42 (с, 1Н, H-6), 4,46 (т, J=5,1Гц, 1Н, OH), 3,82 (т, J=5,9Гц, 4Н, N(CH2CH2Cl)2), 3,68 (т, J=5,9Гц, 4Н, N(CH2CH2Cl)2), 3,49 (кв, J=6,0Гц, 2Н, CH2OH), 3,29 (кв, частково невидимий, J=5,9Гц, 2Н, CONHCH2), 1,68 (пент, J=6,7Гц, 2Н, СН2Сl/2СН2). Аналіз (C14H18Cl2N4O6) С, Η, Ν, СІ. Приклад 2 (схема 2а). N-(3-гідроксипропіл)-5[біс(2-брометил)аміно]-2,4-динітробензамід (IIa-8) Суспензію порошкоподібної 5-[біс(2брометил)аміно]-2,4-динітробензойної кислоти (2) (1,10г, 2,49ммоль) в бензолі (170мл) обробляють при 20°С оксалілбромідом (1,10мл, 11,7ммоль) і ДМФА (2 краплі). Суміш перемішують при 20°С протягом 2год., потім концентрують при зниженому тиску і повторно випаровують досуха у присутності бензолу у високому вакуумі. Одержаний бромангідрид кислоти розчиняють в Ме2СО (20мл) і розчин обробляють при -5°С холодним розчином 3-аміно-1-пропанолу (0,39г, 5,19ммоль) у воді (10мл). Суміш струшують при кімнатній температурі протягом 5хв., потім розбавляють водою і екстрагують EtOAc (2х). Органічний екстракт піддають подальшій обробці і одержаний залишок хроматографують на силікагелі, елююю 89363 38 чи EtOAc, з одержанням сполуки IIа-8 (1,06г, 85%): т.пл. (EtOAc/і-Pr2О) 85-86°С; 1H ЯМР [(CD3)2SO] d 8,64 (т, J=5, Гц, 1H, CONH), 8,53 (с, 1H, H-3), 7,41 (с, 1Н, H-6), 3,77-3,64 (м, 8Н, N(CH2CH2Cl)2), 4,46 (уш.с, 1Н, OH), 3,49 (т, J=6,3Гц, 2Н, CH2OH), 3,33-3,25 (м, частково невидимий, 2H, CONHCH2), 1,68 (пент, J=6,72Гц, 2Н, СН2СН2СН2). Аналіз (C14H18Br2N4O6) С, Η, Ν, Br. Приклад 3 (схема 2а). N-(2-гідроксіетил)-5[біс(2-брометил)аміно]-2,4-динітробензамід (IIа-7) Аналогічна реакція бромангідриду кислоти прикладу 2 з 2-аміноетанолом дає сполуку IIa-7 (0,78г, 46%): т.пл. (МеОН/EtOAc/петролейний ефір) 151-152°С; 1H ЯМР [(CD3)2SO] d 8,73 (т, J=5,7Гц, 1Н, CONH), 8,53 (с, 1Н, Н-3), 7,43 (с, 1Н, Н-6), 4,76 (т, J=5,6Гц, 1Н, ОН), 3,77-3,64 (м, 8Н, N(CH2CH2Br)2), 3,53 (кв, J=6,6Гц, 2Н, СН2ОН), 3,31 (кв, частково невидимий, J=6,1Гц, 2Н, CONHCH2). Аналіз (C13H16Br2N4O6) C, H, N, Br. Приклад 4 (схема 2а). N-(4-гідроксибутил)-5[біс(2-брометил)аміно]-2,4-динітробензамід (IIa-9) Аналогічна реакція бромангідриду кислоти прикладу 2 з 4-аміно-1-бутанолом в холодному Ме2СО з подальшою хроматографією на силікагелі при елююванні EtOAc дає сполуку IIa-9 (69%) у вигляді жовтої твердої речовини: т.пл. (EtOAc/іPr2О) 123-124°С; 1H ЯМР [(CD3)2SO] d 8,62 (т, J=5,6Гц, 1Н), 8,53 (с, 1Н), 7,39 (с, 1H), 4,39 (т, J=5,1Гц, 1H), 3,78-3,64 (м, 8H), 3,47-3,40 (м, 2Н), 3,27-3,20 (м, 2Н), 1,61-1,44 (м, 4Н). Аналіз (C15H20Br2N4O6) С, Η, Ν, Br. Приклад 5 (схема 2а). N-(5-гідроксифеніл)-5[біс(2-брометил)аміно]-2,4-динітробензамід (IIа10) Аналогічна реакція бромангідриду кислоти прикладу 2 з 5-аміно-1-пентанолом в холодному Ме2СО з подальшою хроматографією на силікагелі при елююванні EtOAc дає сполуку IIa-10 (66%) у вигляді жовтої піни: 1H ЯМР [(CD3)2SO] d 8,62 (т, J=5,6Гц, 1Н), 8,53 (с, 1Н), 7,38 (с, 1Н), 4,34 (т, J=5,1Гц, 1Н), 3,79-3,64 (м, 8Н), 3,44-3,37 (м, 2Н), 3,26-3,18 (м, 2Н), 1,59-1,29 (м, 4Н). HRMS (FAB) Обчислено для C16H2379Br2N4O6 [M+H+] m/z 524,9984, знайдено 524,9964. Приклад 6 (схема 2а). N-(6-гідроксигексил)-5[біс(2-брометил)аміно]-2,4-динітробензамід (IIa11) Аналогічна реакція бромангідриду кислоти прикладу 2 з 6-аміно-1-гексанолом в холодному Ме2СО з подальшою хроматографією на силікагелі при елююванні EtOAc дає сполуку IIa-11 39 89363 40 Тонко подрібнену суспензію сполуки 7 (260мг, (72%) у вигляді жовтої піни: 1H ЯМР [(CD3)2SO] d 0,55ммоль) в сухому бензолі (50мл) обробляють 8,61 (т, J=5,6Гц, 1H), 8,53 (с, 1Н), 7,38 (с, 1Н), (СОBr)2 (2,13мл, 0,20ммоль) і каталітичним 4,31 (т, J=5,2Гц, 1Н), 3,79-3,64 (м, 8Н), 3,43-3,36 ДМФА. Суміш перемішують протягом 2год., потім (м, 2Н), 3,27-3,19 (м, 2Н), 1,58-1,26 (м, 4Н). HRMS концентрують досуха при зниженому тиску і по(FAB) Обчислено для C17H2579Br2N4O6 [M+H+] m/z вторно випаровують з бензолом у високому ваку539,0141, знайдено 539,0137. умі. Одержаний неочищений бромангідрид кисПриклад 7 (схема 2b). 5-[біс(2лоти розчиняють в Ме2СО (10мл) і обробляють брометил)аміно]-N-(2-гідроксіетил)-4при -5°С холодним розчином 2-аміноетанолу (метилсульфоніл)-2-нітробензамід (IIa-7s) (101мг, 1,65ммоль) у воді (5мл). Суміш перемі5-фтор-4-(метилсульфоніл)-2-нітробензойну шують при 0°С протягом 5хв., потім підкисляють кислоту [Atwell et al., ACDD, 1996, 11, 553] (3) надо рН 4 1н. водним НBr і концентрують при знигрівають в надлишку SOCl2/каталітичний ДМФА з женому тиску. Залишок хроматографують на сиодержанням хлорангідриду кислоти, який піддалікагелі, елююючи EtOAc, з одержанням сполуки ють взаємодії з сухим МеОН з одержанням 5IIa-7s (222мг, 78%): т.пл. (EtOAc/іPr2О) 126-127°С; фтор-4-(метилсульфоніл)-2-нітробензоату (4): 1 1 H ЯМР [(CD3)2SO] d 8,75 (т, J=5,6Гц, 1H), 8,51 (с, т.пл. (EtOAc/гексан) 134-135°С; H ЯМР 1Н), 7,68 (с, 1Н), 4,79 (т, J=5,4Гц, 1H), 3,76 (т, [(CD3)2SO] d 8,49 (д, J=5,9Гц, 1Н), 8,14 (д, J=7,1Гц, 4H), 3,62 (т, J=7,0 Гц, 4H), 3,54 (кв, J=9,3Гц, 1Н), 3,92 (с, 3Н), 3,46 (с, 3Н). Аналіз J=5,9Гц, 2Н), 3,48 (с, 3Н), 3,31 (після заміни D2O, (C9H8FNO6S) С, Η, Ν. т, J=6,0Гц, 2Н). HRMS (FAB) обчислено для Суміш сполуки 4 (1,48г, 5,34ммоль) і діетаноC14H2079Br2N3O6S (MH+) m/z 515,9440; знайдено ламіну (1,40г, 13,3ммоль) в DMA (6мл) перемі515,9425. шують при 30°С протягом 1год. і потім розбавляПриклад 8 (Схема 2с). 2[(2-брометил)-5-[[(3ють EtOAc (60мл). Розчин промивають гідроксипропіл)аміно]карбоніл]-2,4насиченим розчином солі (2х) і концентрують при динітроаніліно]етилметансульфонат (IIa-13) і 5зниженому тиску. Залишок очищають хроматог[біс(2-йодетил)аміно]-N-(2-гідроксіетил)-2,4рафією на силікагелі, елююючи EtOAc/MeOH з динітробензамід (IIa-14) подальшою перекристалізацією з EtOAc/iPr2O з 5-(біс{2-[(метилсульфоніл)окси]етил}аміно)одержанням метил-5-[біс(2-гідроксіетил)аміно]-42,4-динітробензойну кислоту [Спосіб одержання (метилсульфоніл)-2-нітробензоату (5) (1,41г, цієї сполуки розкритий в одночасно поданій заяв73%): т.пл. 99-100°С; 1H ЯМР [(CD3)2SO] d 8,56 (с, ці на патент Нової Зеландії №521851] (9) нагрі1Н), 7,73 (с, 1H), 4,62 (т, J=4,9Гц, 2Н), 3,89 (с, 3Н), вають при кип'ятінні зі зворотним холодильником 3,59-3,49 (м, 8Н), 3,45 (с, 3Н). Аналіз в надлишку SOCl2 (60мл) і каталітичному ДМФА (C13H18N2O8S) С, Η, Ν. протягом 1год. Випаровування при зниженому Розчин сполуки 5 (1,48г, 4,08ммоль) в сухому тиску з подальшою азеотропною перегонкою з піридині (15мл) обробляють краплями при 0°С бензолом дає неочищений хлорангідрид кислоти. MsCl (0,80мл, 10,3ммоль). Реакційну суміш переЙого розчиняють в сухому Ме2СО і обробляють мішують при 0°С протягом 2год., потім виливають при 0°С 3-аміно-1-пропанолом протягом 5хв. Суу 10% водний NaBr. Одержаний неочищений диміш підкисляють до рН 2-3 0,2н. НCl, концентрумесилат збирають, ретельно промивають водою, ють до половини об'єму і потім додають твердий сушать, розчиняють в ДМФА (15мл) і перемішуNaBr з подальшою екстракцією EtOAc (2х). Випають з NaBr (21,6г, 25ммоль) при 70°С протягом ровування і хроматографія залишку на силікагелі 1,5год. Охолоджену суміш виливають у воду і при елююванні EtOAc/MeOH (9:1) дає 2-(5-{[(3одержану тверду речовину очищають хроматоггідроксипропіл)аміно]карбоніл}{2рафією на силікагелі, елююючи СН2СІ2, потім [(метилсульфоніл)окси]етил}-2,4перекристалізовують з СН2СІ2/іPr2O з одержандинітроаніліно)етилметансульфонат (8) (68%) у ням метил-5-[біс(2-брометил)аміно]-4вигляді жовтої смоли; 1H ЯМР [(CD3)2SO] d 8,54 (метилсульфоніл)-2-нітробензоату (6) (1,47г, (т, J=5,7Гц, 1H), 8,53 (с, 1Н), 7,45 (с, 1Н), 4,43 (т, 74%): т.пл. 161-162°С; 1H ЯМР [(CD3)2SO] d 8,58 J=5,1Гц, 1Н), 4,33 (т, J=5,2Гц, 4Н), 3,69 (т, (с, 1Н), 7,94 (с, 1H), 3,90 (с, 3Н), 3,82 (т, J=7,0Гц, J=5,2Гц, 4Н), 3,57 (кв, J=5,9Гц, 2Н), 3,26 (після 4H), 3,63 (т, J=6,9Гц, 4Н), 3,48 (с, 3Н). Аналіз заміни D2O, т, J=7,0Гц, 2Н), 3,12 (с, 6Н), 1,66 (C13H16Br2O6S) С, Η, Ν. (пент, J=6,7Гц, 2Н). HRMS (FAB) Обчислено для Розчин сполуки 6 (1,00г, 2,05ммоль) в суміші C16H25N4O12S (MH+) m/z 529,0910; знайдено діоксан/МеОН (1:1, 20мл) обробляють при 10°С 529:0904. 4Ν водним КОН (5мл) і перемішують при 10°С Розчин сполуки 8 в ДМФА обробляють в LiBr протягом 45хв. Суміш підкисляють до рН 2 1н. (1,4 еквіваленти), піддають подальшій обробці, як водним НBr, концентрують до маленького об'єму указано вище, і продукт хроматографують на при зниженому тиску і потім розбавляють насисилікагелі. Елюювання EtOAc дає невелику кільченим водним NaBr (20мл). Одержану напівтверкість диброміприту, тоді як елюювання сумішшю ду речовину виділяють і кристалізують двічі з EtOAc/МеОН (19:1) дає сполуку IIa-13 (31%) у МеОН/Н2О з одержанням 5-[біс(2вигляді жовтої смоли: 1H ЯМР [(CD3)2SO] d 8,60 брометил)аміно]-4-(метилсульфоніл)-2(т, J=5,6Гц, 1Н), 8,54 (с, 1Н), 7,44 (с, 1Н), 4,45 (т, нітробензойної кислоти (7) (0,70г, 72%) т.пл. 174J=5,2Гц, 1Н), 4,33 (т, J=5,1Гц, 2H), 3,74 (т, 176°С; 1H ЯМР [(CD3)2SO] d 8,50 (с, 1Н), 7,88 (с, J=5,2Гц, 2H), 3,72-3,66 (м, 4Н), 3,49 (кв, J=5,9Гц, 1Н), 3,79 (т, J=7,0Гц, 4Н), 3,62 (т, J=7,0Гц, 4Н), 2Н), 3,27 (після заміни D2O, т, J=7,0Гц, 2Н), 3,14 3,48 (с, 3Н). Аналіз (C12HI4Br2N2O6S) C, H, N. (с, 3Н), 1,68 (пент, J=6,7Гц, 2H). HRMS (FAB) Об 41 89363 42 числено для C15H2279BrN4O9S (MH+) m/z 515,0270; дом N,N-біс(2-хлоретил)аміну (3,0г, 16,5ммоль) знайдено 515,0283. при 50°С протягом 24год. Суміш виливають у Аналогічна обробка хлорангідриду кислоти 9 воду і екстрагують EtOAc з одержанням неочи(активація (COCl2/ДМФА) з 2-аміноетанолом дає щеного продукту, який хроматографують на силі2-(5-{[(2-гідроксіетил)аміно]карбоніл}{2кагелі. Елюювання сумішшю EtOAc/петролейний [(метилсульфоніл)-окси]етил}-2,4ефір (4:1) і концентрування елюату при зниженодинітроаніліно)етилметансульфонат (10). Суміш му тиску дає маслянистий залишок, який розчисполуки, що перемішується, 10 (1,42г, 2,76ммоль) няють в мінімальній кількості EtOAc. Петролейі Nal (3,3г, 22ммоль) в сухому MeCN (45мл) нагріний ефір повільно додають до початку утворення вають при кип'ятінні зі зворотним холодильником каламутності і розчин залишають на ніч для осапротягом 1год., потім концентрують при знижедження 2-[біс(2-хлоретил)аміно]-N-(2ному тиску. Залишок розподіляють між EtOAc і гідроксіетил)-3,5-динітробензаміду (ІІb-2) (2,07г, водою і органічний шар промивають водою і ви100%) у вигляді жовтих кристалів: т.пл. паровують. Залишок хроматографують на силіка(EtOAc/петролейний ефір) 109-111°С; 1H ЯМР гелі, елююючи СН2СІ2/EtOAc (1:4), з подальшою [(CD3)2SO] d 8,73 (д, J=2,6Гц, 1Н, H-4), 8,72 (м, перекристалізацією з МеОН/EtOAc/і-Pr2О з одер1Н, CONH), 8,34 (д, J=2,6Гц, 1H, Н-6), 4,83 (м, 1Н, жанням сполуки IIa-14 (2,9г, 81%): т.пл. 142ОН), 3,72 (м, 4Н, 2(СН2Сl), 3,55 (м, 2Н), 3,42 (м, 143°С; 1H ЯМР [(CD3)2SO] d 8,73 (т, J=5,7Гц, 1Н), 4Н, 2(CH2N), 3,34 (м, 2Н); 13С ЯМР d 165,3, 145,8, 8,53 (с, 1Н), 7,38 (с, 1Н), 4,76 (т, J=5,5Гц, 1Н), 145,3, 141,0, 136,3, 127,5, 122,1, 59,1, 54,1, 42,1, 3,68 (т, J=6,9Гц, 4H), 3,57-3,49 (м, 2Н), 3,39 (т,. 41,5. HRMS (FAB) [MH+] Обчислено для J=6,9Гц, 4Н), 3,34-3,26 (м, частково невидимий, C13H1735Cl2N4O6 m/z 395,0525, Знайдено 395,0525. 2Н). Аналіз (C13H16I2N4O6) С, Η, Ν. Розчин сполуки ІІb-2 (1,20г, 3,0ммоль) і LiBr Приклад 9. 2-(азиридин-1-іл)-N-(6(5,0г, 58ммоль) в 3-метил-2-бутаноні (20мл) нагідроксигексил)-3,5-динітробензамід (IIa-1) грівають при кип'ятінні зі зворотним холодильниРозчин 2-хлор-N-(6-гідроксигексил)-3,5ком протягом 6год., потім охолоджують і виливадинітробензаміду (16) [одержання див. приклад ють у воду. Екстракція EtOAc дає неочищений 14 нижче] (118мг, 0,34ммоль) і Et3N (200мг) в продукт (чистота
ДивитисяДодаткова інформація
Назва патенту англійськоюNitrophenyl mustard and nitrophenylaziridine alcohols and their corresponding phosphates and their use as targeted cytotoxic agents
Автори англійськоюDenny William Alexander, Atwell Graham John, Yang Shangjin, Wilson William Robert, Patterson Adam Vorn, Helsby Nuala Ann
Назва патенту російськоюНитрофенилипритные и нитрофенилазиридиновые спирты и их соответствующие фосфаты, и их применение как нацеленных цитотоксичных средств
Автори російськоюДенни Уилльям Александер, Этвелл Грехем Джон, Ян Шанцзинь, Уилсон Уилльям Роберт, Петтерсон Адам Ворн, Хелзби Нуала Анн
МПК / Мітки
МПК: C07F 9/09, A61P 35/00, A61K 31/166, C07C 233/67, C07C 317/36, C07C 301/00, A61K 31/396, C07D 203/00, A61K 31/661
Мітки: цитотоксичних, відповідні, нітрофеніліпритні, застосування, спирті, націлених, нітрофенілазиридинові, засобів, фосфати
Код посилання
<a href="https://ua.patents.su/34-89363-nitrofenilipritni-i-nitrofenilaziridinovi-spirti-i-kh-vidpovidni-fosfati-i-kh-zastosuvannya-yak-nacilenikh-citotoksichnikh-zasobiv.html" target="_blank" rel="follow" title="База патентів України">Нітрофеніліпритні і нітрофенілазиридинові спирти і їх відповідні фосфати, і їх застосування як націлених цитотоксичних засобів</a>
Попередній патент: Система корекції біологічної рідини
Наступний патент: Кон’югат пептиду гранулоцитарного колонієстимулюючого фактора (g-csf)
Випадковий патент: Вершковий крем