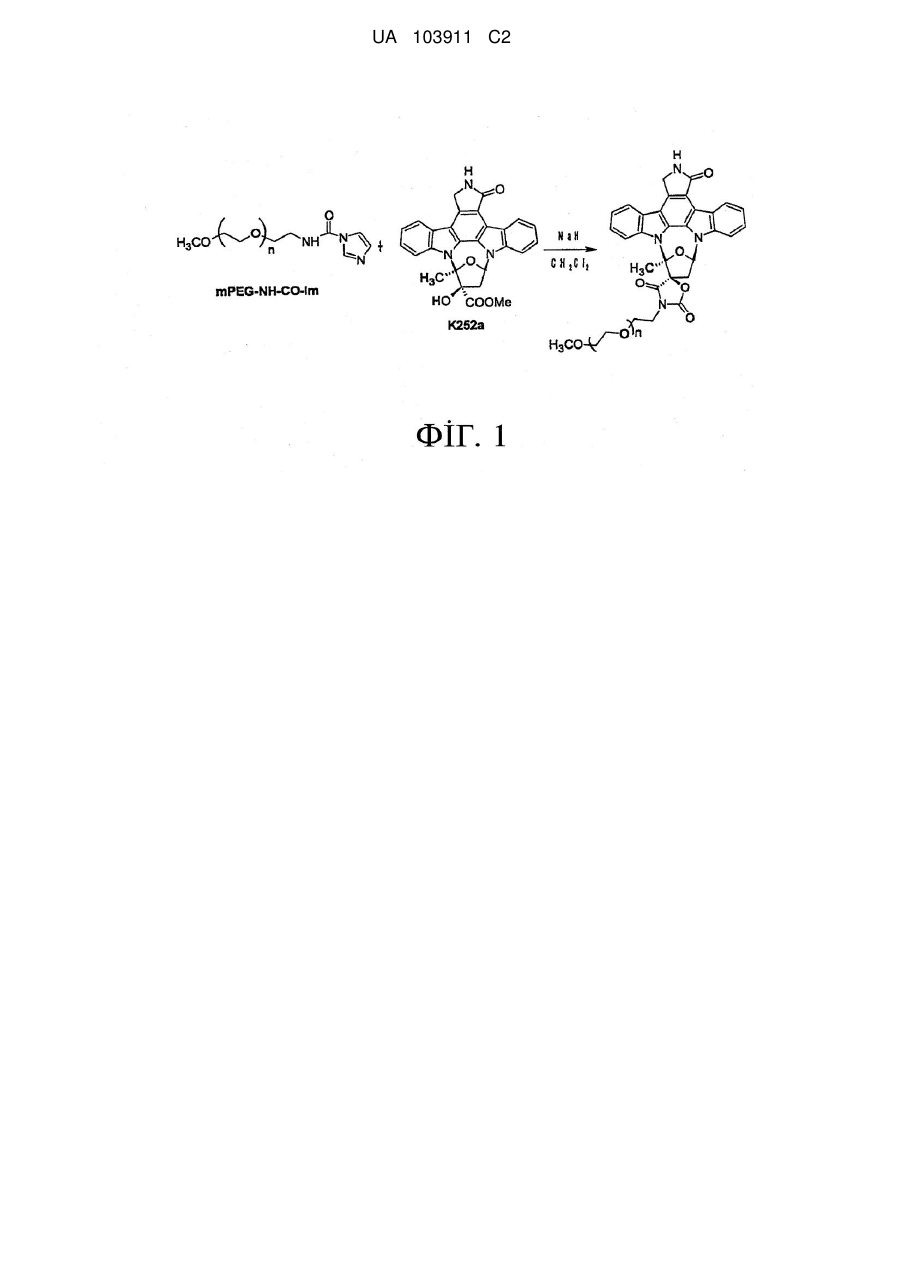
Синтез полімерних кон’югатів індолокарбазольних сполук
Номер патенту: 103911
Опубліковано: 10.12.2013
Автори: Лоренцетто Кьяра, Пінчеллі Карло, Маінеро Валентіна, Марконі Алессандра, Беккаріа Лука, Траверса Сільвіо, Баньод Раффаелла, Кріскуоло Доменіко, Бертаріоне Рава Росса Луїза
Формула / Реферат
1. Спосіб одержання полімерного кон'югата індолокарбазольної сполуки за формулою (І)
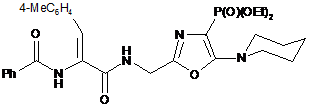 , формула (І)
, формула (І)
де
R1 та R2 є однаковими або різними хімічними залишками, і кожен з них незалежно один від одного вибраний з групи, яку складають:
(a) водень, галоген, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, гідроксил, нижча алкоксигрупа, карбоксил, нижчий алкоксикарбоніл, ацил, нітрогрупа, карбамоїл, нижчий алкіламінокарбоніл, -NR5R6, де кожен з R5 та R6 незалежно один від одного вибраний з-поміж таких замісників, як водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, заміщений або незаміщений арил, заміщений або незаміщений гетероарил, заміщений або незаміщений аралкіл, заміщений або незаміщений нижчий алкіламінокарбоніл, заміщений або незаміщений нижчий ариламінокарбоніл, алкоксикарбоніл, карбамоїл, ацил, або R5 та R6 у поєднанні з атомом азоту утворюють гетероциклічну групу;
(b) -CO(CH2)jR4, де j дорівнює від 1 до 6, та R4 вибраний з групи, яку складають:
(і) водень, галоген, -N3,
(іі) -NR5R6, де R5 та R6 відповідають визначенням, наведеним вище,
(ііі) -SR7, де R7 вибраний з групи, яку складають водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, заміщений або незаміщений арил, заміщений або незаміщений гетероарил, заміщений або незаміщений аралкіл, -(CH2)aCO2R10 (де а - 1 або 2, і де R10 вибраний з групи, яку складають водень і заміщений або незаміщений нижчий алкіл) та -(CH2)aCO2NR5R6,
(iv) -OR8, -OCOR8, де R8 вибраний з групи, яку складають водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, заміщений або незаміщений арил, заміщений або незаміщений гетероарил,
(c) -CH(OH)(CH2)jR4, де j та R4 відповідають визначенням, наведеним вище;
(d) -(CH2)dCHR11CO2R12 aбo -(CH2)dCHR11CONR5R6, де d дорівнює від 0 до 5, R11 - водень, -CONR5R6 або -CO2R13, де R13 - водень або заміщений чи незаміщений нижчий алкіл; та R12 - водень або заміщений чи незаміщений нижчий алкіл;
(e) -(CH2)kR14, де k дорівнює від 2 до 6, і R14 - галоген, заміщений або незаміщений арил, заміщений або незаміщений гетероарил, -COOR15, -OR15 (де R15 - водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, заміщений або незаміщений арил, заміщений або незаміщений гетероарил або ацил), -SR7 (де R7 відповідає визначенню, наведеному вище), -CONR5R6, -NR5R6 (де R5 та R6 відповідають визначенням, наведеним вище) або -N3;
(f) -CH=CH(CH2)mR16, де m дорівнює від 0 до 4, та R16 - водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, заміщений або незаміщений арил, заміщений або незаміщений гетероарил, -COOR15, -OR15 (де R15 відповідає визначенню, наведеному вище), -CONR5R6 або -NR5R6 (де R5 та R6 відповідають визначенням, наведеним вище);
(g) -CH=C(CO2R12)2, де R12 відповідає визначенню, наведеному вище;
(h) -CºC(CH2)nR16, де n - ціле число від 0 до 4, і R16 відповідає визначенню, наведеному вище;
(і) -CH2OR22, де R22 - три-(нижчий алкіл)силіл, у якому три групи нижчого алкілу є однаковими або різними, або де R22 має те саме значення, що й R8;
(j) -CH(SR23)2 та -CH2-SR7, де R23 - нижчий алкіл, нижчий алкеніл або нижчий алкініл, і де R7 відповідає визначенню, наведеному вище; та
R3 - водень, галоген, ацил, карбамоїл, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений алкеніл, заміщений або незаміщений нижчий алкініл або аміногрупа, та
W1 та W2 незалежно один від одного означають водень, гідроксил, або W1 та W2 спільно означають кисень;
і де X означає полімерний фрагмент,
при цьому цей спосіб включає проведення реакції w-1-Н-імідазолокарбоксамідної полімерної сполуки за загальною формулою (II)
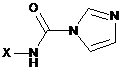 , формула (II)
, формула (II)
де X відповідає визначенню, наведеному вище,
з індолокарбазольною сполукою за загальною формулою (III)
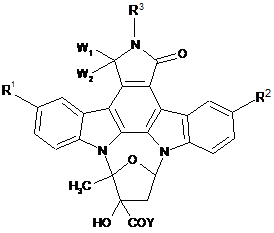 , формула (III)
, формула (III)
де R1, R2, R3, W1 та W2 - групи, які відповідають визначенням, наведеним вище, і які факультативно захищені захисними групами, і де Y являє собою відщеплювану групу, причому спосіб також факультативно включає відщеплення захисних груп від груп R1, R2, R3, W1 та W2 з одержанням сполуки за формулою (І).
2. Спосіб за п. 1, який відрізняється тим, що його здійснюють у присутності основи в органічному розчиннику.
3. Спосіб за п. 2, який відрізняється тим, що молярне співвідношення між основою і сполукою формули (III) становить від приблизно 1:1 до приблизно 4:1, за варіантом, якому віддається перевага, - від приблизно 1:1 до приблизно 1,5:1 і, за варіантом, якому віддається ще більша перевага, - приблизно 1:1.
4. Спосіб за п. 2 або п. 3, який відрізняється тим, що основу вибирають із групи гідридів лужних металів, зокрема нею є гідрид натрію.
5. Спосіб за будь-яким із пп. 1-4, який відрізняється тим, що його здійснюють в органічному розчиннику, за варіантом, якому віддається перевага, в безводному органічному розчиннику, який вибирають з групи, яка складається з дихлорметану, хлороформу та N,N-диметилформаміду.
6. Спосіб за будь-яким із пп. 1-4, який відрізняється тим, що його здійснюють в атмосфері інертного газу, за варіантом, якому віддається перевага, - в атмосфері азоту або аргону.
7. Спосіб за будь-яким із попередніх пунктів, який відрізняється тим, що його здійснюють при температурі від -10 °C до 60 °C, за варіантом, якому віддається перевага, - від 0 °C до 25 °C і, за варіантом, якому віддається найбільша перевага, - при кімнатній температурі після проведення початкової стадії при 0°.
8. Спосіб за будь-яким із попередніх пунктів, який відрізняється тим, що полімерний кон'югат за формулою (І) одержують безпосередньо шляхом хроматографічного очищення.
9. Спосіб за п. 8, який відрізняється тим, що очищення полімерного кон'югата за формулою (І) здійснюють у розчиннику, який за варіантом, якому віддається перевага, вибирають із групи, яка складається з дихлорметану, води, метанолу, ацетонітрилу, буферного розчину форміату амонію, при різних співвідношеннях компонентів у суміші.
10. Спосіб за будь-яким із попередніх пунктів, який забезпечує вихід сполуки за формулою (І) від приблизно 40 % до приблизно 95 % від загальної маси, за варіантом, якому віддається перевага, - від приблизно 50 % до приблизно 95 % від загальної маси, в перерахунку на масу сполуки за формулою (III).
11. Спосіб за будь-яким із попередніх пунктів, який відрізняється тим, що відщеплювану групу Y вибирають із групи, яку складають трифлат, тозилат, мезилат, сульфат, галоген, гідрокси та нижча алкоксигрупа.
12. Спосіб за п. 10, який відрізняється тим, що відщеплюваною групою Y є нижча алкоксигрупа, за варіантом, якому віддається перевага, - метоксигрупа.
13. Спосіб за будь-яким із попередніх пунктів, який відрізняється тим, що полімер X вибирають з-поміж полі(алкіленоксидів), зокрема з-поміж полі(етиленоксидів).
14. Спосіб за п. 13, який відрізняється тим, що полімер X є (поліетилен)гліколем (PEG), який, за варіантом, якому віддається перевага, вибирають з-поміж поліетиленгліколів, заміщених у кінцевому положенні алкоксигрупою, таких як метоксиполіетиленгліколь (mPEG).
15. Спосіб за будь-яким із попередніх пунктів, який відрізняється тим, що полімер X має молекулярну вагу від приблизно 100 Да до приблизно 100000 Да, за варіантом, якому віддається перевага, - від приблизно 200 Да до приблизно 50000 Да.
16. Спосіб за п. 14 або п. 15, який відрізняється тим, що полімер X є полі(етиленгліколем), наприклад, mPEG, із середньою молекулярною масою від приблизно 500 Да до приблизно 10000 Да, наприклад, приблизно 550 Да, приблизно 1100 Да, приблизно 2000 Да або приблизно 5000 Да.
17. Спосіб за будь-яким із попередніх пунктів, який відрізняється тим, що R1, R2, R3, W1 та W2 є воднем.
18. Полімерний кон'югат індолокарбазольної сполуки за формулою (І)
 , формула (І)
, формула (І)
де
R1, R2, R3, W1, W2 та X відповідають визначенню за п. 1 або пп. 13-16;
або його фармацевтично прийнятна сіль.
19. Полімерний кон'югат за п. 18, де R1, R2, R3, W1 та W2 - водень.
20. Полімерний кон'югат за п. 18 або п. 19, який відрізняється тим, що полімер X є полі(етиленгліколем), наприклад mPEG, із середньою молекулярною масою від приблизно 500 Да до приблизно 10000 Да, наприклад, приблизно 550 Да, приблизно 1100 Да, приблизно 2000 Да або приблизно 5000 Да.
21. Полімерний кон'югат за будь-яким із пп. 18-20 для використання в лікарському засобі.
22. Полімерний кон'югат за п. 21 для використання в лікарському засобі для місцевого застосування.
23. Полімерний кон'югат за п. 21 для використання в лікарському засобі для системного застосування (наприклад, для ін'єкції, інфузії або інгаляції).
24. Фармацевтична композиція, яка містить щонайменше один полімерний кон'югат за будь-яким із пп. 18-20, факультативно разом із фармацевтично прийнятними носіями, допоміжними речовинами, розріджувачами та/або домішками.
25. Фармацевтична композиція за п. 24 для діагностичного або/та терапевтичного застосування.
26. Застосування полімерного кон'югата за будь-яким із пп. 18-21 для виготовлення лікарського засобу для запобігання, часткового полегшення симптомів та/або лікування патологій, пов'язаних із HMGB1.
27. Застосування за п. 26, причому патології, пов'язані з HMGB1, вибирають з-поміж таких захворювань, як стеноз, рестеноз, атеросклероз, ревматоїдний артрит, аутоімунні захворювання, пухлини, інфекційні захворювання, сепсис, гостре запальне ушкодження легенів, червоний вовчак, нейродегенеративні захворювання, захворювання центральної і периферичної нервової системи та розсіяний склероз.
28. Застосування за п. 26 або п. 27, причому полімерний кон'югат оборотно іммобілізований на поверхні медичного пристрою.
29. Застосування полімерного кон'югата за будь-яким з пп. 18-21 для виготовлення лікарського засобу для запобігання, часткового полегшення симптомів та/або лікування неврологічних розладів, нейропатій та нейродегенеративних розладів центральної і периферичної нервової системи.
30. Застосування полімерного кон'югата за будь-яким із пп. 18-21 для виготовлення лікарського засобу для запобігання, часткового полегшення симптомів та/або лікування патологій шкіри.
31. Застосування за п. 30, причому патології шкіри характеризуються гіперпроліферацією кератиноцитів.
32. Застосування за п. 30 або п. 31, причому патологією шкіри є псоріаз, атопічний дерматит, хронічна екзема, вугри, червоний волосяний лишай, опікові рубці (келоїди), гіпертрофічні рубці та пухлини шкіри.
33. Застосування за п. 32, причому патологія шкіри є псоріазом.
34. Застосування за будь-яким із пп. 30-33, причому лікарський засіб призначений для місцевого застосування.
35. Застосування за п. 34, причому введення у організм здійснюється у формі ліпосом.
36. Застосування полімерного кон'югата за будь-яким із пп. 18-21 для виготовлення лікарського засобу для запобігання, часткового полегшення симптомів та/або лікування болю, пов'язаного із фактором росту нервової тканини (NGF), та гіпералгезії.
37. Застосування полімерного кон'югата за будь-яким із пп. 18-21 для виготовлення лікарського засобу для запобігання, часткового полегшення симптомів та/або лікування запальних захворювань, автоімунних захворювань, синдрому системної запалювальної реакції, реперфузійного ушкодження після трансплантації органів, серцево-судинних уражень, акушерських і гінекологічних захворювань, інфекційних захворювань, алергічних та атопічних захворювань, солідних та рідинних пухлинних патологій, синдромів відторгнення трансплантата, природжених захворювань, дерматологічних захворювань, неврологічних захворювань, кахексії, ниркової недостатності, станів ятрогенної інтоксикації, метаболічних та ідіопатичних захворювань, а також офтальмологічних захворювань.
38. Застосування полімерного кон'югата за будь-яким із пп. 18-21 для виготовлення лікарського засобу для запобігання, часткового полегшення симптомів та/або лікування синдрому Бехчета, синдрому Гужеро-Шегрена, васкуліту, увеїту та ретинопатій.
39. Застосування за пп. 36-38, причому лікарський засіб призначений для системного застосування.
40. Застосування за будь-яким із пп. 26-39 у поєднанні із щонайменше одним протизапальним лікарським засобом.
Текст
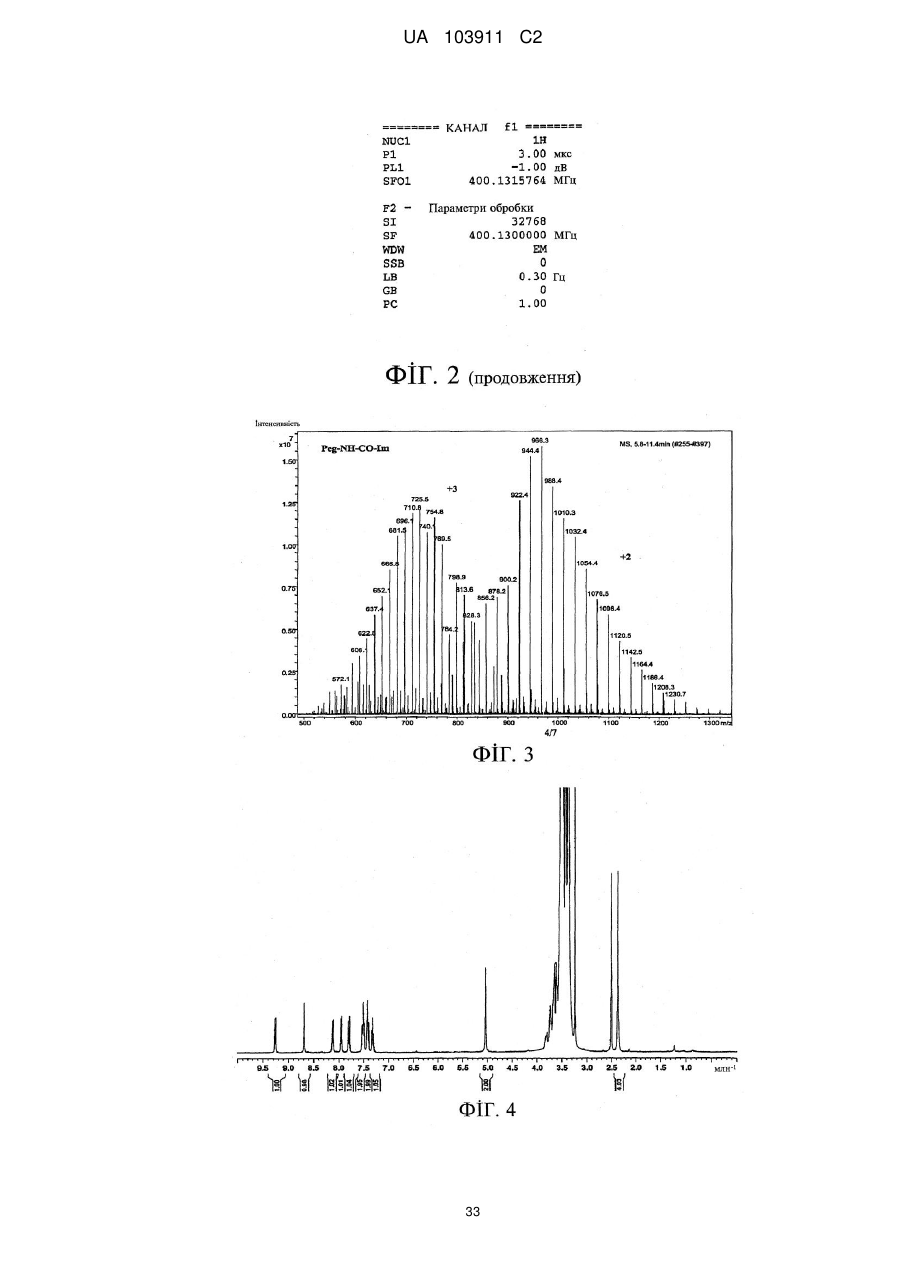
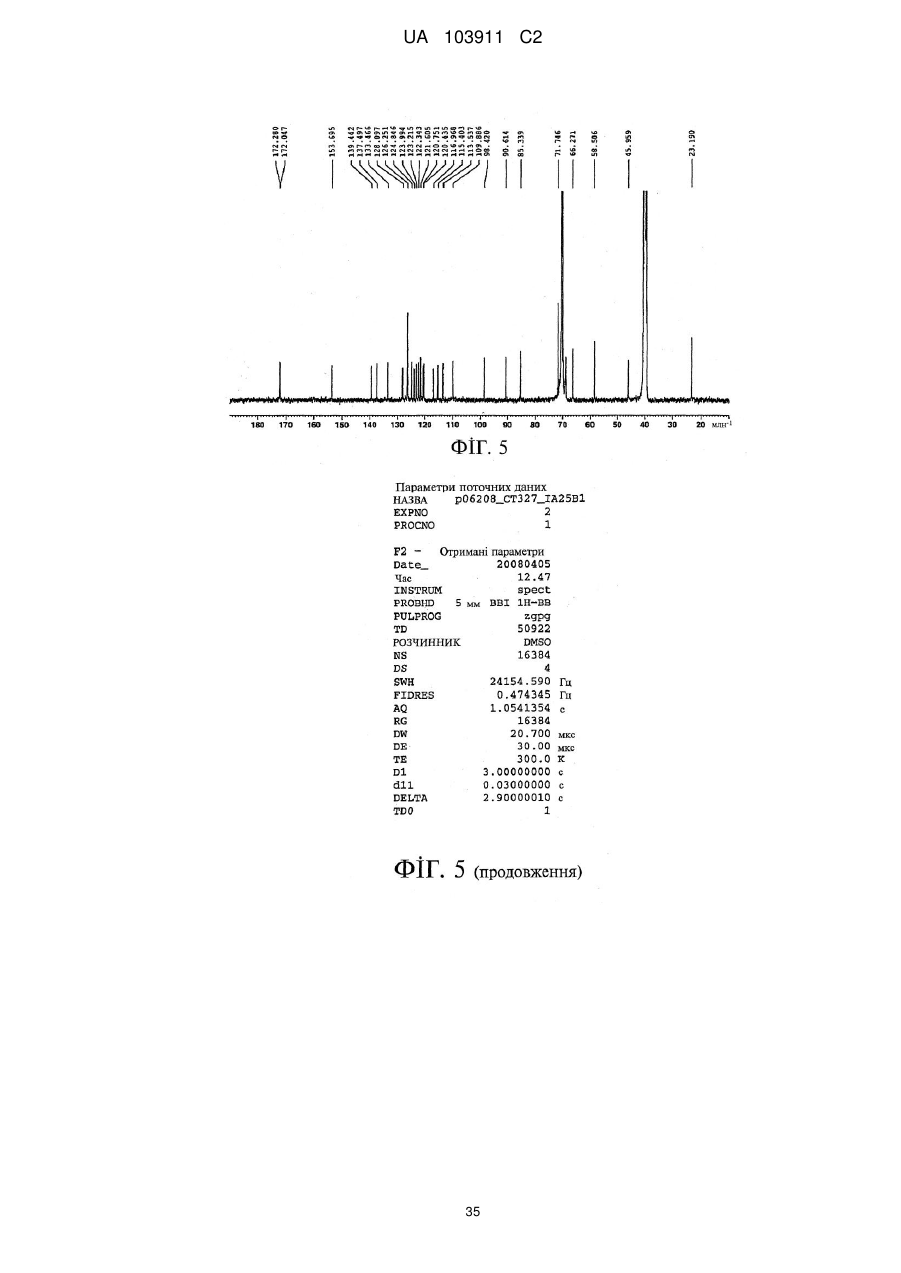
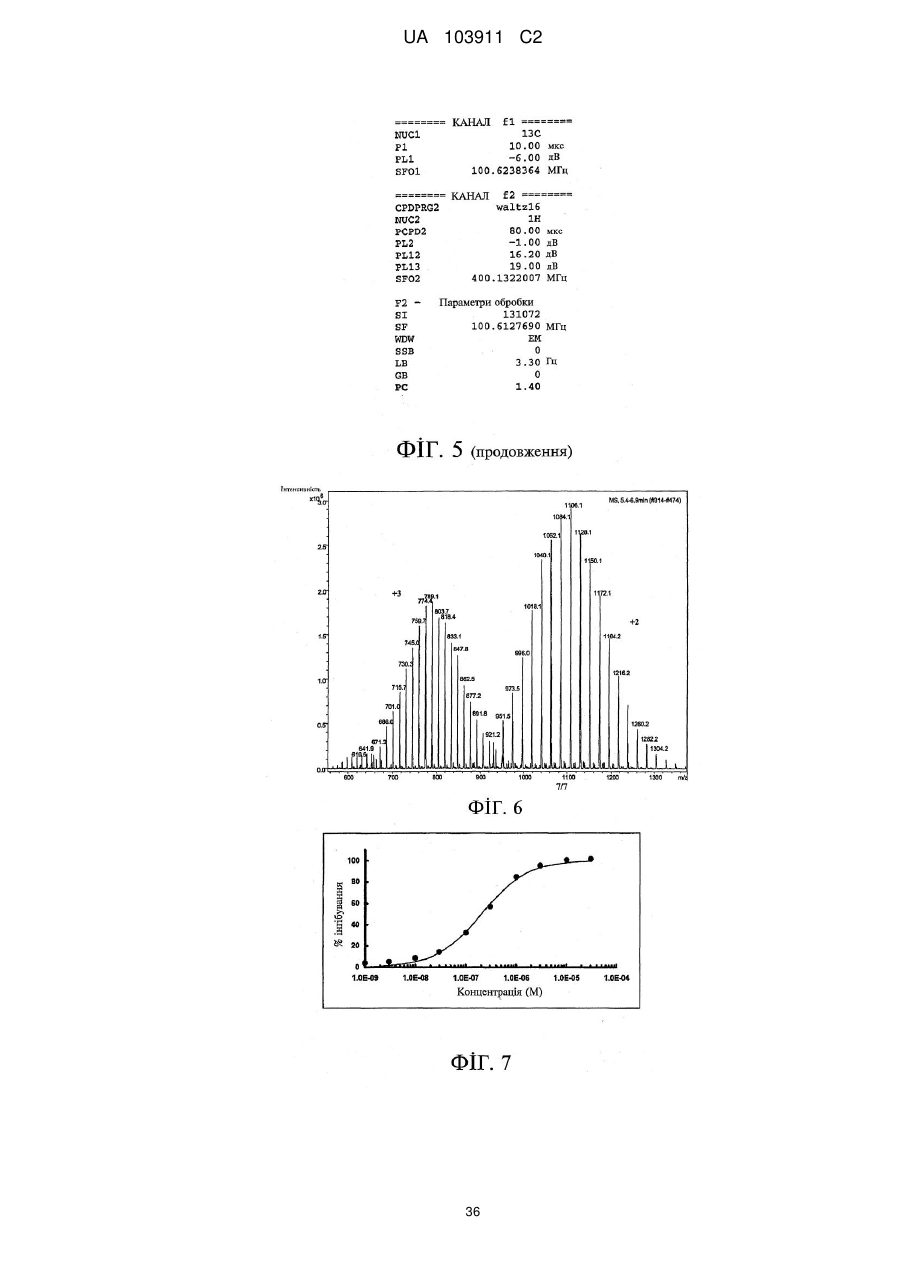
Реферат: Цей винахід стосується способу одержання полімерних кон'югатів індолокарбазольних сполук, зокрема полімерних кон'югатів сполуки K-252а та її похідних, шляхом синтезу, який забезпечує одержання продукту високої чистоти із високим виходом. У подальшому аспекті цей винахід стосується нових полімерних кон'югатів сполуки K-252а та її похідних, у складі яких хімічна група, яка приєднує полімерний фрагмент до сполуки K-252а або до одного з похідних сполуки K-252а, характеризується наявністю 5-членної циклічної структури оксазолідиндіону. Ці нові полімерні кон'югати одержують за допомогою нового способу синтезу з високою чистотою та з високими виходами. UA 103911 C2 (12) UA 103911 C2 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 Опис Цей винахід стосується способу одержання полімерних кон'югатів індолокарбазольних сполук, зокрема полімерних кон'югатів сполуки K-252а та її похідних, шляхом синтезу, в результаті якого одержують продукт високої чистоти із високим виходом. За одним з аспектів цей винахід стосується нових полімерних кон'югатів сполуки K-252а та її похідних, у яких присутня хімічна група, яка приєднує полімерний фрагмент до сполуки K-252а або до похідного сполуки K-252а, і характеризується наявністю циклічної структури оксазолідиндіону. Ці нові полімерні кон'югати одержують із застосуванням нового шляху синтезу, із високою чистотою і з високими виходами. В літературі описані терапевтичні можливості сполуки K-252а та її похідних в запобіганні, частковому полегшенні симптомів і лікуванні патологій, пов'язаних із кіназами, зокрема патологій, пов'язаних із HMGB1, таких як: неврологічні розлади, невропатії та нейродегенеративні захворювання центральної і периферичної нервової системи (дивись, наприклад, РСТ/ЕР2005/008258, Annu. Rev. Pharmacol. Toxicol. 2004;44:451-74; Neurochem Int. 2001 Nov-Dec; 39(5-6):459-68; Neuroport. 2000 Nov. 9; ll(16):3453-6; Neuroscience. 1998 Sep; 86(2):461-72; Brains Res. 1994 Jul 4; 650(1): 170-4). Крім того, аналіз сучасного стану досліджень у галузі свідчить про терапевтичну ефективність цих індолокарбазольних сполук в запобіганні, частковому полегшенні симптомів і лікуванні шкірних патологій, зокрема шкірних захворювань, пов'язаних із надмірною проліферацією кератиноцитів, таких як псоріаз (дивись, наприклад, WO 2005/014003, Raychaudhuri et al., J. Invest. Dermatol. 122:812-819, 2004). Крім того, у публікаціях, які стосуються зазначеної галузі, повідомлялося, що сполука K-252а та її похідні придатні до використання як активні засоби для полегшення болю, пов'язаного з фактором росту нервової тканини (nerve growth factor, NGF) (дивись, наприклад, Koizumi et al., J. Neurosci. 8:715-721, 1988; Doherty et al., Neurosci. Lett. 96:1-6, 1989; Matsuda et al., Neurosci. Lett. 87:11-17, 1988, Winston J.H. et al. /. Pain (2003) 4:329-337). Таким чином, біологічне значення і терапевтична активність індолокарбазольної сполуки K-252а та її похідних докладно описані в літературі (дивись, наприклад, Kim et al., Biol. Pharm. Bull. 21:498-505, 1998, Schneider et al., Org. Lett. 7:1695-1698, 2005). Полімерні кон'югати сполуки K-252a та її похідних, а також їх використання як активної складової у фармацевтичних композиціях, призначених для запобігання, часткового полегшення симптомів та лікування зазначених вище патологій, розкриті у WO 2007/022999. Зміст зазначеної заявки включений в цю заявку шляхом посилання. Відповідно до WO 2007/022999, мета ковалентного приєднання активних сполук похідного індолокарбазолу K-252а до полімеру і, зокрема, до макромолекули PEG, полягає у розробці таких лікарських форм зазначених активних сполук, які мають кращі фармакокінетичні і токсикологічні властивості, завдяки чому досягається найкраща біодоступність сполуки K-252а або її похідного при найрізноманітніших способах і шляхах застосування. Методика синтезу, який має на меті одержання полімерних кон'югатів сполуки K-252а та її похідних, описаний у WO 2007/022999, включає стадію ковалентного сполучення полімерного фрагмента до структури індолокарбазолу у складі сполуки K-252а або її похідних. Зокрема, у WO 2007/022999 розкрита реакція полімеру, активованого ізоціанатною групою, з гідроксильною групою, яка знаходиться в положенні С3 тетрагідрофуранового фрагмента у складі сполуки K252а або її похідного, у відповідних умовах реакції, в результаті чого між полімерним фрагментом та активною сполукою утворюється ковалентний зв'язок у вигляді карбамідного зв'язку. Оскільки полімерні кон'югати сполуки K-252а та її похідних, які характеризуються високою чистотою, дуже необхідні у медицині, метою цього винаходу було запропонувати спосіб одержання полімерних кон'югатів активних індолокарбазольних сполук, який забезпечує одержання продукту високої чистоти, із високими і стабільними виходами. Крім того, ще одна мета цього винаходу полягала в тому, щоб усунути складні стадії очищення і надати можливість легкого очищення і виділення цільового кон'югату сполуки та полімеру, з метою забезпечення максимальної ефективності реакції сполучення з полімером. Винахідники несподівано з'ясували, що проведення реакції сполуки K-252а або її похідного з ω-1-Н-імідазолкарбоксамідним полімерним складником, який є вихідним полімерним реагентом реакції сполучення, забезпечує керований процес сполучення, а отже й бажаний високий вихід і чистоту продукту реакції - полімерного кон'югату індолокарбазолу. Отже, цей винахід стосується способу одержання полімерних кон'югатів індолокарбазольної сполуки за формулою (І) 1 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 де 1 2 R та R є однаковими або різними хімічними залишками, і кожен з них незалежно один від одного вибраний з групи, яку складають: (а) водень, галоген, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, гідроксил, нижча алкоксигрупа, карбоксил, нижчий алкоксикарбоніл, ацил, нітрогрупа, карбамоїл, нижчий алкіламінокарбоніл, 5 6 5 6 -NR R , де кожен з R та R незалежно один від одного вибраний з-поміж таких замісників як водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, заміщений або незаміщений арил, заміщений або незаміщений гетероарил, заміщений або незаміщений аралкіл, заміщений або незаміщений нижчий алкіламінокарбоніл, заміщений або незаміщений нижчий ариламінокарбоніл, 5 6 алкоксикарбоніл, карбамоїл, ацил, або R та R у поєднанні з атомом азоту утворюють гетероциклічну групу; 4 4 (b) -CO(CH2)jR , де j дорівнює від 1 до 6, та R вибраний з групи, яку складають: (і) водень, галоген, -N3, 5 6 5 6 (іі) -NR R , де R та R відповідають визначенням, наведеним вище, 7 7 (ііі) -SR , де R вибраний з групи, яку складають водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, заміщений або незаміщений арил, заміщений або незаміщений гетероарил, заміщений або 10 10 незаміщений аралкіл, -(СН2)аСO2R (де а - 1 або 2, і де R вибраний з групи, яку складають 5 6 водень і заміщений або незаміщений нижчий алкіл) і -(CH2)aCO2NR R , 8 8 8 (iv) -OR , -OCOR , де R вибраний з групи, яку складають водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, заміщений або незаміщений арил, заміщений або незаміщений гетероарил; 4 4 (c) -CH(OH)(CH2)j R , де j та R відповідають визначенням, наведеним вище; 11 12 11 5 6 11 (d) -(CH2)dCHR CO2R або-(CH2)dCHR CONR R , де d - ціле число від 0 до 5, R - водень, 5 6 13 13 12 CONR R або -CO2R , де R - водень або заміщений чи незаміщений нижчий алкіл; та R водень або заміщений чи незаміщений нижчий алкіл; 14 14 (e) -(CH2)kR , де k дорівнює від 2 до 6, і R - галоген, заміщений або незаміщений арил, 15 15 15 заміщений або незаміщений гетероарил, -COOR , -OR , (де R - водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий алкініл, заміщений або незаміщений арил, заміщений або незаміщений 7 7 5 6 5 6 гетероарил або ацил), -SR (де R відповідає визначенню, наведеному вище), -CONR R , -NR R 5 6 (де R та R відповідають визначенням, наведеним вище) або -N3; 16 16 (f) -CH=CH(CH2)mR , де m дорівнює від 0 до 4, та R - водень, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений нижчий алкеніл, заміщений або незаміщений нижчий 15 алкініл, заміщений або незаміщений арил, заміщений або незаміщений гетероарил, -COOR , 15 15 5 6 5 6 5 6 OR (де R відповідає визначенню, наведеному вище), -CONR R або -NR R (де R та R відповідають визначенням, наведеним вище); 12 12 (g) -CH=C(CO2R )2, де R відповідає визначенню, наведеному вище; 16 16 (h) -CC(CH2)nR , де n - ціле число від 0 до 4 і R відповідає визначенню, наведеному вище; 22 22 (і) -CH2OR , де R - три-(нижчий алкіл)силіл, у якому три групи нижчого алкілу є однаковими 22 8 або різними, або де R має те саме значення, що й R . 23 7 23 7 (j) -CH(SR )2 та -CH2-SR , де R - нижчий алкіл, нижчий алкеніл або нижчий алкініл, і де R відповідає визначенню, наведеному вище; та 3 R - водень, галоген, ацил, карбамоїл, заміщений або незаміщений нижчий алкіл, заміщений або незаміщений алкеніл, заміщений або незаміщений нижчий алкініл або аміногрупа, та 2 UA 103911 C2 5 W 1 та W 2 незалежно одне від одного означають водень, гідроксил, або W 1 та W 2 спільно означають кисень; і де X означає полімерний фрагмент, при цьому цей спосіб включає проведення реакції ω-1-Η-імідазолкарбоксамідної полімерної сполуки за загальною формулою (II) де X відповідає визначенню, наведеному вище, з індолокарбазольною сполукою за загальною формулою (III) 10 15 20 25 30 35 40 де R1, R2, R3, W 1 та W2 - групи, які відповідають визначенням, наведеним вище, і які факультативно захищені захисними групами, і де Υ являє собою відщеплювану групу, причому спосіб також факультативно включає відщеплення захисних груп від факультативно захищених груп R1, R2, R3, W 1 та W 2 для одержання сполуки за формулою (І). Реакцію ковалентного сполучення, яка є складовою способу за цим винаходом, для синтезу полімерного кон'югату формули (І) каталізують основою в органічному розчиннику. За варіантом, якому віддається перевага, основа належить до сильних основ. За варіантом, якому віддається перевага, основу вибирають з групи, яка складається з гідридів лужних металів, третинних амінів та/або алкоксиду. У варіанті здійснення винаходу, якому віддається ще більша перевага, основою, яка каталізує реакцію ковалентного сполучення за цим винаходом, є гідрид натрію. Втім, так само можуть бути використані й інші основи, такі як метоксид натрію або триетиламін. Молярне співвідношення між основним каталізатором і сполукою формули (III) за варіантом, якому віддається перевага, становить від приблизно 1:1 до приблизно 4:1, за варіантом, якому віддається ще більша перевага, - від приблизно 1:1 до приблизно 1,5:1 і за варіантом, якому віддається найбільша перевага, - приблизно 1:1. Крім того, згадану реакцію за цим винаходом, ведуть у органічному розчиннику, за варіантом, якому віддається перевага, - за відсутності вологи, тобто у безводному органічному розчиннику. За варіантом, якому віддається перевага, вміст води у суміші для розчинення -1 складових при цьому способі ковалентного сполучення менше ніж 200 млн . Органічний розчинник може бути вибраний з групи, яка складається з дихлорметану, хлороформу та N,Nдиметилформаміду. За варіантом здійснення винаходу, якому віддається велика перевага, органічним розчинником є дихлорметан, за варіантом здійснення винаходу, якому віддається ще більша перевага, ним є безводний дихлорметан. Крім того, відповідно до винаходу, перевагу має ведення реакції в атмосфері інертного газу, такого як азот або аргон. До того ж, реакцію, яка є складовою способу синтезу за цим винаходом, за варіантом, якому віддається перевага, здійснюють при температурі від приблизно -10 °C до приблизно 60 °C, за варіантом, якому віддається більша перевага, - від приблизно 0 °C до приблизно 25 °C і за варіантом, якому віддається найбільша перевага, - при кімнатній температурі після проведення початкової стадії при 0 °C. Після одержання цільової сполуки формули (І) відповідно до способу за цим винаходом полімерний кон'югат формули (І) надалі може бути виділений з реакційної суміші і очищений від неї. Відповідно до варіанта здійснення винаходу, якому віддається перевага, сполуку за 3 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 формулою (І) одержують із реакційної суміші шляхом очищення методом флеш-хроматографії. За варіантом, якому віддається перевага, застосовують автоматичну градієнтну флешхроматографічну систему очищення, споряджену відповідною колонкою, із використанням відповідного розчинника. За варіантом, якому віддається перевага, метод очищення вибирають з-поміж методів, у яких застосовуються колонки з оберненою або нормальною фазою, і розчинник для кондиціонування та/або елюент за варіантом, якому віддається перевага, вибирають з-поміж таких розчинників як дихлорметан, вода, метанол, ацетонітрил, а також буферний розчин на основі форміату амонію, при різних співвідношеннях компонентів у суміші. За варіантом здійснення цього винаходу, якому віддається більша перевага, полімерний кон'югат індолокарбазольної сполуки за формулою (І) піддають очищенню методом флешхроматографії з оберненою фазою на установці, спорядженій касетою С18, при цьому очищення ведуть шляхом ізократичного елюювання сумішшю ацетонітрилу та буферного розчину на основі форміату амонію (5 ммоль/л, рН 3,5) у співвідношенні 40:60 (як показано у прикладі 3). За ще одним варіантом здійснення винаходу, якому віддається перевага, полімерний кон'югат індолокарбазольної сполуки за формулою (І) піддають очищенню методом флеш-хроматографії з нормальною фазою (як описано у прикладі 4 та прикладі 5.3). Продукт може бути висушений, наприклад, над сульфатом натрію, і відфільтрований, а розчинник може бути видалений шляхом випарювання в умовах зниженого тиску при 25 °C. Очищення цільового продукту здійснюють за допомогою звичайних прийомів, відомих фахівцям у цій галузі. Полімерна сполука за формулою (І) після стадії очищення має чистоту щонайменше приблизно 95 %. За варіантом, якому віддається більша перевага, сполука формули (І) після стадії очищення має чистоту щонайменше приблизно 98 %. За варіантом здійснення винаходу, якому віддається найбільша перевага, продукт сполучення з полімером має чистоту 98,5 %, 99 % або навіть 99,5 %. Крім того, спосіб за цим винаходом забезпечує загальний масовий вихід сполуки за формулою (І) від приблизно 40 % до приблизно 98 % від загальної маси, за варіантом, якому віддається перевага, від приблизно 50 % до приблизно 95 % від загальної маси, в перерахунку на масу реагента за формулою (III). Залишок Υ формули (III) є відщеплюваною групою, тобто групою, яку в умовах реакції сполучення з полімером за винаходом відокремлюють від структури сполуки за формулою (III) для одержання оксазолідиндіонового циклу сполуки за формулою (І), який ковалентно сполучає полімерний фрагмент зі структурою індолокарбазолу сполуки K-252а або її похідного. За цим винаходом цикл імідазолу сполуки за загальною формулою (II) під час реакції сполучення відокремлюють від фрагмента полімерного реагенту для одержання сполуки формули (І). За варіантом здійснення винаходу, якому віддається перевага, відщеплювану групу Υ формули (III) вибирають з групи замісників, до якої входять трифлат, тозилат, мезилат, сульфат, галоген, гідроксил або нижча алкоксигрупа. За варіантом здійснення винаходу, якому віддається особлива перевага, відщеплюваною групою Υ формули (III) є нижча алкоксигрупа або гідроксигрупа. За варіантом, якому віддається найбільша перевага, відщеплюваною групою Υ є нижча алкоксигрупа, зокрема метоксигрупа. Полімерний фрагмент, який ковалентно приєднаний до індолокарбазольної сполуки способом за цим винаходом, і який є, наприклад, хімічним залишком X у загальних формулі (І) та формулі (II), має бути біологічно сумісним, може бути природним, напівсинтетичним або синтетичним за походженням і може мати лінійну або розгалужену будову. За варіантом здійснення цього винаходу, якому віддається перевага, полімер X вибирають з-поміж полі(алкіленоксидів), зокрема з-поміж (поліетилен)оксидів. Разом із тим, до інших прикладів полімерів належать, без обмеження ними, поліакрилова кислота, поліакрилати, поліакриламід або його N-алкілпохідні, поліметакрилова кислота, поліметакрилати, поліетилакрилова кислота, поліетилакрилати, полівінілпіролідон, полівініловий спирт), полігликолева кислота, полімолочна кислота, полі(молочна-ко-гликолева) кислота, декстран, хітозан, поліамінокислоти, гідроксіетилкрохмаль. З метою введення в реакцію згідно зі способом за цим винаходом, зокрема, для одержання функціональної придатності полімерного реагента за формулою (II), який використовується в способі за цим винаходом, згаданий вище полімерний фрагмент має нести кінцеву функціональну аміногрупу або має зазнати функціонального перетворення задля одержання кінцевої функціональної аміногрупи. Отже, полімерний фрагмент має бути полімером, активованим аміногрупою, загальної формули X-NH2. 4 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 60 Фактично вихідний полімерний реагент за формулою (II) одержують за реакцією аміногрупи полімерного фрагмента з похідним 1,1-карбонілдіімідазолу, що призводить до одержання ω-1Η-імідазолкарбоксамідної полімерної сполуки загальної формули (II). Реакцію утворення ω-1-Н-імідазолкарбоксамідної полімерної сполуки формули (II) за варіантом, якому віддають перевагу, ведуть у органічному розчиннику, такому як дихлорметан, хлороформ, N,N-диметилформамід. За варіантом здійснення винаходу, якому віддають велику перевагу, органічним розчинником є дихлорметан, за варіантом, якому віддають ще більшу перевагу, ним є безводний дихлорметан. У ще одному варіанті здійснення цього винаходу, якому віддається перевага, активацію ωаміногрупи полімеру здійснювали в атмосфері інертного газу, такого як азот або аргон. Крім того, реакцію утворення ω-1-Н-імідазолкарбоксамідної полімерної сполуки за цим винаходом за варіантом, якому віддається перевага, ведуть при температурі від приблизно 10 °C до приблизно 60 °C, за варіантом, якому віддається більша перевага, - від приблизно 15 °C до приблизно 25 °C і за варіантом, якому віддається найбільша перевага, - при кімнатній температурі. За варіантом здійснення винаходу, якому віддають перевагу, полімерним фрагментом X є фрагмент поліетиленгліколю (PEG), у якому кінцева група ОН може факультативно бути модифікована, наприклад, С1-С5-алкільними або С1-С5-ацильними групами, за варіантом, якому віддається перевага, групами С1-алкіл, С2-алкіл або С3-алкіл або групами C1-ацил, С2-ацил або С3-ацил. За варіантом, якому віддається перевага, модифікований поліетиленгліколь є поліетиленгліколем, заміщеним у кінцевому положенні алкоксигрупою, за варіантом, якому віддається більша перевага, - метоксиполіетиленгліколем (mPEG). Полімер, який використовують згідно цього винаходу, має молекулярну вагу від приблизно 100 Да до приблизно 100000 Да, за варіантом, якому віддається перевага, від приблизно 200 Да до приблизно 50000 Да, і за варіантом, якому віддається більша перевага, від приблизно 500 Да до приблизно 10000 Да. Відповідно до одного з аспектів цього винаходу, якому віддають перевагу, полімером є поліетиленгліколь із коротким ланцюгом, за варіантом, якому віддається перевага, ним є PEG, заміщений у кінцевому положенні алкоксигрупою, наприклад, поліетиленгліколь, заміщений метоксигрупою, із молекулярною вагою від приблизно 200 Да до приблизно 1500 Да, за варіантом, якому віддається перевага, - від приблизно 400 Да до приблизно 1200 Да і за варіантом, якому віддається більша перевага, - від приблизно 550 Да до приблизно 1100 Да. За варіантом, якому віддають найбільшу перевагу, PEG або mPEG із коротким ланцюгом має середню молекулярну вагу від приблизно 550 Да до приблизно 1100 Да. Відповідно до другого аспекту цього винаходу, якому віддають перевагу, полімером є поліетиленгліколь із довгим ланцюгом, за варіантом, якому віддається перевага, ним є PEG, заміщений у кінцевому положенні алкоксигрупою, наприклад, поліетиленгліколь, заміщений метоксигрупою, із молекулярною вагою від приблизно 4000 Да до приблизно 6000 Да, за варіантом, якому віддається перевага, - від приблизно 4500 Да до приблизно 5500 Да. За варіантом здійснення цього винаходу, якому віддають найбільшу перевагу, PEG або mPEG із довгим ланцюгом має середню молекулярну вагу приблизно 2000 Да або приблизно 5000 Да. Термін "приблизно", вжитий вище для визначення числових значень і діапазонів молекулярної маси полімерного фрагмента за цим винаходом, означає, що вказані значення та/або межі діапазону можуть змінюватися на ±20 %, за варіантом, якому віддається перевага, - на ±10 %. В контексті цієї заявки, за винятком випадків, коли в цьому описі прямо передбачено інше, терміни мають значення, встановлені нижче. Термін "нижчий алкіл", коли його вживають окремо або в поєднанні з назвами інших груп, означає нижчу алкільну групу з ланцюгом лінійної або розгалуженої будови, який містить від 1 атома до 6 атомів вуглецю, за варіантом, якому віддається перевага, - від 1 атома до 5 атомів, за варіантом, якому віддається більша перевага, - від 1 атома до 4 атомів і за варіантом, якому віддається особлива перевага, - від 1 атома до 3 атомів або від 1 атома до 2 атомів вуглецю. До цих груп належать, зокрема, метил, етил, пропіл, ізопропіл, бутил, ізобутил, втор-бутил, третбутил, пентил, аміл, ізоаміл, неопентил, 1-етилпропіл, гексил тощо. Фрагмент нижчого алкілу у складі таких груп як "нижча алкоксигрупа", "нижчий алкоксикарбоніл", "нижчий алкіламінокарбоніл" "нижчий гідроксіалкіл" та "три-(нижчий алкіл)силіл", означає те саме, що й "нижчий алкіл", визначення якого наведено вище. Групи, об'єднані терміном "нижчий алкеніл", визначаються як групи С 2-С6-алкеніл, які мають ланцюг лінійної або розгалуженої будови і можуть знаходитися у Ζ або Ε формі. До таких груп належать вініл, пропеніл, бутеніл, ізобутеніл, 2-бутеніл, 1-пентеніл, (Z)-2-пентеніл, (Е)-2пентеніл, (Z)-4-метил-2-пентеніл, (Е)-4-метил-2-пентеніл, пентадієніл, наприклад, 1,3 або 2,4 5 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 60 пентадієніл, тощо. За варіантом, якому віддають більшу перевагу, групи С 2-С6-алкеніл є групами С2-С5-алкеніл, С2-С4-алкеніл, а за варіантом, якому віддається ще більша перевага, ними є групи С2-С3-алкеніл. Термін "нижчий алкініл" означає групи С2-С6-алкініл, які можуть мати ланцюг лінійної або розгалуженої будови, та охоплює етиніл, пропініл, 1-бутиніл, 2-бутиніл, 1-пентиніл, 2-пентиніл, 3-метил-1-пентиніл, 3-пентиніл, 1-гексиніл, 2-гексиніл, 3-гексиніл тощо. За варіантом, якому віддають більшу перевагу, до груп С2-С6-алкініл належать групи С2-С5-алкініл, С2-С4-алкініл, а за варіантом, якому віддається ще більша перевага, ними є групи С2-С3-алкініл. Термін "арил" означає групи С6-С14-арил, які містять від 6 кільцевих атомів до 14 кільцевих атомів вуглецю. Ці групи можуть бути моно-, бі-, а також трициклічними і складаються з конденсованих кілець. За варіантом, якому віддають перевагу, до арильних груп належать феніл, біфеніл, нафтил, антрил (антраценіл), фенантрил (фенантреніл) тощо. Арильний фрагмент у складі "арилкарбонільної" та "ариламінокарбонільної" груп означає те саме, що й у визначенні, наведеному вище. Групи, об'єднані терміном "гетероарил", можуть містити від 1 гетероатома до 3 гетероатомів, які обирають незалежно один від одного з-поміж таких елементів: азот, сірка або кисень, та відносяться до груп С3-С13-гетероарил. Ці групи можуть бути моно-, бі- або трициклічними. До груп С3-С13-гетероарил за цим винаходом належать гетероароматичні сполуки, а також насичені або частково насичені гетероциклічні групи. Ці гетероциклічні групи можуть бути моноциклічними, біциклічними та трициклічними. За варіантом, якому віддають перевагу, до 5або 6-членних гетероциклічних груп належать тієніл, фурил, піроліл, піридил, піраніл, морфолініл, піразиніл, метилпіроліл та піридазиніл. С3-С13-гетероарил може бути біциклічною гетероциклічною групою. Біциклічними групами, яким віддають перевагу, є бензофурил, бензотієніл, індоліл, імідазоліл, а також піримідиніл. Найбільшу перевагу віддають С 3-С13гетероарилам, до яких належать фурил та піридил. Термін "нижчий алкокси[група]" охоплює алкоксигрупи, які містять від 1 атома до 6 атомів вуглецю, за варіантом, якому віддається перевага, від 1 атома до 5 атомів, за варіантом, якому віддається перевага, - від 1 атома до 4 атомів і за варіантом, якому віддається особлива перевага, - від 1 атома до 3 атомів або від 1 атома до 2 атомів вуглецю, і можуть мати ланцюг лінійної або розгалуженої будови. До цих груп належать метокси-, етокси-, пропокси-, бутокси-, ізопропокси-, трет-бутокси-, пентокси-, гексоксигрупа тощо. Термін "ацил" охоплює нижчі алканоїли, які містять від 1 атома до 6 атомів вуглецю, за варіантом, якому віддається перевага, від 1 атома до 5 атомів, від 1 атома до 4 атомів, від 1 атома до 3 атомів або від 1 атома до 2 атомів вуглецю, і можуть мати ланцюг лінійної або розгалуженої будови. За варіантом, якому віддається перевага, до цих груп належать форміл, ацетил, пропіоніл, бутирил, ізобутирил, трет-бутирил, пентаноїл та гексаноїл. Ацильний фрагмент у складі "ацилоксигрупи" означає те саме, що й у визначенні, наведеному вище. Термін "галоген" охоплює фтор, хлор, бром, йод тощо. Термін "аралкіл" означає групу С7-С15-аралкіл, де алкільна група є заміщеною арилом. Алкільну групу та арил можна вибирати відповідно з-поміж груп С1-С6-алкіл та груп С6-С14-арил, як зазначено вище, при цьому загальна кількість атомів вуглецю становить від 7 до 15. За варіантом, якому віддають перевагу, групами С7-С15-аралкіл є бензил, фенілетил, фенілпропіл, фенілізопропіл, фенілбутил, дифенілметил, 1,1-дифенілетил, 1,2-дифенілетил. Аралкільний фрагмент "аралкілоксигруп" означає те саме, що й у визначенні, наведеному вище. Заміщені нижчі алкільні, алкенільні та алкінільні групи містять від 1 замісника до 3 замісників, які незалежно один від одного вибирають з-поміж таких груп як нижчий алкіл, гідроксил, нижча алкоксигрупа, карбоксил, нижчий алкоксикарбоніл, нітрогрупа, галоген, аміногрупа, моно- або ди-(нижча алкіламіногрупа), діоксолан, діоксан, дитіолан та дитіон. Нижчий алкільний замісник у складі заміщеної нижчої алкільної, алкенільної та алкінільної групи, а також нижчий алкільний фрагмент у складі замісників нижчої алкоксигрупи, нижчого алкоксикарбонілу, а також моно- або ди-(нижчої алкіламіногрупи), які входять до складу заміщеної нижчої алкільної, алкенільної та алкінільної групи, мають те саме значення, що й "нижчий алкіл", визначення якого наведено вище. Кожна з таких груп, як заміщений арил, заміщений гетероарил та заміщений аралкіл, містить від 1 замісника до 3 замісників, які незалежно одне від одного вибирають з-поміж таких груп як нижчий алкіл, гідроксил, нижча алкоксигрупа, карбоксил, нижчий алкоксикарбоніл, нітро-, аміногрупа, моно- або ди-(нижча алкіламіногрупа), а також галоген. Нижчий алкільний фрагмент у складі нижчого алкілу, нижчої алкоксигрупи, нижчого алкоксикарбонілу, а також моно- або ди(нижчої алкіламіногрупи), які належать до вказаних замісників, мають те саме значення, що й "нижчий алкіл", визначення якого наведено вище. 6 UA 103911 C2 5 5 10 15 20 25 30 35 40 45 50 55 60 6 Гетероциклічна група, утворена замісниками R та R у поєднанні з атомом азоту, охоплює піролідиніл, піперидиніл, піперидиногрупу, морфолініл, морфоліно-, тіоморфоліногрупу, Nметилпіперазил, індоліл, а також ізоіндоліл. 1 2 За варіантом, якому віддається перевага, R та R незалежно один від одного вибирають із 14 групи замісників, яка складається з водню, галогену, нітрогрупи, -СН2ОН, -(CH2)kR , 16 15 4 4 7 CH=CH(CH2)mR , -CС(CH2)nR , -CO(CH2)jR , де R є -SR , -СН2О-(заміщений або незаміщений нижчий алкіл) (де заміщений нижчий алкіл за варіантом, якому віддається перевага, являє 5 6 собою метоксиметил, метоксіетил або етоксиметил) або -NR R . 1 2 За варіантом, якому віддають перевагу, у наведених вище значеннях R та R , за варіантом, 14 якому віддається перевага, залишок R вибирають з-поміж таких груп як феніл, піридил, 15 15 15 імідазоліл, тіазоліл, тетразоліл, -COOR , -OR (де R за варіантом, якому віддається перевага, 7 7 вибирають з-поміж таких груп як водень, метил, етил, феніл або ацил), -SR (де R за варіантом, якому віддається перевага, вибирають з-поміж таких груп як заміщений або незаміщений 5 6 5 6 нижчий алкіл, 2-тіазолініл та піридил), та -NR R (де R та R за варіантом, якому віддається перевага, вибирають з-поміж таких груп як водень, метил, етил, феніл, карбамоїл та нижчий 16 алкіламінокарбоніл). Крім того, за варіантом, якому віддається перевага, залишок R вибирають з-поміж таких груп як водень, метил, етил, феніл, імідазол, тіазол, тетразол, 15 15 5 6 15 5 6 COOR , -OR та -NR R (де залишки R , R та R за варіантом, якому віддають перевагу, мають значення, які описані вище). За варіантом, якому віддають перевагу, у поданих вище 1 2 7 значеннях R та R залишок R за варіантом, якому віддається перевага, вибирають з групи замісників, яка складається з таких замісників як заміщений або незаміщений нижчий алкіл, заміщений або незаміщений феніл, піридил, піримідиніл, тіазол та тетразол. У свою чергу, k за варіантом, якому віддається перевага, дорівнює 2, 3 або 4, j за варіантом, якому віддається перевага, становить дорівнює 1 або 2, і m та n незалежно одне від одного за варіантом, якому віддається перевага, становлять дорівнює 0 або 1. 3 За варіантом, якому віддається перевага, R означає водень або ацетил, за варіантом, якому віддається більша перевага, - водень. Крім того, кожна з груп W 1 та W 2 за варіантом, якому віддається перевага, являє собою водень. За варіантом здійснення, якому віддають перевагу, цей винахід стосується сполуки K-252а, ковалентно приєднаної до полімерного фрагмента. За варіантом здійснення, якому віддають ще більшу перевагу, він стосується полімерних кон'югатів сполуки K-252а та їхніх похідних, де хімічна група, яка поєднує полімерний фрагмент зі сполукою K-252а або з похідним сполуки K252а, характеризується наявністю 5-членної циклічної структури оксазолідиндіону. Таким чином, за варіантом здійснення винаходу, якому віддають велику перевагу, полімерний кон'югат за 1 2 3 формулою (І) є сполукою, в якій R , R , R , W 1 та W 2 означають водень і X означає полімерний фрагмент. Відповідно до цього варіанта здійснення винаходу, якому віддають велику перевагу, полімерний фрагмент являє собою фрагмент поліетиленгликолю (PEG) або метоксиполіетиленгліколю (mPEG). За варіантом здійснення винаходу, якому віддають більшу перевагу, залишок поліетиленгликолю або метоксиполіетиленгліколю у складі сполуки за варіантом здійснення цього винаходу, якому віддають перевагу, є полімером PEG або mPEG із довгим ланцюгом і середньою молекулярною вагою приблизно 2000 Да або приблизно 5000 Да. Аналогічно, за варіантом, якому віддають перевагу, залишок PEG або mPEG являє собою поліетиленгліколь або метоксиполіетиленгліколь із коротким ланцюгом і середньою молекулярною вагою приблизно 550 Да або приблизно 1100 Да. Спосіб за цим винаходом факультативно включає стадію захисту захисною групою одного, декількох або всіх замісників R1, R2, R3, W 1 та W 2 у фрагменті індолокарбазолу сполуки K-252а або її похідного. Термін "захисні групи" у цьому контексті означає будь-яке похідне замісників R1, R2, R3, W 1 та W 2, відоме фахівцям у цій галузі, яке можна використовувати, за необхідності, для маскування груп R1, R2, R3, W 1 та W 2 під час синтезу і яке можна розщепити у відповідних умовах, в результаті чого замісники R1, R2, R3, W 1 та W 2 відновлюються у первинному вигляді, не завдаючи небажаного впливу на решту молекули. Зокрема, за необхідності, захисну групу вводять до одного, декількох або всіх замісників R1, R2, R3, W 1 та W 2 на час проведення реакції ковалентного сполучення, яка є предметом цього винаходу, для досягнення хемоселективності сполучення полімеру в положення 3 фрагмента індолокарбазолу в складі сполуки K-252а або її похідного. Після проведення реакції ковалентного сполучення одна або більша кількість захисних груп може бути видалена для відновлення у первинному вигляді функціональної групи відповідних замісників R1, R2, R3, W 1 та W 2 і одержання кон'югату індолокарбазолу за формулою (І). Відповідно до цього винаходу для цього може бути використана будь-яка прийнятна захисна група, відома фахівцям у цій галузі. Вибір прийнятної захисної групи, а також будь-яких 7 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 прийнятних засобів і умов для введення івідщеплення захисних груп замісників R1, R2, R3, W 1 та W 2 може здійснити фахівець, спираючись на свої знання з органічного синтезу. Засоби й умови введення і відщеплення захисних груп залежать від природи відповідних функціональних груп R1, R2, R3, W 1 та W 2. Захисні групи для захисту гідроксилу, аміногрупи та/або карбоксилу за варіантом, якому віддається перевага, вибирають з-поміж таких груп як ацетонід, етиліденметоксиметил, 2-метоксіетоксиметил, бензилоксиметил, тетрагідропіраніл, метил, етил, ізопропіл, трет-бутил, бензил, трифенілметил, трет-бутилдиметилсиліл, трифенілсиліл, метоксикарбоніл, трет-бутоксикарбоніл, бензилоксикарбоніл, флуоренілметоксикарбоніл, ацетил, бензоїл, толуолсульфоніл, диметоксибензил, нітрофенілоксикарбоніл, нітробензилоксикарбоніл, аліл, флуоренілметил, тетрагідрофураніл, фенацил, ацетол, феніл, триметилсиліл, піролідил, індоліл, гідразиногрупа та інших захисних груп, відомих фахівцям у цій галузі (дивись, наприклад, Greene T.W., et al., Protective Groups in Organic Synthesis, 4th ed., John Wiley and Son, New York, NY (2007)). Реагенти та умови реакцій введення та зняття захисту вибирають, зокрема, на підставі їхньої здатності забезпечувати селективність приєднання та видалення захисної групи, не завдаючи небажаного впливу на решту молекули сполуки. Прийнятні умови та реагенти відомі фахівцям у цій галузі. Відповідно до цього винаходу сполуки за формулою (І) можна також одержувати у вигляді фармацевтично прийнятних солей неорганічних кислот, зокрема, хлористоводневої, йодистоводневої, бромистоводневої, ортофосфорної, метафосфорної, азотної кислоти, сірчаної кислоти, а також у вигляді солей органічних кислот, зокрема винної, оцтової, лимонної, яблучної, бензойної, гліколевої, глюконової, бурштинової, арилсульфонової (наприклад, nтолуолсульфонової та бензолсульфонової кислот), фосфонових кислот, малонової і таке інше. Кислоти, придатні до утворення фармацевтично прийнятних солей, відомі фахівцям в цій галузі. Крім того, фармацевтично прийнятні солі сполук за формулою (І) можуть бути утворені фармацевтично прийнятними катіонами. Фармацевтично прийнятні катіони відомі фахівцю в цій + + + 2+ галузі і охоплюють катіони лужних металів (Li , Na , K ), катіони лужноземельних металів (Mg , 2+ 2+ Ca , Ва ), катіони амонію та органічні катіони, зокрема катіони четвертинного амонію. Ще одним аспектом цього винаходу є нові полімерні кон'югати сполуки K-252а та її похідних, де хімічна група, яка приєднує полімерний фрагмент до сполуки K-252а або до похідного сполуки K-252а, характеризується наявністю 5-членної циклічної структури оксазолідиндіону. Ці нові полімерні кон'югати одержують новим способом синтезу, розкритим в цьому описі. Зокрема, ще одним аспектом винаходу в свою чергу є полімерний кон'югат індолокарбазольної сполуки за формулою (І) 1 2 3 де R , R , R , W 1 та W 2, а також полімерний фрагмент X відповідають детальному опису, який наведено вище, або його фармацевтично прийнятна сіль. За варіантом, якому віддають найбільшу перевагу, винахід стосується нового полімерного 1 2 3 кон'югату за формулою (І), де R , R , R , W 1 та W 2 означають водень, і полімерний фрагмент X являє собою поліетиленгліколь (PEG) або PEG, заміщений у кінцевому положенні алкоксигрупою, наприклад, за варіантом, якому віддається перевага, метоксиполіетиленгліколь (mPEG). Ця сполука відповідає полімерному кон'югату сполуки K-252а за цим винаходом. За варіантом, якому віддається перевага, полімерний фрагмент являє собою поліетиленгліколь із довгим ланцюгом, за варіантом, якому віддається ще більша перевага, ним є PEG, заміщений у кінцевому положенні алкоксигрупою, наприклад, метоксиполіетиленгліколь (mPEG) із середньою молекулярною вагою приблизно 2000 Да або приблизно 5000 Да. Аналогічно, за варіантом, якому віддається перевага, полімерний фрагмент являє собою поліетиленгліколь із коротким ланцюгом, за варіантом, якому віддається ще більша перевага, ним є PEG, заміщений у кінцевому положенні алкоксигрупою, наприклад, метоксиполіетиленгліколь (mPEG) із середньою молекулярною вагою приблизно 550 Да або приблизно 1100 Да. 8 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 Авторами цього винаходу несподівано з'ясовано, що порівняно з індолокарбазольними сполуками і, зокрема, порівняно із самим K-252а або його похідними, що не містять фрагмента полімеру, відповідні сполуки, які ковалентно зв'язані з полімером і описуються формулою (І), виявляють кращі фармакокінетичні і токсикологічні характеристики завдяки збільшеній розчинності, що забезпечує поліпшення біодоступності терапевтично і біологічно активної сполуки. Крім того, авторами цього винаходу було несподівано з'ясовано, що полімерні кон'юговані індолокарбазольні сполуки за формулою (І) демонструють обмежену системну абсорбцію при місцевому застосуванні через збільшений молекулярний розмір та амфіпатичність, завдяки чому підвищується терапевтична ефективність при місцевому застосуванні і біологічна ефективність, а також зменшується системна токсичність та/або побічні ефекти при місцевому застосуванні. Крім того, авторами цього винаходу несподівано було з'ясовано, що індолокарбазольні кон'югати за формулою (І) виявляють значно підвищену селективність інгібувальної активності щодо тирозинкінази TrkA порівняно з неселективною активністю інгібування кіназ власне індолокарбазольних сполук і, зокрема, сполуки K-252а або його похідних, які не містять фрагмента полімеру. Таким чином, ковалентне приєднання індолокарбазольної сполуки і, зокрема, сполуки K-252а до молекули полімеру за цим винаходом дає змогу одержати активну речовину, селективну по відношенню до її терапевтичної мішені, і, як наслідок, зі зменшеними небажаними побічними ефектами. Отже, ще один аспект цього винаходу полягає у використанні сполук за формулою (І) як активних речовин у лікарському засобі. За аспектом цього винаходу, якому віддають перевагу, сполуки за формулою (І) використовуються як активні речовини у лікарському засобі для системного застосування та лікування. За аспектом цього винаходу, якому також віддають перевагу, цей винахід стосується використання сполук за формулою (І) як активних речовин у лікарському засобі для місцевого застосування. Зокрема, сполуки, ковалентно приєднані до полімеру, за цим винаходом використовуються як активні речовини у лікарському засобі, придатному для запобігання, часткового полегшення симптомів та лікування патологій, пов'язаних із HMGB1. Патологія, пов'язана з HMGB1, визначається як такий стан пацієнта, при якому у біологічних рідинах і тканинах спостерігається підвищена концентрація ядерного білка HMGB1 та/або гомологічних білків у ацетильованій або неацетильованій формі, порівняно з концентрацією в організмі пацієнтів у нормальному стані, коли виявлення зазначених ядерних білків ряду HMGB1 є практично неможливим. Позаклітинні білки ряду HMGB1 виступають як сильнодіючі хемотаксичні прозапальні хемокіни. Отже, патології, пов'язані з HMGB1, є патологіями з міцною збудливою базою і являють собою патології, що виникають в результаті стимуляції цитокіну, такого як TNF- (фактор некрозу пухлин ), IL-1, IL-6 тощо, або в результаті токсичності, наприклад, інтоксикації, інфекції, опіку тощо. Зокрема, високий вміст білка HMGB1 та гомологічних білків був виявлений і підданий кількісному оцінюванню в плазмі крові хворих на сепсис, у плазмі та синовіальній рідині хворих на ревматоїдний артрит, у головному мозку хворих на хворобу Альцгеймера, у плазмі крові та тканинах хворих на меланому, у плазмі крові хворих на системний червоний вовчак, у атеросклеротичних бляшках хворих на атеросклероз тощо. Свідчення наявності та кількісну оцінку білка HMGB1 та/або гомологічних білків у біологічних рідинах і тканинах можна одержати із застосуванням звичайних діагностичних засобів, відомих фахівцю в цій галузі, до яких належить, наприклад, метод імуносорбентного ферментного аналізу в твердій фазі (ELISA) тощо. Таким чином, ціла низка захворювань характеризується відповідною присутністю позаклітинного HMGB1, до цих захворювань, зокрема, належать, але без обмеження ними, запальні захворювання, стеноз, рестеноз, атеросклероз, ревматоїдний артрит, автоімунні захворювання, пухлини, інфекційні захворювання, сепсис, гостре запальне ушкодження легенів, червоний вовчак, нейродегенеративні захворювання, захворювання центральної і периферичної нервової системи, а також розсіяний склероз. За варіантом здійснення винаходу, якому віддають особливу перевагу, кон'юговані полімерні сполуки за формулою (І) застосовують для запобігання, часткового полегшення симптомів та лікування серцевосудинних захворювань, зокрема атеросклерозу та/або рестенозу, які виникають під час або після пластики судин. За варіантом, якому віддається більша перевага, лікарський засіб застосовують для блокування, сповільнення та/або порушення регенерації тканин при рестенозі під час та після пластики судин. За аспектом винаходу, якому віддають особливу перевагу, кон'юговані полімерні сполуки за формулою (І) ефективні при використанні як активна речовина у лікарському засобі для 9 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 профілактики, часткового полегшення симптомів та лікування неврологічних розладів, нейропатій та нейродегенеративних розладів центральної і периферичної нервової системи. Крім того, авторами цього винаходу було показано, що нові полімерні кон'югати при системному лікуванні здатні зменшувати та/або інгібувати секрецію цитокінів у плазмі крові. Таким чином, полімерні кон'югати використовують як активні речовини у лікарському засобі для системного введення, призначеному для запобігання, часткового полегшення симптомів та/або лікування патологій, пов'язаних зі збільшенням секреції цитокінів плазми. Ці патології за варіантом, якому віддається перевага, є патологіями значною мірою пов'язаними із секрецією TNF-, гама-інтерферону (IFN-), моноцитарного хемотаксичного білка (МСР-1), запалювального білка макрофагів (МІР-1) та/або хемокіну, що продукується Т-клітинами при активації (RANTES). Зокрема, в контексті цього винаходу, до патологій, які пов'язані з підвищеною секрецією цитокінів у плазмі, належать, але без обмеження ними, запальні захворювання, автоімунні захворювання, синдром системної запалювальної реакції, реперфузійне ушкодження після трансплантації органів, серцево-судинні ураження, акушерські і гінекологічні захворювання, інфекційні захворювання, алергічні та атопічні захворювання, солідні та рідинні пухлинні патології, синдроми відторгнення трансплантата, природжені захворювання, дерматологічні захворювання, неврологічні захворювання, кахексія, ниркова недостатність, стани ятрогенної інтоксикації, метаболічні та ідеопатичні захворювання, а також офтальмологічні захворювання. За варіантом здійснення винаходу, якому віддається найбільша перевага, сполуки за цим винаходом застосовують як активні речовини у лікарському засобі для системного введення, призначеному для запобігання, часткового полегшення симптомів та/або лікування синдрому Бехчета, синдрому Гужеро-Шегрена, васкуліту, увеїту та ретинопатій. За ще одним конкретним аспектом цього винаходу доцільно, щоб полімерні кон'югати за цим винаходом використовувались як активні речовини у лікарському засобі для місцевого застосування, призначеному для запобігання, часткового полегшення симптомів та/або лікування патологій шкіри. Авторами цього винаходу було показано, що полімерні кон'югати, описані в цій заявці, мають великі переваги при їхньому використанні як лікарський засіб для місцевого застосування, оскільки вони не чинять ані шкідливої або токсичної дії (наприклад, подразнення) при нанесенні на шкіру, ані фототоксичної дії (наприклад, фотомутагенної дії, фототоксичності або фотосенсибілізації) (як це показано у дослідженнях, які описані в наведених нижче прикладах). До патологій шкіри, лікуванню яких віддають перевагу в контексті цього винаходу, належать патології, які характеризуються гіперпроліферацією кератиноцитів, такі як псоріаз, атопічний дерматит, хронічна екзема, вугрі, червоний волосяний лишай, опікові рубці (келоїди), гіпертрофічні рубці, а також пухлини шкіри, такі як кератоакантома, плоскоклітинний рак, базальноклітинна карцинома. За варіантом здійснення, якому віддають більшу перевагу, сполуки за цим винаходом використовуються як активні речовини у лікарському засобі для місцевого застосування, придатному для запобігання, часткового полегшення симптомів та/або лікування псоріазу. Завдяки підвищеній селективності сполук за цим винаходом як інгібіторів тропоміозинрецепторної кінази A (TrkA) ще одним аспектом цього винаходу є використання зазначених кон'югатів для запобігання, часткового полегшення симптомів та/або лікування патологій, у механізмі розвитку яких вирішальну роль відіграє TrkA. У цьому контексті, за варіантом здійснення винаходу, якому віддається велика перевага, кон'юговані K-252а полімерні сполуки (формули (І), формули(II) та/або формули(III)), застосовуються як активні речовини у лікарському засобі для профілактики, часткового полегшення симптомів та лікування гіпералгезії та больових синдромів, пов'язаних із фактором росту нервової тканини (NGF). Один з подальших аспектів цього винаходу полягає у застосуванні сполуки за формулою (І), визначеної вище, факультативно разом із фармацевтично прийнятними носіями, допоміжними речовинами, розріджувачами та/або функціональними домішками, для виготовлення лікарського засобу для профілактики, часткового полегшення симптомів та/або лікування патологій відповідно до опису, який наведено вище. Сполуки за формулою (І) або їхні фармацевтично прийнятні солі можуть бути введені окремо або у вигляді різноманітних фармацевтичних композицій, зважаючи на їхню фармакологічну активність та мету введення. Ще одним аспектом цього винаходу є фармацевтична композиція, яка містить ефективну кількість щонайменше однієї сполуки за формулою (І), факультативно разом із фармацевтично прийнятними носіями, допоміжними речовинами, розріджувачами та/або функціональними домішками. Фармацевтичні носії, 10 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 60 допоміжні речовини, розріджувачі та/або домішки відомі фахівцям у цій галузі і можуть застосовуватись у фармацевтичній композиції, яка містить сполуку за цим винаходом. Сполуки за цим винаходом можуть бути використані як єдина активна речовина у фармацевтичній композиції. Альтернативно, сполуки за формулою (І) можуть бути використані разом з однією або декількома додатковими активними речовинами, наприклад, іншими активними фармацевтичними речовинами, при лікуванні визначених вище патологій. Зокрема, полімерні кон'югати за цим винаходом можуть бути використані в поєднанні із щонайменше одним протизапальним засобом стероїдного характеру та/або однією додатковою активною речовиною, придатною для інгібування одного з початкових медіаторів каскаду прозапального цитокіну, наприклад, антагоністом або інгібітором одного із цитокінів, який вибирають з групи, яка складається зі сполук: TNF, IL-1, IL-1β, IL-Ra, IL-8, ΜΙΡ-1, MIF-1β, ΜΙΡ2, MIF та IL-6. Зокрема, доречні протизапальні засоби вибирають з-поміж таких речовин: алкілометазону дипропіонат, амцинонід, беклометазону дипропіонат, бетаметазон, бетаметазону бензоат, бетаметазону дипропіонат, бетаметазон-натрію фосфат, бетаметазоннатрію фосфат-ацетат, бетаметазону валерат, клобетазолу бутират, клобетазолу пропіонат, клокортолону півалат, кортизол (гідрокортизон), кортизолу (гідрокортизону) ацетат, кортизолу (гідрокортизону) бутират, кортизолу (гідрокортизону) ципіонат, кортизолу (гідрокортизону)натрію фосфат, кортизолу (гідрокортизону)-натрію сукцинат, кортизолу (гідрокортизону) валерат, кортизон ацетат, дезонід, дезоксиметазон, дексаметазон, дексаметазону ацетат, дексаметазон-натрію фосфат, дифлоразону діацетат, дифлукортолону валерат, флудрокортизону ацетат, флудроксикортид, флуметазону півалат, флунізолід, флуоцинолону ацетонід, флуоцинонід, флуокортолон, флуорометолон, флурандренолід, флутіказону пропіонат, галцинонід, галобетазолу пропіонат, медризон, метилпреднізолон, метилпреднізолону ацетат, метилпреднізолон-натрію сукцинат, мометазону фуроат, параметазону ацетат, преднізолон, преднізолону ацетат, преднізолон-натрію фосфат, преднізолону тебутат, преднізон, триамцинолон, триамцинолону ацетат, триамцинолону ацетонід, триамцинолону діацетат, триамцинолону гексацетонід. Доречні антагоністи або інгібітори цитокіну вибирають з-поміж таких речовин як інфіксимаб, етанерцепт або адалімумаб. Крім того, активним речовинами, які можуть бути використані в поєднанні з полімерними сполуками за цим винаходом, є, наприклад, антагоністи та/або інгібітори рецептора кінцевих продуктів глибокого глікозування (RAGE), антагоністи та/або інгібітори HMGB1, антагоністи та/або інгібітори взаємодії Toll-подібного рецептора (рецептора Т-клітин, TCR) з HMGB1, функціональна N-термінальна лектиноподібна ділянка (D1) тромбомодуліну та/або синтетична двониткова нуклеїнова кислота або молекула аналога нуклеїнової кислоти вигнутої форми, які описані у WO 2006/002971, включеній в цей опис шляхом посилання. Фармацевтичну композицію за цим винаходом вводять до організму будь-яким з прийнятних шляхів, відомих кожному фахівцю в цій галузі, наприклад, лікарю. Зокрема, фармацевтична композиція за цим винаходом може бути введена до організму шляхом ін'єкції або інфузії, зокрема шляхом внутрішньовенної, внутрішньом'язової, трансслизової, підшкірної або внутрішньоочеревинної ін'єкції або інфузії, та/або шляхом перорального, місцевого, нашкірного, назального, інгаляційного або аерозольного та/або ректального застосування тощо. Введення до організму може мати локальний або системний характер. За варіантом, якому віддається перевага, введення сполуки та фармацевтичної композиції за цим винаходом може бути реалізоване парентеральним введенням, зокрема у формі рідких розчинів або суспензій, або пероральним введенням, зокрема, у формі таблеток або пігулок, або інтраназальним введенням, зокрема у формі порошків, носових крапель або аерозолів, або дермально, наприклад, у формі мазей, кремів, олій, ліпосом або трансдермальних пластирів. За одним з аспектів цього винаходу фармацевтичну композицію вводять системно. Зокрема, полімерні кон'югати можуть бути введені до організму шляхом ін'єкції або інфузії, зокрема, шляхом внутрішньовенної, внутрішньом'язової, трансслизової, підшкірної або внутрішньоочеревинної ін'єкції або інфузії та/або шляхом перорального введення. За ще одним варіантом здійснення винаходу, якому віддається найбільша перевага, фармацевтичну композицію за цим винаходом вводять до організму шляхом місцевого застосування, зокрема, шляхом дермального застосуванням. У випадку дермального застосування введення до організму сполук за цим винаходом може бути реалізоване у формі ліпосом. У ще одному варіанті здійснення винаходу, якому віддається найбільша перевага, фармацевтичну композицію вводять до організму зі стану, коли вона оборотно іммобілізована на поверхні пристрою медичного призначення, зокрема, шляхом зв'язування, нанесення покриття та/або закріплення сполуки та композиції за цим винаходом з поверхнею або до 11 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 поверхні пристрою медичного призначення, такого як (але без обмеження ними) стенти, катетери, хірургічні інструменти, канюлі, серцеві клапани або судинні протези. Після приведення пристрою медичного призначення в контакт із рідиною або тканиною тіла відбувається вивільнення оборотно іммобілізованих сполук. Таким чином, ці покриті пристрої медичного призначення виконують функцію пристроїв для доставки, що вивільнюють лікарський засіб, отже існує можливість керування кінетикою доставки лікарського засобу, наприклад, негайне вивільнення або контрольована, відстрочена або тривала (пролонгована) доставка препарату. Технолога нанесення препарату на поверхню пристрою медичного призначення добре відомі фахівцям у цій галузі. Фармацевтична композиція за цим винаходом може бути застосована для діагностування або лікування. При використанні для діагностування сполука за формулою (І) може знаходитись у міченій формі, наприклад, у формі, яка містить будь-який ізотоп, наприклад, радіоактивний ізотоп або ізотоп, який можна виявити за допомогою ядерного магнітного резонансу. За варіантом, якому віддають перевагу, у разі місцевого застосування, терапевтичним застосуванням є запобігання, часткове полегшення симптомів і лікування псоріазу та дерматиту, в той час як при системному застосуванні, таким є запобігання, часткове полегшення симптомів і лікування процесів регенерації сполучної тканини при рестенозі. Концентрація сполук за цим винаходом у фармацевтичній композиції може бути різною. Концентрація залежить від таких чинників як загальна доза лікарського засобу, яка має бути введена до організму, хімічні властивості (наприклад, гідрофобність) вживаних сполук, шлях введення, вік, маса тіла пацієнта, а також симптоми захворювання, на яке страждає пацієнт. Сполуки за цим винаходом зазвичай надають у водному фізіологічному буферному розчині із вмістом приблизно від 0,1 % до 10 % сполуки (маса до об'єму розчину), призначеному для парентерального введення. Типові діапазони дозування становлять від приблизно 1 мкг/кг ваги тіла на добу до приблизно 1 г/кг ваги тіла на добу, за варіантом, якому віддають перевагу, приблизно від 0,01 мг/кг ваги тіла на добу до 100 мг/кг ваги тіла на добу, та за варіантом, якому віддається перевага, приблизно від 0,1 мг/кг ваги тіла на добу до 20 мг/кг ваги тіла на добу, із вживанням від одного до чотирьох разів на добу. За варіантом, якому віддають перевагу, доза лікарського засобу, яка має бути введена до організму, як правило, залежить від змінних чинників, таких як тип і ступінь розвитку захворювання або розладу, загальний стан здоров'я певного пацієнта, відносна біологічна ефективність вибраної сполуки, лікарська форма, застосовувані наповнювачі та шлях введення. Вдосконалений метод синтезу за цим винаходом буде роз'яснений нижче за допомогою фігур і прикладів, які, втім, не повинні розглядатися як такі, що накладають обмеження на обсяг цього винаходу. Фіг. 1 ілюструє варіант здійснення способу за цим винаходом, якому віддають перевагу. Індолокарбазольну сполуку K-252а вводять у реакцію з -метокси--(1Н)-імідазолкарбоксамідополіетиленгліколем (mPEG-NH-CO-Im), маючи на меті одержання кон'югату сполуки K-252а за цим винаходом з метоксиполіетиленгліколем. У складі цієї сполуки, яка являє собою варіант здійснення сполуки за цим винаходом, якому віддають перевагу, залишок метоксиполіетиленгліколю ковалентно приєднаний до активної сполуки K-252а через 5-атомну циклічну структуру оксазолідиндіону. 1 Фіг. 2 ілюструє спектр H-ЯМР активованого полімеру mPEG-NH-CO-Im, розчиненого у DMSO-d6, у магнітному полі частотою 400 МГц. Фіг. 3 ілюструє мас-спектр із йонізацією електророзпиленням (ESI-MS) сполуки mPEG-NHCO-Im у діапазоні співвідношень m/z 500-1400 з використанням йонної пастки та йонізації електророзпиленням із прямою інфузією проби. 1 Фіг. 4 ілюструє спектр H-ЯМР полімерного кон'югату сполуки K-252а, поданого на Фіг. 1, розчиненого у DMSO-d6, при 400 МГц. 13 Фіг. 5 ілюструє спектр С-ЯМР полімерного кон'югату сполуки K-252а, поданого на Фіг. 1, розчиненого у DMSO-d6, при 400 МГц. Фіг. 6 ілюструє спектр ESI-MS полімерного кон'югату сполуки K-252а, поданого на Фіг. 1, у діапазоні співвідношень m/z 500-1400 з використанням йонної пастки та йонізації електророзпиленням із прямою інфузією проби. Фіг. 7 ілюструє криву інгібування полімерного кон'югату сполуки K-252а, поданого на Фіг. 1, залежно від концентрації TrkA. Приклади Приклад 1. Синтез -метокси--(1Н)-імідазолкарбоксамід-поліетиленгліколю (mPEG-NH-COIm) 12 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 У круглодонній колбі місткістю 500 мл розчиняли 35,0 г mPEG-NH2 (м.в. 1892) (вміст 96 %, 17,76 ммоль) у 85 мл дихлорметану в атмосфері азоту. Розчинник випарювали при зниженому тиску, і сполуку, що залишилася, висушували за допомогою механічного насоса протягом 2 год. Потім залишок розчиняли у 150 мл дихлорметану в атмосфері азоту, і одержаний розчин переносили у тригорлу круглодонну колбу місткістю 2 л. До розчину при кімнатній температурі додавали 4,80 г 1,1-карбонілдіімідазолу (вміст 90 %, 26,64 ммоль). Суміш перемішували при кімнатній температурі в атмосфері азоту, і контролювали із застосуванням хроматографії в тонкому шарі (ХТШ) (елюент - СН2СІ2/МеОН, 90:10). Хроматограму ТШ обробляли розчином нінгідрину для виявлення плями, яка вказує на присутність первинної аміногрупи (фіолетове забарвлення). Реакція завершується за 2 год. Суміш охолоджували до 0 °C, і осаджували твердий продукт, повільно додаючи діетиловий ефір (700 мл протягом 60 хв) при енергійному перемішуванні. Суміш перемішували протягом 30 хв при 0 °C, і додавали ще 300 мл діетилового ефіру. Продукт відфільтровували на фільтрувальній лійці з пористим скляним диском, промивали 100 мл діетилового ефіру, і висушували у вакуумі. Одержували 34,0 г сухої твердої речовини білого кольору (вихід 94 %). 1 Будова і хімічна ідентичність продукту була підтверджена спектрами H-ЯМР та ESI-MS. 1 -1 H-ЯМР (DMSO-d6) δ (млн ): 8,24 (m, 1H, CH), 7,69 (m, 1H, CH), 7,27 (s, 1H, NH), 7,02 (s, 1H, CH), 3,55 (m, CH2 PEG), 3,40 (m, 2H, CH2NH), 3,22 (s, 3H, OCH3). ESI-MS (кластер +2) … 944,4, 966,4, 988,5, 1010,5, 1032,5 … (зростання маси +47 відносно кластеру кластера +2 сполуки mPEG-NH2 …897,4, 919,4, 941,5, 963,5, 985,5). Приклад 2. Реакція ковалентного сполучення структури K-252а з полімером для одержання оксазолідиндіонового кон'югату Схема процесу наведена на фіг. 1. У круглодонній колбі місткістю 500 мл розчиняли 33,0 г mPEG-NH-CO-Im (16,00 ммоль) у 85 мл дихлорметану в атмосфері азоту. Розчинник випарювали при зниженому тиску, і сполуку, що залишилася, висушували із застосуванням механічного насоса протягом 2 год. У реакторі місткістю 2 л, оснащеному кріостатом із терморегулятором, механічною мішалкою і термометром, розчиняли 6,21 г сполуки K-252а (вміст 98 %, 13,29 ммоль) у 1,85 л дихлорметану в атмосфері азоту, і розчин охолоджували до 0 °C. Підтримуючи атмосферу азоту, додавали 0,53 г гідриду натрію (вміст 60 %, 13,29 ммоль), і суміш перемішували протягом 10 хв. Висушений mPEG-NH-CO-Im розчиняли у 90 мл дихлорметану, і розчин додавали при 0 °C в атмосфері азоту до суміші сполук K-252а та NaH у дихлорметані. Суміш перемішували протягом 30 хв при 0 °C, потім нагрівали до 25 °C, і витримували при перемішуванні при цій температурі протягом 10 хв. Реакційну суміш піддавали аналізу із застосуванням рідинної хроматографії високої ефективності (РХВЕ) з метою оцінювання глибини перетворення сполуки K-252а, а також співвідношення сполук у складі суміші. Після витримування протягом 10 хв при 25 °C до реакційної суміші додавали 3,60 г 1,1-карбонілдіімідазолу (вміст 90 %, 19,93 ммоль), і одержаний розчин перемішували при 25 °C протягом 30 хв. Реакційну суміш піддавали аналізу із застосуванням РХВЕ з метою контролю глибини перетворення амідвмісного напівпродукту (mPEG ковалентно приєднаний через карбоксильну групу у положенні 9 сполуки K-252а), у бажаний оксазолідиндіоновий кон'югат. Реакційну суміш нейтралізували мурашиною кислотою (вміст 98 %) до остаточного рН 6 (приблизно 2 мл, 53 ммоль). Розчинник випарювали при зниженому тиску при 25 °C, і одержували 44,0 г світло-жовтого неочищеного продукту. Чистота кон'югату у складі неочищеного продукту за даними РХВЕ перевищувала 90 %. Вміст бажаного продукту у складі неочищеного продукту становив приблизно 65-70 % (мас). Приклад 3. Очищення оксазолідиндіонового кон'югату сполуки K-252а флешхроматографією з оберненою фазою Неочищену суміш, одержану на стадії ковалентного сполучення (приклад 2), очищали флеш-хроматографією з оберненою фазою. Використовували систему Biotage Horizon із встановленим картриджем Flash 65іМ KР-С18. Виробничу партію розділили на 15 аліквот по 3,0 г у кожній. Аліквоти очищали окремо одну від одної. 13 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 Колонку С18 передусім зрівноважували, використовуючи для цього 200 мл розчинника із застосуванням такого градієнта: від 100 % ацетонітрилу до суміші ацетонітрил/вода (40:60), після чого 200 мл суміші ацетонітрил/5 ммоль/л розчин форміату амонію з рН 3,5 (40:60) у ізократичних умовах. Розчиняли 3,0 г неочищеного продукту у 3,0 мл N,N-диметилформаміду, і розчин вводили у колонку. Очищення здійснювали шляхом ізократичного елюювання сумішшю ацетонітрил/5 ммоль/л розчин форміату амонію з рН 3,5 (40:60). Зібрані окремі фракції піддавали аналізу із застосуванням РХВЕ, і чисті фракції згодом об'єднували. Розчинник випарювали при зниженому тиску при 25 °C, і одержували близько 2 г чистого вологого продукту. Кожну з аліквот очищали за описаною вище методикою; насамкінець кожну із фракцій чистого вологого продукту розчиняли у 10 мл дихлорметану, після чого об'єднували. Розчин висушували сульфатом натрію. Тверду речовину відфільтровували, і розчинник випарювали при зниженому тиску при 25 °C. Одержаний твердий продукт піддавали аналізу із застосуванням спектроскопії ЯМР; при цьому було виявлено близько 1 г-екв. форміату амонію. Для видалення цієї солі продукт розчиняли у 50 мл дихлорметану, і елюювали через шар силікагелю, зволоженого дихлорметаном. Продукт добували елююванням 700 мл суміші розчинників дихлорметан/метанол (9:1). Порції елюату об'єднували, і розчинник випарювали при зниженому тиску при 25 °C. Продукт знову розчиняли у 80 мл дихлорметану, і осаджували при 0 °C і енергійному перемішуванні, додаючи 500 мл діетилового ефіру, в результаті чого утворювався твердий продукт. Продукт відфільтровували на фільтрувальній лійці з пористим скляним диском, промивали 100 мл діетилового ефіру, і висушували у вакуумі протягом 16 год. Одержували 16,0 г порошку світло-жовтого кольору із загальним виходом (на стадіях ковалентного сполучення + очищення) 51 %. Будова і хімічна ідентичність продукту підтверджена спектрами ЯМР, ESI-MS, а також методом РХВЕ. Кількісний склад визначений за допомогою ЯМР із застосуванням внутрішнього стандарту; він відповідав вмісту основної речовини 101 % (мас). 1 -1 H-ЯМР (DMSO-d6) δ (млн ): 9,25 (d, 1H, CH), 8,70 (s, 1H, NH), 8,11 (d, 1H, CH), 7,95 (d, 1H, CH), 7,70 (d, 1H, CH), 7,51 (m, 2H, CH), 7,42 (m, 2H, CH), 7,31 (m, 1H, CH), 5,05 (s, 1H, NHCH2), 3,90-3,40 (m, CH2 PEG), 3,25 (s, 3H, OCH3), 2,35 (m, 4H, CH3+1H CH2). 13 -1 С-ЯМР (DMSO-d6) δ (млн ): 172,3, 172,0, 153,7, 139,4, 137,5, 133,5, 128,1, 126,2, 124,9, 124,0, 123,2, 122,3, 121,6, 120,8, 120,4, 117,0, 115,4, 113,5, 109,9, 98,4, 90,6, 85,3, 71,8, 70,0, 68,9, 66,3, 58,5, 45,9, 40,0, 23,16. ESI-MS (кластер +2) … 1128,2, 1150,3, 1172,3, 1194,3, 1216,3 … (зростання маси +230,8 відносно кластера +2 сполуки mPEG-NH2 …897,4, 919,4, 941,5, 963,5, 985,5). Точна молекулярна маса: розбіжність у точних масах, одержаних із реального і -1 теоретичного мас-спектрів, відповідала 2 млн . Отже, продукт реакції ковалентного сполучення з полімером мав чистоту щонайменше приблизно 98 %. Приклад 4. Очищення оксазолідиндіонового кон'югату сполуки K-252а флешхроматографією з нормальною фазою Був виконаний синтез за способом, наведеним вище у прикладі 1 та прикладі 2; в ході цього синтезу були одержані 21,7 г неочищеного продукту. Неочищену суміш, одержану на зазначеній стадії ковалентного сполучення з полімером, очищали флеш-хроматографією з нормальною фазою із застосуванням системи Biotage Horizon, спорядженої картриджем SNAP (розмір 71 × 168 мм), заповненим 340 г силікагелю KPSIL. Неочищений продукт ділили на дві аліквоти, які очищали окремо один раз кожну (маса аліквот становила відповідно 10,86 г та 10,8 г від загальної маси неочищеного продукту). Картридж SNAP зрівноважували, використовуючи для цього 940 мл суміші дихлорметан/метанол (96:4 за об'ємом). Об'ємна витрата становила 65 мл/хв. Введення проби здійснювали із застосуванням патрона для картриджа SNAP, заздалегідь заповненого адсорбентом (34 г), шляхом розчинення неочищеного матеріалу у 10 мл дихлорметану, нанесення розчину на патрон і заправлення патрона у картридж SNAP. Елюювання картриджа SNAP здійснювали при об'ємній витраті 65 мл/хв, використовуючи для цього: - 705 мл суміші дихлорметан/метанол (96:4 за об'ємом); - 1881 мл суміші дихлорметан/метанол (93:7 за об'ємом); - 942 мл суміші дихлорметан/метанол (85:15 за об'ємом). Перші 999 мл елюату викидали, після чого збирали елюат окремими фракціями по 111 мл. 14 UA 103911 C2 5 10 15 20 25 30 35 40 45 50 55 Зібрані окремі фракції піддавали аналізу методом РХВЕ, і об'єднували фракції, які містять кон'югат із чистотою >98 % (чисті фракції). Аналогічно очищали аліквоту, яка залишилася, неочищеного продукту після стадії ковалентного сполучення (10,8 г). Фракції, які були відібрані після очищення двох аліквот неочищеної суміші, об'єднували, розчинник випарювали при зниженому тиску при 25 °C досуха, одержуючи 8,11 г кон'югату, який знов розчиняли у 29 мл дихлорметану, охолоджували до 2 °C, і осаджували при енергійному перемішуванні, додаючи 150 мл діетилового ефіру протягом 15 хв. Суміш перемішували при 2 °C протягом 15 хв, потім додавали 225 мл діетилового ефіру. Осаджену тверду речовину відділяли фільтрацією на фільтрувальній лійці з пористим скляним диском (G4), і сушили у вакуумі при 25 °C протягом 16 год., одержуючи 6,95 г об'єкта дослідження у вигляді твердої речовини, забарвленої у колір від чисто білого до білого з жовтим відтінком. Чистота за даними аналізу методом РХВЕ становила 99 %. Приклад 5. Спосіб синтезу оксазолідиндіонового кон'югату сполуки K-252а 1) Синтез MeO-PEG-NH-CO-Im Сполуку MeO-PEG-NH2 (м.в. 1892, 8,06 г) розчиняли у дихлорметані (25 мл) в атмосфері азоту, і розчинник випарювали шляхом дистиляції при зниженому тиску при 40 °C. Потім залишок (MeO-PEG-NH2) сушили у вакуумі (
ДивитисяДодаткова інформація
Назва патенту англійськоюSynthesis of polymer conjugates of indolocarbazole compounds
Автори російськоюBagnod, Raffaella, Beccaria, Luca, Bertarione Rava Rossa, Luisa, Criscuolo, Domenico, Lorenzetto, Chiara, Mainero, Valentina, Marconi, Alessandra, Pincelli, Carlo, Traversa, Silvio
МПК / Мітки
МПК: A61K 47/48
Мітки: полімерних, сполук, синтез, індолокарбазольних, кон'югатів
Код посилання
<a href="https://ua.patents.su/39-103911-sintez-polimernikh-konyugativ-indolokarbazolnikh-spoluk.html" target="_blank" rel="follow" title="База патентів України">Синтез полімерних кон’югатів індолокарбазольних сполук</a>
Попередній патент: Здатні до структурування поліуретанові дисперсії
Наступний патент: Антитіла проти ангіопоетину-2 людини
Випадковий патент: Подрібнювач