Сполука n-бензил-3- [5`-(2″-амінотіадіазоліл)дифенілфосфіно]-сукцинімід з потенційними фізіологічними властивостями
Формула / Реферат
Сполука N-бензил-3-[5’-(2’’-амінотіадіазоліл) дифенілфосфіно]- сукцинімід з потенційними фізіологічними властивостями загальної формули:
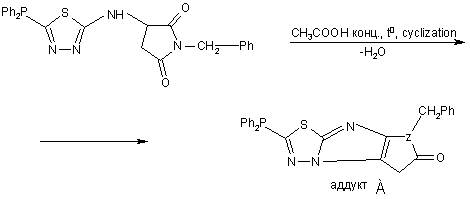 ,
,
що може циклуватися з утворенням аддукту А в результаті реакції дегідратації при нагріванні її в концентрованій оцтовій кислоті.
Текст
Сполука N-бензил-3-[5’-(2’’-амінотіадіазоліл) дифенілфосфіно]- сукцинімід з потенційними фізіологічними властивостями загальної формули: 2 3 13884 4 бензилмалеїнімідом у молярному співвідношенні тримують в концентрованій оцтовій кислоті при 1:1. температурі 18-20°С 30 хвилин. Випарюють оцтову Реакції проводилися у системі розчинників кислоту в вакуумі. В залишку - осад темно(безводний бензол - безводний піридин) при посрожевого забарвлення, який фільтрують, сушать у тійному нагріванні та перемішуванні реакційної вакуумі водострумного насосу. Практичний вихід суміші 4 години з метою забезпечення отримання 0.28г (70%). Т.пл.128-131°С. N-бензил-3-[5'-(2"-амінотіадиазоліл) дифенілфосІндивідуальність синтезованої сполуки та її фіно] - сукцинімід з потенційними фізіологічними адукту А контролюють методом тонкошарової властивостями. хроматографії, склад підтверджували даними O елементного аналізу. Ph2P S NH2 Спектр ПМР синтезованої сполуки та її адукту + Ph N CH2 А записували на приладах "Bruker WP-200" (вироN N бник "Bruker”, Switzerland), "Varian T-60" (виробник O "Varian", USA) з робочою частотою 200-132МГц у t0, виді розчинів ДМСО-D6 та CDCl3 (внутрішні станбензол б/в, піридин б/в дарти ТМС та ГМДС). ІЧ-спектр записували на спектрофотометрі O Ph2P S NH UR-20 (виробник "Charles Ceise Hena", Germany). ТШХ виконували на пластинах Silufol-254. Ph N CH2 N N ГРХ визначали на газорідинному хроматогO рафi "Perkin Еlmer"з УФ-детектором (виробник "Perkin", Germany). СH3COOH конц., cyclization -H2O Хроматограма, IЧ, ПМР-спектри кінцевих проt0 дуктів ідентифікували у порівнянні з хроматограмами, ІЧ-, ПМР-спектрами вихідних сполук. CH2Ph Синтезована сполука - це кристалічний пороPh2P S N адукт А z шок рожевого забарвлення, кристалізується із воO N N дного етанолу. Дані елементного аналізу на С, Η, Ν синтезоМожливо отриманий продукт циклується з ваної сполуки та її адукту А відповідають розрахоутворенням адукту А в результаті реакції дегідраваним значенням. тації при нагріванні його в концентрованій оцтовій ІЧ-спектр синтезованої сполуки характеризукислоті при температурі 18-20°С 30 хвилин. Пракються відсутністю сигналів групи (-NН2) вихідної тичний вихід 50%. молекули 5-(2-амінотіадиазоліл)дифенілфосфіну Таким чином, можна зробити висновок, що при 3280, 3360см-1. Валентні коливання групи сполука з потенційними фізіологічними властивос(С=O) проявляються високоінтенсивним максимутями може бути перспективною у розробці нових мом в області 1630-1750см-1 та є найбільш хараклікарських засобів з протисудомною активністю, з теристичними, оскільки інші сигнали в цій області анксіолітичним типом дії; що впливають на постпрактично відсутні. синаптичні рецептори, психотропних агентів та з Співвідношення інтегральних інтенсивностей іншими типами дії. сигналів в ПМР-спектрі синтезованої сполуки підтМетодика синтезу N-бензил-3-[5'-(2"верджує відсутність протонів первинної групи (амінотіадиазоліл)дифенілфосфіно]-сукциніміду. NH2) при 6.14м.д. в молекулі, спостерігається сиг0.32г малеїніміду (0,0017моль), 0.5г 5-(2нал у вигляді синглету при 5.642м.д. протону втоамінотіадиазоліл)дифенілфосфіну (0,0017моль) ринної групи (-NH-). Спектр ПМР сполуки містить розчиняють в 130мл суміші: безводний бензол сигнал у вигляді мультиплету при 7.268-7.888м.д., безводний піридин, перемішують при температурі що відповідає, згідно до співвідношення інтеграль60-80°С біля 2-х годин. Реакційна суміш стає проних інтенсивностей, протонам трьох ароматичних зорою з рожевого забарвлення. Перемішують реакілець (малюнок 1). кційну суміш при кипінні ще 2 години, при цьому її Спектр ПМР адукту А містить сигнал у вигляді забарвлення поглиблюється до малинового. Замультиплету при 7.388-7.455м.д., що відповідає, лишають реакційну суміш на 12 годин при кімнатзгідно до співвідношення інтегральних інтенсивноній температурі. Випарюють розчинники. До залистей, протонам трьох ароматичних кілець, сигнали шку додають 4мл розчину етилового спирту у воді протонів аміногрупи відсутні (малюнок 2). (1:1). Осад рожевого забарвлення обробляють Фізико-хімічні характеристики та дані елементбезводним бензолом, фільтрують, сушать у вакуного аналізу синтезованої сполуки та її адукту А умі водострумного насосу. Практичний вихід 0,4г наведено в таблиці 1. (50%). Т. пл.160-163°С. Методика синтезу адукту А. 0.4г синтезованої сполуки (0,00084моль) ви 5 13884 6 Таблиця 1 Фізико-хімічні характеристики та дані елементного аналізу синтезованої сполуки та її адукту А. Знайдено, у% СΗΝ Бруттоформула Обчислено, у%. ІЧ-спектр (KBr), см-1 СΗΝ сполука 62.8 4.27 11.5 C25H21N4O2SP 650-900 (Ph), 63.5 4.48 11.8 1630-1750(C=O), 3310,3350 (-NH-). адукт А 64.9 4.14 11.9 C25H19N4ОSP 65.8 4.17 12.3 Таким чином, можна зробити висновок, що сполука з потенційними фізіологічними властивостями може бути перспективною у розробці нових лікарських засобів з протисудомною активністю, з анксіолітичним типом дії; що впливають на постсинаптичні рецептори, психотропних агентів та з іншими типами дії. Завданням корисної моделі є опис хімічної будови нової сполуки N-бензил-3-[5'-(2"амінотіадиазоліл) дифенілфосфіно]- сукцинімід, яка може бути фізіологічно активною за рахунок наявності в будові фрагменту молекули циклічного іміду. Література 1. Magid Abou - Gharbia, Usha R. Patel and all. // J. Med. Chem. - 1988. - Vol.31, №7. P.1382-1385. 2. Richards M.N. (Merrel D., Res. Inst. 67084, 650-900 (Ph), 1715(C=O) СпектрПМР (ДМСО-D6, CDCL3), , м.д. (J, Гц) 1.690(2Н,т.,-СН2-maleinimides), 4.635(2Н, с., -CH2Ph), 5.642 (1H, e.,-N-H),7.268 7.888 (15H,м., 3Ph) 7.388-7.455 (15H,м.,3Ph) Strasbourg, Fr.) // J. Pharmacol. Exp. Ther. - 1990. 255(1). - P.83-89. 3. Amagat P. // Traite de Chemie Organique. 1941. - Vol.13. - P.502-521. 4. Ошовский Г.В., Толмачев Φ.Φ., Меркулов A.C., Пинчук A.M. Тиадиазолилфосфины с азотсодержащими заместителями.// ХГС - 1997, №10, С.1422-1424. 5. Вельчинська O.B., Кузьменко І.Й., Драпайло А.Б. Синтез нових похідних заміщених малеїнімідів як потенційних фізіологічно активних агентів. Тези. доп. XVIII-οϊ Укр.конф.з орг.хімії. 1998. Дніпропетровськ, с.369. 6. Вельчинская Е.В., Кузьменко И.И., Кулик Л.С. Синтез новых производных замещенных урацилов и пиримидинов.// Хим. - фарм. журн. Москва. - 1999, №3, С.40-42. 7 Комп’ютерна верстка М. Мацело 13884 8 Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA compound of n-benzyl-3-[5-(2-aminothiadiazolyl) diphenylphosphino]- succinimide with potential physiological properties
Автори англійськоюVelchynska Olena Vasylivna
Автори російськоюВельчинская Елена Васильевна
МПК / Мітки
МПК: C07D 285/12, C07D 207/40
Мітки: 5`-(2"-амінотіадіазоліл)дифенілфосфіно]-сукцинімід, властивостями, n-бензил-3, потенційними, сполука, фізіологічними
Код посилання
<a href="https://ua.patents.su/4-13884-spoluka-n-benzil-3-5-2-aminotiadiazolildifenilfosfino-sukcinimid-z-potencijjnimi-fiziologichnimi-vlastivostyami.html" target="_blank" rel="follow" title="База патентів України">Сполука n-бензил-3- [5`-(2″-амінотіадіазоліл)дифенілфосфіно]-сукцинімід з потенційними фізіологічними властивостями</a>
Попередній патент: Пристрій для проведення трансальвеолярного електрофорезу
Наступний патент: Спосіб лікування гнійних ран у породіль
Випадковий патент: Спосіб виробництва біогазу та добрива








