Сполука 2-(n-ортотрифторметилфенілсукцинімідо-3)-меркаптобензойна кислота з потенційними біологічними властивостями
Номер патенту: 42372
Опубліковано: 25.06.2009
Автори: Вельчинська Олена Василівна, Губський Юрій Іванович, Драпайло Андрій Богданович, Вільчинська Валерія Валеріївна
Формула / Реферат
Сполука 2-(N-ортотрифторметилфенілсукцинімідо-3)-меркаптобензойна кислота з потенційними біологічними властивостями загальної формули:
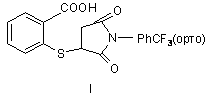 .
.
Текст
Сполука 2-(Nортотрифторметилфенілсукцинімідо-3)меркаптобензойна кислота з потенційними біологічними властивостями загальної формули: COOH O N S PhCF3(орто) O I O N O O Alk або N Ph O Дані вітчизняних і зарубіжних наукових робіт свідчать про залежність і спрямованість фізіологічної дії речовини від будови введеного замісника в молекулу малеїніміду [1, 2]. Було синтезовано похідні малеїніміду з анксіолітичним типом дії (а, б); що впливають на постсинаптичні рецептори (в); психотропні агенти (г) та з іншими типами дії, (схема 2): O 2O S NH O CH3 R3 CH3 O N R2 O б CH3 O R C2H5 в O N R1 CH3 O (CH2)m-Cycl 42372 a (11) NH (13) O U Схема 2 г Зацікавленість до цього класу сполук як до потенційного джерела протиепілептичних препаратів виникла після експериментальних досліджень [3]. N-вмісткі гетероциклічні сполуки менш нуклеофільні, у порівнянні з аліфатичними та ароматичними амінами, але їх нуклеофільність достатня для здійснення реакції Міхаеля [4]. При взаємодії малеїнімідів із заміщеним бензолом в присутності сірчаної кислоти або сірчаної та фосфорної кислот можливе отримання Nарилмалеїнімідів із збереженням або розкриттям циклу малеїніміду (схема 3), [5]: UA Корисна модель належить до хімії гетероциклічних сполук, а саме, до сполуки 2-(Nортотрифторметилфенілсукцинімідо-3)меркаптобензойна кислота (далі, сполука І) з потенційними біологічними властивостями та високою реакційною здатністю, які можуть проявлятися за рахунок наявності в будові молекули спряженої системи між ароматичними ядрами та фрагментом молекули циклічного іміду. В науковому світі інтенсивно досліджуються біологічно активні сполуки, що містять в будові фрагмент молекули насиченого або ненасиченого циклічного іміду і можуть стати основою нових лікарських засобів, (схема 1): Схема 1 . (19) (21) u200904230 (22) 29.04.2009 (24) 25.06.2009 (46) 25.06.2009, Бюл.№ 12, 2009 р. (72) ГУБСЬКИЙ ЮРІЙ ІВАНОВИЧ, ВЕЛЬЧИНСЬКА ОЛЕНА ВАСИЛІВНА, ДРАПАЙЛО АНДРІЙ БОГДАНОВИЧ, ВІЛЬЧИНСЬКА ВАЛЕРІЯ ВАЛЕРІЇВНА (73) НАЦІОНАЛЬНИЙ МЕДИЧНИЙ УНІВЕРСИТЕТ ІМЕНІ О.О. БОГОМОЛЬЦЯ 3 42372 Схема 3 R2 O R1 R2 O N O R3 R5 R4 R1 R3 NH або OR R4 R5 O 4 заміщеного малеїніміду з 2-меркаптобензойною кислотою. Реакції проводилися у системі розчинників (бензол-піридин) при температурі 60-80°С та перемішуванні реакційної суміші 5 годин з обробкою продукту реакції розчином етилового спирту у воді (1:1) та безводним бензолом, фільтруванням, сушкою у вакуумі водострумного насосу, (схема 5). Схема 5 COOH R1-R5=H,Hal,NO2,OH,COOH,Ph,SO3H Огляд літературних даних дає можливість прогнозувати, що в результаті нуклеофільного приєднання молекул ароматичних поук з активною меркаптогрупою до N-заміщеного малеїніміду можливе утворення нових сполук з потенційною біологічною активністю: протипухлинною, протисудомною, а також антимікробною дією [1, 8, 9]. Раніше авторами були синтезовані нові гетероциклічні похідні сукцинімідів шляхом нуклеофільного приєднання по подвійному зв'язку молекули малеїніміду амінотіоурацилів [6, 7]. Даний метод синтезу нових сукцинімідів перенесено нами на ароматичні сполуки з меркаптогрупою, а саме 2-меркаптобензойну кислоту. Структурні аналоги сполуки 2-(Nортотрифторметилфенілсукцинімідо-3)меркаптобензойна кислота (далі, сполука І) з потенційними біологічними властивостями в літературі не описано. Сполука І синтезована з метою отримання нового поліфункціонального циклічного синтону для подальшого вивчення її фізико-хімічних та біологічних властивостей, а також вивчення можливості проходження хімічних реакцій між ароматичними сполуками з активною меркаптогрупою та Nзаміщеними малеїнімідами. В основу корисної моделі поставлено хімічну будову молекули сполуки 2-(Nортотрифторметилфенілсукцинімідо-3)меркаптобензойна кислота (далі, сполука І) з потенційними біологічними властивостями шляхом взаємодії N-ортотрифторметил-фенілмалеїніміду та 2-меркаптобензойної кислоти у молярному співвідношенні 1:1. На відмінність від імідів насичених дикарбонових кислот іміди ненасичених дикарбонових кислот мають у складі молекули активований двома карбонільними групами подвійний зв'язок, який здатен при певних умовах приєднувати нуклеофільні реагенти з утворенням похідних сукциніміду. В результаті спряження карбонільних груп з гетероатомом азоту електрофільна активність карбонільних груп малеїніміду знижена і саме на атомах вуглецю етиленового зв'язку знаходиться значний за величиною позитивний заряд, (схема 4): Схема 4 + + O N O R Типовим прикладом нуклеофільного приєднання по подвійному зв'язку є взаємодія N + SH O N O PhCF3 (орто) to,C6H6 Py COOH O N S PhCF3(орто) O I Позитивними рисами описаного методу синтезу є легкість його проведення та простота обробки кінцевого продукту. Варіювання умов проведення реакцій та внесення змін до методики синтезу, а саме: обробка продукту реакції розчином етилового спирту у воді (1:1) та безводним бензолом, дозволили збільшити практичний вихід сполуки І до 45%. УФ-спектр сполуки І характеризується наявністю lmax при 243нм. В той час, як УФ-спектр стандартної речовини (сукциніміду) відрізняється наявністю інтенсивної смуги при 207нм і малоінтенсивної смуги при 243нм (за рахунок спряження груп С=О , r-електронів гетероатому азоту). В ІЧ-спектрі сполуки І в області 600-900см-1 спостерігаються інтенсивні смуги непласких деформаційних коливань С-Н ароматичних кілець, в той час як валентні коливання С-С зв'язків бензольних ядер при 1585-1600см-1 та 1400-1500см-1 ідентифікувати неможливо, так як дані області спектру близькі до коливань зв'язку С=С, >N-H групи. В ІЧспектрі стандартної речовини (сукцинімід) деформаційні коливання С-Н ароматичного кільця в області 600-900см-1 відсутні. В ІЧ-спектрі сполуки І смуги dN-R спостерігаються в області 1470, 1495см1 , а смуги nCF при бензольному кільці - в області 730-950см-1. Валентні коливання карбонільних груп С=О сполуки І проявляються високоінтенсивним максимумом в області 1680-1750см-1 (дві смуги) і є найбільш характеристичними, так як інші смуги в даній області практично відсутні. ЯMPlH спектр сполуки І має сигнали у вигляді дублетів дублетів при 7,05-7,58м.д., що відповідає протонам ароматичних кілець, сигнал у вигляді дублету при 2,58-2,82м.д., що відповідає двом протонам молекули сукциніміду в четвертому положенні, сигнал у вигляді триплету при 3,864,13м.д., який відповідає протону молекули сукциніміду в третьому положенні. Положення сигналу від протону карбоксильної групи відповідає теоретичному значенню і спостерігається при 10,0412,98м.д. Таким чином, можна зробити висновок, що сполука І з потенційними біологічними властивостями може бути перспективною у розробці нових лікарських засобів з проти-судомною активністю, з анксіолітичним типом дії; що впливають на постсинаптичні рецептори, психотропних агентів та з іншими типами дії. 5 42372 Ознаки способу Методики синтезу сполуки 2-(Nортотрифторметилфенілсукцинімідо-3)меркаптобензойна кислота (І). До розчину 0,57г (0,0024 моль) Nортотрифторметилфенілмалеїніміду в 10мл бензолу безводного додають 0,37г (0,0024моль) 2меркаптобензойної кислоти в 10мл піридину безводного, витримують реакційну суміш при температурі 60-80°С та перемішуванні 5 годин. Осад, що утворився, відфільтровують, промивають розчином етилового спирту у воді (1:1), безводним бензолом, фільтрують, сушать у вакуумі водострумного насосу. Залишок - осад жовтого забарвлення промивають під час фільтрування в вакуумі сухим гексаном, сушать на повітрі. Практичний вихід 0,42г (45%). Ттопл. 142-145°С. Індивідуальність сполуки І контролювали методом тонкошарової хроматографії, склад підтверджували даними елементного аналізу. ТШХ виконували на пластинах Silufol-254. ГРХ проводили на газорідинному хроматографі "Perkin Еlmеr"з УФ-детектором (виробник "Perkin", Germany). УФ-спектр сполуки І записували на спектрофотометрі Mel Temp II (USA). IЧ-спектр записували на спектрофотометрі UR-20 (виробник "Charles Ceise Hena", Germany). Спектри ЯМРlН сполуки І записували на приладах "Bruker WP-200" (виробник "Bruker", Switzerland) або "Varian T-60" (виробник "Varian", USA) з робочою частотою 200-132МГц у виді розчину ДМСО-D6 (внутрішній стандарт ГМДС). Хроматограма, УФ, ІЧ, ЯМРlН спектри сполуки І ідентифікували у порівнянні з хроматограмами, 6 УФ, ІЧ, ЯМРlН спектрами вихідних сполук. Синтезована сполука І - це кристалічний порошок жовтого забарвлення. Дані елементного аналізу на С, Н, N сполуки І відповідають обчисленим значенням. В УФ-спектрі сполуки І ідентифіковано значення lmax при 243нм. В ІЧ-спектрі сполуки І смуги непласких деформаційних коливань С-Н ароматичних кілець спостерігаються в області 600-900см-1, в той час як валентні коливання С-С зв'язків бензольних ядер при 1585-1600см-1 та 1400-1500см-1 ідентифікувати неможливо, так як дані області спектру близькі до коливань зв'язку С = >N-H групи. В ІЧ-спектрі С, сполуки І ідентифіковано смуги dN-R в області 1470, 1495см-1, смуги nCF при бензольному кільці - в області 730-950см-1. Валентні коливання карбонільних груп С=О сполуки І ідентифіковано як високоінтенсивний максимум в області 1680-1750см-1 (дві смуги) і є найбільш характеристичними, так як інші смуги в даній області практично відсутні. Співвідношення інтегральних інтенсивностей сигналів в ЯМРlН спектрі сполуки І підтверджує наявність протонів ароматичних кілець у вигляді дублетів дублетів при7,05-7,58м.д., двох протонів молекули сукциніміду в четвертому положенні та протону молекули сукциніміду в третьому положенні у вигляді дублету при 2,58-2,82м.д. та триплету при 3,86-4,13м.д. відповідно. Ідентифіковано сигнал у вигляді синглету при 10,04-12,98м.д. протону карбоксильної групи. Віднесення сигналів в 14 та ЯМРlН спектрах сполуки І наведено в таблиці. Таблиця 1 Віднесення сигналів в ІЧ, ЯМРlН спектрах, дані елементного аналізу сполуки І Знайдено, у % С Н N 54,88; 3,08; 3,82 Брутто-формула C18H12NO4F3S Обчислено, у % С Н N 54,69; 3,05; 3,54 Таким чином, можна зробити висновок, що сполука І з потенційними біологічними властивостями за рахунок наявності в молекулі фармакофорних угрупувань може бути перспективною у створенні нових лікарських засобів. На основі літературних даних, шляхом порівняння хімічної будови сполуки І із сполуками описаними в літературі, можна передбачити, що наявність в її молекули ароматичних фрагментів та сукциніміду одночасно можуть наділити її анксіолітичними властивостями. Завданням корисної моделі є опис хімічної будови нової сполуки І з потенційними біологічними властивостями та високою реакційною здатністю, які можуть проявлятися за рахунок наявності в будові молекули спряженої системи між аромати ІЧ-спектр Спектр ЯМРlН (ДМСО-1 D6), д, м.д. (J, Гц) (КВr), см g 730-950 (C-F); 2,58-2,82 (д., Sue, 2H (4 600-900 (С-Н, position)); 3,86-4,13 (т., Ph); Suc, 1H (3 position)); 7,051470,1495 7,58 (д.д., д.д., 2 Ph, 8H); (>N-R); 1680- 10,0-13,0 (c, COOH, 1H). 1750 (C=О). чними ядрами та фрагментом молекули циклічного іміду. Джерела інформації: 1. Magid Abou - Gharbia, Usha R. Patel and all. // J. Med. Chem. - 1988. - Vol.31, №7. - P.1382-1385. 2. Richards M.N. (Merrel D., Res. Inst. 67084, Strasbourg, Fr.) // J. Pharmacol. Exp. Ther. - 1990. 255(1). - P. 83-89. 3. Amagat P. // Traite de Chemie Organique. 1941. - Vol. 13. - P. 502-521. 4. N. Fehling // Ann. - 1844. - Vol.49. - P. 198. 5. Bunge // Ann. Suppl. -1870. - Vol.7. - P.118. 6. Пат.18825 Україна. МПК C07D239/553, A61K33/16.C07C 21/00. Сполуки N-феніл-3(уридин-2'-тіо-4'-гідроксі-6'-аміно)сукцинімід та Nпара-метоксифеніл-3-(уридин-2'-тіо-4'-гідроксі-6' 7 42372 аміно)сукцинімід з потенційними фізіологічними властивостями / Губський Ю.І., Вельчинська О.В. (Україна); Заявл.09.06.06; Опубл. 15.11.06, Бюл. №11. - 8с. 7. Пат.18096 Україна. МПК C07D239/553, A61K33/16.C07C 21/00. Сполуки N-пapaбромфеніл-3-(уридин-5'-аміно)сукцинімід та Nпара-бромфеніл-3-(уридин-6'-аміно)сукцинімід з потенційними фізіологічними властивостями / Губ Комп’ютерна верстка М. Ломалова 8 ський Ю.І., Вельчинська О.В. (Україна); Заявл.24.05.06; Опубл. 16.10.06, Бюл. №10. - 8с. 8. М. Farcaslu, R. Istratolu, Rev. Roum. Chim., Vol. 15, №12, 253 (1970). 9. Jnove Massayasu, Jwao Ebashi, Tetsuo Tkigawo Eur. Pat. Appl. Ep 507,348 - (C1.C12N9/02), 07.Oct.1992, Jp. Appl. 91/102,023,05. Apr. 1991.// Chem. Abstr. - 1993. - Vol.118, 55129j. Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюCompound 2-(n-orthotrifluoromethylphenylsuccinimido-3)-mercaptobenzoic acid with potential biological properties
Автори англійськоюHubskyi Yurii Ivanovych, Velchynska Olena Vasylivna, Drapailo Andrii Bohdanovych, Vilchynska Valeria Valeriivna
Назва патенту російськоюСоединение 2-( n-ортотрифторметилфенилсукцинимидо-3)-меркаптобензойная кислота с потенциальными биологическими свойствами
Автори російськоюГубский Юрий Иванович, Вельчинская Елена Васильевна, Драпайло Андрей Богданович, Вильчинская Валерия Валериевна
МПК / Мітки
МПК: A61K 33/16, C07C 21/00, C07D 239/553
Мітки: властивостями, кислота, 2-(n-ортотрифторметилфенілсукцинімідо-3)-меркаптобензойна, сполука, потенційними, біологічними
Код посилання
<a href="https://ua.patents.su/4-42372-spoluka-2-n-ortotriftormetilfenilsukcinimido-3-merkaptobenzojjna-kislota-z-potencijjnimi-biologichnimi-vlastivostyami.html" target="_blank" rel="follow" title="База патентів України">Сполука 2-(n-ортотрифторметилфенілсукцинімідо-3)-меркаптобензойна кислота з потенційними біологічними властивостями</a>
Попередній патент: Спосіб визначення в повітрі наночасток срібла
Наступний патент: Застосування таурину та яктону як антиоксиданта та геномопротектора
Випадковий патент: Спосіб визначення вологоутримуючої здатності м'яса риби за різного ступеня термічної обробки








