Спосіб одержання s(+)-6-арил-3-(трифторо)ацетил-6-трифторометил-5,6-дигідропіридин-2(1н)-онів
Номер патенту: 46588
Опубліковано: 25.12.2009
Автори: Сукач Володимир Андрійович, Головач Наталія Михайлівна, Вовк Михайло Володимирович
Формула / Реферат
Спосіб одержання S(+)-6-арил-3-(трифторо)ацетил-6-трифторометил-5,6-дигідропіридин-2(1Н)-онів загальної формули :
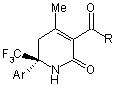 ,
,
де Аr = Ph, 4-РС6Н4, 4-МеС6Н4, 4-МеОС6Н4;
R = Ме, СF3,
який відрізняється тим, що S(-)-4-аміно-4-арил-5,5,5-трифторопентан-2-они піддають взаємодії з етиловими естерами (трифторо)ацетооцтової кислоти в киплячому ксилолі (індивідуальні ізомери або їх суміш) впродовж 4-6 год. з подальшим виділенням цільових продуктів звичайними методами.
Текст
Спосіб одержання S(+)-6-арил-3(трифторо)ацетил-6-трифторометил-5,6дигідропіридин-2(1Н)-онів загальної формули : 2 UA (54) СПОСІБ ОДЕРЖАННЯ ДИГІДРОПІРИДИН-2(1Н)-ОНІВ видається під відповідальність власника патенту (19) ДЕРЖАВНИЙ ДЕПАРТАМЕНТ ІНТЕЛЕКТУАЛЬНОЇ ВЛАСНОСТІ ОПИС 3 46588 діалкіламінокротононітрилів з 1-хлоро-2,2,2трифтороалкілізоціанатами. Незважаючи на те, що такий процес перебігає при кімнатній температурі, його суттєвим недоліком є використання відносно важкодоступних реагентів - відповідних єнамінів та 1-хлоралкілізоціанатів та недешевих органічних основ - діазабіциклононану та діазабіциклоундекану. Окрім того синтетичні можливості методу не дають змоги отримувати високо енантіомерно збагачені похідні 5,6-дигідропіримідин-2(1Н)-ону, що є дуже істотним в сучасних підходах до дизайну препаратів медичного призначення. Задачею корисної моделі є спосіб отримання нових оптично активних похідних 6-арил-3(трифторо)ацетил-б-трифторометил-4-метил-5,6дигідропіримідин-2(1Н)-ону загальної формули : OEt R Me F3C Ar NH2 O O O 4 Me F3C N O H де Аr=Ph, 4-FС6Н4, 4-МеС6Н4, 4-МеОС6Н4; R=Me, СF3. Спосіб отримання сполук, які заявляються , полягає в тому, що S(-)-4-аміно-4-арил-5,5,5трифторопентан-2-они піддають взаємодії з етиловими естерами (трифторо)ацетооцтової кислоти в киплячому ксилолі (індивідуальні ізомери або їх суміш) з подальшим виділенням цільових продуктів стандартними методами. Виходи складають 6391%, оптична чистота 84-91%. Ar Me Me F3C Ar - EtOH O R O HN O O R O F3C - H2O Ar N H O де Аr=Ph, 4-FС6Н4, 4-МеС6Н4, 4-МеОС6Н4; R=Me, СF3. Запропонований підхід є ефективним для одержання нових СF3-вмісних похідних 5,6дигідропіримідин-2(1Н)-ону високої оптичної чистоти на основі доступних хіральних синтонів - S(-)4-аміно-4-арил-5,5,5-трифторопентан-2-онів [10]. Процес утворення цільових продуктів реалізується без участі асиметричного атома вуглецю і тому їх абсолютна конфігурація є ідентичною до вихідних S(-)-4-аміно-4-арил-5,5,5-трифторопентан-2-онів. Завдяки пониженій основності аміногрупи в S()-4-аміно-4-арил-5,5,5-трифторопентан-2-онах, обумовленій адитивним впливом акцепторної трифторометильної групи та стеричним ефектом арильного замісника, отриманий результат не був заздалегідь передбачуваним, оскільки не виключалась можливість перебігу міжмолекулярної реакції Кновенагеля з утворенням ациклічних алкенільних сполук, найімовірніше, транс-конфігурації. В дійсності ж виділення цільових продуктів є вагомим доказом взаємодії за схемою первинного Nацилювання з утворенням відповідних амідів ацетооцтової кислоти, які при підвищеній температурі схильні до внутрішньомолекулярної циклоконденсації за Кновенагелем. При цьому характер ацетильного залишку практично не впливає на здійснення такого процесу, який, на відміну від внутрішньомолекулярної циклізації N-3оксоалкіламідів [11-13], відбувається за відсутності основи. Індивідуальність та склад синтезованих продуктів доказані методами хроматомас-спектрометрії, 1 19 13 будова - ІЧ, ЯМР Н, F та С спектроскопії, а оптичні властивості - вимірюванням кутів питомого обертання. Корисна модель ілюструється загальним способом отримання S(-)-3-(трифторо)ацетил-6трифторометил-4-метил-5,6-дигідропіримідин 2(1Н)-онів і фізико-хімічними характеристиками всіх синтезованих сполук. Загальний спосіб одержання S(+)-6-арил-3(трифторо)ацетил-6-трифторометил-4-метил-5,6дигідропіримідин-2(1Н)-онів. До розчину амінокетону І 0,0016 моль в 15мл сухого толуолу приливали 0,24мл (0.0016моль) трифтороацетооцтового ефіру. Реакційну суміш кип'ятили 4-6 годин. Розчинник упарили, осад перекристалізовували з суміші EtOH-Н2О, 2:1. S(+)-4-Метил-6-феніл-3-(трифтороацетил)-6(трифторометил)-5,6-дигід-ропіридин-2(1Н)-он. Вихід 87%, т.пл. 115-117°С. αD20=+37,7 (с=1,15; МеОН). ІЧ-спектр, ν, см-1: 1675, 1680 (С=О), 3210 1 (NH). Спектр ЯМР Н, δ, м.д.: 2.02 с (3Н, СН3), 3,15 д (1Н, СН2, J 18,0Гц), 3,29 д (1Н, СН2, J 18,0Гц), 7,42-7,51м (5Наром.), 8,22 с (1Н, ΝΗ). Спектр ЯМР 19 13 F, δ, м.д.: -77,16, -78,77. Спектр ЯМР C, δ, м.д.: 21,02 (СН3), 37,07 (СН2), 62,63 кв (J 28,9Гц), 115,04 кв (J 291,74Гц), 124,72 кв (J 284,19Гц), 126,26, 5 126,98, 129,01, 129,55 (Саром.), 135,10 (С ), 155,36 (С4), 163,69 (СО), 184,79 кв (С=О, J 38,9Гц). Масспектр: m/z [M]+ 352. Знайдено, %: C 51,31; H 3,13; N 4,02. C15H11F6NO2. Вирахуваного: С 51,29; H 3,16; N 3,99. S(+)-6-(4-Фторофеніл)-4-метил-3(трифтороацетил)-6-(трифторометил)-5,6дигідропіридин-2(1Н)-он. Вихід 68%, в'язке масло. ІЧ-спектр, ν, см-1: 1675, 1680 (С=О), 3200 (ΝΗ). Спектр ЯМР 1Н, δ, м.д.: 2,02 с (3Н, СН3), 3,09 д (1Н, СН2, J 18. Гц), 3,27 д (1Н, СН2, J 18,0Гц), 7,14 д (2Наром., J 7,5Гц), 7,55 д (2Наром., J 7,5Гц), 8,25 с (1Н, NH). Спектр ЯМР 19F, δ, м.д.: -77,18, -78,98, -112,71. Спектр 13 ЯМР С δ, м.д.: 21,03 (СН3), 37,12 (СН2), 62,28 кв (J 27.6 Гц), 114,23, 114,33, 126,95, 127,54 (Саром.), 116,21 кв (J 291,7Гц), 124,75 кв (J 284,1Гц), 155,11 5 3 4 (С ), 160,30 (С ), 162,08 д (F-Capом., J 296,7Гц), 20 169,75 (С=О), 184,89 кв (С=О, J 38,9Гц), αD=+57,3 (с=1,02; МеОН). Мас-спектр: m/z [М] 368. Знайдено, %: С 48,82; Η 2,70; Ν 3,81. C15H10F7NO2. Вирахувано, %: С 48,79; Η 2,73; Ν 3,79. S(+)-4-Метил-6-(4-метилфеніл)-3(трифтороацетил)-6-(трифторометил)-5,6дигідропіридин-2(1Н)-он. -1 Вихід 91%, т.пл. 164-166°С. ІЧ-спектр, ν, см : 1 1680, 1685 (С=О), 3220 (ΝΗ). Спектр ЯМР Н, δ, м.д.: 1,99 с (3Н, СН3), 2,37 с (3Н, СН3), 3,04 д (1Н, СН2, J 18,0Гц), 3,29 д (1Н, СН2, J 18,0Гц), 7,25 д (2Наром., J 7,8Гц), 7,38 д (2Наром., J 7,8Гц), 7,81 с 19 (1Н, NH). Спектр ЯМР F, δ, м.д.: -77,08, -79,01. 13 Спектр ЯМР С δ, м.д.: 20,96 (СН3), 37,06 (СН2), 62,45 кв (J 27,6Гц), 115,05 кв (J 291,1Гц), 124,76 кв (J 284,1Гц), 126,15, 126,97, 129,66, 132,12 (Саром.), 139,55 (С3), 155,37 (С4), 163,71 (С=О), 184,91 кв 20 (С=О, J 38,9Гц), αD =+65,9 (с=1,39; МеОН). Мас+ спектр: m/z [М] 366. Знайдено, %: С 52,63; Η 3,62; Ν 3,87. C16H13F6NO2. Вирахувано, %: С 52,61; Η 3,59; Ν 3,83. S(+)-6-(4-Метоксифеніл)-4-метил-3(трифтороацетил)-6-(трифторо-метил)-5,6дигідропіридин-2(1Н)-он. Вихід 73%, т.пл. 118-120°С. ІЧ-спектр, ν, см-1: 1685, 1725 (С=О), 3210 (ΝΗ). Спектр ЯМР 1H, δ, м.д.: 2,02 с (3Н, СН3), 3,10 д (1Н, СН2, J 17,5Гц), 3,29 д (1Н, СН2, J 17,5Гц), 3,84 с (3Н, СН3О), 6,96 д (2Наром., J 7,5Гц), 7,46 д (2Наром., J 7,5Гц), 8,39 с (1Н, NH). Спектр ЯМР 19F, δ, м.д.: -77,11, -79,13. Спектр ЯМР 13С δ, м.д.: 21,00 (СН3), 37,07 (СН2), 55,32 (СН3О), 62,25 кв (J 27,6Гц), 114,18, 114,27, 126,91, 127,63 (Саром.), 116,20 кв (7291,7Гц), 124,76 кв (J 284,1Гц), 155,58 (С3), 160,28 (С4), 163,84 20 (С=О), 184,91 кв (С=О, J 38,9Гц), αD =+16,5 (с=1,0; МеОН). Мас-спектр: m/z [Μ] 380. Знайдено, %: С 50,44; Η 3,41; Ν 3,71. C16H13F6NO3. Вирахуваного: С 50,40; Η 3,44; Ν 3,67. Загальний спосіб одержання S(+)-3-Ацетил-4метил-6-арил-6-(трифтороацетил)-5,6дигідропіридин-2(1Н)-онів (III а-г). До розчину амінокетону І 0,0016 моль в 15мл сухого ксилола приливали 0,18мл (0,0016моль) трифторацетооцтового ефіру. Реакційну суміш кип'ятили 4-6 годин. Розчинник упарили залишок кристалізували з суміші ЕtOН-Н2О, 2:1 у випадку Аr=4МеС6Н4, а решту - ділили хроматографічно, елюент - етилацетатгексан, 1:5. S(+)-3-Ацетил-4-метил-6-феніл-6(трифторометил)-5,6-дигідро-піридин-2(1Н)-он. -1 Вихід 76%, т.пл. 113-115°С. ІЧ-спектр, ν, см : 1685, 1705 (С=О), 3210 (ΝΗ). Спектр ЯМР % δ, м.д.: 1,98 с (3Н, СН3), 2,34 с (3Н, СН3), 3,02 д (1Н, СН2, J 18,0Гц), 3,20 д (1Н, СН2, J 18,0Гц), 7,11 с (1Н, ΝΗ), 7,42-7,44 м (3Наром.), 7,50-7,53 м (2Наром.). Спектр ЯМР 19F, δ, м.д.: -78,76. Спектр ЯМР 13С, δ, м.д.: 21,06 (СН3), 31,39 (СН3), 36,93 (СН2), 62,30 кв (J 27,6Гц), 124,93 кв (J 285,4Гц), 126,15, 129,00, 129,38, 132,20 (Саром.), 135,94 (С4), 149,08 (С3), 20 164,31 (С=О), 200,64 (С=О). αD =+37,4 (с=0,98; + МеОН). Мас-спектр: m/z [М] 298. Знайдено, %: С 60,58; Η 4,77; Ν 4,73. C15H14F3NO2. Вирахувано, %: С 60,60; Η 4,75; Ν 4,71. 46588 6 S(+)-3-Ацетил-6-(4-фторофеніл)-4-метил-6(трифторометил)-5,6-дигідропіридин-2(1Н)-он. Вихід 63%, т.пл. 110-113°С. ІЧ-спектр, ν, см-1: 1 1675, 1705 (С=О), 3200 (ΝΗ). Спектр ЯМР Н, δ, м.д.: 1,98 с (3Н, СН3), 2,33 с (3Н, СН3), 2,98 д (1Н, СН2, J 18,0Гц), 3,19 д (1Н, СН2, J 18,0Гц), 7,10-7,13 м (2Наром.), 7,46 с (1Н, ΝΗ), 7,50-7,52 м (2Наром.). 19 Спектр ЯМР F, δ, м.д.: -77,19, -78,95, -112,71. 13 Спектр ЯМР С, δ, м.д.: 21,08 (СН3), 31,38 (СН3), 36,89 (СН2), 62,02 кв (С4, J 27,6Гц), 115,94, 116,11, 128,22, 128,29, 131,76 (Саром.), 127,06 кв (J 4 5 285,4Гц), 132,24 (С ), 148,99 (С ), 164,09 (C-Fapом., 20 J 248,9Гц), 164,42 (С=О), 200,50 (С=О). αD =+23,2 + (с=1,0; МеОН). Мас-спектр: m/z [М] 316. Знайдено, %: С 57,13; Η 4,14; N 4,43. C15H13F4NO2. Вирахувано, %: С 57,15; Η 4,16; N 4,44. S(+)-3-Ацетил-4-метил-6-(4-метилфеніл)-6(трифторометил)-5,6-дигідропіридин-2(1Н)-он. -1 Вихід 91%, т.пл. 145-147°С. ІЧ-спектр, ν, см : 1 1690, 1705 (С=О), 3210 (ΝΗ). Спектр ЯМР Н, δ, м.д.: 1,94 с (3Н, СН3), 2,34 с (3Н, СН3), 2,36 с (3Н, СН3), 2,97 д (1Н, СН2, J 17,5Гц), 3,14 д (1Н, СН2, J 17,5Гц), 6,54 с (1Н, ΝΗ), 7,24 д (2Наром., J 8,0Гц), 7,38 д (2Наром., J 8,0Гц). Спектр ЯМР 19F, δ, м.д.: 78,96. Спектр ЯМР 13С, δ, м.д.: 20,99 (СН3), 21,08 (СН3), 31,39 (СН3), 36,80 (СН2), 62,09 кв (J 27,6Гц), 124,78 (J 284,2Гц), 126,20, 129,62, 132,18, 132,94 (Саром.), 139,30 (С4), 149,28 (С3), 164,70 (С=О), 200,79 (СО), αD20=+2,0 (с=1,0; МеОН). Мас-спектр: m/z [М]+ 312. Знайдено, %: С 61,70; Η 5,23; Ν 4,48. C16H16F3NO2. Вирахуваного: С 61,73; Η 5,18; Ν 4,50. S(+)-3-Ацетил-4-метил-6-(4-метоксифеніл)-6(трифторометил)-5,6-дигідропіридин-2(1Н)-он. Вихід 71%, т.пл. 105-107°С. ІЧ-спектр, ν, см-1: 1 1695, 1705 (СО), 3210 (ΝΗ). Спектр ЯМР Н, δ, м.д.: 1,97 с (3Н, СН3), 2,33 с (3Н, СН3), 2,97 д (1Н, СН2, J 17,5Гц), 3,16 д (1Н, СН2, J 17,5Гц), 3,83 с (3Н, СН3О), 6,94 д (2Наром., J 7,5Гц), 7,41 д (2Наром., J 7,5Гц), 7,41 с (1Н, NH). Спектр ЯМР 19F, δ, м.д.: 13 79,08. Спектр ЯМР С, δ, м.д.: 21,08 (СН3), 31,40 (СН3), 36,88 (СН2), 61,92 кв (J 27,6 Гц), 114,26, 127,52, 127,67, 160,15 (Саром.), 124,80 кв (J 4 3 284,0Гц), 132,18 (С ), 149,21 (С ), 164,53 (С=О), 20 200,77 (С=О). αD =+48,5 (с=0,79; МеОН). Масспектр: m/z [М]+ 312. Знайдено, %: С 58,72; Η 4,95; N 4,25. C16H16F3NO3. Вирахуваного: С 58,71; Η 4,93; Ν 4,28. Література: 1. Pat. ЕР 249149. 16 Dec. 1987. - 3-Benzoyl-4oxolactams, procedure for their preparation, and their use as herbicides / Curtius J.K. Chem. Abstr. 1988.Vol. 109.-73334. 2. Pat. WO 9514011. 26 May 1995. - 5,6Dihydropyrone derivatives as protease inhibitior and antiviral agents / Ellswort EX., Lunney E.T., Bradley D. Chem. Abstr. - 1995. - Vol.123, 339736. 3. Kikushi H., Sasaki K., Sekuya J., Amagai Α., Kubokara Y., Oshima Y. Structural requirements of dictopyrones isoleted from Dictyostellium spp. In the regulation of Dictyostellium developed and in antileukemic activity // Bioorg. Med. Chem. - 2004. Vol. 12, №12. - P.3203-3214. 4. Kawonaka Y., Kobayashi K., Kusuda S., Tatsumi Т., Murota M., Nishiyama Т., Hisaishi K., Fujii 7 46588 Α., Hirai K., Nishizaki M., Naka M., Komeno M., Nakai H., Toda M. Design and synthesis of orally bioavailable inhibitors of inducible nitric oxide synthase, synthesis and biological evaluation of dihydropyridin-2(1H)imines and 1,5,6,7-tetrahydro2H-azepin-2-imines // Bioorg. Med. Chem. - 2003. Vol.11, №5. - P.682-702. 5. Ahmad V.U., Nasir M.A. Androchine, an alkaloid from Androchne aspera // Phytochemistry. 1987. - Vol.26. - P.585-586. 6. Smoth R.M. Pipermethystine, a novel pyridone alkaloid from piper methysticum // Tetrahedron. 1979. - Vol.35, №3. - P.437-439. 7. Hootele C, Colau В., Halin F. Sedum alkaloids. III. A revisez structure for sedinine // Tetrahedron Lett.- 1980. - Vol.21, №52. - P.5063-5066. 8. Boll P/M/, Hansen J., Simonsen O. Synthesis and molecular structure of piplartine (= piperlongumine) // Tetrahedron.-1984. - Vol.40, №1. P.171-175. 9. Filler R., Kobayashi Y., Yagupolski L.M. Organofluorine compounds in medicinal chemistry Комп’ютерна верстка О. Рябко 8 and biomedical applications.- Elsevier, Amsterdam. 1993. 10. Sukach V., Golovach N., Pirozhenko V., Rusanov E., Vovk M.V. Convenient enantioselective synthesis of β-trifluoromethyl-β-amino-kethones by asymmetric Mannich reaction of aryl trifluoromethyl ketimines with acetone // Tetrahedron: Asymmerty. 2008. - Vol.19. - P.761-764. 11. Fissiuk A.S., Vorontsova M.A., Sagitullin R.S. A new synthesis of 3-phenyl-5,6-dihydropyridin-2(1H)ones // Mendeleev Commun. -1993, №6. - P.249-251. 12.Фисюк А.С., Воронцова М.А., Иванов С.А. Новый синтез З-арил-5,6-дигидропиридин-2(1Н)онов // Химия гетероцикл. соед. - 1994. - №6. С.812-815. 13. Fisyuk A.S., Poendaev N.N., Bundel' Y.G. A new route for synthesis of 5,6-dihydropyridin-2(1H)ones, 2-pyridones and (4-hydroxy-2-oxopiperid-3-yl)pyridinium chlorides by intramolecular cyclization of N-3-oxoalkylchloroacetamide derivatives // Mendeleev Commun. - 1998. - №1. - P.12-13. Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of s(+)-6-aryl-(trifluoro)acetyl-6-trifluoromethyl-5-6-dihydropyridine-2(1h)-ones
Автори англійськоюVovk Mykhailo Volodymyrovych, Sukach Volodymyr Andriiovych, Holovach Natalia Mykhailivna
Назва патенту російськоюСпособ получения эс(+)-6-арил-3-(трифторо)ацетил-6-трифторометил-5,6- дигидропиридин-2(1н)-онов
Автори російськоюВовк Михаил Владимирович, Сукач Владимир Андреевич, Головач Наталия Михайловна
МПК / Мітки
МПК: C07B 53/00, C07D 213/00
Мітки: одержання, спосіб, s(+)-6-арил-3-(трифторо)ацетил-6-трифторометил-5,6-дигідропіридин-2(1н)-онів
Код посилання
<a href="https://ua.patents.su/4-46588-sposib-oderzhannya-s-6-aril-3-triftoroacetil-6-triftorometil-56-digidropiridin-21n-oniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб одержання s(+)-6-арил-3-(трифторо)ацетил-6-трифторометил-5,6-дигідропіридин-2(1н)-онів</a>
Попередній патент: Спосіб об’єктивізації м’язового тестування інвалідів
Наступний патент: Спосіб одержання 6-ариліміно[1,3,5]триазино[2,1-а]ізоіндол-2,4 (3н,6н)-діонів
Випадковий патент: Спосіб отримання специфічного імуноглобуліну людини проти вірусу гепатиту с (hcv)








