Спосіб отримання 5-алкілозаміщених 4,5,6,7-тетрагідро-1,2,4-триазоло[1,5-а]піримідин-5-тіонів
Номер патенту: 58287
Опубліковано: 11.04.2011
Автори: Афанасіаді Людмила Михайлівна, Комихов Сергій Олександрович, Петрова Марина Генадіївна, Десенко Сергій Михайлович
Формула / Реферат
Спосіб отримання 5-алкілозаміщених 4,5,6,7-тетрагідро-1,2,4-триазоло[1,5-а]піримідин-5-тіонів
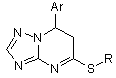 , І
, І
де Аr=Ph, С6Н4ОСН3-4, С6Н4Сl-4, С6Н4СН3-4, С6Н4ОСН3-2, С6Н4Сl-2, С6Н4СН3-2;
R=СН3, С2Н5, СН2С6Н4СН3-4, СН2С6Н4СН3-3, CH2COPh, СН2СНС6Н4Сl-4, СН2СНС6Н4ОСН3-4, CH2CONHPh, CH2CONHC6H4OCH3-4, який включає алкілування 4,5,6,7-тетрагідро-1,2,4-триазоло[1,5-а]піримідин-5-тіонів у розчиннику, який відрізняється тим, що як алкілуючий агент використовують рівномолярні кількості алкілгалогенідів, алкілування проводять при кімнатній температурі у середовищі етилового спирту за присутності етилату натрію протягом 3-5 хвилин до утворення цільової структури.
Текст
Спосіб отримання 5-алкілозаміщених 4,5,6,7тетрагідро-1,2,4-триазоло[1,5-а]піримідин-5-тіонів Ar 2 де Аr=Ph, С6Н4ОСН3-4, С6Н4Сl-4, С6Н4СН3-4, С6Н4ОСН3-2, С6Н4Сl-2, С6Н4СН3-2; R=СН3, С2Н5, СН2С6Н4СН3-4, СН2С6Н4СН3-3, CH2COPh, СН2СНС6Н4Сl-4, СН2СНС6Н4ОСН3-4, CH2CONHPh, CH2CONHC6H4OCH3-4, який включає алкілування 4,5,6,7-тетрагідро-1,2,4-триазоло[1,5а]піримідин-5-тіонів у розчиннику, який відрізняється тим, що як алкілуючий агент використовують рівномолярні кількості алкілгалогенідів, алкілування проводять при кімнатній температурі у середовищі етилового спирту за присутності етилату натрію протягом 3-5 хвилин до утворення цільової структури. N N R S ,І N N S R І де Аr=Ph, C6H4OCH3-4, С6Н4Сl-4, С6Н4СН3-4, С6Н4ОСН3-2, С6Н4Сl-2, С6Н4СН3-2; R=СН3, С2Н5, СН2С6Н4СН3-4, СН2С6Н4СН3-3, CH2COPh, СН2СНС6Н4Сl-4, СН2СНС6Н4ОСН3-4, CH2CONHPh, CH2CONHC6H4OCH3-4. Складні нітрогенвмісні сполуки, що за своєю будовою містять піримідиновий і азольний цикли, достатньо довго привертають увагу хіміківсинтетиків. Це зумовлене їх широким розповсюдженням у природі та першоступеневою важливістю для живих організмів. Враховуючи, що похідні піримідинів входять до складу нуклеїнових кислот, пошук та дослідження лікарських форм в ряду аналогів азагетероциклів, які входять до складу Ph N N N N CH3 Ph II (11) N N UA Ar ДНК та є ефективними у боротьбі з онкологічними захворюваннями, є вельми актуальною задачею. Похідні піримідинів є основою субстанцій багатьох лікарських препаратів, які успішно використовуються при лікуванні захворювань ендокринної та серцево-судинної систем, ефективні при лікуванні захворювань, викликаних вірусом ВІЛ [заявка ЕР 203721, C07D 473/06, заявка ЕР 267607, C07D 473/06], мають антидепресивні властивості [US Patent 5.290.782, C07D 473/02], проявляють гіпнотичну, антиалергічну активності [BaziardMongsset G. et al, Eur. J. Med. Chem., 30, No. 3, 253 (1995)], мають діуретичний ефект. Відомий спосіб отримання структурного аналога сполук І - 4-метил-5,7-дифеніл-4,7-дигідро-1,2,4триазоло [1,5-а]піримідину формули II [Десенко С.М., Орлов В.Л, Липсон В.В., Химия гетероцикл. соедин., 1990, № 12. - С. 1638-1642]. (19) Корисна модель належить до галузі органічної хімії, а саме до технології одержання 5алкілзаміщених 4,5,6,7-тетрагідро-1,2,4триазоло[1,5-а]піримідин-5-тіонів загальної формули І 58287 (13) N U N 3 58287 Спосіб складається здійснюється за схемою: з однієї стадії Ph Ph N N N та + N H CH3I Ph DMF N N KON N N Ph CH3 До суспензії 0,9 г КОН у 10 мл ДМФА додають 0,82 г (3 ммоль) 5,7-дифеніл-4,7-дигідро-1,2,4триазоло[1,5-а]піримідину та 0,85 г (6 ммоль) метиліодиду. Суміш перемішують дві години при кімнатній температурі, змішують з 50 мл води та нейтралізують оцтовою кислотою. Отриманий розчин екстрагують хлороформом, екстракт випаровують, залишок хроматографують на колоні з Аl2О3 (елюент - ацетон). Вихід 4-метил-5,7дифеніл-4,7-дигідро-1,2,4-триазоло[1,5а]піримідину складає 86 %. Час реакції з урахуванням хроматографічної очистки ~ 4-5 годин. Недоліком відомого способу алкілування триазолопіримідинів є те, що процес алкілування йде тільки по атому Нітрогену (4-те положення) піримідинового фрагмента. Процеси Салкілування, за ствердженням авторів, не протікають. Відомий спосіб не дає можливості алкілувати триазолопіримідини як по заміснику у 5му положенні, так і по атому Карбону у 6-му положенні азолопіримідинового біциклу. Крім того, процес алкілування є тривалим, приблизно 4-5 годин, потребує хроматографічної очистки. Авторами описані лише два приклади отриманих сполук, тобто даний спосіб не є універсальнi: описані сполуки отримані з використанням лише одного алкілуючого реагента метиліодиду. Відомий спосіб отримання структурного аналога сполук І - 3-(4,7-дигідро-5,7-дифеніл-1,2,4триазоло[1,5-а]піримідин-6-іл)-1,3-діарил-1пропанонів формули III Ar Ar N N N N NH Ph Ar' O Ar' III де Аr, Аr'=Ph, 4-CH3C6H4, 4-СН3ОС6Н4, 4СlС6Н4 та ін. [V. Lipson, I. Ignatenko, J. Heterocyclic Chem., 40, 1081 (2003)]. Спосіб являє собою алкілування 5,7-діарил4,7-дигідро-1,2,4-триазоло[1,5-а]піримідинів халконами, складається з однієї стадії та здійснюється за схемою: Ar N Ar Ar N N NaOEt + N H Ph Ar' O Ar' EtOH Ar N N N N NH Ph Ar' O Ar' Розчин 0,08 г (1,5 ммоль) метилату натрія, 0,3 г (1,1 ммоль) 4,7-дигідро-5,7-дифеніл-1,2,4триазоло[1,5-а]піримідину та 1,2 ммоль ,ненасиченого кетону (халкону) у 10 мл метанолу нагрівають 2 години. Після охолодження 4 відфільтровують сполуку, промивають метанолом, сушать та перекристалізовують із суміші метанолу та диметилформаміду (2:1). Виходи 3-(4,7-дигідро5,7-дифеніл-1,2,4-триазоло[1,5-а]піримідин-6-іл)1,3-ДІарил-1-пропанонів складають 46-48 %. Час перебігу реакції з урахуванням очистки складає приблизно 4-5 годин. Недоліком способу алкілування сполук формули III є обмеження вибору алкілуючого агента, у якості якого можна використовувати тільки ,ненасичені кетони (халкони). Кінцеві алкіловані триазолопіримідини мають високі молекулярні маси (>500), що робить їх малоперспективними у пошуці нових фізіологічно активних сполук. Крім того, у такий спосіб алкілування проходить тільки по атому карбону, тоді як замісник у 5му положенні азолопіримідинового біциклу не алкілується. Використання у якості розчинника сильнотоксичного метанолу, очистка кінцевих продуктів кристалізацією, тривалість процесу також слід віднести до недоліків даного способу. Неуніверсальність способу алкілування триазолопіримідинів обмежує його використання навіть у лабораторних умовах. У основу корисної моделі поставлено завдання розробки універсального способу алкілування 5-тіонозаміщених 4,5,6,7-тетрагідро-1,2,4триазоло[1,5-а]піримідинів, що дозволяє скоротити час синтезу, підвищити якість кінцевих продуктів. Вирішення поставленої задачі забезпечується тим, що за способом отримання 5-алкілзаміщених 4,5,6,7-тетрагідро-1,2,4-триазоло[1,5-а]піримідин5-тіонів, згідно корисної моделі, проводять алкілування рівномолярних кількостей 4,5,6,7тетрагідро-1,2,4-триазоло[1,5-а]піримідин-5-тіонів з алкілуючими реагентами при кімнатній температурі у середовищі етилового спирту за присутністю етилату натрію протягом 3-5 хвилин до утворення цільової сполуки. У якості алкілуючого реагента використовують: 1) алкілгалогеніди, 2) заміщені фенацилгалогеніди, 3) заміщені алкіл- та ариламіди галогенооцтових кислот. Залежно від замісників у арильній складовій (Аr) та алкілуючого реагента спосіб, що заявляється, дозволяє широко модифікувати хімічну структуру кінцевих продуктів та отримувати велику кількість алкілзаміщених триазолопіримідинів - потенційно фізіологічно активних сполук. Проведення реакції в умовах, що заявляються, забезпечує високу швидкість її протікання (3-5 хв) у межах заявленого температурного режиму (18-25°). Підвищення температури вище кімнатної є недоцільним, що виключає використання енергоресурсів. За необхідності можлива розробка виробничої методики, що не потребує суттєвих затрат робочого часу та енергоресурсів. Продукти алкілування за заявленим способом отримуються чистими, з достатньо високими виходами та легко виділяються фільтрацією. У таблиці 1 наведені порівняльні характеристики заявленого способу алкілування триазолопіримідинів та способів-аналогів. 5 58287 Спосіб, що заявляється, здійснюється за схемою: Ar Ar N N N + N H RX S NaOEt N N EtOH N N S R де Аr=Ph, С6Н4ОСН3-4, С6H4Cl-4, С6Н4СН3-4, С6Н4ОСН3-2, С6Н4Сl-2, С6Н4СН3-2; R=СН3, С2Н5, СН2С6Н4СН3-4, СН2С6Н4СН3-3, CH2COPh, СН2СНС6Н4Сl-4, СН2СНС6Н4ОСН3-4, CH2CONHPh, CH2CONHC6H4OCH3-4. X=Сl, Br, I Заміщений 4,5,6,7-тетрагідро-1,2,4триазоло[1,5-а]піримідин-5-тіон (0,9 моль) розчиняють у 10 мл розчину 1 ммоль етилату натрію (у якості каталізатора) в етанолі, при перемішуванні додають 1 ммоль алкілуючого агента. Витримують реакційну суміш 3-5 хвилин при перемішування при кімнатній температурі. Осад, що випав, відфільтровують, сушать. Нижче наведені приклади конкретного виконання. Приклад 1. Отримання 7-феніл-5-фенацилтіо6,7-дигідро-1,2,4-триазоло[1,5-а]піримідину 200 мг (0,9 ммоль) 7-феніл-4,5,6,7-тетрагідро1,2,4-триазоло[1,5-а]піримідин-5-тіону розчиняють у 10 мл розчину 1 ммоль етилату натрію в етанолі, при перемішуванні додають 1 ммоль алкілуючого реагента - енацилброміду. Осад, що випав протягом 3-4 хвилин, відфільтровують. Вихід 250 мг (80 %). Т. пл. >200 С (розкл). Спекр ЯМР 1Н: 3.19 (1H, НА, 2JAB=17.2 Hz, 3 JAX=4.6 Hz), 3.60 (1H, НB, 3JBX=7.8 Hz), 4.86 (2H, s, CH2), 5.70 (1H, HX),7.07 (2H, m), 7.32 (3H, m), 7.52 (2H, m), 7.59 (1H, m), 7.82 (1H, s, 2-H), 8.03 (2H, m). 6 Приклад 2. Отримання 7-феніл-5-метилтіо-6,7дигідро-1,2,4-триазоло [1,5-а] піримідину 200 мг (0,9 ммоль) 7-феніл-4,5,6,7-тетрагідро1,2,4-триазоло[1,5-а]піримідин-5-тіону розчиняють у 10 мл розчину 1 ммоль етилату натрію в етанолі, при перемішуванні додають 1 ммоль алкілуючого реагента - метиліодиду. Осад, що випав протягом 3-4 хвилин, відфільтровують. Вихід 170 мг (77 %). Т. пл. 152-154 °С. Спекр ЯМР 1Н: 2.48 (3Н, s, СН3), 3.12 (1Н, НА, 2 JAB=17.2 Hz, 3JAX=4.6 Hz), 3.52 (1H, HB, 3JBX=7.6 Hz), 5.69 (1H, HX), 7.03 (2H, m), 7.32 (3H,m), 7.86 (1H, s, 2-H). Приклад 3. Отримання N-феніл-2-(7-(4метоксифеніл)-6,7-дигідро-1,2,4-триазоло[1,5a]піримідин-5-ілсульфаніл)-ацетаміду 235 мг (0,9 ммоль) 7-(4-метоксифеніл)-4,5,6,7тетрагідро-1,2,4-триазоло[1,5-а]піримідин-5-тіону розчиняють у 10 мл розчину 1 ммоль етилату натрію в етанолі, при перемішуванні додають 1 моль алкілуючого реагента ариламіду хлорооцтової кислоти. Осад, що випав протягом 35 хвилин, відфільтровують. Вихід 290 мг (82 %). Т. пл. 102-104 °С (розкл). Спекр ЯМR 1Н: 3.19 (1H, НА, 2JAB=17.0 Hz, 3 JAX=5.0 Hz), 3.53 (1H, Нв, 3JBX=7.8 Hz), 4.18 (2H, s, CH2), 5.65 (1H, HX), 6.90 (2H, m), 7.02 (3H, m), 7.30 (2H, m), 7.59 (1H, m), 7.54 (2H, m), 7.85 (1H, s, 2-H). Як видно з тексту матеріалів, що заявляються, запропоноване технічне рішення має наступні переваги: - тривалість технологічного процесу складає 35 хвилин (за способами-аналогами 4-5 годин); - спосіб алкілування, що заявляється, дозволяє отримувати чисті продукти, що не потребують перекристалізації; - дозволяє широко варіювати замісники як у арильній, так і у тіоновій складових. Таблиця 1 Найменування показника Кількість стадій Тривалість процесу, год Виходи цільових продуктів, % 1 Аналог за статею [Десенко С.М., Орлов В.Л., Липсон В.В., Химия гетероцикл. соедин., 1990, № 12.-С. 1638-1642] 1 3-5 хвилин 4-5 години 4-5 годин 77-82 70-73 37-38 Спосіб, що заявляється Розчинник етиловий спирт Каталізатор Чистота цільових продуктів етилат натрію не потребує кристалізації етиловий спирт або диметилформамід гідроксид натрію потребує кристалізації або хроматографування Інше метод дозволяє використання алкілуючих реагентів різної природи метод не є універсальним передбачає використання лише одного алкілуючого реагенту (метиліодиду) Аналог за статею [V. Lipson, І. Ignatenko, J. Heterocyclic Chem., 40, 1081 (2003)] 1 метанол етилат натрію потребує кристалізації продукти мають високу молекулярну масу (>500) та є малопридатними для вивчення фізіологічної активності 7 Комп’ютерна верстка Д. Шеверун 58287 8 Підписне Тираж 23 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюProcess for the preparation of 5-alkylthiosubstituted 4,5,6,7-dihydro-1,2,4-triazolo[1,5-a]pyrimidin-5-thiones
Автори англійськоюKomikhov Serhii Oleksandrovych, Petrova Maryna Hennadiivna, Desenko Serhii Mykhailovych, Afanasiadi Liudmyla Mykhailivna
Назва патенту російськоюСпособ получения 5-алкилозамещенных 4,5,6,7-тетрагидро-1,2,4-триазоло[1,5-а]пиримидин-5-тионов
Автори російськоюКомихов Сергей Александрович, Петрова Марина Геннадиевна, Дэсэнко Сергей Михайлович, Афанасиади Людмила Михайловна
МПК / Мітки
МПК: C07D 471/00
Мітки: 4,5,6,7-тетрагідро-1,2,4-триазоло[1,5-а]піримідин-5-тіонів, отримання, 5-алкілозаміщених, спосіб
Код посилання
<a href="https://ua.patents.su/4-58287-sposib-otrimannya-5-alkilozamishhenikh-4567-tetragidro-124-triazolo15-apirimidin-5-tioniv.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання 5-алкілозаміщених 4,5,6,7-тетрагідро-1,2,4-триазоло[1,5-а]піримідин-5-тіонів</a>
Попередній патент: Біофільтр
Наступний патент: Пристрій вимірювання рівня
Випадковий патент: Композиція інгредієнтів для приготування пшеничного хліба








