Спосіб отримання речовини з протипухлинною активністю 1,1′-(2″-бром-2″-хлоретеніл)-біс-(6-метилурацил)
Формула / Реферат
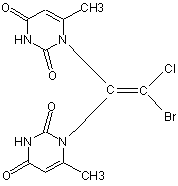
Спосіб отримання речовини з протипухлинною активністю 1,1'-(2"-бром-2"- хлоретеніл)-біс-(6-метилурацил) шляхом взаємодії 6-метилурацилу з фторотаном (молярне співвідношення 2:1,5) в системі розчинників (бензол-диметилформамід) в умовах міжфазного каталізу дибензо-18-краун-6-ефіром в присутності гідроксиду калію
 .
.
Текст
Спосіб отримання речовини з протипухлинною активністю 1,1'-(2"-бром-2"- хлоретеніл)-біс-(6метилурацил) шляхом взаємодії 6-метилурацилу з фторотаном (молярне співвідношення 2:1,5) в системі розчинників (бензол-диметилформамід) в умовах міжфазного каталізу дибензо-18-краун-6ефіром в присутності гідроксиду калію Корисна модель відноситься до хімії гетероциклічних сполук, а саме, до 1,1'-(2"-бром-2"хлоретеніл)-біс-(6-метилурацил)-у (далі, сполука), яка може бути використана у якості субстанції для виготовлення протипухлинного лікарського засобу, та способу його отримання. Сполука має виражену протипухлинну активність, яка досліджена на моделях експериментального пухлинного зросту різного гістогенезу: Лімфосаркомі Пліса, Карциномі Герена, Саркомі 45. Вказана властивість дозволяє передбачити можливість використання синтезованої сполуки в практичній медицині, а саме, в онкології. Структурні аналоги (біциклічні адукти), які мають протипухлинну активність, не відомі (літературний опис відсутній). Однак, структурними компонентами молекули біциклічного адукту- сполуки є дві молекули 6метилурацилу та фрагмент молекули фторогану (2-бром-1,1,1 -трифтор-2-хлоретан), які застосовуються у якості лікарських засобів при лікуванні онкологічних захворювань. Після синтезу похідних урацилу, а особливо, 5-фторурацилу та фторафуру, які продемонстрували високу протипухлинну активність, значно зросла кількість досліджень з цього напрямку. Починаючи з 1981 року в світі щорічно публікують біля 100 наукових робіт та патентів, які стосуються методів синтезу, вивчення будови й хімічних властивостей урацилу та його похідних. За останні роки кількість публікацій на дану тему зросла до 130-150 на рік. Серед них біля половини присвячена 5-фторурацилу та сполукам, які створені на його основі. Стало відомо, що пухлини використовують молекули урацилу активніше, ніж нормальні клітини. Оскільки ван-дер-ваальсові радіуси водню та фтору близькі, можна очікувати, що 5-фторурацил (або його похідне) буде виконувати роль субстрату та/або інгібітору ферментів і буде переважно поглинатися тканинами пухлини. З іншого боку, молекули 5 (б)-заміщеного урацилу та його похідних, інших гало-геновмісних гетероциклів, здатні виконувати роль фтор(галоген)вмісних синтонів в органічному синтезі з метою створення оригінальних біологічноактивних молекул. Введення фтор(галоген)вмісних фармакофорів в гетероциклічну молекулу призводить до підвищення розчинності сполук в ліпідах та робить лікарські засоби ефективнішими у зв'язку із легкістю їх транспорту в організмі [1, 2]. В основу корисної моделі поставлено розробку способу отримання 1,1'-(2"-бром-2"-хлоретеніл)біс-(6-метилурацил)-у, який має протипухлинну активність, шляхом взаємодії відомого реагенту та •СІ с=с Вг снз О) 00 (О о> 6891 складової лікарських засобів 6-метилурацилу з фторотаном у молярному співвідношенні 2:1,5. Реакції проводилися у системі розчинників (бензол-диметилформамід) в умовах міжфазного каталізу дибензо-18-краун-6-ефіром в лужному середовищі з метою забезпечення отримання 1,1і(2"-бром-2"-хлоретеніл)-біс-(6-метилурацил)-у, який має протипухлинну активність. Спосіб отримання був розроблений під час виконання дисертаційної роботи [3, 4]. 1,1 '-(2"-бром-2"-хлоретеніл)-біс-(6метилурацил) отримують взаємодією 6метилурацилу з фторотаном (молярне співвідношення 2:1,5). Реакція проводиться в системі розчинників (бензол - диметилформамід) в умовах міжфазного каталізу дибензо-18-краун-б-ефіром в присутності гідроксиду калію. Практичний вихід 43%. Методика синтезу 1,1'-(2"-бром-2"-хлорегеніл)біс-(б-метилурацил)-у. Приготування розчину №1. 0,5г гідроксиду калію (0,008моль), 0,05г дибензо-18-краун-б-ефіру, Юмл сухого бензолу перемішують при температурі 60°С біля 15 хвилин до утворення на синках хімічного реактора білого полімерного нальоту, тобто утворення калієвого комплексу з дибензо-18-краун-б-ефіром. Отриманий розчин охолоджують до кімнатної температури, додають до нього краплями розчин 2,43г (0,012 моль) фторотану в 20мл діетилового ефіру. Приготування розчину №2. 1,6г (0,006 моль) 6-метилурацилу розчиняють в 50мл диметилформаміду при температурі 60°С в окремому хімічному посуді. Гарячий розчин №2 додають краплями через ділильну лійку до розчину № 1, перемішують при температурі 80-90°С 6 годин, фільтрують у гарячому стані, відганяють простою перегонкою розчинники. Залишок обробляють безводними гексаном, бензолом. Отриманий осад фільтрують, промивають гарячим безводним гексаном, перекристалізовують із суміші гексан-етанол (1:1). Сушать у вакуумі водострумного насосу. Практичний вихід 1,05г (43%). Т. пл. 286289°С. Y сю Індивідуальність синтезованої сполуки контролювали методом тонкошарової хроматографії, склад підтверджували даними елементного аналізу. Спектр ПМР синтезованої сполуки І записували на приладах "Bruker WP-200" (виробник "Bruker", Switzerland), "Varian T-60" (виробник "Varian", USA) з робочою частотою 200-132МГц у виді розчинів ДМСО-De та CFBr3 (внутрішні стандарти ТМС та ГМДС). ІЧ-спектр записували на спектрофотометрі UR-20 (виробник "Charles Ceise Hena", Germany). ТШХ виконували на пластинах Silufol-254. ГРХ визначали на газорідинному хроматограф і "Perk in ЕІтеґз УФ-детектором (виробник "Perkin", Germany). Хроматограма, ІЧ-, ПМР-спектри кінцевого продукту ідентифікували у порівнянні з хроматограмами, ІЧ-, ПМР-спектрами вихідних сполук. Синтезована сполука - це кристалічний порошок жовтого забарвлення, нестійкий до дії гарячого органічного розчинника; при перекристалізації він розпадаються до вихідного урацилу. Дані елементного аналізу на С, Н, N синтезованої сполуки відповідають розрахованим значенням. ІЧ-спектр синтезованої сполуки характеризуються інтенсивними сигналами карбонільних груп С=О гетероциклічних фрагментів молекули при 1710, 1750см"1. В ІЧ-спектрі синтезованої сполуки ідентифіковано сигнали галогенів (F, Вг, СІ) при 515, 550, 690, 850см'1. Співвідношення інтегральних інтенсивностей сигналів в ПМР-спектрі синтезованої сполуки підтверджує відсутність протонів у атомів N(1) молекули урацилу при 11.00-11.25 м. д. (малюнок 1). Фізико-хімічні характеристики та дані елементного аналізу синтезованої сполуки наведено в таблиці 1. Таблиця 1 Фізико-хімічні характеристики та дані елементного аналізу сполуки І. Знайдено, у% CHN Бруттоформула 38,83,2 14,8 Ci2HioN404BrCI Обчислено, у%, СН N 37,1 2,58 14,38 ІЧ-спектр (КВг), см' 1 7 С-НаІ. 7 С=О 515,550,690,850 (С-СІ, С-Вг); 960-970 (trans -С=С-): 1710, 1750 (С=О); 2800-3000 (СНз) Завданням корисної моделі є синтез нових хімічних сполук, які мають підвищену протипухлинну Спектр ПМР (ДМСО-De), 5, M.fl.(J, Гц) 2.004(6Н, с.,2 СНз),5.313(2Н,с, 2С(5)-Н), 10.832(2Н,д.,2 N(3) H,J H ,H 4 9,6ГЦ) активність під час лікування Лімфосаркоми Пліса, Карциноми Герена, Саркоми 45. 6891 Вивчення фізіологічної активності біциклічного адукту - синтезованої сполуки проводилося згідно із літературними вказівками у відділі онкофармакології Інституту фармакології та токсикології АМН України [5, 6]. Протипухлинна активність вивчена на перевивних моделях експериментального пухлинного росту різного гістогенезу : Саркома 45, Лімфосаокома Пліса, Карцинома Герена. Література 1. Соединения фтора. Синтез и применение./ Под ред. П. Исикава. - М.: Мир, 1990. - Гл.5. С. 183-265. 2. Ягупольский Л.М.// Ароматические и гетероциклические соединения с фторсодержащими заместителями. - Киев: Наукова думка, 1988. С.90-105. 3. Вельчинская Е.В., Радченко О.А., Ильченко А.Я. Полифторзамещенные алкины и алкадииновые кислоты. III. Замещенные пропаргиловые эфиры и их реакции.// ЖОрХ. - 1992. - Т.28. Вып.6.-С.1120-1125. 4. Вельчинська О.В. Поліфторозаміщені кисневмісні мето- та діацетиленові сполуки. //Автореферат дис. ... канд. хім. наук. - К., 1992. 16с. 5. Прозоровский В.Б., Прозоровский В.П., Демченко В.М. Експрес метод визначення середньої ефективності дози та її помилки. // Фармакол. та токсикол. -1978. - Вип.4. - С.497. 6. Експериментальна оцінка протипухлинних препаратів в СРСР та СПІА. М.: Медицина, 1979. 286с. L-J Комп'ютерна верстка В. Мацело Підписне Тираж 28 прим. Міністерство освіти і науки України Державний департамент інтелектуальної' власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП "Український інститут промислової власності", вул. Глазунова, 1, м. Київ - 4 2 , 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for the preparation of substance with antitumor activity 1,1'-(2"-bromine-2"- chloroethenyl)-bis-(6-methyluracil)
Автори англійськоюVelchynska Olena Vasylivna
Назва патенту російськоюСпособ получения вещества с противоопухолевой активностью 1,1'-(2"-бром-2"-хлорэтенил)-бис-(6-метилурацил)
Автори російськоюВельчинская Елена Васильевна
МПК / Мітки
МПК: A61P 35/00, C07D 239/54, A61K 31/506, C07C 21/00
Мітки: активністю, протипухлинною, отримання, речовини, 1,1'-(2"-бром-2"-хлоретеніл)-біс-(6-метилурацил, спосіб
Код посилання
<a href="https://ua.patents.su/4-6891-sposib-otrimannya-rechovini-z-protipukhlinnoyu-aktivnistyu-11-2-brom-2-khloretenil-bis-6-metiluracil.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання речовини з протипухлинною активністю 1,1′-(2″-бром-2″-хлоретеніл)-біс-(6-метилурацил)</a>
Попередній патент: Апарат для обробки дисперсних матеріалів
Наступний патент: Спосіб отримання речовини з протипухлинною активністю 1,1′-/2″-хлоретеніл/-біс-/бензімідазол/
Випадковий патент: Спосіб підвищення стійкості ґрунтів відвалів і звалищ








