Спосіб отримання (е)-5-(2-бромвініл)-2′-дезоксіуридину
Номер патенту: 75110
Опубліковано: 15.03.2006
Автори: Манціні Стефано, Туроцці Даміано, Маджі Карло Альберто, Салімбені Альдо
Формула / Реферат
1. Спосіб отримання (Е)-5-(2-бромвініл)-2'-β-дезоксіуридину формули І
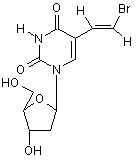 , (I)
, (I)
в якому
а) здійснюють реакцію сполуки формули II
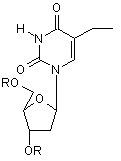 , (II)
, (II)
в якій R є алканоїльною С1-С8 групою, бензоїльною групою або бензоїльною групою, заміщеною в параположенні С1-С4 алкільною групою, або атомом галогену, з бромувальним засобом у присутності ініціатора радикалів, у вільному від галогену розчиннику, вибраному з алкільного естеру або циклічного етеру;
b) здійснюють дегідробромування отриманої сполуки формули (III)
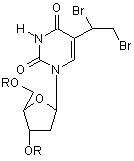 , (III)
, (III)
де R визначено вище, з або без основ, у вільному від галогену розчиннику для отримання інтермедіату формули (IV)
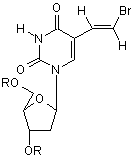 , (IV)
, (IV)
де R визначено вище;
с) знімають захист з інтермедіату формули (IV).
2. Спосіб за п. 1, в якому бромування на етапі а) здійснюють у вільному від галогену розчиннику, вибраному з групи, що складається з метилу, етилу, n-пропілу, ізопропілу, n-бутилу, ізобутилацетату, 1,4-діоксану.
3. Спосіб за п. 1 або 2, в якому при реакції сполуки формули II, R є групою 4-СlС6Н4СО.
4. Спосіб за п. 1 або 2, де реакцію здійснюють з молекулярним бромом у присутності ініціатора радикалів.
5. Спосіб за п. 1 або 2, де реакцію здійснюють з N-бромсукцинімідом у присутності ініціатора радикалів.
6. Спосіб за п. 1 або 2, де реакцію здійснюють з N-бромсукцинімідом у присутності 2,2'-азобісізобутиронітрилу (AIBN) в етилацетаті при температурі кипіння розчинника.
7. Спосіб за п. 1 або 2, де реакцію здійснюють з N-бромсукцинімідом у присутності AIBN в 1,4 діоксані при температурі 70-90°С.
8. Спосіб за будь-яким з вищезазначених пунктів, в якому дегідробромування на етапі b) здійснюють в етилацетаті або N,N-диметилформаміді або N,N- диметилацетаміді.
Текст
1. Спосіб отримання (Е)-5-(2-бромвініл)-2'- дезоксіуридину формули І O H Br 3 75110 4 де R визначено вище; 5. Спосіб за п. 1 або 2, де реакцію здійснюють з Nс) знімають захист з інтермедіату формули (IV). бромсукцинімідом у присутності ініціатора радика2. Спосіб за п. 1, в якому бромування на етапі а) лів. здійснюють у вільному від галогену розчиннику, 6. Спосіб за п. 1 або 2, де реакцію здійснюють з Nвибраному з групи, що складається з метилу, етибромсукцинімідом у присутності 2,2'лу, n-пропілу, ізопропілу, n-бутилу, ізобутилацетаазобісізобутиронітрилу (AIBN) в етилацетаті при ту, 1,4-діоксану. температурі кипіння розчинника. 3. Спосіб за п. 1 або 2, в якому при реакції сполуки 7. Спосіб за п. 1 або 2, де реакцію здійснюють з Nформули II, R є групою 4-СlС6Н4СО. бромсукцинімідом у присутності AIBN в 1,4 діоксані 4. Спосіб за п. 1 або 2, де реакцію здійснюють з при температурі 70-90°С. молекулярним бромом у присутності ініціатора 8. Спосіб за будь-яким з вищезазначених пунктів, в радикалів. якому дегідробромування на етапі b) здійснюють в етилацетаті або N,N-диметилформаміді або N,Nдиметилацетаміді. Цей винахід описує спосіб отримання (Е)-5-(2бромвініл)-2'-дезоксиуридину (Бривудину), де вільні від галогену розчинники використовують в усьому способі і, зокрема, на першому етапі бромування 5-етил-2'-дезоксиуридину діацилату. (Е)-5-(2-бромвініл)-2'-дезоксиуридин (Бривудин) формули l є сполукою, що характеризується сильною антивірусною активністю, зокрема, є придатною для лікування інфекцій Herpes Zoster. Перший спосіб синтезу описано в DE 2915254, який полягає в алкілуванні (Е)-5-(2бромвініл)урацилу з 1-хлор-2-дезокси-3,5-ди-O-ртолiл- -D-еритро-пентафуранозою, а і потім у деацилюванні для отримання сполуки формули І. Вадою цього способу є те, що синтез (Е)-5-(2бромвініл)урацилу є важким і має низький вихід. Крім того, сполука формули І, яку отримують у такий спосіб, не є чистою, а є сумішшю і ізомерів, яка в свою чергу має практичне значення і має бути виділена хроматографією. Інший спосіб описано в GB 2125399 (відповідає DE 3328238) і полягає у бромуванні сполук формули ІІ (де R є алканоїловою С1-С8 групою, бензоїловою групою або бензоїловою групою, заміщеною в пара позиції С1-С4 алкіловою групою або атомом галогену) бромом у галогенованому гідрокарбоновому розчиннику (як-то, 1,2-дихлоретан, метиленхлорид, хлороформ, тетрахлорид карбону) у присутності світла, для отримання дибромпохідного формули ІІІ (де R визначено вище). Тоді, зазначену сполуку ІІІ дегідробромінують у галогенованому гідрокарбоновому розчиннику, у присутності третинної основи, для отримання нуклеозиду формули ІV (де R визначено як для сполук формули ІІ), з виходом 62-69%: після видалення протектувальних груп, (Е)-5-(2-бромвініл)-2'-дезоксиуридин формули і отримують з виходом приблизно 93%. За останні роки бромхлорметан стали використовувати на практиці як розчинник вибору в радикальних реакціях, здійсненню якої сприяють термальні ініціатори, через їх відносно високу температуру кипіння (68°С) і через низьку токсич 5 75110 6 ність, у порівнянні з іншими галогенованими розазобісізобутиронітрилу (AlBN) в етилацетаті при чинниками, як-то, наприклад, хлороформ, карбону температурі кипіння розчиннику або реакція з Nтетрахлорид, 1,2-дихлоретан. Незважаючи на це, бромсукцинімідом у присутності ΑlΒΝ в 1,4 діоксані використання цього розчиннику було нещодавно при температур 70-90°С. заборонено, через ризик, пов'язаний із зменшенНа додаток до економічних переваг, що виням озонового шару [див. Постанову СЕЕ Європливають з низьких витрат, низької токсичності і з пейського Парламенту №2037/2000]. відповідності нормам захисту навколишнього сеНещодавно було виявлено, що Бривудин моредовища, як було описано вище, спосіб згідно з жна переважно отримати реакцією сполук формувинаходом також характеризується відносно висоли ll i lll, як описано вище, у розчиннику, вибраному кими виходами. Це досить несподіваний факт, з алкілових естерів або циклічних етерів. оскільки з хімічної літератури відомо, що більшість Використання вільних від галогену розчинників реакцій радикального бромування звичайно проє переважним, у порівнянні з використанням галоводять в галогенованих розчинниках: наприклад, у генованих розчинників, оскільки вони мають нижчу вищезгаданій заявці GB 2125399 описується лише токсичність, задовольняють Європейські стандарвикористання хлорувальних . розчинників для синти захисту навколишнього середовища і дають тезу Бривудину, у відповідності з загальними можливість зменшити приблизно на 50% промисзнаннями, наявними з рівня техніки. лові витрати. Крім того, не усі вільні від галогену розчинники Отже, винахід стосується способу, який поляможна переважно використовувати у способі сингає у: тезу і лише декілька з них дають задовольняючі a) радикальному бромуванні сполук формули ll результати. (в якій R визначено вище) за допомоги бромуваНаприклад, у способі отримання Бривудину, льного засобу у вільному від галогену розчиннику, описаному в DE 2915254, бромування (Е)-5-вінілвибраному з алкілових естерів та циклічних етерів, урацилу відбувається в безводному диметилфору присутності ініціатору радикалів, для отримання маміді. Однак, коли диметилформамід використосполук формули (lll), в якій R визначено вище; вувати у цьому способі на етапі бромування споb) дегідробромуванні у вільному від галогену лук формули ll, виходи перетворення будуть розчиннику, з або без основ, для отримання спонесподівано низькими, і буде утворюватися число лук формули lV, в якій R визначено вище; не точно визначених побічних продуктів. lншим c) знятті захисту для отримання сполуки форвільним від галогену розчинником, що інколи замули (l). Бажаною R групою є пара-хлор-бензоїл. стосовують у радикальному бромуванні, є ацетоніБромувальний засіб, яким може бути бром або трил [J.A.C.S. 1969 (91) 7398-740; J.A.C.S. 1971 N-бромсукцинімід, N-бромфталімід, 1,3-дибром(93) 5846-5850; J.A.C.S. 1974 (96) 5616-5617], але 5,5-диметилідантоїн, N-бромацетамід, Nцей розчинник також не давав задовольняючих броммалеїмід, N-бромсульфонамід, використовурезультатів у бромуванні сполук формули ll. Такі ж ють у молярному надлишку у межах 2-3, у порівне сприйнятливі результати отримують з етерних нянні зі сполукою ll. Бром і N-бромсукцинімід є зокрозчинників, як-то 1,2-диметоксіетан або метилцерема переважними. лозольв. До вільних від галогену розчинників для викоДалі, спосіб згідно з винаходом буде ілюстрористання на етапі а) належать алкілацетати, як-то вано у наступних прикладах. метил, етил, n-пропіл, ізопропіл, n-бутил, ізобутиВихідні інтермедіати формули ll (де R визналацетат або циклічний аліфатичний етер, як-то чено вище) отримують відомим способом, як опи1,4-діоксан, переважно у відношенні від 3:1 до сано в GB 2125399. 12:1, у порівнянні зі сполукою ll. Етилацетат і 1,4Приклад 1 діоксан є зокрема переважними. 10,0г (18,7ммоль) 3',5'-ди-О-р-хлорбензоїл-5Розчинником, який використовують для дегідетил-2'- -дезоксиуридину формули Н, де R=4робромування (етап b) є диметилформамід або СlСбН4СО, і 175мг (1,1ммоль) , 'диметилацетамід, або їм може бути такий же, який азоізобутиронітрилу (ΑlΒΝ) додають до 60мл етивикористовують на етапі бромування. Етилацетат і лацетату і суміш нагрівають під зворотним холоΝ,Ν-диметилформамід є зокрема переважними. дильником. 2,2'-Азобісізобутиронітрил (AlBN), 2,2'2,05мл (6,33г; 39,6ммоль) брому у 8мл етилаазобіс(2,4-диметилвалеронітрил), 2,2'-азобіс(2цетату додають краплями у суміш, в залежності метилбутиронітрил), азобісізовалеронітрил, 1,1'від витрачання галогенованого засобу (можна споазобіс-(циклогексанкарбонітрил), 2,2'-азобіс(2стерігати знебарвлення суміші). Розчин, отримаамідинопропан)гідрохлорид, диметил 2,2'ний в кінці додавання, нагрівають протягом ще азобісізобутират можуть бути використані як ініціа15хв., доки флегма зі зворотного кольору не стане тори радикалів. Азобісізонітрили є . бажаними, безбарвною. Розчинник випаровують під зниженим зокрема AlBN. тиском. Зазначені сполуки використовують в молярЗалишок, який складається з дибромпохідного ному процентному вмісті у межах 1-6% (3 і 6% для формули lll, де R=4-СlСбН4СО, дегідробромінують, ΑlΒΝ), у порівнянні зі сполукою ll. подібно до того, як описано, в GB 2125399, викоТемпература реакція складає межі від кімнатристовуючи ДМФ як розчинник. ної температури до температури кипіння розчин8,0г 3',5'-ди-О-р-хлорбензоїл-(Е)-5-(2нику, а час реакції складає межі від 15хв. до 4 гобромвініл)-2' -дезоксиуридину формули lV, де дин. Бажаними умовами є реакція з NR=4-СlСбН4СО, отримують (вихід: 70%), а потім бромсукцинімідом у присутності 2,2'деацилюють відомим способом, наприклад, як 7 75110 8 описано в GB 2125399. 4,1г (Е)-5-(2-бромвініл)-2'отримують (вихід: 94%). Приклад 4 -дезоксиуридину формули і отримують (вихід: Бромування здійснюють відповідно до прикла94%). ду 2 при температурі 80°С, використовуючи ізобуПриклад 2 тилацетат як розчинник. 10,0г (18,7ммоль) 3',5'-ди-O-р-хлорбензоїл-5Продовжуючи здійснювати процедуру, як опиетил-2'- -дезоксиуридину формули II, де R=4сано в прикладі 2, 9,0г сполуки формули IV, в якій СlСбН4СО, та 175мг (1,1ммоль) , 'R=4-СlСбН4СО, отримують (вихід: 79%), а тоді деазоізобутиронітрилу (ΑIΒΝ) додають до 60мл етиацилюють відомим способом, наприклад, як опилацетату і нагрівають під зворотним холодильнисано в GB 2125399. 4,6г сполуки формули i отриком. мують (вихід: 94%). 7,85г (44,1 моль) N-бромсукциніміду додають Приклад 5 до суміші відповідно до швидкості реакції (прибли10,0г (18,7ммоль) 3',5'-ди-О-р-хлорбензоїл-5зно 25хв.). В кінці додавання суміш нагрівають ще етил-2'-дезоксиуридину формули ll, де R=4протягом 15хв., доки вона не стане чистою. ЗалиСlСбН4СО, і 175мг (1,1ммоль) , 'шок, що складається з дибромпохідного формули азоізобутиронітрилу (ΑlΒΝ) додають до 25мл 1,4III, де R=4-СlСбН4СО, розчиняють в 60мл гарячого діоксану. Суміш нагрівають при 80°С, а тоді розчин AcOEt і 3,3мл (23,6ммоль) триетиламіну додають 8,5г (47,7ммоль) Ν-бромсукциніміду в 35мл 1,4краплями у розчин. Осад фільтрують і оброблюдіоксану додають краплями відповідно до швидкоють 80% EtOH. Нерозчинений матеріал, що скласті реакції (приблизно 30хв.). По завершенні додадається із сполуки формули IV, де R=4-СlСбН4СО, вання, розчин нагрівають ще протягом 15хв., доки фільтрують, промивають EtOH і висушують під він не стане безбарвним. Реакцію продовжують як зниженим тиском. 9,4г сполуки формули IV, де описано в прикладі 1; 8,8г сполуки формули lV, де R=4-СlСбН4СО, отримують (вихід: 82%), а потім R=4-СlСбН4СО, отримують (вихід: 77%), а тоді дедеацилюють відомим способом, наприклад, як ацилюють відомим способом, наприклад, як опиописано в GB 2125399. 4,8г сполуки формули ί сано в GB 2125399. 4,5г сполуки формули l отриотримують (вихід: 94%). мують (вихід: 94%). Приклад 3 Приклад 6 Бромування проводять відповідно до прикладу Слідуючи процедурі, описаній в прикладі 2 і 1 при температурі 80°С, використовуючи ізобутивикористовуючи етилацетат як розчинник, а 1,1'лацетат як розчинник. біс(циклогексанкарбонітрил) (270мг, 1,1ммоль) як Додавання розчину брому в ізобутилацетат ініціатор радикалів, 8,1г (71%) сполуки формули здійснюють у межах 20хв. В кінці додавання, розlV, де R=4-СlСбН4СО, отримують, а тоді деацилючин нагрівають протягом ще 15хв., доки він не стають відомим способом, наприклад, як описано в не безбарвним, тоді реакцію здійснюють як описаGB 1125399. 4,2г сполуки формули l отримують но у прикладі 2. 8,6г сполуки формули IV, де R=4(вихід: 95%). СlСбН4СО, отримують (вихід: 75%), а тоді деацилюють відомим способом, наприклад, як описано в GB 2125399. 4,4г (вихід: 94%) сполуки формули I Комп’ютерна верстка О. Гапоненко Підписне Тираж 26 прим. Міністерство освіти і науки України Державний департамент інтелектуальної власності, вул. Урицького, 45, м. Київ, МСП, 03680, Україна ДП “Український інститут промислової власності”, вул. Глазунова, 1, м. Київ – 42, 01601
ДивитисяДодаткова інформація
Назва патенту англійськоюA method for the preparation of (e)-5-(2-bromovynyl)-2'-deoxyuridine
Автори англійськоюMaggi Carlo Alberto
Назва патенту російськоюСпособ получения (е)-5-(2-бромвинил)-2'-дезоксиуридина
Автори російськоюМаджи Карло Альберто
МПК / Мітки
МПК: C07H 19/06, C07B 61/00, C07H 19/073
Мітки: отримання, спосіб, е)-5-(2-бромвініл)-2'-дезоксіуридину
Код посилання
<a href="https://ua.patents.su/4-75110-sposib-otrimannya-e-5-2-bromvinil-2-dezoksiuridinu.html" target="_blank" rel="follow" title="База патентів України">Спосіб отримання (е)-5-(2-бромвініл)-2′-дезоксіуридину</a>








