Пестицидні композиції
Номер патенту: 107566
Опубліковано: 26.01.2015
Автори: Крауз Гарі, Сіддалл Томас, Спаркс Томас, Браун Аннетт, Маклауд КаСандра
Формула / Реферат
1. Сполука загальної формули
 ,
,
де
(a) Аr1 являє собою заміщений або незаміщений феніл,
де вказаний заміщений феніл містить один або декілька замісників, незалежно вибраних із групи, яка включає С1-С6 галогеналкіл, С1-С6 алкокси, С1-С6 галогеналкокси, С(=О)(С1-С6 алкіл), (С1-С6 галогеналкіл)О(С1-С6 галогеналкіл)О або С1-С6 (гідрокси)галогеналкіл;
(b) Е являє собою N, С або CR5;
(c) G являє собою подвійний або потрійний зв'язок;
(d) М являє собою N, С або CR5 (за умови, що, коли Е являє собою атом азоту "N", тоді М являє собою атом азоту "N"; коли Е являє собою атом вуглецю "С", тоді М являє собою атом вуглецю "С"; і, коли Е являє собою "CR5", тоді М являє собою "CR5");
(e) Аr2 являє собою:
заміщений або незаміщений феніл,
де вказаний заміщений феніл містить один або декілька замісників, незалежно вибраних із групи, яка включає Н, F, Сl, Вr, І, CN, NO2, С1-С6 алкіл, С1-С6 галогеналкіл, С1-С6 гідроксіалкіл, С3-С6 циклоалкіл, С3-С6 галогенциклоалкіл, С3-С6 гідроксициклоалкіл, С3-С6 циклоалкокси, С3-С6 галогенциклоалкокси, С3-С6 гідроксициклоалкокси, С1-С6 алкокси, С1-С6 галогеналкокси, С2-С6 алкеніл, С2-С6 алкініл, S(=O)n(С1-С6 алкіл), S(=O)n(С1-С6 галогеналкіл), OSO2(С1-С6 алкіл), OSO2(С1-С6 галогеналкіл), С(=О)Н, C(=O)NRxRy, (С1-С6 алкіл)NRxRy, C(=O)(С1-С6 алкіл), С(=О)О(С1-С6 алкіл), С(=О)(С1-С6 галогеналкіл), С(=О)О(С1-С6 галогеналкіл), С(=О)(С3-С6 циклоалкіл), С(=О)О(С3-С6 циклоалкіл), С(=О)(С2-С6 алкеніл), С(=О)О(С2-С6 алкеніл), (С1-С6 алкіл)О(С1-С6 алкіл), (С1-С6 алкіл)S(С1-С6 алкіл), (С1-С6 галогеналкіл)О(С1-С6 галогеналкіл)О, С1-С6 (гідрокси)(галоген)алкіл, С(=О)( С1-С6 алкіл)С(=О)О(С1-С6 алкіл), феніл, фенокси, заміщений феніл і заміщений фенокси (де вказаний заміщений феніл і заміщений фенокси містять один або декілька замісників, незалежно вибраних із групи, яка включає Н, F, Сl, Вr, І, CN, NO2, С1-С6 алкіл, С1-С6 галогеналкіл, С1-С6 гідроксіалкіл, С3-С6 циклоалкіл, С3-С6 галогенциклоалкіл, С3-С6 гідроксициклоалкіл, С3-С6 циклоалкокси, С3-С6 галогенциклоалкокси, С3-С6 гідроксициклоалкокси, С1-С6 алкокси, С1-С6 галогеналкокси, С2-С6 алкеніл, С2-С6 алкініл, S(=O)n(С1-С6 алкіл), S(=O)n(С1-С6 галогеналкіл), OSO2(С1-С6 алкіл), OSO2(С1-С6 галогеналкіл), С(=О)Н, C(=O)NRxRy, (С1-С6 алкіл)NRxRy, C(=O)(С1-С6 алкіл), С(=О)О(С1-С6 алкіл), С(=О)(С1-С6 галогеналкіл), С(=О)О(С1-С6 галогеналкіл), С(=О)(С3-С6 циклоалкіл), С(=О)О(С3-С6 циклоалкіл), С(=O)(С2-С6 алкеніл), С(=О)О(С2-С6 алкеніл), (С1-С6 алкіл)О(С1-С6 алкіл), (С1-С6 алкіл)S(С1-С6 алкіл), С(=О)(С1-С6 алкіл)С(=О)О(С1-С6 алкіл), феніл і фенокси);
(f) J являє собою О, N, NR5, CR5 або C=О;
(g) L являє собою одинарний або подвійний зв'язок;
(h) К являє собою CR5, С=О, N, NR5 або C=S;
(і) R1 являє собою Н, ОН, F, Сl, Вr, І, оксо, С1-С6 алкіл, С1-С6 галогеналкіл, С1-С6 алкокси, С3-С6 циклоалкокси, С1-С6 галогеналкокси, С2-С6 алкенілокси, (С1-С6 алкіл)О(С1-С6 алкіл), (С1-С6 алкіл)О(С1-С6 алкокси), OC(=О)( С1-С6 алкіл), OC(=О)(С3-С6 циклоалкіл), OC(=О)(С1-С6 галогеналкіл), OC(=О)(С2-С6 алкеніл) або NRxRy;
(j) R2 являє собою Н, F, Сl, Вr, І, оксо, С1-С6 алкіл, С1-С6 галогеналкіл, С1-С6 алкокси, С3-С6 циклоалкокси, С1-С6 галогеналкокси, С2-С6 алкенілокси, (С1-С6 алкіл)О(С1-С6 алкіл), (С1-С6 алкіл)О(С1-С6 алкокси), OC(=О)(С1-С6 алкіл), OC(=О)(С3-С6 циклоалкіл), OC(=О)(С1-С6 галогеналкіл), OC(=О)(С2-С6 алкеніл) або NRxRy;
(k) R3 являє собою Н, ОН, F, СІ, Вr, І, оксо, С1-С6 алкіл, С1-С6 галогеналкіл, С1-С6 алкокси, С3-С6 циклоалкокси, С1-С6 галогеналкокси, С2-С6 алкенілокси, (С1-С6 алкіл)О(С1-С6 алкіл), (С1-С6 алкіл)О(С1-С6 алкокси), OC(=О)(С1-С6 алкіл), OC(=О)(С3-С6 циклоалкіл), OC(=О)(С1-С6 галогеналкіл), OC(=О)(С2-С6 алкеніл), або NRxRy;
(l) R4 являє собою Н, С1-С6 алкіл, С1-С6 галогеналкіл, С1-С6 алкокси, С1-С6 галогеналкокси, С2-С6 алкенілокси, (С1-С6 алкіл)О(С1-С6 алкіл);
(m) R5 являє собою (кожний незалежно) Н, С1-С6 алкіл, С1-С6 галогеналкіл, С3-С6 циклоалкіл або С3-С6 галогенциклоалкіл; і
(n) Rx і Ry незалежно вибрані із групи, яка включає Н, С1-С6 алкіл, С1-С6 галогеналкіл, С1-С6 гідроксіалкіл, С3-С6 циклоалкіл, С3-С6 галогенциклоалкіл, С3-С6 гідроксициклоалкіл, С3-С6 циклоалкокси, С3-С6 галогенциклоалкокси, С3-С6 гідроксициклоалкокси, С1-С6 алкокси, С1-С6 галогеналкокси, С2-С6 алкеніл, С2-С6 алкініл, S(=O)n(С1-С6 алкіл), S(=O)n(С1-С6 галогеналкіл), OSO2(С1-С6 алкіл), OSO2(С1-С6 галогеналкіл), С(=О)Н, С(=О)ОН, С(=О)( С1-С6 алкіл), С(-О)О(С1-С6 алкіл), С(=О)(С1-С6 галогеналкіл), С(=О)О(С1-С6 галогеналкіл), С(=О)(С3-С6 циклоалкіл), С(=О)О(С3-С6 циклоалкіл), С(=О)(С2-С6 алкеніл), С(=О)О(С2-С6 алкеніл), (С1-С6 алкіл)О(С1-С6 алкіл), (С1-С6 алкіл)S(С1-С6 алкіл), С(=О)(С1-С6 алкіл)С(=О)О(С1-С6 алкіл), феніл і фенокси.
2. Сполука за п. 1, структура якої відповідає наступним структурам:
 ,
,  ,
,
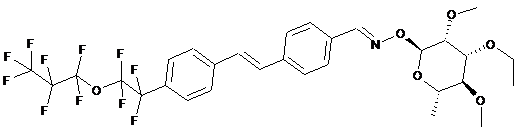 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
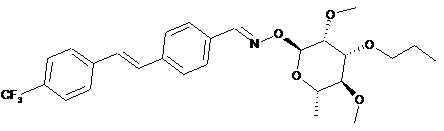 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
 ,
,
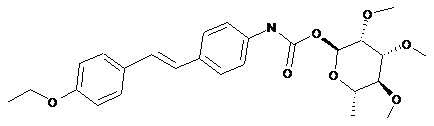 ,
,
 ,
,
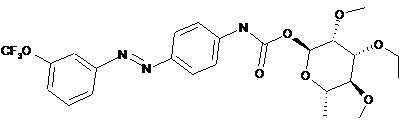 ,
,
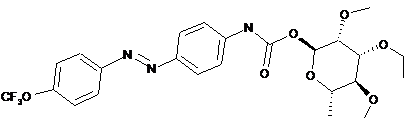 ,
,
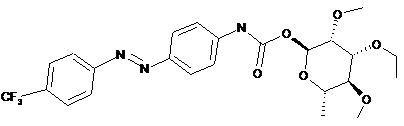 , і
, і
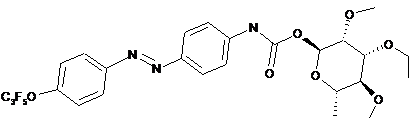 .
.
3. Сполука, яка являє собою пестицидно прийнятну кислотно-адитивну сіль сполуки за п. 2.
4. Спосіб боротьби з сільськогосподарськими шкідниками, що включає нанесення сполуки за п. 1 на ділянку, де живуть шкідники.
5. Композиція, що включає суміш сполуки за п. 2 щонайменше з одним пестицидом.
6. Спосіб за п. 4, де сполуку за п. 1 наносять на насіння.
7. Спосіб за п. 6, де насіння є генетично модифіковане для експресії однієї або декількох характерних ознак.
8. Спосіб за п. 4, де сполуку за п. 1 наносять на генетично модифіковану рослину, яка була генетично модифікована для експресії однієї або декількох характерних ознак.
9. Спосіб за п. 4, де сполуку за п. 1 наносять на тварину або перорально вводять тварині.
Текст
Реферат: Винахід належить до галузі пестицидів і їх застосування для боротьби із сільськогосподарськими шкідниками, що включає нову індивідуальну хімічну сполуку та композиції, що її містять. UA 107566 C2 (12) UA 107566 C2 UA 107566 C2 5 10 15 20 25 30 35 40 45 50 55 ГАЛУЗЬ ТЕХНІКИ, ДО ЯКОЇ НАЛЕЖИТЬ ВИНАХІД Дана заявка вимагає пріоритет Попередньої Заявки на Патент США Сер. № 61/151549, заявленої 11 лютого 2009 року, зміст якої у всій повноті введений в даний опис у вигляді посилання. Винахід, розкритий в даному документі, належить до технічної галузі пестицидів і їх застосування для боротьби із сільськогосподарськими шкідниками. РІВЕНЬ ТЕХНІКИ Сільськогосподарські шкідники щорічно викликають мільйони людських смертей в усьому світі. Крім того, існує більше десяти тисяч різновидів сільськогосподарських шкідників, які викликають втрати в сільському господарстві. Вказані сільськогосподарські втрати щороку становлять мільярди доларів США. Терміти викликають ушкодження різних структур, таких як будинки. Вказані ушкодження, викликані термітами, щороку становлять мільярди доларів США. І нарешті, велика кількість шкідників харчових продуктів, які підлягають зберіганню, поїдають і псують продукти харчування, які знаходяться на зберіганні. Вказані втрати продуктів харчування, які знаходяться на зберіганні, щороку становлять мільярди доларів США, але що більш важливо, позбавляють людей необхідної їжі. Існує гостра потреба в нових пестицидах. Комахи виробляють резистентність до пестицидів, використовуваних у цей час. Сотні видів комах є резистентними до одного або декількох пестицидів. Добре відомий розвиток резистентності до деяких раніше розроблених пестицидів, таких як ДДТ, карбамати і органічні фосфати. Однак резистентність розвилася навіть до деяких більш нових пестицидів. Тому є потреба в нових пестицидах і, особливо, у пестицидах, які мають нові механізми дії. ЗАМІСНИКИ (НЕВИЧЕРПНИЙ ПЕРЕЛІК) Представлений перелік прикладів замісників не є (за винятком галогенів) вичерпним і не повинен розглядатися як обмеження винаходу, розкритого в даному документі. Термін "алкеніл" означає ациклічний ненасичений (який містить щонайменше один подвійний вуглець-вуглецевий зв'язок) розгалужений або нерозгалужений замісник, що містить атоми вуглецю і водню, наприклад, вініл, аліл, бутеніл, пентеніл, гексеніл, гептеніл, октеніл, ноненіл і деценіл. Термін "алкенілокси" означає алкеніл, що додатково містить одинарний вуглець-кисневий зв'язок, наприклад, алілокси, бутенілокси, пентенілокси, гексенілокси, гептенілокси, октенілокси, ноненілокси і деценілокси. Термін "алкокси" означає алкіл, що додатково містить одинарний вуглець-кисневий зв'язок, наприклад, метокси, етокси, пропокси, ізопропокси, 1-бутокси, 2-бутокси, ізо-бутокси, третбутокси, пентокси, 2-метилбутокси, 1,1-диметилпропокси, гексокси, гептокси, октокси, нонокси і декокси. Термін "алкокси" означає ациклічний насичений розгалужений або нерозгалужений замісник, що містить атоми вуглецю і водню, наприклад, метил, етил, пропіл, ізо-пропіл, 1-бутил, 2-бутил, ізо-бутил, трет-бутил, пентил, 2-метилбутил, 1,1-диметилпропіл, гексил, гептил, октил, ноніл і децил. Термін "алкініл" означає ациклічний ненасичений (який містить щонайменше один потрійний вуглець-вуглецевий зв'язок і будь-яку кількість подвійних зв'язків) розгалужений або нерозгалужений замісник, що містить атоми вуглецю і водню, наприклад, етиніл, пропаргіл, бутиніл, пентиніл, гексиніл, гептиніл, октиніл, нонініл і дециніл. Термін "галоген" означає фтор, хлор, бром і йод. Термін "галогеналкокси" означає галогеналкіл, що додатково містить одинарний вуглецькисневий зв'язок, наприклад, фторметокси, дифторметокси і трифторметокси, 2-фторетокси, 1,1,2,2,2-пентафторетокси, 1,1,2,2-брометокси і 1,1,2, 2-тетрафторетокси. Термін "галогеналкіл" означає алкіл, що додатково містить від одного до максимально можливої кількості однакових або відмінних атомів галогенів, наприклад, фторметил, дифторметил, трифторметил, 2-фторетил, 2,2,2-трифторетил, хлорметил, трихлорметил і 1,1,2,2-тетрафторетил. Термін "галогенфенілокси" означає фенілокси, що містить один або декілька однакових або відмінних атомів галогенів. Термін "гідроксіалкіл" означає алкіл, що містить одну або декілька гідроксильних груп. ДОКЛАДНИЙ ОПИС ВИНАХОДУ Сполуки згідно із даним винаходом відповідають наступній формулі: 1 UA 107566 C2 5 10 15 20 25 30 35 40 45 50 , де (а) Ar1 являє собою (1) фураніл, феніл, піридазиніл, піридил, піримідиніл, тієніл або (2) заміщений фураніл, заміщений феніл, заміщений піридазиніл, заміщений піридил, заміщений піримідиніл або заміщений тієніл, де вказані заміщений фураніл, заміщений феніл, заміщений піридазиніл, заміщений піридил, заміщений піримідиніл і заміщений тієніл містять один або декілька замісників, незалежно вибраних із групи, яка включає H, F, Cl, Br, I, CN, NO 2, C1-C6 алкіл, C1-C6 галогеналкіл, С1-C6 гідроксіалкіл, C3-C6 циклоалкіл, C3-C6 галогенциклоалкіл, C3-C6 гідроксициклоалкіл, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гідроксициклоалкокси, С1-C6 алкокси, С1-C6 галогеналкокси, C2-C6 алкеніл, C2-C6 алкініл, S(=O)n(C1-C6 алкіл), S(=O)n(С1-C6 галогеналкіл), OSO2(C1-C6 алкіл), OSO2(C1-C6 галогеналкіл), C(=О)H, C(=О)NR xRy, (С1-C6 алкіл)NRxRy, C(=O)(C1-C6 алкіл), C(=O)O(C1-C6 алкіл), C(=O)(C1-C6 галогеналкіл), C(=O)O(C1-C6 галогеналкіл), C(=O)(C3-C6 циклоалкіл), C(=O)O(C3-C6 циклоалкіл), C(=O)(C2-C6 алкеніл), C(=O)O(C2-C6 алкеніл), (С1-C6 алкіл)O(С1-C6 алкіл), (С1-C6 алкіл)S(С1-C6 алкіл), (C1-C6 галогеналкіл)O(С1-C6 галогеналкіл)O, C1-C6 (гідрокси)галогеналкіл, C(=O)(С1-C6 алкіл)C(=O)O(С1-C6 алкіл), феніл, фенокси, заміщений феніл і заміщений фенокси (де вказаний заміщений феніл і заміщений фенокси містить один або декілька замісників, незалежно вибраних із групи, яка включає H, F, Cl, Br, I, CN, NO2, С1-C6 алкіл, С1-C6 галогеналкіл, C1-C6 гідроксіалкіл, C3-C6 циклоалкіл, C3-C6 галогенциклоалкіл, C3-C6 гідроксициклоалкіл, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гідроксициклоалкокси, С1-C6 алкокси, С1-C6 галогеналкокси, C2-C6 алкеніл, C2-C6 алкініл, S(=O)n(C1-C6 алкіл), S(=O)n(C1-C6 галогеналкіл), OSO2(С1-C6 алкіл), OSO2(С1-C6 галогеналкіл), C(=О)H, C(=О)NRxRy, (С1-C6 алкіл)NRxRy, C(=O)(C1-C6 алкіл), C(=O)O(C1-C6 алкіл), C(=O)(C1-C6 галогеналкіл), C(=O)O(C1-C6 галогеналкіл), C(=O)(C3-C6 циклоалкіл), C(=O)O(C3-C6 циклоалкіл), C(=O)(C2-C6 алкеніл), C(=O)O(C2-C6 алкеніл), (С1-C6 алкіл)O(С1-C6 алкіл), (С1-C6 алкіл)S(С1-C6 алкіл), C(=O)(C1-C6 алкіл)C(=O)O(С1-C6 алкіл)феніл і фенокси); (b) E являє собою N, C або CR5; (c) G являє собою подвійний або потрійний зв’язок; (d) M являє собою N, C або CR5 (за умови, що коли E являє собою атом азоту "N", тоді M являє собою атом азоту "N"; коли E являє собою атом вуглецю "C", тоді M являє собою атом вуглецю "C"; і коли E являє собою "CR5", тоді M являє собою "CR5"); (c) Ar2 являє собою (1) фураніл, феніл, піридазиніл, піридил, піримідиніл, тієніл або (2) заміщений фураніл, заміщений феніл, заміщений піридазиніл, заміщений піридил, заміщений піримідиніл або заміщений тієніл, де вказані заміщений фураніл, заміщений феніл, заміщений піридазиніл, заміщений піридил, заміщений піримідиніл і заміщений тієніл містять один або декілька замісників, незалежно вибраних із групи, яка включає H, F, Cl, Br, I, CN, NO 2, C1-C6 алкіл, C1-C6 галогеналкіл, С1-C6 гідроксіалкіл, C3-C6 циклоалкіл, C3-C6 галогенциклоалкіл, C3-C6 гідроксициклоалкіл, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гідроксициклоалкокси, С1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкеніл, C2-C6 алкініл, S(=O)n(C1-C6 алкіл), S(=O)n(С1-C6 галогеналкіл), OSO2(C1-C6 алкіл), OSO2(C1-C6 галогеналкіл), C(=О)H, C(=О)NR xRy, (C1-C6 алкіл)NRxRy, C(=O)(C1-C6 алкіл), C(=O)O(C1-C6 алкіл), C(=O)(C1-C6 галогеналкіл), C(=O)O(C1-C6 галогеналкіл), C(=O)(C3-C6 циклоалкіл), C(=O)O(C3-C6 циклоалкіл), C(=O)(C2-C6 алкеніл), C(=O)O(C2-C6 алкеніл), (C1-C6 алкіл)O(C1-C6 алкіл), (C1-C6 алкіл)S(C1-C6 алкіл), (C1-C6 галогеналкіл)O(C1-C6 галогеналкіл)O, C1-C6 (гідрокси)(галоген)алкіл, C(=О)(С1-C6 алкіл)C(=O)O(С1-C6 алкіл), феніл, фенокси, заміщений феніл і заміщений фенокси (де вказані заміщений феніл і заміщений фенокси містять один або декілька замісників, незалежно вибраних із групи, яка включає H, F, Cl, Br, I, CN, NO2, C1-C6 алкіл, C1-C6 галогеналкіл, C1-C6 гідроксіалкіл, C3-C6 циклоалкіл, C3-C6 галогенциклоалкіл, C3-C6 гідроксициклоалкіл, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гідроксициклоалкокси, С1-C6 алкокси, С1-C6 галогеналкокси, C2-C6 алкеніл, C2-C6 алкініл, S(=O)n(C1-C6 алкіл), S(=O)n(C1-C6 галогеналкіл), OSO2(C1-C6 алкіл), OSO2(C1-C6 галогеналкіл), C(=О)H, C(=О)NRxRy, (С1-C6 алкіл)NRxRy, C(=O)(C1-C6 алкіл), C(=O)O(C1-C6 алкіл), C(=O)(C1-C6 2 UA 107566 C2 5 10 15 20 25 30 35 40 45 50 55 60 галогеналкіл), C(=O)O(C1-C6 галогеналкіл), C(=O)(C3-C6 циклоалкіл), C(=O)O(C3-C6 циклоалкіл), C(=O)(C2-C6 алкеніл), C(=O)O(C2-C6 алкеніл), (С1-C6 алкіл)O(С1-C6 алкіл), (С1-C6 алкіл)S(С1-C6 алкіл), C(=O)(C1-C6 алкіл)C(=O)O(С1-C6 алкіл)феніл і фенокси); (d) J являє собою O, N, NR5, CR5 або C=O; (e) L являє собою одинарний або подвійний зв’язок; (f) K являє собою CR5, C=O, N, NR5 або C=S; (g) R1 являє собою H, OH, F, Cl, Br, I, оксо, C1-C6 алкіл, C1-C6 галогеналкіл, C1-C6 алкокси, C3-C6 циклоалкокси, C1-C6 галогеналкокси, C2-C6 алкенілокси, (C1-C6 алкіл)O(C1-C6 алкіл), (C1-C6 алкіл)O(С1-C6 алкокси), °C(=O)(C1-C6 алкіл), °C(=O)(C3-C6 циклоалкіл), °C(=O)(C1-C6 галогеналкіл), °C(=O)(C2-C6 алкеніл) або NRxRy; (h) R2 являє собою H, F, Cl, Br, I, оксо, C1-C6 алкіл, C1-C6 галогеналкіл, C1-C6 алкокси, C3-C6 циклоалкокси, C1-C6 галогеналкокси, C2-C6 алкенілокси, (C1-C6 алкіл)O(С1-C6 алкіл), (C1-C6 алкіл)O(С1-C6 алкокси), °C(=O)(C1-C6 алкіл), °C(=O)(C3-C6 циклоалкіл), °C(=O)(C1-C6 галогеналкіл), °C(=O)(C2-C6 алкеніл) або NRxRy; (i) R3 являє собою H, OH, F, Cl, Br, I, оксо, C 1-C6 алкіл, C1-C6 галогеналкіл, C1-C6 алкокси, C3C6 циклоалкокси, C1-C6 галогеналкокси, C2-C6 алкенілокси, (C1-C6 алкіл)O(C1-C6 алкіл), (C1-C6 алкіл)O(C1-C6 алкокси), °C(=O)(C1-C6 алкіл), °C(=O)(C3-C6 циклоалкіл), °C(=O)(C1-C6 галогеналкіл), °C(=O)(C2-C6 алкеніл) або NRxRy; (j) R4 являє собою H, С1-C6 алкіл, С1-C6 галогеналкіл, С1-C6 алкокси, С1-C6 галогеналкокси, C2-C6 алкенілокси, (С1-C6 алкіл)O(С1-C6 алкіл); (k) R5 являє собою (кожний незалежно) H, C1-C6 алкіл, C1-C6 галогеналкіл, C3-C6 циклоалкіл або C3-C6 галогенциклоалкіл; і (l) Rx і Ry незалежно вибрані із групи, яка включає H, С 1-C6 алкіл, С1-C6 галогеналкіл, С1-C6 гідроксіалкіл, C3-C6 циклоалкіл, C3-C6 галогенциклоалкіл, C3-C6 гідроксициклоалкіл, C3-C6 циклоалкокси, C3-C6 галогенциклоалкокси, C3-C6 гідроксициклоалкокси, C1-C6 алкокси, C1-C6 галогеналкокси, C2-C6 алкеніл, C2-C6 алкініл, S(=O)n(C1-C6 алкіл), S(=O)n(C1-C6 галогеналкіл), OSO2(С1-C6 алкіл), OSO2(С1-C6 галогеналкіл), C(=О)H, C(=О)ОH, C(=O)(C 1-C6 алкіл), C(=O)O(C1C6 алкіл), C(=O)(C1-C6 галогеналкіл), C(=O)O(C1-C6 галогеналкіл), C(=O)(C3-C6 циклоалкіл), C(=O)O(C3-C6 циклоалкіл), C(=O)(C2-C6 алкеніл), C(=O)O(C2-C6 алкеніл), (C1-C6 алкіл)O(С1-C6 алкіл), (C1-C6 алкіл)S(С1-C6 алкіл), C(=О)(C1-C6 алкіл)C(=O)O(С1-C6 алкіл), феніл і фенокси. В іншому варіанті здійснення винаходу: Ar1 являє собою заміщений феніл, де вказаний заміщений феніл містить один або декілька замісників, незалежно вибраних із групи, яка включає С 1-C6 галогеналкіл, С1-C6 алкокси, С1-C6 галогеналкокси, C(=O)(C1-C6 алкіл), (С1-C6 галогеналкіл)O(С1-C6 галогеналкіл)O і С1-C6 (гідрокси)галогеналкіл. У ще одному варіанті здійснення винаходу: Ar1 являє собою заміщений феніл, де вказаний заміщений феніл містить один або декілька замісників, незалежно вибраних із групи, яка включає С 1-C6 галогеналкіл, С1-C6 алкокси, С1-C6 галогеналкокси і (C1-C6 галогеналкіл)O(C1-C6 галогеналкіл)O. У ще одному варіанті здійснення винаходу Ar2 являє собою феніл. У ще одному варіанті здійснення винаходу J являє собою N, NR5 або CR5. У ще одному варіанті здійснення винаходу: K являє собою C=O або N. У ще одному варіанті здійснення винаходу R1, R2 і R3 (кожний незалежно) являє собою С 1C6 алкокси. У ще одному варіанті здійснення винаходу R4 являє собою С1-C6 алкіл. В іншому варіанті здійснення винаходу R5 являє собою H. Поряд з описаними варіантами здійснення винаходу можливі і інші варіанти здійснення винаходу і їх комбінації. ОДЕРЖАННЯ ПІРАНОЗНИХ ПРОМПКНИХ ПРОДУКТІВ Для одержання сполук згідно із даним винаходом може використовуватися широкий спектр піраноз (у різних структурних формах, наприклад, D- і L-). Наприклад, можуть використовуватися піранози, вибрані з наступного переліку, який не є вичерпним: рибоза, аробіноза, ксилоза, ліксоза, рибулоза, ксилулоза, алоза, альтроза, глюкоза, маноза, гулоза, ідоза, галактоза, талоза, псикоза, фруктоза, сорбоза, тагатоза, фукоза, мікароза, квіновоза, олеандроза, рамноза і паратоза. У більшості прикладів, представлених нижче, для одержання проміжних піраноз використовувалася L-рамноза. Звичайно піранози, які використовуються як проміжні продукти, можуть бути отримані наступним чином (з використанням, наприклад, L-рамнози). О-алкіловані похідні рамнози можуть бути отримані з комерційно доступної L-рамнози або гідрату L-рамнози з використанням алкілйодиду і порошкоподібного гідроксиду калію (КОН) у сухому диметилсульфоксиді (ДМСО) 3 UA 107566 C2 5 10 15 при температурі в інтервалі від 5 °C до 15 °C. Повністю алкілований продукт потім виділяється екстракцією ДМСО розчину гексанами з наступним концентруванням гексанового шару в вакуумі. Отриманий проміжний алкілпіранозид потім піддається обробці безпосередньо водною соляною кислотою (HCl) або іншої водною кислотою, яка утворює вільний гідроксицукор звичайно у вигляді суміші α і β аномерів. Альтернативно, пералкілована L-рамноза може бути виділена гідролізом спіносаду або іншого три-(О-алкіл)рамнозилованого натурального продукту з використанням умов, аналогічних умовам, описаним для виділення метилолеандросиду з авермектину В 2 (Loewe et al. J. Org. Chem. 1994, 59, 7870). Таким чином, обробка технічного спіносаду надлишком концентрованої сірчаної кислоти в сухому метиловому спирті (МеОН) приводить до гідролізу рамнозного цукру і перетворення його в метилпіранозид. Чистий метилпіранозид далі може видалятися з реакційного середовища повною екстракцією гексанами або іншим вуглеводневим розчинником. Після цього чистий рамнопіранозид може виділятися із приблизно 65-75% виходом відгоном із сирого рідкого продукту у вакуумі. 3-О-етил-2,4-ди-О-метилрамноза може бути отримана аналогічним чином виходячи зі спінетораму. Інші алкіловані похідні можуть бути отримані аналогічно, виходячи з прийнятним чином функціоналізованих спіносоїдних похідних, отриманих зі спіносинового фактора, який містить одну або декілька вільних гідроксильних груп, приєднаних до рамнози, (наприклад, спіносину J) в умовах, описаних у Патенті США 6001981 (Deamicis et al., 1999). 20 25 30 Рамнозний попередник, селективно алкілований замісником великої молекулярної маси в С3 положенні, був описаний (див., наприклад, Pozsgay et al. Can. J. Chem. 1987, 65, 2764). Альтернативний спосіб одержання, у якому не застосовується олововмісний реагент, описаний нижче. Взаємодія метилпіранозиду L-рамнози з одним еквівалентом фенілборонової кислоти в умовах, які дозволяють видаляти воду, приводять до утворення боронового ацеталю. Обробка отриманого ацеталю алкілйодидом і оксидом срібла в полярному апротонному розчиннику, такому як N,N-диметилформамід (ДМФА), при температурі в інтервалі від 0 °C до 110 °C приводить до селективного алкілування при С3-ОН, даючи 3-О-алкілметилпіранозид. Отриманий продукт далі може додатково метилуватися в положеннях 2-ОН і 4-ОН з використанням метилйодиду в умовах, описаних вище. Повністю алкілована рамноза потім може піддатися гідролізу як описано вище з одержанням 2,4-ди-О-метил-3-О-алкіл-L-рамнози. 4 UA 107566 C2 5 10 15 20 25 30 Ілюстрації одержання таких проміжних піраноз представлені в прикладах. Можуть бути отримані і проміжні гідроксіамінопіранози. Наприклад, вони можуть бути отримані з відповідного похідного рамнози і N-гідроксисукциніміду (NHS) в умовах, при яких вода, що утворюється, видаляється азеотропно для одержання N-сукцинімідоїлгідроксіаміного аддукту. В одному варіанті здійснення винаходу ці умови включають об'єднання рамнози і NHS у толуолі або бензолі, додавання каталітичної кількості кислоти, такої як п-толуолсульфонова кислота (TsOH) і нагрівання до температури кипіння зі зворотним холодильником в апарату, оснащеному пасткою Діна-Старка. Перетворення у вільний гідроксіамінний проміжний продукт проводиться обробкою сукцинімідоїльного аддукту надлишком гідразингідрату або безводного гідразину в спиртовому розчиннику, такому як МеОН або етиловий спирт (EtOH). Наступна взаємодія О-рамнозилгідроксиламіну з альдегідом або кетоном з використанням EtOH або іншого розчинника, що представляє собою нижчий спирт, при температурі в інтервалі від температури навколишнього середовища до температури утворення флегми приводить до одержання О-рамнозилоксима. ОДЕРЖАННЯ ПРОМПКНИХ ДІАРИЛЬНИХ ПОХІДНИХ Сполуки згідно із даним винаходом одержують зв'язуванням описаних вище піраноз із діарильним проміжним продуктом Ar1-E[G]M-Ar2 з використанням агента ковалентного зв'язування J[L]KQ (визначеного вище). Для одержання сполук згідно із даним винаходом може застосовуватися широкий спектр діарильних попередників за умови, що вони містять прийнятну функціональну групу на Ar2, до якої піранозний проміжний продукт може приєднуватися для одержання агента ковалентного зв'язування. Прийнятні функціональні групи включають аміногрупу, оксоалкільну групу, формільну групу або групу карбонової кислоти. Вказані проміжні продукти можуть бути отримані способами, описаними раніше в хімічній літературі. Деякі із цих способів представлені далі. ОДЕРЖАННЯ ОКСИМЗВ'ЯЗАНИХ СПОЛУК Оксимзв'язані сполуки можуть бути отримані з відповідних арилальдегідів або кетонів взаємодією з відповідним 2-гідроксіаміноцукром в органічному розчиннику, такому як МеОН або EtOH, при температурі в інтервалі від 0 до 100 °C. 5 UA 107566 C2 5 ОДЕРЖАННЯ КАРБАМАТЗВ'ЯЗАНИХ СПОЛУК Карбамат- або тіокарбаматзв'язані сполуки можуть бути отримані з відповідних ариламінів за допомогою перетворення в ізоціанат, ізотіоціанат або п-нітрофенілкарбамат з наступною обробкою прийнятним -ROH і органічною або неорганічною основою в прийнятному розчиннику, такому як тетрагідрофуран (ТГФ), при температурі в інтервалі від 0 до 100 °C: 10 15 20 25 30 35 У цих реакціях α-конфігурація при С1 рамнозного фрагмента є звичайно основним продуктом, хоча також утворюється незначна кількість β-аномеру. Два ці ізомери можуть розділятися хроматографічно або вони можуть використовуватися у вигляді суміші. Одержання сполук згідно із даним винаходом може здійснюватися за допомогою синтезу прийнятного проміжного продукту, що містить функціональну кислотну, альдегідну, кетонову або аміногрупу для приєднання до проміжної піранози. ПРИКЛАДИ Дані приклади представлені для ілюстрації і не повинні розглядатися як обмеження винаходу, розкритого в даному документі. ПРИКЛАД 1: (3R,4R,5S,6S)-2,3,4,5-тетраметокси-6-метилтетрагідропірану (сполука Е-1) Розчин гідрату L-рамнози (40 грамів (г), 0,22 моль (моль)) у сухому диметилсульфоксиді (ДМСО; 450 мілілітрів (мл)) завантажують в тригорлу круглодонну колбу об’ємом 2 літри (л) і механічно перемішують, додаючи однієї порцією порошкоподібний гідроксид калію (KOH; 75 г, 1,34 моль). До отриманого розчину додають йодметан (187 г, 1,32 моль) таким чином, щоб температура розчину залишалася нижчою 30 °C. Для підтримки вказаної температури використовують баню із сумішшю сухий лід/ацетон. Після завершення додавання (приблизно протягом 2 годин) розчин перемішують протягом додаткових 3 годин, і потім суміш залишають на ніч при кімнатній температурі. Після цього отриманий прозорий розчин екстрагують гексанами (4×500 мл), об'єднану гексанову фракцію промивають розчином солі, сушать і випарюють розчинник, одержуючи розчин світло-жовтогарячого кольору (44 г, 92%). Перегонка приводить до одержання 40 г безбарвного масла, температура кипіння 150 °C (0,5 мм Hg = 66,66 Па). ПРИКЛАД 2: Одержання (3R,4R,5S,6S)-3,4,5-триметокси-6-метилтетрагідропіран-2-ол (сполука E-2) 6 UA 107566 C2 5 10 15 20 25 30 35 40 Розчин сполуки E-I (35,7 г, 0,162 моль) в 2N соляній кислоті (HCl; 300 мл) нагрівають до 98 °C і витримують при вказаній температурі протягом 5 годин, потім охолоджують до кімнатної температури і екстрагують дихлорметаном (CH2Cl2; 4×170 мл). Об'єднані екстракти сушать над сульфатом магнію (MgSO4) і знебарвлюють деревним вугіллям. Упарювання розчину приводить до одержання вказаної в заголовку сполуки (24,7 г, 74%) у вигляді в’язкого масла. Частину сирого продукту (960 міліграмів (мг)) піддають вакуумній перегонці з використанням апарата Кугельроха (Kuhgelrohr), збираючи 890 мг при 145-155 °C (1-2 мм = 133,32-266,64 Па). ПРИКЛАД 3: Одержання (3R,4R,5S,6S)-4-етокси-2,3,5-триметокси-6-метилтетрагідропірана (сполука E-3) До розчину метилового спирту (2,5 літра (л)) у колбі Ерленмейера (Erlenmeyer) об’ємом 4 л при перемішуванні повільно додають сірчану кислоту (H2SO4, 98%; 300 мл, 5,6 моль). Після охолодження розчину до температури навколишнього середовища до розчину додають 3'-ОEtспіносин J/L (350 г, 0,47 моль) (отриманий відповідно до методики, описаної в Патенті США № 6001981, Deamicis et al., 1999) і отриманий розчин кип'ятять зі зворотним холодильником протягом 6 годин. Охолоджений розчин переносять у ділильну лійку об’ємом 4 л і екстрагують гексанами (3×1 л). Об'єднану органічну фракцію сушать і концентрують у вакуумі, потім переганяють із використанням апарата Кугельроха, одержуючи безбарвне масло (65 г, 60%), температура кипіння 165 °C (10 мторр = 1,333 Па). ПРИКЛАД 4: Одержання (2R,3R,4R,5R,6S)-2,3,5-триметокси-6-метил-4пропокситетрагідропірана (сполука E-5) Стадія 1. (2R,3R,4R,5R,65)-2-Метокси-6-метил-4-пропокситетрагідропіран-3,5-діол. Відповідно до методики, описаної в публікації Oshima et al., Tetrahedron Lett. 1997, 38, 5001, для одержання 3, 4-боронатного ефіру метил-α-L-фукопіранозида метил-OC-L-рамнопіранозид перетворюють в 2,3-боронатний ефір. Сирий ефір (10,0 г, 37,7 мілімоль (ммоль)) розчиняють у толуолі (150 мл) і обробляють йодпропаном (8,0 г, 47 ммоль), оксидом срібла (21,8 г, 94,3 ммоль) і триетиламіном (4,77 г, 47,1 ммоль). Розчин нагрівають до 100 °C і перемішують протягом ночі (16 годин). Після охолодження і фільтрації розчин концентрують до в’язкого масла і очищають хроматографією (силікагель, елюювання із градієнтом: (EtOAc)-гексан), одержуючи 5,9 г чистого продукту. Стадія 2. Продукт, отриманий на стадії 1, метилують з використанням MeI і KOH в умовах, описаних у прикладі 1, для одержання сполуки E-5. Проміжні піранози, представлені в таблиці 1, одержують способами, описаними вище і представленими в прикладах 1-4. Приклад одержання проміжної 2-O-сукцинимидоїлпіранози описаний нижче. ПРИКЛАД 5: Отримання 1-(2S,3R,4R,5S,6S)-3,4,5-триметокси-6-метилтетрагідропіран-2ілокси)піролідин-2,5-діону (сполука E-23) 45 7 UA 107566 C2 5 10 До розчину 2,3,4-три-O-метил-L-рамнози (6,5 г, 31,5 ммоль) і N-гідроксисукциніміду (5,4 г, 47 ммоль) у бензолі (50 мл) при перемішуванні додають п-толуолсульфонову кислоту (50 мг, кат.). Розчин нагрівають до температури утворення флегми і збирають воду (H 2O), використовуючи пастку Діна-Старка. Через 4 години розчин охолоджують, і верхній толуоловий шар відділяють від невеликої кількості нерозчинної смоли. Органічний шар промивають насиченим розчином гідрокарбонату натрію (NaHCO3; 20 мл), потім сушать над MgSO4 і упарюють до твердого залишку. Перекристалізація із суміші ефір (Et2O)-гексани приводить до одержання вказаної в заголовку сполуки (4,95 г, 52%) у вигляді твердої не зовсім білої речовини. ПРИКЛАД 6: Отримання 1-(2S,3R,4R,5S,6S)-5-гідрокси-3,4-диметокси-6метилтетрагідропіран-2-ілокси)піролідин-2,5-діону (сполука E-24) 15 20 25 30 Розчин (2R,3R,4R,5S,6S)-5-бензилокси-3,4-диметокси-6-метилтетрагідропіран-2-олу (отриманого відповідно до методики, описаної в публікації Wu et al., Carbohydr. Res. 1998, 306, 493; 10,5 г, 26,6 ммоль), N-гідроксисукциніміду (5,0 г, 50 ммоль) і TsOH (250 мг,кат.) у бензолі (100 мл) кип'ятять зі зворотним холодильником протягом 24 годин з видаленням H 2O, використовуючи пастку Діна-Старка. Розчин коричневого кольору охолоджують, фільтрують, промивають насиченим розчином NaHCO3 і концентрують. Смолисте масло очищають хроматографією (силікагель, елюювання: гексани-ацетон 70:30). Після цього чистий Oсукцинімід (7,5 г, 14,5 ммоль) переносять в апарат гідрогенізації Парра об’ємом 500 мл і піддають дебензилуванню з використанням Pd(OH)2/C (0,95 г) в EtOH (75 мл). Через розчин протягом 24 годин пропускають водень під тиском 19 фунтів/кв.дюйм (131,005 кПа), потім розчин фільтрують і упарюють до твердого залишку, який потім перекристалізовують з EtOH, одержуючи продукт у вигляді твердої білої речовини (3,25 г). Проміжні O-сукцинімідипіранози, представлені в таблиці 2, були отримані способами, які описані вище і проілюстровано в прикладах 5 і 6. Приклад одержання проміжних 2-гідроксиламінопіраноз із відповідних проміжних Oсукцинімідоїлпіраноз описаний далі. ПРИКЛАД 7: Отримання О-((2S,3R,4R,5S,6S)-3,4,5-триметокси-6-метилтетрагідропіран-2іл)гідроксиламіну (сполука E-30) 35 40 45 Е-23, похідне 2,3,4-три-O-метил-N-сукцинімідилрамнози (0,50 г, 1,65 ммоль), отримане відповідно до методики прикладу 5, розчиняють в абсолютному EtOH (5 мл) і обробляють надлишком гідразингідрату (0,4 г, 8 ммоль). Розчин перемішують при температурі навколишнього середовища протягом 60 хвилин (хв.), у процесі чого утворюється об'ємний білий осад. Додають додаткову кількість EtOH (5 мл) і розчин перемішують при температурі навколишнього середовища протягом ночі. Розчин фільтрують і концентрують, потім очищають хроматографією (елюювання: 100% EtOAc), одержуючи 265 мг (74% вихід) гідроксиламіну у вигляді твердої кристалічної речовини. Проміжні піранози, представлені в таблиці 3, одержують способами, які описані вище, як показано в прикладі 7. 8 UA 107566 C2 ПРИКЛАД 8: Одержання 4-[(Е)-2-(4-трифторметоксифеніл)вініл]бензальдегіду O((2S,3R,4R,5S,6S)-3,5-диметокси-6-метил-4-пропокситетрагідропіран-2-іл)оксиму (сполука 1) 5 10 15 20 25 30 35 40 Стадія 1. 4-[(Е)-2-(4-трифторметоксифеніл)вініл]бензонітрил. У круглодонну колбу, через яку пропущений потік азоту, додають триосновний фосфат калію (617 мг, 2,9 ммоль) у диметил ацетаміді (DMA; 2 мл), 4-трифторметоксибромбензол (500 мг, 2,1 ммоль) і 4-ціановінілбензол (322 мг, 2,5 ммоль) з наступним додаванням ацетату паладію (23 мг, 5 моль %). Розчин нагрівають до 140 °C і витримують при вказаній температурі з перемішуванням протягом 12 годин. Після цього розчину дають можливість охолонути до кімнатної температури, розчин виливають в H2O, екстрагують EtOAc і промивають розчином солі. Об'єднані органічні шари сушать над MgSO4, фільтрують і концентрують. Сирий продукт очищають колонковою хроматографією (елюювання: EtOAc у гексанах, 0-75%), одержуючи твердий продукт жовтого кольору (543 мг, 90%), який очищають газовою хроматографією/мас-спектральним (ГХ-МС) аналізом. Отриманий продукт використовують у наступній стадії без додаткового очищення. Стадія 2. 4-[(Е)-2-(4-трифторметоксифеніл)вініл]бензальдегід. Ціанодифенілстирол (543 мг, 1,88 ммоль) розчиняють у сухому CH2Cl2 (10 мл) і охолоджують до -78 °C на бані із сумішшю сухий лід/ацетон. До отриманого розчину по краплях додають гідрид діізобутилалюмінію в гексанах (3,7 мл, 3,7 ммоль). Реакційну суміш перемішують протягом 4 годин, у процесі чого вона нагрівається до кімнатної температури. Цільовий альдегід утворюється винятково за допомогою ГХ/МС. До реакційної суміші додають воду і метанол, що викликає виділення пухирців газу і утворення гелю. Отриману гетерогенну суміш розбавляють CH 2Cl2 і фільтрують через фритовий роздільник фаз (Biotage). Органічний шар збирають і упарюють, одержуючи тверду речовину жовтого кольору (450 мг, 81%), яку очищають ГХ-МС. Отриманий продукт використовують у наступній реакції без додаткового очищення. Стадія 3. 4-[(Е)-2-(4-трифторметоксифеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-3,5диметокси-6-метил-4-пропокситетрагідропіран-2-іл)оксим. Альдегід, отриманий на стадії 1 (0,1 г, 0,3 ммоль), і сполуку E-32 (0,3 ммоль) розчиняють в абсолютованому EtOH (10 мл), отриманий розчин нагрівають до 40 °C і витримують при вказаній температурі з перемішуванням протягом ночі. Після цього в охолоджений розчин додають воду (5 мл), що викликає утворення білого осаду. Розчин розподіляють між H2O (5 мл) і EtOAc (3×5 мл) і об'єднані органічні шари сушать над MgSO4, фільтрують і упарюють, одержуючи твердий продукт темно-жовтого кольору. Очищення колонковою хроматографією з нормальною фазою (елюювання із градієнтом: EtOAcгексани) приводить до одержання цільового продукту (72 мг, 40%) у вигляді твердої речовини 1 світло-жовтого кольору: т. пл. 124-132 °C; H ЯМР (300 МГц, CDCl3) δ 8,13 (с, 1Н), 7,63 (д, J=9,0 Гц, 2H), 7,54 (м, 4H), 7,21 (д, J=9,0 Гц, 2H), 7,11 (д, J=9,0 Гц, 2H), 5,63 (с, 1Н), 3,71 (м 1Н), 3,703,50 (м, 4H), 3,59 (с, 3H), 3,55 (с, 3H), 3,20 (т, J=9,0 Гц, 1Н), 1,68 (м, 2H), 1,31 (д, J=6,0 Гц, 3H), + 0,98 (т, J=7,6 Гц, 3H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 524 ([M+H] ). Представлені далі сполуки одержують із використанням умов, описаних у прикладі 8. 4-[(E)-2-(4-трифторметилфеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-4-етокси-3,5диметокси-6-метилтетрагідропіран-2-іл)оксим (сполука 2) 45 50 1 Вихід оксиму: 60%, тверда речовина жовтувато-коричневого кольору: т. пл. 150-153 °C; Н ЯМР (400 МГц, ДМСO-d6) δ 8,41 (с, 1Н), 7,84 (д, J=8,1 ГЦ, 2H), 7,75-7,67 (м, 6H), 7,46 (с, 2H), 5,49 (д, J=2,0 ГЦ, 1Н), 3,73-3,66 (ушир. с, 2H), 3,56-3,47 (м, 3H), 3,45 (с, 3H), 3,43 (с, 3H), 3,04 (т, J=10,0 Гц, 1Н), 1,17 (м, 6H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 494 + ([M+H] ). 9 UA 107566 C2 4-{(E)-2-[4-(1,1,2,2-тетрафтор-2-гептафторпропілоксіетил)феніл]вініл}бензальдегід ((2S,3R,4R,5S,6S)-4-етокси-3,5-диметокси-6-метилтетрагідропіран-2-іл)оксим (сполука 3) 5 10 15 20 25 30 1 Вихід оксиму: 85%; масло жовтого кольору: H ЯМР (400 МГц, ДМСO-d6) δ 8,40 (с, 1Н), 7,68 (м, 4H), 7,50 (м, 3H), 7,40 (д, J=4,0 Гц, 1Н), 7,15 (д, J=8,0 Гц, 1Н), 5,48 (с, 1Н), 3,74 (м, 1Н), 3,67 (м, 1Н), 3,55-3,46 (м, 4H), 3,45 (с, 3H), 3,43 (с, 3H), 3,04 (т, J=9,2 Гц, 1Н), 1,17 (м, 6H); Масспектроскопія з іонізацією електророзпиленням: m/z 707 ([M-H] ). 4-[(Е)-2-(4-Ацетилфеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-4-етокси-3,5-диметокси-6метилтетрагідропіран-2-іл)оксим (сполука 4) 1 Вихід оксиму 56%; тверда речовина жовтувато-коричневого кольору: т. пл. 164-167 °C; H ЯМР (400 МГц, ДМСO-d6) δ 8,41 (с, 1Н), 7,97 (д, J=8,0 Гц, 2H), 7,77 (д, J=8,0 Гц, 2H), 7,72 (д, J=8,0 Гц, 2H), 7,68 (д, J=8,3 Гц, 2H), 7,45 (с, 2H), 5,48 (с, 1Н), 3,86 (с, 3H), 3,74 (ушир. с, 1Н), 3,73-3,66 (м, 1Н), 3,54-3,46 (м, 3H), 3,45 (с, 3H), 3,43 (с, 3H), 3,04 (т, J=8,0 Гц, 1Н), 1,17 (м, 6H); + Мас-спектроскопія з іонізацією електророзпиленням: m/z 485 ([M+H2O] ). 4-[(Е)-2-(4-трифторметоксифеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-4-етокси-3,5диметокси-6-метилтетрагідропіран-2-іл)оксим (сполука 5) Вихід оксиму 24%; тверда речовина світло-жовтого кольору: т. пл. 91-101 C; H ЯМР (300 МГц, CDCl3) δ 8,13 (с, 1Н), 7,63 (д, J=9,0 Гц, 2H), 7,55-7,51 (м, 3H), 7,23-7,17 (м, 3H), 7,11 (д, J=9,0 Гц, 2H), 5,64 (д, J=3,0 Гц, 1Н), 3,79-3,60 (м, 5H), 3,59 (с, 3H), 3,55 (с, 3H), 3,20 (т, J=9,0 Гц, + 1Н), 1,32-1,24 (м, 6H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 532 ([M+Na] ). 4-[(Е)-2-(3-Трифторметилфеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-4-етокси-3,5диметокси-6-метилтетрагідропіран-2-іл)оксим (сполука 6) 1 1 35 O Вихід оксиму 62%; масло коричневого кольору: H ЯМР (400 МГц, ДМСO-d6) δ 8,40 (с, 1Н), 7,99 (с, 1Н), 7,94 (ушир. с, 1Н), 7,72-7,63 (м, 6H), 7,47 (с, 2H), 5,48 (с, 1Н), 3,74 (м, 1Н), 3,73-3,68 (м, 1Н), 3,54-3,47 (м, 3H), 3,45 (с, 3H), 3,43 (с, 3H), 3,04 (т, J=8,0 Гц, 1Н), 1,17 (м, 6H); Мас+ спектроскопія з іонізацією електророзпиленням: m/z 494 ([M+H] ). 4-[(Е)-2-(4-Пентафторетилоксифеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-4-етокси-3,5диметокси-6-метилтетрагідропіран-2-іл)оксим (сполука 7) 10 UA 107566 C2 1 5 Вихід оксиму 7 мг (6%) у вигляді склоподібної речовини блідо-жовтого кольору: H ЯМР (300 МГц, CDCl3) δ 8,13 (с, 1Н), 7,63 (д, J=8,1 Гц, 2H), 7,56-7,51 (м, 5H), 7,24 (д, J=4,5 Гц, 2H), 7,11 (д, J=8,1 Гц, 2H), 5,63 (д, J=1,8 Гц, 1Н), 3,79-3,60 (м, 5H), 3,59 (с, 3H), 3,55 (с, 3H), 1,32-1,25 (м, 6H); + Мас-спектроскопія з іонізацією електророзпиленням ESIMS m/z 582 ([M+H] ). 4-[(Е)-2-(4-трифторметилоксифеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-3,4,5триметокси-6-метилтетрагідропіран-2-іл)оксим (сполука 8) 10 1 15 20 25 30 35 Вихід оксиму 37 мг (30%) у вигляді твердої білої речовини: т. пл. 120-128 °C; H ЯМР (400 МГц, CDCl3) δ 8,40 (с, 1Н), 7,75 (д, J=8,0 Гц, 2H), 7,68-7,65 (м, 4H), 7,42-7,30 (м, 4H), 5,50 (с, 1Н), 3,80-3,79 (м, 1Н), 3,56-3,52 (м, 1Н), 3,43 (с, 3H), 3,42 (с, 3H), 3,40-3,37 (м, 1Н), 3,38 (с, 3H), 3,05 (т, J=8,0 Гц, 1Н), 1,17 (д, J=4,0 Гц, 3H); Мас-спектроскопія з іонізацією електророзпиленням: m/z + 496 ([M+H] ). 44-[(Е)-2-(3-трифторметилфеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-3,4,5-триметокси-6метилтетрагідропіран-2-іл)оксим (сполука 9) 1 Продукт (65 мг, 50%) виділяють у вигляді прозорої склоподібної речовини: H ЯМР (400 МГц, ДМСO-d6) δ 8,40 (с, 1Н), 7,98 (с, 1Н), 7,72 (ушир. с, 1Н), 7,70 (дд, J=12,0, 8,0 Гц, 4H), 7,64 (ушир. с, 2H), 7,48 (с, 2H), 5,51 (ушир. с, 1Н), 3,56-3,43 (м, 3H), 3,43 (с, 3H), 3,42 (с, 3H), 3,38 (с, 3H), 3,05 (т, J=8,0 Гц, 1Н), 1,17 (д, J=4,0 Гц, 3H); Мас-спектроскопія з іонізацією електророзпиленням: + m/z 480 ([M+H] ). 4-[(Е)-2-(4-трифторметилфеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-4-пропокси-3,5диметокси-6-метилтетрагідропіран-2-іл)оксим (сполука 10) 1 Продукт (210 мг, 77%) виділяють у вигляді твердої безбарвної речовини: т. пл. 163-166; H ЯМР (300 МГц, CDCl3) δ 8,16 (с, 1Н), 7,66 (д, J=8 Гц, 2H), 7,63 (с, 4H), 7,56 (д, J=8 Гц, 2H), 7,2 (с, 2H), 5,66 (с, 1Н), 3,73-3,57 (м, 10H), 3,23 (т, J=9 Гц, 1Н), 1,71 (м, 2H), 1,33 (д, J=6 Гц, 2H), 1,0 (т, J=7,5 Гц, 3H). 4-{(E)-2-[4-(2,2,2-трифтор-1-гідрокси-1-трифторметилетил)феніл]вініл}бензальдегід O((2S,3R,4R,5S,6S)-4-етокси-3,5-диметокси-6-метилтетрагідропіран-2-іл)оксим (сполука 11) 11 UA 107566 C2 1 5 10 Продукт (250 мг, 86%) виділяють у вигляді смоли жовтого кольору: H ЯМР (300 МГц, CDCl3) δ 8,16 (с, 1Н), 7,74 (д, J=8 Гц, 2H), 7,65-7,45 (м, 6H), 7,15 (с, 2H), 5,62 (д, J=1,4 Гц, 1Н), 4,67 (с, 1Н), 4,8-4,5 (м, HH), 3,22 (т, J=8 Гц, 1Н), 1,35-1,2 (м, 6H); Мас-спектроскопія з іонізацією + електророзпиленням: m/z 614 ([M+Na] ). 4-[(Е)-2-(4-трифторметилфеніл)вініл]бензальдегід O-((2S,3R,4R,5S,6S)-3,4,5-триметокси-6метилтетрагідропіран-2-іл)оксим (сполука 12) 1 Продукт (95 мг, 56 %) виділяють у вигляді твердої білої речовини: т. пл. 147-151 °C; H ЯМР (400 МГц, ДМСO-d6) δ 8,42 (с, 1Н), 7,85 (д, J=8,0 Гц, 2H), 7,76-7,67 (м, 6H), 7,47 (с, 2H), 5,52 (д, J=4,0 Гц, 1Н), 3,80 (т, J=4,0 Гц, 1Н), 3,56-3,51 (м, 1Н), 3,43 (с, 3H), 3,42 (с, 3H), 3,41-3,39 (м, 1Н), 3,38 (с, 3H), 3,04 (т, J=8,0 Гц, 1Н), 1,17 (д, J=4,0 Гц, 3H). ПРИКЛАД 9: Загальна методика зв'язування алкіну із бромбензолом 15 20 25 Алкін (0,5 г, 2,7 ммоль), бромбензальдегід (0,45 г, 2,4 ммоль), Pd каталізатор (0,04 г, 0,06 ммоль), CuI (0,02 г, 0,12 ммоль), трифенілфосфін (0,03 г, 0,12 ммоль) і триетиламін (3,5 мл) об’єднують в 1,5 мл безводного ДМФА. Розчин нагрівають до 100 °C в атмосфері азоту з перемішуванням і витримують у вказаних умовах протягом 12 годин. Після цього розчин охолоджують до кімнатної температури, фільтрують через целіт і упарюють з одержанням твердого залишку коричневого кольору, який очищають колонковою хроматографією з нормальною фазою (елюювання: EtOAc у гексанах), одержуючи діарилований ацетилен (512 мг, 65%), який використовують без додаткової ідентифікації. ПРИКЛАД 10: Отримання 4-(4-трифторметоксифенілетиніл)бензальдегіду O((2S,3R,4R,5S,6S)-4-етокси-3,5-диметокси-6-метилтетрагідропіран-2-іл)оксима (сполука 13) 30 35 40 45 Альдегід (0,12 г, 0,42 ммоль) в EtOH (10 мл) обробляють гідроксиламінним проміжним продуктом E-31 (0,10 г, 0,42 ммоль) і отриманий розчин нагрівають до 50 °C при перемішуванні. Після завершення реакції (відповідно до РХ-МС аналізом) розчин охолоджують до кімнатної температури, розбавляють H2O і екстрагують EtOAc (3×10 мл). Об'єднані органічні шари сушать над MgSO4, фільтрують і упарюють, одержуючи твердий залишок жовтого кольору, який очищають колонковою хроматографією з нормальною фазою (елюювання: EtOAc у гексанах). Цільовий продукт (120 мг, 56%) виділяють у вигляді в’язкої твердої речовини жовтого кольору: т. 1 пл. 82-87 °C; H ЯМР (300 МГц, CDCl3) δ 8,13 (с, 1Н), 7,63 (д, J=9,0 Гц, 2H), 7,55 (м, 4H), 7,21 (д, J=9,0 Гц, 2H), 5,63 (с, 1Н), 3,75-3,60 (м, 5H), 3,59 (с, 3H), 3,55 (с, 3H), 3,19 (т, J=9,0 Гц, 1Н), 1,32+ 1,27 (м, 6H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 509 ([M+H] ). Представлені далі сполуки одержують відповідно до методик, описаних у прикладах 9 і 10. 4-(4-Трифторметилфенілетиніл)бензальдегід O-((2S,3R,4R,5S,6S)-4-етокси-3,5-диметокси-6метилтетрагідропіран-2-іл)оксим (сполука 14) Продукт виділяють у вигляді твердої не зовсім білої речовини (137 мг, 76%): т. пл. 1301 132 °C; H ЯМР (400 МГц, ДМСO-d6) δ 8,46 (с, 1Н), 7,81 (с, 4H), 7,73 (д, J=8 Гц, 2H), 7,70 (д, J=8 Гц, 2H), 5,49 (с, 1Н), 3,75 (ушир. с, 1Н), 3,52 (м, 1Н), 3,51-3,46 (м, 3H), 3,45 (с, 3H), 3,43 (с, 3H), 12 UA 107566 C2 3,04 (т, J=8,0 Гц, 1Н), 1,19-1,15 (м, 6H); Мас-спектроскопія з іонізацією електророзпиленням: m/z + 492 ([M+H] ). 4-(4-Трифторметилфенілетиніл)бензальдегід O-((3R,4R,5S,6S)-3,4,5-триметокси-6метилтетрагідропіран-2-іл)оксим (сполука 15) 5 1 10 Продукт (78 мг, 84%) виділяють у вигляді твердої білої речовини: т. пл. 128-136 °C; H ЯМР (400 МГц, CDCl3) δ 8,14 (с, 1Н), 7,65-7,63 (м, 6H), 7,56 (д, J=8,0 Гц, 2H), 5,65 (с, 1Н), 3,76-3,75 (м, 1Н), 3,68-3,64 (м, 1Н), 3,58 (с, 3H), 3,55 (с, 3H), 3,54 (с, 3H), 3,51-3,49 (м, 1Н), 3,20 (т, J=8,0 Гц, 1Н), 1,32 (д, J=4,0 Гц, 3H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 500 + ([M+Na] ). ПРИКЛАД 11: Одержання (2S,3R,4R,5S,6S)-4-етокси-3,5-диметокси-6-метилтетрагідропіран2-ілового ефіру {4-[(E)-2-(4-трифторметилфеніл)вініл]феніл}карбамінової кислоти (сполука 16) 15 20 25 30 До розчину 4-(4-трифторметилфенілвініл)феніламіну (25 мг, 0,095 ммоль) у сухому ТГФ (4 мл) додають 4-нітрофенілхлорформіат (19 мг, 0,095 ммоль). Розчин перемішують в атмосфері азоту протягом 1 години, потім додають рамнопіранозу (сполука E-8; 20 мг, 0,95 ммоль) і порошкоподібний KOH (25 мг, 0,4 ммоль). Розчин перемішують при температурі навколишнього середовища протягом 4 годин, потім розбавляють Et2O (25 мл), промивають H2O, сушать MgSO4 і концентрують. Сире масло червоного кольору очищають хроматографією (силікагель), 1 одержуючи сполуку 16: H ЯМР (300 МГц, CDCl3) δ 7,61 (с, 4H), 7,52 (д, J=8 Гц, 2H), 7,47 (д, J=8 Гц, 2H), 7,2 (д, J=15 Гц, 1Н), 7,05 (д, J=15 Гц, 1Н), 6,74 (с, 1Н), 6,2 (д, J=1,5 Гц, 1Н), 3,8-3,5 (м, HH), 3,23 (т, J=8,0 Гц, 1Н), 1,33-1,25 (м, 6H); Мас-спектроскопія з іонізацією + електророзпиленням: m/z 531 ([M+Na] ). Представлені далі сполуки одержують відповідно до методики, описаної в прикладі 11. (2S,3R,4R,5S,6S)-3,4,5-Триметокси-6-метилтетрагідропіран-2-іловий ефір {4-[(Е)-2-(4етоксифеніл)вініл]феніл}карбамінової кислоти (сполука 17) 1 35 40 Продукт (68 мг, 40%) виділяють у вигляді піни жовтого кольору: H ЯМР (300 МГц, CDCl3) δ 7,38-7,22 (м, 8H), 6,84 (д, J=8,24 Гц, 2H), 6,64 (с, 1Н), 5,65 (с, 1Н), 4,06 (q, J=7,24 Гц, 2H), 3,763,75 (м, 1Н), 3,68-3,64 (м, 1Н), 3,58 (с, 3H), 3,55 (с, 3H), 3,54 (с, 3H), 3,51-3,49 (м, 1Н), 3,20 (т, J=8,0 Гц, 1Н), 1,38-1,28 (м, 6H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 485 + ([M] ). (25,3R,4R,55,65)-4-Пропокси-3,5-диметокси-6-метилтетрагідропіран-2-іловий ефір {4-[(E)-2(4-пентафторетилоксифеніл)вініл]феніл}карбамінової кислоти (сполука 18) 13 UA 107566 C2 1 5 Продукт (18 мг, 12%) виділяють у вигляді смолоподібної твердої речовини: H ЯМР (300 МГц, CDCl3) δ 7,5-7,45 (м, 6H), 7,21 (д, J=8,4 Гц, 2H), 7,05 (с, 2H), 6,91 (с, 1Н), 5,27 (ушир. с, 1Н), 3,8 (м, 1Н), 3,69-3,50 (м, 10H), 3,23 (т, J=8 Гц, 1Н), 1,69 (м, 2H), 1,3 (д, J=6 Гц, 3H), 0,98 (т, J=7,5 + Гц, 3H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 591 ([M+H] ). ПРИКЛАД 12: Одержання (2S,3R,4R,5S,6S)-3,5-диметокси-4-етокси-6-метилтетрагідропіран2-ілового ефіру [4-(3-трифторметоксифенілазо)феніл]карбамінової кислоти (сполука 19) 10 15 20 25 30 35 Стадія 1. 4-(3-Трифторметоксифенілазо)анілін. 3-Трифторметоксіанілін (2,0 г, 11 ммоль) розчиняють в CH2Cl2 (20 мл), отриманий розчин обробляють сумішшю Oxone™ (11 г, 18 ммоль) і H2O (20 мл), розчин перемішують протягом 20 годин при 25 °C. Органічну фазу відділяють, водну фазу екстрагують CH2Cl2 (2×20 мл), об'єднані органічні фази сушать (Na 2SO4) і упарюють. Сиру нітрозосполуку розчиняють в оцтовій кислоті (40 мл), розчин обробляють пфенілендіаміном (2,0 г, 19 ммоль) і суміш перемішують протягом 60 годин. Леткі компоненти видаляють у вакуумі і залишок очищають хроматографією (силікагель, елюювання із градієнтом: EtOAc/гексан від 0 до 20%), одержуючи азоанілін (900 мг, 27%) у вигляді масла 1 жовтогарячого кольору: H ЯМР (300 МГц, CDCl3) δ 7,77-7,84 (м, 3H), 7,71 (с, 1Н), 7,46-7,52 (м, 1Н), 7,22-7,26 (м, 1Н), 6,71-6,75 (м, 2H), 4,12 (ушир. с, 2H); Мас-спектроскопія з іонізацією + електророзпиленням: m/z 282 ([M+H] ). Стадія 2. Сполука 19. 4-(3-Трифторметоксифенілазо)анілін (200 мг, 0,71 ммоль) розчиняють у безводному ТГФ (5 мл), суміш обробляють 4-нітрофенілхлорформіатом (170 мг, 0,82 ммоль) і перемішують протягом 1 години при 25 °C. До суміші додають (3R,4R,5S,6S)-4-етокси-3,5диметокси-6-метилтетрагідропіран-2-ол (175 мг, 0,78 ммоль) і 95% гідрид натрію (NaH; 35 мг, 2,1 ммоль) і суміш перемішують протягом 2 годин. До суміші додають H 2O (20 мкл, 1 ммоль) і суміш перемішують протягом 1 години. Суміш розбавляють H2O (10 мл) і EtOAc (15 мл). Відділену органічну фазу промивають H2O (5 мл) і розчином солі (5 мл), сушать (Na2SO4) і упарюють. Залишок очищають хроматографією (силікагель, елюювання із градієнтом: EtOAc/гексан, від 0 до 30%), одержуючи вказане в заголовку сполуку (220 мг, 59%) у вигляді 1 масла: H ЯМР (400 МГц, CDCl3) δ 7,87-7,97 (м, 3H), 7,77 (с, 1Н), 7,54-7,57 (м, 4H), 6,94 (с, 1Н), 6,22(с, 1Н), 3,56-3,78 (м, HH), 3,24 (т, J=9,2 Гц, 1Н), 1,28-1,36 (м, 6H); Мас-спектроскопія з + іонізацією електророзпиленням: m/z 528 ([M+H] ). Представлені далі сполуки одержують відповідно до методики, описаної в прикладі 12. (2S,3R,4R,5S,6S)-4-Етокси-3,5-диметокси-6-метилтетрагідропіран-2-іловий ефір [4-(4трифторметоксифенілазо)феніл]карбамінової кислоти (сполука 20) 40 45 1 Стадія 1. 4-(4-трифторметилоксифенілазо)анілін. H ЯМР (300 МГц, CDCl3) δ 7,79-7,83 (м, 4H), 7,25-7,33 (м, 2H), 6,72-6,75 (м, 2H), 4,09 (ушир. с, 2H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 282 (M+H). 1 Стадія 2. Сполука 20. Т. пл. 158-159 °C; H ЯМР (400 МГц, CDCl3) δ 7,95-7,92 (м, 4H), 7,597,57 (д, J=8,6 Гц, 2H), 7,34 (д, J=8,1 Гц, 2H), 6,86 (с, 1Н), 6,21 (с, 1Н), 3,8-3,5 (м, HH), 3,22 (т, J=9,4 Гц, 1Н), 1,35-1,25 (м, 6H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 528 + ([M+H] ). 14 UA 107566 C2 (2S,3R,4R,5S,6S)-4-Етокси-3,5-диметокси-6-метилтетрагідропіран-2-іловий трифторметилфенілазо)феніл]карбамінової кислоти (сполука 21) 5 10 ефір [4-(4 1 Стадія 1. 4-(4-Трифторметилфенілазо)анілін. H ЯМР (300 МГц, CDCl3) δ 7,81-7,91 (м, 4H), 7,72 (д, J=8,2 Гц, 2H), 6,71-6,75 (м, 2H), 4,12 (ушир. с, 2H); Мас-спектроскопія з іонізацією + електророзпиленням: m/z 266 ([M+H] ). 1 Стадія 2. Сполука 21. Т. пл. 186-188 °C; H ЯМР (400 МГц, CDCl3) δ 7,89-8,2 (м, 4H), 7,77 (д, J=8,3 Гц, 2H), 7,60 (д, J=8,6 Гц, 2H), 6,91 (с, 1Н), 6,21 (с, 1Н), 3,77-3,57 (м, 11H), 3,22 (т, J=9,4 Гц, + 1Н), 1,34-1,28 (м, 6H); Мас-спектроскопія з іонізацією електророзпиленням: m/z 512 ([M+H] ). (2S,3R,4R,5S,6S)-4-Етокси-3,5-диметокси-6-метилтетрагідропіран-2-іловий ефір [4-(4пентафторетилоксифенілазо)феніл]карбамінової кислоти (сполука 22) 15 1 20 25 30 35 40 45 Стадія 1. 4-(4-Пентафторетоксифенілазо)анілін. H ЯМР (300 МГц, CDCl3) δ 7,89-7,79 (м, 4H), 7,32 (д, J=8,5 Гц, 2H), 6,73-6,76 (м, 2H), 4,09 (ушир. с, 2H); Мас-спектроскопія з іонізацією + електророзпиленням: m/z 332 ([M+H] ). Стадія 2. Сполука 22.1H ЯМР (300 МГц, CDCl3) δ 7,96-7,92 (м, 4H), 7,60-7,57 (м, 2H), 7,387,35 (м, 2H), 6,86 (с, 1Н), 6,26 (с, 1Н), 3,75-3,45 (м, HH), 3,22 (т, J=9,3 Гц, 1Н), 1,33-1,26 (м, 6H); + Мас-спектроскопія з іонізацією електророзпиленням: m/z 578 ([M+H] ). ВИПРОБУВАННЯ БІОЛОГІЧНОЇ АКТИВНОСТІ СПОЛУК Випробування біологічної активності на совці малій (BAW; Spodoptera exigua: лускокрилі (Lepidoptera)) проводять за допомогою біотесту з використанням 96-ямкового мікропланшета високої пропускної здатності (high throughput - HTS) або біотесту з використанням 128-ямкового харчового планшета. HTS біотест оснований на модифікації способу, описаного в публікації Lewer et al. J. Nat. Prod. 2006, 69, 1506. Яйця BAW поміщають на штучний корм (100 мкл) у кожну ямку 96-ямкового титраційного мікропланшета. Корм попередньо обробляють випробовуваними сполуками (12 мкг, розчинені в 30 мкл суміші ДМСО-ацетон-H2О), наносячи їх шарами зверху корму з використанням рідинної системи нанесення і потім залишаючи для сушіння на декілька годин. Після цього інвазовані планшети закривають шаром стерильного бавовняного ватину і кришкою планшета і потім витримують у темряві при 29 °C. Смертність підраховують на 6 день після обробки. Кожний планшет піддають шести реплікаціям. Відсоток смертності підраховують як середнє значення шести реплікацій. У випадку біотесту з використанням 128-ямкового планшета з кормом від трьох до п'яти BAW личинок других вікових стадій поміщають у кожну ямку (3 мл) планшета з кормом, які попередньо заповнюють 1 мл штучного корму з нанесеним на нього 50 мкг/см випробовуваної сполуки (розчиненої в 50 мкл суміші (90:10) ацетон-вода) (на кожну з восьми ямок) і потім залишають для сушіння. Планшети закривають прозорою самоклейкою кришкою і витримують при 25 °C з режимом світло-темрява 14:10 протягом шести днів. Відсоток смертності личинок записують для кожної ямки; активності, отримані для восьми ямок, усереднюють. Результати представлені в таблиці 4. У таблиці 4 під шапками BAW HTS і BAW 50 в обох стовпцях "A" означає, що сполука була випробувана і спостерігалася щонайменше 50 процентна смертність, у той час як "B" означає, що або (1) сполука була випробувана і спостерігалася смертність менше 50 відсотків, або (2) сполука не випробовувалася. 15 UA 107566 C2 Таблиця 1 Загальна формула # A R1 R2 R3 R4 Цукор МС Температур а кипіння Е-1 OCH3 OCH3 OCH3 OCH3 CH3 L-рамноза 150 °C (0,5 мм Hg = 66,66 Па) E-2 OCH3 OCH3 OCH3 CH3 L-рамноза 145-155 °C (1 мм Hg = 133,32 Па) E-3 OCH3 OCH3 OC2H5 OCH3 CH3 L-рамноза 202,9 (М-МеОН) 165 °C (10 мторр = 1,333 Па) E-4 OC2H5 OC2H5 OC2H5 OC2H5 CH3 L-рамноза 299,1 (M+Na) 180 °C (10 мторр = 1,333 Па) Е-5 OCH3 OCH3 OC3H7 OCH3 CH3 L-рамноза 175 °C (10 мторр = 1,333 Па) Е-6 OCH3 OCH3 О-аліл OCH3 CH3 L-рамноза 175 °C (10 мторр = 1,333 Па) Е-7 OCH3 OCH3 OC4H9 OCH3 CH3 L-рамноза 165 °C (5 мторр = 0,667 Па) OH 16 1 Н ЯМР (CDCl3, δ) 5,28 (м, 1H), 3,85 (м, 1H), 3,66 (м, 1H), 3,60-3,50 (м, 1H), 3,58 (с, 3H), 3,53 (с, 6H), 3,37 (с, 3H), 3,16 (т, 1H), 1,31 (д, J=6,2 Гц, 3H) 5,28 (с, 1H), 3,83 (м, 1H), 3,7-3,45 (м, 11H), 3,16 (т, J=9,2 Гц, 1Н),3,0(с, 1H), 1,31 (д, J=6 Гц, 3H) 4,71 (д, J=1,8 Гц, 1H), 3,77-3,50 (м, 11H), 3,37 (с, 3H), 3,13 (т, J=9,4 Гц, 1Н), 1,32 (д, J=6,3 Гц, 3H), 1,27 (т, J=7,0 Гц, 3H) 4,72 (д, J=1,8 Гц) і 4,30 (с, сукупний 1H), 4,0-3,35 (серії м, 10H), 3,2 (м, 2H), 1,3-1,1 (м, 15H) 4,70 (д, J=1,8 Гц, 1H), 3,77-3,50 (м, 11H), 3,37 (с, 3H), 3,13 (т, J=9,4 Гц, 1H), 1,62 (м, 2H), 1,32 (д, J=6,3 Гц, 3H), 0,98 (т, J=7,5 Гц, 3H) 5,98 (м, 1H), 5,32 (д, 1H), 5,20 (д, 1H), 4,50 (с, 1H), 4,18 (д, 2H), 3,62-3,50 (м, 9H), 3,28 (с, 3H), 3,17 (т, J=6,3 Гц, 1H), 1,33 (д, J=6,3 Гц, 3H) 4,71 (с, 1H), 3,623,50 (м, 11H), 3,35 (с, 3H), 3,17 (т, 1H), 1,6 (м, 2H), 1,4 (м, 2H), 1,33 (д, J=6,3 Гц, 3H), 0,98 (т, J=7,5 Гц, 3H) UA 107566 C2 Е-8 ОН OCH3 OC2H5 OCH3 CH3 L-рамноза 202,9 (М-Н2О) 165 °C (9 мторр = 1,1999 Па) Е-9 ОН OC2H5 OC2H5 OC2H5 CH3 L-рамноза 248,2 (М+) 203 °C (5 мторр = 0,667 Па) Е-10 ОН OCH3 OC3H7 OCH3 CH3 L-рамноза 220,2 (М+) 185 °C (5 мторр = 0,667 Па) Е-11 ОН OCH3 О-аліл OCH3 CH3 L-рамноза 254,9 (M+Na) 175 °C (10 мторр = 1,333 Па) Е-12 ОН OCH3 OC4H9 OCH3 CH3 L-рамноза 248,2 (М+) 189 °C (5 мторр = 0,667 Па) Е-13 -ОН -OCH3 -OCH3 -OCH3 CH2OCH3 L-маноза Е-14 -ОН -OCH3 -OCH3 -OCH3 CH2OCH3 D-глюкоза 17 5,35 (м, J=3,2, 2,0 Гц, 1H), 3,84-3,62 (м, 5H), 3,59 (с, 3H), 3,53 (с, 3H), 3,16 (т, J=9,5 Гц, 1H), 2,73 (д, J=3,4 Гц, 1H), 1,33-1,26 (м, 6H) 5,2 (с) і 4,65 (дд, J=1,2, 9 Гц, сигнали аномерних протонів, сукупний 1H, співвідношення α:β = 64:36); 4,103,45 (м, 8H), 3,363,20 (м, 2H), 1,371,13 (м, 12H) 5,25 (дд, J=3,2, 2,0 Гц) і 4,61 (м, сукупний 1H), 3,80 (м, 1H), 3,70-3,50 (м, 9H), 3,36-3,05 (м, 1H), 1,60 (м, 2H), 1,30 (м, 5H), 0,95 (т, J=7,5 Гц, 3H) 5,95 (м, 1H), 5,3 (м, 1H), 5,19 (м, 1H), 5,21 і 4,61 (обоє м, α і β аномери, сукупний 1H), 4,20 (м, 2H), 3,80 (м, 1H), 3,70-3,50 (м, 7H), 3,40-3,10 (м, 3H), 1,3 (м, 3H) 5,35 (дд, J=3,2, 2,0 Гц) і 4,45 (м, сукупний 1H), 3,80 (м, 1H), 3,70-3,50 м, 10H), 3,36-3,05 (м, 1H), 2,73 (д, J=3,4 Гц, 1H), 1,60 (м, 2H), 1,40 (м, 2H), 1,33 (д, J=6 Гц, 3H), 0,95 (т, J=7,5 Гц, 3H) 5,32 (с, 1H), 3,9 (м, 1H), 3,66-3,53 (серії м, 4H), 3,52 (с, 3H), 3,51 (с, 3H), 3,49 (с, 3H), 3,40 (с, 3H), 3,35 (м, 1H), 3,18 (д, J=3 Гц, 1H) 5,33 (д, J=3,6 Гц) і 4,60 (д, J=4 Гц, α і β аномери, сукупний 1H), 3,9 (м, 1H), 3,63,3 (серії с і м, 14H), 3,28 (м, 3H), 1,7 (с, 1H) UA 107566 C2 Е-15 -OCH3 -OCH3 -OCH3 -OCH3 -Н2 L-ксилоза 207 (М+Н) Е-16 -ОН -OCH3 -OCH3 -OCH3 -Н2 L-ксилоза 175 (М-Н2 О) Е-17 -OCH3 -OCH3 -OCH3 -OCH3 -Н2 L-ліксоза 207 (М+Н2О) Е-18 -ОН -OCH3 -OCH3 -OCH3 -Н2 L-ліксоза 175 (М-Н2О) Е-19 -OCH3 -OCH3 -OCH3 -OCH3 CH2OCH3 L-глюкоза 205 (МCH2OCH3) Е-20 -ОН -OCH3 -OCH3 -OCH3 CH2OCH3 L-глюкоза 191 (МТ. пл. CH2OCH3) 63-67 °C Е-21 -OCH3 -Н2 -OCH3 -OCH3 CH2OCH3 2-дезоксиD-глюкоза 18 220 + (М ) 4,77 (д, J=3,5 Гц) і 4,15 (д, J=7,4 Гц, сукупний 1H у співвідношенні 0,27:1 α:β), 4,00 (дд, J=11,6, 5,0 Гц, 1H), 4,03-2,93 (серії с і м, 16H) 5,23 (т, J=3,4 Гц) і 4,60 (т, J=6,3 Гц, сукупний 1H у співвідношенні 1,5:1 α:β), 4,01-2,97 (серії с і м, 15H) 4,69 (д, J=3,0 Гц, 1H, α aнoмeр), 3,77 (дд, J=10,8, 4,7 Гц, 1H), 3,62-3,32 (серії с і м, 16H) 5,18-5,11 (м, 1H, суміш α і β аномерів), 4,84 (д, J=10,1 Гц, 0,4H), 3,98-3,37 (серії с і м, 14H), 3,11 (д, J=4,2 Гц, 0,6H) (600 МГц, CДC13) 4,83 (д, J=4,1 Гц) і 4,14 (д, J=7,8 Гц, сукупний 1H у співвідношенні 0,2:1 α:β), 3,66-3,36 (серії с і м, 18H), 3,29-3,26 (м, 1H), 3,17-3,13 (м, 1H), 3,01-2,94 (м, 1H) 5,33 (д, J=3,7 Гц) і 4,58 (д, J=7,9 Гц, сукупний 1H у співвідношенні 2,5:1 α:β), 3,92-3,86 (м, 0,8H), 3,65-3,08 (серії с і м, 18H), 2,96 (дд, J=8,8, 7,8 Гц, 0,2H) 4,81 (дд, J=3,6, 1,1 Гц) і 4,34 (дд, J=9,5, 1,9 Гц, сукупний 1H у співвідношенні 0,29:1 α:β), 3,713,23 (м, 16H), 3,183,05 (м, 1H), 2,332,16 (м, 1H), 1,601,41 (м, 1H) UA 107566 C2 Е-22 -OCH3 -Н2 -OCH3 ОН CH3 4,78 (д, J=3,3 Гц, 1H), 3,52 (м, 1H), 3,47 (м, 1H), 3,45 (с, 3H), 3,30 (с, 3H), 3,19 (м, 1H), 2,67 (ушир. с, 1H), 2,29 (дд, J=4,8, 12,9 Гц, 1H), 1,51 (м, 1H), 1,32 (д, J=6,3 Гц, 3H) lолеандроза Таблиця 2 Загальна формула R4 Цукор МС Е-23 OCH3 OCH3 OCH3 CH3 L-рамноза 326,1 + [M+Na] Е-24 OCH3 OCH3 CH3 L-рамноза 288 [М-Н] E-25 OCH3 OC2H5 OCH3 CH3 L-рамноза E-26 OCH3 OC3H7 OCH3 CH3 L-рамноза # R1 R2 R3 ОН 19 354 + [M+Na] Т. пл. 1 Н ЯМР (CDCl3, δ) 5,35 (д, J=2,0 Гц, 1H), 4,29 (м, 1 H), 3,89 (дд, J=3,3, 2,1 Гц, 1H), 3,55 (с, 3H), 135 °C 3,54 (с, 3H), 3,52 (с, 3H), 3,51 (м, 1H), 3,18 (т, J=9,3 Гц, 1H), 2,74 (с, 4H), 1,27 (д, J=6,1 Гц, 3H) 5,42 (с, 1H), 4,40 (м, 1H), 4,0 (м, 1H), 3,63 (д, J=8 Гц, 1H), 3,55163-166 °C 3,45 (м, 7H), 2,78 (с, 4H), 2,2 (ушир. с, 1H), 1,30 (д, J=6,3 Гц, 3H) 5,35 (м, 1H), 4,29 (м, 1H), 3,85 (м, 1H), 3,78-3,50 (м, 9H), 3,19 (т, J=9,5 Гц, 1H), 2,75 (с, 4H), 1,33-1,26 (м, 6H) 5,35 (с, 1H), 4,29 (м, 1H), 3,84 (м, 1H), 3,78-3,50 (м, 9H), 3,19 (т, J=9,5 Гц, 69-71 °C 1H), 2,75 (с, 4H), 1,64 (м, 2H), 1,25 (д, J=6,1 Гц, 3H), 0,95 (т, J=7,5 Гц, 3H) UA 107566 C2 E-27 OCH3 OC4H9 OCH3 CH3 5,32 (д, J=1,8 Гц, 1Н),4,29(м, 1H), 3,84 (м, 1H), 3,6-3,45 (м, 9H), 3,17 (т, J=9,3 Гц, 1H), 2,73 (с, 4H), 1,6 (м, 2H), 1,4 (м, 2H), 1,26 (д, J=5,7 Гц, 3H), 0,93 (т, J=7,5 Гц, 3H) 5,52 (д, J=4 Гц, 1H), 4,45 (д, J=10 Гц, 1H), 3,68-3,47 (м, 12H), 3,4-3,27, (серії м, 5H), 2,72 (с, 4H) 5,44 (с, 1H), 4,29 (м, 1H), 3,90 (м, 1H), 3,7-3,55 (м, 3H), 3,54 (с, 3H), 3,53 (с, 3H), 3,52 (с, 3H), 3,53 (м, 1H), 3,38 (с, 3H), 2,73 (с, 4H) L-рамноза E-28 OCH3 OCH3 OCH3 CH2OCH3 D-глюкоза Е-29 OCH3 OCH3 OCH3 CH2OCH3 L-рамноза Таблиця 3 R4 Цукор МС Е-30 OCH3 OCH3 OCH3 CH3 L-рамноза 221,7 + (М+Н ) Е-31 OCH3 OC2H5 OCH3 CH3 L-рамноза 258,1 + (M+Na ) Е-32 OCH3 OC3H7 OCH3 CH3 L-рамноза 249,1 + (М+Н ) Е-33 OCH3 OC4H9 OCH3 CH3 L-рамноза # R1 R2 R3 20 Т. пл. 1 Н ЯМР (CDCl3, δ) 5,51 (с, 2H), 4,98 (д, J=1,8 Гц, 1H), 3,60 (м, 2H), 3,55 (с, 3H), 3,50 (с, 3H), 3,48 (с, 55 °C 3H), 3,35 (дд, J=9,2, 3,3 Гц, 1H), 3,13 (т, J=9,4 Гц, 1H), 1,34 (д, J=6,2 Гц, 3H) 5,51 (с, 2H), 4,98 (д, J=1,8 Гц, 1H), 3,60 (м, 4H), 3,55 (с, 3H), 88 °C 3,48 (с, 3H), 3,35 (дд, J=9,2, 3,3 Гц, 1H), 3,13 (т, J=9,4 Гц, 1H), 1,34-1,26 (м, 6H) 5,6 (с, 2H), 4,95 (д, J=1,8 Гц, 1H), 3,6-3,3 (м, 11H), 3,13 (т, 49 °C J=9,3 Гц, 1H), 1,65 (м, 2H), 1,34 (д, J=6,2 Гц, 3H), 0,97 (т, J=7,5 Гц, 3H) 5,6 (с, 2H), 4,97 (д, J=1,8 Гц, 1Н), 3,6-3,3 (м, 11H), 3,13 (т, 40-42 °C J=9,3 Гц, 1Н), 1,62 (м, 2H), 1,40 (м, 2H), 1,34 (д, J=6,2 Гц, 3H), 0,94 (т, J=7,5 Гц, 3H) UA 107566 C2 Е-34 OC2H5 OC2H5 OC2H5 CH3 L-рамноза 264,1 + (M+Na ) Масло Е-35 OCH3 OCH3 CH3 L-рамноза 268 (М+АсОН) Масло Е-36 OCH3 OCH3 OCH3 CH2OCH3 L-маноза 251,1 + (М+Н ) 58 °C Е-37 OCH3 OCH3 OCH3 L-фукоза 5,5 (с, 2H), 4,90 (с, 1H), 3,9 (м, 1H), 3,803,50 (м, 7H), 3,4 (м, 1H), 3,25 (т, J=9 Гц, 1H), 1,35 (д, J=6,3 Гц, 3H), 1,27 (м, 9H) 5,6 (ушир. с, 2H), 4,96 (с, 1H), 3,7-3,5 (м, 3H), 3,48 (с, 3H), 3,42 (с, 3H), 3,25 (дд, J=10, 3 Гц, 1H), 2,75 (ушир. с, 1H), 1,7 (д, J=7 Гц, 3H) 5,5 (ушир. с, 2H), 5,04 (д, J=2 Гц, 1H), 3,65-3,58 (м, 4H), 3,52 (с, 3H), 3,48 (два с, 6H), 3,42 (с, 3H), 3,45-3,39 (м, 2H) 5,58 (с, 2H), 5,1 (д, J=4 Гц, 1H), 3,60 (кВ, J=6,8 Гц, 1H), 3,66 (м, 1H), 3,60 (с, 3H), 3,53 (с, 3H), 3,51 (с, 3H), 3,5-3,4 (м, 2H), 1,34 (д, J=6,4 Гц, 3H) 5,6 (ушир. с, 2H), 5,1 (д, J=4 Гц, 1H), 3,7 (с, 3H), 3,55 (с, 3H), 3,53 (с, 3H), 3,41 (с, 3H), 3,65-3,35 (серії м, 3H), 3,4 (м, 1H), 3,2 (м, 2H) ОН CH3 Е-38 OCH3 OCH3 OCH3 CH2OCH3 91 °C 251,8 + (М+Н) D-глюкоза 82 °C Таблиця 4 BAW BAW Спо50 HTS лука A A 1 Ar1 CH Подвійний CH R4 ано- Цукор мер LCH Подвійний N OCH3 OC3H7 OCH3 CH3 α E G M Ar2 зв’язок J L K R1 R2 R3 зв’язок рамноза A A 2 CH Подвійний CH CH Подвійний N OCH3 OC2H5 OCH3 CH3 α Lрамноза B B 3 CH Подвійний CH CH Подвійний N OCH3 OC2H5 OCH3 CH3 α Lрамноза B B 4 CH Подвійний CH CH Подвійний N OCH3 OC2H5 OCH3 CH3 α Lрамноза A B 5 CH Подвійний CH CH Подвійний N OCH3 OC2H5 OCH3 CH3 α Lрамноза зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок 21 UA 107566 C2 A 6 CH Подвійний CH CH Подвійний N OCH3 OC2H5 OCH3 CH3 α Lрамноза A B 7 CH Подвійний CH CH Подвійний N OCH3 OC2H5 OCH3 CH3 α Lрамноза A A 8 CH Подвійний CH CH Подвійний N OCH3 OCH3 OCH3 CH3 α Lрамноза A B 9 CH Подвійний CH CH Подвійний N OCH3 OCH3 OCH3 CH3 α Lрамноза A A 10 CH Подвійний CH CH Подвійний N OCH3 OC3H7 OCH3 CH3 α Lрамноза B A 11 CH Подвійний CH CH Подвійний N OCH3 OC2H5 OCH3 CH3 α Lрамноза A A 12 CH Подвійний CH CH Подвійний N OCH3 OCH3 OCH3 CH3 α Lрамноза A A 13 C Подвійний C CH Подвійний N OCH3 OC2H5 OCH3 CH3 α Lрамноза A A 14 C Подвійний C CH Подвійний N OCH3 OC2H5 OCH3 CH3 α Lрамноза A A 15 C Подвійний C CH Подвійний N OCH3 OCH3 OCH3 CH3 α Lрамноза A A 16 CH Подвійний CH NH Подвійний CO OCH3 OC2H5 OCH3 CH3 α Lрамноза A B 17 CH Подвійний CH NH Подвійний CO OCH3 OCH3 OCH3 CH3 α Lрамноза A B 18 CH Подвійний CH NH Подвійний CO OCH3 OC3H7 OCH3 CH3 α Lрамноза A A 19 N Подвійний N N Подвійний CO OCH3 OC2H5 OCH3 CH3 α Lрамноза A A 20 N Подвійний N N Подвійний CO OCH3 OC2H5 OCH3 CH3 α Lрамноза B A 21 N Подвійний N N Подвійний CO OCH3 OC2H5 OCH3 CH3 α Lрамноза A 5 A A 22 N Подвійний N N Подвійний CO OCH3 OC2H5 OCH3 CH3 α Lрамноза зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок зв’язок КИСЛОТНІ І СОЛЬОВІ ПОХІДНІ І СОЛЬВАТИ Сполуки, розкриті в даному винаході, можуть бути представлені формі пестицидноприйнятних кислотно-адитивних солей. Як приклад, який не є обмеженням даного винаходу, амінна функція може утворювати солі із соляної, бромистоводневої, сірчаної, фосфорної, оцтової, бензойної, лимонної, малонової, саліцилової, яблучної, фумарової, щавлевої, винної, молочної, глюконової, аскорбінової, малеїнової, аспаргінової, бензолсульфонової, метансульфонової, етансульфонової, гідроксиметансульфонової і гідроксіетансульфонової кислотами. 22 UA 107566 C2 5 10 15 20 25 30 35 40 45 50 55 60 Крім того, як приклад, який не є обмеженням даного винаходу, кислотна функція може утворювати солі, включаючи солі лужних і лужноземельних металів і солі амонію і амінні солі. Приклади переважних катіонів включають катіони натрію, калію, магнію і амінію. Солі одержують контактуванням вільної основи з достатньою кількістю бажаної кислоти для одержання солі. Сполуки у формі вільної основи можуть регенеруватися обробкою солі прийнятним розведеним водним розчином основи, таким як розведений водний розчин гідроксиду натрію (NaOH), карбонату калію, амонію і гідрокарбонату натрію. Наприклад, у ряді випадків пестицид модифікується в більш розчинну форму, наприклад, диметиламінна сіль (2, 4-дихлорфенокси)оцтової кислоти є більш розчинною у воді формою (2, 4дихлорфенокси)оцтової кислоти, яка являє собою відомий гербіцид. Сполуки, розкриті в даному винаході, також можуть утворювати стабільні комплекси з молекулами розчинника, які залишаються інтактними після видалення із сполуки. Ці комплекси найчастіше називають "сольватами". СТЕРЕОІЗОМЕРИ Деякі сполуки, розкриті в даному винаході, можуть існувати у формі одного або декількох стереоізомерів. Різні стереоізомери включають геометричні ізомери, діастереомери і енантіомери. Таким чином, сполуки, розкриті в даному винаході, включають рацемічні суміші, окремі стереоізомери і оптично активні суміші. Фахівець в даній галузі техніки повинен уявляти, що один стереоізомер може бути більш активним, ніж інші. Окремі стереоізомери і оптично активні суміші можуть бути отримані з використанням методик селективного синтезу, методик стандартного синтезу з розділенням вихідних речовин або стандартними методиками поділу. ШКІДНИКИ В одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби із сільськогосподарськими шкідниками. У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби із круглими хробаками (Phylum Nematoda). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби зі членистоногими (Phylum Arthropoda). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби із представниками класу членистоногих з підтипу хеліцерових (Subphylum Chelicerata). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби зі шкідниками класу павукоподібних або арахнід (Class Arachnida). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби зі шкідниками підтипу членистоногих (Subphylum Myriapoda). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби зі шкідниками класу симфіл (Class Symphyla). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби зі шкідниками підтипу шестиногих (Subphylum Hexapoda). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби зі шкідниками класу комах (Class Insecta). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби із представниками ряду Coleoptera (жорсткокрилі або жуки). Невичерпний перелік вказаних шкідників включає, але без обмеження, наступних представників вказаного ряду: Acanthoscelides spp. (довгоносики), Acanthoscelides obtectus (зернівка квасолева), Agrilus planipennis (златка ясенова смарагдова вузькотіла), Agriotes spp. (дротяники), Anoplophora glabripennis (вусань азіатський), Anthonomus spp. (квіткогризи), Anthonomus grandis (довгоносик бавовняний), Aphidius spp., Apion spp. (насіннєїди), Apogonia spp. (личинки), Ataenius spretulus (Black Turfgrass Ataenius), Atomaria linearis (крихітка бурякова), Aulacophore spp., Bothynoderes punctiventris (довгоносик буряковий), Bruchus spp. (зернівки), Bruchus pisorum (зернівка горохова), Cacoesia spp., Callosobruchus maculatus (зернівка чотириплямистя), Carpophilus hemipteras (блискітник сухофруктовий), Cassida vittata, Cerosterna spp., Cerotoma spp. (листоїди), Cerotoma trifurcata (листоїд бобовий), Ceutorhynchus spp. (скритохоботники), Ceutorhynchus assimilis (скритохоботник ріпаковий насінний), Ceutorhynchus napi (скритохоботник суріпковий), Chaetocnema spp. (crystomelids), Colaspis spp. (soil beetlеs), Conoderus scalaris, Conoderus stigmosus, Conotrachelus nenuphar (сливовий довгоносик), Cotinus nitidis (Green June beetle), Crioceris asparagi (спаржева льоночистка), Cryptolestes ferrugineus (борошноїд рижий коротковусий), Cryptolestes pusillus (борошноїд малий), Cryptolestes turcicus (Turkish grain beetle), Ctenicera spp. (wireworms), Curculio spp. (свинки, довгоносики), 23 UA 107566 C2 5 10 15 20 25 30 35 40 45 50 55 60 Cyclocephala spp. (grubs), Cylindrocopturus adspersus (sunflower stem weevil), Deporaus marginatus (mango leaf-Cutting weevil), Dermestes lardarius (шкіроїд шинковий), Dermestes maculates (шкіроїд плямистий), Diabrotica spp. (chrysomelids), Epilachna varivestis (Mexican bean beetle), Faustinus cubae, Hylobius pales (pales weevil), Hypera spp. (слоники, довгоносики), Hypera postica (листовий люцерновий довгоносик), Hyperdoes spp. (Hyperodes weevil), Hypothenemus hampei (coffee berry beetle), Ipsspp. (короїди), Lasioderma serricorne (жук тютюновий), Leptinotarsa decemlineata (жук колорадський картопляний), Liogenys fuscus, Liogenys suturalis, Lissorhoptrus oryzophilus (довгоносик рисовий водяник), Lyctus spp. (деревогризи), Maecolaspis joliveti, Megascelis spp., Melanotus communis, Meligethes spp., Meligethes aeneus (ріпаковий квіткогриз), Melolontha melolontha (хрущ західний звичайний), Oberea brevis, Oberea linearis, Oryctes rhinoceros (носоріг пальмовий), Oryzaephilus mercator (плоскотілка арахісова), Oryzaephilus surinamensis (рисоїд сурінамський), Otiorhynchus spp. (плосконоси), Oulema melanopus (пиявиця червоногруда), Oulema oryzae, Pantomorus spp. (слоники), Phyllophaga spp. (May/June beetlе), Phyllophaga cuyabana, Phyllotreta spp. (chrysomelids), Phynchites spp., Popillia japonica (японський жук), Prosteрhanus truncates (larger grain borer), Rhizopertha dominica (шашіль зерновий), Rhizotrogus spp. (European chafer), Rhynchophorus spp. (weevils), Scolytus spp. (заболонники), Shenophorus spp. (Billbug), Sitona lineatus (довгоносик смугастий бульбочковий), Sitophilus spp. (довгоносики комірні), Sitophilus granaries (довгоносик комірний звичайний), Sitophilus oryzae (довгоносик комірний рисовий), Stegobium paniceum (шашіль хлібний), Tribolium spp. (flour beetles), Tribolium castaneum (хрущак малий булавовусий), Tribolium confusum (хрущак борошняний малий), Trogoderma variabile (трогодерма мінлива) і Zabrus tenebioides (жужелиця хлібна). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Dermaptera (шкірястокрилі, щипавки). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Dictyoptera (таргани). Невичерпний перелік вказаних шкідників включає, але без обмеження наступних представників вказаного ряду: Blattella germanica (тарган рудий), Blatta orientalis (тарган чорний), Parcoblatta pennsylvanica, Periplaneta americana (тарган американський), Periplaneta australoasiae (тарган австралійський), Periplaneta brunnea (тарган коричневий), Periplaneta fuliginosa (тарган димчасто-коричневий), Pycnoscelus surinamensis (тарган суринамский), Supella longipalpa (тарган буросмугастий). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Diptera (двокрилі або мухи). Невичерпний перелік вказаних шкідників включає, але без обмеження наступних представників вказаного ряду: Aedes spp. (комарі), Agromyza frontella (мінер листовий люцерновий), Agromyza spp. (мінери листові), Anastrepha spp. (осетниці), Anastrepha suspensa (Caribbean fruit fly), Anopheles spp. (комарі малярійні), Batrocera spp. (осетниці, мухи фруктові), Bactrocera cucurbitae (східна диняча муха), Bactrocera dorsalis (східна плодова муха), Ceratitis spp. (плодові мухи), Ceratitis capitata (середземноморська плодова муха), Chrysops spp. (ґедзі-золотоочки), Cochliomyia spp. (личинки мухи м'ясної), Contarinia spp. (галиці), Culex spp. (комарі), Dasineura spp. (галиці), Dasineura brassicae (галиця ріпакова), Delia spp., Delia platura (муха паросткова), Drosophila spp. (мушкидрозофіли, плодові мушки), Fannia spp. (кімнатні мухи), Fannia canicularis (муха кімнатна мала), Fannia scalaris (муха сходова), Gasterophilus intestinalis (ґедзь кінський), Gracillia perseae, Haematobia irritans (horn fly), Hylemyia spp. (root maggots), Hypoderma lineatum (стравохідник, ґедзь малий), Liriomyza spp. (мінери), Liriomyza brassica (мінер хрестоцвітий), Melophagus ovinus (вовноїд овечий), Musca spp. (мухи справжні), Musca autumnalis (муха польова, корівниця осіння), Musca domestica (муха кімнатна), Oestrus ovis (курчак овечий), Oscinella frit (муха шведська), Pegomyia betae (муха бурякова), Phorbia spp., Psila rosae (муха морквяна), Rhagoletis cerasi (муха вишнева), Rhagoletis pomonella (осетниця яблунева), Sitodiplosis mosellana (галиця злакова жовтогаряча), Stomoxys calcitrans (жигалка осіння), Tabanus spp. (ґедзі) і Tipula spp. (довгоніжки). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Hemiptera (напівжорсткокрилі або клопи). Невичерпний перелік вказаних шкідників включає, але без обмеження наступних представників вказаного ряду: Acrosternum hilare (клоп-щитник), Blissus leucopterus (chinch bug), Calocoris norvegicus (клопик картопляний), Сimex hemipterus (tropical bed bug), Сimex lectularius (клоп постільний), Dagbertus fasciatus, Dichelops furcatus, Dysdercus suturellus (червоноклоп бавовняний), Edessa meditabunda, Eurygaster maura (черепашка маврська), Euschistus heros, Euschistus servus (brown stink bug), Helopeltis antonii, Helopeltis theivora (сліпняк чайний індійський), Lagynotomus spp. (щитники), Leptocorisa oratorius, Leptocorisa varicornis, Lygus spp. (сліпняки), Lygus hesperus 24 UA 107566 C2 5 10 15 20 25 30 35 40 45 50 55 (western tarnished plant bug), Maconellicoccus hirsutus, Neurocolpus longirostris, Nezara viridula (southern green stink bug), Phytocoris spp. (plant bugs), Phytocoris californicus, Phytocoris relativus, Piezodorus guildingi, Poecilocapsus lineatus (fourlined plant bug), Psallus vaccinicola, Pseudacysta perseae, Scaptocoris castanea і Triatoma spp. (кровососні конусоносні тріатоми/поцілункові клопи). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Homoptera (рівнокрилі - попелиці рослинні, червчики, щитівки, білокрилки, цикадки, кобилки). Невичерпний перелік вказаних шкідників включає, але без обмеження наступних представників вказаного ряду: Acrythosiphon pisum (попелиця горохова), Adelges spp. (хермеси), Aleurodes proletella (cabbage whitefly), Aleurodicus disperses, Aleurothrixus floccosus (білокрилка шерстиста), Aluacaspis spp., Amrasca bigutella bigutella, Aphrophora spp. (пінниці), Aonidiella aurantii (щитівка помаранцева червона), Aphis spp. (афіди), Aphis gossypii (попелиця баштанна (бавовняна)), Aphis pomi (попелиця яблунева), Aulacorthum solani (попелиця картопляна звичайна), Bemisia spp. (білокрилки), Bemisia argentifolii, Bemisia tabaci (білокрилка тютюнова), Brachycolus noxius (попелиця ячмінна), Brachycorynella asparagi (попелиця аспарагусова), Brevennia rehi, Brevicoryne brassicae (попелиця капустяна), Ceroplastes spp. (несправжньощитівки), Ceroplastes rubens (red wax scale), Chionaspis spp. (щитівки), Chrysomphalus spp. (щитівки), Coccus spp. (scales), Dysaphis plantaginea (rosy apple aphid), Empoasca spp. (leafhoppers), Eriosoma lanigerum (попелиця кров'яна яблунева, попелиці волохата), Icerya purchasi (австралійський жолобчастий червчик), Idioscopus nitidulus (mango leafhopper), Laodelphax striatellus (цикадка темна), Lepidosaphes spp., Macrosiphum spp., Macrosiphum euphorbiae (попелиця велика картопляна), Macrosiphum granarium (попелиця злакова), Macrosiphum rosae (попелиця розанно-зелена), Macrosteles quadrilineatus (aster leafhopper), Mahanarva frimbiolata, Metopolophium dirhodum (попелиця розанно-злакова), Mictis longicornis, Myzus persicae (попелиця персикова (оранжерейна, тютюнова)), Nephotettix spp. (цикадки), Nephotettix cinctipes (green leafhopper), Nilaparvata lugens (brown planthopper), Parlatoria pergandii (щитівка цитрусова фіолетова), Parlatoria ziziphi (щитівка чорна), Peregrinus maidis (цикадка кукурудзяна), Philaenus spp. (цикадки, пінниці), Phylloxera vitifoliae (філоксера виноградна), Physokermes piceae (несправжньощитівка ялинова), Planococcus spp. (борошнисті червчики, повстярі), Pseudococcus spp. (борошнисті червчики), Pseudococcus brevipes (борошнистий червчик ананасовий), Quadraspidiotus perniciosus (щитівка каліфорнійська), Rhapalosiphum spp. (афіди), Rhapalosiphum maida (corn leaf aphid), Rhapalosiphum padi (oat birdCherry aphid), Saissetia spp. (scales), Saissetia oleae (несправжньощитівка маслинная, червчик маслиновий), Schizaphis graminum (попелиця злакова звичайна), Sitobion avenae (попелиця злакова більша), Sogatella furcifera (цикадка білоспинна), Therioaphis spp. (попелиці), Toumeyella spp. (червчики), Toxoptera spp. (aphids), Trialeurodes spp. (білокрилки), Trialeurodes vaporariorum (білокрилка теплична), Trialeurodes abutiloneus (bandedwing whitefly), Unaspis spp. (щитівки), Unaspis yanonensis (щитівка цитрусова східна) і Zulia entreriana. У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Hymenoptera (пертинчатокрилі - мурахи, оси і бджоли). Невичерпний перелік вказаних шкідників включає, але без обмеження наступних представників вказаного ряду: Acromyrrmex spp., Athalia rosae, Atta spp. (мурахи-листорізи, атта), Camponotus spp. (мурахи-деревоточці), Diprion spp. (трачі), Formica spp. (форміки), Iridomyrmex humilis (аргентинська мураха, іридомірмекс), Monomorium spp., Monomorium minumum (мураха чорна мала), Monomorium pharaonis (мураха фараонів), Neodiprion spp. (трачі), Pogonomyrmex spp. (мурахи-женці), Polistes spp. (паперові оси), Solenopsis spp. (мурахи вогненні), Tapoinoma sessile (мураха домашня пахуча), Tetranomorium spp. (мурахи дернові), Vespula spp. (yellow jackets) і Xylocopa spp. (бджоли-теслі). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Isoptera (терміти). Невичерпний перелік вказаних шкідників включає, але без обмеження наступних представників вказаного ряду: Coptotermes spp., Coptotermes curvignathus, Coptotermes frenchii, Coptotermes formosanus (Formosan subterranean termite), Cornitermes spp. (nasute termites), Cryptotermes spp. (drywood termites), Heterotermes spp. (desert subterranean termites), Heterotermes aureus, Kalotermes spp. (drywood termites), Incistitermes spp. (drywood termites), Macrotermes spp. (fungus growing termites), Marginitermes spp. (drywood termites), Microcerotermes spp. (harvester termites), Microtermes obesi, Procornitermes spp., Reticulitermes spp. (subterranean termites), Reticulitermes banyulensis, Reticulitermes grassei, Reticulitermes flavipes (терміт жовтоногий), Reticulitermes hageni, Reticulitermes hesperus (western subterranean termite), Reticulitermes santonensis, Reticulitermes 25 UA 107566 C2 5 10 15 20 25 30 35 40 45 50 55 speratus, Reticulitermes tibialis, Reticulitermes virginicus, Schedorhinotermes spp. і Zootermopsis spp. (rotten-wood termites). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Lepidoptera (лускокрилі і метелики). Невичерпний перелік шкідників вказаного ряду включає наступних представників: Achoea janata, Adoxophyes spp., Adoxophyes orana, Agrotis spp. (совки), Agrotis ipsilon (гусениця совки іпсилон), Alabama argillacea (гусениця совки бавовняної), Amorbia cuneana, Amyelosis transitella (navel orangeworm), Anacamptodes defectaria, Anarsia lineatella (міль фруктова виїмчастокрила), Anomis sabulifera (jute looper), Anticarsia gemmatalis (velvetbean caterpillar), Archips argyrospila (листовійка плодових дерев), Archips rosana (листовійка розанно золотава), Argyrotaenia spp. (листовійки), Argyrotaenia citrana (листовійка цитрусова), Autographa gamma, Bonagota cranaodes, Borbo cinnara (rice leaf folder), Bucculatrix thurberiella (кривовуса міль бавовняна), Caloptilia spp. (міль худа), Capua reticulana, Carposina niponensis (карпосина плодова, плодожерка персикова), Chilo spp., Chlumetia transversa (mango shoot borer), Choristoneura rosaceana (скошеносмугаста листовійка), Chrysodeixis spp., Cnaphalocerus medinalis (вогнівка рисова), Colias spp., Conpomorpha cramerella, Cossus cossus (червиця вербова), Crambus spp. (вогнівки), Cydia funebrana (плодожерка сливова), Cydia molesta (плодожерка східна), Cydia nignicana (плодожерка горохова), Cydia pomonella (плодожерка яблунева), Darna diducta, Diaphania spp. (stem borers), Diatraea spp. (stalk borers), Diatraea saccharalis (вогнівка цукрового очерету), Diatraea grandiosella (вогнівка кукурудзяна південно-західна), Earias spp. (совки), Earias insulata (совка бавовняна єгипетська), Earias vitella (rough northernbollworm), Ecdytopopha aurantianum, Elasmopalpus lignosellus (метелик малий кукурудзяний), Epiphysias postruttana (light brown apple moth), Ephestia spp. (вогнівки), Ephestia cautella (вогнівка сухофруктова), Ephestia elutella (tobacco moth), Ephestia kuehniella (вогнівка млинова), Epimeces spp., Epinotia aporema, Erionota thrax (banana skipper), Eupoecilia ambiguella (листовійка дворічна виноградна), Euxoa auxiliaris (army cutworm), Feltia spp. (cutworms), Gortyna spp. (совки), Grapholita molesta (плодожерка східна), Hedylepta indicata (метелик соєвий), Helicoverpa spp. (совки бавовняні), Helicoverpa armigera (совка бавовняна), Helicoverpa zea (совка бавовняна/кукурудзяна), Heliothis spp. (совки), Heliothis virescens (совка тютюнова нічна), Hellula undalis (вогнівка капустяна), Indarbela spp. (root borers), Keiferia lycopersicella (tomato pinworm), Leucinodes orbonalis (eggplant fruit borer), Leucoptera malifoliella, Lithocollectis spp., Lobesia botrana (листовійка гронова виноградна), Loxagrotis spp. (noctuid moths), Loxagrotis albicosta (western bean cutworm), Lymantria dispar (шовкопряд непарний), Lyonetia clerkella (міль-крихітка яблунева біла), Mahasena corbetti (oil palm bagworm), Malacosoma spp. (кононопряди), Mamestra brassicae (совка капустяна), Maruca testulalis (вогнівка жовта лугова), Metisa plana (bagworm), Mythimna unipuncta (совка однокрапкова), Neoleucinodes elegantalis (small tomato borer), Nymphula depunctalis (rice caseworm), Operophthera brumata (п'ядак зимовий), Ostrinia nubilalis (метелик стебловий), Oxydia vesulia, Pandemis cerasana (листовійка смородинова кривовуса), Pandemis heparana (листовійка вербова), Papilio demodocus, Pectinophora gossypiella (міль бавовняна), Peridroma spp. (совки), Peridroma saucia (совка маргариткова), Perileucoptera coffeella (white coffee leafminer), Phthorimaea operculella (міль картопляна), Phyllocnisitis citrella, Phyllonorycter spp. (моліпістрянки), Pieris rapae (білявка ріпна), Plathypena scabra, Plodia interpunctella (вогнівка південна комірна), Plutella xylostella (міль капустяна), Polychrosis viteana (листовійка виноградна), Prays endocarpa, Prays oleae (міль маслинова), Pseudaletia spp. (noctuid moths), Pseudaletia unipunctata (совка лугова), Pseudoplusia includens (soybean looper), Rachiplusia nu, Scirpophaga incertulas, Sesamia spp. (stemborers), Sesamia inferens (pink rice stem borer), Sesamia nonagrioides, Setora nitens, Sitotroga cerealella (міль зернова), Sparganothis pilleriana, Spodoptera spp. (совки), Spodoptera exigua (карадрина, совка мала), Spodoptera frugiperda (совка трав'яна), Spodoptera oridania (southern armyworm), Synanthedon spp. (склівки), Thecla basilides, Thermisia gemmatalis, Tineola bisselliella (міль платтяна), Trichoplusia ni (cabbage looper), Tuta absoluta, Yponomeuta spp., Zeuzera coffeae (red branch borer) і Zeuzera pyrina (древесниця в'їдлива). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Mallophaga (пухоїди). Невичерпний перелік шкідників вказаного ряду включає наступних представників: Bovicola ovis (волосоїд овечий), Menacanthus stramineus (chicken body louse) і Menopon gallinae (пухоїд курячий). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Orthoptera (прямокрилі - коники, цикади і цвіркуни). Невичерпний перелік шкідників вказаного ряду включає наступних його представників: Anabrus simplex (коник-мормон), Gryllotalpidae (капустянки), Locusta migratoria, Melanoplus spp. (кобилки), 26 UA 107566 C2 5 10 15 20 25 30 35 40 45 50 55 60 Microcentrum retinerve (коник вузькокрилий), Pterophylla spp. (коники кутастокрилі), Schistocerca gregaria, Scudderia furcata (forktailed bush katydid) і Valanga nigricornis. У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Phthiraptera (воші). Невичерпний перелік шкідників вказаного ряду включає наступних представників: Haematopinus spp. (воша великої рогатої худоби, свиняча воша), Linognathus ovillus (воша овеча), Pediculus humanus capitis (воша головна), Pediculus humanus humanus (воша платтяна) і Pthirus pubis (воша лобкова). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Siphonaptera (блохи). Невичерпний перелік шкідників вказаного ряду включає наступних його представників: Ctenocephalides canis (блоха собача), Ctenocephalides felis (блоха котяча) і Pulex irritans (блоха людська). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Thysanoptera (трипси). Невичерпний перелік шкідників вказаного ряду включає наступних представників: Frankliniella fusca (tobacco thrips), Frankliniella occidentalis (трипс західний квітковий), Frankliniella schultzei, Frankliniella williamsi (corn thrips), Heliothrips haemorrhaidalis (трипс оранжерейний), Riphiphorothrips cruentatus, Scirtothrips spp., Scirtothrips citri (трипс цитрусовий), Scirtothrips dorsalis (трипс чайний жовтий), Taeniothrips rhopalantennalis і Thrips spp. У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Thysanura (щетинохвістки). Невичерпний перелік шкідників вказаного ряду включає наступних представників: Lepisma spp. (лусківниці) і Thermobia spp. (firebrats). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Acarina (кліщі і іксодові кліщі). Невичерпний перелік шкідників вказаного ряду включає наступних представників: Acarapsis woodi (tracheal mite of honeybees), Acarus spp. (food mites), Acarus siro (кліщ борошняний), Aceria mangiferae (mango bud mite), Aculops spp., Aculops lycopersici (іржастий кліщ томатів), Aculops pelekasi, Aculus pelekassi, Aculus schlechtendali (кліщ іржастий яблуневий), Amblyomma americanum (кліщ іксодовий), Boophilus spp. (іксодові кліщі), Brevipalpus obovatus (плоскотілка оранжерейна), Brevipalpus phoenicis (кліщ неправильний паукоподібний), Demodex spp. (кліщі коростяні), Dermacentor spp. (hard ticks), Dermacentor variabilis (кліщ іксодовий собачий), Dermatophagoides pteronyssinus (кліщ домашнього пилу), Eotetranycus spp., Eotetranychus carpini (жовтий грабовий павутинний кліщ), Epitimerus spp., Eriophyes spp., Ixodes spp. (кліщі іксодові), Metatetranycus spp., Notoedres cati, Oligonychus spp., Oligonychus coffee, Oligonychus ilicus (southern red mite), Panonychus spp., Panonychus citri (червоний цитрусовий кліщ), Panonychus ulmi (кліщ червоний плодовий), Phyllocoptruta oleivora (кліщ іржастий цитрусовий), Polyphagotarsonemun latus (кліщ прозорий оранжерейний), Rhipicephalus sanguineus (кліщ іксодовий бурий собачий), Rhizoglyphus spp. (кліщики кореневі), Sarcoptes scabiei (кліщ коростяний), Tegolophus perseaflorae, Tetranychus spp., Tetranychus urticae (кліщ павутинний звичайний) і Varroa destructor (кліщ варроа). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Nematoda (нематоди). Невичерпний перелік шкідників вказаного ряду включає наступних представників: Aphelenchoides spp. (bud and leaf & pine wood nematodes), Belonolaimus spp. (sting nematodes), Criconemella spp. (ring nematodes), Dirofilaria immitis (гельмінт серцевий), Ditylenchus spp. (стеблові і бульбочкові нематоди), Heterodera spp. (cyst nematodes), Heterodera zeae (corn cyst nematode), Hirschmanniella spp. (кореневі нематоди), Hoplolaimus spp. (lance nematodes), Meloidogyne spp. (root knot nematodes), Meloidogyne incognita (нематода коренева галлова), Onchocerca volvulus (hook-tail worm), Pratylenchus spp. (lesion nematodes), Radopholus spp. (burrowing nematodes) і Rotylenchus reniformis (kidney-shaped nematode). У ще одному варіанті здійснення винахід, розкритий в даному документі, може застосовуватися для боротьби з Symphyla (симфіли). Невичерпний перелік шкідників вказаного ряду включає наступних представників: Scutigerella immaculata. Більш докладний опис див. у публікації "Handbook of Pest Control-The Behavior, Life History, і th Control of Household Pests" by Arnold Mallis, 9 Edition, copyright 2004 by GIE Media Inc. СУМІШІ Деякі з пестицидів, які можуть успішно застосовуватися в комбінації з винаходом, описаним у даному документі, включають, але без обмеження, наступні: 1, 2-дихлорпропан, 1, 3-дихлорпропен, абамектин, ацефат, ацеквіноцил, ацетаміприд, ацетіон, ацетопрол, акринатрин, акрилонітрил, аланікарб, алдикарб, алдоксикарб, алдрин, алетрин, алосамідин, аліксикарб, 27 UA 107566 C2 5 10 15 20 25 30 35 40 45 50 55 60 альфа-циперметрин, альфа-екдизон, альфа-ендосульфан, AKD-1022, амідитіон, амідофлумет, амінокарб, амітіон, амітраз, анабасин, оксид миш'яку, атидатіон, азадирахтин, азаметифос, азинфос-етил, азинфос-метил, азобензол, азоциклотин, азотоат, Bacillus thuringiensis, гексафторсилікат барію, бартрин, бенклотіаз, бендиокарб, бенфуракарб, беноміл, беноксафос, бенсултап, бензоксимат, бензилбензоат, бета-цифлутрин, бета-циперметрин, біфеназат, біфентрин, бінапакрил, біоалетрин, біоетанометрин, біфеназат, біфентрин, бінапакрил, біоалетрин, біоетанометрин, біоперметрин, бістрифлурон, боракс, борна кислота, бромфенвінфос, бром-ДДТ, бромоциклен, бромофос, бромофос-етил, бромопропілат, буфенкарб, бупрофезин, бутакарб, бутантіофос, бутокарбоксим, бутонат, бутоксикарбоксим, кадусафос, арсенат кальцію, полісульфід кальцію, камфехлор, карбанолат, карбарил, карбофуран, дисульфід вуглецю, тетрахлорид вуглецю, карбофенотіон, карбосульфан, картап, хінометіонат, хлорантраніліпрол, хлорбензид, хлорбіциклен, хлордан, хлордекон, хлордимеформ, хлоретоксифос, хлортенапір, хлорфенетол, хлорфенсон, хлорфенсульфид, хлорфенвипфос, хлорфлуазурон, хлормефос, хлоробензилат, 3-(4-хлор-2,6-диметилфенил)-4гідрокси-8-окса-1-азаспіро[4,5]дец-3-ен-2-он, 3-(4'-хлор-2,4-диметил[1,1'-біфеніл]-3-іл)-4гідрокси-8-окса-1-азаспіро[4,5]дец-3-ен-2-он, 4-[[(6-хлор-3-піридиніл)метил]метиламіно]-2(5H)фуранон, 4-[[(6-хлор-3-піридиніл)метил]циклопропіламіно]-2(5H)-фуранон, 3-хлор-N2-[(1S)-1метил-2-(метилсульфоніл)етил]-N1-[2-метил-4-[1,2,2,2-тетрафтор-1-(трифторметил)етил]феніл]1,2-бензолдикарбоксамід, хлороформ, хлоромебуформ, хлорометиурон, хлорпікрин, хлорпропілат, хлорфоксим, хлорпразофос, хлорпірифос, хлорпірифосиметил, хлортіофос, хромафенозид, цинерин I, цинерин II, цисметрин, клоетокарб, клофентезин, клосантел, клотіанідин, ацетоарсеніт міді, арсенат міді, нафтенат міді, олеат міді, кумафос, кумітоат, кротамітон, кротоксифос, круентарен A & B, круфомат, кріоліт, ціанофенфос, ціанофос, ціантоат, ціантраніліпрол, циклетрин, циклопротрин, цієнопірафен, цифлуметофен, цифлутрин, цигалотрин, цигексатин, циперметрин, цифенотрин, циромазин, цитіоат, 2-ціано-N-етил-4-фтор3-метоксибенсульфонамід, 2-ціано-N-етил-3-метоксибензолсульфонамід, 2-ціано-3дифторметокси-N-етил-4-фторбензолсульфонамід, 2-ціано-3-фторметокси-Nетилбензолсульфонамід, 2-ціано-6-фтор-3-метокси-N, N-диметилбензолсульфонамід, 2-ціаноN-етил-6-фтор-3-метокси-N-метилбензолсульфонамід, 2-ціано-3-дифторметокси-N, Nдиметилбензолсульфонамід, d-лімонен, дазомет,DBCP, DCIP, ДДТ, декарбофуран, дельтаметрин, демефіон, демефіонО, демефіон-С, деметон, деметонометил, деметон-О, деметон-О-метил, деметон-S, деметон-Sметил, деметон-S-метилфульфон, діафентіурон, діаліфос, діамідафос, діазинон, дикаптон, дихлорфентіон, дихлорфлуанід, дихлорвос, дикофол, дикрезил, дикротофос, дицикланіл, діелдрин, дієнохлор, дифловідазин, дифлубензурон, 3-(дифторметил)-N-[2-(3,3диметилбутил)феніл]-1-метил-1H-піразол-4-карбоксамід, дилор, диметфлутрин, димефокс, диметан, диметоат, диметрин, диметилвінфос, диметилан, динекс, динобутон, динокап, динокап-4, динокап-6, диноктон, динопентон, динопроп, диносам, диносульфон, динотефуран, динотербон, діофенолан, діоксабензофос, діоксакарб, діоксатіон, дифенілсульфон, дисульфирам, дисульфотон, дитикрофос, DNOC, дофенапін, дорамектин, екдистерон, емамектин, емамектинібензоат, EMPC, емпентрин, ендосульфан, ендотіон, ендрин, EPN, епофенонан, еприномектин, есфенвалерат, етафос, етіофенкарб, етіон, етипрол, етоат-метил, етопрофос, етил-DDD, етилформіат, етилендибромід, етилендихлорид, етиленоксид, етофенпрокс, етоксазол, етримфос, EXD, F1050, фамфур, фенаміфос, феназафлор, феназаквін, фенбутатинтоксид, фенхлорфос, фенетакарб, фенфлутрин, фенітротіон, фенобукарб, фенотіокарб, феноксакрим, феноксикарб, фенпіритрин, фенпропатрин, фенпіроксимат, фенсон, фенсульфутіон, фентіон, фентіоніетил, фентрифаніл, фенвалерат, фіпроніл, FKI-1033, флонікамід, флуакрипірим, флуазурон, флубендіамід, флубензимін, флукофурон, флуциклоксурон, флуцитринат, флуенетил, флуфенерим, флуфеноксурон, флуфенпрокс, флуметрин, флуорбенсид, флувалінат, фонофос, форметанат, формотіон, формпаранат, фосметилан, фоспірат, фостіазат, фостієтан, фостієтан, фуратіокарб, фуретрин, фурфурал, гамма-цигалотрин, гама-ΗCΗ, галфенпрокс, галофенозид, ΗCΗ, ΗEOD, гептахлор, гептенофос, гетерофос, гексафлумурон, гекситіазокс, ΗΗDN, гідраметилнон, ціанистоводнева кислота, гідропрен, хіквінкарб, іміціафос, імідаклоприд, імідаклотиз, іміпротин, індоксакарб, йодометан, IPSP, ізамідофос, ісазофос, ісобензан, ісокарбофос, ісодрин, ісофенфос, ісопрокарб, ісопротіолан, ісотіоат, ісоксатіон, івермектин, 28
ДивитисяДодаткова інформація
Назва патенту англійськоюPesticidal compositions
Автори російськоюCrouse, Gary, Sparks, Thomas, McLeod, CaSandra, Brown, Annette, Siddall, Thomas
МПК / Мітки
МПК: A01N 43/16, A01P 7/04, C07H 15/02
Мітки: пестицидні, композиції
Код посилання
<a href="https://ua.patents.su/41-107566-pesticidni-kompozici.html" target="_blank" rel="follow" title="База патентів України">Пестицидні композиції</a>
Попередній патент: Титановий сляб для гарячого вальцювання, одержаний за допомогою електронно-променевої печі, спосіб його виготовлення та спосіб вальцювання титанового сляба
Наступний патент: Спосіб одержання фторованих хлоридів м-нітро-бензойної кислоти
Випадковий патент: Ливарна формувальна лінія












